固体物理化学第三章习题
固体物理-第三章 金属自由电子论讲解

3.1.量子自由电子理论
I2=(1/2!)-(E-EF)2(-f/E) dE 不难算出, I0=1(d-函数积分), I1=0 (根据d-函数的性质) 为了计算I2, 而令h=(E-EF)/kBT,于是, I2=[(kBT)2/2]-{h2/[(eh+1)(e-h+1)] }dh=(pkBT)2/6
波长),可见k为电子的波矢, 是3 维空间矢量. r:电 子的位置矢量。
由波函数的归一化性质:vy*(r) y(r)d(r)=1, v:金属体积, 假设为立方体,边长为L,把3.1.1.3式 代入归一化式子, 得: A=L-3/2=V-1/2, 所以
y(r)= V-1/2eik•r 3.1.1.4, 此即自由电子的本征态。 由周期性边界条件, y(x,y,z)= y(x+L,y,z) = y(x,y+L,z) = y(x,y,z+L)
一状态的电子具有确定的动量ħk和能量ħ2k2/(2m),因而 具有确定的速度,v=ħk/m,故一个k全面反映了自由电子 的一个状态,简称态。
2. k-空间
以kx, ky , kz 为坐标轴建立的 波矢空间叫k-空间。电子的 本征态可以用该空间的一点
来代表。点的坐标由3.1.1.5 式确定。
3.1.量子自由电子理论
T>0K的费米能EF 把3.1.2.2和3.1.3.1代入3.1.3.2, 分步积分, 得:
N= (-2C/3) 0 E3/2(f/E) dE 3.1.3.3 令G(E)= 2C E3/2/3, 3.1.3.3.式化简为 N= 0G(E) (-f/E) dE 3.1.3.4 (-f/E)函数具有类似d函数的特性,仅仅在EF附近kBT范 围内才有显著的值,且为E-EF偶函数. 由于(-f/E)函数 具有这些性质,把G(E)在EF附近展开为泰勒级数, 且积分 下限写成 -,不会影响积分值. 3.1.3.4化为:
历年成人高考《物理化学》试题及答案汇总(高起点)

6.某旋风分离器的分离因数 k=100,旋转半径 R=0.3m,则切向速度 ut= 7.对板框式过滤机,洗涤面积 AW 和过滤面积 A 的定量关系为
,洗水走过的距离 Lw 和滤液在过滤终了时
走过的距离 L 的定量关系为
dV dV )W ( )E ,洗涤速率( dq 和终了时的过滤速率 dq 的定量关系为
3 3 2 2 0.5 -5 0.5 1.5 1.5
=5.66 m
3
=23.2 m
3
4、 (1)过滤 52min 时的滤液量 A=0.635×0.635×25×2=20.16m
2
V =KA θ=1.7×10 ×(20.16) ×52×60=215.57; V=14.68m
3
2
2
-5
2
3
(2)(dV/dθ)W=(1/4)(dV/dθ)=V/8q=14.68/(8×52) =0.0353m /min θW=VW/(dV/dθ)W =0.08×14.68/0.0353 =33.27min (3)过滤机的生产能力 θ 总=52+33.27+30=115.27min; 生产能力=14.68/(115.27/60)=7.64m /h 5、 为要了解滤液量随过滤时间而变化的关系,需先求出恒压下的过滤常数 K 及 qe。恒压过滤方程式亦可写成如下 形式,即: q +2qeq=Kθ
2 -3 -6 -2 2 -7
-3
2
则△p=67KN/m 时的过滤方程式为:
将 θ=(5+5+5)×60=900s 代入上式,即 q +2×7×10 q=8×10 ×(900); 解得 q=2.1×10 m V=(2.1×10 )×0.1=2.1×10 m =2.1 升 由此可知,若再过滤 5 分钟,可再得滤液量为:[2.1-(1+0.6)]=0.5 升 第三章 一、填空题 1.某颗粒的重力沉降服从斯托克斯定律,若在水中的沉降速度为 u1,在空气中为 u2,则 u1 沉降速度为 u3,冷空气中为 u4,则 u3 u4。(>,<,=) u2;若在热空气中的
物理化学简明教程习题答案

第一章气体的pVT性质1.1 物质的体膨胀系数与等温压缩率的定义如下试推出理想气体的,与压力、温度的关系。
解:根据理想气体方程1.2 0℃,101.325kPa的条件常称为气体的标准状况,试求甲烷在标准状况下的密度。
解:将甲烷(Mw =16.042g/mol)看成理想气体: PV=nRT , PV =mRT/ Mw甲烷在标准状况下的密度为=m/V= PMw/RT=10116.042/8.314515(kg/m3)=0.716 kg/m31.3 一抽成真空的球形容器,质量为25.0000g充以4℃水之后,总质量为125.0000g。
若改充以25℃,13.33 kPa的某碳氢化合物气体,则总质量为 25.0163g。
试估算该气体的摩尔质量。
水的密度1g·cm3计算。
解:球形容器的体积为V=(125-25)g/1 g.cm-3=100 cm3将某碳氢化合物看成理想气体:PV=nRT , PV =mRT/ MwMw= mRT/ PV=(25.0163-25.0000)×8.314×298.15/(13330×100×10-6)M w =30.31(g/mol)1.4 两个容积均为V的玻璃球泡之间用细管连结,泡内密封着标准状态下的空气。
若将其中的一个球加热到 100℃,另一个球则维持 0℃,忽略连接细管中气体体积,试求该容器内空气的压力。
解:由题给条件知,(1)系统物质总量恒定;(2)两球中压力维持相同。
标准状态:因此,1.5 0℃时氯甲烷(CH 3Cl )气体的密度ρ随压力的变化如下。
试作p p-ρ图,用外推法求氯甲烷的相对分子质量。
1.6 今有20℃的乙烷-丁烷混合气体,充入一抽成真空的200 cm3容器中,直至压力达101.325 kPa,测得容器中混合气体的质量为0.3897 g。
试求该混合气体中两种组分的摩尔分数及分压力。
解:将乙烷(M w=30g/mol,y1),丁烷(M w=58g/mol,y2)看成是理想气体:PV=nRT n=PV/RT=8.3147⨯10-3mol(y1⨯30+(1-y1) ⨯58)⨯8.3147⨯10-3=0.3897y1=0.401 P1=40.63kPay2=0.599 P2=60.69kPa1.7 如图所示,一带隔板的容器内,两侧分别有同温同压的氢气与氮气,二者均可视为理想气体。
固体物理参考答案(前七章)

固体物理习题参考答案(部分)第一章 晶体结构1.氯化钠:复式格子,基元为Na +,Cl -金刚石:复式格子,基元为两个不等价的碳原子 氯化钠与金刚石的原胞基矢与晶胞基矢如下:原胞基矢)ˆˆ()ˆˆ()ˆˆ(213212211j i a a i k a a k j a a +=+=+= , 晶胞基矢 ka a j a a ia a ˆˆˆ321===2. 解:31A A O ':h:k;l;m==-11:211:11:111:1:-2:1 所以(1 1 2 1) 同样可得1331B B A A :(1 1 2 0); 5522A B B A :(1 1 0 0);654321A A A A A A :(0 0 0 1)3.简立方: 2r=a ,Z=1,()63434r 2r a r 3333πππ===F体心立方:()πππ833r4r 342a r 3422a 3r 4a r 4a 33333=⨯=⨯=∴===F Z ,,则面心立方:()πππ622r 4r 34434442r 4a r 4a 233ar 33=⨯=⨯=∴===F Z ,,则 六角密集:2r=a, 60sin 2c a V C = a c 362=,πππ622336234260sin 34223232=⨯⨯⨯=⨯=⎪⎭⎫ ⎝⎛a a c a r F a金刚石:()πππ163r 38r 348a r 3488Z r 8a 33333=⨯=⨯===F ,, 4. 解:'28109)31arccos(312323)ˆˆˆ()ˆˆˆ(cos )ˆˆˆ()ˆˆˆ(021*******12211=-=-=++-⋅+-=⋅=++-=+-=θθa a k j i a k j i a a a a a kj i a a kj i a a 5.解:对于(110)面:2a 2a a 2S =⋅=所包含的原子个数为2,所以面密度为22a2a22=对于(111)面:2a 2323a 22a 2S =⨯⨯= 所包含的原子个数为2,所以面密度为223a34a 232=8.证明:ABCD 是六角密堆积结构初基晶胞的菱形底面,AD=AB=a 。
材料物理化学习题

第三章熔体与非晶态固体知识点:1.黏度与组成的关系答:组成是通过改变熔体结构而影响黏度的。
①一价金属氧化物碱金属氧化物R2O引入到硅酸盐熔体中,使熔体黏度降低。
在简单碱金属硅酸盐系统(R2O—SiO2)中,碱金属离子R+对黏度的影响与其本身的含量有关。
当R2O含量较低时(O/Si比值较低),加入的正离子的半径越小,降低黏度的作用就越大,起次序是:L i+>Na+>K+;当熔体中R2O含量较高(O/Si比值较高)时,R2O对黏度影响的次序是:L i+>Na+>K+。
②二价金属氧化物二价碱土金属氧化物对黏度的影响比较复杂,综合各种效应,R2+降低黏度的次序是:Pb2+>Ba2+>Sr2+>Cd2+>Ca2+>Zn2+>Mg2+.③高价金属氧化物一般地,在熔体中引入SiO2、Al2O3、B2O3、ZrO2等高价氧化物时,会导致黏度升高。
2.硼反常现象:当数量不多的碱金属氧化物同B2O3一起熔融时,碱金属所提供的氧不像熔融SiO2玻璃中作为非桥氧出现在结构中,而是使硼氧三角体转变为由桥氧组成的硼氧四面体,致使B2O3玻璃从原来两度空间的层状结构部分转变为三度空间的架状结构,从而加强了网络结构,并使玻璃的各种物理性能变好。
这与相同条件下的硅酸盐玻璃相比,其性能随碱金属或碱土金属加入量的变化规律相反,所以称之为硼反常现象。
3.非晶态固体——玻璃的通性①各项同性:无内应力存在的均质玻璃在各个方向的物理性质,如折射率、硬度、导电性、弹性模量、热膨胀系数、导热系数等都是相同的;②热力学介稳性:玻璃具有析晶不稳定性与析晶困难相对稳定性的统一;③熔融态向玻璃态转化的可逆性与渐变性:熔体向玻璃体转化的过程是在较宽的温度范围内完成得,随着温度的下降,熔体的黏度越来越大,且变化是连续的,最后形成固相的玻璃,其间没有新相出现,因此具有渐变性;由玻璃加热变为熔体的过程也是渐变的,因此具有可逆性。
④熔融态向玻璃态转化时物理、化学性质随温度变化的连续性⑤物理、化学性质随成分变化的连续性。
物理化学3-4章练习题

第三章 多组分系统热力学一.选择题:选择正确答案的编号,填在各题后的括号内:1.下面各个偏导式中,哪个是偏摩尔量( ) A.j n T p Bn ,,⎪⎪⎭⎫⎝⎛∂∂μ B.jn V S B n U ,,⎪⎪⎭⎫ ⎝⎛∂∂ C. jn T p B m n S ,,⎪⎪⎭⎫ ⎝⎛∂∂ D. j n T p B n V ,,⎪⎪⎭⎫ ⎝⎛∂∂ 2.下面各个偏导式中,哪个不是化学势( ) A. jn V S B n U ,,⎪⎪⎭⎫⎝⎛∂∂ B. jn p T Bn H ,,⎪⎪⎭⎫ ⎝⎛∂∂ C. jn p T Bn G ,,⎪⎪⎭⎫ ⎝⎛∂∂ D. jn V T Bn F ,,⎪⎪⎭⎫ ⎝⎛∂∂ 3.理想液态混合物中任一组分B,其偏摩尔量和摩尔量的关系为( ) A.B H =*B m H , B. B V VBm *≠, C.B G =*B m G , D. B S =*B m S , 4.一定温度下,纯液体A 的饱和蒸汽压为pA*,化学势为*A μ,凝固点为*f T ,当A 中加入少量不挥发性溶质后,上述三个量p A,μA,T f ,它们的关系为( )A, p A*<pA*Aμ<μA*f T <T fB. p A*>pA*Aμ <μA*f T < T fC. p A*<pA*Aμ<μA*f T >T fD.p A*>pA*Aμ>μA*f T >T f5.一定温度和压力下的乙醇水溶液中,若使乙醇的偏摩尔体积的变化dV>0.此时水的偏摩尔体积的变化dV水( )A. >0B.=0C. <0D.不能确定 6.对多组分体系中B 物质的偏摩尔量XB=Bj n p T Bn X ≠⎪⎪⎭⎫⎝⎛∂∂,,,下列叙述中不正确的是( ) A.X B是无限大量体系中B 物质每变化1 mol 时该体系容量性质X 的变化量B.X 为容量性质, XB也为容量性质C.XB不仅取决于T,p,而且取决于浓度D.X=X n B B ∑7.将固体NaCl 投放到水中, NaCl 逐渐溶解,最后达到饱和.开始溶解时溶液中的NaCl 的化学式为µ(a),饱和时溶液中NaCl 的化学势为µ(b),固体NaCl 的化学势为,则( ) A. µ(a)= µ(b)< µ(c) B. µ(a)= µ(b)> µ(c) C. µ(a)> µ(b)= µ(c) D. µ(a)<µ(b)= µ(c) 8.下列物理量中,( )既是偏摩尔量,又是化学势. A. Bj n p T Bn F ≠⎪⎪⎭⎫⎝⎛∂∂,, B. Bj n p S Bn H ≠⎪⎪⎭⎫ ⎝⎛∂∂,, C. Bj n p T Bn G ≠⎪⎪⎭⎫ ⎝⎛∂∂,, D. Bj n p S Bn U ≠⎪⎪⎭⎫ ⎝⎛∂∂,, 9.理想液态混合物的通性是( ) A 、 ΔV 混合=0 ΔH 混合=0 ΔS 混合>0 ΔG 混合<0 B 、 ΔV 混合=0 ΔH 混合=0 ΔS 混合>0 ΔG 混合=0 C 、 ΔV 混合> 0 ΔH 混合> 0 ΔS 混合>0 ΔG 混合<0 D 、 ΔV 混合=0 ΔH 混合=0 ΔS 混合=0 ΔG 混合=0 10.7、298K 时A 和B 两种气体在某一溶剂中溶解的亨利系数分别为kA 和kB ,且kA>kB ,则当A 和B 压力相同时,在该溶剂中溶解的量是 ( ) A 、 A 的量大于B 的量 B 、 A 的量小于B 的量 C 、 A 的量等于B 的量D 、 A 的量和B 的量无法比较11、313K 时纯液体A 的饱和蒸汽压是纯液体B 的21倍,A 和B 能形成理想液态混合物。
固体物理习题带答案

第二章:原子的结合
1. 设原子间的互作用能表示为 u (r ) 态,则 n>m. 解:原子间的相互作用能为: u (r )
作用能处于极小值: 这时有
r
m
rn
。证明:要使两原子处于平衡状
r
m
rn
。若两原子处于平衡状态时,则其相互
du (r ) (m) m 1 (n) n 1 dr r r
子晶格的情形比较, 与 q 之间存在着两种不同的色散关系。一维复式晶体中可以存在两 种独立的格波。两种不同的格波的色散关系:
2 2
(m M ) 4mM {1 [1 sin 2 aq]1 / 2 } 2 mM (m M ) (m M ) 4mM {1 [1 sin 2 aq]1 / 2 } 2 mM (m M )
xn (t ) A cos(t 2 naq) 。试求格波的色散关系。
解:一维单原子链中,牛顿方程为:
n ( x n 1 xn 1 2 xn ) m x
若将其振动位移写成 xn (t )
A cos(t 2 naq) 代入牛顿方程,则有
2
2 [1 cos(2aq)] 因此其色散关系为 m
0 。 所 以 有
r0
m
r0
m 1
n
r0
n 1
。所以
m nm r0 。 n
0
r0
同
时
有
d 2u ( r ) (m)( m 1) m 2 (n)( n 1) n 2 2 dr r r
。
所
以
固体物理复习_简述题

"固体物理"根本概念和知识点第一章根本概念和知识点1) 什么是晶体、非晶体和多晶?(H)*晶面有规则、对称配置的固体,具有长程有序特点的固体称为晶体;在凝结过程中不经过结晶(即有序化)的阶段,原子的排列为长程无序的固体称为非晶体。
由许许多多个大小在微米量级的晶粒组成的固体,称为多晶。
2) 什么是原胞和晶胞?(H)*原胞是一个晶格最小的周期性单元,在有些情况下不能反响晶格的对称性;为了反响晶格的对称性,选取的较大的周期单元,称为晶胞。
3) 晶体共有几种晶系和布拉伐格子?(H)*按构造划分,晶体可分为7大晶系, 共14布拉伐格子。
4) 立方晶系有几种布拉伐格子?画出相应的格子。
(H)*立方晶系有简单立方、体心立方和面心立方三种布拉伐格子。
5) 什么是简单晶格和复式格子?分别举3个简单晶格和复式晶格的例子。
(H)*简单晶格中,一个原胞只包含一个原子,所有的原子在几何位置和化学性质上是完全等价的。
碱金属具有体心立方晶格构造;Au、Ag和Cu具有面心立方晶格构造,它们均为简单晶格复式格子则包含两种或两种以上的等价原子,不同等价原子各自构成一样的简单晶格,复式格子由它们的子晶格相套而成。
一种是不同原子或离子构成的晶体,如:NaCl、CsCl、ZnS等;一种是一样原子但几何位置不等价的原子构成的晶体,如:具有金刚石构造的C、Si、Ge等6) 钛酸钡是由几个何种简单晶格穿套形成的?(H)BaTiO在立方体的项角上是钡(Ba),钛(Ti)位于体心,面心上是三组氧(O)。
三组氧(OI,OII,*3OIII)周围的情况各不一样,整个晶格是由 Ba、 Ti和 OI、 OII、 OIII各自组成的简立方构造子晶格(共5个)套构而成的。
7) 为什么金刚石是复式格子?金刚石原胞中有几个原子?晶胞中有几个原子?(H)*金刚石中有两种等价的C原子,即立方体中的8个顶角和6个面的中心的原子等价,体对角线1/4处的C原子等价。
第三章第一节_金属的化学性质(习题巩固)

第三章第一节 金属的化学性质一、金属钠的性质与应用练习题一、选择题1.通过你的观察和推理,判断下列实验室中对于少量Na的保存方法正确的是()A.保存在水中 B.密封,保存在广口瓶中C.用铝箔包裹,密封在广口瓶中 D.密封,保存在煤油中2.钠与水反应的现象与钠的下列性质无关的是()A.钠的熔点较低 B.钠的密度比水的小C.钠的硬度小 D.钠有很强的还原性3.下列有关钠的叙述中,错误的是()A.钠的很活泼,可以用来冶炼金属钛、锆、铌等B.钠的化学性质非常活泼,钠元素只能以化合态存在于自然界C.钠是一种灰黑色的固体D.钠的质地软,可用小刀切割4.关于钠原子与钠离子,下列叙述错误的是()A.它们相差1个电子层 B.它们的化学性质相似C.钠原子比钠离子稳定 D.钠原子、钠离子均为钠元素5.金属钠着火后,可用于灭火的物质和器材有()A.水 B.泡沫灭火器 C.干冰灭火剂 D.干砂6.取一小块钠放在玻璃燃烧匙里加热,下列实验现象正确的是()①金属先熔化②在空气中燃烧火焰呈黄色③燃烧时火星四射④燃烧后生成淡黄色固体⑤燃烧后生成白色固体A.①②③ B.①②④ c.①②⑤ D.①③⑤7.钠的下列用途与其化学性质无关的是()A.制过氧化钠 B.原子反应堆的导热剂.C.冶炼金属钛 D.制取贵重金属钽8、将钠放置在空气中,是生成白色的Na2O还是淡黄色的Na2O2,主要取决于下列因素中的A、反应温度B、空气的量C、钠粒的大小D、钠的形状9.将一小块钠投入盛有5mL饱和石灰水的试管中,不可能观察到的现象是()A.钠熔成光亮的小球,在液面四处游动 B.有气体产生C.溶液底部有银白色的物质 D.溶液变浑浊10.(2002年上海春季考题)在烧杯中加入水和苯(密度:0.88g/cm3)各50mL。
将一小粒金属钠(密度:0.97g/cm3)投入烧杯中。
观察到的现象可能是()A 钠在水层中反应并四处游动B 钠停留在苯层中不发生反应C 钠在苯的液面上反应并四处游动D.钠在苯与水的界面处反应并可能作上、下跳动11.将一定质量的钠投入到24.6g t℃的水中,得到t℃的NaOH饱和溶液31.2g。
固体化学复习题及答案

第一章绪论1、固体化学的研究内容是什么?基本内容包括:固体物质的合成,固体的组成和结构,固相中的化学反应,固体中的缺陷,固体表面化学,固体的性质与新材料等。
固体化学主要是研究固体物质(包括材料)的合成、反应、组成和性能及相关现象、规律和原因的科学。
固体化学的研究内容十分广泛。
它与固体物理及其他许多学科相互交叉渗透,因此很难给出明确的,全面的研究范围。
它着重于研究固态物质(包括单晶、多晶、玻璃、陶瓷、薄膜、超微粒子等)的合成、反应、组成、结构和各种宏观和微观性质。
2、假如你是从事无机材料方面的研究者,你的研究成果可以在哪些国内外期刊上投稿,试列举出其中的20种期刊。
《中国稀土学报》《功能材料》《无机材料学报》《无机化学学报》《人工晶体学学报》《硅酸盐通报》《材料科学与工艺》《SCI》《材料科学技术学报(英文版)》《材料工程》《材料导报》《纳米科技》《Chemistry of Materials》《Crystal Growth & Design》《Inorganic Chemistry》《ACS Nano》《NANO letter》《Solar energy materials and solar cells》《Rare Earth Bulletin 》《Journal of Applied Crystallography 》《Journal of the Energy Institute 》《半导体学报》《玻璃与搪瓷》《无机硅化合物》《材料研究学报》;(10)《crystal growth and disign》;(11)《internatianal journal of inorganic materials》;(12)《inorganic materials 》;(13)《crystal research and techonolgy》;(14);《journal of crystal growth 》;(15)《inorganic chemistry》;(16)《advanced founctional materials》;(17)《chemistry of materials》;(18)《japanese new materials》;(19)《journal of materials chemistry》;(20)《advanced materials》。
《物理化学》课后习题答案(天津大学第四版)

因此,由标准摩尔生成焓
由标准摩尔燃烧焓
2.37 已知25 °C甲酸甲脂(HCOOCH3, l)的标准摩尔燃烧焓 为 ,甲酸(HCOOH, l)、甲醇(CH3OH, l)、水 (H2O, l)及二氧化碳(CO2, g)的标准摩尔生成焓 分别 为 、 、 及 应用这些数据求25 °C时下列反应的标准摩尔反应焓。 解:显然要求出甲酸甲脂(HCOOCH3, l)的标准摩尔生成焓
2.14 容积为27 m3的绝热容器中有一小加热器件,器壁上有一小孔与 100 kPa的大气相通,以维持容器内空气的压力恒定。今利用加热器 件使器内的空气由0 °C加热至20 °C,问需供给容器内的空气多少 热量。已知空气的 假设空气为理想气体,加热过程中容器内空气的温度均匀。 解:在该问题中,容器内的空气的压力恒定,但物质量随温度 而改变
-46.11
NO2(g) 33.18
90.25
HNO3(l) -174.10
-241.818
Fe2O3(s) -824.2
-285.830 CO(g) -110.525
(1) (2) (3)
2.35 应用附录中有关物资的热化学数据,计算 25 °C时反应 的标准摩尔反应焓,要求: (1) 应用25 °C的标准摩尔生成焓数据; (2) 应用25 °C的标准摩尔燃烧焓数据。 解:查表知
可由
表出(Kirchhoff公式)
设甲烷的物质量为1 mol,则 最后得到
,
,
,
第三章 热力学第二定律
3.1 卡诺热机在 的高温热源和 的低温热源间工作。 求(1) 热机效率 ; (2) 当向环境作功 时,系统从高温热源吸收的热 及 向低温热源放出的热 。
固体物理 第三章 相图
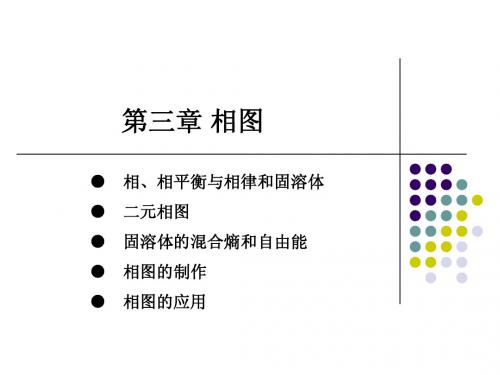
相图分析(相图三要素) (1)点:纯组元熔点;共晶点等。 (2)线:结晶开始、结束线;溶解度曲线;共晶线等。 (3)区:3个单相区;3个两相区;1个三相区。
(1)Sn<2%的合金 凝固过程(冷却曲线、相变、组织示意图)。
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning™ is a trademark used herein under license.
共晶合金
%
de cd 100%; % 100% ce ce
合金的平衡结晶及其组织(以Pb-Sn相图为例)
(4)亚共晶合金 ① 凝固过程(冷却曲线、相变、组织示意图)。 ② 共晶线上两相的相对量计算。 ③ 室温组织(α+βⅡ+(α+β))及其相对量计算。
(c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning™ is a trademark used herein under license. (c)2003 Brooks/Cole, a division of Thomson Learning, Inc. Thomson Learning™ is a trademark used herein under license.
+ Ld c
+ e
共晶转变:由一定成分的液相同时结晶出两个一定成分固相 的转变。 共晶相图:具有共晶转变特征的相图。 (液态无限互溶、固态有限互溶或完全不溶,且发生共 晶反应)。 共晶组织:共晶转变产物。(是两相混合物)
特征:三相点的温度低于A 和B的纯组元的凝固点
固体物理学习题解答

:
对于氯化钠晶胞:
(1)当衍射面指数全为偶数时, 衍射强度最大,
(2)当衍射面指数全为奇数时, 由于 与 具有不同的散射本领,使衍射指数全为奇数的衍射具有不为零但较低的强度。
6.试求金刚石型结构的几何结构因子,设原子散射因子为 。
解:几何结构因子
其中
为晶胞的体积。
。
金刚石型结构的晶胞内八个原子的位矢为(0 0 0),(1/2 1/2 1/2),(1/2 0 1/2),(0 1/2 1/2),(1/4 1/4 1/4),(3/4 3/4 1/4),(3/4 1/4 3/4),(1/4 3/4 3/4)且八个原子为同种原子,
由此可得面心立方的倒格子基矢:
同理可得体心立方的倒格子基矢:
比较可得面心立方和体心立方互为正倒格子。
2. 为简单正交格子的基矢,试证明晶面族(h k l)的晶面间距为
解:
由 知
可得:
再由 中 和 的关系: 可得:
得证。
3.六角密集结构如取如下原胞基矢
试写出其倒格子基矢。
方法一:
解得。
方法二:由正格子和倒格子之间的关系:
所以,其夹角的余弦为:
5.试求面心立方结构(110)和(111)晶面族的原子数面密度,设晶格常数为a。
解:
如图所示,面ABCD即(110)面,面CDE即为(111)面。设该面心立方的晶格常数为a,则
在(110)面内选取只包含一个原子的面AFGD,其面积为 ,所以其原子数面密度为:
在(111)面内选取只包含一个原子的面DHIG,其面积为: ,
杨氏模量为
故,
光波波长为
8.立方晶体有三个弹性模量 , 和 。铝的 , ,铝沿 方向传播的弹性纵波的速度 ,横波速度 , 的密度 。求德拜模型中铝的振动模式密度 。
方俊鑫版固体物理习题解答

方一陆固物习题参考答案1、布格子:每个原胞内只有一个原子的晶格或组成晶体结构的基元之结点:如以Cl 原子为结点,取面心立方晶胞,就是NaCl 的布氏格子;金刚石结构中位于正四面体中心的原子和顶角上的原子化学组份虽相同,但电子云配置方位不同,所以是复式格子。
2、如以321,,→→→a a a 为正格子基矢则满足。
当相应的同理得则得相应格点则得当令法线上确定一长度在面间距为则对应晶石的所决定之晶石矢标面为正晶格内原胞基座含晶格之倒格子确定的格子叫的或Ω⨯=Ω⨯=±±=Ω⨯===⨯⋅=Ω=Ω⨯=Ω⨯=⋅=⋅→→→→→→→→→→→→→→→→→→→→→→→→→→→→→313132321213212132132132131323212;2,2,12,10,2,,,,,,,,)(,2,22a a b a a b a a b d a a d a a a a a a a b b b a a a b a a b a a b a a ij j i ππμπμπμρρπππδ.,,,,2,1321个倒格点集合即得整原胞在倒易空间中平移即相当于以时→→→±±=b b b μ3、体心立方格子和面心立方格子互为正倒格子,试证明之。
设体心立方格子的结晶学晶胞(Convention cell )的基矢是,,11→→→c b a 令→→→k j ,,i 为直角坐标的三个互垂直的单位矢a k c a jb a i a →→→→→===,,这个体心立方格子的固体物理学原胞(Primitive cell )的三个基矢,按规定)(2),(2),(2321→→→→→→→→→→→→++=--=++-=k j a a k j a a k j a a λλλ的三个基矢理学原胞它们是倒点阵的固体物定义cell)(Primitive )(2)(2)(2)(221,2:321232332132321⎪⎪⎪⎪⎭⎪⎪⎪⎪⎬⎫+=+=+=+=⨯=⨯⋅=Ω==Ω⨯=→→→→→→→→→→→→→→→→→→→→→j i a b i k a b k j ab k j a a a a a a a b b a a b ππππ这个倒点阵的结晶学胞原(Convention cell )应当是显示其立方晶系对称性的最小重复单元。
物理化学课后习题与答案

逆过程。设气体的
Cv,m
=
3 2
R
。试计算各个状态的压力
p
并填下表。
V/dm3•mol-1
44.8 C B
22.4 A
273
546
T/K
1
步骤
A B C
过程的名称
等容可逆 等温可逆 等压可逆
Q/J W/J △U/J
8. 一摩尔单原子理想气体,始态为 2×101.325kPa、11.2dm3,经 pT = 常数的可逆过程(即过
(1) 298K 时的“平衡常数”; (2) 正、逆反应的活化能; (3) 反应热;
(4) 若反应开始时只有 A,pA,0=105Pa,求总压达 1.5×105Pa 时所需时间(可忽略逆反应)。
8.有一反应,其速率正比于反应物浓度和一催化剂浓度。因催化剂浓度在反应过程中不变, 故表现为一级反应。某温度下,当催化剂浓度为 0.01 mol·dm-3 时,其速率常数为 5.8×10-6 s-1。 试问其真正的二级反应速率常数是多少?如果催化剂浓度为 0. 10 mol·dm-3,表现为一级反应
4. 固体 CO2 的饱和蒸汽压在 -103℃ 时等于 10.226kPa,在 -78.5℃ 时等于 101.325 kPa,求: (1)CO2 的升华热;(2)在 -90℃ 时 CO2 的饱和蒸汽压。
5. 设你体重为 50kg,穿一双冰鞋立于冰上,冰鞋面积为 2cm3,问温度需低于摄氏零下几 度,才使冰不熔化?已知冰的 ΔfusHm = 333.4kJ·kg-1,水的密度为 1000 kg·m3,冰的密度为 900kg·m3。
(2) 1mol 水在 100℃恒 温下于真 空容器中 全部蒸发 为蒸气, 而且蒸气 的压力恰 好为
第03章化学反应系统热力学习题及答案物理化学

第三章 化学反应系统热力学习题及答案§ 标准热化学数据(P126)1. 所有单质的 Om f G ∆ (T )皆为零为什么试举例说明答:所有处于标准态的稳定单质的O m f G ∆ (T ) 皆为零,因为由稳定单质生成稳定单质的状态未发生改变。
如:单质碳有石墨和金刚石两种,O m f G ∆ ,石墨)=0,而O m f G ∆ ,金刚石)= kJ·mol -1 (课本522页),从石墨到金刚石状态要发生改变,即要发生相变,所以O m f G ∆ ,金刚石)不等于零。
2. 化合物的标准生成热(焓)定义成:“由稳定单质在和100KPa 下反应生成1mol 化合物的反应热”是否准确为什么答:标准生成热(焓)的定义应为:单独处于各自标准态下,温度为T 的稳定单质生成单独处于标准态下、温度为T 的1mol 化合物B 过程的焓变。
此定义中(1)强调压力为一个标准大气压,而不强调温度;(2)变化前后都单独处于标准态。
3. 一定温度、压力下,发生单位化学反应过程中系统与环境交换的热Q p 与化学反应摩尔焓变r m H ∆是否相同为什么答: 等压不作其他功时(W’=0),数值上Q p =n r H ∆。
但Q p 是过程量,与具体的过程有关;而r m H ∆是状态函数,与过程无关,对一定的化学反应有固定的数值。
如将一个化学反应至于一个绝热系统中,Q p 为零,但r m H ∆有确定的数值。
§ 化学反应热力学函数改变值的计算(P131)1. O m r G ∆(T )、m r G ∆(T )、O m f G ∆(B,相态,T )各自的含义是什么答:Om r G ∆(T ): 温度为T ,压力为P θ,发生单位反应的ΔG;m r G ∆(T ):温度为T ,压力为P ,发生单位反应的ΔG;Omf G ∆(B,相态,T ):温度为T ,压力为P θ,由各自处于标准状态下的稳定单质,生成处于标准态1mol 化合物反应的ΔG。
物理化学习题答案.

物理化学习题第一章热力学第一定律一、问答题1. 什么是系统?什么是环境?答:将一部分物质从其他部分中划分出来,作为研究的对象,这一部分物质就称为系统;系统之外与系统密切相关的部分称为环境。
2. 什么是状态函数?答:由系统状态确定的系统的各种热力学性质,称为系统的状态函数。
3. 什么是等压过程?答:在环境压力恒定下,系统始、终态压力相同且等于环境压力的过程。
4. 什么是热力学能?答:是系统中物质的所有能量的总和5. 什么是热力学第一定律?答:将能量守恒与转化定律应用于宏观的热力学系统即为热力学第一定律。
6. 什么是体积功答:因系统的体积变化而引起的系统与环境之间交换的功7. 可逆过程有哪些特点?答:(1)可逆过程是以无限小的变化进行,系统始终无限接近于平衡态,即整个过程由一系列无限接近于平衡的状态所构成。
(2)系统在可逆过程中作最大功,环境在可逆过程中作最小功,即可逆过程效率最高。
(3)沿与过程原来途径相反方向进行,可是系统和环境完全恢复原态,而没有任何耗散效应。
8. 什么是理想气体?答:分子本身不占有体积,分子之间没有作用力,实际不存在的假想气体。
当温度不是很低或很高,压力不是很低或很高,或没有其他特殊条件时,一般气体均视为理想气体。
9. 什么是标准摩尔生成焓?答:规定在标准压力p(100kpa)和指定温度T时,由最稳定单质生成标准状态下1摩尔化合物的焓变称为该化合物在此温度下的标准摩尔生成焓。
10. 夏天为了降温,采取将室内电冰箱门打开,接通电源并紧闭门窗(设墙壁门窗均不传热)。
该方法能否使室内温度下降?为什么?答:不能。
该情况相当于一个绝热系统中作电功,电机发热只能使室温升高。
二、判断题(正确打√,错误打×)1. 由于p和V都是状态函数,则pV也是状态函数。
(√)2. 状态函数改变后,状态一定改变。
(√)3. 孤立系统内发生的一切变化过程,其U Δ 必定为零。
(√)4. 温度越高, Q值越大。
固体物理 第三章_ 晶体中的缺陷

4
由以上讨论可知: 刃位错: 外加切应力的方向、原子的滑移方向和位错 线的运动方向是相互平行的。 螺位错: 外加切应力的方向与原子的滑移方向平行, 原子的滑移方向与螺位错的运动方向垂直。 在左右两部分受到向上和向下的切应力的作 用时,位错线向前移动,直到位错线移动到 尽头表面,这时左右两部分整个相对滑移b 的距离,晶体产生形变。
固体物理第三章
1. 热缺陷:由热起伏的原因所产生的空位和填隙原 子,又叫热缺陷,它们的产生与温度直接有关
(a) 肖脱基缺陷
(b)弗伦克耳缺陷
(c) 间隙原子
固体物理第三章
( a )肖特基缺陷 (vacancy) :原子脱离正常格点 移动到晶体表面的正常位置,在原子格点位置 留下空位,称为肖特基缺陷。 (b)弗伦克尔缺陷(Frenkel defect),原子脱离格 点后,形成一个间隙原子和一个空位。称为弗 伦克尔缺陷。 (c)间隙原子(interstitial):如果一个原子从正常 表面位置挤进完整晶格中的间隙位置则称为间 隙原子,由于原子已经排列在各个格点上,为 了容纳间隙原子,其周围的原子必定受到相当 大的挤压。
固体物理第三章 固体物理第三章
产生位错的外力: 机械应力:挤压、拉伸、切割、研磨 热应力:温度梯度、热胀冷缩 晶格失配: 晶体内部已经存在位错,只用较小的外力就 可推动这些位错移动,原来的位错成为了位错 源,位错源引起位错的增殖,有位错源的晶体 屈服强度降低。 晶体的屈服强度强烈地依赖于温度的变化。 T升高,原子热运动加剧,晶体的屈服强度下 降,容易产生范性形变。
固体物理第三章
在实际晶体中,由于存在某种缺陷,所以晶 面的滑移过程,可能是晶面的一部分原子 先发生滑移,然后推动同晶面的另一部分 原子滑移。按照这样的循序渐移,最后使 上方的晶面相对于下方的晶面有了滑移。 1934 年, Taylor( 泰勒 ), orowan( 奥罗万 ) 和 Polanyi( 波拉尼)彼此独立提出滑移是借助 于位错在晶体中运动实现的,成功解释了 理论切应力比实验值低得多的矛盾。
物理化学复习题答案(part 3)

[2]
s l dT T fusV T dp fus H fus H l s
(1)绘制对二甲苯和间二甲苯的熔点-组成图; (2)若有 100 kg 含对二甲苯的摩尔分数为 0.70 的溶液由 10 ℃冷至-15 ℃时, 能析出对 二甲苯多少? (3)当继续降温时,可析出纯对二甲苯最多能有多少千克?此时液相的质量为若干? 解 30:(1)绘制相图如下:
间二甲苯
x(对二甲苯)
对二甲苯
为 D) + 固相 B → 固体 AB2 (不稳定化合物)。此时,体系三相平衡,F*= 0,温度不能 改变,随温度不断冷却,固体 AB2 不断增加,液相量不断减少,直到溶液全部消失,剩下 固体 B 和 AB2,温度又不断下降。 [3 分]
30.
用热分析法测得对二甲苯和间二甲苯的步冷曲线转折点如下表所示:
答案(part 3)
相平衡部分 21. 指出下列各体系的独立组分数、相数和自由度数各为若干? (1)NH4Cl(s)部分分解为 NH3(g)和 HCl(g); (2)若在上述体系中再加入少量的 NH3(g); (3)NH4HS(s)和任意量的 H2S(g)和 NH3(g)混合达平衡; (4)C(s)与 CO(g),CO2(g),O2(g) 在 973 K 时达平衡。 解 21:(1) C S R R' 1=, P 2 F=C-P+2=1-2+2=1 (2) C S R R' 3 1 0 2 , P 2
[5 分]
(2)当温度从 P 点降到 O 点 (物系点) 时, 由图可看出, 液相组成为 x (对二甲苯) 056 . ,
设此时析出的对二甲苯的质量为 m ,则液相的质量应为(100 kg-m),根据杠杆规则: m(1.00-0.70)=(100 kg-m)(0.70-0.56) 解得: m=31.8 kg (3)设析出纯对二甲苯的质量为 m(s),则液相的质量 m(l)=100 kg-m(s), 则 m(s) (1.00-0.70)=[100 kg-m(s)] (0.70-0.133) 解得: m(s)=65.4 kg 故 m(l)=100 kg-65.4 kg=34.6 kg 31. 根据相图回答: [2 分]
