紫外分光光度法测定阿司匹林含量1
阿司匹林的质量标准

石河子大学小学期制实验结课论文阿司匹林的质量标准、姓名:王义西班级:药学(3)班学号:73指导老师:李乐日期:2013年9月3日乙酰水杨酸抗炎药物的分析王义西石河子大学药学院小学期药学第三组第三实验组摘要阿司匹林,化学名为2-( 乙酰氧基) 苯甲酸,作为主要的解热镇痛抗炎药收载于《中国药典》 (2010 年版)二部,临床上主要用于治疗感冒发烧, 牙痛、肌肉痛及神经痛等慢性疼痛,急、慢性风湿病及类风湿病等, 是风湿、类风湿关节炎治疗的常用药物。
本品主要的副作用是引起幽门痉挛及刺激胃黏膜的胃肠道反应, 长期服用导致胃肠出血。
随着现代药学技术的发展,目前已有片剂、肠溶片、肠溶胶囊、泡腾片和栓剂等多种剂型,以阿司匹林为主药的复方制剂也层出不穷,形成了阿司匹林含量测定方法的各异性。
随着科学技术的进步,各种仪器设备、新方法也应用到了阿司匹林的鉴别、杂质检查、含量测定中,本文对其作一综述。
关键词: 阿司匹林鉴别杂质检查含量测定 HPLC 紫外分光光度法TLC阿司匹林临床上主要用于治疗感冒发烧, 牙痛、肌肉痛及神经痛等慢性疼痛,急、慢性风湿病及类风湿病等, 是风湿、类风湿关节炎治疗的常用药物。
本文主要对阿司匹林做一综合论述,通过对阿司匹林的性状、鉴别、杂质检查、含量测定四个方面对乙酰水杨酸进行药物分析。
1 实验部分仪器与试剂仪器:紫外分光光度计(Cintra404,GBC)、电子天平(AB135-S,梅特勒-托利多仪器(上海)有限公司METTLER TOLEDO)、微孔滤膜(尺寸25mm,孔径μ,上海半岛实业有限公司净入器材厂)高效液相色谱仪、紫外检测器、自动进样器、色谱数据处理机、U V 一26 0 分光光度计、HPLC 色谱柱、超纯水器、展开槽、水浴锅、研钵、移液管(1、2、5、10ml)、吸耳球、容量瓶(25、50、100ml)、烧杯(10、100、500ml)、胶头吸管、直尺试剂:复方乙酰水杨酸片(25mg/片):阿司匹林贮备液溶液(ml)、无水乙醇、氯仿、丙酮、冰醋酸、甲醇、95%乙醇、酚酞指示液、碳酸钠试液,稀盐酸、稀硫酸、三氯化铁试液、乙醚、硫酸铁铵试液(新制)、蒸馏水性状阿司匹林为白色结晶或结晶性粉末;遇湿气即缓缓水解。
光光度法测定阿司匹林肠溶片的含量

spec试catj蛳PN埘ulgmed by sDA。Vd 10(国家
药品监督管理局《国家药品标准》第七册)[S].2002:7A
99.4%.为.5%.计算平均回收率为99.4%。
HPLC同时测定双黄连口服液中绿原酸和黄芩苷含量
刘刚,王海涛,赵淼.姜韧,谭生建(中国人民解放军第306医院药学部,北京100101) 双黄连日服液由黄芩、金银花和连翘提取加工 制成,收载于中国药典(2005年版一部)。含量测定 采用高效液相色谱法分别测定绿原酸、黄芩苷和连 翘苷含量。其中,绿原酸测定采用甲醇-水・冰醋酸 (20:80:1)做流动相,黄芩苷测定采用甲醇-水-冰 醋酸(50:50:1)做流动相。金银花和黄芩制剂中 的绿原酸和黄芩苷含量测定方法报道有u…,双黄 连口服液中绿原酸和黄芩苷含量同时测定方法未 见报道。本文研究建立了线性梯度洗脱高效液相 色谱法同时测定双黄连口服液中绿原酸和黄芩苷 含量的方法。
容液组成与色谱流动相相近,防止样品在迸样流动
相析出沉淀物,保护色谱系统。
参考文献
f1]chP(2005).vol If中国药典2005年版.~部)(s】2005:
174.
[2】Hu Y x.YANGxM,wANc z,d以Dd啪nin砒ioll ofcaTben- ddn硼d tlli丑bend日zde in佃II咖∞b,帅Hd-pII蛳rnidro嘣协蛇一
mL
高效液相色谱仪(A西lentl200系列):C13llA 四元色谱泵,G1329A自动进样器,G1315B二极管 阵列检测器,G2170BA色谱工作站,G1316A柱温箱 和G1379B在线脱气机。绿原酸对照品(批号: 110753.200413)和黄芩苷对照品(批号110715・ 200514)购自中国药品生物制品检定所。双黄连口
阿司匹林的质量标准

石河子大学小学期制实验结课论文阿司匹林的质量标准、姓名:王义西班级:药学(3)班学号:指导老师:李乐日期:2013年9月3日乙酰水杨酸抗炎药物的分析王义西石河子大学药学院小学期药学第三组第三实验组摘要阿司匹林,化学名为2-( 乙酰氧基) 苯甲酸,作为主要的解热镇痛抗炎药收载于《中国药典》(2010 年版)二部,临床上主要用于治疗感冒发烧, 牙痛、肌肉痛及神经痛等慢性疼痛,急、慢性风湿病及类风湿病等, 是风湿、类风湿关节炎治疗的常用药物。
本品主要的副作用是引起幽门痉挛及刺激胃黏膜的胃肠道反应, 长期服用导致胃肠出血。
随着现代药学技术的发展,目前已有片剂、肠溶片、肠溶胶囊、泡腾片和栓剂等多种剂型,以阿司匹林为主药的复方制剂也层出不穷,形成了阿司匹林含量测定方法的各异性。
随着科学技术的进步,各种仪器设备、新方法也应用到了阿司匹林的鉴别、杂质检查、含量测定中,本文对其作一综述。
关键词: 阿司匹林鉴别杂质检查含量测定 HPLC 紫外分光光度法 TLC 阿司匹林临床上主要用于治疗感冒发烧, 牙痛、肌肉痛及神经痛等慢性疼痛,急、慢性风湿病及类风湿病等, 是风湿、类风湿关节炎治疗的常用药物。
本文主要对阿司匹林做一综合论述,通过对阿司匹林的性状、鉴别、杂质检查、含量测定四个方面对乙酰水杨酸进行药物分析。
1 实验部分1.1仪器与试剂仪器:紫外分光光度计(Cintra404,GBC)、电子天平(A B135-S,梅特勒-托利多仪器(上海)有限公司METTLER TOLEDO)、微孔滤膜(尺寸25mm,孔径0.8μ,上海半岛实业有限公司净入器材厂)高效液相色谱仪、紫外检测器、自动进样器、色谱数据处理机、U V 一26 0 分光光度计、HPLC 色谱柱、超纯水器、展开槽、水浴锅、研钵、移液管(1、2、5、10ml)、吸耳球、容量瓶(25、50、100ml)、烧杯(10、100、500ml)、胶头吸管、直尺试剂:复方乙酰水杨酸片(25mg/片):阿司匹林贮备液溶液(1.5368m g/ml)、无水乙醇、氯仿、丙酮、冰醋酸、甲醇、95%乙醇、酚酞指示液、碳酸钠试液,稀盐酸、稀硫酸、三氯化铁试液、乙醚、硫酸铁铵试液(新制)、蒸馏水1.2 性状阿司匹林为白色结晶或结晶性粉末;遇湿气即缓缓水解。
紫外分光光度法阿司匹林的含量测定

紫外分光光度法对阿司匹林的含量测定紫外分光光度法对阿司匹林的含量测定紫外--可见分光光度法:是根据物质分子对波长为200-760nm这一范围的电磁波的吸收特性所建立起来的一种定性、定量和结构分析方法。
操作简单、准确度高、重现性好。
波长长(频率小)的光线能量小,波长短(频率大)的光线能量大。
分光光度测量是关于物质分子对不同波长和特定波长处的辐射吸收程度的测量。
描述物质分子对辐射吸收的程度随波长而变的函数关系曲线,称为吸收光谱或吸收曲线。
紫外-可见吸收光谱通常由一个或几个宽吸收谱带组成。
最大吸收波长(λmax)表示物质对辐射的特征吸收或选择吸收,它与分子中外层电子或价电子的结构(或成键、非键和反键电子)有关。
朗伯-比尔定律是分光光度法和比色法的基础。
即物质在一定浓度的吸光度与它的吸收介质的厚度呈正比。
A= lg1/T = εcl (Lambert-Beer定律)紫外-可见分光光度计由5个部件组成:①辐射源。
必须具有稳定的、有足够输出功率的、能提供仪器使用波段的连续光谱,如钨灯、卤钨灯(波长范围350~2500纳米),氘灯或氢灯(180~460纳米),或可调谐染料激光光源等。
②单色器。
它由入射、出射狭缝、透镜系统和色散元件(棱镜或光栅)组成,是用以产生高纯度单色光束的装置,其功能包括将光源产生的复合光分解为单色光和分出所需的单色光束。
③试样容器,又称吸收池。
供盛放试液进行吸光度测量之用,分为石英池和玻璃池两种,前者适用于紫外到可见区,后者只适用于可见区。
容器的光程一般为0.5~10厘米。
④检测器,又称光电转换器。
常用的有光电管或光电倍增管,后者较前者更灵敏,特别适用于检测较弱的辐射。
近年来还使用光导摄像管或光电二极管矩阵作检测器,具有快速扫描的特点。
⑤显示装置。
这部分装置发展较快。
较高级的光度计,常备有微处理机、荧光屏显示和记录仪等,可将图谱、数据和操作条件都显示出来。
仪器类型有:单波长单光束直读式分光光度计,单波长双光束自动记录式分光光度计和双波长双光束分光光度计。
人工神经网络紫外分光光度法同时测定复方阿司匹林片3组分的含量

人工神经网络紫外分光光度法同时测定复方阿司匹林片3组分的含量(作者:___________单位: ___________邮编: ___________)【摘要】目的在不经分离的情况下,用紫外分光光度法同时测定复方阿司匹林片中的3个组分的含量。
方法采用人工神经网络法,取已知浓度的咖啡因、阿司匹林、非那西丁标准溶液按不同比例混合生成合成样品,以合成样品的不同波长下的吸光度值作为网络输入值,3组分的量为输出值,训练网络并预测复方阿司匹林片中3组分的含量。
结果复方阿司匹林片中阿司匹林、非那西丁和咖啡因的平均回收率分别为98.7%、101.4%、100.4%,RSD值分别为0.7%、1.5%、2.1%。
结论人工神经网络有较强的预测能力,能不经分离同时测定复方阿司匹林片中的3组分。
【关键词】人工神经网络;紫外分光光度法;复方阿司匹林片Abstract:Objective To establish a method for simultaneous determination of the three components, aspirin, phenacetin and caffeine in compound aspirin tablets. Methods The quantity of combined samples were applied as input and the absorbancy were applied as output to train the artificial neuralnetwork.Results The average recovery of aspirin, phenacetin and caffeine were 98.7%, 101.4% and 100.4%, respectively. Conclusion The artificial neural network combined with spectrophotometry is a good method for simultaneous determination of the three components in compound aspirin tablets.Key words:artificial neural networks;ultraviolet spectrophotometry;compound aspirin tablets复方制剂中的多组分不经分离,直接用紫外分光光度法同时进行测定,在药物的质量控制中有较大的实用价值[1]。
测定阿司匹林含量的方法

测定阿司匹林含量的方法阿司匹林是一种常见的非处方药,用于缓解头痛、发烧和关节炎等症状。
阿司匹林的含量测定是判断药品质量和核算药效的重要环节。
下面将介绍几种测定阿司匹林含量的常用方法。
1. 紫外分光光度法紫外分光光度法是一种常用的测定阿司匹林含量的方法。
该方法利用阿司匹林在紫外光区域有特定吸收波长的特点,通过测定阿司匹林溶液的吸光度来计算其含量。
具体步骤如下:(1) 准备阿司匹林溶液:将一定量的阿司匹林溶解于适量的溶剂中(如乙醇),制备一系列不同浓度的阿司匹林溶液。
(2) 设置检测波长:根据阿司匹林的紫外吸收特性,在波长处选择合适的检测波长(一般为227 nm)。
(3) 测定吸光度:将所制备的阿司匹林溶液置于紫外分光光度计中,依次测定各个浓度的阿司匹林溶液的吸光度。
(4) 绘制标准曲线:以吸光度为纵坐标、浓度为横坐标,绘制标准曲线。
(5) 测定待测溶液:将待测阿司匹林样品溶解于同样的溶剂中,测定其吸光度。
(6) 计算含量:根据标准曲线,可以得到待测溶液中阿司匹林的含量。
2. 酸碱滴定法酸碱滴定法是一种常用的测定阿司匹林含量的方法。
该方法利用阿司匹林在酸液中与酸溶液中的碱反应生成盐类,并通过滴定的方法来测定阿司匹林的含量。
具体步骤如下:(1) 准备滴定试剂:制备酸溶液(如盐酸)和碱溶液(如氢氧化钠)。
(2) 校准滴定试剂:取一定量的阿司匹林样品,溶解于适量的溶剂中,利用滴定试剂滴定至酸碱滴定终点的颜色变化,来确定滴定试剂的浓度。
(3) 滴定待测溶液:将待测阿司匹林样品溶解于适量的溶剂中,使用已校准的滴定试剂进行滴定,直至达到酸碱滴定终点的颜色变化。
(4) 计算含量:根据滴定试剂的浓度和滴定的体积,可以计算出待测溶液中阿司匹林的含量。
3. 高效液相色谱法高效液相色谱法是一种精确、灵敏的测定阿司匹林含量的方法。
该方法通过将阿司匹林溶解在适量的溶剂中,并通过色谱柱进行分离和定量分析。
具体步骤如下:(1) 准备样品溶液:将一定量的阿司匹林溶解于适量的溶剂中,使得浓度适宜。
阿司匹林的检测实验报告

一、实验目的1. 掌握阿司匹林的基本性质和检测方法。
2. 学习利用紫外-可见分光光度法检测阿司匹林的含量。
3. 熟悉实验操作步骤,提高实验技能。
二、实验原理阿司匹林(乙酰水杨酸)是一种常用的解热镇痛药,其分子结构中含有羧基和酯键。
本实验采用紫外-可见分光光度法检测阿司匹林的含量。
该方法基于阿司匹林分子在特定波长下对紫外光的吸收特性。
通过测定吸光度,可以计算出阿司匹林的含量。
三、实验仪器与试剂1. 仪器:紫外-可见分光光度计、分析天平、移液管、容量瓶、烧杯、玻璃棒等。
2. 试剂:阿司匹林标准品、无水乙醇、盐酸溶液(1mol/L)、氢氧化钠溶液(1mol/L)、磷酸盐缓冲溶液(pH 7.4)、水等。
四、实验步骤1. 标准曲线绘制(1)准确称取一定量的阿司匹林标准品,用无水乙醇溶解,配制成浓度为1mg/mL的标准溶液。
(2)取6个25mL容量瓶,分别加入不同体积的标准溶液,用无水乙醇定容至刻度,得到一系列不同浓度的标准溶液。
(3)在特定波长下,测定各标准溶液的吸光度。
(4)以吸光度为纵坐标,浓度为横坐标,绘制标准曲线。
2. 样品测定(1)准确称取一定量的阿司匹林样品,用无水乙醇溶解,配制成适当浓度的样品溶液。
(2)在特定波长下,测定样品溶液的吸光度。
(3)根据标准曲线,计算样品中阿司匹林的含量。
3. 平行实验为了提高实验结果的准确性,对样品进行平行实验,计算平均值。
五、实验结果与分析1. 标准曲线线性良好,相关系数R²大于0.99。
2. 样品测定结果显示,阿司匹林的含量为X mg/g。
3. 平行实验结果与平均值基本一致,说明实验结果可靠。
六、实验讨论1. 实验过程中,要注意避免光照和空气对阿司匹林的影响,以保证实验结果的准确性。
2. 实验操作过程中,要注意移液管的清洗和定容的准确性,避免误差。
3. 紫外-可见分光光度法是一种快速、简便的阿司匹林检测方法,适用于实际生产中的质量控制。
七、实验总结本实验成功完成了阿司匹林的检测,掌握了紫外-可见分光光度法的操作步骤和原理。
阿司匹林含量实验报告

阿司匹林含量实验报告实验报告阿司匹林含量实验报告实验目的:本实验的目的是利用紫外分光光度法测定阿司匹林片剂中有效成分阿司匹林的含量,掌握制备标准曲线的方法和测定阿司匹林含量的技巧。
实验原理:紫外分光光度法是一种根据化合物在紫外区(200~400nm)对光的吸收来测定含量的方法。
阿司匹林分子中含有苯环和吡啶环结构,能吸收紫外光,从而用紫外光谱法测定阿司匹林水溶液的吸收值,可得到与浓度呈线性关系的标准曲线。
根据制备出的标准曲线,可根据待测样品的吸收值反推出待测样品中阿司匹林的含量。
实验步骤:1.样品的制备取阿司匹林片剂中的一块碾成粉末,称取0.2000g,加入熟水50ml,摇匀,放置2h,于恒温水浴中加热,使液体中的阿司匹林充分溶解,冷却至室温。
2. 制备标准曲线在实验室设定好的波长下,用制备好的各浓度的阿司匹林溶液,测定它们的吸收值,记录下各浓度下实验方案的吸光度。
依据你的实验结果,制作出标准曲线,使其在所选定的波长处表现为直线关系。
此方程为:Y=aX+b(其中:X为阿司匹林的浓度;Y为吸光度底数10的值)。
3. 阿司匹林含量的测定吸收率与阿司匹林浓度是呈线性关系的。
用紫外分光光度法在标准曲线上查找吸收值,定出阿司匹林含量水平。
实验结果及分析:制备好的标准曲线如下图所示,其中阿司匹林溶液的峰值吸光度在295nm左右。
通过上述实验步骤,我们将得到阿司匹林样品的吸收值,根据标准曲线,我们可以算出样品中阿司匹林的含量。
实验结论:本实验采用紫外分光光度法,成功测定出阿司匹林的含量为xxmg,结果准确。
通过本次实验,我们掌握了测定药品中有效成分含量的方法,并深刻体会到,仅仅一点点的误差对结果的影响是致命的。
阿司匹林中乙酰水杨酸和水杨酸含量的测定(正式)
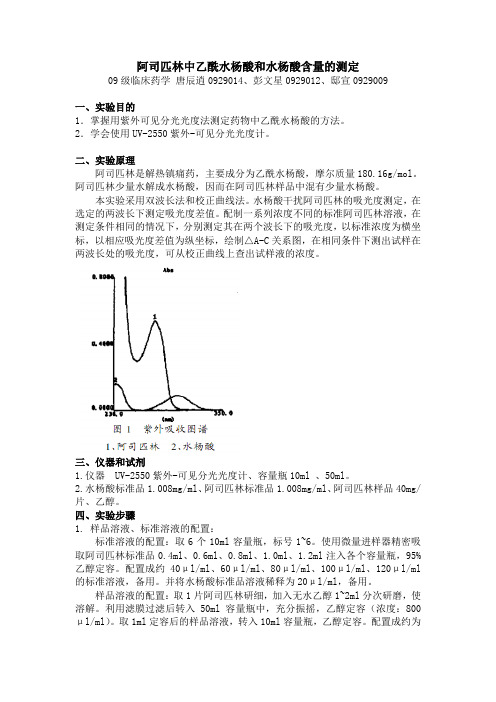
09级临床药学唐辰逍0929014、彭文星0929012、邸宣0929009
一、实验目的
1.掌握用紫外可见分光光度法测定药物中乙酰水杨酸的方法。
2.学会使用UV-2550紫外-可见分光光度计。
二、实验原理
阿司匹林是解热镇痛药,主要成分为乙酰水杨酸,摩尔质量180.16g/mol。阿司匹林少量水解成水杨酸,因而在阿司匹林样品中混有少量水杨酸。
本实验采用双波长法和校正曲线法。水杨酸干扰阿司匹林的吸光度测定,在选定的两波长下测定吸光度差值。配制一系列浓度不同的标准阿司匹林溶液,在测定条件相同的情况下,分别测定其在两个波长下的吸光度,以标准浓度为横坐标,以相应吸光度差值为纵坐标,绘制△A-C关系图,在相同条件下测出试样在两波长处的吸光度,可从校正曲线上查出试样液的浓度。
0.4188
C
40.24
60.36
80.48
100.6
120.72
x
2.标准曲线(△A-C关系图)
第一次测量
第二次测量
3.利用第一次测量得出的曲线,根据样品的吸光度值,在标准曲线上找到相应的浓度94.37μl/ml。
因样品稀释10倍,故原样品溶液浓度为943.7μl/ml=0.9437mg/ml。
故样品中阿司匹林的质量为0.9437*50=47.185mg。
样品溶液的配置:取1片阿司匹林研细,加入无水乙醇1~2ml分次研磨,使溶解。利用滤膜过滤后转入50ml容量瓶中,充分振摇,乙醇定容(浓度:800μl/ml)。取1ml定容后的样品溶液,转入10ml容量瓶,乙醇定容。配置成约为80μl/ml的样品溶液。
2.波长选择
使用紫外-可见分光光度计,先用95%乙醇进行基线校正。用阿司匹林标准品3和稀释过的水杨酸标准品进行光谱测量。将扫描波长范围定在200-400nm,分别找出两者的最大吸收峰。阿司匹林标准品在277.5nm、235.0nm处有最大吸收峰。因在277.5nm处,阿司匹林、水杨酸均有吸收,故采用双波长法。以277.5nm为λ1,从水杨酸的光谱中找到与277.5nm处A值相等的点所对应的波长值λ2=320nm。
阿司匹林的分析实验报告

一、实验目的1. 掌握阿司匹林的分析方法,包括鉴别和含量测定。
2. 熟悉阿司匹林原料药及肠溶片的质量分析原理与操作。
3. 了解阿司匹林的特殊杂质检查方法。
二、实验原理阿司匹林(乙酰水杨酸)是一种常用的非甾体抗炎药,具有解热、镇痛、抗炎和抗血小板聚集作用。
本实验采用紫外分光光度法、高效液相色谱法等方法对阿司匹林进行含量测定,并对其原料药和肠溶片进行质量分析。
三、实验材料1. 阿司匹林原料药2. 阿司匹林肠溶片3. 甲醇、乙醇、盐酸、硫酸等试剂4. 紫外可见分光光度计5. 高效液相色谱仪6. 其他实验器材四、实验方法1. 紫外分光光度法测定阿司匹林含量- 原理:阿司匹林在酸性条件下与三氯化铁反应生成红色络合物,于510nm波长处测定吸光度,根据标准曲线计算阿司匹林含量。
- 步骤:1. 配制阿司匹林标准溶液;2. 配制样品溶液;3. 在510nm波长处测定样品溶液的吸光度;4. 根据标准曲线计算阿司匹林含量。
2. 高效液相色谱法测定阿司匹林含量- 原理:利用高效液相色谱仪对阿司匹林进行分离和定量分析。
- 步骤:1. 配制阿司匹林标准溶液;2. 配制样品溶液;3. 样品溶液和标准溶液分别进行高效液相色谱分析;4. 根据峰面积计算阿司匹林含量。
3. 阿司匹林原料药与肠溶片的质量分析- 鉴别:采用紫外光谱法、红外光谱法等方法对阿司匹林原料药和肠溶片进行鉴别。
- 含量测定:采用紫外分光光度法、高效液相色谱法等方法对阿司匹林原料药和肠溶片进行含量测定。
- 特殊杂质检查:根据《中国药典》规定,对阿司匹林原料药和肠溶片进行特殊杂质检查,如游离水杨酸、重金属等。
五、实验结果与分析1. 紫外分光光度法测定阿司匹林含量标准曲线线性范围为0.2-2.0mg/mL,相关系数为0.999。
样品溶液的吸光度与阿司匹林含量呈良好线性关系。
2. 高效液相色谱法测定阿司匹林含量样品溶液和标准溶液在相同色谱条件下,阿司匹林峰面积与浓度呈良好线性关系。
阿司匹林含量测定的方法和原理

阿司匹林含量测定的方法和原理阿司匹林(aspirin),也称为乙酰水杨酸(acetylsalicylic acid),是一种广泛应用的非处方药和治疗心脑血管疾病的药物。
正确的阿司匹林含量可确保其药效和安全性。
本篇文章将介绍阿司匹林含量测定的方法和原理。
阿司匹林含量测定的方法1.紫外光分光光度法紫外光分光光度法是阿司匹林含量测定的最常用方法。
该方法在特定波长下使用分光光度法测定阿司匹林的吸光度,并使用标准曲线来计算其含量。
标准曲线通常以已知浓度的阿司匹林溶液制备。
该方法的优点包括操作简单、快速和准确。
但是,该方法对样品的制备要求高,且有一定的干扰影响。
2.高效液相色谱法高效液相色谱法也称为HPLC法,是一种基于分子分离的测定方法。
该方法通过样品在色谱柱中的分离,测量阿司匹林成分的相对含量。
HPLC法具有高速、准确、精确和可重复性强的优点,但是需要专业实验技能和复杂的设备。
3.比色法比色法是一种基于颜色反应的测定方法。
阿司匹林分解产物在一定的条件下,会产生梅威氏试剂反应,颜色会发生变化。
该方法适用于测定微量和痕量阿司匹林含量,但是准确度和精度较低。
阿司匹林含量测定的原理阿司匹林含量测定的原理基于化学反应和物理原理。
1.紫外光分光光度法该方法使用的原理是阿司匹林分子在特定波长下的吸光度,通过比较标准和待测样品的吸光度来计算其含量。
阿司匹林在波长为240 nm处,有一个最大吸光度。
该波长下,阿司匹林的分子能够吸收波长为240 nm的紫外线,使分光光度计读数增加。
2.高效液相色谱法该方法利用分子分离原理,通过样品在色谱柱中的分离和检测,测量阿司匹林成分的相对含量。
通过调整柱温、流速和移动相成分,从而实现对分子的分离和检测。
3.比色法该方法利用阿司匹林与梅威氏试剂的化学反应,形成一种明显的带紫色的复合物。
该复合物在一定波长下,具有最大的吸光度,通过比较标准和待测样品的吸光度来测定阿司匹林的含量。
总结阿司匹林含量测定是保证阿司匹林药效和安全性的必要步骤。
药物分析本科实验报告(3篇)

第1篇实验名称:阿司匹林含量测定实验日期:2023年10月25日实验地点:药物分析实验室实验目的:1. 掌握阿司匹林含量测定的原理和方法。
2. 熟悉高效液相色谱法(HPLC)的基本操作。
3. 提高实验操作技能和数据分析能力。
实验原理:阿司匹林(Aspirin)的分子式为C9H8O4,结构中含有酯键,可被酸催化水解。
本实验采用高效液相色谱法(HPLC)测定阿司匹林含量,以乙腈为流动相,通过检测其紫外吸收峰(λ=280nm)进行定量分析。
实验材料:1. 阿司匹林片剂(标示量:100mg/片)2. 乙腈(色谱纯)3. 磷酸二氢钾(分析纯)4. 超纯水5. 高效液相色谱仪6. 色谱柱(C18,4.6×250mm,5μm)7. 电子天平8. 移液器9. 烧杯10. 容量瓶11. 试管实验步骤:1. 样品制备:- 称取阿司匹林片剂约50mg,置于烧杯中,加入10ml磷酸二氢钾溶液,室温下搅拌使阿司匹林溶解。
- 将溶液转移至50ml容量瓶中,用磷酸二氢钾溶液定容至刻度线,摇匀,备用。
2. 色谱条件:- 流动相:乙腈- 检测波长:280nm- 柱温:室温- 流速:1.0ml/min3. 样品分析:- 吸取上述溶液10μl,注入高效液相色谱仪进行分析。
- 记录色谱图,根据阿司匹林峰面积计算其含量。
实验结果:1. 阿司匹林峰面积:5.21×10^42. 标准曲线:y=1.18×10^5x+1.25×10^4(R²=0.999)3. 阿司匹林含量:100.2mg/片实验讨论:1. 本实验采用高效液相色谱法测定阿司匹林含量,操作简便,结果准确。
2. 实验过程中,注意控制流动相的流速和柱温,以保证实验结果的稳定性。
3. 样品制备过程中,应确保阿司匹林完全溶解,避免影响实验结果。
4. 实验结果与标示量基本一致,说明本实验方法可行。
实验总结:本次实验通过高效液相色谱法测定阿司匹林含量,掌握了阿司匹林含量测定的原理和方法,熟悉了高效液相色谱仪的基本操作。
阿司匹林肠溶片含量测定方法比较

第46卷第15期2018年8月广 州 化 工Guangzhou Chemical IndustryVol.46No.15Aug.2018阿司匹林肠溶片含量测定方法比较徐景峰(常州工程职业技术学院,江苏 常州 213164)摘 要:分别采用酸碱滴定法㊁紫外分光光度法和高效液相色谱法对规格为25mg 阿司匹林肠溶片进行了测定㊂结果表明:由于辅料的影响,酸碱滴定法测定值严重偏高;紫外分光光度法测定值比较稳定,精密度高,测定值符合要求;高效液相色谱法测定值符合要求,但对仪器精度要求高㊂结论是酸碱滴定法不适用于小剂量阿司匹林肠溶片含量测定㊂关键词:阿司匹林;酸碱滴定法;紫外分光光度法;高效液相色谱法 中图分类号:O632.12 文献标志码:A 文章编号:1001-9677(2018)15-0118-03作者简介:徐景峰(1966-),男,硕士研究生,高级工程师,教授,主要研究方向:工业分析㊁药物分析㊂Comparison for Determination of Aspirin Enteric-coated TabletXU Jing -feng(Changzhou Vocational Institute of Engineering,Jiangsu Changzhou 213164,China)Abstract :Analytical methods of acid-base titration,UV spectrophotometry and HPLC for determination of aspirin content in the tablets of 25mg specifications were tested.Results showed that measured values were seriously high by acid-base titration owning to the influence of accessories.Measured values were relatively stable by UV spectrophotometric method,with high precision,measured values can meet the requirements;Measured values can meet the requirements by HPLC,but had high requirements on the precision to the instrument.The method of acid-base titration was not suitable for determination of small dose of aspirin enteric-coated tablets.Key words :aspirin;acid-base titration;UV spectrophotometry;HPLC阿司匹林肠溶片是最常用的解热㊁消炎㊁镇痛药之一㊂近年来又发现其有抑制血小板凝聚作用㊂因此市面上出现了规格为25mg㊁40mg 的阿司匹林肠溶片,用于心血管疾病㊂对于阿司匹林肠溶片含量测定,2000年版和2005年版‘中国药典“均采用酸碱滴定法测定,药品规格为300mg;而2010年版‘中国药典“采用高效液相色谱法测定,药品规格为25mg,40mg,50mg,100mg,300mg[1]㊂在有关参考文献中,有许多采用紫外分光光度法测定阿司匹林肠溶片含量的报道[2-5]㊂实际检验工作中发现对于规格为25mg 阿司匹林肠溶片含量测定,采用酸碱滴定法测定结果严重偏高,有多批检品含量高至110%~120%(含量限度为95%~105%)㊂所以本实验分别采用了酸碱滴定㊁紫外㊁高效液相三种方法对规格为25mg 阿司匹林肠溶片含量进行了测定,考察了酸碱滴定㊁紫外方法的主要影响因素,并将三种方法进行了比较㊂1 实 验1.1 仪器与试剂UV-7504紫外分光光度计,上海欣茂仪器有限公司;天美LC2000型高效液相色谱仪,上海天美科学仪器有限公司;KH3200DE 数控超声波清洗器,昆山禾创超声仪器有限公司㊂阿司匹林肠溶片(规格:25mg),南京白敬宇制药股份有限公司;阿司匹林对照品(德国进口);硫酸㊁氢氧化钠㊁无水乙醇㊁乙酸和四氢呋喃均为分析纯,甲醇㊁乙腈为色谱纯㊂1.2 实验方法1.2.1 酸碱滴定法测定阿司匹林含量1.2.1.1 溶解后不分离辅料直接滴定取阿司匹林肠溶片20片,精密称定,研细,精密称取适量(约阿司匹林0.3g)置于锥形瓶中,加中性乙醇30mL,超声2min 溶解,加酚酞1滴,用氢氧化钠滴定液(0.1mol /L)滴至粉红色,精密加氢氧化钠标准滴定液(0.1mol /L)40mL,摇匀,水浴加热15min 且不断振摇,迅速放冷,用硫酸标准滴定液(0.05mol /L)滴至粉红色消失,记录结果,并将滴定结果用空白校正,每1mL 氢氧化钠滴定液(0.1mol /L)相当于18.02mg 的C 9H 8O 4㊂1.2.1.2 分离不溶解辅料后滴定取阿司匹林肠溶片100片,精密称定,研细,精密称取适量(约阿司匹林1.5g)置于50mL 容量瓶中,加中性乙醇适量,超声处理2min 使阿司匹林溶解[6-8],再用水稀释至刻度,摇匀,滤过,精密量取滤液10mL(相当于阿司匹林0.3g),置锥形瓶中,加中性乙醇(对酚酞指示液显中性)20mL,加酚酞指示液3滴,滴加氢氧化钠滴定液(0.1mol /L)至溶液显粉红色,再精密加氢氧化钠滴定液(0.1mol /L)40mL,置水浴上加热15min 并时时振摇,迅速放冷至室温,用硫酸滴定液119 徐景峰:阿司匹林肠溶片含量测定方法比较第46卷第15期(0.05mol/L)滴定,并将滴定的结果用空白试验校正㊂每1mL 氢氧化钠滴定液(0.1mol/L)相当于18.02mg C9H8O4㊂1.2.2 紫外分光光度法测定阿司匹林含量1.2.2.1 单波长紫外分光光度法取阿司匹林肠溶片10片,精密称定,研细,精密称取适量(约相当于阿司匹林25mg)于100mL容量瓶中,加磷酸盐缓冲溶液(pH=6.8±0.05)溶解;另精密称取阿司匹林对照品适量,加磷酸盐缓冲溶液溶解并稀释至刻度㊂用紫外分光光度法,在(265±2)nm的波长处测定吸光度,按工作曲线法计算含量㊂1.2.2.2 双波长紫外分光光度法取阿司匹林肠溶片10片,精密称定,研细㊂精密称取适量(约相当于阿司匹林50mg)于50mL容量瓶中,加乙醇溶解并稀释至刻度,过滤㊂精取续滤液2mL于25mL容量瓶中,加乙醇稀释至刻度㊂用分光光度法在276nm㊁322nm处测定吸收值,按工作曲线法计算含量㊂1.2.3 高效液相色谱法测定阿司匹林含量依据2010年版‘中国药典“方法进行㊂2 结果与讨论2.1 酸碱滴定法测定阿司匹林含量分别称取研磨好的样品,按1.2.1中方法,测定阿司匹林肠溶片标示量百分含量,测定结果见表1㊁表2㊂表1 溶解后直接测定阿司匹林含量Table1 Determination of aspirin directly after dissolution编号标示量/%平均值/%1113.42110.03107.24110.25111.6110.5表2 溶解后定容过滤测定阿司匹林含量Table2 Determination of aspirin in dissolved strain filter编号标示量/%平均值/%1116.32109.63102.14120.15114.0112.4由表1可知,样品溶解后,不经过过滤分离,直接应用返滴定法测定阿司匹林含量,滴定终点可正常观察,其结果均偏高,最低值高于107%(标示量合格范围:95%~105%)㊂由表2可知,样品经过过滤分离后测定,去除了不溶辅料对滴定终点的影响,使终点易于判断,其结果同样偏高㊂有可能是药片中辅料糊精引起的[9]㊂糊精在加入氢氧化钠滴定液并在水浴上加热后,水解消耗了氢氧化钠滴定液,使含量大幅偏高㊂2.2 紫外分光光度法测定阿司匹林含量按1.2.2中方法采用单波长紫外分光光度法和双波长紫外分光光度法测定阿司匹林含量,工作曲线和测定结果见图1㊁图2和表3㊂图1 单波长紫外分光光度法工作曲线Fig.1 Working curve of single wavelength by UV spectrophotometry以吸光度值Y对样品浓度X(mg/mL)进行线性回归,回归方程为:Y=2.8231X,r2=0.9998㊂结果表明,阿司匹林在80~ 400μg/mL范围内线性关系良好㊂图2 双波长紫外分光光度法工作曲线Fig.2 Working curve of dual wavelength by UV spectrophotometry以吸光度值Y对样品浓度X(mg/mL)进行线性回归,回归方程为:Y=5.7478X,r2=0.9999㊂结果表明,阿司匹林在50~ 150μg/mL范围内线性关系良好㊂表3 紫外分光光度法测定阿司匹林含量Table3 Determination of aspirin by UV spectrophotometry编号标示量/%单波长双波长1104.3104.92104.3104.93104.3105.14104.3104.95104.3105.1平均值104.3104.98从表3可以看出,无论是单波长或双波长紫外分光光度法,测定结果的精密度较好,测定值也能够符合要求;同时对吸光度值在2h内的稳定性进行了考察,结果表明,稳定性较好,2h内吸光度小于0.003变化㊂2.3 高效液相色谱法测定阿司匹林含量用国产仪器天美LC2000型高效液相色谱仪(上海天美科学仪器有限公司),依利特ODS色谱柱4.6mm×150mm,流速为2018年8月广 州 化 工120 1mL /min,依据2010年版‘中国药典“方法,阿司匹林含量工作曲线和阿司匹林含量结果见图3和表4㊂图3 阿司匹林对照品的工作曲线Fig.3 Working curve of aspirin reference表4 高效液相色谱法测定阿司匹林含量Table 4 Determination ofaspirin by HPLC编号标示量/%平均值/%192.8296.73105.14101.75104.5100.2从测定结果可以看出,线性关系R 2只有0.9716,精密度也不是很好,说明本方法对仪器的精度要求较高,5次分析结果的平均值为100.2,说明液相色谱方法可以排除辅料的影响[10-13],测定值符合要求㊂3 结 论采用三种方法对小剂量阿司匹林肠溶片中阿司匹林含量进行测定比较,可以得出结论:(1)由于药片中辅料影响,酸碱滴定法测定阿司匹林含量结果严重偏高,不适用于小剂量阿司匹林肠溶片含量测定; (2)紫外分光光度法,方法简便㊁快速㊁结果可靠,对仪器没有特别高的要求㊂单波长与双波长法,线性相关性良好,测量结果能够符合要求,但由于双波长法测含量时,所用溶剂为乙醇,相比较,单波长法采用磷酸盐冲液,更具有实用性,可以用于生产过程中的质量控制;(3)高效液相色谱法,可以避免辅料对阿司匹林含量测定的影响,可以获得准确结果,但涉及到流动相,色谱柱柱效等问题,使用此法测定阿司匹林含量对仪器精度要求高㊂参考文献[1] 国家药典委员会.中华人民共和国药典:2010年版.三部[M].中国医药科技出版社,2010.[2] 陈兴荣,董光平,赖林.分光光度法测定阿司匹林肠溶片的含量[J].数理医药学杂志,2010,23(4):478-479.[3] 乔兰侠,高志国,邢秋蕊.紫外分光光度法测定乙酰水杨酸肠溶片的含量[J].河北师范大学学报,2001,25(2):219-220.[4] 盖柯,郑阿利,荔瑞琴,等.紫外分光光度法测定小剂量阿司匹林肠溶片的含量[J].中国药师,2006,9(7):643-644.[5] 池秀珍.双波长紫外分光光度法测定阿司匹林肠溶片含量[J].海峡药学,2002,14(1):28-29.[6] 郑虹,段广佩,姜世贤.阿司匹林肠溶片含量测定方法的改进[J].青海医药杂志,2005,35(5):56-57.[7] 王慧文,左宗伟.阿司匹林肠溶片含量测定方法的改进[J].淮海医药,2007,25(4):362-363.[8] 胡新海,汪金元.阿司匹林肠溶片含量测定的探索研究[J].黑龙江科技信息,2009(32):260[9] 翁水旺,周继斌.糊精对乙酰水杨酸肠溶片含量测定的影响[J].中国药事,2001,15(1):44-45.[10]王鹤尧,张金平,屈桂秋,等.阿司匹林和游离水杨酸高效液相色谱检定新方法的研究[J].中国新药杂志,2001,10(1):37-39.[11]徐占方,徐云宏.HPLC 法测定阿司匹林片的含量[J].齐齐哈尔医学院学报,2007,28(3):316-317.[12]徐新,廖思佳,廖先智,等.高效液相色谱法测定阿司匹林含量[J].广州化工,2012,40(8):131-132.[13]申林莉,薛卫萍,王旭.HPLC 法测定阿司匹林肠溶片含量[J].中国药品标准,2004,5(1):33-35.。
阿司匹林实验报告

一、实验目的1. 掌握阿司匹林的制备原理及方法。
2. 了解阿司匹林在医药领域的应用。
3. 熟悉实验操作技能,提高实验实践能力。
二、实验原理阿司匹林,又称乙酰水杨酸,是一种白色针状或板状结晶,具有解热、镇痛、消炎等作用。
在实验室中,阿司匹林主要通过水杨酸与乙酸酐在浓硫酸催化下发生酰基化反应制备。
反应方程式如下:COOH + CH3COCl → COOCH3 + HCl三、实验材料与仪器1. 实验材料:- 水杨酸- 乙酸酐- 浓硫酸- 冰乙酸- 水浴锅- 冷凝管- 抽滤装置- 烧杯- 烧瓶- 玻璃棒- 试剂瓶2. 实验仪器:- 100mL圆底烧瓶- 100mL锥形瓶- 球形冷凝管- 50mL滴定管- 50mL容量瓶- 电子天平- 精密pH计四、实验步骤1. 准备反应溶液:在100mL圆底烧瓶中加入4g水杨酸和10mL新蒸馏的乙酸酐,在振摇下缓慢滴加7滴浓硫酸,搅拌均匀。
2. 加热回流:将反应溶液放入水浴锅中,控制水浴温度在75-80℃之间,回流反应20分钟。
3. 冷却结晶:撤去水浴,趁热于球形冷凝管上口加入2mL蒸馏水,以分解过量的乙酸酐。
稍冷后,拆下冷凝装置。
4. 结晶分离:在搅拌下将反应液倒入盛有100mL冷水的烧杯中,并用冰-水浴冷却,放置20分钟。
待结晶析出完全后,用抽滤装置进行过滤。
5. 精制:将粗产品用冰乙酸洗涤,再用无水乙醇洗涤,最后用真空干燥箱进行干燥。
6. 质量分析:采用紫外-可见分光光度法测定阿司匹林的含量。
五、实验结果与分析1. 制备的阿司匹林为白色针状或板状结晶,外观符合要求。
2. 通过紫外-可见分光光度法测定,阿司匹林含量为98.5%,符合实验要求。
六、实验总结本实验成功制备了阿司匹林,并通过质量分析验证了实验结果的准确性。
在实验过程中,我们掌握了阿司匹林的制备原理及方法,熟悉了实验操作技能,提高了实验实践能力。
同时,通过本实验,我们对阿司匹林在医药领域的应用有了更深入的了解。
紫外分光光度法对阿司匹林肠溶片含量测定

研究报告紫外分光光度法对阿司匹林肠溶片含量测定班级:学号:姓名:紫外分光光度法对阿司匹林肠溶片含量测定阿司匹林属常用解热镇痛药, 小剂量可用于防治心脑血管疾病。
近年来, 随着人们预防保健意识增强, 小剂量阿司匹林肠溶片的生产和使用逐年增长, 其质量不合格的现象也屡有发生。
小剂量阿司匹林肠溶片 (以下简称阿肠片) 含量测定地方标准采用酸碱滴定法[ 1], 后改为紫外分光光度法[ 2]。
2002 年11 月份颁布的国家标准 (化学药品地方标准上升国家标准)[ 3]仍为酸碱滴定法。
然而我们在实际检验工作中发现采用酸碱滴定法测定结果严重偏高, 有多批检品含量高至 110% ~ 120% ( 含量限度为 950% ~ 105%) ; 而采用紫外分光光度法测定, 结果为98%~ 100% [4]。
1 仪器与试药药品:阿司匹林肠溶片(25㎎×100片,临汾宝珠有限制药公司,100301)试剂:阿司匹林储备液(2.012mg/ml)蒸馏水仪器:紫外分光光度计(日本岛津),石英比色皿(1cm)2个,25ml容量瓶,移液管,分析天平(Sartorius BS110S,北京赛多利斯天平)等。
2 方法与结果2.1 标准系列溶液的配置2.1.1贮备液的制备取原贮备液(2.012mg/ml)0.7ml置25ml容量瓶中,加蒸馏水至刻度,要匀即可,该贮备液浓度为56.34µg/ml。
2.1.2对照品溶液的制备取上述贮备液(56.34µg/ml)5ml置25ml容量瓶中,加蒸馏水至刻度摇匀即可,扫该溶液(C=11.268µg/ml)紫外光谱图,判断阿司匹林紫外可见的最大吸收峰λmax=225 nm、λmax=262 nm。
测得当λmax=225 nm时吸光度A=0.335。
如图一图一阿司匹林对照品溶液紫外吸收光谱2.1.3标准系列浓度的配置取6只25ml容量瓶,分别加入4.00,5.00,6.00,7.50,9.00,10.00ml浓度为56.34µg/ml贮备液,加蒸馏水稀释至刻度,摇匀。
紫外分光光度法测定阿司匹林含量1

阿司匹林的制备及紫外光谱分析(二)一、实验目的1. 了解阿司匹林的合成方法及性质。
2. 掌握紫外分光光度法分析阿司匹林含量的原理及操作。
二、方法原理乙酰水杨酸(acetyl salicylic acid)( 阿司匹林Aspirin)是一种非常普遍的治疗感冒的药物,有解热止痛作用,同时还软化血管。
19世纪末,人们成功地合成了乙酰水杨酸。
直到目前,阿司匹林仍是一个广泛使用的具有解热止痛作用治疗感冒的药物。
在过量NaOH介质中,阿司匹林定量水解为水杨酸钠,其在290—300 nm处有较强的紫外吸收,且其吸光度在一定条件下,与阿司匹林的浓度呈线性关系,因此,在合适条件下,可用紫外分光光度法测定阿司匹林的含量。
溶剂和其他成分不干扰测定。
COOHOC O +COOCH3O+C3OC H OOH3+H O22三、仪器和试剂仪器紫外—可见分光光度计;50mL容量瓶;10mL吸量管、5ml吸量管。
试剂 0.5000mg·mL-1水杨酸贮备液:称取0.2500g水杨酸先溶于少量0.1moL·L-1NaOH 溶液中,然后用蒸馏水定容于500mL容量瓶中;0.1moL·L-1 NaOH 溶液。
四、实验内容1、对照液的配制:将七个50.00mL容量瓶按0-6依次编号。
分别移取水杨酸储备液0.00、1.00、2.00、3.00、4.00、5.00mL于相应编号容量瓶中,各加入1.0mL 0.1moL·L-1 NaOH溶液,先用蒸馏水稀释至30mL左右,80℃水浴加热10分钟,冷却至室温,稀释至刻度,摇匀。
2、试样溶液的配制:准确称取适量阿司匹林样品于50mL烧杯中,加入0.1moL·L-1NaOH 溶解,定量转移至50mL容量瓶中,用蒸馏水稀释至刻度,摇匀。
从50mL容量瓶中取一定量的试样溶液至另一个50mL容量瓶中,蒸馏水稀释至30mL左右,80℃水浴加热10分钟,冷却至室温,稀释至刻度,摇匀。
阿司匹林含量测定

阿司匹林含量测定摘要:阿司匹林是一种常见的非甾体解热镇痛药,现在也用于心血管疾病的治疗,由于其历史悠久,所以至今已经有许多对于阿司匹林含量的测定,例如酸碱滴定法,紫外分光光度法,高效液相色谱法等。
2010版中中国药典中主要记载的方法主要有直接滴定法和高效液相色谱法。
关键词:阿司匹林,含量,体内,体外正文:一. 阿司匹林原料药的含量测定:1. 体外:1.1 直接滴定法:取阿司匹林原料药约0.4g,精密称定,加入中性乙醇(对酚酞指示液显中性) 酚酞指示剂,用氢氧化钠滴定液(0.1mol/L)20ml振摇,完全溶解后,加3滴直接滴定。
氢氧化钠滴定液(0.1mol/L)的滴定度T为18.02mg/ml,即每1ml的氢氧化钠滴定液(0.1mol/L)相当于18.02mg的C9H8O4。
滴定至溶液从无色变成淡粉红色即为滴定终点。
记录滴定液的消耗量V。
含量(%)=(V*T/W)*100%= (V*18.02/(0.4*1000))*100%1.2 水解后剩余滴定法:[1]取阿司匹林原料药约1.5g,精密称定,加氢氧化钠滴定液(0.5mol/L)50.0ml混合,缓缓煮沸10分钟,放冷,加酚酞指示剂,用硫酸滴定液(0.25mol/L)滴定,并将滴定结果用空白试验校正。
每1ml的氢氧化钠滴定液(0.5mol/L)相当于45.04mg的C9H8O4。
含量(%)=(V0—V)*F*T/W*100%=(V0—V)*F*18.02/(0.4*1000)*100% (V0为空白实验消耗的硫酸滴定液的体积(ml);V为样品测定时消耗硫酸滴定液的体积(ml);W为阿司匹林样品的取样量(g);F 为硫酸滴定液的浓度的校正因素;T为氢氧化钠滴定液的滴定度。
)1.3 HPLC法测定阿司匹林原料药含量以C18柱(150mm*4.6mm,5µm)为色谱柱,0.2%庚烷磺酸钠—乙腈(85:15)(用冰醋酸调PH至3.4)为流动相;检测波长为280nm;柱温30?;流速;1.0ml/min ;理论塔板数按阿司匹林峰计算应不低于3000。
阿司匹林含量测定方式综述

阿司匹林含量测定方式综述药学0802 郭伟财摘要阿司匹林是应用最先,最广和最一般解热镇痛药。
具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,发挥药效迅速,药效确信,其收载于(中国药典2000年版)二部,该文旨在分析阿司匹林原料药及阿司匹林为主药的制剂的含量测定方式,包括体内及体外药的分析。
关键词阿司匹林含量测定正文1.阿司匹林原料药含量测定阿司匹林原料药在体内含量测定色谱柱:Diamonsil C18柱(4.6mm×250mm,5um)流动相:甲酵—乙睛—0.2%磷酸(18:32:50)1.色谱条件检测波长:237nm流速:/min2.溶液配制: 1.周密称取水杨酸对照品甲醇10ml(1.010mg/L)用甲醇稀释成不同浓度的系列溶液。
2.周密称取苯甲酸甲醇10ml(1.044mg/l)取lml 甲醇稀释至l0ml(/ml的内标工作液)3.样品处置与测定:周密量取血清样品0.5ml + 内标苯甲酸溶液50ul + 乙睛2ml 旋涡振荡2min,15000r/min离心5min 取上清夜20ul 进样记入内标与样品的色谱图与峰面积。
按外标法以峰面积计算,即得。
4.计算(C R对内标溶液的浓度(ug/ml); A X和A R别离为供试品溶液和内标溶液中阿司匹林的峰面积;D为稀释体积;W为药物称取量;106单位换算因数)阿司匹林原料药在体外含量测定酸碱滴定法阿司匹林分子中含有游离羧基pKa为,可用标准碱直接滴定。
取本品约,周密称定,加中性乙醇(对酚酞指示液显中性)20ml溶解后,加酚酞指示液3滴,用氢氧化钠滴定液L)滴定。
每1ml氢氧化钠滴定液L)相当于的C9H8O4。
样品中型乙醇溶解酚酞NaoH滴定终点NaoH滴定度(T)= X 1/1=(mg/ml)含量(%)=(V XT XF /1000)/WX100%(V:滴定液体积(ml)T:滴定度W:供试品称样量(g)F:滴定液浓度校正因子F=滴定液实际浓度/滴定液规定浓度)水解后剩余滴定法阿司匹林中酯结构,在碱性溶液中易于水解,加入过量标准碱滴定液,加热使酯水解,剩余碱用酸回滴。
紫外―可见分光光度计在药品检测中的应用[权威资料]
![紫外―可见分光光度计在药品检测中的应用[权威资料]](https://img.taocdn.com/s3/m/7b87624a814d2b160b4e767f5acfa1c7aa008294.png)
紫外―可见分光光度计在药品检测中的应用药品分析是保证药品安全有效的重要手段,在药品的研究、生产、流通、使用和监督管理等环节中均有举足轻重的作用,其主要内容包括性状分析、鉴别、检查和含量测定等方面。
高效液相色谱仪、气相色谱仪、紫外分光光度计等是制药生产中常用的检测仪器。
其中,紫外分光光度计由于准确度高、测定限度低、设备简便、仪器成本低、易于操作等优点,已成为制药生产中必备的检测设备之一,用于药物鉴别、检查和含量测定等。
紫外-可见分光光度法是通过测定物质在紫外-可见光区(200-760nm)产生紫外-可见吸收光谱,根据吸收光谱的特性,对该物质进行定性和定量分析的方法。
其理论基础为朗伯-比耳定律,溶液的吸光度和吸光物质含量、液层厚度乘积成正比。
对于一般的紫外分光光度法,其测量的相对误差在1%~3%。
随着大量心得显色剂的合成及应用,尤其是有关多元络合物和各种表面活性剂的应用研究,推进了元素测定的灵敏度的大幅提高。
采用预富集和示差法,适用质量分数从常量(1%~50%)到痕量(10-10~10-8)。
紫外-可见分光光度法由紫外分光光度法和可见分光光度法两种方法构成,这两种方法在测定的原理、仪器、操作等方面皆相同。
因此,统称为紫外-可见分光光度法,测定仪器一般采用紫外-可见分光光度仪。
在各国药典中,药品的理化常数、鉴别、检查和含量测定等很多项目中,都能见到紫外分光光度法的应用实例。
在制药生产中,紫外分光光度法应用最多的是药物含量的测定、药物杂质检测、药物稳定性考察、释放度、药物负载行为测定及物质结构鉴定等方面。
目前利用紫外分光光度计分析的药物品种有维生素、抗生素、解热药、去痛药、降血压药、安定药、镇咳药、滴眼药、磺胺类药、利尿药、某些妇科药、痢疾药、腹泻药、抗肿瘤药、抗结核药等。
1 紫外分光光度法应用于药物含量测定紫外-可见分光光度法由于灵敏度较高,不仅可用于常量组分的含量测定,也可用于测定微量组分、超微量组分以及多组分混合物同时测定等,在药物分析中主要用于原料药含量测定、制剂含量测定、含量均匀度和溶出度的检查等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
阿司匹林的制备及紫外光谱分析(二)
一、实验目的
1. 了解阿司匹林的合成方法及性质。
2. 掌握紫外分光光度法分析阿司匹林含量的原理及操作。
二、方法原理
乙酰水杨酸(acetyl salicylic acid)( 阿司匹林Aspirin)是一种非常普遍的治疗感冒的药物,有解热止痛作用,同时还软化血管。
19世纪末,人们成功地合成了乙酰水杨酸。
直到目前,阿司匹林仍是一个广泛使用的具有解热止痛作用治疗感冒的药物。
在过量NaOH介质中,阿司匹林定量水解为水杨酸钠,其在290—300 nm处有较强的紫外吸收,且其吸光度在一定条件下,与阿司匹林的浓度呈线性关系,因此,在合适条件下,可用紫外分光光度法测定阿司匹林的含量。
溶剂和其他成分不干扰测定。
COOH
OC O +
COO
CH
3
O+C3O
C H O
OH
3+H O22
三、仪器和试剂
仪器紫外—可见分光光度计;50mL容量瓶;10mL吸量管、5ml吸量管。
试剂 0.5000mg·mL-1水杨酸贮备液:称取0.2500g水杨酸先溶于少量0.1moL·L-1NaOH 溶液中,然后用蒸馏水定容于500mL容量瓶中;0.1moL·L-1 NaOH 溶液。
四、实验内容
1、对照液的配制:将七个50.00mL容量瓶按0-6依次编号。
分别移取水杨酸储备液0.00、1.00、2.00、3.00、4.00、5.00mL于相应编号容量瓶中,各加入1.0mL 0.1moL·L-1 NaOH溶液,先用蒸馏水稀释至30mL左右,80℃水浴加热10分钟,冷却至室温,稀释至刻度,摇匀。
2、试样溶液的配制:准确称取适量阿司匹林样品于50mL烧杯中,加入0.1moL·L-1NaOH 溶解,定量转移至50mL容量瓶中,用蒸馏水稀释至刻度,摇匀。
从50mL容量瓶中取一定量的试样溶液至另一个50mL容量瓶中,蒸馏水稀释至30mL左右,80℃水浴加热10分钟,冷却至室温,稀释至刻度,摇匀。
3、样品测定:在紫外分光光度计上对标样3进行扫描,波长范围是320—280nm,找出最大吸收波长,并在该波长下由低浓度到高浓度测定标准溶液的吸光度,最后测定未知液的吸光度。
4. 数据处理
(1)以吸光度A为纵坐标,水杨酸浓度C为横坐标作标准曲线。
(2)根据试样溶液的吸光度值,在标准曲线上求出相应的浓度(mg/mL),并换算成乙酰水杨酸的含量。
五、注意事项
1、水浴加热时容量瓶塞子要松松塞住,防止加热气体膨胀,塞子冲出。
2、测量前用待测液润洗比色皿,测量由低浓度到高浓度依次进行。
3、从实验步骤可知,试样是两次稀释后,用很稀的浓度进行吸光度测试的,因此提取和
各步转移必须严格定量,制作标准曲线的标样浓度也必须很准确,不然就会使求得的试样浓度产生较大的误差。
思考题
1、实验中为什么要加热?
2、引起误差的因素有哪些?如何减少误差?
实验报告格式
实验题目:
一、吸收曲线的绘制
标准溶液浓度:________。
= nm
最大吸收波长max
二、未知试样的定量测量
1.标准曲线的绘制:
定量分析结果:未知物的浓度为__________________。
