不同培养基检测单核细胞增生李斯特氏菌的结果比较
乳粉中单核细胞增生李斯特氏菌能力验证结果与分析

乳粉中单核细胞增生李斯特氏菌能力验证结果与分析樊惠华,侯磊磊,方 莹,柴梅梅(榆林市食品检验检测中心,陕西榆林 719000)摘 要:为了提升食品检验检测机构对食品中单核细胞增生李斯特氏菌的检验能力,提高微生物实验室外部质量控制水平。
本实验室参加中国检验检疫科学研究院测试评估中心组织的ACAS-PT1108(2021)乳粉中单核细胞增生李斯特氏菌检测能力验证,参考参试指导书、《食品安全国家标准食品微生物学检验单核细胞增生李斯特氏菌检验》(GB 4789.30—2016)、海博单增李斯特氏菌成套生化鉴定管和MicroScan WalkAway 40 Plus全自动微生物生化鉴定仪。
结果表明,参试样品编号21-T031为单核细胞增生李斯特氏菌,样品编号21-U887未检出单核细胞增生李斯特氏菌,经鉴定为伊氏李斯特氏菌,最终能力验证结果评价为满意,可见本实验室具有成熟的单核细胞增生李斯特氏菌检验能力。
关键词:乳粉;单核细胞增生李斯特氏菌;能力验证Results and Analysis of the Proficiency Testing of ListeriaMonocytogenes in Milk PowderFAN Huihua, HOU Leilei, FANG Ying, CHAI Meimei(Yulin Food Inspection and Testing Center, Yulin 719000, China)Abstract: In order to improve the ability of food inspection and testing institutions to detect Listeria monocytogenes in food and to improve the external quality control level of microbiology laboratory. The laboratory participated in the proficiency testing of Listeria monocytogenes in ACAS-PT1108 (2021) milk powder organized by the Testing and Evaluation Center of the Chinese Academy of Inspection and Quarantine Sciences. Reference was made to the test guidelines, the GB 4789.30—2016, the complete biochemical identification tubes of Listeria monocytogenes in Haibo and the MicroScan WalkAway 40 Plus automatic microbial biochemical identification instrument. The results showed that the sample number 21-T031 was detected as Listeria monocytogenes, and the sample number 21-U887 was not detected as Listeria monocytogenes, which was identified as Listeria.ivanovii. The final proficiency test results were satisfactory. It can be seen that the laboratory has a mature ability to test Listeria monocytogenes.Keywords: milk powder; Listeria monocytogenes; proficiency test李斯特菌属目前包括17种公认的短杆状革兰氏阳性菌,其中单核细胞增生李斯特氏菌和伊氏李斯特氏菌被认为是病原体[1]。
单核细胞增生李斯特氏菌检验技术

•小的圆形灰绿色菌落,周围有棕黑色水解圈,有些菌落有黑色凹陷
10mLLB2
TSA-YE
鼠李糖
TSA-YE
阳性
选择木糖阴性、鼠李糖阳性的纯培养物继续进行鉴定
革兰氏染色
单增李斯特氏菌和斯氏李斯特氏菌在刺种点周围产生狭小的透明溶血环;在靠近金黄色葡萄球菌的接种端溶血增强
革兰氏阳性短杆菌
动力试验
MR试验
一、单核增生李斯特氏菌概况
生物学特性
该菌对理化因素抵抗力较强,在土壤、粪便、青储饲料和食品中能长期存活;对碱和盐抵抗力强,60-70℃经5-20min可杀死,70%酒精5min、2.5%石炭酸、2.5%氢氧化钠、2.5%福尔马林20min 可杀死此菌;湿热灭菌(121℃,至少15min)和干热灭菌(160-170℃,至少1hr)可杀灭该菌,对紫外线和γ射线敏感;对青霉素、氨苄青霉素、氨基糖苷类、氯霉素均敏感。
食品中单核增生李斯特氏菌检验
食品微生物检验技术
李斯特氏菌属(Listeria )普遍存在于环境中,最新的分类学研究表明,其分为六个 种:单核增生李斯特氏菌(Listeria monocytogenes)、绵羊(伊氏)李斯特氏菌、 英诺克(无害)李斯特氏菌、斯氏李斯特氏菌、威氏李斯特氏菌、格氏李斯特氏菌在李斯特氏菌属只有两种致病菌:单核增生李斯特氏菌和伊氏李斯特氏菌可以引起老鼠和其他动物发病。但是,其中通常只有单核增生李斯特氏菌和人类的李斯特氏菌症(listeriosis)相关。因此,李斯特氏菌中最有检测意义是单核增生李斯特氏菌。
一、单核增生李斯特氏菌概况
李斯特氏菌属
革兰氏阳性,老龄培养物多转为革兰阴性;兼性厌氧,无芽孢、无荚膜;生长温度范围为2-42℃(也有报道在0℃能缓慢生长),pH范围pH4.4-pH9.6;LM的幼龄菌(16~24h的培养物),为革兰阳性小杆菌,常呈V字形,成对排列。在22~25℃环境中形成4根鞭毛,故在25℃肉汤培养液中出现轻微旋转或翻滚样的运动。而在32℃时仅形成一根鞭毛,动力缓慢。
单核细胞增生李斯特氏菌生化鉴定

单核细胞增生李斯特氏菌生化鉴定引言单核细胞增生李斯特氏菌(Listeria monocytogenes)是一种常见的食源性致病菌,可引起严重的食物中毒和感染疾病。
为了及时诊断和控制该菌的传播,对其进行准确的生化鉴定非常重要。
本文将介绍单核细胞增生李斯特氏菌的生化鉴定方法及相关实验步骤。
实验材料与方法实验材料•单核细胞增生李斯特氏菌培养基•Listeria Enrichment Broth(LEB)•Listeria Agar Base(LAB)•乳清素蛋白水解物培养基(Trypticase Soy Broth,TSB)•乳清素蛋白水解物琼脂培养基(Trypticase Soy Agar,TSA)•碱性亮绿液实验方法1.取一份食物样品,如肉类、奶制品等,加入适量LEB中,并在37℃孵育24小时。
2.取0.1ml培养液,在TSB中进行预培养,37℃孵育24小时。
3.从TSB中取出适量菌液,用胶体金法进行菌落计数,并将菌液稀释至10-4倍。
4.取适量的稀释液分别接种于LAB和TSA琼脂培养基上,并在37℃孵育24小时。
5.观察菌落形态、颜色等特征,并记录下来。
生化鉴定实验单核细胞增生李斯特氏菌生化鉴定步骤如下:1.琼脂凝胶双扩散试验:将单核细胞增生李斯特氏菌抗原与相应的抗血清共同扩散于琼脂凝胶板上,观察是否发生免疫反应。
若有明显的线条或沉淀形成,则说明存在抗原-抗体反应,可以初步判断为单核细胞增生李斯特氏菌。
2.碱性亮绿液试验:将培养基中的单核细胞增生李斯特氏菌与碱性亮绿液接触,观察是否产生绿色荧光。
若产生绿色荧光,则说明菌株具有单核细胞增生李斯特氏菌的特性。
3.单核细胞增生李斯特氏菌脂多糖(LPS)鉴定:采用酚-硫酸法或酚-硝基苯法,将培养基中的单核细胞增生李斯特氏菌进行LPS提取,然后进行比色反应。
若出现红色或紫色沉淀,则说明存在LPS,可以进一步确认为单核细胞增生李斯特氏菌。
结果与讨论通过上述实验方法,我们可以对食物样品中的单核细胞增生李斯特氏菌进行生化鉴定。
单核细胞增生李斯特菌污染调查及快速检验方法的比较(精)

单核细胞增生李斯特菌污染调查及快速检验方法的比较余淑冰1 梁景涛1 周强忠1 孔繁钧1 陈庆韶1 李婉霞2单核细胞增生李斯特菌(LM)能引起人畜共患病,致病性强,临床病死率高达30%~70%。
目前,国际上对其研究非常重视,已将其列为90年代食品四大致病菌(致病性大肠菌、肉毒梭菌、亲水气单胞菌和LM)之一。
我国在LM研究及检验起步较晚,经验较少,1994年才颁布该菌的标准检验方法。
为了解食品中LM的污染状况,开展应用快速检验方法,作者于1996年5月至1997年4月对佛山地区的市场销售点,抽取6类不同的食品共309份,作为LM污染调查对象,同时根据现有的检验方法,探索出一种快速可行的检验方法,现报告如下:一、材料与方法1.样本来源:选取佛山市区5个肉菜市场的各个肉档、鱼档、烧腊档、菜农等6类食品,每类食品50份以上。
其中乳和水产品分别由水牛奶厂和水产加工场提供。
6类食品具体包括有:①生肉类:猪肉、猪肉馅、鸡肉、牛肉、羊肉。
②熟肉制品:猪肉、猪肉肠、鸡肉、牛肉。
③乳类:生牛奶、消毒牛奶。
④乳制品:冰淇淋、奶酪、酸奶、果奶。
⑤蔬菜:黄瓜、香菜(去根)、菠菜(去根)、菜花(指花菜)、莲藕。
⑥水产品:鱼、虾。
2.标准菌株:LM(54004和54007)、金黄色葡萄球菌、马红球菌(R.equi)由卫生部食品卫生监督检验所提供。
3.培养基和试剂:本实验室配制,并以有关阳性菌株进行质量控制。
4.试验动物:采用广东省卫生厅医用实验动物所饲养的瑞士小白鼠,选取体重在16~18 g之间作试验用。
5.试剂盒:由生物-梅里埃公司提供,使用时按说明书进行。
6.方法:按国标食品卫生检验方法GB4789.30-94进行。
二、结果1.6类食品检测情况:在受检的6类食品共309份中,检出阳性菌株16份(已由卫生部食品卫生监督检验所鉴定),总污染率为5.18%(16/309),其中在生肉、熟肉制品、生牛奶和水产品中均检出LM。
采用LB法检出率为62.5%(10/16),EB法检出率为37.5%(6/16),LB法明显高于EB法,见表1。
食品中单核细胞增生李斯特氏菌的检验能力验证结果分析

食品中单核细胞增生李斯特氏菌的检验能力验证结果分析作者:彭怡许红玉黄厚强张曲来源:《中国食品》2024年第02期单核细胞增生李斯特氏菌(Listeria monocytogenes,LM),简称为单增李斯特氏菌,是一种需氧兼性厌氧的食源性病原菌、革兰氏阳性短杆菌,广泛存在于自然界中。
其中,奶制品、肉制品、水产品、海产品、禽类食品、蔬菜等容易受到该菌污染,误食用含有该菌的新生儿、老年人等免疫力低者易患脑膜炎、败血症,孕妇则易发生早产或流产,致死率高达20%-30%,给食品安全造成严重威胁。
近年来,国内外关于单增李斯特氏菌的主要检测方法包括国标法、免疫学检测法、生物传感器检测法等,这些方法各有优缺点。
能力验证通过对实验室间的检验能力进行比对,评价参加者的能力,是证明实验室检验能力的重要方式之一。
资阳市食品药品检验检测中心生物检验科参加了由四川省食品检验研究院组织的“食品中单核细胞增生李斯特氏菌的检验能力验证”,采用国标法《GB 4789.30-2016 食品安全国家标准食品微生物学检验单核细胞增生李斯特氏菌检验》第一法对样品进行定性检验。
一、材料与方法1.样品。
由四川省食品检验研究院提供3份单核细胞增生李斯特氏菌样品,每份样品包括一瓶白色球状西林瓶装和一袋质量约为25g的奶粉,样品编号分别为LM-029、LM-177和LM-307。
2.菌种。
单增李斯特氏菌ATCC 19115、斯氏李斯特氏菌ATCC 35967、伊氏李斯特氏菌ATCC 19119、英诺克李斯特氏菌ATCC 33090,均由广东环凯生物科技有限公司提供。
3.主要试剂。
脑心浸出液肉汤(BHI)、李氏菌增菌肉汤(LB1,LB2)基础、PALCAM 琼脂、李斯特氏菌显色培养基、SIM生化管、HBI单增李斯特氏菌生化鉴定条(GB),购自青岛高科技工业园海博生物技术有限公司;李斯特氏菌显色培养基、PALCAM琼脂、含0.6%酵母浸膏的胰酪胨大豆琼脂(TSA-YE)、血平板、革兰氏染色液试剂盒、3%过氧化氢、单增李斯特氏菌干制生化鉴定试剂盒,购自北京陆桥技术股份有限公司。
应用不同培养基检测单增李斯特菌结果比较

基室制备。显色培养基 A O L A出 自法 国 A SLb r o e E aoa i 公 较大菌 落边 缘粗 糙 , 透 明晕 圈也 没 有 A O tr 不 L A上 的 明显 司 , H O aa Ls r C R M gr iei 自法 国 C R Maa 公 司。所 t a出 H O gr
1 1 1 菌株 来 源 ..
心菌种保藏室提供 ; 试验菌株来 自食 品检测样 品 , 主要包 A O L A上 由于 L t i sp 缺少 明显 的晕 圈 , 容 易与 单 ie a p . s r 很
括 : 制品、 奶 肉制品、 海鲜类产 品和蔬菜 , 共计 2 8份 。 6
1 12 培 养基 .. 传统 培养基 M A、 X 由本 中心 培养 征较 为明显 , H O aa Ls r 上 细 菌 大 小差 异 较 大 , M OA C R M gr iei t a
文章编号 : 0 — 2 1 20 ) 1 0 3 0 1 4 93 I 0 8 O — 02— 2 0
・
检 验 技 术 ・
应用不同培养基检测单增李斯特菌结果比较
居 建华 ,叶虹 , 伟 忠 ,张巧 英 ( 顾 上海 市疾病 预 防控制 中心 ,上海 20 3 ) 0 36
据 中国预 防医学科学 院流行病学 微生物学 研究所 的 有培养基均在有效期 内配制并使用 。
表1
单增李斯特菌及李斯特菌标 准菌株在不 同培养基 的菌落特征
作者简介 : 居建华 ( 94 ) 男 , 1 5一 , 主管技师 。
维普资讯
20 0 8年 第 2 O卷 第 1期
2 0 Vo . 0 No 1 0 8, 1 2 .
上 海 预 防 医 学杂 志
单核细胞增生李斯特氏菌生化鉴定

单核细胞增生李斯特氏菌生化鉴定
李斯特氏菌(Listeria monocytogenes)是一种革兰氏阳性杆菌,是一种常见的细菌性食物中毒病原体。
单核细胞增生组织均为生化鉴定的一种常见方法。
以下是李斯特氏菌生化鉴定的一些特征:
1. 嗜冷性:李斯特氏菌生长适宜温度为2-45℃,菌株能够在4℃下生长,并在冷藏食品中繁殖。
2. β-溶血素产生:李斯特氏菌能够产生β-溶血素,可以通过血琼脂(Blood agar)培养基上的溶血环进行观察。
3. 乳酸发酵:李斯特氏菌是一种革兰氏阳性乳酸菌,能够进行乳酸发酵。
可以使用乳糖发酵基质(Lactose fermentation medium)进行鉴定,如果产生乳酸则为阳性。
4. 半胱氨酸脱羧:李斯特氏菌具有半胱氨酸脱羧酶活性,可以将半胱氨酸转化为硫代氨基酸。
可使用兰氏差异培养基(LDC medium)进行鉴定。
5. 半乳糖酶活性:李斯特氏菌具有半乳糖酶活性,可以将乳糖转化为半乳糖。
可使用半乳糖发酵基质(Rhamnose fermentation medium)进行鉴定。
此外,李斯特氏菌还可以进行PCR扩增目标基因进行鉴定,
如16S rRNA基因、Internal Transcribed Spacer(ITS)区域等。
需要指出的是,单纯进行生化鉴定可能存在一定的误判率,结合其他检测方法可以提高鉴定的准确性。
此外,由于李斯特氏菌在环境中广泛存在,饮食中也常常带菌,所以对于临床病例的确诊还需要结合患者的临床表现、流行病学调查等综合分析。
生鲜牛肉中单核细胞增生李斯特氏菌检验方法的比较

单 核 细 胞 增 生 李 斯 特 氏 菌 (Listeria monocyto.
即使 在 0 ̄C的冷 藏环 境 下仍 然 可 以生长 ,一 旦被 人 食 进行 生 化 试 验 的 确 定 ,整 个 检 验 周 期 能 达 到 4 ~
用可能会引起疾病甚至死亡[1 ]。随着我 国经济的
7d[8] 。
随着技 术 的进 步 ,一些 基 于免 疫 学 方 法 、分 子
发展 ,牛 肉成为人们餐 桌上的常见食用 肉类 。我 国 生 物 学方法 的新 型 技 术 已经 成 熟 ,逐 步 的 成 为 被 专
肉品安全与检测
内凑摹业
MEAT INDUSTRY
2018年第 2期 总 第 442期
生 鲜 牛 肉 中 单 核 细 胞 增 生 李 斯 特 氏菌 检 验 方 法 的 比较
王利刚 重庆 市食品 药品检 验检测研 究院 重庆 401123
摘 要 采 用常规培 养法、全 自动酶联免疫 荧光 分析 仪法、实时 荧光定量 PCR检 测法三种 方法对 80批 次的生 鲜牛 肉进行检 验 ,并 比较 分析三种检验 方法。结果显 示:常规培养 法存在 较 多缺点 ,而全 自动酶联 免疫 荧光分析仪 筛选 法、实时荧光定 量 PCR检 测法在特异性等 方面均存在较 大优 势 .尤其是 实时 荧光定量 PCR检测 法不仅假 阳性 率低 ,最低检测 浓度也 非常低 。因此 ,后两者 可作 为实验 室 日常 筛查和应 急检 验的方 法,发现 阳性 样本后 再使 用常 规培养 法进行 确认 。
单增李斯特氏菌能力验证结果与分析

单增李斯特氏菌能力验证结果与分析作者:白雯静王艳炜王海峰来源:《食品界》2022年第10期引言单核细胞增生李斯特氏菌是普遍存在于自然环境中的革兰氏阳性、嗜冷、兼性厌氧细菌。
同时,也是一种食源性的人畜共患病的病原菌,欧美国家曾多次暴发由于食用了受单增李斯特氏菌污染的肉制品、奶制品、蔬菜及水果等而引发的严重的食物中毒事件。
在《GB 29921-2021 食品安全国家标准食品中致病菌限量》中,对乳制品、肉制品(包括熟肉制品和即食生肉制品)、水产制品、即食果蔬制品、冷冻饮品均有五份样品中均不得检出单增李斯特氏菌(n=5,c=0,m=0)的规定;同样,在2022年3月7日实施的《GB 31607-2021 食品安全国家标准散装即食食品中致病菌限量》中“部分或未经热处理散装即食食品”:单核细胞增生李斯特氏菌限量为0/25g(mL)。
由此类标准可见,国家对于食品中“单核细胞增生李斯特氏菌”的管理是十分严格的。
目前,国内单核增生李斯特氏菌的检验方法主要有:分子生物学检测技术(结合等温扩增技术、结合聚合酶链式反应技术)、免疫学检测技术、生物传感器检测技术、光谱学检测技术、其它检测技术(除了基于核酸檢测、特有蛋白检测之外,还可以与色谱、核磁等多项技术技术相结合对单增李斯特氏菌进行检测)。
《GB 4789. 30-2016食品安全国家标准食品微生物学检验单核细胞增生李斯特氏菌》与旧版标准相比较,主要增加了“第二法单核细胞增生李斯特氏菌平板计数法”和“第三法单核细胞增生李斯特氏菌MPN计数法”。
目前,对单核细胞增生李斯特氏菌的检验方法是比较成熟的。
而且,随着检验检测技术日新月异的发展,使得较短时间内完成精准检测成为可能。
另外,对于实验室而言,质量控制具有十分重要的意义。
质量控制的工作包括很多方面。
比如,实验室内部控制和实验室间控制等等。
实验室内部控制工作可通过多种工作方式来展开。
比如,内部质量监督以及通过购买质控样品开展相关检验检测工作等等。
单核细胞增生李斯特氏菌检验培养基和试剂(一)

单核细胞增生李斯特氏菌检验培养基和试剂(一)单核细胞增生李斯特氏菌(LM)是一种由李斯特氏菌属(Listeria)引起的感染性疾病,该疾病主要感染免疫功能低下人群,通常会导致败血症和脑膜炎等严重并发症,严重威胁人类健康。
因此,开发出一种快速、敏感、高效的LM检验培养基和试剂至关重要,这可以加速LM 的检测和诊断,有效地减少疾病的传播。
一. 检验培养基1. 构成成分:单核细胞增生李斯特氏菌检验培养基是由肉汤、肉汤胰蛋白胨、乳糖、黄曲霉素、普鲁兰甲酸和酵母提取物等组成的。
2. 作用:肉汤是一种富含氮源和其他必需营养成分的培养基,在培养微生物中发挥着重要的作用。
肉汤胰蛋白胨是一种蛋白质水解物,可为细菌提供营养和生长因子,促进其繁殖。
乳糖则是一种碳源,能够促进细胞的代谢和繁殖。
黄曲霉素作为一种广谱抗生素,可以有效地抑制杂菌的生长。
普鲁兰甲酸和酵母提取物则可以用来增加LM在培养基上的特异性和灵敏度。
3. 优点:单核细胞增生李斯特氏菌检验培养基在培养LM时具有快速、敏感、特异性好等优点,可以大大缩短LM的检测时间,确保病菌的检测率。
二. 检验试剂1. 依赖性及非依赖性试剂:检验试剂可分为依赖和非依赖试剂。
依赖试剂需要依赖细菌代谢产物或生长结果的变化来作出结果,如葡萄糖酶试剂。
而非依赖试剂则不需要依赖于细菌代谢的结果,如反应纸片试剂。
2. LM检测常用试剂:LM检测常用试剂包括气体生成剂试剂和反应纸片试剂。
前者是一种单元试剂,含有半胱氨酸脱氨酶和甲酸氢化酶等催化剂,当培养基内细菌产生气体时,该试剂会发生颜色变化,表示LM检测阳性。
而反应纸片试剂则能够迅速地检测LM生长的结果,并呈现出明显的颜色变化。
这种试剂具有使用方便、结果稳定等优点。
3. 优点:LM检验试剂具有便于使用、结果稳定和灵敏度高等特点,可以有效地加速LM的检测和诊断,从而避免其传播和蔓延。
结论:单核细胞增生李斯特氏菌检验培养基和试剂是一对极为重要的检测手段,在LM的检测过程中发挥着至关重要的作用。
食品中单核细胞增生李斯特氏菌检测分析

食品中单核细胞增生李斯特氏菌检测分析石红霞(内蒙古乌兰察布市疾病预防控制中心,内蒙古乌兰察布 012000)摘 要:目的:分析食品中单核细胞增生李斯特氏菌的检测结果,以及时发现食品安全隐患,为食品安全监管提供参考依据。
方法:严格按照《全国食源性致病菌监测工作手册》中的单核细胞增生李斯特氏菌检验标准,对某市2021年1—12月定期采样的10类常用食品进行单核细胞增生李斯特氏菌检测,分析其阳性检出率。
结果:897份10类常用食品中,检出单核细胞增生李斯特氏菌36份,阳性检出率为4.01%,结论:食品中存在单核细胞增生李斯特氏菌污染的风险,其中以凉拌菜及冷藏食品的污染风险最高,应加强该方面的防控,确保食品安全。
关键词:单核细胞增生李斯特氏菌;食品安全;检测Detection and Analysis of Listeria Monocytogenes in FoodSHI Hongxia(Ulanqab Center for Disease Control and Prevention Inner Mongolia, Ulanqab 012000, China)Abstract: Objective: To analyze the detection results of Listeria monocytogenes in food, find the hidden dangers of food safety in time, and provide reference basis for food safety supervision. Methods: The detection of Listeria monocytogenes in the national manual for the monitoring of foodborne pathogens shall be strictly followed. According to the test standard, 10 kinds of common foods regularly sampled in a city from January to December 2021 were tested for Listeria monocytogenes, and the positive detection rate was analyzed. Conclusion: There is a risk of Listeria monocytogenes contamination in foods, among which cold dishes and refrigerated foods have the highest risk of contamination. Prevention and control in this regard should be strengthened to ensure food safety.Keywords:listeria monocytogenes; food safety; testing单核细胞增生李斯特氏菌广泛存在于土壤、蔬菜、粪便及多数食品中,该病菌对低温环境具有较好的耐受性,在5℃时可大量繁殖,当该病菌进入生物表层后会形成生物膜,并能提高对理化因素的抵抗力,是食源性疾病的主要致病菌之一,可通过粪便或食物进行传播。
食品中单核细胞增生李斯特氏菌检测结果的分析
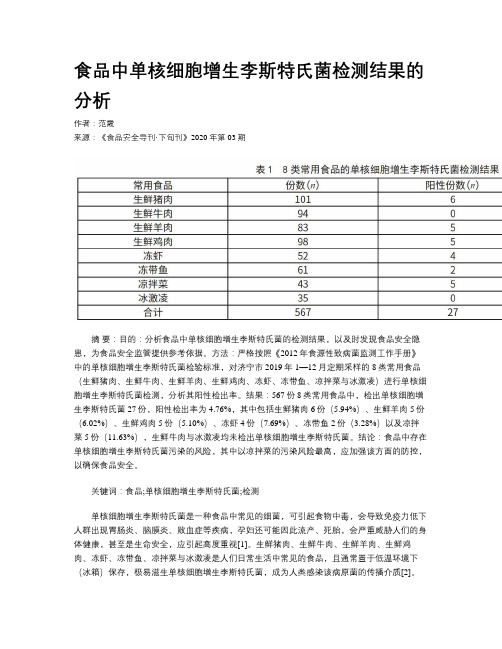
食品中单核细胞增生李斯特氏菌检测结果的分析作者:范霞来源:《食品安全导刊·下旬刊》2020年第03期摘要:目的:分析食品中单核细胞增生李斯特氏菌的检测结果,以及时发现食品安全隐患,为食品安全监管提供参考依据。
方法:严格按照《2012年食源性致病菌监测工作手册》中的单核细胞增生李斯特氏菌检验标准,对济宁市2019年1—12月定期采样的8类常用食品(生鲜猪肉、生鲜牛肉、生鲜羊肉、生鲜鸡肉、冻虾、冻带鱼、凉拌菜与冰激凌)进行单核细胞增生李斯特氏菌检测,分析其阳性检出率。
结果:567份8类常用食品中,检出单核细胞增生李斯特氏菌27份,阳性检出率为4.76%,其中包括生鲜猪肉6份(5.94%)、生鲜羊肉5份(6.02%)、生鲜鸡肉5份(5.10%)、冻虾4份(7.69%)、冻带鱼2份(3.28%)以及凉拌菜5份(11.63%),生鲜牛肉与冰激凌均未检出单核细胞增生李斯特氏菌。
结论:食品中存在单核细胞增生李斯特氏菌污染的风险,其中以凉拌菜的污染风险最高,应加强该方面的防控,以确保食品安全。
关键词:食品;单核细胞增生李斯特氏菌;检测单核细胞增生李斯特氏菌是一种食品中常见的细菌,可引起食物中毒,会导致免疫力低下人群出现胃肠炎、脑膜炎、败血症等疾病,孕妇还可能因此流产、死胎,会严重威胁人们的身体健康,甚至是生命安全,应引起高度重视[1]。
生鲜猪肉、生鲜牛肉、生鲜羊肉、生鲜鸡肉、冻虾、冻带鱼、凉拌菜与冰激凌是人们日常生活中常见的食品,且通常置于低温环境下(冰箱)保存,极易滋生单核细胞增生李斯特氏菌,成为人类感染该病原菌的传播介质[2]。
为了分析食品中单核细胞增生李斯特氏菌检测结果,现就济宁市定期采样的8类常用食品的检测过程与阳性检出率进行分析,汇报如下。
1 资料与方法1.1 样本来源选取本市2019年1—12月定期采样的8类常用食品共567份,其中包括生鲜猪肉101份,生鲜牛肉94份,生鲜羊肉83份,生鲜鸡肉98份,冻虾52份,冻带鱼61份,凉拌菜43份以及冰激凌35份。
食品中单核细胞增生李斯特氏菌能力

食品中单核细胞增生李斯特氏菌能力验证结果分析与讨论马秋莲,周 露,潘馨竹,王 健,马 蓉,徐程伟(宝应县有机食品质量监督检验中心,江苏扬州 225800)摘 要:目的:通过检验食品中单增李斯特氏菌了解实验室关于食品中微生物的检验和检测水平,通过检验技术的更新和检测方法的不断优化,增强实验室整体竞争能力,提升食品检验检测机构检验能力,使微生物实验室外部质控水平得以维护和巩固。
方法:利用BAX Q7对能力验证中的3个样品进行快速筛查,严格依据《食品安全国家标准食品微生物学检验单核细胞增生李斯特氏菌检验》(GB 4789.30—2016),对疑似菌进行鉴定。
结果:编号为270的样品检出为单增李斯特氏菌,编号为318和159的这两个样品中均未检出该致病菌,经过进一步实验,发现这两个样品中的致病菌为英诺克李斯特氏菌。
结论:本实验室顺利完成本次能力验证,结果较满意。
综上表明本实验室具备检验检测单增李斯特氏菌的能力,且检测方法和结果具有一定的准确性。
关键词:食品;能力验证;单核细胞增生李斯特氏菌;检测Proficiency Testing Results and Analysis of Listeriamonocytogenes in FoodMA Qiulian, ZHOU Lu, PAN Xinzhu, WANG Jian, MA Rong, XU Chengwei (Baoying Quality Supervision and Testing Center for Organic Food, Yangzhou 225800, China)Abstract: Objective: Through the inspection of Listeria monocytogenes in food to understand the laboratory on the inspection and detection level of microorganisms in food, through the update of inspection technology and continuous optimization of detection methods, enhance the overall competitiveness of the laboratory, improve the inspection ability of food inspection and detection institutions, so that the microbiology laboratory external quality control level can be maintained and consolidated. Method: BAX Q7 was used to quickly screen 3 samples in the ability verification, and the suspected bacteria were identified in strict accordance with the GB 4789.30—2016. Result: Listeria monocytogenes was detected in the sample numbered 270, while no such pathogen was detected in the two samples numbered 318 and 159. After further experiments, it was found that the pathogenic bacteria in the two samples were Listeria inoknock. Conclusion: The laboratory successfully completed the ability verification, the results are satisfactory. To sum up, this laboratory is capable of testing Listeria monocytogenes, and the detection methods and results have certain accuracy.Keywords: food; capability verification; Listeria monocytogenes; testing自然环境中存在大量的李斯特氏菌,该菌有7个菌株,单增李斯特氏菌作为该菌中的一种,能够引发人、动物共同患病[1]。
食品中单核细胞增生李斯特氏菌的能力验证结果分析

分析检测食品中单核细胞增生李斯特氏菌的能力验证结果分析于 潇(上海中维检测技术有限公司,上海 201600)摘 要:为了提升实验室综合检测能力,保证日常出具的抽检结果准确可靠,本实验室参加了2022年南京市食品药品监督检验院组织的能力验证,能力验证结果评价为满意,表明实验室具备单核细胞增生李斯特氏菌的检验能力。
关键词:单核细胞增生李斯特氏菌;能力验证;质量控制Profificiency Testing Analysis of Listeria monocytogenesin FoodYU Xiao(Shanghai Zhongwei Testing Technology Company, Shanghai 201600, China) Abstract: In order to improve the comprehensive testing ability of the laboratory and ensure the accuracy and reliability of the daily sample test results, the laboratory participated in the ability verification organized by Nanjing Food and Drug Supervision and Inspection Institute in 2022, and the ability verification results were evaluated as satisfactory, indicating that the laboratory has the ability to test Listeria monocytogenes.Keywords:Listeria monocytogenes; profificiency testing; quality control李斯特氏菌属革兰氏阳性菌,广泛存在于自然界中,具有耐低温、耐酸、耐高盐等特点。
单核细胞增生李斯特氏菌国家标准检验方法的验证与探讨

斯特氏菌和英诺克李斯特氏菌菌落形
态与单增李斯特氏菌相似,只是菌落
周围没有水解圈。
2.2 菌株生化特征
实验样品及四种李斯特氏菌标准
菌株生化反应中,与葡萄糖、MR-VP、
麦芽糖、七叶苷、甘露醇等具有相同
的反应结果。另外,与木糖反应结果中,
除伊氏李斯特氏菌的木糖反应为阳
性,其他都为阴性。其中,通过溶血
反应区分单增细胞李斯特氏菌和英诺
关键词:李斯特氏菌;方法验证;生化鉴定
单核细胞增生李斯特氏菌(Listeria monocytogenes) 是 李 斯 特 氏 菌 属 中唯一具有致病性,也是致病力最强 的细菌,是一种人畜共患的病原菌。 它 可 以 穿 过 宿 主 三 个 屏 障, 即 肠 屏 障、血脑屏障和胎盘屏障,然其引起 的疾病的发生率不高,但死亡率可达 20%~30%[1]。单增李斯特氏菌易于在 冷藏食品中存活,是对人类健康危害 最大的一种。在 4 ℃的储存条件下依 然能够生存繁殖,主要存在于牛奶、 乳 制 品、 生 牛 排、 羊 肉、 腌 腊 食 品、 西红柿、沙拉、水产品等中。在我国, 食品中单增李斯特菌要求为不得检出。
按国家标准检验检测方法 GB4789.30-2010[2]。 首 先 使 用 酒 精 灯 对样品表面进行烧灼消毒,之后用无 菌剪刀切割并取样 25 g 深层肌肉,然 后 加 入 225 mL LB1 增 菌 液,30 ℃ 培 养 24 h。 取 0.1 mL, 转 种 于 10 mL LB2 增菌液内,30 ℃培养 24 h。在李 斯特氏菌显色平板以及 PALCAM 平板 上,通过接种环将 LB2 增菌液以划线方 式接种,并于 36 ℃环境中培养 24~48 h; 同时,接种单增李斯特氏菌、英诺克李 斯特氏菌、伊氏李斯特氏菌、斯氏李斯 特氏菌、马红球菌标准菌株 [3],分别作 为阳性对照和阴性对照。从李斯特氏菌 显色平板、PALCAM 琼脂平板上取 5 个 以上的可疑菌落,然后,将菌落接种于 木糖、鼠李糖中,在 36 ℃条件下培养 24 h;并在 TSA-YE 培养基上纯培养后, 再按照染色镜检、动力试验、生化鉴定、 溶血试验和协同溶血试验的顺序进行操 作。最后,使用李斯特氏菌属鉴定试 剂盒和全自动微生物生化鉴定仪鉴定 了 TSA-YE 上纯培养的菌株。
乳粉中单核细胞增生李斯特氏菌能力验证结果与分析

乳粉中单核细胞增生李斯特氏菌能力验证结果与分析单核细胞(monocytes)是一类存在于人体血液和组织中的白细胞(leukocytes)。
它们作为免疫系统中的重要成分,具有很强的吞噬能力和免疫调节功能。
李斯特氏菌(Listeria monocytogenes)是一种革兰氏阳性杆菌,它能够引起严重的人类食物中毒,尤其是婴儿和免疫缺陷患者。
乳粉作为婴幼儿的主要食物,其安全性尤为重要。
为了对乳粉中单核细胞增生李斯特氏菌的能力进行验证,可以进行以下步骤:1.材料准备:-乳粉样品- 特定培养基(如Listeria Enrichment Broth)-李斯特氏菌(已知培养物)-离心管-培养皿2.试验步骤:a.预处理乳粉样品:-取适量的乳粉样品,加入适量的特定培养基-将混合物在摇床上以适当速度摇匀-使用离心机将样品离心,以除去悬浮的杂质b.培养李斯特氏菌:-取一定量的已知培养物,加入特定培养基中-在适当的温度和湿度下,培养李斯特氏菌至适宜的生长期c.接种乳粉样品:-取适量的乳粉样品,加入特定培养基中-添加已培养的李斯特氏菌(适量)到乳粉样品中-使混合物充分混合d.孵化和观察:-将接种混合物接种到适当的培养皿中-将培养皿置于适当的环境中(温度、湿度等)-在一定时间内观察培养皿中是否有李斯特氏菌的生长3.结果与分析:通过观察培养皿中的生长情况,可以得出以下结论和分析:-如果培养皿中出现了李斯特氏菌的生长,说明乳粉样品中存在单核细胞增生的李斯特氏菌能力。
-如果培养皿中未观察到李斯特氏菌的生长,说明乳粉样品中不存在单核细胞增生的李斯特氏菌能力。
-结果应与对照组进行比较,以确定是否存在显著差异。
需要注意的是,这是仅仅通过培养方法进行初步验证,不能判断乳粉样品的感染风险和食用安全性。
为了更准确地评估乳粉中李斯特氏菌的存在和潜在传播风险,还需要进一步的实验和分析方法,如PCR检测、测定菌群数量等。
同时还应结合临床和流行病学调查数据,做出综合评估和判断。
食品中单增李斯特菌检验方法的应用分析

食品中单增李斯特菌检验方法的应用分析摘要:目的:单增李斯特菌定性检测结合实时荧光PCR和MPN计数法,在食品源性致病菌检测中快速进行定性和定量检测。
方法:将单增李斯特菌的菌悬液样品依据不同浓度用细菌培养法和实时荧光PCR法进行比较;分别对当日、冷冻2小时和6小时的增菌液进行MPN计数法定量检测,对三种情况下MPN计数结果进行比较。
结果:细菌培养法和实时荧光PCR法检测两者结果一致;MPN计数法定量检测,(1)和(2)结果吻合,与(3)结果有差异。
结论:实时荧光PCR检测和MPN计数法相结合,避免样品细菌培养法检测出阳性结果,定量检测时重新取样而导致的结果差异,减短检验周期和工作量,使工作效率得到提升。
关键词:食品;单增李斯特菌;检验方法连年来,因食品污染单增李斯特菌导致食品中毒的事件逐渐增多,引起社会各界的广泛关注。
单增李斯特菌是一种人畜共患病的病原菌[1],多存在于土壤、水产品和动物中,食物中涉及较多的是急冻食品、生菜食物和熟食店食物等。
易感人群为新生儿、孕妇和40岁以上的成年人,临床症状表现为发热、化脓性结膜炎和败血症等,死亡率高达30%以上。
本文将从实时荧光定量PCR法和MPN计数法相结合,对单增李斯特菌定量检测进行研究,有关情况如下。
1.材料与方法1.1仪器和试剂标准菌株采用我市提供的50000株单增李斯特菌,使用实时荧光定量PCR仪和离心机,选取实时荧光定量PCR试剂、全自动微生物鉴定仪和革兰氏阳性细菌鉴定卡,培养基选自李氏增菌肉汤等,均在有效期内使用培养基和试剂。
用脑心浸液培养基将80℃标准菌株过夜培养温度控制在30℃,科玛嘉单李斯特显色琼脂平板培养24小时,温度设置为36℃至37℃。
菌落的挑选规格为天蓝色、大小适中和周围有白色晕环,将菌落接种于脑心浸液琼脂平板分纯24小时30℃,菌液的浓度利用生理盐水控制在0.5至0.6麦氏单位,将调整好的菌液作为原液,1ml菌液和9ml无菌生理盐水放在试管中,把试管的液体进行均匀搅拌,制作成10-1菌液,重复上面的步骤,菌液制作成10位系列菌液。
不同培养基检测单核细胞增生李斯特氏菌的结果比较

不同培养基检测单核细胞增生李斯特氏菌的结果比较
陈雨欣;石建华
【期刊名称】《农产品加工·学刊》
【年(卷),期】2015(000)008
【摘要】选择更加适合单增李斯特氏菌检测的固体选择性培养基,同时对国内及国际上常用的4种固体培养基进行比较选择.结果表明,李斯特氏菌显色培养基的选择效果较好,单增李斯特氏菌在李斯特氏菌显色培养基上具有特征性菌落形态,容易与其他李斯特氏菌相区别.建议在采用ISO方法检测及日常工作中增加李斯特氏菌显色培养基的使用,可有效提高单增李斯特氏菌的检出率.
【总页数】2页(P40-41)
【作者】陈雨欣;石建华
【作者单位】苏州出入境检验检疫局,江苏苏州215104;苏州出入境检验检疫局,江苏苏州215104
【正文语种】中文
【中图分类】R115
【相关文献】
1.应用LAMP检测方法检测乳制品中的单核细胞增生李斯特氏菌 [J], 程潇;汪永信;刘娟娟;张波;徐晨;贾贞;安虹
2.不同食品基质中单核细胞增生李斯特氏菌核酸提取方法的比较 [J], 周阳;祝长青;郭云昌;郭桂萍;蒋原;刘秀梅;付瑞燕
3.新疆不同来源单核细胞增生李斯特氏菌血清型的多重PCR鉴定 [J], 尚文婧;赵新
斐;王静梅;剡根强
4.新疆不同来源单核细胞增生性李斯特氏菌分离株的部分生物学特性及相关性分析[J], 尚文婧;赵新斐;王静梅;剡根强
5.可视化跨越式滚环扩增技术检测食品中单核细胞增生李斯特氏菌 [J], 苑宁;张蕴哲;张海娟;于泽;卢鑫;张伟
因版权原因,仅展示原文概要,查看原文内容请购买。
乳粉中单核细胞增生李斯特氏菌能力验证结果与分析

乳粉中单核细胞增生李斯特氏菌能力验证结果与分析总结经验教训为日常的检验工作提供技术性支持。
1 材料与方法1.1 材料、试剂与仪器2瓶白色冻干块状的乳品样品,于2~6 ℃下保存,中国检验检疫科学研究院测试评价中心提供,代码分别为18-Y493,18-X650。
含0.6% 酵母浸膏的胰酪胨大豆琼脂(TSA- YE)、李氏增菌肉汤LB(LB1,LB2)、PALCAM 培养基、李斯特氏菌显色平板、革兰氏染色液试剂盒、单增李斯特氏菌生化鉴定套装,均购自北京陆桥技术股份有限公司。
BSC-1300IIA2型生物安全柜、SW-CJ-2FD型超净工作台、BPX-272型电热恒温培养箱、BXM- 75VE型立式压力灭菌器,上海博迅医疗生物仪器股份有限公司产品。
1.2 标准菌株(1)阳性对照菌株。
单核细胞增生李斯特氏菌,菌株编号:BNCC314197(ATCC19115等效菌株),购于北京北纳创联生物技术研究院。
(2)阴性对照菌株。
英诺克李斯特氏菌,菌株编号:BNCC186087(ATCC33090等效菌株),购于北京北纳创联生物技术研究院。
以上菌株传代次数均未超过5代。
1.3 试验方法[14-15]1.3.1 样品处理样品需要用40.0 mL无菌再水化。
无菌开启样品后,立即加入4 mL无菌水进行再水化,待溶解后,吸出放入无菌瓶中,再反复用余下的无菌水清洗西林瓶内壁,回收清洗液放入上述无菌瓶中,此溶液即为待测样品原液。
1.3.2 增菌以无菌操作吸取取25 mL样品原液转至含有225 mL LB1增菌液的均质袋中,在拍击式均质器上连续均质1~2 min,于30±1 ℃下培养24±2 h,移取0.1 mL,转种于10 mL LB2增菌液内,于30±1 ℃下培养24±2 h。
单增李斯特氏菌常见的增菌方法有LB二次增菌法,EB法、改良FDA法及Fraser肉汤增菌法,通过4种方法对同一样品进行增菌,采用PALCAM选择性平板进行分离,再进行国标生化鉴定,对比4种增菌方法对样品的检出率,LB二次增菌法是4种方法中检出率较高且较为稳定的增菌方法,因此选择LB二次增菌法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Ke y w o r d s :L i s t e r i a ;c u l t u r e me d i a ;c o mp a r i s o n
单 核细胞 增 生李 斯特 氏菌 ( L i s t e r i a m o n o c y t 0 一 培 养基 、O x f o r d琼脂 、营养 肉汤 、T S A — Y E等 ,北京 g e n e s )广 泛 存 在 于 自然 界 中 ,并 在 食 品加 工 生 产 及 陆桥技 术有 限责 任公 司产 品 。 贮 藏 中对 大 多 数 食 品 ( 如奶 酪 、生 肉及 肉制 品 、鸡 1 . 2 方法 蛋 、蔬 菜 沙 拉 、海 产 品及 即食 食 品) 都 有 不 同程 度 依据 G B 4 7 8 9 . 3 0 —2 0 1 0食 品安 全 国家 标 准 食 品 的污 染 ,对 不 同盐 质 量分 数 、p H值 及 温度 有 很强 的 微 生 物 学 检 验 单 核 细 胞 增 生 李 斯 特 氏菌 检 验 ;I S O 1 1 2 9 0-1 Mi c r o b i o l o g y o f f o o d a nd a n i ma l f e e d i n g s t uf f s — — 耐受 性 ,并 可 在 低 温 条 件 下 生长 。单 核 细 胞 增 生 李 r i z o n t a l me t ho d f o r t h e d e t e c t i o n a n d e nu me r a t i o n o f 斯特 氏菌 对 人 类 和 动 物 可 引起 流产 、败 血 症 和 脑 膜 Ho Li s t e r i a m o no c y t o g e n e s Pa r t 1 De t e c t i o n m e t ho d。 炎 等严 重 疾 病 ,其 易感 人 群 主要 为 孕 妇 、老 人 、新 生儿 和免 疫 缺 陷人群 l 1 J 。单 核 细 胞增 生李 斯 特 氏菌 与 将5 种标准菌株经过 2 4 h增菌后 的营养 肉汤分 A L C A M、科 玛 嘉 李 斯 特 菌 显 色 培 养 大 肠 杆 菌 、沙 门 氏菌 、金 黄 色 葡 萄球 菌 并 称 为 四大 别 划 线 分 离 至 P 食源性细菌l 2 l 。 因此 ,采用合适的培养基提高食品中 基 、O fo x r d琼 脂 及 T S A — Y E这 4种 培 养 基 平 板 上 , 的检 出率 对人 类食 品 安全有 着 重要 意义 。 T S A — Y E于 3 O℃下 培 养 2 4 h ,其 余 则 在 3 6 c c下 培 养2 4 ~ 4 8 h ,观察 菌 落 的生 长 特征 。
Abs t r a c t : Cho o s e mo r e s ui t a bl e f o r 山e de t e c t i on o f Li s t e r i a mo no c y t o g e ne s s o l i d s e l e c t i v e me di um . m e a nwhi l e on t he
( S u z h o u E n t r y - e x i t I n s p e c t i o n a n d Q u a r a n t i n e B u r e a u ,S u z h o u ,J i a n g s u 2 1 5 1 0 4 ,C h i n a )
性菌落形态 ,容 易与其他李斯特 氏菌相 区别 。建议在采用 I S O方 法检测及 日常工作 中增加李斯 特氏菌显色培养基 的 使用 ,可有效提高单增李斯特氏菌 的检 出率 。
关键词 :李斯特菌 ;培养基 ;结果 比较
中 图分 类号 :R1 1 5 文 献标 志码 :A d o i :1 0 . 3 9 6 9 / j i s s n . 1 6 7 1 — 9 6 4 6 ( X) . 2 0 1 5 . 0 8 . 0 4 1
d o me s t i c a n d i n t e r n a t i o n a l me d i a c o mmo n l y u s e d f o u r k i n d s o f s o l i d c o mp a r e s e l e c t i o n .T h e r e s u l t s h o we d t h a t L i s t e r i a c h r o mo g e n i c me d i a i s b e t t e r ,L i s t e r i a mo n o e y t o g e n e s b a c t e r i a wi t h c h a r a c t e r i s t i c c o l o n y mo r p h o l o g y o n L i s t e r i a c h r o mo g e n i c me d i a ,r e a d i l y d i s t i n g u i s h e d f r o m o t h e r L i s t e r i a . I s r e c o mme n d e d t o a d o p t I S 0 me t h o d d e t e c t i o n a n d d a i l y wo r k t o i n c r e a s e t h e
C o mp a r i s o n o f Di fe r e n t C u l t u r e Me d i a f o r De t e c t i o n o f Li s t e r i a Mo n o c y t o g e n e s
CHEN Yu x i n.S HI J i a n h u a
第8 期 ( 总第 3 90期) 2 0 1 5年 8月
农 产 品加 工
F a r m Pr o d u c t s P r o c e s s i n g
No . 8
Au g .
文章 编 号 :1 6 7 1 — 9 6 4 6( 2 0 1 5 )0 8 b 一 0 0 4 0 — 0 2
us e o f Li s t e r i a c h r o mo g e ni c me di a c a n e fe c t i v e l y i mpr o v e t h e de t e c t i o n r a t e o f Li s t e r i a mon o c y t o g e ne s .
不 同培 养基检测 单核 细胞增 生李 斯特 氏菌 的结果 比较
陈 雨欣 ,石 建 华
( 苏州 出入境检验检疫局 ,江苏 苏州 2 1 5 1 0 4 )
摘 要 :选择更加 适合单增李斯特 氏菌检测 的固体 选择性培养基 ,同时对 国内及 国际上常用 的 4种固体培养基进行 比 较选择 。结果表 明 ,李斯特氏菌显色培养基 的选 择效果较好 ,单 增李斯特 氏菌 在李斯特 氏菌显 色培养基上具有特 征
