最新人教版高中化学教师下载中心:专题一 物质的组成、性质、分类和化学用语
专题一:物质的组成、分类、性质变化及化学用语

成 与
三、物质的性质与变化
分
类 四、化学用语
一、物质的组成
宏观角度 由元素组成
物
质
分子
原子
微观角度 由微粒
构成
离子
注意:
金属阳离子和电子
元素只讲种类、不讲个数。微粒既可以讲种类又可讲个数!
由分子构成的物质:
(1).所有非金属氢化物
物 (2).常见的除:金刚石、石墨、晶体硅、锗、 质 硼等外部分非金属单质 类 别 (3).常见的除SiO2外的部分非金属氧化物
D. C、Al2O3、Ar、I2
√ 例2、判断正误(正确的打“√”,错误的打“×”)。
(1)元素在自然界的存在形式有原子、分子或离子 ( )
× (2)在化学变化中,分子可以再分,离子和原子不可以
再分。( )
√ (3)同一种元素可能有多种不同原子,同一种原子也可
能形成不同的离子。( ) (4)原子与该原子形成的简单离子相对质量几乎相等。
③离子电子层结构(注意书写)
注意:
1.由离子构成的化合物, 其固体属离子晶体, 其基本微粒是 离子。 思考:有离子存在一定是离子晶体? 2.离子晶体中一定有阴阳离子。 不一定;如:金属单质
问题:有阳离子存在的晶体一定有阴离子吗? 不一定;如:金属单质
3.在离子晶体中必有离子键,同时可能还含有共价键或配 位键。
(5)晶体硅
(6)酒精
(7)固态KOH
(8)熔融状态的KNO3
(9)葡萄糖
(10)CO2
(11) Na2O
(12)醋酸
1.元素:
(1).定义:具有相同核电荷数(质子数)的同一类原子的总称
注意: ①元素只讲种类, 没有数量的含义 ②同一类原子包括同位素、离子
优秀课件专题一 物质的组成、性质、分类和化学用语(共49张PPT)

考点二 物质的性质与变化
主干回扣
1.(1)物理变化: 成的变化。 (2)化学变化的实质:① 学键的形成。 (3)物理变化过程中一定 理变化。 答案 (1)无 有 (2)原子 (3)无 化学变化,化学变化过程中可能有物 的重新组合;②旧化学键的断裂和新化 新物质生成的变化;化学变化: 新物质生
2.正误判断,正确的划“√”,错误的划“✕”。 (1)臭氧变成氧气是物理变化 ( ) ) )
组成的纯净物;化合物:由
组成的纯净
物。
(4)纯净物:由 成。 组成;混合物:由 组
(5)酸:在水溶液中电离出的阳离子全部为 液中电离出的阴离子全部为
H (或N 4 )和
的化合物;碱:在水溶 的化合物;盐:由 种元素组
组成的化合物;氧化物:由
成且其中一种元素为氧元素的化合物。 (6)酸性氧化物:与 反应生成盐和水的氧化物;碱性氧化物:与
(2)将蓝色的硫酸铜晶体放入浓硫酸中发生了物理变化 (
(3)煤的“气化”、煤的“液化”、煤的“干馏”都是化学变化 ( (4)分馏、蒸馏、蒸发、萃取、分液、过滤都属于物理变化 ( (5)加热NH4Cl晶体,固体从试管底部移到上部属于物理变化 ( (6)用铂丝蘸取NaCl溶液进行焰色反应是化学变化 ( (7)正丁烷转化为异丁烷属于物理变化 (
物。 氯气是单质,不属于非电解质,故 C 不正确。
3.(2017北京理综,6)古丝绸之路贸易中的下列商品,主要成分属于无机 物的是 (
)
A.瓷器
B.丝绸
C.茶叶
D.中草药
答案 A 瓷器的主要成分是硅酸盐,属于无机物;丝绸的主要成分是蛋 白质,属于有机物;茶叶、中草药的主要成分是有机物。
典题精练
题组一 物质的组成和分类 ) 1.(2017东北三省四市二模,7)化学与人类生活、生产息息相关,下列说 法错误的是 (
高考化学 专题精讲 物质的组成、性质和分类 新人教版【精品教案】

非极性键 极性键
极性分子
空间结构 不对称
正负电荷重心 极性键(可能
不重叠,由于分 还含有非极
布不均匀
性键)
判断要点
空间结构 对称
空间结构 不对称
实例 H2 、 CO2 、 BF3 、 CCl4 、 C2H2、C2H4、 C6H6
HCl 、 H2O 、 NH3、CH3Cl
10、晶体的结构与性质
类型
规
核外电子总是尽先排满能量最低、离核最近的电子层,然后才由里往外,依次排
律 4 在能量较高,离核较远的电子层。
原 原子结构
子 示意图和
结 离子结构
构 示意图
的
表
示 电子式
方
法
6、简单微粒半径的比较方法
原 1、电子层数相同时,随原子序数递增,原子半径减小。
子 例:rNa>rMg>rAl>rSi>rp>rs>rCl 半 2、最外层电子数相同时,随电子层数递增原子半径增大。
物的熔沸点就越高。
8、共价键 定义 形成条件 本质 表示方法 形成过程
分
类
键能 键 参
键长 数
键角
原子间通过共用电子对所形成的化学键,叫共价键。 一般是非金属元素之间形成共价键,成键原子具有未成对电子。 成键的两原子核与共用电子对的静电作用。 1、电子式 2、结构式
分类依据:共用电子对是否发生偏移
定义:共用电子对不偏于任何一方。
碱
正盐
盐 酸式盐 碱式盐
复盐
酸性氧化物 碱性氧化物 两性氧化物
知识结构
※比较四个概念
同位素
同素异形体
同系物
同分异构体
对象
核素
单质
有机化合物
2025年高考化学总复习(人教版)第1讲物质的组成、性质和分类

A.NaOHB.Mg3N2
C.NH4CNOD.CaO
答案:C
考点二 物质的性质和变化
1.物理变化与化学变化的两种判断方法
(1)从宏观上判断:有新物质生成的是化学变化,反之为物理变化。
(2)从微观上判断:有旧化学键断裂,同时有新化学键形成的是化学变化;只有化学键断裂或形成的不一定是化学变化,如NaCl晶体的熔化、NaCl的结晶等。
A.石墨烯B.不锈钢
C.石英光导纤维D.聚酯纤维
答案:D
解析:石墨烯是一种由单层碳原子构成的平面结构新型碳材料,为碳的单质,属于无机物,A不符合题意;不锈钢是Fe、Cr、Ni等的合金,属于金属材料,B不符合题意;石英光导纤维的主要成分为SiO2,属于无机非金属材料,C不符合题意;聚酯纤维俗称“涤纶”,是有机高分子材料,属于有机物,D符合题意。
符合上述转化关系的常见非金属有C、S、P等,但N、Si等不符合上述转化关系。
学生用书第4页
[正误辨析]
1.蛋白质的变性、纳米银粒子的聚集都是化学变化()
2.用铂丝蘸取Na2SO4、Na2CO3、NaCl溶液进行焰色试验是化学变化()
3.232Th转化成233U是化学变化()
4.Na2CO3·10H2O的风化是化学变化()
考向一 纯净物和混合物的判断
1.按要求回答问题。
①冰水混合物;②水煤气;③铝热剂;④普通玻璃;⑤水玻璃;⑥有机玻璃;⑦漂白粉;⑧TNT;⑨H2SO4;⑩含氧40%的氧化镁;花生油;福尔马林;密封保存的NO2气体;CuSO4·5H2O;液氯;王水;KAl(SO4)2·12H2O;分子式为C5H10的烃;分子式为C7H8的芳香烃。
2019-2020年高中化学 专题一 物质的组成、性质和分类 化学用语教案

2019-2020年高中化学专题一物质的组成、性质和分类化学用语教案【专题要点】物质的组成、性质和分类、化学用语是化学最基础的主干知识,是对物质及其变化的本质特征的反映。
它们涉及的化学概念、物质的分类方法和它们相互转化的方式,是中学化学最基本的知识,也是学生从化学视觉观察和思考问题的必备知识,同时也是高考的重点内容。
复习本考点是应深刻理解化学概念的内涵和外延,掌握不同概念间的区别和联系,掌握物质的分类方法及物质间相互转化的方式和转化条件;要理解各个化学用语的的实际含义,掌握反应的条件与本质,正确、科学、规范的进行运用。
本考点在高考中的题型主要以选择题为主,常常结合元素化合物来进行考查。
从09年和10年高考考题来看高考题除了直接考查基本概念外,还考查以物质组成和分类的概念为出发点,以反映高新科技和人们普遍关注的社会问题为切入点,逐步向环保、高科技、生产等方面渗透发展。
除此之外我们还可以看出来元素、物质的组成与分类、化学用语,以成为高考的一个热点,而且融入其他专题进行考查。
【考纲要求】1.理解分子、原子、离子、元素等概念的涵义,初步了解原子团的定义。
2.理解物理变化与化学变化的区别和联系3.理解混合物和纯净物、单质和化合物、金属和非金属的概念4.了解同素异形体的概念,注意其与同位素、同系物、同分异构体等的区别。
5.理解酸、碱、盐、氧化物的概念及其相互联系。
6. 熟记并正确书写常见元素的名称、符号、离子符号7. 熟悉常见元素的化合价。
能根据化合价正确书写化学式(分子式),或根据化学式判断化合价。
8. 了解原子结构示意图、分子式、结构式和结构简式的表示方法9. 掌握溶液、悬浊液、乳浊液、胶体的概念,区别及鉴别它们的方法;10.掌握胶体的本质特征及性质;【教法指引】复习此专题时要做到“准确”、“系统”、“灵活”,可以从三点入手:1.以高考的热点、考点、难点为依据,合理设置复习内容和练习题,熟练掌握解题思路、注重方法、技巧,不求面面俱到,但求在某些考点的深度和广度的挖掘上有所突破2.加强区别相似概念的异同,理顺不同概念间的联系,进而形成连贯的知识系统。
物质的组成、性质和分类

2021年高考化学二轮精品讲练析物质的组成、性质和分类一、物质的组成1.元素——宏观概念,说明物质的宏观组成。
元素是质子数一样的一类原子的统称。
质子数一样的微粒不一定是同一种元素,因为微粒的含义要比原子广泛。
2.分子、原子、离子、“基〞、“根〞、“碳正离子〞——微观概念,说明物质的微观构成。
★原子(1)原子是化学变化中的最小粒子。
确切地说,在化学反响中,原子核不变,只有核外电子发生变化。
(2)原子是组成某些物质(如金刚石、晶体硅等)和分子的根本粒子。
(3)原子是由更小的粒子构成的。
(4)原子的概念是古希腊哲学家德谟克利特从哲学的角度首先提出来的。
1803年英国化学家道尔顿提出了原子说。
目前人类对原子构造的认识正在不断地深入。
注意:化学反响的本质就是原子的重新排列和组合。
原子与元素的联系与区别★离子离子是指带电荷的原子或原子团。
①离子的种类:②离子的生成途径:③存在离子的物质:离子化合物:NaCl、CaC2、C17H35COONa;电解质溶液中:盐酸、稀硫酸等;金属晶体中:钠、铁、铜等。
注意:在金属晶体中只有阳离子,而没有阴离子。
分子、原子、离子均是组成物质的根本粒子,是参加化学反响的根本单元,是化学研究的微观对象。
★分子:分子是能够独立存在并保持物质化学性质的一种粒子。
完整理解分子的概念,应包括以下几个方面。
①分子是一种粒子,它同原子、离子一样是构成物质的根本粒子。
如:水、氧气、干冰、蔗糖等就是由分子组成的物质。
②分子有质量,其数量级约为10—26kg。
③分子间有间隔,并不断运动着。
④同种分子的性质一样,不同种分子的性质不同。
⑤每个分子一般是由一种或几种元素的假设干原子按一定方式通过化学键结合而成的。
⑥按组成分子的原子个数,可把分子分成⑦分子间存在相互作用,此作用称作分子间作用力(又称范德华力),它是一种较弱的作用力。
★“基〞、“根〞、“碳正离子〞“基〞是指分子中除去一个原子或原子团以后剩下的原子团(也可能是单个原子),它是电中性的,通常不能稳定存在,如—NO2硝基、—CH3甲基、—SO3H磺酸基等(注意磺酸基不能写成—HSO3)。
最新【PPT】专题一物质的组成、性质、分类及化学用语ppt课件

从组成看,1个HNO3分子只电离出1个H+,故它是一元 酸;HNO3在溶液中完全电离成H+和NO-3,故它是强 酸;HNO3容易挥发,故它是挥发性酸;强酸性和挥发 性反映了HNO3的性质。Mg(OH)2是二元碱是从组 成看的,说明1 mol Mg(OH)2能电离出2 mol OH-, 而难溶性碱、中强碱是它的性质。Al2O3是两性氧化 物,说明它既能与OH-反应,又能与H+反应,是从性
素形成的该物质,来判断是单质还是化合物。 (2)对于单质,根据结构和性质可判断是否是同素异形体。
(3)对于化合物可根据化学键来判断:①若含有 离子键,则一定是离子化合物,如NaCl、 NH4Cl、Na2SO4;②若全以共价键形成,则是 共价化合物,如CO、SiO2、HNO3。
(4)对于化合物可根据组成元素(是否含碳)分 为无机化合物和有机化合物:①无机化合物 根据组成又可分为氧化物、氢化物、酸、碱、 盐,它们可由原子组成,也可由分子或离子组
[点拨] (1)化学变化中常伴有发光、放热现象, 但有发光、放热现象的变化不一定属于化学 变化,如金属受热发光。
(2)化学变化中一定存在化学键的断裂和形成, 但存在化学键断裂的变化不一定是化学变 化,如HCl溶于水、熔融NaCl电离等。
(3)原子的裂变、聚变虽有新物质生成,但它不 属于中学化学意义上的化学变化。
【PPT】专题一物质的组成 、性质、分类及化学用语
一、物质的组成
(2)对于化合物可根据晶体类型判断:离子晶体是由 阴、阳离子构成的;分子晶体是由分子构成的;原子 晶体是由原子构成的。
(3)对于单质也可根据晶体类型判断:金属单质是由 金属阳离子和自由电子构成的;原子晶体、分子晶 体分别由原子、分子构成。
空气中燃烧后消失 B.块状生石灰在空气中逐渐变成粉末;晶体碳
物质的组成、性质与分类化学用语
12.下列可用相同的方法除去混有的杂质的是( B ) A.淀粉溶液中混有少量NaCl杂质;蔗糖中混有少量NaCl杂质
B.Fe(OH)3胶体中混有少量盐酸;淀粉溶液中混有少量KI C.Na2CO3中混有少量NaHCO3;NaHCO3中混有少量Na2CO3 D.铁粉中混有少量硫粉;碘中混有少量NaCl
18.X、Y、Z 是三种常见元素的单质,甲、乙是两种常见 的化合物,这些单质和化合物之间存在如图所示的关系,下列 说法正确的是( C )
A.X、Y、Z 一定都是非金属单质 B.X、Y、Z 中至少有一种是金属单质 C.若 X、Y 都为金属单质,则 Z 必为非金属单质 D.若 X、Y 都为非金属单质,则 Z 必为金属单质
1.熟记并正确书写常见元素的名称、符号、离子符号。
化学用 2.熟悉常见元素的化合价。能根据化合价正确书写化
3语
学式(分子式),并能根据化学式判断化合价。 3.了解原子结构示意图、分子式、结构式和结构简式
的表示方法。
一、物质的组成
1.下列广告用语在科学性上没有错误的是( D ) A.这种饮料中不含任何化学物质 B.这种蒸馏水绝对纯净,其中不含任何离子 C.这种口服液含丰富的氮、磷、锌等微量元素 D.没有水就没有生命
二、物质的分类
二、物质的分类
一)物质的分类分析
1. 物质是否有固定的熔、沸点是区别纯净物和混合物的重要标
志。如玻璃无固定的熔点,石油无固定的沸点,两者均为混
合物。
2. 常见的混合物:溶液、悬浊液、乳浊液、胶体、高分子材料、
漂白粉(漂粉精)、铝热剂、天然油脂、碱石灰、福尔马林、
王水、同素异形体组成的物质(如红磷和白磷)等。
HClO中H与O相连,应写成
高一化学复习专题一
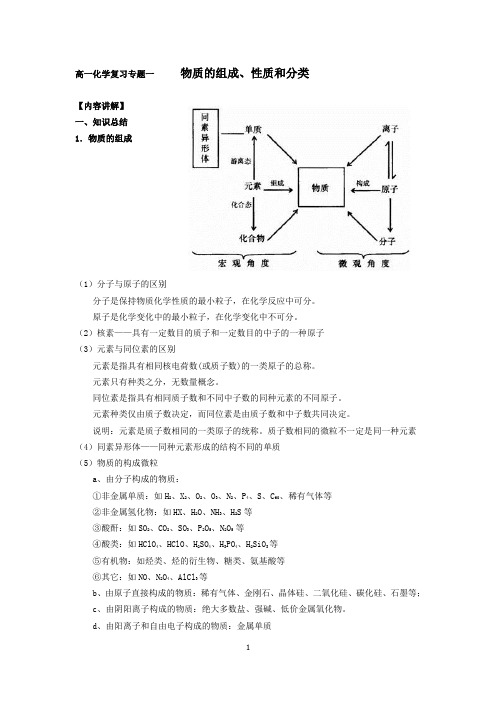
高一化学复习专题一物质的组成、性质和分类【内容讲解】一、知识总结1.物质的组成(1)分子与原子的区别分子是保持物质化学性质的最小粒子,在化学反应中可分。
原子是化学变化中的最小粒子,在化学变化中不可分。
(2)核素——具有一定数目的质子和一定数目的中子的一种原子(3)元素与同位素的区别元素是指具有相同核电荷数(或质子数)的一类原子的总称。
元素只有种类之分,无数量概念。
同位素是指具有相同质子数和不同中子数的同种元素的不同原子。
元素种类仅由质子数决定,而同位素是由质子数和中子数共同决定。
说明:元素是质子数相同的一类原子的统称。
质子数相同的微粒不一定是同一种元素(4)同素异形体——同种元素形成的结构不同的单质(5)物质的构成微粒a、由分子构成的物质:①非金属单质:如H2、X2、O2、O3、N2、P4、S、C60、稀有气体等②非金属氢化物:如HX、H2O、NH3、H2S等③酸酐:如SO2、CO2、SO3、P2O5、N2O5 等④酸类:如HClO4、HClO、H2SO4、H3PO4、H2SiO3等⑤有机物:如烃类、烃的衍生物、糖类、氨基酸等⑥其它:如NO、N2O4、AlCl3等b、由原子直接构成的物质:稀有气体、金刚石、晶体硅、二氧化硅、碳化硅、石墨等;c、由阴阳离子构成的物质:绝大多数盐、强碱、低价金属氧化物。
d、由阳离子和自由电子构成的物质:金属单质2.物质的分类(1)混合物与纯净物的区别①分散系(如溶液、胶体、浊液等);②高分子化合物(如蛋白质、纤维素、聚合物、淀粉等);③常见特殊名称的混合物:石油、石油的各种馏分、煤、福尔马林、油脂、天然气、水煤气、液化石油气、黄铜(含Zn)、青铜(含Sn)、苦卤等。
④常见无机混合物:ⅠA 碱石灰(NaOH+CaO)草木灰(主要成分K2CO3)ⅡA大理石(主要CaCO3)、电石(主要CaC2)、水垢(CaCO3+Mg(OH)2)ⅢA铝热剂(Al粉和某些金属氧化物)ⅣA玻璃、水泥、陶瓷、水玻璃(即硅酸钠的水溶液)、黑火药ⅤA王水(体积比(浓HCl:浓HNO3)=3:1)VIIA 漂白粉、漂白液、漂粉精、84消毒液Ⅷ钢铁说明:①由同种元素构成的物质不一定是纯净物,例如同素异形体。
专题一 物质的组成、性质、分类及化学用语

一、 选择题 ( 每小题 4 分, 共 60 分 ) 1. 下列物质分类正确的是 ( ) A. SO2 、 SiO2 、 CO 均为酸性氧化物 B. 稀豆浆、 硅酸、 氯化铁溶液均为胶体 C. 烧碱、 冰醋酸、 四氯化碳均为电解质 D. 福尔马林、 水玻璃、 氨水均为混合物 2. 氰酸铵 (NH4 OCN) 与尿素[CO(NH 2)2( ] A. 都是共价化合物 C. 互为同分异构体 A. 丙烯的结构简式: C3H 6 ∶ B. 氢氧根离子的电子式: ∶ [ O ∶ H]∶
+17 2 C. 氯原子的结构示意图: 8 8
B. 都是离子化合物 D. 互为同素异形体 )
3. 下列有关化学用语表示正确的是 (
)
A. HCl 、 NO2 溶于水都有化学键断裂 , 因此均属于
D. 中子数为 146 、 质子数为 92 的铀原子: 4. 下列有关化学用语使用正确的是 ( H ∶ A. NH4 Br 的电子式: [H∶ N ∶ H]+Br∶ H
A
HCl H SO
2 4
B
酚酞 石蕊
CNΒιβλιοθήκη Cl NaO H7. 下列说法错误的是 (
)
A. 天然油脂的分子中含有酯基, 属于酯类
1
高三二轮复习专题 化学 B. 所得的分散系中的分散质为 Fe2O3 C. 给分散系通电时阳极周围黑色不变 D. 该分散系能产生丁达尔效应 13. 纳米是长度单位, 1 nm=10 - 9 m, 当物质的颗粒 达到纳米级时, 会具有一 些特殊的性质。如由 铜制成 的 “ 纳米铜” 具 有非常强的化学活性 , 在空气中 可以燃 烧。下列关于 “纳米铜” 的叙述正确的是 ( A.“纳米铜” 比铜片的金属性强 B. “纳米铜” 比铜片更易失去电子 C. “纳米铜” 比铜片的氧化性强 D.“纳米铜” 的还原性与铜片相同 14. 《美国化学会志》 报道: 中国科学家以二氧化碳 为碳源、 金属钠为还原剂, 在 470 ℃, 80 MPa 条件下合成 出金刚石, 具有深远意义。下列说法不正确的是 ( A. 此反应中金刚石是氧化产物 B. 由二氧化碳合成金刚石是化学变化 C. 金刚石是碳单质的一种同素异形体 D. 此反应中钠元素发生氧化反应 15. 以下推理中正确的是 ( 的物质一定是纯净物 B. 金属 铝排在金属 活动性顺序 表中氢元素 的前 面, 铝与酸反应一定放出氢气 C. 中 和反 应都 有盐 和水生 成, 有 盐和水 生成 的 反应都属于中和反应 D. 氧化 物中 都含有 氧元 素, 含氧 元素 的化合 物 不一定是氧化物 二、 非选择题 (共 4 小题, 40 分) 16. ( 10 分 ) 现 有 NH3 、 F2 、 Cl2 、 Na、 Fe、 Na2O、 Na2O2、 SO2 、 CO2、 NO2 等物 质, 根据 它们与 水是否发 生氧化 还 原反应进行分类。 生成物水溶液呈酸性) A组 ( 甲组 题 给 物 质 乙组 C组 D组 E组 请回答下列问题: ( 1) 图中所示的分类方法叫 ( 2) 淡 黄色 固体 位 于 mol 该物质与水反应转移电子 ; 组 (填 “A~E ” ) , 1 mol; (水作氧化剂 ) (水作还原剂) (水既 不作 氧化 剂又 不 作作还原剂 ) B组 ( 生成物水溶液呈碱性) ) A. 单质 都是 由同种 元素 组成的 , 只含 一种元 素 ) 为 ) 其水溶液呈弱酸性的原因 应, 其化学方程式为 成, 其化学方程式为 ; ; 。
专题一 物质的性质、组成和化学用语

仁一北
高三化学备课
C
)
二轮复习
专题一 物质的组成、性质和化学用语
3. 化学家将研究气体与固体(或液体)在界面上所发生的物理、化学现象 的科学称为表面化学。对下列现象的研究不属于表面化学范畴的是 ( A ) A.氯化银在水中的溶解平衡 B.氢氧燃料电池中电极上的反应 C.铁在潮湿的空气中生锈 D.氮气与氢气在铁触媒作用下化合 4. 下列变化中属于物理变化的是 ( D ) A.剩饭变馊 B.自行车生锈 C.牛奶变酸 D.电灯发光 5. 下列变化不能说明发生了化学变化的是 A.变化时有电子的得失或共用电子对的形成 B.变化时释放出能量 C.变化过程中有旧化学键的断裂和新化学键的形成 D.变化前后原子的种类和数目没有改变,分子种类增加了
(2)物理变化:金属导电、盐析、活性炭吸附、渗析。
1. (2012·重庆理综,6)化学工业是国民经济的支柱产业。下列生产过 程中不涉及化学变化的是 ( D ) A.氮肥厂用氢气和氮气合成氨 B.钢铁厂用热还原法冶炼铁 C.硫酸厂用接触法生产硫酸 D.炼油厂用分馏法生产汽油
2. 下列诗句或谚语都与化学现象有关,下列说法不正确的是 ( A.“水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化 B.“落汤螃蟹着红袍”肯定发生了化学变化 C.“滴水石穿,绳锯木断”不包含化学变化 D.“野火烧不尽,春风吹又生”包含了多种化学变化
仁一北
高三化学备课
二轮复习
专题一 物质的组成、性质和化学用语
题组一 概念的判断与理解 1.正误判断,正确的划“√”,错误的划“×” (1)金属氧化物均为碱性氧化物 (× ) (2)HClO是弱酸,所以NaClO是弱电解质 (× ) (3)HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均为离子化合物 × ( ) (4)石油是混合物,其分馏产品汽油为纯净物 (× ) (5)BaSO4的水溶液不易导电,故BaSO4是弱电解质 (× ) (6)SO2、SiO2、CO均为酸性氧化物 ( ×) (7)烧碱、冰醋酸、四氯化碳均为电解质 ( ×) (8)福尔马林、水玻璃、氨水均为混合物 (√) (9)黑火药由硫黄、硝石、木炭三种物质按一定比例混合而成 (√) (10)KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 (× )
高考化学 二轮复习 专题一 基本概念 第1讲 物质的组成、性质、分类及常用化学用语

2. (2015·湖北武汉四校联考)下列叙述与胶体无关的是( D ) A.鸡蛋白溶液中分散质的微粒直径在10-9~10-7 m之间 B.当日光从窗隙射入暗室时,可观察到一条光柱 C.明矾[KAl(SO4)2·12H2O]可用作净水剂 D.向氯化铁溶液中加入氢氧化钠溶液,产生红褐色沉淀
解析:由 A 项可知鸡蛋白溶液属于胶体;由 B 项可知暗室里 的空气能产生丁达尔效应;C 项,明矾电离出的 Al3+水解产 生 Al(OH)3 胶体,Al(OH)3 胶体粒子吸附水中悬浮物后形成沉 淀而净水;D 项,发生反应:Fe3++3OH-===Fe(OH)3↓,产 生红褐色沉淀,与胶体无关。
2.下列物质:①冰醋酸 ②NaOH溶液 ③CaO ④小苏打
⑤纯碱 ⑥SiO2 ⑦CO2 ⑧淀粉溶液 ⑨水玻璃 ⑩Al ⑪Cl2 ⑫碱石灰 (1)属于纯净物的是__①__③_④__⑤__⑥__⑦__⑩_⑪______,属于酸性氧化 物的是_⑥_⑦_______,属于酸式盐的是④________。 (2)属于混合物的是___②__⑧__⑨_⑫______,其中②__⑨____属于溶液, __⑧_____属于胶体。
解析:A 项,S 燃烧生成的是 SO2,错误;B 项,铜锈的主要 成分为碱式碳酸铜:Cu2 (OH)2CO3,而明矾溶液中的 Al3+发 生水解使溶液显酸性,可以与碱式碳酸铜发生反应,正确;C 项,碳酸氢钠可以与水杨酸反应,正确;D 项,水中的钙离子 与肥皂发生反应生成高级脂肪酸钙,降低了肥皂的去污能力, 正确。
下列物质分类正确的是(D ) A.SO2、SiO2、CO均为酸性氧化物 B.稀豆浆、硅酸、氯化铁溶液均为胶体 C.烧碱、冰醋酸、四氯化碳均为电解质 D.福尔马林、水玻璃、氨水均为混合物 解析:CO为不成盐氧化物,A错;氯化铁溶液不是胶体,B 错;四氯化碳属于非电解质,C错;故选D。
高考化学二轮复习专题1物质的组成、性质、分类及化学用语课时作业

专题一物质的组成、性质、分类及化学用语一、选择题1.“化学是人类进步的关键”。
下列有关说法能反映正确化学观点的是() A.改变物质的性质不一定要通过化学变化B.天然物质都比人造物质好C.一种元素可有多种离子,但只有一种原子D.根据分散系是否具有丁达尔效应,分散系分为溶液、胶体和浊液2.下列情况不能用胶体知识加以解释的是() A.氯化铝溶液中加入小苏打溶液会产生白色沉淀和无色气体B.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗C.水泥厂、冶金厂常用高压电除工厂烟尘,以减少对空气的污染D.牛油与烧碱溶液共热,向反应所得溶液中加入食盐,则有固体析出3.(2010·上海,5)下列判断正确的是() A.酸酐一定是氧化物B.晶体中一定存在化学键C.碱性氧化物一定是金属氧化物D.正四面体分子中键角一定是109°28′4.下列各组物质的分类都正确的是(括号里的是类别) () A.空气(混合物)、C2H5OH(醇)、H2SO4(离子化合物)、CO2(非电解质)B.液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强电解质)C.HCl(共价化合物)、CH3COOH(羧酸)、Na2O2(碱性氧化物)、CH3I(卤代烃)D.NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯)5.生活中遇到的某些问题,常常涉及化学知识,下列各项叙述不正确的是() A.鱼虾放置时间过久,会产生令人不愉快的腥臭味,应当用水冲洗,并在烹调时加入少量食醋B.“酸可以除锈”、“洗涤剂可以去油”都是发生了化学变化C.被蜂蚁蜇咬会感觉疼痛难忍,这是由于人的皮肤被注入了甲酸的缘故,此时立即涂抹稀氨水或碳酸氢钠溶液,则可以减轻疼痛D.苯酚皂溶液可用于环境消毒,医用酒精可用于皮肤消毒,其原因均在于可使蛋白质变性凝固6.我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10-9 m)恢复了磁性。
高中化学知识点总结物质的组成性质和分类

高中化学知识点总结物质的组成性质和分类高中化学知识点总结:物质的组成、性质和分类化学作为一门自然科学,研究物质的组成、性质和变化规律。
在高中化学的学习过程中,我们积累了许多关于物质的基本概念和知识点。
本文将对物质的组成、性质和分类进行总结,希望对化学的学习者有所帮助。
一、物质的组成物质是由不同种类的原子或分子组成的。
原子是构成物质的基本粒子,它由质子、中子和电子组成。
元素是由具有相同原子序数的原子组成的,可以用元素符号表示,如氢(H)、氧(O)等。
化合物是由不同元素的原子按照一定的比例和方式结合而成。
物质的组成还可以根据物质的形态进行分类。
常见的物态有固态、液态和气态。
固态物质具有固定的形状和体积,原子或分子之间的相互作用力较强;液态物质具有固定的体积但可流动,原子或分子之间的相互作用力相对较弱;气态物质具有可压缩性和可流动性,原子或分子之间的相互作用力较弱。
二、物质的性质物质的性质可以分为物理性质和化学性质。
物理性质是物质自身固有的性质,可以通过观察和测量进行判断,而不改变物质的组成。
常见的物理性质有颜色、硬度、密度、熔点和沸点等。
化学性质是物质参与化学反应时表现出来的性质,会导致物质的组成发生变化。
化学性质包括可燃性、氧化性、还原性和酸碱性等。
物质的性质还可以根据其可溶性进行分类。
溶解是指固体、液体或气体溶质与溶剂之间的混合过程。
可溶性是指物质在一定条件下能否溶解于某种溶剂中。
常见的可溶性规律包括“相似相溶原则”和“亲水性和疏水性原则”。
三、物质的分类根据物质的组成和化学性质,可以将物质分为元素和化合物。
元素是由相同原子组成的物质,可以根据其在元素周期表中的位置进行分类,如金属元素、非金属元素和半金属元素等。
化合物是由不同元素的原子组成的物质,可以根据其化学式和结构进行分类,如无机化合物和有机化合物。
根据物质的物理性质和可溶性,可以将物质分为溶液、悬浮液和胶体。
溶液是由溶质溶解于溶剂中而形成的均匀透明的混合物,如盐水、糖水等。
【人教版】高考化学复习指导:《物质的组成、性质和分类化学用语》.docx

物质的组成、性质和分类化学用语【教法指引】复习此专题吋要做到“准确”、“系统”、“灵活”,可以从三点入手:1.以高考的热点、考点、难点为依据,合理设置复习内容和练习题,熟练掌握解题思路、•注重方法、技巧,不求血血俱到,但求在某些考点的深度和广度的挖掘上有所突破。
2.加强区别相似概念的异同,理顺不同概念间的联系,进而形成连贯的知识系统。
3.必须将化学知识总结归纳成规律,并运用规律解决实际问题。
【知识网络】一、物质的组成1.物质的组成关系定义离了带电的原了或原了团基团化学屮对原了团和基的总称2.4.离子与基团区别 带有正电荷或负电荷 不带电,为缺电子物质,呈电中性联系两者通过得失电子可以互相转化实例 OH' N0~ Cl~ CH 3+・°H-N02 -Cl -CH 34. 同素异形体与同位素、同系物、同分异构体的区别:二、物质的分类按化学键分—离子化合物——共价化合物I —金I —非金雇(含稀有气体)无机化合物的分类1.按组成性质分类:按组成成分分混合物化合物按水濬液或 濬液导电性分按有无碳元素分纯浄物按元素电解质非电解质 按电离强电解质程度分 弱电解质无机化合物 有机化合物TSARUK Zf)如 NaziL 寸画列US (S) in Ml2. 按微粒间成键种类分类3. 按能否电离来分类4. 胶体的分类:分散剂是液体——液溶胶。
如A1(OH )3胶体,蛋口质胶体Sfsta如阿CO. HDaHI 无机化合恂KltBt agRJHbd »TO> HM Q D4 还原性酸如HL liS发it如阳PQ. IfaSCJt----------- ► UB 獰发廉抑限Her 帘H4Q3T IkEttW 9U 3 haSUfe tfeFU l 不St 走性SB 迹 田* HI, US. FtSOw血性 r 可涪性・E 如KfaOH, N%・⑷----- ►[ 躍眸嫌如他0匕)2・ 心吨3aU ft EOH @3tt ir m ・ z厂正盐Hbt& Y IK 式空Xj 络fi n 如 如 如 如住SCU KHSCUCnXOHhCOa ECAXSO^h* :2%O b^3AlFrt 化合物分为共价化合物如C02, SiCh 和离了化合物如NaCX NH4CI化合物「电解质-I 非电解质电离程度厂强电解质1弱电解质如 HCOi 如HC1电團吕—元K ft HN» #-in» tfl 旧0・HQ I Q I劳廉如Hu. i^sa SSL tLFbS. CHCO3H捱sat电(1)按分散剂的状态分 分散剂是气体——气溶胶。
人教版高中化学高考总复习 第1讲 物质的组成、性质和分类

第1讲物质的组成、性质和分类复习目标1.了解分子、原子、离子和原子团等概念的含义;2.理解物理变化与化学变化的区别与联系;3.理解混合物和纯净物、单质和化合物、金属和非金属的概念;4.理解酸、碱、盐、氧化物的概念及其相互联系;5.了解胶体是一种常见的分散系,了解溶液和胶体的区别。
考点一物质的组成与分类必备知识梳理·夯实学科基础一、物质的组成1.物质的微观组成(物质是由微观粒子构成的)2.物质的宏观组成(物质是由元素组成的)(1)元素:具有相同________的一类原子的总称(2)元素的存在形态①游离态:元素以________形式存在的状态。
②化合态:元素以________形式存在的状态。
(3)同素异形体定义:同一种元素形成的____________形成方式:①原子个数不同;②原子排列方式不同性质差异:物理性质________;化学性质________ 相互转化:属于________变化(4)元素与物质的关系元素组成→{单质:__________________的纯净物化合物:________________的纯净物(5)纯净物和混合物①纯净物:由同种______或______组成的物质。
②混合物:由几种不同的______或______组成的物质。
③纯净物和混合物的区别微元素、物质及微粒间的关系二、物质的分类1.简单分类法概述(1)分类是学习和研究化学物质及其变化的一种常用科学方法。
(2)分类应依据事先设定的“标准”进行,“标准”不同,分类方法也不相同。
2.分类方法(1)交叉分类法同时用多个标准对同一物质进行分类。
如:(2)树状分类法——每次用一个标准对物质进行再分类。
①树状分类法②几类物质概念辨析③树状分类法在无机化合物分类中的应用无机化合物特别提醒有关氧化物中的“一定”和“不一定”(1)酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸或碱,如SiO2、Fe2O3。
(2)能与酸反应生成盐和水的氧化物不一定是碱性氧化物,如Al2O3。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
教师下载中心
教学建议
化学基本概念是化学的根本,也是研究化学的出发点,它既是解释各种化学现象的基础,也是我们解决有关化学问题进行思考和分析研究的工具,更是创造性思维的基点。
高考中对基本概念的考查是通过设置一些化学情景进行的,有些知识点本身不好理解,易疏忽或混淆,如果在情景中再和其他化学知识交叉糅合,要求就很高。
要在高考中做好这些题目,平时就要对各种概念经常进行有针对性的辨析,在大脑中形成知识网络,到时才能调用自如,思维才能深刻、敏捷和准确。
物质的组成、性质、分类和变化涉及概念较多,许多概念之间极易混淆。
在复习过程中,要注意掌握有关概念之间的相互联系,形成完整、系统的概念知识网络,要抓住概念的实质进行比较,找出有关概念之间的细微差别,避免概念混淆。
如物理变化和化学变化的区别是有无新物质生成,其本质是有无化学键的断裂;酸性氧化物的通性是与碱反应生成盐和水,而不是跟水反应生成相应的酸(二氧化硅和水不能发生反应);同素异形体与同分异构体的异同点等。
在解答考查基本概念的选择题时,要正确理解题干的要求,注意选项间的比较,不失时机地进行排除,凭借已知推断未知,得出正确答案。
拓展题例
1.物质分类
【例1】上海环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。
其中塑料袋、废纸、旧橡胶制品等属于( )
A.无机物
B.有机物
C.盐类
D.非金属单质
解析:本题结合现实生活,考查物质分类的知识,同时也渗透着环保的意识。
要求我们从化学角度,知道有机物与无机物的组成和区别,并加以判别,并能把日常生活中的物质处理与所学化学知识结合起来。
垃圾一般分为工业垃圾、建筑垃圾、生活垃圾等几大类,其中相当一部分属于有机物,如厨房废弃物、塑料袋、废纸(报纸、杂志、纸箱等)、旧橡胶、旧泡沫塑料、旧衣料等等,故选B。
答案:B
【例2】中央电视台《科技博览》报道,2004年3月中科院首创用CO2合成可降解塑料——聚二氧化碳。
下列相关说法合理的是( )
A.二氧化碳塑料是通过聚合反应得到的
B.二氧化碳塑料与干冰互为同素异形体
C.二氧化碳塑料与干冰都是纯净物
D.使用二氧化碳塑料会产生白色污染
解析:本题从二氧化碳的聚合物出发,考查我们对同素异形体、纯净物、混合物等高考要求的内容的了解,同时使学生在了解化学知识的同时,又能开阔视野。
预计这种结合新物质进行物质分类考查的选择题出现的几率较高。
解此类题目要理清物质的组成、结构、性质之间的关系,对照概念进行判断,不要混淆相似或相近概念,更不要被原来熟悉的物质所影响。
塑料是高分子化合物,由小分子形成高分子必须通过聚合反应,A项正确。
同素异形体是对同一元素的不同单质而言,而二氧化碳塑料与干冰都是化合物,B项错误。
高分子化合物有一定的聚合度,二氧化碳的聚合度有一定范围,所以干冰是纯净物,二氧化碳塑料是混合物,C项错误。
题干中已说明二氧化碳塑料可降解,故该塑料不会造成白色污染,D项不正确。
答案:A
【例3】物质分类的依据通常有组成和性质,下列物质分类中,只考虑组成的是( )
A.Na2SO4是钠盐、硫酸盐、正盐
B.HNO3是一元酸、强酸、挥发性酸
C.Mg(OH)2是二元碱、难溶性碱、中强碱
D.Al2O3是两性氧化物、金属氧化物、最高价氧化物
解析:具有相同组成的物质在某些性质上具有相似性,具有相同的某一性质的不同物质,其组成不一定相同,从掌握组成、性质等方面对单质、酸、碱、盐、氧化物进行分类,可加深对物质性质的理解,这种类型是以前高考命题中没有出现过的,是今后高考中值得注意的一
个问题。
Na2SO4中含Na+,它是钠盐;含-2
4
SO,它是硫酸盐;电离出的阳离子只有Na+,
阴离子只有-2
4
SO,没有其他的阴、阳离子,故它属正盐。
从组成看,1个HNO3分子只电
离出1个H+,故它是一元酸;HNO3在溶液中完全电离成H+和-
3
NO,故它是强酸;HNO3容易挥发,故它是挥发性酸。
强酸性和挥发性反映了HNO3的性质。
Mg(OH)2是二元碱是从组成看的,说明1 mol Mg(OH)2能电离出2 mol OH-,而难溶性碱、中强碱是它们的性质。
Al2O3是两性氧化物,说明它既能与OH-反应,又能与H+反应,是从性质方面来分类的;它是金属氧化物、最高价氧化物,是从组成方面分类的。
答案:A
2.化学方程式的书写
【例4】(2006重庆理综,8)能正确表示下列反应的化学方程式是( )
A.黄铁矿煅烧:2FeS2+5O2高温2FeO+4SO2
B.石英与石灰石共熔:SiO2+CaO高温CaSiO2
C.氨的催化氧化:4NH3+5O2催化剂
△
4NO+6H2O
D.氯气与石灰乳反应:2Cl2+2Ca(OH)2====CaCl2+CaClO2+2H2O
解析:本题以正误判断的形式考查化学方程式的书写。
一个正确的化学方程式一般满足下列条件:①符合化学反应实际,反应物、生成物的化学式表达正确;②遵守质量守恒定律,是氧化还原反应的还要遵守电子得失守恒;③注明必须的反应条件、沉淀及气体符号。
A选项中产物应为Fe2O3和SO2;B中石灰石的化学式应为CaCO3,B不正确;D中产物应为CaCl2、Ca(ClO)2和H2O,D不正确,本题答案为C。
答案:C
3.化学用语
【例5】下列化学用语中,书写错误的是( )
A.硫离子的结构示意图:
B.氟化钠的电子式:
C.甲基的电子式:
D.次氯酸的结构:H—Cl—O
解析:本题从几种典型粒子的结构示意图、电子式、结构式等角度考查学生对这些基础知识的掌握情况。
近几年来高考中对电子式、结构示意图、结构简式考查的重现率较高,体现了
高考重视基础的命题宗旨,预计此类题目还会以适当的粒子为素材出现在高考题中。
硫原子有16个电子,分三层排布,最外层6个电子,而硫离子比硫原子多2个电子,最外层有8个电子,A项正确;氟化钠由钠离子和氟离子构成,钠离子的电子式为Na+,氟离子的电子
式为,B项正确;甲基是1个碳原子与3个氢原子以单键形成的基团,其中碳
原子最外层有7个电子,而不是8个电子,C项错误;次氯酸中氯为+1价,氧为-2价,因此,次氯酸的结构式应为H—O—Cl,D项错误。
答案:CD。
