R2A medium
常用培养基配方范文

常用培养基配方范文培养基(Culture medium)是一种用于细菌、真菌、植物细胞、动物细胞和其他微生物的繁殖和生长的营养物质。
常用的培养基可分为发酵培养基、微生物培养基和细胞培养基。
下面列举了一些常用的培养基配方。
1. LB培养基(Luria-Bertani medium)成分:-牛肉提取物:10克-酵母提取物:5克-热可溶性淀粉:10克-氯化钠:10克-水:1升2. NB培养基(Nutrient broth)成分:-牛肉提取物或肉蔻精:8克-酵母提取物:4克-葡萄糖:4克-水:1升3. MacConkey培养基成分:-水解动物蛋白:17克-中和胆盐:1.5克-中性红:0.03克-水:1升4. TSB培养基(Tryptic soy broth)成分:-大豆胨:17克-酵母提取物:3克-水:1升5. BHIA培养基(Brain Heart Infusion Agar)成分:-脑心汤固体:37克-水:1升6.R2A培养基成分:-水解酵母提取物:0.5克-蛋白胨:0.5克-葡萄糖:0.5克-脱脂乳粉:0.5克-黄豆粉:0.5克-高氯酸钠:0.3克-多聚体1466:0.05克-水:1000毫升7.比尔斯氏培养基(BHI培养基)成分:-大豆胨:37克-脑心汤固体:2克-水:1升8. 培养基199(Medium 199)成分:-高锰酸钾:0.015克-硫酸:1.55克-磷酸一氢钠:0.184克-高氯酸钠:8.0克-溴酚蓝:0.4克-d-葡萄糖:5.55克-l-谷氨酸:40.525克-苏打粉:0.84克-水:1升9. DMEM培养基(Dulbecco's Modified Eagle's Medium)成分:-苔藓胶原酸:1克-乳糖:1克- 谷氨酸:584mg- 水:1000ml这只是一小部分常见的培养基配方,实际上有很多种不同的培养基,它们根据不同的生物特性和培养需求来设计。
不同的培养基可以提供细菌、真菌、细胞等微生物生长需要的各种营养物质。
饮用水中2-甲基异莰醇降解菌的筛选和生物降解能力初探

饮用水中2-甲基异莰醇降解菌的筛选和生物降解能力初探王方睿;陈克云;赵宇;曹楠;郭庆园;于建伟【摘要】嗅味是饮用水中普遍关注的关键指标之一,其中2-甲基异莰醇(2-MIB)和土臭素(geosmin)导致的土霉味问题最为常见.以2-MIB为目标,探讨从水厂生物活性炭滤池中分离特定降解菌的可行性,并对2-MIB的降解效果进行评估.结果表明,试验筛选得到了三株对2-MIB具有降解能力的降解菌,经16S rRNA系统进化分析,分别为假单胞菌,鞘氨醇单胞菌以及金黄杆菌;初步的降解能力评价表明,三种降解菌对2-MIB的降解效果类似,且均表现出相对较高的降解能力,接种后不经延滞即开始2-MIB的降解;试验期内对2-MIB的降解率可达94%以上,最终可将初始浓度为200 ng/L的2-MIB降解至阈值浓度以下.后续将对于不同环境条件以及实际连续流操作条件下的降解效果和运行方式进行进一步的评价,探讨其用于实际工艺中强化生物降解2-MIB的可行性.【期刊名称】《净水技术》【年(卷),期】2018(037)0z2【总页数】4页(P1-4)【关键词】嗅味;2-甲基异莰醇;降解菌;降解效果【作者】王方睿;陈克云;赵宇;曹楠;郭庆园;于建伟【作者单位】人大附中朝阳分校,北京100028;中国科学院生态环境研究中心,北京100085;中国科学院生态环境研究中心,北京100085;北京市自来水集团,北京100031;北京市自来水集团,北京100031;中国科学院生态环境研究中心,北京100085;盐城工学院,江苏盐城224051;中国科学院生态环境研究中心,北京100085【正文语种】中文【中图分类】TU991.2嗅味是饮用水中普遍关注的关键指标之一。
水源水中藻类等微生物的过度增殖是季节性嗅味问题发生的主要原因之一,其中2-甲基异莰醇(2-MIB)和土臭素(geosmin)导致的土霉味问题最为常见[1-3]。
对此类嗅味物质,自来水厂的混凝沉淀过滤等常规工艺去除效果有限,一旦水源水中发生此类嗅味问题,多采用粉末活性炭(PAC)投加的方式加以应急处理。
饮用水中几种细菌计数方法的比较

ႂႨඣᇏࠫᇕ༥ऩ࠹ඔٚم֥бࢠ鲁巍,王云,张晓健(清华大学环境科学与工程系,北京 100084)ᅋေ:比较采用不同培养基的平板计数(Plate Counts ,PC )方法,以及不同荧光染色剂的显微镜直接计数方法与常规计数方法的差别.研究认为,常规平板计数方法并不能准确反映饮用水中实际存活的细菌数量;吖啶橙直接计数(Acridine Orange DirectCounts ,AODC )的结果最高,较常规平板计数方法高出3~4个量级;活细菌直接计数(Direct Viable Counts ,DVC )中,DVC 2N.A.、DVC 2CTC 和DVC 2BacLight 等计数方法的结果较常规平板计数结果高出2~3个量级.以地表水为水源的水厂出水中活细菌数占总细菌数的比例在10%左右.ܱՍ:饮用水;直接计数;平板计数;活细菌直接计数;细菌ᇏٳোݼ:X832;TU991125 ໓ངѓ്:A ໓ᅣщݼ:025023301(2004)0420167203൬۠ರ௹:2003208207;ྩרರ௹:2003209225ࠎࣁཛଢ:国家自然科学基金资助项目(50238020);国家高技术研究发展计划(863计划)资助项目(2002AA601140)ቔᆀࡥࢺ:鲁巍(1978~),男,博士研究生,主要从事水污染防治技术研究.Methods of Enumeration of B acteria in Drinking W aterL U Wei ,WAN G Yun ,ZHAN G Xiao 2jian(Department of Environmental Science and Engineering ,Tsinghua University ,Beijing 100084,China )Abstract :Methods of the enumeration of total bacteria and Coliform in drinking water were researched in this paper.The differences between heterotrophic plate count and direct viable count method were compared.It is concluded that the total number of bacteria in R2A medium is one order of quantity higher than the traditional plate count agar ,and the results of acridine orange direct counts (AODC )is the highest.S ome different staining methods in direct viable count were also compared in this paper ,such as nalidixic acid ,CTC staining and BacLight staining.The proportion of the live bacteria to the dead is about 10%.K ey w ords :drinking water ;enumeration ;PC ;DVC ;bacteria 在饮用水处理中,出厂水加氯消毒后进入管网,部分存活的微生物和管网中生物膜中的微生物会利用管网水中的微量可生物降解有机物进行再生长,引起所谓的生物稳定性问题[1].长期以来,国内多采用异养菌平板计数法(Heterotrophic Plate Counts ,HPC )和最大或然数法(Most Probable Number ,MPN )来测定饮用水中的活菌数.但由于饮用水中的贫营养环境有别于传统培养基提供的富营养环境,大多数在显微镜下观察到的细菌不能在传统培养基中生长(Nonculturable ),致使活菌计数结果偏低.近些年来,国外先后应用吖啶橙染色直接计数(Acridine Orange Direct Counts ,AODC )、活菌直接计数(Direct Viable Counts ,DVC )等方法对饮用水中的细菌总数及活菌数进行快速、直接的镜检计数.一些新的染色方法,如采用52氰基22,32联甲苯四唑盐酸盐(52Cyano 22,32ditolyltetrazolium chloride ,CTC )、核酸探针(BacLight )等对活细菌计数,都取得了很好地效果.国内这方面的研究却未见报道.本文应用AO 、CTC 、BacLight 等试剂染色,采用显微镜直接计数对饮用水中的细菌数量进行测定,并与常规平板计数方法所得结果进行了比较与讨论.1൫ဒҋਘބٚم111 水样的采集本试验所用水样分别取自实验室自来水和北方某市管网水.水样均采用无菌磨口玻璃瓶采集.实验室自来水未经特殊处理直接测定.现场水样采集后立即放入冷却箱中保存,4h 内测定.消毒试验所用水样为实验室自配水.112 细菌计数11211 总细菌计数(1)AODC 法[2] 水样采集后迅速加入甲醛固定,甲醛最终浓度2%;取10mL 固定后水样加入015mL 012%吖啶橙(Acridine Orange ,Sigma 公司)染色1~2min ;将染色水样经滤膜(孔径012μm ,直径25mm ,黑色聚碳酸脂滤膜,Nuclepore 公司)过滤;过滤后将滤膜置于载玻片上,用落射荧光显微镜(日本Nikon ,EF 2D 型)计数视野中发橙色或绿色荧光的菌体;显微镜光源为200W 汞灯,激发光滤光片第25卷第4期2004年7月环 境 科 学ENV IRONM EN TAL SCIENCEVol.25,No.4J uly ,20041༥ऩ࠹ඔࢲݔFig.1 The results of bacteria enumeration为450~490nm ,光束分离滤光片510nm ,阻挡滤光片520nm.(2)BacLight 染色直接计数法 将试剂按照产品要求配制后,取2mL 固定后水样加入60μL 所配BacLight 染色试剂,避光培养15~20min ;然后按照AODC 处理方法制片,观察计数视野中发红色或绿色荧光的菌体.所用滤光片波段同AODC 相同.11212 活细菌计数(1)DVC 法 方法①(DVC 2N.A.):向水样中加入01002%萘啶酮酸(N.A.,Nalidixic Acid ,Fluka 公司)和01025%酵母膏(均为最终浓度),避光,25℃培养6h ,然后2%甲醛固定,再按照AODC 法直接镜检计数.视野中长大或变粗的菌体被认为是活菌;方法②(DVC 2CTC ):将012mL 1167%的CTC 加入10mL 水样中(CTC 最终浓度1mmol/L ),避光室温培养4h ,然后2%甲醛固定,再按照AODC 法直接镜检计数视野中的红色菌体;方法③(DVC 2BacLight ):参见11211,只镜检计数视野中发绿色荧光的菌体.(2)HPC 法 采用传统营养琼脂培养基和R2A 培养基进行平板计数,详见相关检验手册[3].R2A 培养基基本组成为:酵母浸膏015g ,蛋白胨015g ,酸水解干酪素015g ,葡萄糖015g ,可溶性淀粉015g ,丙酮酸钠013g ,K 2HPO 4013g ,MgSO 4・7H 2O 0105g ,琼脂15g ,溶于1L 水.11213 总大肠菌群计数消毒试验考察消毒剂的灭菌效果,配水中投加的大肠杆菌菌液为实验室自培养.(1)滤膜法 常规检测方法,详见检验手册[3].(2)荧光显微计数 参见11211,11212.2൫ဒࢲݔაษં211 细菌计数方法比较应用AODC 、DVC 及HPC 等方法对实验室自来水及城市管网水中细菌总数及活菌数计数的结果见图1,表1中计算了活菌数占总细菌数的比例.і1ࠃऩඔᅝሹ༥ऩඔ֥б২/%Table 1 Proportion of the live bacteria to the total/%样品计数方法N.A./AODCCTC/AODC Bac 2live/AODC HPC/AODC营养琼脂R2A 实验室自来水13191717251701094111某水厂出水6119181217未检出01068管网水818101512140100770112管网末梢水7191113915010100112 由图1可以看出,AODC 和BacLight 2种方法得出的总细菌数无显著性差异.北方某市各点水样中细菌总数在105个/mL 量级,活菌数在104个/mL 量级.实验室自来水中细菌总数在104个/mL量级,活菌数在103个/mL 量级.以营养琼脂作为培养基的平板计数只有几十个CFU/mL ,以R2A 作为培养基的平板计数也只达到102个/mL 量级.实验室自来水是高校自供水,水源为地下水,所调查水厂的水源为地表水,水源水质差异可能是引起细菌数差异的因素之一.由表1看出,实验室自来水中活菌数所占比例在10%~25%之间,而以地表水为水源的水厂出水中活菌数所占比例基本在10%左右.活菌计数中计数结果大小顺序为:BacLight >CTC >N.A.>R2A >营养琼脂.R2A 培养基是一种贫营养培养基,其提供的培养条件更接近饮用水中的贫营养环境,因此其结果较常规营养琼脂培养基高.但是由于自然环境中大多数微生物是不可培养的(Nonculturable ),所以DVC 结果又远高于平板计数结果.萘啶酮酸可以抑制细菌DNA 的复制,但不影响细胞中其它合成途径的继续运转,在一定浓度营养物存在下,菌体伸长、变大(如图2所示).但是由于部分格兰氏阳性及格兰氏阴性菌对萘啶酮酸有抗性,低浓度的NA 不能抑制它们的繁殖,致使计数结果出现偏差[4].BacLight 是近年来由分子探针公司研制出的新型荧光染色剂,由SYTO9和碘化丙锭(propidium iodide )2种核酸探针组成.SYTO9能将所有细菌染色,发绿色荧光,而碘化丙锭能穿透细胞膜受损细胞,发红色荧光(如图2所示)[5].由于碘化丙锭只能穿透受损细胞,因此部分细胞膜完好但实际不能存活的部分细菌未能被染色,这就导致了BacLight 的活菌计数结果高于CTC 、NA 的计数结果.应用CTC 进行活菌计数时,由于细菌的呼吸作用,CTC 被还原成CTF (CTC Formazan ),其在荧光显微镜下发红色荧光(如图2所示)[6],从理论上看,CTC 方法的基本原理是利用活细胞的呼吸作用,因此能够比较准确地反映活细菌的数量,而且该方法的试验费用相对较低,适合实验室研究使用.212 消毒试验大肠杆菌计数2ࠃऩ࠹ඔم႐ܻಙཞ(ᅶோनູՂऩအު෮ജ,٢նПඔູ࣍රᆴ,ࣇ܂ҕॉ)Fig.2 The images of fluorescent staining methods 实验室通过配水试验,考察一定浓度余氯对大肠菌群的灭活效果,大肠菌群计数方法采用常规膜滤法和DVC 方法.当初始加氯量015mg/L 时,存活细菌数与时间的关系如图3所示.3թࠃ༥ऩඔაൈࡗ֥ܱ༢Fig.3 The relationship of time and the number of the live bacteria从图3中可以看出,AODC 计数结果基本不随时间变化,始终停留在初始量级105.N.A.,CTC ,BacLight 3种药剂的DVC 计数结果基本相同,从105逐渐下降到103.传统的膜滤法平板计数结果同样都随着时间的推移而逐渐减少,但是计数结果与DVC 方法存在显著的差异,这说明常规计数方法并不能准确反映水体中微生物的存活状况.3ࢲં (1)显微镜直接计数的结果远远高于常规平板计数,更能准确反映饮用水中的微生物数量.(2)活菌计数中计数结果大小顺序为:DVC 2BacLight >DVC 2CTC >DVC 2N.A.>R2A >营养琼脂.其中CTC 方法能够比较准确地反映活细菌的数量,而且该方法的试验费用相对较低,适合实验室研究使用.(3)在考察消毒剂对细菌的灭活效果时,直接计数可以更准确地反映细菌存活的状况.ҕॉ໓ང:[1] 王占生,等.微污染水源饮用水处理[M ].北京:中国建筑工业出版社,1999.236~243.[2] Hobbie J E ,et e of nuclepore filters for counting bacteriaby fluorescence microscopy [J ].Appli.Environ.Micriobiol.,1976,33(5):1225~1228.[3] 俞毓馨,等.环境工程微生物检验手册[M ].北京:中国环境科学出版社,1990.136~144.[4] Kazuhiro K ogure ,et al .An improved direct viable countmethod for aquatic bacteria[J ].Arch.Hydrobiol.,1984,102:117~122.[5] Lina Boulos ,et al.L IVE/DEAD BacLight TM :application of a new rapid staining method for direct enumeration of viable and total bacteria in drinking water [J ].J.Microbiological Methods.,1999,37:77~86.[6] Rodriguez G G ,et e of a fluorescent redox probe fordirect visualization of actively respiring bacteria.Appli.Environ.Micriobiol.,1992,58(6):1801~1808.。
R2A琼脂培养基即用型平板说明书

R2A琼脂培养基即用型平板说明书【产品名称】通用名称:R2A琼脂英文名称:R2A Agar【型号规格】Φ90mm,10皿/包。
【预期用途】用于纯化水中菌落总数的测定。
【检验原理】蛋白胨、酵母浸出粉、酪蛋白水解物提供氮源及生长因子;葡萄糖、可溶性淀粉提供碳源亦可吸收细菌代谢过程中产生的废物;丙酮酸钠有利细菌生长;磷酸盐是pH稳定剂;琼脂是凝固剂。
【组成成份】由蛋白胨、酵母浸出粉、酪蛋白水解物、葡萄糖、可溶性淀粉、丙酮酸钠、磷酸盐和琼脂等组成。
【使用方法】样本按药典标准规定进行前处理后接种于培养基,30~35℃培养18~24h 后,观察结果。
【检验结果】枯草芽孢杆菌、铜绿假单胞菌生长良好。
【注意事项】1.该培养基仅用于科研研究。
2.采集的标本必须尽快接种培养,以保证结果准确。
3.所用标本及其培养废弃物应视为有潜在传染性的物质,应按传染病实验室操作规范处理。
【贮存条件】2~25℃,避光保存。
【有效期】有效期6个月。
【参考文献】1.中国药典2020年版2.SN/T1538.1-2005培养基制备指南第1部分:实验室培养基制备质量保证通则3.SN/T1538.2-2007培养基制备指南第2部分:培养基性能测试实用指南4.WS/T232-2002商业性微生物培养基质量检验规程5.GB4789.28-2013食品安全国家标准食品微生物学检验培养基和试剂的质量要求【基本信息】生产企业名称:上海申启生物科技有限公司住所:上海市普陀区绥德路118弄60号4层、56号2层联系方式:电话:************************传真:************生产地址:上海市普陀区绥德路118弄62号4层邮编:200331网址:/。
培养基配方

培养基配方一、R2A/R3A培养基配方(g/L):R2A R3A酵母粉 0.5 g 1.0 g胰蛋白胨 0.5 g 1.0 g酪蛋白氨基酸(casamino acid)0.5 g 1.0 g葡萄糖0.5 g 1.0 g可溶性淀粉0.5 g 1.0 g磷酸氢二钾0.3 g 0.6 g七水硫酸镁0.05 g 0.1g丙酮酸钠 0.3 g 0.5g琼脂15.0 g 15.0 g用磷酸氢二钾或磷酸二氢钾调pH到7.2后,加1L蒸馏水,搅拌溶解,121℃灭菌15min。
特点:R2A培养基主要用于水的菌落计数,它可以修复被氯气损伤的细菌,支持耐受氯气的微生物的生长。
培养要求,低温(20-30℃)长时间培养(5-7天)这样得到的菌落数比常规菌落总数检测的菌落数更符合实际。
R3A培养基主要用于菌株的生化特征描述和鉴定。
参考文献:Reasoner DJ, Geldreich EE. A new medium for the enumeration and subculture of bacteria from potable water. Appl Environ Microbiol. 1985,49(1):1-7.二、VL55培养基(Sait M et al,2002)(土壤筛菌)配方(g/L)1×2×2-(N-吗啉基)乙磺酸 1.95 g 3.9 gMgSO4 0.024 g(0.2mM)0.048 g(0.4mM)CaCl20.033294 g(0.3mM)0.066588 g(0.6mM)(NH4)2HPO40.026421 g(0.2mM)0.052824 g(0.4mM)亚硒酸盐/钨酸盐溶液1mL 2mL微量溶液SL10 1mL 2mL用0.2mol/L的NaOH和0.1mol/L的KOH混合液调pH到5.5(这与土壤的pH一致)Sait M等取2×的培养基121℃灭菌15min后,冷却至56℃,加入10mL5%(w/v)的木聚糖溶液,2mL的维生素溶液1,6mL的维生素溶液2。
常用25种培养基详细配方

常用25种培养基详细配方以下是常用的25种培养基的详细配方:1. LB培养基(Luria-Bertani medium)-天然培养基:10g蛋白胨,5g酵母粉,10gNaCl,添加适量蒸馏水,pH值调至7.0。
- 固体培养基:添加15g agar。
2. TSA培养基(Tryptic Soy Agar)-17g蛋白胨,3g酵母提取物,5gNaCl,添加适量蒸馏水,pH值调至7.3-7.5- 固体培养基:添加15g agar。
3. NB培养基(Nutrient Broth)-8g蛋白胨,2g胰蛋白胨,5gNaCl,添加适量蒸馏水,pH值调至7.4 - 固体培养基:不添加agar。
4. R2A培养基(Reasoner's 2A medium)- 0.5g peptone,0.5g casein hydrolysate,0.5g yeast extract,0.5g glucose,0.5g soluble starch,0.3g dipotassium phosphate,0.05g magnesium sulfate,0.3g sodium pyruvate,10μg m anganese sulfate,添加适量蒸馏水,pH值调至7.2-7.4- 固体培养基:添加15g agar。
5. BHIS培养基(Brain Heart Infusion with 20% Sucrose)- 37.5g BHIS培养基,10g sucrose,添加适量蒸馏水,pH值调至7.5- 固体培养基:添加15g agar。
6. PDA培养基(Potato Dextrose Agar)-200g马铃薯,20g葡萄糖,添加适量蒸馏水,pH值调至5.6- 固体培养基:添加20g agar。
7. MRS培养基(de Man Rogosa Sharpe medium)- 10g peptone,10g beef extract,4g yeast extract,20g glucose,5g sodium acetate,2g dipotassium phosphate,0.02g magnesium sulfate,添加适量蒸馏水,pH值调至6.2-6.6- 固体培养基:添加20g agar。
中、美、英、欧药典制药用水微生物检查法对比研究

中、美、英、欧药典制药用水微生物检查法对比研究杨晓莉;李辉;绳金房【摘要】Objective In order to provide a reference for the revision of Chinese Pharmacopoeia (Ch .P .) and offer a rational propos-al to promote the microbiological test of pharmaceutical water .Method Different media and cultural conditions were used to detect samples 20 pharmaceutical water .The difference among different methods was inspected and statistically analyzed by a paired t-test .Result The results exhibited that using R2A medium ,30-35 ℃ ,120 h ,membrane filtra tion method to examine the microbi-ological of pharmaceutical water was better than other methods .Meanwhile ,the method recorded in Ch .P of 2010 was reasona-ble .Conclusion Using R2A medium ,30-35 ℃ ,120 h ,and membrane filtration method is workable for microbial limit tests .%目的比较中、美、英、欧药典制药用水微生物检查法,为《中国药典》的修订提供参考,为推动制药用水微生物检查法与国际接轨提供合理化建议。
r2a胶管参数

r2a胶管参数
1. 材质:
r2a胶管通常由合成橡胶或热塑性弹性体制成,能够承受高压和高温,耐腐蚀性也很好。
2.尺寸规格:
内径范围从1/8英寸到2英寸不等,壁厚可选择标准或加强型。
长度可根据需求定制。
3.工作温度范围:
-40°F(-40°C)至302°F(150°C)
4.工作压力范围:
体现在爆破压力值上,通常为400-6000psi。
5.耐化学腐蚀性:
对大多数酸、碱、溶剂以及海水等具有良好的耐腐蚀性能。
6.柔韧性:
优异的柔韧性使其能够适应扭曲环境和较小的弯曲半径。
7. 防静电性:
部分型号添加了导电剂,具备一定的防静电能力。
8. 标识:
管身上通常印有尺寸、工作压力、材质等重要参数。
9. 接头选择:
可选配多种标准接头,如卡套接头、大折弯接头等。
r2a胶管在柔性、耐压、耐温和耐腐蚀等方面表现出色,广泛应用于工业、化工、航空等领域。
R2A琼脂培养基适用性检查方案

R2A琼脂培养基适用性检查方案清晨的阳光透过窗帘,洒在了我的书桌上,一股莫名的动力涌上心头。
十年的方案写作经验告诉我,此刻正是沉浸在创意的海洋中,挥洒文字的最佳时刻。
那么,就让我们来谈谈R2A琼脂培养基适用性检查方案吧。
一、方案背景近年来,微生物实验室在科研和生产中的应用越来越广泛,培养基作为微生物生长繁殖的基础物质,其质量直接关系到实验结果的准确性。
R2A琼脂培养基作为一种常用的培养基,其适用性检查显得尤为重要。
二、方案目标1.评估R2A琼脂培养基的质量,确保其适用于微生物实验室的各项实验。
2.为实验室人员提供一套完整的R2A琼脂培养基适用性检查方案。
三、方案内容1.培养基的外观检查我们要对R2A琼脂培养基的外观进行检查。
观察其颜色、透明度、有无杂质等。
合格的R2A琼脂培养基应为淡黄色,透明度好,无杂质。
2.培养基的溶解性检查将R2A琼脂培养基加入蒸馏水中,观察其溶解性。
合格的R2A琼脂培养基应在短时间内完全溶解,无沉淀。
3.培养基的PH值检查使用PH计对R2A琼脂培养基的PH值进行测定。
合格的R2A琼脂培养基的PH值应在6.8-7.2之间。
4.培养基的微生物生长情况检查将R2A琼脂培养基接种到已知微生物菌种中,观察其在培养基上的生长情况。
合格的R2A琼脂培养基应能支持目标微生物的生长。
5.培养基的稳定性检查将R2A琼脂培养基在室温下放置一定时间,观察其是否发生变质。
合格的R2A琼脂培养基应在一定时间内保持稳定,不发生变质。
6.培养基的保存期检查对R2A琼脂培养基的保存期进行测定,确保其在有效期内使用。
合格的R2A琼脂培养基的保存期一般不应低于6个月。
四、方案实施1.准备实验材料实验所需材料包括:R2A琼脂培养基、蒸馏水、PH计、微生物菌种、培养皿等。
2.实施检查按照方案内容逐项进行检查,详细记录实验数据。
3.数据分析对实验数据进行分析,评估R2A琼脂培养基的适用性。
4.结果报告将实验结果整理成报告,提交给实验室负责人。
r2a培养基的配置方法

r2a培养基的配置方法R2A培养基是一种广泛应用的微生物培养基,用于检测和鉴定多种微生物。
它具有良好的培养和活性性能,对于留性要求较严格的实验,也是理想的选择。
本文将从R2A培养基构成,配置步骤,应用领域等方面介绍R2A培养基的配置方法。
一、R2A培养基的构成R2A培养基是由多种成分组成的,其中主要有碳源,氮源,矿物质,维生素,普通和特殊的增添剂,酸碱度调节剂,发芽因子和抗生素等组分。
在培养基中,氮源常用的有氨基酸,尿素,硝酸盐等;碳源常用的有葡萄糖,淀粉,植物提取液等;矿物质组分常用的有碳酸钠,氯化钾,氯化钠,磷酸钠等。
二、R2A培养基的配置步骤R2A培养基的配置步骤主要分为两个部分,一是溶液的配制,二是培养基的制备。
(1)溶液的配制:首先,将矿物质、氮源、碳源按相应的质量比例混合,充分搅拌,然后加入必要的维生素和抗生素,进行混合;再将其搅拌均匀,在适当的情况下,加入酸碱度调节剂和发芽因子,搅拌均匀。
最后,在室温下加入适当的水,搅拌均匀,即完成了溶液的配制(注意:添加维生素和抗生素时,应按培养基添加量混合溶解)。
(2)培养基的制备:将预先制备好的溶液,放入特殊装置中滤过,以确保培养基液的无菌性。
然后,在温度控制合适的情况下,进行熔融固化操作,固化时加入抗氧化剂,以防止培养基液中的微生物活性,最后再进行静置固化,即可完成R2A培养基的制备。
三、R2A培养基的应用领域R2A培养基由于其优良的性能,可广泛应用于食品安全领域、食品工程、环境科学、生物工程等领域。
其中,在食品安全领域,常用于检测食品中的腐败微生物,如大肠杆菌群,霉菌,酵母菌等。
另外,还可用于菌种鉴定,抗药性研究等;在食品工程中,常用于发酵过程中的微生物定性检测和定量检测;在环境科学领域,常用于太阳能发电场、河流水质、湖泊水质等环境样品的微生物和污染物检测;在生物工程领域,常用于菌株培养、生物反应器研究以及重组蛋白表达等应用。
四、总结R2A培养基是一种广泛应用的微生物培养基,由碳源、氮源、矿物质、维生素、普通和特殊的增添剂、酸碱度调节剂、发芽因子和抗生素等组成,配置步骤主要分为溶液的配制和培养基的制备。
培养基灵敏度检查表
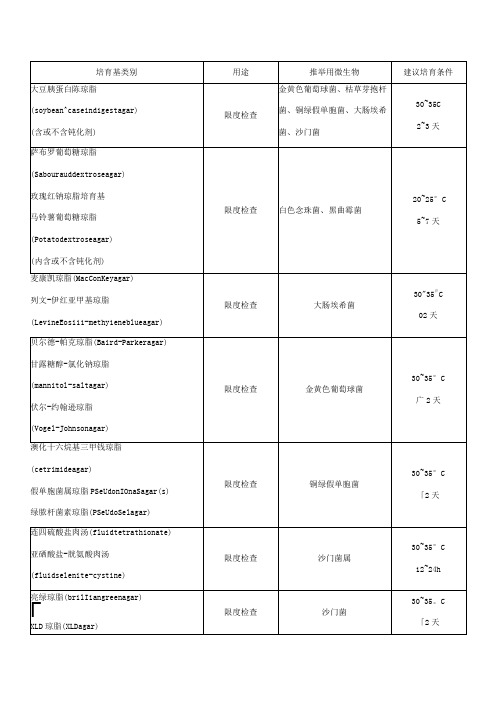
厌氧菌检测
梭状芽花杆菌
35~37。C
2天
大豆胰蛋白陈琼脂
(soybeancaseindigestagar)
生物指示剂
(蒸汽灭菌)
嗜热脂肪芽泡杆菌
55~60C
2天
大豆胰蛋白陈琼脂
(soybeancaseindigestagar)
生物指示剂
环氧乙烷灭菌
枯草芽泡杆菌
(Potatodextroseagar)
(内含或不含钝化剂)
限度检查
白色念珠菌、黑曲霉菌
20~25°C
5~7天
麦康凯琼脂(MacConKeyagar)
列文-伊红亚甲基琼脂
(LevineEosi11-methy1eneblueagar)
限度检查
大肠埃希菌
30"35βC
02天
贝尔德-帕克琼脂(Baird-Parkeragar)
(airstrips/mediaforaerobicbacteria)
空气监测
金黄色葡萄球菌、枯草杆菌
30~35C
02天
空气浮游需氧细菌检测培育基
(airstrips/mediaforfungi)
空气监测
白色念珠菌、黑曲霉
20~25°C
5~7天
厌氧琼脂(anaerobicagar)
梭状芽花杆菌琼脂(CloStridiaagars)
「2天
亚硫酸钿琼脂(bismuthsulfiteagar)
三糖铁琼脂(triplesugarIronagar)
胰酪陈大豆肉汤
(CaseinDigest-Soybroth)
(内含或不含钝化剂)
限度检查
饮用水细菌总数的测定及相关指标关系

饮用水细菌总数的测定及相关指标关系来源:生物信息网饮用水水质直接关系到人们的身体健康,为了研究饮用水中影响细菌总数的实验条件及理化指标,以便及时准确的为控制饮用水细菌学水质提供充分可靠的信息,于2004年5~ 11月间。
对北方某市的市区配水管网水质进行检测。
测定项目包括总余氯、自由余氯、浊度、pH、温度、细菌总数、总铁、可同化有机碳(asimilable organic carbon,AOC)、总有机碳(to—taI organic carbon,TOC)等,并对各指标间的关系进行研究。
1 材料与方法1.1 水样的采集在北方某市的市区配水管网上选取6个取样点。
于2004年5~11月对选定取样点进行取样及相关指标的水质分析。
取样点包括实验小区管网入口点、沿程点及末梢点。
还有一高层水箱点(4号点)。
其中1、6号点为管网入口点,2、3号点为管网末梢点,5号点为沿程点。
管材均为铸铁管。
2号点管网较为陈旧.为2O世纪5O年代铺设;6号点管网较新,为2002年辅设;其他取样点管网为2O世纪8O~90年代铺设。
取样均按照标准方法进行,水样采集后尽快送回实验室进行实验,按照国家标准方法对水样进行测定。
1.2 实验仪器及方法总余氯与自由余氯;采用HACH46 700—001型余氯仪进行测定。
细菌总数:异养菌平板计数(Heterotrophlc Plate Counts,HPC)法采用营养琼脂培养基和R2A培养基(R2A Agar medium)进行平板计数。
AOC:按照文献方法进行。
2 结果与讨论2.1 实验条件对细菌总数测定影响2.1.1 不同培养基对细菌总数测定的影响越来越多的检测结果证实,采用营养琼脂培养基进行细菌总数的测定明显低估了异养菌的真实数量,根据其计数结果来评价水处理的有效性及管网的清洁、卫生程度并不可靠。
饮用水的致病风险很可能较预期高得多。
因此,本实验采用了营养琼脂和目前国际上常用的R2A 两种培养基对细菌总数进行测定,并对测定结果进行比较。
纯化水微生物限度检测法的优化

纯化水微生物限度检测法的优化孙琳琳;王海亮;刘益明;卢会芬;吴国强【摘要】目的建立更为科学合理的纯化水微生物限度检测法.方法采用薄膜过滤法,检验量分别为1 mL和10 mL,培养基分别选用营养琼脂、玫瑰红钠琼脂、平板计数琼脂、R2A培养基,对纯化水样进行微生物限度检查.结果采用10 mL薄膜过滤法,R2A平板培养基进行纯化水的微生物限度检查,菌体检出率高于其他方法1~2倍,菌落培养效果好.结论确认了最优化的检验量和检验用培养基,建立了能更准确反映纯化水质量的检测方法.该研究有利于纯化水检测方法的改进和纯化水质量控制水平的提高.%Objective To establish a more scientific and reasonable purified water microbial limit test method.Methods Membrane filtration method (sample quantity:1 mL and 10 mL) were used to do the test,and nutrient agar,rose bengal agar medium,plate count agar and R2A medium were used to demonstrate the microbiology separately.Results Membrane filtration method (sample quantity:10 mL) and R2A were better than the routine method and the other medium with a much higher occurrence of total aerobic plate count.The detection rate was 1-2 times higher than the rate of other method and medium.Conclusion The selected testing sample quantity and culture medium are optimal,and the optimized test method will reflect the real quality of the purified water.The study will provide support for the testing improvement and quality control level.【期刊名称】《中国医药导报》【年(卷),期】2017(014)018【总页数】3页(P4-6)【关键词】纯化水;微生物限度检查;薄膜过滤法;检验量【作者】孙琳琳;王海亮;刘益明;卢会芬;吴国强【作者单位】石家庄以岭药业股份有限公司国际制药部,河北石家庄050035;石家庄以岭药业股份有限公司国际制药部,河北石家庄050035;石家庄以岭药业股份有限公司国际制药部,河北石家庄050035;石家庄以岭药业股份有限公司国际制药部,河北石家庄050035;石家庄以岭药业股份有限公司国际制药部,河北石家庄050035【正文语种】中文【中图分类】R927《中国药典》2010版、2015版纯化水微生物限度检查中要求使用薄膜过滤法进行检查[1-2],但未对薄膜过滤法的检测量等进行明确规定。
R2A琼脂培养基产品说明书

化学品安全技术说明书第一部分化学品及企业标识产品中文名称:R2A琼脂培养基产品英文名称:R2A Agar产品编号:022029企业名称:广东环凯微生物科技有限公司地址:广东省广州市黄埔区广州开发区科学城神舟路788号邮编:510663公司网址电子邮件地址:*********************传真号码:************销售热线:************-8602技术热线:************-8877/8876推荐用途和限制用途:生化研究/分析第二部分危险性概述GSH危害性类别非危险物质或混合物GSH标签要素非危险物质或混合物其它危害(健康危害、环境危害)未见报道第三部分成分/组成信息混合物化学品成分:参考培养基使用说明。
有害物质成分:无第四部分急救措施一般信息:无特殊的措施要求。
皮肤接触:立即用清水彻底清洗。
眼睛接触:立即提起眼睑,用大量流动清水冲洗15min。
如不适就医。
吸入:如果吸入,将人员移动到新鲜空气处,如果没有呼吸,进行人工呼吸操作,并联系医生。
食入:如误食,用水冲洗口腔,如不适就医。
就医信息:出示产品使用说明或者此SDS。
第六部分 泄露应急处理个人防护: 穿个人实验服,佩戴手套和口罩,避免吸入干粉。
环境保护措施: 用湿布和地拖擦拭干净。
清洁/收集措施: 保持干燥。
迅速清洗弄脏的区域。
第七部分 操作处置与储存安全操作注意事项: 防止粉尘扬起,应提供通风设备。
储存注意事项: 贮存于避光、干燥处,用后立即旋紧瓶盖。
第八部分 接触控制/个人防护职业接触限值 没有已知的国家规定的暴露极限。
工程控制: 提供安全淋浴和洗眼设备个人保护措施 呼吸系统防护: 在通风橱里称取产品,佩戴口罩。
眼睛防护: 佩戴安全眼镜。
身体防护: 穿实验室服。
手防护: 戴防化学品手套。
其他防护: 常规的工业卫生操作,工作后及时清洗双手。
第九部分 理化特性外观: 粉末 pH 值: 7.2±0.2 颜色: 淡黄色 气味: 特征性 熔点: 无数据资料 沸点: 无数据资料 燃点: 无数据资料 闪点: 无数据资料 爆炸限度 下限: 无数据资料 上限: 无数据资料 热分解: 无数据资料溶解性: 按产品使用说明上的用量比例加蒸馏水,加热煮沸至完全溶解,溶液呈黄色澄清无沉淀。
纯化水R2A培养基适用性验证

编号:FAL-YZ-005.1R2A培养基适用性验证报告科技发展有限公司目录R2A培养基适用性验证报告1.目的因2015版药典纯化水检验用培养基变更,依1105 非无菌产品微生物限度检查方法,通过此次实验对所更换的R2A琼脂培养基进行适用性检查,以证明该方法及所采用的培养基适用于纯化水微生物限度检查日常检测。
2.范围适用于本公司纯化水的微生物限度检查。
3.依据中华人民共和国药典(2015年版)4. 职责权限5. 验证方法5.1R2A培养基的适用性检查5.1.1R2A培养基应进行培养基的适用性检查。
5.1.2菌种试验用菌株的传代次数不得超过5 代,试验用菌种应采用适宜的菌种保藏技术进行保存,以保证试验菌株的生物学特性。
5.1.3菌液制备铜绿假单胞菌、枯草芽孢杆菌的微生物培养基质控品,使用前注入1.1ml稀释液充分溶解后,在漩涡混合器上振荡混匀,制成1ml(相当于10~100cfu/0.1ml)菌悬液。
5.1.4适用性检查取铜绿假单胞菌、枯草芽孢杆菌各10~100cfu,分别注入无菌平皿中,立即倾注R2A琼脂培养基,每株试验菌平行制备2 个平皿,混匀,凝固,置30~35℃培养不少于5天,计数;5.1.5结果判定被检定的固体培养基上的菌落平均数与对照培养基上的菌落平均数的比值在0.5~2范围内,且菌落形态大小应与对照培养基上的菌落一致。
判该培养基的适用性检查符合规定。
5.1.6实验前的准备5.1.6.1仪器设备确认人: 日期:5.1.6.2操作环境微生物限度检查应在环境洁净度10000 级下的局部洁净度100 级的单向流空气区域内进行。
检验全过程必须严格遵守无菌操作,防止再污染。
单向流空气区域、工作台面及环境应定期按《医药工业洁净室(区)悬浮粒子、浮游菌和沉降菌的测试方法》的现行国家标准进行洁净度验证。
5.1.6.3器具无菌培养皿:(直径90mm)1ml注射器5.2计数方法的验证5.2.1当建立纯化水微生物限度检查法时,应进行细菌、霉菌及酵母菌计数方法的验证,以确认所采用的方法适合于该产品的细菌、霉菌及酵母菌数的测定。
R2A琼脂对照培养基使用说明

R2A琼脂对照培养基
R2A琼脂对照培养基用途:
培养基适用性实验
R2A琼脂对照培养基注意事项:
1.检查平板内是否干裂或染菌,如长菌请勿使用;
2.请在洁净的环境下操作,避免杂菌干扰;
3.在冰箱储存很久的培养基容易出现一些冷凝水,请在洁净的环境下将水倒出,
然后在培养箱放置10-30Min,待其表面干燥后再接种;或在使用前,提前一到两周放置室温即可;
4.弃物处理:使用后应高压灭菌或焚烧后按一般垃圾处理,也可按专业技术人
员指示方法处理。
保存:避光保存,放于阴凉干燥处。
R2A琼脂对照培养基其他相关对照培养基:
硫乙醇酸盐流体对照培养基
改良马丁对照培养基
营养琼脂对照培养基
营养肉汤对照培养基
玫瑰红钠琼脂对照培养基
胆盐乳糖对照培养基
甘露醇氯化钠琼脂对照培养基
沙氏葡萄糖肉汤对照培养基
麦康凯琼脂对照培养基
沙门、志贺菌属琼脂对照培养基
4-甲基伞形酮葡萄苷酸(MUG)对照培养基
沙氏葡萄糖琼脂对照培养基
念珠菌显色对照培养基
绿脓菌素测定用对照培养基基础
梭菌增菌对照培养基
哥伦比亚琼脂对照培养基
溴化十六烷基三甲铵琼脂对照培养基基础
四硫磺酸钠亮绿对照培养基基础
乳糖发酵对照培养基
酵母浸出粉胨葡萄糖琼脂(YPD)对照培养基
胰酪大豆胨琼脂对照培养基
胰酪大豆胨肉汤对照培养基
R2A琼脂对照培养基
三糖铁琼脂对照培养基
麦康凯液体对照培养基
紫红胆盐葡萄糖琼脂对照培养基肠道菌增菌液体对照培养基
木糖赖氨酸脱氧胆酸盐对照培养基。
培养基配方

培养基配方培养基配方一、R2A/R3A培养基配方(g/L):R2A R3A酵母粉 0.5 g 1.0 g胰蛋白胨 0.5 g 1.0 g酪蛋白氨基酸(casamino acid)0.5 g 1.0 g葡萄糖0.5 g 1.0 g可溶性淀粉0.5 g 1.0 g磷酸氢二钾0.3 g 0.6 g七水硫酸镁0.05 g 0.1g丙酮酸钠 0.3 g 0.5g琼脂15.0 g 15.0 g用磷酸氢二钾或磷酸二氢钾调pH到7.2后,加1L蒸馏水,搅拌溶解,121℃灭菌15min。
特点:R2A培养基主要用于水的菌落计数,它可以修复被氯气损伤的细菌,支持耐受氯气的微生物的生长。
培养要求,低温(20-30℃)长时间培养(5-7天)这样得到的菌落数比常规菌落总数检测的菌落数更符合实际。
R3A培养基主要用于菌株的生化特征描述和鉴定。
参考文献:Reasoner DJ, Geldreich EE. A new medium for the enumeration and subculture of bacteria from potable water. Appl Environ Microbiol. 1985,49(1):1-7.二、VL55培养基(Sait M et al,2002)(土壤筛菌)配方(g/L)1×2×2-(N-吗啉基)乙磺酸 1.95 g 3.9 gMgSO4 0.024 g(0.2mM)0.048 g(0.4mM)CaCl20.033294 g(0.3mM)0.066588 g(0.6mM)(NH4)2HPO40.026421 g(0.2mM)0.052824 g(0.4mM)亚硒酸盐/钨酸盐溶液1mL 2mL 微量溶液SL10 1mL 2mL用0.2mol/L的NaOH和0.1mol/L的KOH混合液调pH到5.5(这与土壤的pH一致)Sait M等取2×的培养基121℃灭菌15min后,冷却至56℃,加入10mL5%(w/v)的木聚糖溶液,2mL的维生素溶液1,6mL的维生素溶液2。
061-00 R2A琼脂培养基培养基适用性检查记录

第1页共2页检品培养基名称培养基来源批号配制编号检验日期
R2A琼脂培养基
检验人:复核人:
检品培养基名称培养基来源批号配制编号检验日期R2A琼脂培养基
第2页共2页
与对照培养基上的菌落阴性皿1皿2平均A阴性皿1皿2平均B
铜绿假单胞菌□一致□不一致
枯草芽孢杆菌□一致□不一致
标准判定
被检固体培养基上的菌落平均数与对照培养基上的菌落平均数的比值应在0.5~2范围内,且菌落形态大小应与对照培养基上一致。
判该培养基的适用性检查符合规定。
结论□符合规定□不符合规定
检验人:复核人:。
