高二有机化学醇和酚课件(2).ppt
合集下载
有机化学课件-醇和酚

酚具有抗菌和消毒作用,被用 于制造医用药物和防腐剂。
醇在清洁用品中的应用
醇是常见的清洁剂成分,用于 去除污垢和杀菌消毒。
比较醇和酚的性质和反应
分子结构 性质 化学性质 应用
醇 含有羟基的碳链 有酒精味 加成、消除、氧化、磺化 清洁剂、溶剂
酚 苯环上有羟基 有特殊香味 亲电取代、缩合、酯化 药物、化妆品
缩合反应类型 酚的烷基化反应 酚的羧酸化反应 酚的醚化反应
反应条件 酚与醇在酸催化下缩合 酚与羧酸在酸催化下缩合 酚与醇在酸催化下缩合
酚的酯化反应
1 定义
酚与酸反应生成酯。
2 反应条件
酚和酸在酸催化下反应。
醇和酚在生活中的应用
醇在化妆品中的应用
醇常用作保湿剂和溶剂,广泛 应用于各种化妆品中。
酚在药物中的应用
有机化学课件-醇和酚
本课件介绍醇和酚的基本概念,包括分子结构、物理性质、化学性质以及在 生活中的应用。我们将深入探讨各种反应,并提供考试中可能出现的相关题 目及解析。
醇与酚的分子结构与化学式
醇
CnH2n+1OH
酚
C6H6O
醇和酚的物理性质
1醇
一般为无色液体或固体,具有特有的酒精味。
2酚
常为无色结晶固体,具有特殊香味。和氧化反应。
2酚
具有芳香性,可进行亲电取代、缩合和酯化反应。
醇和酚的加成反应
1
醇的酸碱反应
与强碱反应生成盐和水。
2
酚的氧化反应
与氧气反应生成酚醛或酚酮。
3
醇和酚的磺化反应
与磺酰氯反应生成磺酸酯。
醇和酚的消除反应
1
酚的缩合反应
2
通过缩合反应,酚可以形成醚。
3
醇在清洁用品中的应用
醇是常见的清洁剂成分,用于 去除污垢和杀菌消毒。
比较醇和酚的性质和反应
分子结构 性质 化学性质 应用
醇 含有羟基的碳链 有酒精味 加成、消除、氧化、磺化 清洁剂、溶剂
酚 苯环上有羟基 有特殊香味 亲电取代、缩合、酯化 药物、化妆品
缩合反应类型 酚的烷基化反应 酚的羧酸化反应 酚的醚化反应
反应条件 酚与醇在酸催化下缩合 酚与羧酸在酸催化下缩合 酚与醇在酸催化下缩合
酚的酯化反应
1 定义
酚与酸反应生成酯。
2 反应条件
酚和酸在酸催化下反应。
醇和酚在生活中的应用
醇在化妆品中的应用
醇常用作保湿剂和溶剂,广泛 应用于各种化妆品中。
酚在药物中的应用
有机化学课件-醇和酚
本课件介绍醇和酚的基本概念,包括分子结构、物理性质、化学性质以及在 生活中的应用。我们将深入探讨各种反应,并提供考试中可能出现的相关题 目及解析。
醇与酚的分子结构与化学式
醇
CnH2n+1OH
酚
C6H6O
醇和酚的物理性质
1醇
一般为无色液体或固体,具有特有的酒精味。
2酚
常为无色结晶固体,具有特殊香味。和氧化反应。
2酚
具有芳香性,可进行亲电取代、缩合和酯化反应。
醇和酚的加成反应
1
醇的酸碱反应
与强碱反应生成盐和水。
2
酚的氧化反应
与氧气反应生成酚醛或酚酮。
3
醇和酚的磺化反应
与磺酰氯反应生成磺酸酯。
醇和酚的消除反应
1
酚的缩合反应
2
通过缩合反应,酚可以形成醚。
3
邳州市第二中学高二化学选修五3.1醇酚课件

2.消去反应 消去反应:有机化合物在适当的条件下,从 一个分子中脱去一个小分子(如水、卤化氢 等),而生成不饱和(含双键或三键等)化合物 的反应。
【例5】 下列条件下能发生消去反应的是 ( ) A.1-溴丙烷与NaOH醇溶液共热 B.乙醇与浓H2SO4共热至140℃ C.溴乙烷与NaOH水溶液共热 D.乙醇与浓H2SO4共热至170℃ 【解析】 1-溴丙烷与NaOH醇溶液共热可 以发生消去反应得到丙烯;而溴乙烷与 NaOH水溶液共热发生的是水解反应;乙醇 与浓H2SO4共热至140℃发生的是取代反应 得到乙醚;乙醇与浓H2SO4共热至170℃发
用浓硫酸跟分子式分别为C2H6O和C3H8O的 醇所组成的混合液反应,可能得到的醚的种 类有( ) A.四种 B.五种 C.六种 D.七种 【答案】 C
由于醇分子中与羟基相连的碳原子的氧化数未达到碳 原子的最高氧化数+4,说明醇有被氧化的趋势. 1.醇的燃烧 乙醇在空气里点燃后易燃烧,发出淡蓝色火焰,同时 放出大量的热。乙醇完全燃烧生成二氧化碳和水: 点燃 CH3CH2OH+3O2――→2CO2+3H2O 2.与强氧化剂的反应
)
【解析】 A项中—OH未与苯环直接相连, 所以是醇;B、C项中—OH皆与苯环直接相连, 都属于酚类;D项中 不是苯环,而是环烷基,故D属于 醇类。
【答案】 BC
【答案】
C
下列物质中互为同系物的是(
)
【解析】 A是酚与醇,C是醇与醚,D是酚 与醚,结构都不相似,故选B。 【答案】 B
zxxk/w
Zxx k
4.醇的化学性质 (1)跟金属钠反应,生成________和 ________。 (2)跟氢卤酸反应,生成________和 ________。 (3)在________催化和一定温度下发生 ________反应生成烯烃。 (4)氧化反应:既可以在空气中燃烧,又可以 被催化氧化成醛或酮,还可以被酸性高锰酸 钾溶液和酸性重铬酸钾溶液氧化。 (5)与含氧酸发生________反应生成酯和水
【高中化学】醇的化学性质 高二化学同步课件(人教版2019选择性必修3)

CH3CH2-OH + H-OCH2CH3
浓H2SO4 140℃
CH3CH2-O-CH2CH3
+
H2O
应用:实验室制取乙烯
乙醇的消去反应实验装置
②温度计水银球 的位置?
液面下
①酒精与浓硫酸 混合液如何配置 体积比约为1∶3 浓硫酸加入酒精中
③为何使液体温度迅速升到 170℃,不能过高或高低?
防止发生副反应
④用何法收集乙烯? 排水法
思考与讨论1:混合液颜色如何变化?为什么? →烧瓶中的液体逐渐变黑。 →在加热的条件下,浓硫酸能将无水乙醇脱水生成碳的单质等, 碳的单质使烧瓶内的液体带上了黑色。
思考与讨论2:为何使用NaOH溶液进行洗气? 因乙烯中混有的SO2气体能使酸性KMnO4溶液褪色影响乙烯的检验,
第二节 醇、酚
第二课时 醇(2)
——醇的化学性质
醇的化学性质
结构决定性质
元素 H
C
O
电负性 2.1 2.5 3.5
对比:乙烷与乙醇结构有何不同? 导致化学性质有何不同 ?
HH H−C−Cδ+−Oδ-−Hδ+
HH
δ+ δ- δ+
➢ C—O—H 键具有较强的极性,易断裂。
➢ O—H容易断裂,使羟基中的氢原子被取代;同样C—O也易断裂, 使羟基被取代或脱去,从而发生取代反应或消去反应。
2.取代反应 [以2-丙醇( CH3-CH-CH3 )为例写出下列反应方程式]
—
OH
①与浓的氢溴酸反应
—
CH3-CH-CH3+H-3; Br
H2O
②分子间脱水成醚 2 CH3-CH-CH3 OH
—
浓硫酸
△
—
CH3-CH-O -CH-CH3 CH3 CH3
【高中化学】醇 高二化学同步课件(人教版2019选择性必修3)
油状液体 可部分溶于水 蜡状固体 难溶于水
结论:1.饱和一元醇的熔、沸点随碳原子数的增加而升高。 (通常C1—C11:液态;C12以上:无色蜡状固体)
2.在水中的溶解度随碳原子数的增加而降低
烃基: 憎水基 —OH: 亲水基
烃基越大,憎水基占比例大,削弱了-OH的亲水作用,因而水溶性降低
5、醇的重要物理性质 (课本P58 思考与讨论)
➢ 醇分子间存在氢键,增强了分子间的作用力。
➢醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着较强的 相互吸引作用,这种吸引作用叫氢键。
醇分子间形成氢键示意图:
R (—)O (+) HH
(+) H
R(—) O (+)
H
H
RO(—)(+) H
O(—)
O
O
氢键
R
R
R
➢ 含碳原子少的低级醇不仅分子间易形成氢键, 它们与水分子间也能形成氢键!
2) 水溶性: 烃基: 憎水基 —OH: 亲水基
∴ 烃基碳数越多,越难溶于水;羟基越多,越易溶于水 ①甲醇、乙醇、丙醇、乙二醇、丙三醇等与水可以任意比例混溶 (因为氢键) ② 4-11个碳的醇为油状液体,部分溶于水 ③ C12以上的醇为无色固体,不溶于水 3) 醇的密度均小于水
同步练习
B 1.下列关于醇类的说法错误的是
工业酒精有毒!
4.几种重要的醇简介
2.乙二醇(
)和丙三醇(
)(课本P58)
➢ 都是无色、黏稠、有甜味的液体,易溶于水和乙醇,能与水以任意比例互溶。
➢ 都是重要的化工原料。 ➢ 乙二醇: 是汽车防冻液的主要成分、合成涤纶的主要原料。
4.几种重要的醇简介
2.乙二醇(
《有机化学酚》课件

1 溴化反应
详细解释酚与醇在溴水中 的反应差异,从而区分它 们。
2 碘化反应
介绍酚与醇在碘化试剂中 产生的颜色变化及反应机 理。
3 氧化反应
说明酚在氧化剂的作用下 发生的氧化反应,而醇则 不会。
酚在工业中的应用
石油化工
酚在石油化工行业中的广泛应用,包括生产塑料、 合成纤维和胶粘剂。
化学研究
酚在化学研究中的重要性,用于合成具有特定功能 的化合物。
药物制造
探索酚在医药制造中的应用,以及其作为抗菌、止 痛和抗氧化剂的作用。
化妆品生产
介绍酚在化妆品中的用途,包括作为防晒剂、抗皱 成分和抗菌剂。
结论:有机化学酚的重要性
总结酚在有机化学中的关键作用,鼓励更多的研究和应用以推动科学进步。
《有机化学酚》PPT课件
探索有机化学酚的奇妙世界,从基础概念到合成方法、反应性质和应用,带 您领略这一重要有机化合物的魅力。
有机化学酚简介
了解什么是有机化学酚以及其在化学领域的重要性,探索其独特的化学性质 和结构特点。
酚的定义和性质
揭示酚的几何构型、物理性质和一些特殊化学性质,解释其在化学反应中的 重要作用。
酚的命名法
学习酚的命名规则,包括使用IUPAC命名法和常用命名法来命名不同结构的酚类化合物。
酚的分类
Alkyl Phenols
说明碳基取代酚的命名方法,以及几种常见的 烷基酚类化合物。
Halogenated Phenols
详细解释卤代酚化合物的结构和性质,以及卤 代酚在环境中的影响。
Aryl Phenols
3
氧化法
解释通过氧化反应将酚、芳香族醇和应
1
酚的酸碱性质
说明酚与碱、酸反应的机理,以及酚作为酸碱指示剂的应用。
有机化学第八章醇和酚

第8章 醇和酚 (Alcohols & Phenols)
1
◼醇
结构、分类和命名 物理性质 化学性质
弱酸性、氧化和脱氢、取代、脱水 邻二醇特殊反应、与无机含氧酸的作用(无机酸酯形成)
◼酚
结构、命名和主要来源 物理性质 化学性质
◼ 硫醇和苯硫酚
物理性质 化学反应
2
3
◼从《唐诗三百首》中白居易的《问刘十九》说起
55
酸性 与
溶解性
酚: 不溶于NaHCO3水溶液 羧酸: 既溶于NaOH,也溶于NaHCO3水溶液 (高级)醇:既不溶于NaOH,也不溶于NaHCO3水溶液
56
➢ 硫酸二甲酯:一种无机酸酯,可作为甲基化试剂
O 2 CH3OH + HO S OH
O
应用:
O H3C O S O CH3
O
硫酸二甲酯
37
➢ 举例:
38
机理:SN2 ➢ 举例:
39
4. 醇的脱水反应:b-消除反应
+
CC H OH
+ −
− H2O
CC
➢ 酸性条件下的脱水反应:活化羟基 常用的酸:硫酸、磷酸等
➢ 使用脱水剂进行脱水反应 常用的脱水剂:P2O5,Al2O3等
40
(1) 在酸性条件下的分子内脱水反应:
H3C OH
CH3
温度控制的分子内和分子间反应
➢ 分子内双羟基脱水成环醚
H2SO4
HO
OH
O 四氢吡喃
43
➢ 分子间脱水:
R OH + H O R
H
R OR
机理:以乙醇为例
44
5. 邻二醇的特殊反应
(1) Pinacol重排
1
◼醇
结构、分类和命名 物理性质 化学性质
弱酸性、氧化和脱氢、取代、脱水 邻二醇特殊反应、与无机含氧酸的作用(无机酸酯形成)
◼酚
结构、命名和主要来源 物理性质 化学性质
◼ 硫醇和苯硫酚
物理性质 化学反应
2
3
◼从《唐诗三百首》中白居易的《问刘十九》说起
55
酸性 与
溶解性
酚: 不溶于NaHCO3水溶液 羧酸: 既溶于NaOH,也溶于NaHCO3水溶液 (高级)醇:既不溶于NaOH,也不溶于NaHCO3水溶液
56
➢ 硫酸二甲酯:一种无机酸酯,可作为甲基化试剂
O 2 CH3OH + HO S OH
O
应用:
O H3C O S O CH3
O
硫酸二甲酯
37
➢ 举例:
38
机理:SN2 ➢ 举例:
39
4. 醇的脱水反应:b-消除反应
+
CC H OH
+ −
− H2O
CC
➢ 酸性条件下的脱水反应:活化羟基 常用的酸:硫酸、磷酸等
➢ 使用脱水剂进行脱水反应 常用的脱水剂:P2O5,Al2O3等
40
(1) 在酸性条件下的分子内脱水反应:
H3C OH
CH3
温度控制的分子内和分子间反应
➢ 分子内双羟基脱水成环醚
H2SO4
HO
OH
O 四氢吡喃
43
➢ 分子间脱水:
R OH + H O R
H
R OR
机理:以乙醇为例
44
5. 邻二醇的特殊反应
(1) Pinacol重排
有机化学课件——Chapter 07 醇、酚、醚

有机化学课件
32
第七章 醇、酚、醚
3. 醇的脱水反应
在浓硫酸催化下,醇通常发生脱水反应得到烯烃或醚. 反应涉及碳正离子中间体. 如果产物为烯烃则遵从Saytzeff规则. 较低温度下反应主要发生分子间脱水成醚, 通常低于140oC . 较高温度下主要发生分子内脱水成烯烃的反应, 通常高于 180oC.
有机化学课件 26 第七章 醇、酚、醚
醇和氢卤酸反应的局限性在于: 所期待的卤代烃不是总能 高收率地得到, 具体表现为四个方面. ① 大多数醇不能和HI反应得到碘代烷烃; ② 1o和2o醇制备氯代烷收率很低; ③ 总是有消除反应产物(烯烃)生成; ④ 碳正离子中间体经常发生重排,得到重排产物.
有机化学课件
OH CH2CH2CH2COOH
有机化学课件 5 第七章 醇、酚、醚
三、醇的物理性质
Unusually high boiling points due to hydrogen bonding between molecules. Small alcohols are miscible in water, but solubility decreases as the size of the alkyl group increases.
有机化学课件
17
第七章 醇、酚、醚
1º, 2º, 3º碳的氧化还原程度
氧化: 分子中C-H 变成C-O. 还原: 分子中C-O 变成C-H.
有机化学课件
18
第七章 醇、酚、醚
1) 仲醇的氧化
许多氧化剂都可以将2o醇氧化为酮. 常用氧化剂如: Na2Cr2O7/H2SO4 H2CrO4 可能是氧化反应的活性物种. 氧化反应伴随明显的颜色变化: 反应溶液由橙色(Cr6+) 变为深蓝色(Cr3+).
酚-高二化学同步精品课件(人教版2019选择性必修3)

Na___3_m__o__l ___
NaOH_2_m__o__l__
NaHCO31_m__o__l_
Na2CO3 _2_m__o__l___
醇、酚、羧酸酸性强弱对比
代表 物
是否具 有酸性
与钠反应
与NaOH 的反应
与Na2CO3 的反应
乙醇
√
苯酚 √
√
乙酸 √
√
√
√
√
√
与NaHCO3 的反应
√
课堂练习4:为了把制得的苯酚从溴苯中分离出来,正确操作是( B )
结论: 酚羟基对苯环影响,使苯环上羟基邻、对位的氢原
子的活性增强,易被取代
②硝化反应
OH
O2N
+3HNO3浓硫△酸
OH NO2
+3H2O
(三硝基苯酚N又O2称苦味酸)
课堂练习6:1mol的
—CH3 HO
——
CH3
—CH3 —OH
OH
分别与足量的饱和溴水反应消耗溴的物质的量分别为__3__m__o_l__、
质B是__N_a_H__C_O_3____;设备③中发生的化学反应方程式为_______________
-ONa+ CO2 + H2O
-OH + NaHCO3
(3)在设备④中,物质B的水溶液 和反应产是 NaOH 、 CaCO3 和水,可通过过滤 操 作分离产物。
(4)上图中,能循环使用的物质是C6H6、CaO、 CO2 、 NaOH水溶液。 (5)写出同时满足下列条件的苯酚的一种同分异构体的结构简式 ____C_H__3-_C__≡_C_-_O_-_C__≡_C_-_C_H__3______。
课堂练习2:下列关于苯酚的叙述中正确的是( B )
一轮复习醇和酚ppt课件

2、-OH所连碳上有1个H的醇 氧化 酮(R-CO-R’)
3、醇-OH所连碳上无H,则不能被氧化。如 R’
R-C-OH R”
➢醇的消去反应规律 :
连羟基的碳的邻位碳上有H才能发生消去反应。
思考与交流:
溴乙烷与乙醇都能发生消去反应,它们有什么异同?
反应条件
CH3CH2Br
NaOH的乙醇溶 液、加热
慎沾腐到蚀皮性肤上,应立即用
酒精洗涤。
纯净的苯酚露置在空气中因小部分发生氧化而 显 粉红色。
请根据苯酚的结构,推测、回忆其化学性质:
OH 羟基:弱酸性、氧化反应 苯环:取代反应、加成反应
3、苯酚的化学性质
1)苯酚的弱酸性 (又名石炭酸)
OH + H2O
O- + H3O+
OH + NaOH
ONa+ CO2 + H2O
小烃结、:卤代烃、醇之间的衍变关系
加成
水解
CH2=CH2 消去 CH3CH2-Br
CH3CH2-OH
?
➢卤代烃在有机合成方面的应用: 引入官能团——碳碳双键、-OH
烃的衍生物复习
二、醇 乙醇
1、醇的定义 —OH与烃基或苯环侧链碳相连结的化合物 一元醇通式: R-OH 饱和一元醇通式: CnH2n+1OH或CnH2n+2O
合物。
➢醇和酚在结构上区别: 醇: 羟基与链烃基(饱和碳原子)直接相连 酚: 羟基与苯环直接相连
练习:
判断下列化合物,分别属于哪类有机物?
CH3
OH A 酚 OH
CH2CH2OH B醇
CH=CH2 OH
C酚
OH
COOH
D 二酚
3、醇-OH所连碳上无H,则不能被氧化。如 R’
R-C-OH R”
➢醇的消去反应规律 :
连羟基的碳的邻位碳上有H才能发生消去反应。
思考与交流:
溴乙烷与乙醇都能发生消去反应,它们有什么异同?
反应条件
CH3CH2Br
NaOH的乙醇溶 液、加热
慎沾腐到蚀皮性肤上,应立即用
酒精洗涤。
纯净的苯酚露置在空气中因小部分发生氧化而 显 粉红色。
请根据苯酚的结构,推测、回忆其化学性质:
OH 羟基:弱酸性、氧化反应 苯环:取代反应、加成反应
3、苯酚的化学性质
1)苯酚的弱酸性 (又名石炭酸)
OH + H2O
O- + H3O+
OH + NaOH
ONa+ CO2 + H2O
小烃结、:卤代烃、醇之间的衍变关系
加成
水解
CH2=CH2 消去 CH3CH2-Br
CH3CH2-OH
?
➢卤代烃在有机合成方面的应用: 引入官能团——碳碳双键、-OH
烃的衍生物复习
二、醇 乙醇
1、醇的定义 —OH与烃基或苯环侧链碳相连结的化合物 一元醇通式: R-OH 饱和一元醇通式: CnH2n+1OH或CnH2n+2O
合物。
➢醇和酚在结构上区别: 醇: 羟基与链烃基(饱和碳原子)直接相连 酚: 羟基与苯环直接相连
练习:
判断下列化合物,分别属于哪类有机物?
CH3
OH A 酚 OH
CH2CH2OH B醇
CH=CH2 OH
C酚
OH
COOH
D 二酚
《有机化学醇硫醇酚》课件
多酚
多酚是含有多个羟基的酚,例 如咖啡因。
1 定义
醇是由羟基(-OH)取代烃基得到的化合物。
2 性质
醇具有溶解性强、可与酸发生酯化反应等特点。
不同种类的醇以及它们的命名方法
一元醇
一元醇是含有一个羟基的醇, 例如甲醇。
二元醇
二元醇是含有两个羟基的醇, 例如乙二醇。
三元醇
三元醇是含有三个羟基的醇, 例如甘油。
醇的制备方法
1
氢醇法
通过羰基化合物的加氢反应得到醇。
硫醇的定义和性质
1 定义
硫醇是含有硫原子的类似醇的有机化合物。
2 性质
硫醇具有特殊的气味,可溶于有机溶剂,容 易发生氧化反应。
不同种类的硫醇以及它们的命名方法
一硫醇
一硫醇是含有一个硫原子的硫 醇,例如巯基甲烷。
二硫醇
二硫醇是含有两个硫原子的硫 醇,例如二巯基硫。
多硫醇
多硫醇是含有多个硫原子的硫 醇,例如巯基乙烷。
硫醇的制备方法
1
还原反应
通过还原硫酸盐或硫醇醚制备硫醇。
2
硫化反应
通过硫化物与硒醇反应制备硫醇。
3
亲电加成反应
通过亲电物质与硫醇反应制备含硫化合物。
硫醇的主要用途
1 化学合成
硫醇用于有机合成反应中的硫化、酰化和叔 碳与炔烃的氧化反应。
2 医药领域
硫醇作为医药合成中的中间体,广泛应用于 药物制备。
《有机化学醇硫醇酚》 PPT课件
这个PPT课件将带您深入了解有机化学醇硫醇酚的知识,包括定义、性质、 命名方法、制备方法、主要用途以及在生活中的应用。
什么是有机化学醇硫醇酚?
有机化学醇硫醇酚是一类重要的有机化合物,具有醇、硫醇和酚的结构特点。 这些化合物在生物、化工和医药领域有着广泛的应用。
高三第一轮复习醇酚课件.ppt
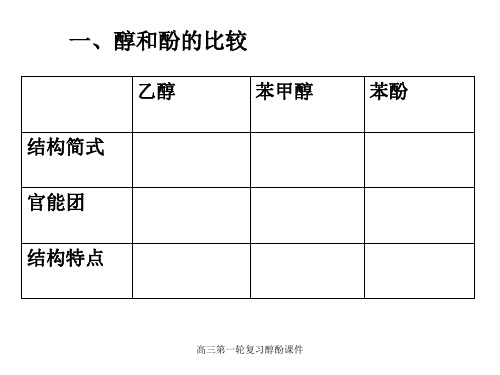
燃烧: C2H5OH +3 O2
2CO2 +3H2O
催化氧化:2C2H5OH
高三第一催轮复化习醇剂酚课件
+ O2
2CH3CHO
+
H2O
浓硫酸
CH3COOH+C2H5OH
CH3COOC2H5+H2O
三、醇的分类 分析低级醇的沸点比其相对应的烷烃要高得多的原因?
高三第一轮复习醇酚课件
思考:哪些醇不能进行消去反应?哪些醇不能氧化成醛?
4、当生成的气体通过苯酚钠溶液 时,可以发现溶
液变浑浊。说明碳酸的酸性比苯酚 强。
CO2+H2O+C6H5ONa= C6H5OH↓+NaHCO3
5、停止实验,填写好实验现象。 6、拆除装置,洗净仪器。
如果要分离出苯酚, 采用 分液 操作
高三第一轮复习醇酚课件
写出六种化学性质不同,且在同类物质中分子 量最小的有机物的结构简式,这些物质燃烧
VCO 2:VH2O1: 1
这些物质是_____、_____、___、___、____、_____
(提示:找最简式中:C:H=1:2的有机物, 它们为烯、环烷烃CnH2n;醛、酮CnH2nO;羧酸、 酯CnH2nO2;然后再找每一类有机物中分子量最小 的物质,注意思维的有序性)
CH2 CH2
HCHO
、
HCOOH、 HCOOCH 高三第一轮复习醇酚课件
3
NaOH 饱和Na2CO3 溶液 溶液
分液
分液
溴苯(溴)
NaOH 溶液 分液
乙醇 (水)
CaO
蒸馏
思路总结:先生成盐,然后利用不相溶 或者 有机物 沸点低、盐沸点高的特点来进行分离。
