空气恒算,物料衡算,热量衡算
化工原理物料衡算和热量衡算

化工原理物料衡算和热量衡算引言化工工程涉及许多物料的处理和转化过程,同时也需要考虑热量的平衡。
物料衡算和热量衡算是化工原理的重要内容,对于工程实践和过程优化具有重要的意义。
本文将介绍化工原理中的物料衡算和热量衡算的基本原理和计算方法。
物料衡算物料衡算是指对于化工工程中物料流动和转化过程的计算和分析。
在化工工程中,物料的流动和转化是实现各种反应和分离操作的基础,因此正确的物料衡算是保证工程设计和操作的关键。
在物料衡算中,我们通常需要考虑以下几个方面: 1. 物料的质量衡算:即对物料的质量输入和输出进行计算和分析。
对于物料的质量衡算,我们需要注意物料流动的平衡原则,即质量的输入必须等于输出。
2. 物料的能量衡算:即对物料的能量输入和输出进行计算和分析。
能量的输入和输出会影响物料的温度和相变过程,因此在能量衡算中需要考虑物料的热力学性质。
3. 物料的流动速度衡算:即对物料流动速度进行计算和分析。
物料的流动速度决定了反应和分离操作的效率,因此在物料衡算中需要合理地确定流量和速度的关系。
4. 物料的浓度衡算:即对物料中组分浓度的计算和分析。
物料的浓度会影响其反应和分离的速率和效果,因此在物料衡算中需要考虑不同组分浓度的变化规律。
物料衡算通常使用质量守恒和能量守恒等基本原理进行计算。
同时,还可以利用化学反应平衡的原理和质量流动的平衡原则进行衡算过程中的参数确定。
热量衡算热量衡算是化工工程中热力学过程的计算和分析。
在化工工程中,热量的平衡是保证反应和分离操作能够正常进行的基础。
热量衡算需要考虑以下几个方面: 1. 热量的输入和输出:即对于热量的输入和输出进行计算和分析。
在化工工程中,我们通常需要对热量的输入和输出进行平衡,以保证工程操作的稳定性。
2. 热量的传递和转化:即对于热量的传递和转化过程进行计算和分析。
热量的传递可以通过传导、对流和辐射等方式进行,因此在热量衡算中需要考虑传热方式的影响。
3. 热平衡的计算:即对于反应和分离过程中热量平衡的计算和分析。
物料衡算和热量衡算

3 物料衡算依据原理:输入的物料量=输出的物料量+损失的物料量3.1 衡算基准年生产能力:2000吨/年年开工时间:7200小时产品含量:99%3.2 物料衡算反应过程涉及一个氧化反应过程,每批生产的产品相同,虽然有原料对叔丁基甲苯和溶剂甲苯的循环,第一批以后循环的物料再次进入反应,但每批加料相同。
在此基础上,只要计算第一个批次的投料量,以后加料一样。
反应釜内加热时间2h、正常的反应时间18h、冷却时间1h。
加上进料和出料各半个小时,这个生产周期一共2+18+1+1=22h。
所以在正常的生产后,每22小时可以生产出一批产品。
每年按300天生产来计算,共开工7200小时,可以生产327个批次。
要求每年生产2000吨对叔丁基苯甲酸,则每批生产2000÷327=6.116吨。
产品纯度99 %( wt %)实际过程中为了达到高转化率和高反应速率,需要加入过量对叔丁基甲苯做溶剂,反应剩余的原料经分离后循环使用。
3.2.1 各段物料(1) 原料对叔丁基甲苯的投料量设投料中纯的对叔丁基甲苯为X kg,则由C11H16C11H14O2 M 148.24 178.23m x 6054.8得x=6054.8×148.24÷178.23=5036.0 kg折合成工业原料的对叔丁基甲苯质量为5036.0÷0.99=5086.9kg实际在第一批生产过程加入的对叔丁基甲苯为6950.3kg(2)氧气的通入量生产过程中连续通入氧气,维持釜内压力为表压0.01MPa,进行氧化反应。
实际生产过程中,现场采集数据结果表明,通入的氧气量为1556.8 kg,设反应消耗的氧气量为x kg3/2O2C11H14O2 M 31.99 178.23m x 6054.8 得x= 3/2×6054.8×31.99÷178.23=1630.1kg此时采用的空气分离氧气纯度可达99%,因此折合成通入的氧气为1630.1÷0.99=1646.6 kg即在反应过程中,需再连续通入1646.6kg氧气。
化工中物料衡算和热量衡算公式

化工中物料衡算和热量衡算公式一、物料衡算公式1.物料总量计算公式物料总量计算公式可以根据物质的密度(ρ)和体积(V)来计算。
公式如下:物料总量=密度×体积2.物料质量计算公式物料质量计算公式可以根据物质的密度(ρ)、体积(V)和物质的质量(m)之间的关系得出。
公式如下:质量=密度×体积3.物料浓度计算公式物料浓度计算公式可以根据溶质的质量(m)和溶液的体积(V)来计算。
公式如下:浓度=质量/体积4.溶液的重量和体积之间的关系溶液的重量可以根据溶液的密度(ρ)和溶液的体积(V)相乘得到。
公式如下:重量=密度×体积1.热量传递计算公式热量传递计算公式可以用于计算传热功率(Q)和传热面积(A)之间的关系。
公式如下:Q=h×A×ΔT其中,h为传热系数,ΔT为温差。
2.物料的热量计算公式物料的热量计算公式可以根据物料的质量(m)、比热容(Cp)和温度变化(ΔT)来计算。
公式如下:热量=质量×比热容×温度变化3.水的蒸发热计算公式水的蒸发热计算公式可以根据水的质量(m)和蒸发热(ΔHvap)来计算。
热量=质量×蒸发热三、补充说明1. 密度(ρ)是物质单位体积的质量,常用的单位有千克/立方米(kg/m^3)或克/立方厘米(g/cm^3)。
2. 比热容(Cp)是物质单位质量的热容量,表示单位质量物质温度升高1℃所需的热量,常用的单位是千焦/千克·℃(kJ/kg·°C)或焦/克·℃(J/g·°C)。
3.传热系数(h)是衡量热传导性能的参数,表示单位面积上的热量流入或流出的速率,常用的单位是瓦特/平方米·℃(W/m^2·°C)。
4.温度变化(ΔT)是物质的温度差,常用的单位是摄氏度(℃)或开尔文(K)。
5. 蒸发热(ΔHvap)是物质从液态转变为气态所需的热量,常用的单位是焦耳/克(J/g)或千焦/千克(kJ/kg)。
2化工设计概论第三章_物料衡算与能量衡算

2化工设计概论第三章_物料衡算与能量衡算物料衡算与能量衡算是化工设计中非常重要的内容,本文将从物料衡算和能量衡算两个方面进行介绍。
一、物料衡算物料衡算是指在化工生产过程中,对各种原料、中间体和产品的质量、数量和成分进行准确计算的过程。
物料衡算的目的是确定生产过程中各种物料的需求量,确保生产过程稳定和产品质量符合要求。
物料衡算的方法主要有质量衡算和量衡衡算两种。
质量衡算是以物料的质量为基础进行计算,通过分析反应进入和离开反应器的质量,计算物料的损失和转化率等。
量衡衡算是以物料的容积或重量为基础进行计算,通过对物料流动的速度、压力、体积和化学反应速率等参数的测量,来计算物料的数量和流动性。
物料衡算的具体步骤包括:确定物料流程图,定义物料的属性和流动参数,编写物料表,进行物料平衡方程的建立,计算各物料的需求量和产量等。
二、能量衡算能量衡算是指在化工生产过程中,对能量的输入、输出和损失进行准确计算和分析的过程。
能量衡算的目的是确保生产过程中的能量平衡和能源利用效率的提高。
能量衡算的方法主要有热平衡法和能量流平衡法两种。
热平衡法是基于热力学原理,通过测量和计算热量的流入和流出来进行能量衡算。
能量流平衡法是基于能量守恒原理,通过对能量流动的速度、温度和压力等参数的测量,来计算能量的输入和输出。
能量衡算的具体步骤包括:确定能量流程图,定义能量的属性和流动参数,编写能量表,进行能量平衡方程的建立,计算各能量的输入量和输出量等。
三、物料衡算和能量衡算的关系在进行物料衡算和能量衡算时,需要考虑以下几个方面:1.反应进程的热力学和动力学特性对物料和能量衡算有重要影响。
在确定衡算方法和参数时,需考虑反应的热效应和速率等因素。
2.物料的组成和性质对衡算结果有重要影响。
不同物料具有不同的热容量、蒸发潜热和燃烧热等参数,这些参数直接影响到能量衡算的结果。
3.流程设计和设备选择对衡算结果也有影响。
不同的流程和设备对物料流动的速度、压力和温度等参数有不同的要求,这些参数直接影响到物料和能量衡算的结果。
干燥过程中的物料衡算和热量衡算

干燥过程中的物料衡算和热量衡算
式中qmw——水分的蒸发量,kg水分/s qmc——绝干物料 的质量流量,kg绝干料/s L——绝干空气的消耗量,kg绝干气/s H1,H2——分别为空气进出干燥器时的湿度,kg/kg绝干气; X1,X2——分别为湿物料进出干燥器的干基含水量,kg水分/kg
q′m1,q′m2——分别为湿物料进出干燥器的流量,kg物料/s。
Q=Qp+QD=L(I2-I0)+qmc (I′2-I′1)+QL
(9-24) (9-25)
(9-26)
干燥过程中的物料衡算和热量衡算
式中H0,H1,H2——湿空气进入预热器、离开预热器(即进 入干燥器)及离开干燥器时的湿度,kg/kg
I0,I1,I2——分别为湿空气进入预热器、离开预热器(即进 入干燥器)及离开干燥器时的焓,kg/kg
干燥过程中的物料衡算和热量衡算
图9-8 各流股进出逆流干燥器的示意图
干燥过程中的物料衡算和热量衡算
(1)对预热器进行热量衡算
LI0+Qp=LI1
(9-23)
在预热器中,空气的状态变化是等湿升温过程,即H1=H0,故预热器
Qp=L(I1-I0)=L(1.01+1088H0)(t1-t0) (2
QD=L(I2-I1)+qmc (I′ 2-I′1)+QL (3
干燥过程中的物料衡算和热量衡算
一般干燥过程,湿空气中水汽的量(H0)相对于绝干空气来 说,数值较小,同时湿物料进入干燥器的温度偏低。若忽略空气 中水汽进出干燥系统的焓变1.88H(t2-t0)和湿物料中水分带入干 燥系统的焓4.18Wθ1,则Q=Qp+QD=1.01L(t2-t0)+qmcM (θ2θ1)+qmw (2490+1.88t2)+QL (9-29)
化工设计概论物料衡算与能量衡算

CH3OH HCHO
H2O N2
13
基准:1 mol CH3OH 根据反应方程式 O2(需要)= 0.5 mol;
O2(输入)= 1.5 × 0.5 = 0.75 mol; N2(输入)= N2(输出)= 0.75(79/21)= 2.82 mol CH3OH为限制反应物 反应的CH3OH = 0.75 × 1 = 0.75 mol 因此,HCHO(输出)= 0.75mol
17
二、能量衡算可以解决的问题
(4)为充分利用余热,必须采取有效措施,使过程的 总能耗降低到最低程度。为提高能量利用率,降 低能耗提供重要依据。
(5)最终确定总需求能量和能量的费用。
18
三、能量平衡方程式
能量衡算平衡方程式
△E = Q - W △E:表示体系能量总变化; Q: 表示体系从环境吸收的热量; W: 表示环境对体系所做的功。
100.0
15
§3.2 能量衡算
一、能量衡算定义
根据能量守恒定律,利用能量传递和转化 的规则,用以确定能量比例和能量转变的定量 关系的过程称为能量衡算。
16
二、能量衡算可以解决的问题
(1)确定物料输送机械和其它操作机械所需要的功率; (2)确定各单元操作过程所需热量或冷量,及其传递
速率;计算换热设备的工艺尺寸;确定加热剂或 冷却剂的消耗量,为其他专业如供汽、供冷、供 水专业提供设条件; (3)化学反应常伴有热效应,导致体系的温度上升或 下降,为此需确定为保持一定反应温度所需的移 出或加入的热传递速率;
19
四、热量衡算
1、热量衡算有两种情况: 1)对单元设备做热量衡算; 2)整个过程的热量衡算。
(当各个工序或单元操作之间有热量交换时, 必须做全过程的热量衡算。)
7.3干燥过程的物料衡算和热量衡算

预热器
G, t1 , H1
干 燥 器
废气
G, t2 , H2
产品 L2, w2 (X2), θ2
湿物料 L1, w1 (X1), θ1
连续干燥流程图
G ——干空气质量流量,kg干气/h L1、L2 ——物料进出干燥器总量,kg物料/h
2
一、绝干物料量LC
( kg干物料/h )
LC L1 (1 w 1 ) L2 (1 w 2 )
8
三、空气出口状态的确定方法 ——确定H2、I2 (1)计算法
W G ( H 2 H 1 ) LC ( X 1 X 2 )
( H 2 、 I2 )
QD G ( I 2 I1 ) LC ( I 2 ' I1 ' ) QL
I1 I2 B t1 D C =1
7.3 干燥过程的物料衡算和热量衡算
7.3.1 干燥过程的物料衡算 湿基含水量 w [kg水/kg湿物料]
湿物料中水分质量 w 湿物料总质量
干基含水量 X
[kg水/kg干物料]
湿物料中水分质量 X 湿物料中绝干物料质量
X 换算关系: w 1 X
w X 1 w
1
G, t0 , H0
预热(t0t1) :AB 干燥(t1t2) :
• 等焓过程:BD • 不等焓过程:BC
t2 t0
A
10
补充热量: QD G ( I 2 I1 ) LC ( I 2 ' I1 ' ) QL 外加热量: Q Q
P
Q
D
Q G ( I 2 I 0 ) LC ( I 2 ' I 1 ' ) Q L
《化工设计》 第三章物料衡算和热量衡算

对于没有化学反应的过程,一般上列写各组分的衡算方程, 只有涉及化学反应量,才列写出各元素的衡算方程。
• 稳态过程(连续),体系内无物料积累。
F
x f1
P
xp1
W
xw1
F
x f2
P xp2
W
xw2
7.将物料衡算结果列成输入-输出物料表(物料平 衡表),画出物料平衡图。
物料衡算表
组分
输入
质量,kg/d
组分
输出
质量,kg/d
杂质 合计
杂质 合计
8.校核计算结果(结论)。
五、无化学反应的物料衡算
• 在系统中,物料没有发生化学反应的过程, 称为无反应过程。
(三)、物料衡算基准 物料衡算过程,必须选择计算基准,并在整个运算
中保持一致。若基准选的好,可使计算变得简单。
①时间基准 (单位时间可取1d、1h或1s等等)。 ②批量基准; ③质量基准 例如: 可取某一基准物流的质量为100Kg
为基准计算。 ④物质的量基准; ⑤标准体积基准;
(四)、物料衡算的基本程序
100.00
解:
水F1 1200kg/h
吸 收 塔
混合气体F2,1.5 (mol)%丙酮
空气F3
蒸 馏 塔
冷凝器
废料F5:丙酮5%,
95% 水
产品F4 丙酮99%,水1%
本系统包括三个单元.即吸收塔、蒸馏塔和冷凝器。由于 除空气进料外的其余组成均是以质量百分数表示的,所以 将空气-丙酮混合气进料的摩尔百分数换算为质量百分数。 基准:100kmol气体进进料。
化工设计物料衡算与能量衡算

• 1.求燃料气组成以C作联系组分,燃烧前后碳原子数不 变,所以CO2mol数等于CH4的mol数,即CH4= 8.12mol,
• 需要氧气量为2×8.12=16.24mol。
• 计算进料的空气量,以N2作联系组分,由烟道气中的N2 可得进料中的总氧气量:72.28×20.92/79=19.14mol,
Φ=
×100%
限制组分的消耗量
(5) 收率
生成目的产物所消耗限制组分的量
η=
×100%
限制组分的输入量
η =xA· Φ
“独立”的含义
对有化学反应的过程,应写独立的反应方
程式或独立反应数。例如碳与氧的燃烧过
程 :C O2 CO2 ①
C
1 2
O2
CO
② ③
CO
1 2
O2
CO2
CO2 C 2CO
湿纸浆 浆: 0.29 水: 0.71
干燥器
干燥纸浆 浆:? 水:?
水分
• 例:每小时将20kmol含乙醇40%的酒精水溶液进 行精馏,要求馏出液中含乙醇89%,残液中含乙醇 不大于3%(以上均为摩尔分数),试求每小时馏出 液量和残液量。
• 解:由全塔物料衡算式可得
•
20 = D + W
(1)
• 20×0.4 = 0.89D + 0.03W
化工设计物料衡算与能 量衡算
2021年7月13日星期二
化工基础数据
化工计算以及化工工艺和设备设计中,要 用到有关化合物的物性数据。例如,进行化 工过程物料与能量衡算时,需要用到密度或 比容、沸点、蒸汽压、焓、热容及生成热等 等的物性数据;设计一个反应器时,则需要 知道化学反应热的数据;计算传热过程时, 需要导热系数的数据等等。
化工设计第3、4章物料衡算和能量衡算和过程模拟

输出: HCHO(输出)= 0.75mol; CH3OH(输出)= 1- 0.75 = 0.25mol; O2(输出)= 0.75- 0.75×0.5=0.375mol; H2O(输出)= 0.75mol
循环过程(两种解法)
1) 确定加热剂或冷却剂的消耗量; 2)为公用工程(热工、电、锅炉、给水、冷暖)提供设计条件; 3) 为提高能量利用率,降低能耗提供重要依据; 4)确定总需求能量和能量的费用。
热量衡算步骤
(1)以单位时间为基准的物料流程图,确定热量平衡范围; (2)在物料流程图上标明已知温度、压力、相态等已知条件; (3)选定计算基准温度; (4)列出热量衡算式,求解未知值; (5)整理并校核计算结果,列出热量平衡表。
F1=2000kg/h 75%液体 25%固体
过滤机
滤饼 90%固体 F3=?kg/h 10%液体
F2=?kg/h 1%固体 99%液体
滤液
精馏过程
F3
F1 料液 乙醇 40% 水 60%
馏出液
乙醇=1% 水 24% 苯 75%
F2 苯
乙醇产品 F4=1000kg/h
化学反应过程的物料衡算
1.直接计算法
化工工程设计中需要大量的时间查找、筛选和估算物性数据。 衡算时必须有足够而准确的原始数据。原始数据的来源根据计算 性质而不同。 对于设计一个新的工艺过程,有关数据可由实验室试验或中试提 供,对于生产过程,则由生产装置测定而得到。当某些数据不能精确 测定或缺少时,可在工程设计计算所允许的范围内推算或假设。
过程模拟简介
过程模拟类型 模拟型、设计型、优化型
过程模拟的三要素 系统模型、物性数据和热力学方法、算法
干燥过程的物料衡算和热量衡算

第三节 干燥过程的物料衡算和热量衡算对干燥流程的设计中,物料衡算解决的问题:(1)物料气化的水分量W (或称为空气带走的水分量);(2)空气的消耗量(包括绝干气消耗量L 和新鲜空气消耗量L 0)。
而热量衡算的目的,是计算干燥流程的热能耗用量及各项热量分配(即预热器换热量pQ ,干燥器供热量D Q 及干燥器热损失L Q )。
一、湿物料中含水率表示法湿物料=水分+绝干物料 (一)湿基含水量w%100⨯=总质量水m m w (8-12)工业上常用这种方法表示湿物料的含水量。
(二)干基含水量XX =湿物料中水分质量/湿物料中绝干料质量 (8-13) 式中 X ――湿物料的干基含水量,kg 水分.(kg 绝干料)-1。
两者关系:X Xw +=1 (8-14)或w wX -=1 (8-15)二、干燥器的物料衡算图8-7 各流股进、出逆流干燥器的示意图图8-7中,G ――绝干物料流量,kg 绝干料.s -1; L ――绝干空气消耗量,kg 绝干气.s -1;H 1 ,H 2――分别为湿空气进、出干燥器时的湿度,kg.(kg 绝干气)-1; G 1 ,G 2――分别为湿物料进、出干燥器时的流量,kg 湿物料.s -1; X 1 ,X 2――分别为湿物料进、出干燥器时的干基含水量,kg 水分.(kg 绝干料)-1。
(一)水分蒸发量W)()(122121H H L G G X X G W -=-=-= (8-16) 其中)1()1(2211w G w G G -=-= (8-17)(二)空气消耗量L对干燥器作水分物料衡算:2211GX LH GX LH +=+ 则:()121221H H WH H X X G L -=--=(8-18)若设:121H H WLl -== (8-19)式中 l ――每蒸发1kg 水分消耗的绝干空气量,称为单位空气消耗量,kg 绝干气.(kg 水分)-1;L ――单位时间内消耗的绝干空气量,kg 绝干气.s -1。
物料衡算和热量衡算

物料衡算和热量衡算在化工生产过程中,原料、水、电、蒸汽消耗量、主副产品产量等,都是十分重要的工艺指标。
为了得到这些数值,衡量生产过程的先进性,需要进行生产过程中局部的或全过程的物料衡算和热量衡算。
第一节物料衡算一、物料衡算及其分类物料衡算是根据质量守恒定律,对化工过程中的各股物料进行分析和定量计算,以确定它们的数量、组成和相互比例关系,并确定它们在物理变化或化学变化过程中相互转移或转化的定量关系的过程。
通过物料衡算计算转化率、选择性,筛选催化剂、确定最佳工艺条件,对装置的生产情况做出分析,判断装置是否处于最佳运转状态,为强化生产过程提供依据和途径。
因此,物料衡算是化工科研、设计、生产及其它工艺计算、设备计算的基础。
物料衡算按其衡算范围,有单元操作(或单个设备)的物料衡算与全流程(即包括各个单元操作的全套装置)的物料衡算;按其操作方式,有连续操作的物料衡算与间歇操作的物料衡算;按有无反应过程,有无化学反应过程的物料衡算与有化学反应过程的物料衡算;此外,还有带循环的化工过程的物料衡算。
物料衡算的计算一般分为两种情况。
一种是在已有的装置上,对一个车间、一个工段、一个设备或几个设备,利用实际测定的数据(或理论计算数据),算出另外一些不能直接测定的物料量,由此,对这个装置的生产情况作出分析,找出问题,为改进生产提出措施。
另一种是对新车间、新工段、新设备作出设计,即利用本厂或别的工厂已有的生产实际数据(或理论计算数据),在已知生产任务下算出需要原料量,副产品生成量和三废的生成量,或在已知原料量的情况下算出产品,副产品和三废的量。
二、物料衡算的依据和衡算范围物料衡算的理论依据是质量守恒定律,即在一个孤立的系统中,不论物质发生任何变化,其质量始终不变。
质量守恒定律是对总质量而言的,它既不是一种组分的质量,也不是指体系的总摩尔数或某一组分的摩尔数。
在化学反应过程中,体系中组分的质量和摩尔数发生变化,而且在很多情况下总摩尔数也发生变化,只有总质量是不变的。
物料衡算与热量衡算的方法

物料衡算与热量衡算的方法由于物料衡算与热量衡算是化工设计的基础,是生产中检查考核、定额分析的重要手段,也是本课程中化工计算的基础,因此,在进入后几章的学习之前,必须把物、热衡算的方法搞清楚。
一、物料衡算的具体作法对于连续稳定过程,物料衡算的方程是:ΣMλ=ΣM出或进 = 出为代数方程对不稳定过程,物料衡算的方程为:ΣMλ=ΣM出+M累积或进 = 出 + 累积为代数方程在本书的范围之内,绝大多数情况为连续稳定过程,故将重点讨论这种情况。
一般情况下,物料衡算的步骤如下:首先,确定衡算对象,根据题目要求它可以是总物料、某个组分、某个元素等;其次,确定衡算范围,根据题目要求它可以是一个系统、一个车间、某个设备;设备的某个局部等……;最后,确定衡算基准,根据题目要求它可以是单位质量,单位时间等。
在上述三者确定后,根据物料衡算方程分别列出具体的物料衡算方程(一个或多个),再解方程或方程组即可。
现举例如下:例1-1 如图1-2A所示,浓度为20%(质量百分数,下同)的KNO3水溶液以1000kg/hr流量送入蒸发器,在某温度下蒸出一部分水而得到浓度为50%的KNO3水溶液,再送入结晶器冷却析出含有4%水分的KNO3晶体并不断取走。
浓度为37.5%的KNO3饱和母液则返回蒸发器循环处理,该过程为连续稳定过程,试求:1. 结晶产品量P,水分蒸发量W;2. 循环母液量R,浓缩量S。
图1-2A解: 1. 衡算对象:总物料KNO3衡算范围:如图所示的用一条封闭的虚线所包围的部分衡算基准:单位时间--每小时列方程:凡是穿过封闭虚线进入的衡算范围的物料为入;凡是穿出封闭虚线排出的衡算范围的物料为出;总物料ΣMλ=ΣM出则 F = W + P (1)同理,对KNO30.2F = 0×W + P(1-4%)(2)将(1)(2)代入数据后组成方程组1000 = W + P0.2×1000 = P(1-4%)解这个方程组得:P = 208.3 kg/hrW = 791.7 kg/hr2. 衡算对象的基准不变,改变衡算范围如图1-2B所示。
干燥过程的物料衡算和热量衡算.

图7-8 各物流进出逆流干燥器的示意图第三节 干燥过程的物料衡算和热量衡算对流干燥过程利用不饱和热空气除去湿物料中的水分,所以常温下的空气通常先通过预热器加热至一定温度后再进入干燥器.在干燥器中热空气和湿物料接触,使湿物料表面的水分气化并将水气带走.在设计干燥器前,通常已知湿物料的处理量、湿物料在干燥前后的含水量及进入干燥器的湿空气的初始状态,要求计算水分蒸发量、空气用量以及干燥过程所需热量,为此需对干燥器作物料衡算和热量衡算,以便选择适宜型号的风机和换热器。
7-3-1 物料中含水量的表示方法1.湿基含水量 湿物料中所含水分的质量分率称为湿物料的湿基含水量。
湿物料总质量湿物料中水分的质量=w (7-21)2.干基含水量 不含水分的物料通常称为绝对干料或干料。
湿物料中水分的质量与绝对干料质量之比,称为湿物料的干基含水量. 量湿物料中绝对干物料质湿物料中水分的质量=X (7—22) 上述两种含水量之间的换算关系如下: ww X -=1 kg 水/kg 干物料XX w +=1 kg 水/kg 湿物料 (7—23)工业生产中,通常用湿基含水量来表示物料中水分的多少.但在干燥器的物料衡算中,由于干燥过程中湿物料的质量不断变化,而绝对干物料质量不变,故采用干基含水量计算较为方便。
7—3—2 干燥器的物料衡算通过物料衡算可求出干燥产品流量、物料的水分蒸发量和空气消耗量.对图7-8所示的连续干燥器作物料衡算。
设 G 1——进入干燥器的湿物料质量流量,kg/s ;G 2-—出干燥器的产品质量流量,kg/s ; G c ——湿物料中绝对干料质量流量,kg/s ;w 1,w 2—-干燥前后物料的湿基含水量,kg 水/kg 湿物料; X 1,X 2——干燥前后物料的干基含水量,kg 水/kg 干物料; H 1,H 2——进出干燥器的湿空气的湿度,kg 水/kg 绝干空气; W -—水分蒸发量,kg/s ;L —-湿空气中绝干空气的质量流量,kg/s 。
化工中物料衡算和热量衡算公式

化工中物料衡算和热量衡算公式物料衡算和热量衡算物料衡算根据质量守恒定律,以生产过程或生产单元设备为研究对象,对其进出口处进行定量计算,称为物料衡算。
通过物料衡算可以计算原料与产品间的定量转变关系,以及计算各种原料的消耗量,各种中间产品、副产品的产量、损耗量及组成。
物料衡算的基础物料衡算的基础是物质的质量守恒定律,即进入一个系统的全部物料量必等于离开系统的全部物料量,再加上过程中的损失量和在系统中的积累量。
∑G1=∑G2+∑G3+∑G4∑G2:--输人物料量总和;∑G3:--输出物料量总和;∑G4:--物料损失量总和;∑G5:--物料积累量总和。
当系统内物料积累量为零时,上式可以写成:∑G1=∑G2+∑G3物料衡算是所有工艺计算的基础,通过物料衡算可确定设备容积、台数、主要尺寸,同时可进行热量衡算、管路尺寸计算等。
物料衡算的基准(1)对于间歇式操作的过程,常采用一批原料为基准进行计算。
(2)对于连续式操作的过程,可以采用单位时间产品数量或原料量为基准进行计算。
物料衡算的结果应列成原材料消耗定额及消耗量表。
消耗定额是指每吨产品或以一定量的产品(如每千克针剂、每万片药片等)所消耗的原材料量;而消耗量是指以每年或每日等时间所消耗的原材料量。
制剂车间的消耗定额及消耗量计算时应把原料、辅料及主要包装材料一起算入。
热量衡算制药生产过程中包含有化学过程和物理过程,往往伴随着能量变化,因此必须进行能量衡算。
又因生产中一般无轴功存在或轴功相对来讲影响较小,因此能量衡算实质上是热量衡算。
生产过程中产生的热量或冷量会使物料温度上升或下降,为了保证生产过程在一定温度下进行,则外界须对生产系统有热量的加入或排除。
通过热量衡算,对需加热或冷却设备进行热量计算,可以确定加热或冷却介质的用量,以及设备所需传递的热量。
热量衡算的基础热量衡算按能量守恒定律\在无轴功条件下,进入系统的热量与离开热量应该平衡\,在实际中对传热设备的衡算可由下式表示Q1+Q2+Q3=Q4+Q5+Q6(1-1)式中:Q1-所处理的物料带入设备总的热量,KJ;Q2-加热剂或冷却剂与设备和物料传递的热量(符号规定加热剂加入热量为\,冷却剂吸收热量为\),KJ;Q3-过程的热效率,(符号规定过程放热为\;过程吸热为\)Q4-反应终了时物料的焓(输出反应器的物料的焓)Q5-设备部件所消耗的热量,KJ;Q6-设备向四周散失的热量,又称热损失,KJ;热量衡算的基准可与物料衡算相同,即对间歇生产可以以每日或每批处理物料基准。
物料衡算及热量衡算
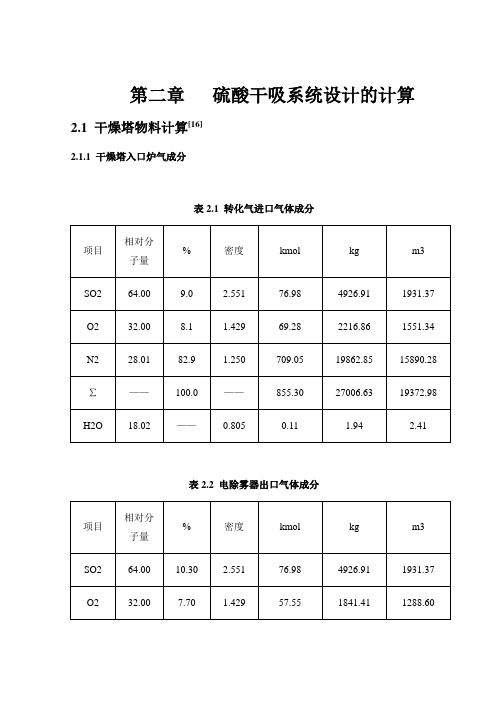
第二章硫酸干吸系统设计的计算2.1 干燥塔物料计算[16]2.1.1 干燥塔入口炉气成分表2.1 转化气进口气体成分表2.2 电除雾器出口气体成分2419.052.1.2 干燥塔入口炉气含水量设补加空气全部在电除雾器之后加入,空气温度20摄氏度、相对湿度75%,由湿含图查得水含量为103干空气,则补加空气带水量为:g/m2419.05×0.01=24.19kg/h=1.34kmol/h=30.8m3/h2.1.3 干燥塔入口气体带水设出塔气体中含水量为30.1g/m,则干燥后气体带水量为:(0.1÷1000)×19372.98=1.94kg/h2.1.4 循环酸量决定循环酸量的方法一般有两种,一种是根据进出口酸浓度差决定,酸浓度差一般选在0.2%~0.4%范围内,第二个是根据塔的喷淋密度来决定,喷淋密度一般选在14~20m3/(m2·h)的范围内。
在这里采用浓度差计算循环酸量。
H SO比重 1.7993入塔酸:浓度93.00%24m/h温度50O C 酸量x3出塔酸:浓度92.7%干燥塔吸收水量=(1115.81+24.19)-1.94=1138.06kg/h由物料平衡得:X×1.7993×1000×93%=(X×1.7993×1000+1146)×92.7%X=195.44m3/h所以采用扬量为200m3/h酸泵,型号为IHIHF125-100-250酸泵。
2.2 干燥塔热量衡算2.2.1 炉气带入热量Q1t=40O C时SO2带入热量:q1=76.98×40×41.57=127997.80KJ/hO2带入热量:q2=69.28×40×29.37=81389.60KJ/hN 2带入热量: q 3=709.05×40×28.45=806894.52KJ/hH 2O 带入热量: q 4=(1.34+61.94)×40×32.716=82810.74KJ/h式中41.57,29.37,28.45,32.716分别为0~40O C 时SO 2、O 2、N 2、H 2O 的摩尔热熔KJ/(mol·K) 。
化工设计之物料衡算及热量衡算

化工设计之物料衡算及热量衡算化工设计中的物料衡算和热量衡算是非常重要的步骤,可以帮助工程师确定所需的原料数量和能源消耗。
本文将讨论物料衡算和热量衡算的原理、方法和应用。
一、物料衡算物料衡算是指根据化工过程的原理和条件,计算出所需原料的数量。
1.原料衡算的原理在化工过程中,根据反应式、反应的平衡常数、物料的摩尔平衡和原料的纯度等信息,可以得出原料的物质平衡方程。
2.原料衡算的方法(1)平衡更新法:根据反应式及其他物质平衡方程,利用线性方程组求解方法,逐步逼近平衡条件,得出原料数量的近似解。
(2)摩尔关系法:利用反应的摩尔比例来计算原料的摩尔数量。
根据反应的平衡常数和其他物质平衡方程,可以得到原料的摩尔数量。
3.原料衡算的应用物料衡算在化工过程中有广泛的应用。
例如,在合成反应中,根据反应需求,确定所需原料的摩尔数量;在萃取过程中,根据溶剂和溶质的摩尔比例,计算溶液中的溶质浓度。
二、热量衡算热量衡算是指根据化工过程的热力学原理和条件,计算出所需的能量消耗。
1.热量衡算的原理根据热力学定律,可以计算化学反应的焓变,并以此来确定反应所需的热量。
热量衡算也需要考虑其他因素,如物料的温度、压力变化等。
2.热量衡算的方法(1)焓变法:根据反应的焓变和反应的摩尔比例,计算出反应所需的热量。
焓变可以通过实验测量或热力学数据库来获取。
(2)能量平衡法:考虑物料流动和热交换等因素,通过能量平衡方程求解,计算出能量的输入和输出。
3.热量衡算的应用热量衡算在化工过程中的应用非常广泛。
例如,在高温燃烧反应中,需要计算反应所需的燃料气体的热量;在蒸汽发生器中,需要计算蒸汽的产生量和燃料的热量供应。
物料衡算和热量衡算是化工设计中不可或缺的两个步骤,可以帮助工程师确定原料的用量和能量消耗,从而优化过程设计、提高生产效率和节约能源。
在进行衡算时,需要准确地获取物料的性质数据,合理地选择计算方法,并考虑到实际操作条件的变化,以保证设计结果的可靠性和实用性。
干燥过程的物料衡算与热量衡算

干燥过程的物料衡算与热量衡算1. 引言在工业生产中,许多物料需要经过干燥过程才能达到所需的水分含量。
干燥过程是将物料中的水分蒸发或驱除的过程,其中物料的衡算和热量的衡算是非常重要的。
本文将介绍干燥过程中的物料衡算和热量衡算的基本原理和方法。
2. 物料衡算物料衡算是指在干燥过程中对物料的质量进行衡量和追踪的过程。
通常情况下,物料的衡算可以分为进料衡算和出料衡算两个部分。
2.1 进料衡算在干燥过程中,物料的进料衡算是指对进入干燥设备的物料进行质量的测量和记录。
通常情况下,进料衡算可以通过称重装置、质量流量计等设备进行。
物料的进料衡算可以用以下公式表示:进料量 = 初始物料质量 - 终止物料质量2.2 出料衡算在干燥过程中,物料的出料衡算是指对从干燥设备中出来的物料进行质量的测量和记录。
同样地,出料衡算也可以通过称重装置、质量流量计等设备进行。
物料的出料衡算可以用以下公式表示:出料量 = 初始物料质量 - 终止物料质量3. 热量衡算热量衡算是指在干燥过程中对热量的衡量和追踪的过程。
热量衡算是确定干燥设备所需的热量输入和物料中的水分蒸发所需的热量的关键。
3.1 热量平衡公式热量平衡公式是用于计算干燥过程中所需的热量输入和物料中的水分蒸发所需的热量的关系。
热量平衡公式如下:热量输入 = 热量输出 + 热量损失其中,热量输入是指干燥设备所需的热量输入,热量输出是指物料中的水分蒸发所需的热量,热量损失是指在干燥过程中因为传导、对流和辐射等现象导致的热量损失。
3.2 热量输入的计算热量输入可以通过以下公式计算:热量输入 = 干燥空气的热量 + 干燥空气的水分蒸发热量 + 加热设备的热量其中,干燥空气的热量可以通过湿空气焓值表或湿空气定压比热容表进行查找,干燥空气的水分蒸发热量可以通过水的蒸发热量进行计算,加热设备的热量可以通过加热元件的功率和加热时间进行计算。
3.3 热量输出的计算热量输出可以通过以下公式计算:热量输出 = 出料量 * 物料的比热 * (物料的初始水分含量 - 物料的终止水分含量)其中,出料量是指干燥过程中物料的出料量,物料的比热可以通过物料的物性表进行查找,物料的初始水分含量和物料的终止水分含量可以通过物料的质量衡算进行计算。
物料衡算和热量衡算

物料衡算和热量衡算以下计算部分将对石灰石-石膏法的脱硫工艺进行物料衡算、热量衡算、反应器的设计和换热器的设计等具体的步骤物料衡算简化运算条件:物料衡算主要针对脱硫装置系统(即喷淋塔)和制浆系统(石灰石浆液)来进行的,两个系统之间来联系的纽带是在脱硫塔内进行的脱硫反应,即钙硫比(Ca/S )(选择为1.02,下面将详细论述)。
以下条件在计算方法中被简化(1)不包括吸收塔的损失(2)假设烟气带入的粉尘为零(3)假设工艺水和石灰石不含杂质(4)假设原烟气和净烟气没有夹带物代入和带出系统(5)假设没有除雾器冲洗水(6)假设没有泵的密封水(7)假设工艺系统是封闭的,没有环境物质的进入和流出3.1吸收系统物料衡算和相关配置喷淋塔内主要进行脱硫反应,由锅炉引风压机引来的烟气,经过增压风机升压后,从吸收塔中下部进入吸收塔,脱硫除雾后的净烟气从吸收塔顶部侧向离开吸收塔,塔的下部为浆液池。
前面已经详细地介绍了脱硫反应的机理,由此可知反应的物料比例为 CaCO 3∽Ca ∽1.02S ∽1.02SO 21.02 : 1.02 : 1 : 1设原来烟气二氧化硫SO 2质量浓度为 a (mg/m 3),根据理想气体状态方程PV=nRT可得: K K ma m g m mg )145273(273//770033+= 求得: a=1.18×104mg/m 4而原来烟气的流量(145℃时)为20×104(m 3/h)换算成标准状态时(设为V a )KK V h m a 273)273145(/2000003+= 求得 V a =1.31×105 m 3/h=36.30 m 3/s故在标准状态下、单位时间内每立方米烟气中含有二氧化硫质量为M SO2 =36.30×1.18×104mg/m 3=42.83×104mg=428.3g/s N SO2=428.3/64 mol/s = 6.69mol/s ≈7.0mol/s对应的石灰石(CaCO 3)物质的量 n CaCO3=1.02×7.0 =7.14mol/s石灰石(CaCO 3)质量为m CaCO3=1.02×7.0×100 =1.02×700g/s=714g/s综合以上计算结果,本部分给出的是一些近似的简化物料平衡计算方法,物料点涵盖了一些主流程。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
联合干燥。
在工业上应用最普遍的是对流干燥。通常使用的干燥介质是
空气,被除去的湿分是水分。空气既是载热体又是载湿体。
物料的干燥过程是属于传热和传质相结合的过程。 干燥过程进行的条件:被干燥物料表面所产生水汽(或其
它蒸汽)的压力大于干燥介质中水汽(或其它蒸汽)的分压,
由于水的饱和蒸气压仅与温度有关,故湿空气的饱和湿 度是温度和总压的函数,即
H s f (t , P )
3 相对湿度 φ
在一定温度及总压下,湿空气的水汽分压pv 与同温度下
水的饱和蒸汽压 pS 之比的百分数,称为相对湿度(relative humidity),用符号φ表示,即
pv ps 100 %
当空气的干球温度t不变时,I与H成直线关系,故在I-H图中 对应不同的t,可作出许多等t线。 各种不同温度的等温线,其 斜率为(1.88t+2492),故温度愈高,其斜率愈大。因此,这许多 成直线的等t线并不是互相平行的。
4 等相对温度线(等φ线)
H 0 . 622
ps
P ps
当湿空气的湿度H为一定值时,温度愈高,其相对湿度φ值 愈低,即其作为干燥介质时,吸收水汽的能力愈强,故湿空气 进入干燥器之前必须经过预热器预热提高温度,目的除了提高 湿空气的焓值使其作为载热体外,也是为了降低其相对湿度而 作为载湿体。 5 水蒸汽分压线
塔顶和塔底处湿空气的焓分别为:
I 1 ( c g Hc v ) t Hr 0
0
I 2 ( c g H as c v ) t as H as r0
0
湿空气在绝热增湿过程中为等焓过程,即:I1=I2 由于H和Has值与l相比皆为一很小的数值,故可视为CH 、 CHas不随湿度而变,即CH=CHas 。则有
A
φ=1
凝结出来的水分设法除去,
再将所得的饱和空气加热, 则不会恢复原来的状态,而 空气的湿度小于原空气的湿 度,即达到减湿的目的。
B
HB
HA
H
3 不同状态空气的混合
设有状态不同的空气1和2,对应的干空气的量为G1和G2, 对应的状态为(H1,I1),(H2,I2)。两空气混合后,由物 料衡算和热量衡算,可求得
I=122kJ/kg干空气
td=24oC tw=33o C
三、湿空气的基本状态变化过程
1 间壁式加热和冷却
若空气的温度变化范围在露点以上,则空气中的含水量始终 保持不变,且为不饱和状态,为等湿过程,过程线为垂直线。 I tB tA A B A
tA
B tB φ=1
H
2 间壁式冷却减湿
上述间壁式冷却过程当进行至露点,空气即达到饱和状态, 继续冷却时,水蒸气就在冷却壁面上凝结出来,而且温度不断 降低,但空气始终在饱和状态。 I 利用上述方法,如果将
t as t
r0
0
(H
cH
as
H)
实验测定表明,对于在湍流状态下的空气-水蒸气系统 而言,a/kH≈ CH , 同时 r00≈ rtw,故在一定温度t和湿度H下, 有
t w t as
强调:绝热饱和温度tas与湿球温度tw是两个完全不的概念。
但是两者都是湿空气状态(t和H)的函数。特别是对空气-水
o 式中 cH——湿空气的比热, kJ/(㎏绝干气·C); o cg——绝干空气的比热, kJ/(㎏绝干气·C); o cv——水气的比热, kJ/(㎏水气·C)
在常用的温度范围内,有
c H 1 . 01 1 . 88 H
上式说明:湿空气的比热只是湿度的函数。
5 湿空气的焓 I
湿空气中1kg绝干空气的焓与相应水汽的焓之和,称为湿 空气的焓,用符号I表示,单位是kJ/kg干空气。
在一定总压和温度下,两者之间的关系为
H 0 . 622
ps
P ps
4 湿空气的比热CH
在常压下,将湿空气中1kg绝干空气及相应Hkg 水汽的温度
升高(或降低)1oC所需要(或放出)的热量,称为比热,又
o 称为湿热,用符号CH表示,单位是kJ/(㎏绝干气·C),即
c H c g Hc v
I=Ig+IvH
式中I——湿空气的焓,kJ/kg绝干气; Ig ——绝干空气的焓,kJ/kg绝干气; Iv——水气的焓,kJ/kg水气。 注:空气的焓是根据干空气及液态水在0 oC时焓为零作基准而计算的, 因此,对于温度为t 及湿度为H的湿空气,其焓包括由0o C的水变为0o C 的水汽所需的潜热及湿空气由0oC升温至t oC所需的显热之和,即
物理化学去湿法:用吸湿性物料如石灰、无水氯化钙等吸
收水分。该法费用高,操作麻烦,只适用于小批量固体物料 的去湿,或用于除去气体中的水分。
热能去湿法:如蒸发、干燥等
用加热的方法使水分或其它溶剂汽化,并将产生的蒸气排 除,藉此来除去固体物料中湿分的操作,称为固体的干燥。
干燥过程的分类
按操作压力:常压干燥、真空干燥 按操作方式:连续式、间歇式 按传热方式:传导干燥、对流干燥、辐射干燥和
压差越大,干燥过程进行越快。所以干燥介质须及时将汽化 的水汽带走,以保持一定的汽化水的推动力。
第二节
湿空气的性质及湿度图
一、湿空气的性质
1 水蒸气分压pv
空气中水蒸气分压愈大,水分含量就愈高,根据气体分 压定律,则有 pv pv nv
pg P pv ng
2 湿度(humidity)H
又称为湿含量或绝对温度(absolute humidity)。它以湿空 气中所含水蒸汽的质量与绝对干空气的质量之比表示,使用 符号H,其单位为:kg水气/kg干空气 。
A
A
3
φ=1
t 1 2 td
3
φ=1
t 1 0
φ=1
0
H
0
H
H
例: 已知湿空气的总压为101.3kN/m2 , 湿度为H=0.02 kg水/kg 干空气,干球温度为70o C。试用I-H图求解:
(a)水蒸汽分压p; (b)相对湿度φ ; (c)热焓I; (d)露点td ;
(e)湿球温度tw ;
解 由已知条件:P=101.3kN/m2, H=0.02 kg水/kg干空气, t=20o C,在I-H图上定出湿空气的状态点A点。 pv=3kN/m2 φ=10%
当pv=0时,φ=0,表示湿空气不含水分,即为绝干空气。 当pv=ps时,φ=1,表示湿空气为饱和空气。
相对湿度和绝对湿度的关系
相对湿度:可以说明湿空气偏离饱和空气的程度,能用
于判定该湿空气能否作为干燥介质,φ值与越小,则吸湿
能力越大。
湿度:是湿空气含水量的绝对值,不能用于分辨湿空气
的吸湿能力。
第八章 物料干燥
重点:空气的焓湿图、干燥机理、干燥
曲线、干燥时间的计算;
难点:空气的焓湿图、干燥机理;
干燥设备交流论坛:
第一节
过程。
概述
去湿:除去物料中的水分和或其它溶剂(统称为湿分)的
去湿的方法:
机械去湿法:即通过过滤、压榨、抽吸和离心分离等方法
除去湿分。
vH m 绝干气 m 水气
3 3
kg 绝干气
273 t 273 273 t 273 1 . 013 10 P 1 . 013 10 P
5 5
vH (
1 29
H 18
) 22 . 4
( 0 . 772 1 . 244 H ) 22 . 4
7 露点 td
当空气从露点继续冷却时,其中部分水蒸汽便会以露珠的 形式凝结出来。空气的总压一定,露点时的饱和水蒸汽压ps,td 仅与空气的湿度Hs,td有关,即 ps,td=f(Hs,td) 或 度越大,td 越大。 td= (Hs,td) 湿
8 干球温度t和湿球温度tw
干球温度t:空气的温度 湿球温度tw: 不饱和空气的湿球温度tw低于干球温度t。 形成原理(如图所示): tw
气系统,两者在数值上近似相等,对其他系统而言,不存在 此关系。
对空气-水蒸气系统 ,干球温度、绝热饱和温度(或湿
球温度)及露点之间的关系为:
对于不饱和湿空气: t>tas(或tw)>td 对于饱和的湿空气: t= tas(或tw)
=td
二、湿空气的湿度图
在工程计算中,常用的是以湿空气的焓值I为纵坐标,湿度
Hn G1 H 1 G 2 H 2 G1 G 2 In G1 I1 G 2 I 2 G1 G 2
I
I1
1
In
I2
2
H2 4
I H Hn 1 e t d 3
φ=1
H
若混合后的空气状态点落 入超饱和区,例如图中3-4 直线上的d点,则混合物将 分成气态的饱和空气和液态 的水两部分,前者的状态点 为过d点的等温线与φ=1线 的交点e。
补充液,温度tw
空气 湿度H 温度t
在稳定状态时,空气向湿纱布表面的传热速率为: Q=αS(t-tw)
气膜中水气向空气的传递速率为:N=kH(Hs,tw-H)S
在稳定状态下,穿热速率和传质速率之间的关系为:Q=Nrtw
tw t
k H rtw
( H s , tw H )
对空气~水蒸气系统而言, α/kH=1.09
形成原理: 绝热降温增湿过程及等焓过程 饱和,则空气的温度不再下降,
而等于循环水的温度,称此温度为 该空气的绝热饱和温度,用符号tas 表示,其对应的饱和湿度为Has,此 刻水的温度亦为tas。 tas
水
空气 t,H,I1
补充水 tas
在空气绝热增湿过程中,空气失去的是显热,而得到的是汽 化水带来的潜热,空气的温度和湿度虽随过程的进行而变化, 但其焓值不变。
