法国进口药品
进口药品国内总代理企业名称

吸入用七氟烷(奇弗美)
250ml
Hospira Australia Pty Ltd(澳大利亚)
紫杉醇注射液(安素泰)
5ml:30mg
Gedeon Richter Plc(匈牙利)
门冬氨酸钾镁注射液(潘南金)
10ml:400mg无水门冬氨酸镁和452mg无水门冬氨酸钾
Allergan Pharmaceuticals Ireland(爱尔兰)
注射用A型肉毒毒素(保妥适)
50单位/支
Allergan Pharmaceuticals Ireland(爱尔兰)
注射用A型肉毒毒素(保妥适)
100单位/支
日东电工株式会社东北事业所
妥洛特罗贴剂(阿米迪)
0.5mg/贴
日东电工株式会社东北事业所
妥洛特罗贴剂(阿米迪)
1mg/贴
日东电工株式会社东北事业所
妥洛特罗贴剂(阿米迪)
2mg/贴
Kowa Company,Ltd.,Nagoya Factory(日本)
匹伐他汀钙片(力清之)
2mg
Kowa Company,Ltd.,Nagoya Factory(日本)
匹伐他汀钙片
4mg
RECIPHARM FONTAINE(法国)
进口药品国内总代理企业名称
序号企业名称Fra bibliotek生产企业代理产品
规格
备注
1
益普生(天津)医药商贸有限公司
Beaufour Ipsen Industrie(法国)
银杏叶片(达纳康)
40mg*15片,30片/盒
Beaufour Ipsen Industrie(法国)
阿米三嗪萝巴新片商品名都可喜-国家药品不良反应监测中心

阿米三嗪萝巴新片临床疗效再评价相关情况介绍1.阿米三嗪萝巴新片的基本情况如何?阿米三嗪萝巴新片由法国施维雅公司研制,商品名为“都可喜(Duxil)”,于1978年在法国首次注册,随后在全球55个国家上市。
阿米三嗪萝巴新片于1988年8月在我国首次获得进口许可。
2005年5月,施维雅(天津)制药有限公司获准在国内生产阿米三嗪萝巴新片(国药准字H20054931)。
阿米三嗪萝巴新片的适应症为“治疗老年人认知和慢性感觉神经损害的有关症状(不包括阿尔茨海默病和其他类型的痴呆);血管源性视觉损害和视野障碍的辅助治疗;血管源性听觉损害、眩晕和/或耳鸣的辅助治疗。
”该药品的不良反应有:体重减轻,周围神经病变;恶心、上腹部沉闷或烧灼感、消化不良、排空障碍;失眠、嗜睡、激动、焦虑、头晕;心悸。
另外,我国有两家企业生产复方阿米三嗪片,其有效成分组成与阿米三嗪萝巴新片相同,这两家企业分别为常州制药厂有限公司和南阳普康集团衡淯制药有限公司,首次获批时间分别为1997年2月(国药准字H10970117)和2000年1月(国药准字H20000060)。
2.阿米三嗪萝巴新片为何在法国撤市?法国卫生安全和健康产品局(AFSSAPS)在重新评价血管扩张剂的风险效益比后,认为阿米三嗪萝巴新片在治疗已批准的三个适应症方面疗效证据不充分,该药有少见的外周神经病变及体重减轻的副作用,要求法国施维雅药厂按照新的疗效评价标准提交相关临床研究证据。
法国施维雅药厂从企业发展策略及经济角度考虑,不愿再对都可喜进行新的临床试验,随后主动在法国市场撤出该产品。
基于法国施维雅药厂的决定,AFSSAPS撤销阿米三嗪萝巴新片的法国市场授权许可证,该决定于2005年9月28日生效。
3.目前阿米三嗪萝巴新片在国际市场的生产与销售情况如何?法国施维雅药厂主动在法国市场撤出阿米三嗪萝巴新片后,也停止了向海外其它国家的出口,因此从法国进口该药品的国家陆续停止了阿米三嗪萝巴新片的销售。
法国进口市场分析及中国产品出口策略

法国进口市场分析及中国产品出口策略法国作为西欧经济强国之一,商品经济十分发达,是一个具有强大发展潜力的消费市场。
同时法国也是一个进口大国,目前其自国际市场上进口的大宗产品主要为:汽车及其配件和汽车设备、石油、天然气、煤炭、有色金属矿产品、办公用电脑和信息设备、有机化工品、药品、航空和宇航制造业用品、食品、服装、电气设备、钢材、机械设备、种植和养殖业产品、塑料、有色金属、普通机器、以及电子元件等产品。
一、中国产品出口法国的总体现状在中法两国政府和经贸企业界的共同努力下,中法两国在商贸、核能、金融保险和信息技术等领域的合作不断发展,加上法国在欧盟成员国中巨大的影响力,法国已成为中国商品下一个极具发展潜力的消费市场。
中国政府商务部的统计数字显示,法国是中国在欧盟的第4大贸易伙伴,中国是法国第7大全球贸易伙伴和第1大亚洲贸易伙伴。
2008年1月至10月期间,中法双边贸易总额为324.8亿美元,与上一年同期相比上升了21. 6%,全年有望突破400亿美元,比2005年翻了一番,提前两年实现两国领导人制定的目标。
其中法国对中国的出口额为131.3亿欧元,与上一年同期相比上升了26.2%;法国自中国的进口额为193.5亿欧元,与上一年同期相比增长了18.6%。
而根据法国海关总署的统计数字显示,在2003年至2006年期间,法国与中国进出口贸易总额均保持强劲增长势头,每年的增长率均超过20%。
但该增长率在2007年时开始放缓,仅为16.5%。
而在2008年期间,由于受全球金融和经济危机的影响,尽管法中贸易继续保持上升趋势,但是增速却明显下滑。
法中贸易总额达到399.6亿欧元,较上一年的380.7亿欧元增长4.9%,明显低于上一年16.5%的增长幅度;其中法国对中国的出口额为90.01亿欧元,较上一年的90.8亿欧元减少了1%左右;法国自中国的进口额为309.5亿欧元,与上一年的289.8亿欧元相比增长了6.8%。
碧兰麻

碧兰麻复方盐酸阿替卡因注射液(compound articaine hydrochloride injection)成分:每1.7ml含盐酸阿替卡因68.000mg(相当于阿替卡因盐基60.2800mg),盐酸肾上腺素0.0204mg(相当于肾上腺素0.0170mg)。
赋形剂:氯化钠,盐酸,氢氧化钠,无水亚硫酸钠,注射用水。
剂型与规格:注射剂,1.7ml/支,50支/盒。
药物分类:局部麻醉剂,α和β拟交感神经兴奋剂(N:中枢神经系统)生产厂家:法国碧兰公司(produits dentaires pierre rolland)厂址:法国-波尔多-梅力奈力33708,216信箱,Avenue Gustave Eiffel-BP216-ZI du Pharee-33708 MERIGNAC Cedex FRANCE适应症:口腔用局部注射麻醉剂,特别适用于涉及切骨术及黏膜切开的外科手术过程。
注意事项:1.禁忌症:本品禁止用于下列情况:4岁以下儿童;对局部麻醉剂高度敏感者;严重肝功能不全,扑林症(紫癜症);静脉注射(因含有肾上腺素);胆碱酯酶缺乏;阵发性心搏过速;高频率心率失常;窄角青光眼;甲状腺功能亢进。
2.特别警告;由于含亚硫酸盐可能出现过敏性休克。
3.使用时注意:患高血压,糖尿病及应用单胺氧化酶抑制剂治疗的患者慎用本麻醉剂。
4.对运动员:本品可引起运动员药检不合格。
5.赋形剂成分中亚硫酸盐对某些病人的安全性尚有待认识。
用法:剂量:成人:阿替卡因最大用量不超过7mg/kg/天。
4岁以上儿童:阿替卡因最大用量不超过5mg/kg/天。
所有麻醉过程:一次浸润注射0.8-1.7ml牙间隔麻醉:每次0.3ml即足。
给药方法:粘膜下注射,切勿静脉注射。
注射前请回抽血以检查是否误入血管。
每15秒钟注射量勿超过0.5ml,即每支注射时间为1分钟。
储存:25℃以下避光储存。
勿使用过期药品。
进口药品注册证号:X19990003。
进口药

爱全乐(吸入用异丙托溴铵溶液)使用说明

爱全乐(吸入用异丙托溴铵溶液)【用法用量】1.剂量:剂量应按病人个体需要做适量调节;在治疗过程中病人应该在医疗监护之下。
除非另有医师处方,以下为推荐剂量:2.维持剂量:成人(包括老人)和12岁以上青少年:每天3-4次,每次1个单剂量小瓶。
3.急性发作治疗:成人(包括老人)和12岁以上青少年:每次1个单剂量小瓶;病人病情稳定前可重复给药。
给药间隔可由医生决定。
爱全乐可与吸入性β受体激动剂联合使用。
单剂量小瓶中每1毫升雾化吸入液可用生理盐水稀释至终体积2-4毫升或者可以和Berotec雾化吸入液联合使用。
成人及12岁以上儿童日剂量超过2毫克应在医疗监护下给药。
无论急性期治疗或维持治疗,建议都不要超过推荐剂量太多。
如果治疗后未产生病情显著的改善或病人情况更趋严重,必须寻求医生的建议以决定新的治疗方案。
发生急性或迅速恶化的呼吸困难时应立即咨询医生。
爱全乐雾化吸入液可使用市面上一般的雾化吸入器。
在有墙式给氧设施情况下,吸入液最好以每分钟6-8升的流速给予。
吸入用异丙托溴铵溶液(爱全乐)可以和祛痰剂盐酸氨溴索(沐舒坦)雾化吸入液﹑盐酸溴己新(Bisolvon)雾化吸入液和非诺特罗(Berotec)雾化吸入液共同吸入使用。
由于可出现沉淀,爱全乐和含有防腐剂苯扎氯铵的色苷酸钠雾化吸入液不要在同一雾化器中同时吸入使用。
4.使用方法:单剂量雾化吸入液只能通过合适的雾化装置吸入,不能口服或注射。
(1)按生产厂商或医生指导准备雾化器以加入雾化吸入液。
(2)从生产条板上撕下一个单剂量小瓶。
(3)用力扭顶部,打开小瓶。
(4)将单剂量小瓶中的药液挤入雾化器药皿中。
(5)安装好雾化器,按说明使用。
(6)按厂商的指示弃去雾化器药皿中剩余药液并将雾化器清洗干净。
由于此单剂量小瓶中不含防腐剂,为防止细菌污染,在药物打开后应立即使用且每次吸入治疗时应使用一新的单剂量小瓶是非常重要的。
部分使用后的﹑已开瓶的或有破损的药瓶应丢弃。
【注意事项】有狭角性青光眼倾向﹑前列腺增生或膀胱癌颈部梗阻的患者应慎用爱全乐。
递法明片说明书

递法明片篇
商品名:递法明片 厂家:Laboratoires LEURQUIN MEDIOLANUM
【递法明片药品名称】 通用名称:递法明片 汉语拼音:Difaming Pian 【递法明片成份】 越桔果提取物、β-胡萝卜素。
【递法明片性状】 递法明片为蓝色糖衣片,除去糖衣后显红棕褐色; 气香,味微涩。 递法明片功能主治】 增加静脉张力及起到保护血管的作用。用于糖尿 病等引起的视网膜病变。
【递法明片贮藏】遮光,密封,常温保存。
【递法明片包装】PVC/PVDC铝塑泡罩包装。20片/ 盒。 【递法明片有效期】36个月。
【递法明片执行标准】进口药品注册标 准JZ20030012
【递法明片进口药品注册证号】 Z20040004
【递法明片生产企业】 企业名称:法国乐康-美的澜制药厂 Laboratoires LEURQUIN MEDIOLANUM
【百济药师温馨提示】
如果递法明片与其他药物同时使用,可能会发生药物相互作 用,详情请咨询您的主治医师或指导药师。同时在服用递法 明片之前,请耐心阅读如下5个注意事项: 1、如妊娠时,通知医生; 2、如存有任何疑问,请随时向医生或药剂师咨询。为了 避免多种药物之间的交叉反应,如有同时接受其他疗法,应 及时向医师或药师报告; 3、此药应置于儿童触不到的地方; 4、病人应避免日光曝晒及过方炎热的环境,避 免站立时间过长及身体过重; 5、散步及穿合适的袜子会改善血液循环。
者健康”的经营理念。
【递法明片规格】 每片重0.4g(含越桔果提取物100mg,β-胡萝卜素 5mg)。 【递法明片用法用量】 口服。1次3片,一日2次,一个疗程为3-6个月。 【递法明片不良反应】 少数病例出现胃肠道不适等症。
法国进口管理制度

法国进口管理制度法国是欧洲大国之一,拥有发达的经济和丰富多样的产品和服务。
作为一个出口国,法国也是一个重要的进口国,每年都有大量的商品和产品进入法国市场。
为了保护国内产业和消费者利益,法国对进口商品和产品实行严格的管理制度。
本文将从法国进口管理制度的法律法规、进口商品的申报和检验、进口货物的清关和税费、进口商品的禁止和限制等方面进行详细介绍。
一、法国进口管理制度的法律法规法国的进口管理制度是建立在严格的法律法规基础之上的。
根据欧盟法律和法国国内法律,所有进口商品都必须符合相关规定和标准。
同时,法国也会根据需要对进口商品制定进一步的管理措施,以保护国内市场和消费者权益。
除了欧盟法律规定的标准之外,法国还有一些特定的法律法规,比如消费品安全法、食品安全法、化妆品法等,这些法律法规对进口商品的质量和安全提出了更高的要求。
二、进口商品的申报和检验在进口商品进入法国市场之前,必须经过严格的申报和检验程序。
根据欧盟规定,所有进口商品都必须提供进口申报单和相关的证明文件,以确保其符合相关标准和规定。
同时,法国海关和检验机构会对进口商品进行检验,以确保其质量和安全。
尤其是对于一些重要的产品,如食品、药品、化妆品等,更是会进行严格的检验和抽样检查,以保护消费者的权益。
三、进口货物的清关和税费进口货物到达法国后,必须经过海关的清关程序,以完成进口手续。
根据法国的税收法律,进口商品会收取相应的进口关税和增值税。
同时,一些特定的产品可能还需要支付额外的消费税或特别税。
此外,法国对一些特定的产品还设有进口配额和进口许可证,这意味着这些产品的进口数量和条件受到限制。
四、进口商品的禁止和限制为了保护国内产业和消费者的健康与安全,法国对部分产品实行了禁止或限制进口。
比如一些有害物质的产品、仿冒品、侵权产品等都被禁止进口。
同时,对于一些特定的产品,如枪支和弹药、毒品和管制药品等,法国也实行了严格的限制措施。
综上所述,法国的进口管理制度是严格的,且建立在完善的法律法规之上。
【法国进口】达纳康达纳康(银杏叶片)()-药品说明书

【法国进口】达纳康达纳康(银杏叶片)
药品规格:
40mg*30片
生产企业:
用法用量:
口服一次1片一日3次或者遵循医嘱。
分类:
化学药品
类型:
处方药
适应症:
活血化瘀通络。本品主要用于瘀血阻络引起的胸痹心痛﹑中风﹑半身不遂﹑舌强语謇,冠心病稳定型心绞痛﹑脑梗死见上述证候者。
相关疾病:
瘀血阻络,冠心病稳定型心绞痛,脑梗死
说明书:
商品名称:达纳康
通用名称:银杏叶片
主要成份:主要成份是银杏叶提取物。
适应症:活血化瘀通络。本品主要用于瘀血阻络引起的胸痹ቤተ መጻሕፍቲ ባይዱ痛﹑中风﹑半身不遂﹑舌强语謇,冠心病稳定型心绞痛﹑脑梗死见上述证候者。
不良反应:1.偶有胃部不适。
2.极少见轻微的胃肠不适及皮肤过敏等。
禁忌:对本品过敏者慎用。
注意事项:1.心力衰竭者,孕妇及过敏体质者慎用。
2.药品性状发生改变时禁止使用。
3.请将此药品放在儿童不能接触的地方。
孕妇及哺乳期妇女用药:孕妇慎用。
儿童用药:尚不明确。
老人用药:尚不明确。
药物相互作用:1.清除自由基的生成,抑制细胞膜脂质过氧化;提高红细胞SO的活性。
2.拮抗血小板活化因子引起的血小板聚集,防止血栓的形成。
3.对离体及在体心脏局部肌缺血、肥大心脏局部主肌缺血引起的心功能紊乱等均有改善作用。
4.改善血液的流变性,增进红细胞的变形能力,降低血液粘度,改善循环障碍。
5.对脑部血液循环及脑细胞代谢有较好的改善和促进作用,对大脑具有保护作用。
药物过量:尚未明确。
药物毒理:1.动物离体心脏灌流和兔耳灌流法证明,本品其具有扩张冠状动脉和拮抗肾上腺素收缩血管的药理作用;动物口服本品后,显示其能增加脑血流,降低血管阻力;本品具有较强的抗血小板聚集作用。
医药工业:金融危机下的法国医药工业

医药工业:金融危机下的法国医药工业法国医药业受危机冲击较小的缘由:1、注意医药业的结构调整。
法国医药工业凭借其悠久的历史、先进的科学技术,在全球医药工业中,保持着大国的地位。
依据《福布斯》2022年公布的全球各国企业的营业额、利润额、总资产和市值四大数据的综合排名,在全球前500强企业中,医药行业共18家入围,美国辉瑞公司、强生公司和法国赛诺菲-安万特公司分别稳居前三甲。
鉴于医药产品、技术和市场的及其多样化,制药工业无论在全球还是在法国都不属劳动力密集的行业,医药业在法国工业门类中是竞争力较强的行业。
自1995年法国成为欧盟最大的药品生产国后,面对激烈的国际竞争,该行业通过多次重大的技术变革和重组合并后,其企业已从上世纪50年月的近1000家,削减到2022年的326家,此外还有177家企业完全服务于生物技术。
2022年法国制药工业工薪人员约为103,633名,雇用人员近11,000人。
近十几年以来,随着法制药业的进展其就业人员在不断增加,每年制造就业岗位约2000人,增速在20%以上。
法国目前是欧洲第一,全球第三大制药市场,2022年全球药品市场销售额高达7,730亿美元,同比增长4.8%,法国排美国(37.9%)和日本(9.9%)之后占全球市场份额的5.5%,德国占5.3%。
2、重视研发和创新。
从科研与开发经费所占行业产值的比率相比,法国医药业仅次于航空和航天业,但国家拨给医药业的科研经费仅为1%,与其它行业相差甚远,拨给航空和航天业的科研经费为33%。
法医药业科研经费的99%是由制药企业自己投入,因制药业新技术的开发需要专业水平特别高而且酬薪高的人员,企业每年投入制药业和开发新药品的研发预算为46亿欧元(2022年)。
企业在研发方面的投资占其营业总额的12.3%。
此外医药企业从事研发的人员也在逐年增加,20年间增长了3倍,2022年法医药研发人员达22,594名。
目前在法国制药行业,研发与制药分别正在成为一种趋势。
法国入境药品申报流程和注意事项

法国入境药品申报流程和注意事项下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor.I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!入境法国携带药品时,需要遵循一定的流程和注意事项以确保合规并避免潜在的问题。
进口药

七叶洋地黄双苷滴眼液 施图伦 10*0.4ml 德国视都灵药品有限责任公司 进口药品注册证号:H20130295 银杏叶提取物片 金纳多 20片 德国威玛舒培博士药厂 进口药品注册证号:H20090296 卵磷脂络合碘片 沃丽汀 60p 东京 进口H20110014 吸入用复方异丙托溴铵溶液 可必特 2.5ml*10支 法国 进口药品注册证号H20100608 非诺贝特胶囊 力平之 10粒 法国利博福尼制药公司 进口药品注册证号:H20100602 暖宫贴无精油 娇爽暖贴 6贴 法国梦彦药业 甲泼尼龙片 美卓乐 4mg*30片 砝码西亚普强(中国)有限公司 进口注册证号:H20100730 华法林钠片 3mg*100片 芬兰奥立安集团奥立安药厂 H20110108 沙美特罗替卡松粉吸入剂 舒利迭 50微克 葛兰史克 进口药品注册证号H20140165 舒立跌小 100微克 葛兰素史克 国药准字H20090240 丙酸氟替卡松吸入气雾剂 辅舒酮 125微克 葛兰素史克 进口药品注册证号H20130190 沙美特罗卡松粉吸入剂 舒利迭 500微克 葛兰素史克 进口药品注册证号H20090242 丙酸氟替卡松鼻喷雾剂 辅舒良 120喷 葛兰素史克药业有限公司 进口药品注册证号:H20091100 硫酸沙丁胺醇气雾剂 万托林 200揿 葛兰素史克制药 进口药品注册证号H20090514 优泌林 精蛋白锌重组人胰岛素混合注射液 3ml*300单位 礼来苏州制药有限公司 国药准字J20140029 诺和平地特胰岛素注射液 特充 300u:3ml 诺和诺德 进口药品注册证号:S20090063 分包装:国药准字J20090100 诺和笔 5 胰岛素笔式数显注射器 诺和诺德 诺和灵N注射液 精蛋白生物合成人胰岛素注射液 400IU/10ml 诺和诺德(中国)制药有限公司 国药准字J20120034 诺和灵R 生物合成人胰岛素注射液 400IU/10ml 诺和诺德(中国)制药有限公司 国药准字J20120026 诺和灵30R 精蛋白生物合成人胰岛素注射液 3ml 诺和诺德制药 国药准字J20100088 诺和平 地特胰岛素 3ml*300单位 诺和诺德制药 诺和锐 门冬胰岛素注射液 3ml 诺和诺德制药 诺和灵N笔芯 精蛋白生物合成人胰岛素注射液 3ml:300单位 诺和诺德制药有限公司 国药准字J20100116 甲磺酸伊马替尼片 格列卫 0.1g*60片 诺华制药 进口药品注册证号:H20100263 草木犀流浸液片 30片 日本/生晃荣养药品株式会 复方甘草酸苷片 美能 100片 日本米诺发源制株式会社 国药准字J20080080 格列美脲片 (亚莫利) 2mg/片*15片 赛诺菲(北京)制药有限公司 甘精胰岛素注射液 来得时 3ml 赛诺菲安万特(北京)制药有限公司 国药准字J20120021 多烯磷脂酰胆碱胶囊 易善复 24粒 赛诺菲制药有限公司 厄贝沙坦氢氯噻嗪片 安博诺 7片 *150mg/12.5mg 赛诺菲制药有限公司 国药准字J20130041 门冬氨酸钾镁片 50片 匈牙利吉瑞大药厂 进口药品注册证号H20080496 甲磺酸溴隐亭片 佰莫亭 30片 匈牙利吉瑞制药厂 进口药品注册证号H20110116 乙酰半胱氨酸泡腾片富露施片 4片 意大利 进口药品注册证号:H20090620 沙美特罗替卡松粉吸入剂 舒利迭 250微克 英国葛兰素史克有限公司 H20090241
必兰用于乳牙麻醉效果观察

第21卷第4期河南医学研究Vol.21No.42012年12月HENANMEDICALRESEARCHDecember 2012收稿日期:2012-11-20;修订日期:2012-12-18作者简介:韩东超(1969-),男,河南郑州人,本科,副主任医师,从事儿童牙病临床诊疗。
文章编号:1004-437X (2012)04-0409-02·临床研究·必兰用于乳牙麻醉效果观察韩东超,牛志英(郑州市口腔医院儿童口腔科河南郑州450000)摘要:目的:验证必兰用于乳牙麻醉的效果。
方法:选取50名患者,采取自身对照的方法,随机选择1侧下颌乳磨牙采用局部颊粘膜浸润麻醉,对侧下颌乳磨牙采用神经阻滞麻醉。
结果:阻滞麻醉注射过程的疼痛程度显著低于浸润麻醉,阻滞麻醉的麻醉效果显著高于浸润麻醉(P <0.01)。
结论:下牙槽神经阻滞麻醉对于下颌乳磨牙牙髓麻醉是一种较好的方法。
关键词:必兰;乳牙麻醉;疗效观察中图分类号:R614.3文献标识码:Bdoi :10.3969/j.issn.1004-437X2012.04.008Anesthesia effect observation of primacaine adrenaline on de-ciduous teethHAN Dong-chao ,NIU Zhi-ying(Department of Pediatric Dentistry ,Zhengzhou Stomatological Hospital ,Zhengzhou 450000,China )Abstract :Objective :To verify the anesthesia effect of Primacaine Adrenaline for deciduous teeth.Methods :Fifty patients ,using their own control method ,are anesthetic for one side mandibular molar milk by local infiltration anesthesia of buccal mucosa randomly ,and the other side by nerve block anesthesia.Results :The pain degree of block anesthesia injection process is significantly lower than that of infiltration anesthesia ;the effect of block anesthesia is significantly higher than infiltration anesthesia.Conclusion :Nerve block anesthesia of inferior alveolar for mandibular milk grinding fang pulp is a better method.Keywords :primacaine adrenaline ;deciduous teeth anesthesia ;curative effect observation 必兰是由法国赛特力—碧兰公司所属碧兰分公司生产的一种口腔专用局部麻醉剂(进口药品注册证号H20090172),其具有较强的组织浸润性和局麻效能强等特点,目前在临床上应用越来越广泛,以往的研究大都集中在必兰在成人口腔治疗中的应用,本文就必兰在儿童牙髓治疗中的应用作以探讨。
泰舒达说明书

泰舒达说明书【药品名称】通用名称:吡贝地尔缓释片商品名称:泰舒达英文名称:Piribedil SR Tablets(Trastal)汉语拼音:Bibeidi‘er Huanshipian【成份】本品主要成份为吡贝地尔。
化学名称:吡贝地尔,[(亚甲二氧基-3,4苄基)-4哌嗪基-1]-2嘧啶【适应症】-用于老年患者的慢性病理性认知和感觉神经障碍的辅助性症状性治疗(除阿尔茨海默病和其它类型的痴呆)。
-用于下肢慢性阻塞性动脉病(第2期)所致间歇性跛行的辅助性治疗。
注释:这一适应症是鉴于行走距离的改善来确定的。
-建议用于眼科的缺血性症状。
-用于帕金森病的治疗:1,可作为单一用药(治疗震颤明显的类型)2,或在最初或稍后与多巴治疗联合用药,尤其是对伴有震颤的类型。
【规格】50mg 【价格】:52.9元【用法用量】口服除帕金森病之外的所有适应症:每日1片于正餐结束时服用,或对于病情较严重者每日2片分别于两次正餐结束时服用。
药片应于进餐结束时,用半杯水吞服,不要咀嚼。
帕金森病的治疗:1、作为单一用药:150mg到250mg,即每日3到5片,分3到5次服用。
2、作为多巴治疗的补充:每日1到3片(每250mg左旋多巴大约需50mg吡贝地尔)。
药片应于进餐结束时用半杯水吞服,不要咀嚼。
剂量必须逐渐增加,每三天增加一片。
或遵医嘱。
【不良反应】可能出现下列症状:1、轻微的消化道不适(恶心、呕吐、胀气),可在剂量个体化调整后消失。
2、服用吡贝地尔有出现昏睡的报道,在极少个体中,日间出现过度的昏睡和突然进入睡眠状态。
3、也可出现心理紊乱如混浊或激越,尽管比较罕见。
这些症状可在停药后消失。
4、血压紊乱(直立性低血压)或血压不稳非常少见。
5、由于含有胭脂红,有可能引起过敏反应。
如服用本药后,发生本说明书之外的任何不良事件和/不良反应,请与医生联络。
【禁忌】该药物在下列情况下禁忌使用:1、对本品中任何成份过敏者2、心血管性休克3、心肌梗死急性期4、联合应用:止吐类精神安定药(参考[药物相互作用]);安定类精神安定药(不包括氯氮平)(帕金森患者除外)(参考[药物相互作用])【注意事项】1、在使用吡贝地尔进行治疗的患者中有出现昏睡和突然进入睡眠状态的情况,特别是帕金森患者。
匹维溴铵、蒙脱石散及双歧杆菌四联活菌片治疗腹泻型肠易激综合征的临床疗效
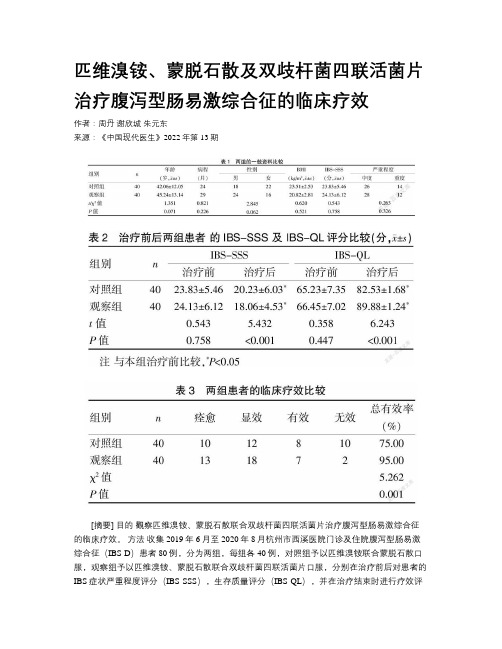
匹维溴铵、蒙脱石散及双歧杆菌四联活菌片治疗腹泻型肠易激综合征的临床疗效作者:周丹谢欣城朱元东来源:《中国现代医生》2022年第13期[摘要] 目的觀察匹维溴铵、蒙脱石散联合双歧杆菌四联活菌片治疗腹泻型肠易激综合征的临床疗效。
方法收集2019年6月至2020年8月杭州市西溪医院门诊及住院腹泻型肠易激综合征(IBS-D)患者80例,分为两组,每组各40例,对照组予以匹维溴铵联合蒙脱石散口服,观察组予以匹维溴铵、蒙脱石散联合双歧杆菌四联活菌片口服,分别在治疗前后对患者的IBS症状严重程度评分(IBS-SSS),生存质量评分(IBS-QL),并在治疗结束时进行疗效评判,同时记录可能相关的不良反应。
结果治疗后,观察组的IBS-SSS为(18.06±4.53)分,低于对照组的(20.23±6.03)分,两组比较,差异有统计学意义(P0.05)。
结论采用匹维溴铵、蒙脱石散联合双歧杆菌四联活菌片治疗腹泻型肠易激综合征的临床效果确切。
[关键词] 匹维溴铵;蒙脱石散;双歧杆菌四联活菌片;腹泻型;肠易激综合征[中图分类号] R574.4 [文献标识码] B [文章编号] 1673-9701(2022)13-0031-03[Abstract] Objective To observe the clinical efficacy of pinaverium bromide, montmorillonite powder combined with bifidobacterium quadruple viable bacteria tablets in treating diarrhea-type irritable bowel syndrome. Methods A total of 80 cases of outpatient and inpatient diarrheal irritable bowel syndrome (IBS-D) in Hangzhou Xixi Hospital from June 2019 to August 2020 were collected, with 40 cases in each group.The control group took pinaverium bromide combined with montmorillonite powder orally.The observation group took pinaverium bromide, montmorillonite powder,and bifidobacterium quadruple viable bacteria tablets orally. The patients′ IBS symptom severity score (IBS-SSS) and quality of life score (IBS-QL) were scored before and after treatment. The efficacy was evaluated at the end of the treatment, and the possible related adverse reactions were recorded. Results After treatment, the IBS-SSS (18.06±4.53)points of the observation group was lower than the IBS-SSS(20.23±6.03)points of the control group,and the difference between the two groups was statistically significant(P0.05). Conclusion The pinaverium bromide, montmorillonite powder combined with bifidobacterium quadruple viable bacteria tablets, has a clinical effect on treating diarrhea-type irritable bowel syndrome.[Key words] Pinaverium bromide; Montmorillonite powder; Bifidobacteria quadruple viable tablets; Diarrhea type; Irritable bowel syndrome肠易激综合征(irritable bowel syndrome,IBS)主要表现为与排便或排便习惯的改变而出现的反复发作性腹痛、腹胀、腹泻等腹部不适症状[1],影响着全球约10%的人群,在亚洲国家的发病率为5%~10%[2-3]。
法国进口药品

2 2 2 2 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1
PolyPeptide Laboratories France Rohm and Haas France S.A.S. SEPTODONT ZaCH SYSTEM BASF Orgamol Pharma Solutions France SAS BASF PHARMA (SAINT VULBAS) SAS Capsugel France CARGILL France SAS CATALENT FRANCE BEINHEIM SA DELPHARM LILLE SAS Finorga S.A. FINORGA SAS INDENA S.A.S JANSSEN CILAG LABORATOIRE AGUETTANT LABORATOIRES ALCON S.A Laboratoires Besins International Laboratoires Chemineau LABORATOIRES MAYOLY SPINDLER Laboratoires Merck Sharp & Dohme Chibret (Mirabel) Lilly France S.A.S MERCK SANTE SAS Merck Sharp & Dohme Chibret NextPharma SAS NOFI WINTHROP INDUSTRIE PCAS (SELOC France site) PRODUITS DENTAIRES PIERRE ROLLAND S.I.O SANOFI-WINTHROP INDUSTRIE Scora S.A. SEPPIC S. ASEPPIC S. A Unither Liquid Manufacturing SAS (空白)
国家药品监督管理局关于同意进口德巴金等国内分装生产用制剂的批复-药管注[1999]195号
![国家药品监督管理局关于同意进口德巴金等国内分装生产用制剂的批复-药管注[1999]195号](https://img.taocdn.com/s3/m/dc1565c251e2524de518964bcf84b9d528ea2c75.png)
国家药品监督管理局关于同意进口德巴金等国内分装生产用制剂的批复正文:---------------------------------------------------------------------------------------------------------------------------------------------------- 国家药品监督管理局关于同意进口德巴金等国内分装生产用制剂的批复(药管注[1999]195号)上海市药品检验所:法国赛诺菲集团中国分公司来函,申请准予其专供国内分装生产用的7种制剂进口,以满足其合资厂分装生产的需要。
鉴于所申请品种都已取得《进口药品分装生产批件》,其原包装药品已获得《进口药品注册证》,为保证其国内分装生产的正常进行,经研究,同意德巴金、诺仕帕等按附件规定的数量进口,其他内容遵照原各《进口药品管理注册证》的规定执行。
今后,所有相关品种必须按照《进口药品管理办法》的规定,取得专供进口分装使用的《进口药品注册证》,否则一律不得进口。
附件:进口品种名单国家药品监督管理局药品注册司1999年6月24日附件:进口品种名单品名剂型规格注册证号分装批件号进口数量德巴金针剂400mg/支×980005 (98)-22号4995盒(4支/盒) 德巴金片剂500mg/片×980004 (98)Jb-11号39801盒(30片/盒) 诺仕帕片剂40mg/片×970132 (96)Jb-10号24000盒(20片/盒) 诺仕帕针剂40mg/2ml ×970133 (98)J-17号 10203盒(5支/盒) 速避凝针剂0.3ml/支×970207 (98)-19号2200盒(10支/盒) 速避凝针剂0.4ml/支×970208 (98)-20号18000盒(10支/盒) 速避凝针剂0.6ml/支×970209 (98)-21号3500盒(10支/盒)——结束——。
得舒特-匹维溴铵片说明书

得舒特-匹维溴铵片说明书(总2页)-CAL-FENGHAI.-(YICAI)-Company One1-CAL-本页仅作为文档封面,使用请直接删除匹维溴铵片说明书【药物名称】通用名称:匹维溴铵片商品名称:得舒特英文名称:Pinaverium Bromide Tablets汉语拼音:Piweixiuan Pian【成份】化学名称:N(2-溴-4,5-二甲基苄基)-N(2[2-双甲基-2-去甲蒎烷基]乙氧基)乙基)吗啉溴化学结构式:分子式:C26H41O4NB r2分子量:591.45【性状】本品为橙色薄膜衣片,除去包衣后显白色。
【适应证】-对症治疗与肠道功能紊乱有关的疼痛、排便异常和胃肠不适;-对症治疗与胆道功能紊乱有关的疼痛;-为钡灌肠做准备。
【规格】50mg【用法用量】成人:常用推荐剂量3-4片/天,少数情况下,如有必要可增至6片/天。
为钡灌肠做准备时,应于检查前三天开始用药,剂量为4片/天。
切勿咀嚼或掰碎药片,宜在进餐时用水吞服。
不要在卧位时或临睡前服用。
【不良反应】-极少数人中观察到轻微的胃肠不适。
-极个别人出现皮疹样过敏反应。
【禁忌】孕妇忌服。
【注意事项】如果您有疑问,请咨询医生或药剂师。
为避免可能的药物相互作用,请告诉医师或药剂师您正在接受其他的医学治疗。
建议孕妇不使用本品。
如在服药期间发现妊娠,请向医生咨询。
由医生判断是否继续治疗。
哺乳期间,不建议使用本品。
通常在孕期或哺乳期,服用任何药物之前,应首先咨询医生或药剂师。
【孕妇及哺乳期妇女用药】动物实验中未见致畸作用,在临床应用中,目前尚缺乏评价匹维溴铵的致畸或胎儿毒性作用的充足资料,故妊娠期间禁止服用。
另外在妊娠晚期摄入溴化物,可能影响新生儿神经系统(低张和镇静)。
由于尚无是否进入乳汁的相关资料,哺乳期间应避免服用。
【儿童用药】因临床数据不足,本品不推荐给儿童使用。
【老年用药】据现有资料料,本品可用于老年患者。
【药物相互作用】尚不明确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
生产厂商(英文) 汇总 总计 383 SANOFI WINTHROP INDUSTRIE 80 LES LABORATOIRES SERVIER INDUSTRIE 26 Lilly France 23 Glaxo Wellcome Production 22 Roquette Freres 19 SANOFI PASTEUR S.A. 18 GUERBET 14 Laboratoires Galderma 10 Catalent France Beinheim S.A. 9 PATHEON FRANCE 8 PFIZER PGM 7 Beaufour Ipsen Industrie 6 DELPHARM Lille S.A.S. 6 IPSEN PHARMA BIOTECH 6 NP Pharm S.A.S. 6 Abbott Healthcare SAS 5 GATTEFOSSE SAS 5 Laboratoires Merck Sharp & Dohme Chibret 5 ORIL INDUSTRIE 5 SEPPIC S.A.SEPPIC S.A. 5 APTALIS PHARMA SAS 4 Delpharm Reims 4 SANOFI CHIMIE 4 Evonik Rexim S.A.S. 3 Genzyme Polyclonals S.A.S. 3 Laboratoire Unither 3 Laboratoires Sophartex 3 ORIL INDUSTRIE (Site de Baclair) 3 RECIPHARM FONTAINE 3 AXCAN PHARMA S.A. 2 AXCAN PHARMA SAS 2 Bayer Sante Familiale 2 BIOCODEX 2 BIO-RAD 2 Boehringer Ingelheim France 2 Capsugel 2 CHIESI S.A. 2 Creapharm Bessay S.A.S. 2 Delpharm Huningue S.A.S. 2 Delpharm Huningue SAS 2 Ethypharm 2 Excelvision 2 Laboratoires LEURQUIN MEDIOLANUM 2 MINAKEM DUNKERQUE 2 Pierre Fabre Medicament Production-Aquitaine Pharm International 2
2 2 2 2 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1
