2019高考化学一轮复习选习练题10含解析新人教版
2019高考化学一轮训练学题含解析新人教版(全套共12份)

人教化学2019高考一轮训练学题(1)李仕才一、选择题1、常温下,在水溶液中发生如下反应①16H ++10C -+2XO -4===2X 2++5C 2+8H 2O ;②2A 2++B 2===2A 3++2B -;③2B -+C 2===B 2+2C -。
下列说法错误的( )A .反应C 2+2A 2+===2A 3++2Cl -可以进行 B .还原性由强到弱的顺序是C ->A 2+>B ->X 2+C .氧化性由强到弱的顺序是XO -4>C 2>B 2>A 3+D .反应③是置换反应3、电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。
下图是KOH 溶液分别滴定HCl 溶液和CH 3COOH 溶液的滴定曲线示意图。
下列示意图中,能正确表示用NH 3·H 2O 溶液滴定HCl 和CH 3COOH 混合溶液的滴定曲线的是( )解析:HCl 为强电解质,CH 3COOH 为弱电解质,滴加NH 3·H 2O ,先与HCl 反应,生成同样为强电解质的NH 4Cl ,但溶液体积不断增大,溶液稀释,所以电导率下降。
当HCl 被中和完后,继续与CH 3COOH 弱电解质反应,生成CH 3COONH 4,为强电解质,所以电导率增大。
HCl 与CH 3COOH 均反应完后,继续滴加弱电解质NH 3·H 2O ,电导率变化不大,因为溶液被稀释,有下降趋势。
固体,3·H 2+4的值都变小倍后,稀释后④溶液中的pH 大mol·L -1,一水合氨是弱电解质,·H 2+4+平衡左移,3·H 2+4的值都增大,错误;稀释后③④溶液中3、5,D 选项正确。
D5、现有下列仪器,①集气瓶;②量筒;③烧杯;④表面皿;⑤蒸发皿;⑥容量瓶;⑦圆底烧瓶。
其中能用酒精灯加热的是( ) A .②③⑤ B .③⑥⑦C.①③④ D.③⑤⑦解析:集气瓶、量筒、表面皿、容量瓶不能加热,烧杯、圆底烧瓶要垫石棉网加热,蒸发皿可直接加热。
2019高考化学一轮复习选训习题10含解析新人教版

人教化学2019高考一轮选训习题(10)李仕才一、选择题1、下列有关金属的工业制法中,正确的是( B )A .制钠:用海水制得精盐,再电解纯净的NaCl 溶液B .制铁:用CO 还原铁矿石得铁C .制镁:用海水经一系列过程制得氧化镁固体,再用H 2还原得镁D .制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得到铝 解析 电解法制取金属钠时,需要电解熔融的NaCl ,而不是其溶液,A 项错误;镁的还原性很强,不能用热还原法来制取,而应用电解熔融氯化镁的方法,C 项错误;熔融的氯化铝不导电,故不能电解其熔融物制取金属铝,而应电解熔融的氧化铝,D 项错误。
2、下列溶液中溶质的物质的量浓度为1 mol·L -1的是( B )A .将58.5 g NaCl 溶于1 L 水中配成的溶液B .将80 g SO 3溶于水并配成1 L 溶液C .将100 mL 0.5 mol·L -1的NaNO 3溶液加热蒸发掉50 g 水的溶液D .含K +为2 mol 的K 2SO 4溶液3、新型纳米材料氧缺位铁酸盐(MFe 2O x :3<x <4,M =Mn 、Co 、Zn 或Ni ,在该盐中均显+2价)由铁酸盐(MFe 2O 4)经高温与氢气反应制得,常温下,它能使工业废气中的氧化物(SO 2、NO 2等)转化为其单质除去,转化流程如图。
关于此转化过程的叙述不正确的是( C )A .MFe 2O 4在与H 2的反应中表现了氧化性B .MFe 2O 4与MFe 2O x 的相互转化反应均属于氧化还原反应C .MFe 2O x 与SO 2反应中MFe 2O x 被还原D .若4 mol MFe 2O x 与1 mol SO 2恰好完全反应,则MFe 2O x 中x 的值为3.5解析 MFe 2O 4在与H 2的反应中,Fe 元素的化合价降低,表现了氧化性,A 项正确;MFe 2O 4与MFe 2O x 的相互转化反应中有元素化合价的升降,属于氧化还原反应,B 项正确;MFe 2O x 与SO 2反应中,Fe 元素的化合价升高,MFe 2O x 被氧化,C 项错误;若4 mol MFe 2O x 与1 mol SO 2恰好完全反应,由电子守恒可知,4 mol×2×(3-2x -22)=1 mol×(4-0),解得x =3.5,D 项正确。
2019高考化学一轮复习 选习练题(3)(含解析)新人教版

人教化学2019高考一轮选习练题(3)含答案李仕才一、选择题1、在一个密闭容器中,中间有一可自由滑动的隔板,将容器分成两部分。
当左边充入 28gN2,右边充入 8gCO 和 CO2的混合气体时,隔板处于如图所示位置(两侧温度相同)。
则混合气体中 CO 和 CO2 的分子个数比为()A.1:1 B.1:3 C.2:1 D.3:1【答案】D【解析】根据阿伏加德罗定律可知相同条件下气体的体积之比是物质的量之比,根据示意图可知氮气和混合气体的体积之比是4:1。
28g氮气是1mol,所以混合气体的物质的量是0.25mol,设混合气体中CO和CO2的物质的量分别是xmol、ymol,则x+y=0.25、28x+44y =8,解得x=0.1875、y=0.0625,所以混合气体中CO和CO2的分子个数比为3:1,答案选D。
2、下列化学方程式或离子方程式正确的是A.苏打溶液与过量的澄清石灰水反应:Ca2++OH-+HCO3-= CaCO3↓+H2OB.少量SO2通入氢氧化钠溶液中:OH-+SO2=HSO3-C.双氧水作脱氯剂,用于消除水中的氯气:Cl2+H2O2=2HCl+O2D.FeI2溶液中通入一定量的氯气:2Fe2++2I-+ 2Cl2 = 2Fe3++I2+ 4Cl-【答案】C3、下列各组物质,不能按a、b、c(“→”表示反应一步完成)关系转化的是( )A.A B.B C.C D.DC【答案】分别滴加下图所示的试剂。
下列关于实验现象的解释或结论正确的是【答案】C5、已知:H2(g)+Cl2(g) 2HCl(g)反应的能量变化示意图如下:下列说法正确的是A.点燃条件和光照条件下,反应的ΔH不同B.反应的ΔH约为[2c- (a+b)]kJ·mol-1C.“假想的中间物质”的总能量低于起始态H2和Cl2的总能量D.反应涉及的物质中,既有含极性键的物质,也有含非极性键的物质【答案】D应是放热反应,焓变应为△H=-[2c- (a+b)]kJ·mol-1。
2019高考化学一轮复习选训习题9含解析新人教版.docx

人教化学2019高考一轮选训习题(9)李仕才一、选择题1、己知NH’dSOs与足量的3 mol/L硫酸混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。
据此判断下列说法正确的是(D )A.反应中硫酸作氧化剂B.NHiCuSOj中硫元素被氧化C.刺激性气味的气体是氨气D. 1 mol NH4C U S03完全反应转移0. 5 mol电子解析反应中硫酸表现的是酸性,A项错误;NH.CuSOa屮硫元素变成SO2气体,化合价没变,B项错误;反应生成的刺激性气体是S02, C项错误;反应中Cu元素的化合价一半由+ 1升至+ 2, 一半由+ 1降至0,因此1 mol NH4CUSO3完全反应转移0.5 mol电子,D项正确。
2、设瓜为阿伏加德罗常数的值。
下列说法正确的是(B )A. 1.8 g重水中含有的中子数为加B.标准状况下,22.4 L C0和C2H1的混合气体的总分子数为加,质量为28 gC. 1 L 0. 1 mol・稀盐酸中,HC1的分子数为0. 1MD.常温常压下,1 mol甲基(一CHJ所含的电子数为10加1 8 g解析1.8g重水中所含的中子的物质的量为20 g 5^1X10 = 0.9 0101, A项错误;因为C0 和C2H4的摩尔质量均为28 g • mol-1,所以1 mol CO和C2H4的混合气体的总分子数为加,质量为28 g, B项正确;稀盐酸屮不存在HC1分子,C项错误,1 mol 一CH:<所含的电子数为9血,D项错误。
3、下列有关金属及其化合物的说法屮,正确的个数为(A )①在人类对金属材料的使用过程中,性质活泼的金属单质最早被人们冶炼和使用②纯铁比生铁抗腐蚀性更强③单质铝在空气中比较耐腐蚀,所以铝是不活泼金属④向紫色石蕊试液中加入过量的岛2。
2粉末,振荡,溶液变为蓝色并有气泡产生⑤青铜、不锈钢、硬铝都是合金⑥可通过焰色反应区分钾元素和钠元素⑦将FeCb溶液滴入KI —淀粉溶液中,溶液变蓝色⑧铝粉和氧化镁粉末混合,高温能发生铝热反应A. 4B. 5C. 6D. 7解析①金属活泼性越弱,越易被冶炼和使用;③A1是活泼金属,表面易形成致密氧化膜,耐腐蚀;④、氐02具有强氧化性,紫色石蕊试液变蓝后褪色;®A1不能把Mg置换出来,A1 与MgO不能发生铝热反应。
2019高考化学一轮复习练习题含解析新人教版(全套10份)

人教化学2019高考一轮练习题(1)李仕才一、选择题1、在密闭容器中发生下列反应aA(g)cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.5倍,下列叙述正确的是( )A.A的转化率变大B.平衡向正反应方向移动C.D的体积分数变大D.a<c+d解析:气体体积刚压缩平衡还未移动时D的浓度应是原来的2倍,当再次达到平衡时,D 的浓度为原平衡的1.5倍,D的浓度减小,所以压缩体积使平衡向逆反应方向移动。
平衡向逆反应方向移动,A的转化率变小,A错误;平衡向逆反应方向移动,B错误;平衡向逆反应方向移动,D的体积分数减小,C错误;增大压强,平衡向气体体积减小的方向移动,该平衡向逆反应方向移动,所以a<c+d,D正确。
答案:D2、下图是某有机物分子的比例模型,有关该物质的叙述中正确的是( )A.其结构简式为CH3—O—CH3B.其官能团为OH-C.能与金属钠反应D.能使紫色石蕊溶液变蓝解析:该比例模型对应的有机物为乙醇,结构简式为CH3CH2OH,官能团为—OH,不能使紫色石蕊溶液变蓝。
答案:C3、实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )A.装置①可用于石油的分馏B.装置②可用于酒精提取溴水中的Br2C.装置③可用于吸收HCl气体,并能防止倒吸D.装置④验证乙烯的生成解析:①是蒸馏装置,可用于石油的分馏,A项正确;因为酒精易溶于水,与溴水互溶,故不能用酒精提取溴水中的Br2,B项错误;HCl极易溶于水,导气管的出口在水中,所以会引起倒吸,应将苯换为CCl4,C项错误;温度计测得的是溶液的温度,水银球应该放在液面以下,并且制得的乙烯气体中可能混有挥发出的乙醇也能使乙烯的检验造成干扰,D项错误。
答案:AA.测量锌与稀硫酸反应的速B.证明非金属性:率C.进行酸碱中和滴定实验D.测定中和热解析:利用测单位时间内生成H2的量来测量锌和稀硫酸反应的速率,A项正确;一是盐酸酸性比H2CO3强,不能说明非金属性Cl>C,二是因为盐酸易挥发,挥发的HCl进入烧杯发生反应:2HCl+Na2SiO3===2NaCl+H2SiO3↓,不能说明酸性H2CO3强于H2SiO3,B项错误;NaOH是碱,应盛装在碱式滴定管中,图示盛装NaOH溶液的是酸式滴定管,C项错误;测定中和热时,大、小烧杯口应相平,以减少热量的损失,D项错误。
2019高考化学一轮基础选习 选择题2含解析新人教版.doc

人教化学2019高考一轮基础选习:选择题(2)李仕才1、向等物质的量浓度的HCl、AICk、NH4CK MgCL混合溶液中逐滴加入1 mol - L-1的NaOH 溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。
下列有关说法正确的是()A.在0〜a段加入的NaOH溶液与NH4C1反应B.在b〜c段加入NaOH溶液发生反应的离子方程式为Al3+ + 30r= Al(OH)3lC.在d~e段加入NaOH溶液发生反应的离子方程式为Al3++40r=A10r + 2H20D.在滴加NaOH溶液全过程中主要粒子参与反应的先后顺序是甘、Al3+, Mg2+, NH〕、Al (OH) 3解析A项错误,加入的NaOH溶液应先与前反应;B项错误,由图像中耗用NaOH溶液的体积可知,在b〜c 段加入NaOH溶液发生反应的离子方程式为Mg'+ + 20H- =Mg (OH) 2 J ; C项错误,在d~e段加入NaOH溶液发生反应的离子方程式为Al (0H) 3+ 0H「=A10『 + 2H20; D 项正确。
答案D2、如图是某同学设计的原电池装置,下列叙述中正确的是()A.氧化剂和还原剂必须直接接触才能发生反应B.电极II上发生还原反应,作原电池的正极C.该原电池的总反应式为:2Fe3++Cu=Cu2++2Fe2+D.盐桥中装有含氯化钾的琼脂,K+移向负极区解析该原电池反应中氧化反应和还原反应在两个不同的烧杯中进行,因此氧化剂和还原剂没有直接接触,A项错误;B项,Cu电极为原电池的负极,发生氧化反应,电极反应式为:Cu—2e_^Cu2+,错误;D项,正极发生反应:2Fe"+ + 2e_^2Fe2+,正电荷数减小,K+移向正极补充正电荷,错误。
答案C3、某固体混合物中可能含有:K\ Na\ Cl\ CO32\ SO厂等离子,将该固体溶解所得到的溶液进行如下实验:下列说法正确的是A.该混合物一定是bCOs和NaClB.该混合物可能是Na2C03和KC1C.该混合物一定是Nads和NaClD.该混合物可能是NaAO。
2019高考化学一轮复习选训习题1含解析新人教版.docx

人教化学2019高考一轮选训习题(1)李仕才一、选择题K (2018 •江西九江联考)设佩为阿伏加德罗常数的值。
下列说法正确的是(C )A.0.5 mol Cu与足量的S反应转移的电子数为佩B.在粗铜精炼的实验中,阳极质量减少6.4 g,则电解过程中转移的电子数为0.2加C. 2 g D2O和也%的混合物中含有的中子数为加D.46 g有机物GHeO中含有极性共价键的数0 一定为7抠解析Cu与S反应生成Cu2S, 0. 5 mol Cu与足量的S反应转移的电子数为0. 5加,A项错误;精炼铜时,阳极减少的不都是Cu,还有Zn、Fe、Ni等杂质金属,所以阳极质量减少6. 4 g时转移的电子数不是0.2僦,B项错误;D2O和出叱的摩尔质量相同,均为20g・ mol"1, 中子数也相同,均为10,故2 g址0和山"0的混合物的物质的量是0. 1 mol,所含中子数为汕,C项正确;CJIcO可以是乙醇,也可以是二甲(CIh—0—CIh),若是二甲醛,则46 g CzHsO 中含有的极性共价键的数目是8批,D项错误。
2、下列离子方程式书写正确的是(B )A.CL通入水中:Cl2+H20=2H++Cr+C10'B.双氧水加入稀硫酸和KI溶液:H202+2H+ + 2r=I2+2H20C.用铜作电极电解CuSOj溶液:2Cu2+ + 2H20^S2Cu+02 t +4H+D.NQ2S2O3溶液中加入稀硫酸:2S20r + 4H+=S0r + 3S ! +2H203、某校化学兴趣小组用如图所示过程除去AlCls溶液中含有的Mg2\广杂质离子并尽可能减少A1C13的损失。
|->Mg(OH)2沉淀足就NaOH溶液厶-严液,盐酸「沉淀a邑空A1C1;溶液ci-丄介" L溶液b下列说法正确的是(D )A.NaOH溶液可以用氨水来代替B.溶液a 中含有Alt K\ Cl"> NaS 0H_C.溶液b中只含有NaClD.向溶液a中滴加盐酸筒控制溶液的pll解析A项,用氨水将会使Al:,\ Mg2+均沉淀下来,达不到分离的目的;B项,溶液a屮,A13 +已转化为A10;; C项,b中含有KChNaCKHCl等物质;D项,若不控制pH,沉淀a[Al(0H)3] 将不能分离出来。
2019高考化学一轮复习训练选10含解析新人教版.docx
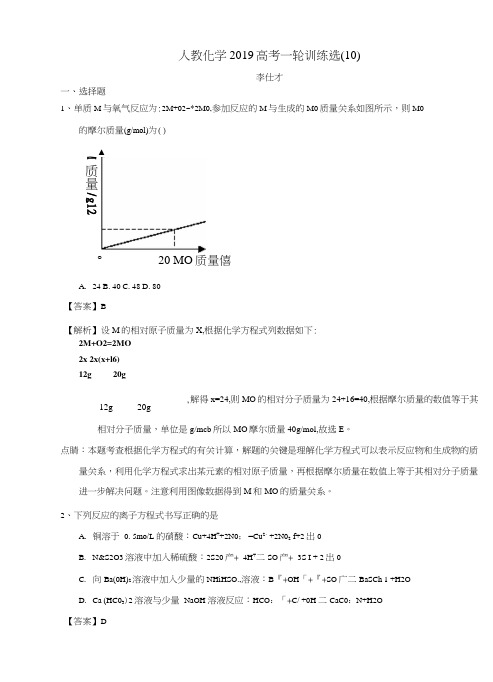
人教化学2019高考一轮训练选(10)李仕才一、选择题1、单质M 与氧气反应为:2M+02~*2M0,参加反应的M 与生成的M0质量关系如图所示,则M0的摩尔质量(g/mol)为()° 20 MO 质量僖A. 24B. 40C. 48D. 80【答案】B【解析】设M 的相对原子质量为X,根据化学方程式列数据如下:2M+O2=2MO2x 2x(x+l6)12g 20g,解得x=24,则MO 的相对分子质量为24+16=40,根据摩尔质量的数值等于其 相对分子质量,单位是g/mcb 所以MO 摩尔质量40g/mol,故选E 。
点睛:本题考查根据化学方程式的有关计算,解题的关键是理解化学方程式可以表示反应物和生成物的质量关系,利用化学方程式求出某元素的相对原子质量,再根据摩尔质量在数值上等于其相对分子质量 进一步解决问题。
注意利用图像数据得到M 和MO 的质量关系。
2、下列反应的离子方程式书写正确的是A. 铜溶于 0. 5mo/L 的硝酸:Cu+4H ++2N0; =Cu 2,+2N02 f+2出0 B. N&S2O3溶液中加入稀硫酸:2S20产+ 4H +二SO 产+ 3S I + 2出0C. 向Ba(0H)2溶液中加入少量的NHiHSO.,溶液:B 『+OH 「+『+SO 广二BaSCh 1 +H2OD. Ca (HC03)2溶液与少量 NaOH 溶液反应:HCO :「+C/ +0H 二CaC0:N+H2O【答案】DM质量/g12 12g 20g ▲【解析】铜濬于0. 5mo/L 的硝酸生成NO,离子方程式是3Cu+8FT+2N8 =3Cu 尹+2NO | +4曲0,故A 错 误;N H 2S 2O3滚'液中加入稀硫酸,+2价S 发生歧化反应2生成S 单质、S6气体,反应离子方程式是 S2O 产+ 2rf=S6 t +S | +H2O,故B 错误;向Ba (OH) 2溶液中加入少量的NHiHSd 溶液,反应离子方程式是 Ba 2>+2OH-+fT+SO42 +NH4-=BaSO41 +股6 NH 3 - H 2O ,故 C 错误:Ca (HCO3) 2 滚滋与少量 NaOH 溶液反应生成碳酸钙、碳酸氢钠、水,反应离子方程式是:HCCWhf 二CaCO 昇+HX ),故D 正确。
2019高考化学一轮复习选习练题含解析新人教版(全套10份)

人教化学2019高考一轮选习练题(1)含答案李仕才一、选择题1、对物质的量的理解正确的是()A.物质的量就是物质的质量的另一种表达方式,单位是g/molB.物质的量就是物质的数量,数值上等于式量,单位是molC.物质的量就是6.02×1023个微粒的质量,单位是gD.物质的量是国际单位制中的一个物理量,表示含有一定数目微粒的集体【答案】D2、下列离子方程式书写正确的是()A.NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性:H++OH-+Ba2++SO42-=H2O+BaSO4↓B.FeBr2溶液中通入足量的Cl2:2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-C.用两个铜电极电解食盐水:2Cl-+2H2O=2OH-+H2↑+Cl2↑D.用三氯化铁溶液腐蚀印刷线路板:Fe3++Cu=Fe2++Cu2+【答案】B【解析】A.溶液呈中性的反应为:2H++2OH-+Ba2++SO42-=2H2O+BaSO4↓,A错误;B.Cl比Br 的非金属性强,能将Br-氧化,同时将铁离子氧化,根据电荷守恒和物料守恒,B正确;C.阳极为金属时,将首先失去电子生成Cu2+,负极为H得到电子生成氢气,C错误;D.未配平,2Fe3++Cu=2Fe2++Cu2+,D错误。
故选择B。
3、下列物质的性质和用途描述错误的是A.铜质地漏具有独特的杀菌功能,能较好的抑制细菌生长B.明矾溶于水生成氢氧化铝胶体,起消毒杀菌的作用C.铁粉具有还原性,可用作食品袋内的抗氧化剂D.镁燃烧发出耀眼的白光,可以制造照明弹【答案】B【解析】A.细菌是由蛋白质构成的,铜是重金属,可使蛋白质变性,从而杀灭细菌,故A 正确;B.明矾溶于水生成胶状物可吸附悬浮于水中的杂质,不能除掉可溶性杂质和细菌等,不能起到消毒杀菌的作用,故B错误;C.铁粉具有还原性,易与氧气反应,可作食品抗氧化剂,故C正确;D.镁能在空气中燃烧发出耀眼的白光,可以用于制造照明弹,故D正确;故答案选B。
2019高考化学一轮复习选习练题含解析新人教版(全套10份)

人教化学2019高考一轮选习练题(1)含答案李仕才一、选择题1、对物质的量的理解正确的是()A.物质的量就是物质的质量的另一种表达方式,单位是g/molB.物质的量就是物质的数量,数值上等于式量,单位是molC.物质的量就是6.02×1023个微粒的质量,单位是gD.物质的量是国际单位制中的一个物理量,表示含有一定数目微粒的集体【答案】D2、下列离子方程式书写正确的是()A.NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性:H++OH-+Ba2++SO42-=H2O+BaSO4↓B.FeBr2溶液中通入足量的Cl2:2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-C.用两个铜电极电解食盐水:2Cl-+2H2O=2OH-+H2↑+Cl2↑D.用三氯化铁溶液腐蚀印刷线路板:Fe3++Cu=Fe2++Cu2+【答案】B【解析】A.溶液呈中性的反应为:2H++2OH-+Ba2++SO42-=2H2O+BaSO4↓,A错误;B.Cl比Br的非金属性强,能将Br-氧化,同时将铁离子氧化,根据电荷守恒和物料守恒,B正确;C.阳极为金属时,将首先失去电子生成Cu2+,负极为H得到电子生成氢气,C错误;D.未配平,2Fe3++Cu=2Fe2++Cu2+,D错误。
故选择B。
3、下列物质的性质和用途描述错误的是A.铜质地漏具有独特的杀菌功能,能较好的抑制细菌生长B.明矾溶于水生成氢氧化铝胶体,起消毒杀菌的作用C.铁粉具有还原性,可用作食品袋内的抗氧化剂D.镁燃烧发出耀眼的白光,可以制造照明弹【答案】B【解析】A.细菌是由蛋白质构成的,铜是重金属,可使蛋白质变性,从而杀灭细菌,故A正确;B.明矾溶于水生成胶状物可吸附悬浮于水中的杂质,不能除掉可溶性杂质和细菌等,不能起到消毒杀菌的作用,故B错误;C.铁粉具有还原性,易与氧气反应,可作食品抗氧化剂,故C正确;D.镁能在空气中燃烧发出耀眼的白光,可以用于制造照明弹,故D正确;故答案选B。
2019高考化学一轮训练学题含解析新人教版(全套共12份)

人教化学2019高考一轮训练学题(1)李仕才一、选择题1、常温下,在水溶液中发生如下反应①16H++10C-+2XO-4===2X2++5C2+8H2O;②2A2++B2===2A3++2B-;③2B-+C2===B2+2C-。
下列说法错误的( )A.反应C2+2A2+===2A3++2Cl-可以进行B.还原性由强到弱的顺序是C->A2+>B->X2+C.氧化性由强到弱的顺序是XO-4>C2>B2>A3+D.反应③是置换反应3、电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。
下图是KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线示意图。
下列示意图中,能正确表示用NH3·H2O溶液滴定HCl和CH3COOH混合溶液的滴定曲线的是( )解析:HCl 为强电解质,CH 3COOH 为弱电解质,滴加NH 3·H 2O ,先与HCl 反应,生成同样为强电解质的NH 4Cl ,但溶液体积不断增大,溶液稀释,所以电导率下降。
当HCl 被中和完后,继续与CH 3COOH 弱电解质反应,生成CH 3COONH 4,为强电解质,所以电导率增大。
HCl 与CH 3COOH 均反应完后,继续滴加弱电解质NH 3·H 2O ,电导率变化不大,因为溶液被稀释,有下降趋势。
固体,3·H 2+4的值都变小倍后,稀释后④溶液中的pH 大=0.001 mol·L -1,一水合氨是弱电解质,·H 2+4平衡左移,3·H 2+4的值都增大,错误;稀释后③④溶液中3、5,D5、现有下列仪器,①集气瓶;②量筒;③烧杯;④表面皿;⑤蒸发皿;⑥容量瓶;⑦圆底烧瓶。
其中能用酒精灯加热的是( ) A .②③⑤ B .③⑥⑦ C .①③④ D .③⑤⑦解析:集气瓶、量筒、表面皿、容量瓶不能加热,烧杯、圆底烧瓶要垫石棉网加热,蒸发皿可直接加热。
2019高考化学一轮选练编题(10)(含解析)新人教版

人教化学2019高考一轮选练编题(10)李仕才解析:A 项中四种离子能共存,但通入氯气后,氯气能将HSO 、I 一氧化,故不符合题意;B 项中四种离子能共存,通入二氧化硫,二氧化硫被硝酸根离子氧化而不能共存,故不符合题意; C 项中Fe 3 j CO 「之间反应生成沉淀,所以不能共存,故不符合题意; 通入二氧化碳后也不反应,故符合题意。
答案:D2.下列离子组能大量共存且加入相应试剂后发生反应的离子方程式正确的是H +,则Fe 2 j NQ 、屮发生氧化还原反应, A 选项正确;Fe 3+具有氧化性,I 「具有还原性,二者发生氧化还原反应而不能大量共存, CIO 「也具有氧化性,CIO 「与I 「也不能大量共存,B 选项错 误;C 项,加入NaOH 溶液后,发生反应的离子方程式应为 Ba 2++ HCO + OH===BaCOj + H 2O,C 选项错误;D 项,加入过量浓氨水后,会生成银氨络离子, 答案:A 3.为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有或K22颗粒的装置,它的用途是产生氧气。
下列关于N Q Q 的叙述正确的是()1. A. B. C. D.、选择题下列各离子组在溶液中能共存且通入括号中相应气体后,仍能大量存在的是 + 2 + — —Na 、Ba 、HSO 、I (氯气) Ca 、NQ 、Na 、Cl (二氧化硫) Fe 3+、SO 一、CO 一、NQ (氨气)Na +、K +、HCO 、Cl —(二氧化碳)D 项中四种离子能共存,D 选项错误。
NaOA. N&Q中阴、阳离子的个数比为1 :1B. N32Q分别与水及CO反应产生相同量的Q时,需要水和CO的质量相等C. Na2Q分别与水及CO反应产生相同量的Q时,转移电子的物质的量相等D. Na2Q的漂白原理与SQ的漂白原理相同解析:Nc t Q b的电子式为W —」Ml ,故阴、阳离子的个数比为 1 : 2, A项错误;生成相同量的Q2时消耗的水和二氧化碳的物质的量相同,但质量不同,B项错误;由得失电子守恒知二者转移电子的物质的量相同,C项正确;Na^Q因具有强氧化性而有漂白性,SQ易与有色物质化合生成无色不稳定的物质,故二者漂白原理不同,D项错误。
2019高考化学一轮复习基础习练含解析新人教版(全套共11份)

人教化学2019高考一轮基础习练(1)李仕才一、选择题1、应用(1)含答案1.下列两种气体的分子数一定相等的是( A ) A .质量相等、密度不同的N 2和C 2H 4 B .体积相等的CO 和N 2 C .等温、等体积的O 2和N 2D .等压、等体积的N 2和CH 42、我国古代文献资料中记载了大量的化学研究过程与成果。
下列选项不涉及化学变化的是( A )化,A 项符合题意;曾青的主要成分为CuSO 4,Fe 和CuSO 4发生置换反应得到Cu ,属于化学变化,B 项不符合题意;该转化过程为HgS=====△Hg +S 、Hg +S===HgS ,属于化学变化,C 项不符合题意;黏土烧结成陶瓷,有新物质生成,属于化学变化,D 项不符合题意。
3、下列做法不正确的是( B )A .Na 2O 2用作呼吸面具的供氧剂B .NaHCO 3的热稳定性强于Na 2CO 3C .乙醇可与金属钠反应放出H 2D .金属钠着火时,用细沙覆盖灭火解析 NaHCO 3的热稳定性弱于Na 2CO 3。
4、下列关于硅单质及其化合物的说法正确的是( D )①硅酸盐Na 2Fe 2Si 3O 10用氧化物的形式表示为:Na 2O·2FeO·3SiO 2 ②水泥、玻璃、水晶饰物都是硅酸盐制品 ③高纯度的硅单质广泛用于制作光导纤维 ④单质硅是将太阳能转变为电能的常用材料 A .②③ B .①③ C .①④D .④解析从化合价代数和为0可知Na2Fe2Si3O10中铁的化合价是+3价,①错误;水晶的主要成分是SiO2,②错误;光导纤维的主要成分是SiO2,③错误。
5、下列化学用语的表达正确的是( D)A.中子数为22的钙原子:22CaB.S2Cl2的结构式:S—Cl—Cl—SC.可表示CH4或CCl4分子D.氟离子的结构示意图:解析钙原子的质子数为20,中子数为22的钙原子表示为4220Ca,A项错误;根据S2Cl2中S、Cl原子最外层电子数及成键规律可知,其结构式为Cl—S—S—Cl,B项错误;根据比例模型,中间原子半径大,外面四个原子半径小,能表示CH4或CF4分子,不能表示CCl4分子,C项错误。
2019高考化学一轮复习选习练题含解析新人教版(全套10份)

人教化学2019高考一轮选习练题(1)含答案李仕才一、选择题1、对物质的量的理解正确的是()A.物质的量就是物质的质量的另一种表达方式,单位是g/molB.物质的量就是物质的数量,数值上等于式量,单位是molC.物质的量就是6.02×1023个微粒的质量,单位是gD.物质的量是国际单位制中的一个物理量,表示含有一定数目微粒的集体【答案】D2、下列离子方程式书写正确的是()A.NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性:H++OH-+Ba2++SO42-=H2O+BaSO4↓B.FeBr2溶液中通入足量的Cl2:2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-C.用两个铜电极电解食盐水:2Cl-+2H2O=2OH-+H2↑+Cl2↑D.用三氯化铁溶液腐蚀印刷线路板:Fe3++Cu=Fe2++Cu2+【答案】B【解析】A.溶液呈中性的反应为:2H++2OH-+Ba2++SO42-=2H2O+BaSO4↓,A错误;B.Cl比Br 的非金属性强,能将Br-氧化,同时将铁离子氧化,根据电荷守恒和物料守恒,B正确;C.阳极为金属时,将首先失去电子生成Cu2+,负极为H得到电子生成氢气,C错误;D.未配平,2Fe3++Cu=2Fe2++Cu2+,D错误。
故选择B。
3、下列物质的性质和用途描述错误的是A.铜质地漏具有独特的杀菌功能,能较好的抑制细菌生长B.明矾溶于水生成氢氧化铝胶体,起消毒杀菌的作用C.铁粉具有还原性,可用作食品袋内的抗氧化剂D.镁燃烧发出耀眼的白光,可以制造照明弹【答案】B【解析】A.细菌是由蛋白质构成的,铜是重金属,可使蛋白质变性,从而杀灭细菌,故A 正确;B.明矾溶于水生成胶状物可吸附悬浮于水中的杂质,不能除掉可溶性杂质和细菌等,不能起到消毒杀菌的作用,故B错误;C.铁粉具有还原性,易与氧气反应,可作食品抗氧化剂,故C正确;D.镁能在空气中燃烧发出耀眼的白光,可以用于制造照明弹,故D正确;故答案选B。
2019高考化学一轮基础选习习题10含解析新人教版

人教版化学2021高考一轮基础选习题〔10〕李仕才一、选择题1.古代的很多成语、谚语都包括着很多科学知识,以下对成语、谚语的讲解正确的选项是()A.“冰,水为之,而寒于水〞说明相同质量和温度的水和冰,冰的能量高B.“玉不琢不行器〞“百炼方能成钢〞发生的均为化学变化C.“甘之如饴〞说明糖类均有甜味D.“火树银花〞中的焰火实质上是金属元素的焰色反响剖析:相同质量的同种物质,固态的能量比液态的低,所以水和冰比较,水的能量高, A 项错误;“玉不琢不行器〞是物理变化,“百炼方能成钢〞是化学变化,B项错误;不是所有的糖类都有甜味,如淀粉、纤维素属于糖类,它们均没有甜味,C项错误。
答案: D2.我国有着悠久的文明历史,其中青铜、陶瓷、造纸及黑火药等与现代化学亲近相关。
以下说法中正确的是()A.青铜的熔点比纯铜和锡都高B.陶瓷的主要成分为硅酸盐C.古代的纸张主要成分为蛋白质D.黑火药爆炸时,氧化剂只有硝酸钾剖析:青铜是铜锡合金,合金的熔点一般比组分金属都低,A项不正确;古代的纸张主要成分是纤维素, C点燃项不正确;黑火药的主要成分是KNO3、S、C,爆炸时发生以下反响:2KNO3+3 C+S=====K2S+N2↑+3CO2↑,氧化剂是KNO3 和S,D项不正确。
答案: B3.局部氧化的Fe-Cu 合金样品( 氧化产物为Fe2O3、CuO)共5.92 g ,经以下办理:以下说法中正确的选项是()2+3++①滤液 A 中的阳离子为Fe 、Fe 、H②样品中氧元素的物质的量为0.03 mol③溶解样品的过程中耗资H2SO4 的总的物质的量为0.04 mol④V=224 mL⑤V=336 mLA.①③④B.②③④C.②③⑤D.①③⑤2+剖析:由滤液 A 中不含Cu 可知,样品中参加足量稀硫酸发生的反响有Fe+H2SO4===FeSO4+H2↑,Fe2O3+3H2 SO4===Fe2(SO4) 3+3H2O,CuO+H2SO4===CuSO4+H2O,Fe+Cu +Cu,Fe+2Fe2+===Fe2+3+===3Fe2+。
2019高考化学一轮复习训练选10含解析新人教版201809221128

2019高考化学一轮复习训练选10含解析新人教版201809221128B.MgO(s)Mg(NO3)2(aq)Mg(s)C.Al NaAlO2(aq)NaAlO2(s)D.Cu2(OH)2CO3CuO Cu(OH)2【答案】C【解析】A.氯化钠溶液与二氧化碳不能反应,故A错误;B.氧化镁溶于吸收生成硝酸镁,电解硝酸镁溶液,生成氢氧化镁沉淀,电解硝酸镁溶液不能得到金属镁,故B错误;C.铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,偏铝酸钠是强碱弱酸盐,水解生成氢氧化钠和氢氧化铝加热蒸发是蒸发水,得到偏铝酸钠,故C正确;D.CuO 和水不发生反应,不能生成氢氧化铜,故D错误;故选C。
4、下列制取SO2、验证其漂白性、氧化性并进行尾气处理的装置和原理不能达到实验目的的是A.A B.B C.C D.D【答案】B5、下列物质放入水中,会显著降温的是A.氢氧化钠 B.蔗糖 C.生石灰D.氯化铵【答案】D【解析】A.氢氧化钠溶于水放热,溶液温度升高,故A不选;B.蔗糖溶于水,热效应不明显,温度几乎无变化,故B不选;C.生石灰与水反应放出大量的热,溶液温度升高,故C不选;D.氯化铵溶于水吸热,溶液温度降低,故D选;答案选D。
6、特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如右图,A极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。
隔膜只允许特定的离子通过,电池反应式Lix C6+Li1-xCoO2C6+LiCoO2,下列说法不正确的是A.据题意分析可知该隔膜只允许Li+通过,放电时Li+从左边移向右边B.放电时,正极锂的化合价未发生改变C.废旧钴酸锂电池进行“放电处理”让Li+进入石墨中而有利于回收D.充电时阳极的电极反应式为:LiCoO2-xe-=Li1-xCoO2+xLi+【答案】C【解析】电解质是能传导Li+的高分子材料,所以隔膜只允许Li+通过,根据图示,A是负极,放电时Li+从左边移向右边,故A正确;放电时,正极Co元素化合价降低、锂的化合价未发生改变,故B正确;“放电处理”,Li+进入Li1-x CoO2中,故C错误;充电时阳极失电子发生氧化反应,电极反应式为:LiCoO2-xe-=Li1-xCoO2+xLi+,故D正确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
人教化学2019高考一轮选习练题(10)
一、选择题
1、下列解释事实的方程式中,不正确
...的是
A.铜和浓HNO3反应可用于制NO2气体:Cu+ 4HNO3((浓) = Cu(NO3)2 + 2NO2↑+ 2H2O
B.“84”消毒液中滴少量白醋可增强漂白性:ClO- + H+ = HClO
C.氨水吸收少量SO2防止污染空气:2NH3·H2O + SO2 = 2NH4+ + SO32-+ H2O
D.Na2O2在潜艇中可用于吸收二氧化碳并供氧:2Na2O2 +2CO2=2Na2CO3 + O2
【答案】B
【解析】A.铜和浓HNO3反应生成Cu(NO3)2 、NO2和H2O,反应方程式为Cu+ 4HNO3((浓) = Cu(NO3)2 + 2NO2↑+ 2H2O,故A正确;B.“84”消毒液的主要成分是NaClO,因醋酸比次氯酸的酸性强,则在“84”消毒液中滴少量白醋,醋酸可以和NaClO反应生成次氯酸,增强漂白性,但醋酸是弱酸,应写成化学式,正确的离子方程式为ClO-+CH3COOH=HClO+CH3COO-,故B错误;C.少量SO2与氨水反应生成亚硫酸铵和水,反应的离子方程式为2NH3·H2O + SO2= 2NH4++ SO32-+ H2O,故C正确;D.Na2O2与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2 +2CO2=2Na2CO3 + O2,故D正确;答案选B。
2、将0.1 mol镁和铝的混合物溶于100 mL 2 mol/L 稀硫酸中,然后滴加1 mol/L的NaOH溶液。
若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液体积的变化如图所示,下列说法正确的是
A.当V1=150 mL时,金属粉末中镁粉的质量分数为50%
B.若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=400mL。
C.若其中镁粉的物质的量分数为a,用100 mL 2 mol/L稀硫酸溶解此混合物后,再加入450 mL
1 mol/L NaOH溶液,所得沉淀中无Al(OH)3,则a的取值范围为1
2
<a<1
D.若在滴加NaOH溶液的体积为V2时,溶液中溶质为NaAlO2
【答案】D
【解析】A、当V1=150mL时,此时溶液是MgSO4、Al2(SO4)3和Na2SO4混合液,由Na+离子守恒可知,n(Na2SO4)=1/2 n(Na+)=1/2 n(NaOH)=1/2×0.15L×1mol·L-1=0.075mol,设MgSO4为xmol,Al2(SO4)3为ymol,根据Mg原子、Al原子守恒可得:x+2y=0.1,根据SO42-离子守恒可知:x+3y=0.2-0.075,联立方程解得:x=0.05、y=0.025,镁粉的物质的量分数为50%,而不是质量分数,故A错误;B、当溶液中Mg2+、Al3+恰好沉淀完全时,此时的溶液为Na2SO4溶液,根据SO42-离子和Na+离子守恒可得:n(Na+)=2n(Na2SO4)=2(H2SO4)=2×0.1L×2mol·L-1=0.4mol,所以滴入NaOH
3、向物质的量浓度均为1mol/L的HCl、AlCl3、MgC12、NH4Cl混合溶液中逐滴加入1mol/L的NaOH
溶液,得到如图图像。
下列有关说法正确的是
A.沉淀的最大物质的量为2mol
B.c-d段会产生标况下22.4LNH3
C.d-e段发生的反应为Al3++40H-=AlO2-+2H2O
D.滴加NaOH溶液过程中,微粒反应的先后顺序是H+、Mg2+、NH4+、Al(OH)3
【答案】D
4、将SO2分别通入四种不同溶液,对应的现象及结论都正确且两者具有因果关系的是
5、在下列说法中正确的是
A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.已知C(石墨,s)=C(金刚石,s)ΔH>0,则金刚石比石墨稳定
C.Ba(OH)2·8H2O与NH4Cl反应是氧化还原反应,且反应的焓变大于零
D.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1) ΔH=-57.4kJ/mol
【答案】D
6、直接煤一空气燃料电池原理如图所示,下列说法错误的是()
A.随着反应的进行,氧化物电解质的量不断减少
B.负极的电极反应式为C+2CO32--4e-=3CO2↑
C.电极X为负极,O2-向X极迁移
D.直接煤一空气燃料电池的能量效率比煤燃烧发电的能量效率高
【答案】A
7、已知反应:2NO(g)+2H2 (g)==N2 (g)+2H2O(g)生成N2的初始速率与NO、H2的初始浓度的关系为
V=kc x( NO).c y( H2),k是为速率常数。
在800℃时测得的相关数据如下表所示。
实验数据初始浓度
生成N2的初始速率、mol/(L·s) c(NO)/mol/L c(H2)/mol/L
1 2.00×10-3 6.00×10-3 1.92×10-3
2 1.00×10-
3 6.00×10-3 4.80×10-4
3 2.00×10-3 3.00×10-39.60×10-4
A.关系式中x=l、y=2
B.800℃时,k的值为8×104
C.若800℃时,初始浓度c(NO) =c( H2)=4.00×10-3 mol·L-l,则生成N2的初始速率为5.12×10-3 mol/(L·s)
D.当其他条件不变时,升高温度,速率常数是将增大
【答案】A
8、已知常温下CH3COOH和NH3·H2O的电离平衡常数分别为K a、K b。
若在常温下向0.1mol/L的醋酸
溶液中逐滴加入相同浓度的氨水直至完全过量,则下列说法正确的是
A.加入氨水的过程中,溶液的导电性一直不断增强
B.CH3COONH4在水溶液中的水解平衡常数K h=K w/(K a+K b)
C.若K a≈K b,当加入等体积的氨水时,溶液基本呈中性
D.该等式在滴加过程中始终成立c(CH3COO-)+c(CH3COOH)=c(NH4+)+c(NH3·H2O)
【答案】C
二、非选择题
元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。
已知Y元素原子最外层电子数与核外电子总数之比为3∶4,M元素原子的最外层电子数与次外层电子数之比为3∶4,且M原子的质子数是Y原子的2倍;N-、Z+、X+的半径逐渐减小;化合物XN在常温下为气体。
据此回答下列问题:
(1)写出Z与N形成的化合物的电子式________。
(2)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__________________________________(分解反应)。
(3)如图表示由上述元素组成的两种气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式
________________________________________________________________________。
(4)A、B均为由上述五种元素中的三种元素组成的强电解质,且组成元素的原子个数之比为1∶1∶1。
若在各自的水溶液中,A能抑制水的电离,B能促进水的电离,则A的化学式为________________,B 的化学式为__________________________________________。
解析:根据Y元素原子最外层电子数与核外电子总数之比为3∶4,则Y是O元素;M元素原子的最外层电子数与次外层电子数之比为3∶4,则M是S元素,N为短周期主族元素,原子序数大于S元素,N为Cl元素,根据化合物XN在常温下为气体,推断X为H,根据N-、Z+、X+的半径逐渐减小,推断Z为Na元素。
答案:(1)
(2)2H 2O 2=====MnO 2
2H 2O +O 2↑
(3)2SO 2+O 2催化剂
加热2SO 3 (4)NaOH NaClO(或NaHS)。
