电解质16 鲁科版精选教学PPT课件
合集下载
最新鲁科版化学必修1《电解质》ppt复习课件课件ppt

①①看CKO2C物3O2-3质+与2H的HC+l溶书=液CO写2 ↑形+ H式2O是(否√)正确; ②②看NNaa离+C+l溶子NO液反3与- =H应NNOa是3N溶O否液3(符×合)客观事实; ③③C看CuCu2u2是++S++O否2O4O溶HH符液- -=与=合CNCua质u(O(OHOH量溶H))2液守↓2↓(恒×和)电荷守恒; ④看是否漏掉离子反应; ④H2SO4溶液与Ba(OH)2溶液反应
子反应的式子。
交流·研讨
若稀能硫发酸生与氢的,氧你化能钡溶否仿液硫的酸反应溶液和氢氧化钡溶液从 电2H解+ 质+ 电SO离42的- +角B度a分2+析+出2O他H们- =发B生aS反O应4↓+的2实H质2O
√① NaCl 与 AgNO3
Ag+ + Cl- = AgCl↓
×② Ba(NO3)2 与 NaOH
问题 请说明下列反应实质: 迁移3 Na2CO3和盐酸的反应
Na2CO3和盐酸的反应的实质是 : CO32-与 H+结合生成碳酸, 碳酸分解为H2O和CO2气体
本质点是:
溶液中离子间结合生成了 难电离的物质和挥发性物质
一、离子反应
1、概念:在溶液中有离子参加的化学反应 叫做离子反应。
电解质溶液之间发生的反应都是 离子反应 ,使溶液中的离子浓度降低。
①NaOH溶液和H2SO4溶液的反应 H+ +OH- =H2O
②KOH溶液和盐酸的反应 H+ +OH- =H2O
③BaCl2溶液和Na2SO4溶液的反应
Ba2+ +SO42- =BaSO4↓ ④Ba(NO3)2溶液和Na2SO4溶液的反应
子反应的式子。
交流·研讨
若稀能硫发酸生与氢的,氧你化能钡溶否仿液硫的酸反应溶液和氢氧化钡溶液从 电2H解+ 质+ 电SO离42的- +角B度a分2+析+出2O他H们- =发B生aS反O应4↓+的2实H质2O
√① NaCl 与 AgNO3
Ag+ + Cl- = AgCl↓
×② Ba(NO3)2 与 NaOH
问题 请说明下列反应实质: 迁移3 Na2CO3和盐酸的反应
Na2CO3和盐酸的反应的实质是 : CO32-与 H+结合生成碳酸, 碳酸分解为H2O和CO2气体
本质点是:
溶液中离子间结合生成了 难电离的物质和挥发性物质
一、离子反应
1、概念:在溶液中有离子参加的化学反应 叫做离子反应。
电解质溶液之间发生的反应都是 离子反应 ,使溶液中的离子浓度降低。
①NaOH溶液和H2SO4溶液的反应 H+ +OH- =H2O
②KOH溶液和盐酸的反应 H+ +OH- =H2O
③BaCl2溶液和Na2SO4溶液的反应
Ba2+ +SO42- =BaSO4↓ ④Ba(NO3)2溶液和Na2SO4溶液的反应
【鲁科版】电解质PPT公开课课件1
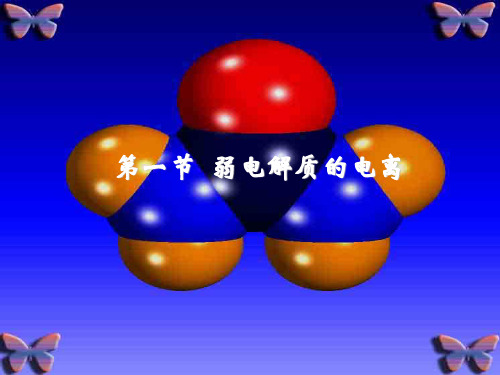
试根据课本中“一些弱酸和弱碱的电离平衡 常数”比较它们的相对强弱。
草酸>磷酸>柠檬酸>碳酸
【鲁科版】电解质PPT公开课课件1
【鲁科版】电解质PPT公开课课件1
再见 祝同学们学习进步
【鲁科版】电解质PPT公开课课件1
【鲁科版】电解质PPT公开课课件1
探究实验设计建议:
【鲁科版】电解质PPT公开课课件1
3
CH3COOH
CH3COO-+H+
电离程 n(H+) C(H+) 导电能
度
力
加水 升温
加 NH4Cl 加HCl
加 NaOH
【鲁科版】电解质PPT公开课课件1
【鲁科版】电解质PPT公开课课件1
练习
1.将0 .1mol/L的氨水稀释10倍A,C随着氨水浓度 的降低,下列数据逐渐增大的是( )
A. [H+]
B. [OH]-
C. [OH]- /[NH3·H2O] D. [NH4]+
2 .一定量的盐酸跟过量的铁粉反应时,为减
缓反应速率而不影响生成氢气的总量,可向盐
酸中加入BD适量的( )
A.NaOH(固) B.H2O C.NH4Cl(固) D.CH3COONa (固)
【鲁科版】电解质PPT公开课课件1
H2S
H++HS-
[H+]=1×10-4mol/L
HS-
H++S2-
[H+]=1×10-13mol/L
电离难的原因:
a、一级电离出H+后,剩下的酸根阴离子带
负电荷,增加了对H+的吸引力,使第二个H+离
子电离困难的多;
草酸>磷酸>柠檬酸>碳酸
【鲁科版】电解质PPT公开课课件1
【鲁科版】电解质PPT公开课课件1
再见 祝同学们学习进步
【鲁科版】电解质PPT公开课课件1
【鲁科版】电解质PPT公开课课件1
探究实验设计建议:
【鲁科版】电解质PPT公开课课件1
3
CH3COOH
CH3COO-+H+
电离程 n(H+) C(H+) 导电能
度
力
加水 升温
加 NH4Cl 加HCl
加 NaOH
【鲁科版】电解质PPT公开课课件1
【鲁科版】电解质PPT公开课课件1
练习
1.将0 .1mol/L的氨水稀释10倍A,C随着氨水浓度 的降低,下列数据逐渐增大的是( )
A. [H+]
B. [OH]-
C. [OH]- /[NH3·H2O] D. [NH4]+
2 .一定量的盐酸跟过量的铁粉反应时,为减
缓反应速率而不影响生成氢气的总量,可向盐
酸中加入BD适量的( )
A.NaOH(固) B.H2O C.NH4Cl(固) D.CH3COONa (固)
【鲁科版】电解质PPT公开课课件1
H2S
H++HS-
[H+]=1×10-4mol/L
HS-
H++S2-
[H+]=1×10-13mol/L
电离难的原因:
a、一级电离出H+后,剩下的酸根阴离子带
负电荷,增加了对H+的吸引力,使第二个H+离
子电离困难的多;
鲁科版高中化学必修一课件化学《电解质》ppt课件1.pptx

1.书写离子方程式的注意事项 (1)强酸、强碱和可溶性盐写成离子形式,弱酸、弱 碱、难溶盐、单质、氧化物、气体用化学式表示。 (2)固体之间的反应(如消石灰与氯化铵)或固体与特定 溶液(如铜和浓硫酸)的反应不能用离子方程式表示。只 有在水溶液中或熔融状态下进行的离子反应,才能写离 子方程式。 (3)对于微溶物的处理有三种情况:
2.(2008年广东高考)下列化学反应的离子方程式正确 的是( )
答案:A
2.离子的推断 (1)解题思路:依据溶液性质推出溶液中一定含有的 离子(或一定不含的离子),然后依据离子共存,推出一 定不含的离子。
(2)解题技巧 ①先看题干:如溶液颜色、pH值、酸碱性等。 ②再据溶液性质或实验现象推断。
1.下列叙述正确的是( )
①硝酸钾溶液能导电,所以硝酸钾溶液是电解质
②固态氯化钾不导电,但氯化钾是电解质
③氯化氢溶液能导电,所以氯化氢是电解质
④SO2溶于水能导电,所以SO2是电解质 ⑤铁导电,所以铁是电解质
⑥H2不导电,所以H2是非电解质
A.①④
B.②③
C.①②③④
D.④⑤⑥
答案:B
离子方程式的书写及正误判断
书写方法步骤:
a.定义完全反应物质的物质的量为1 mol。 b.找出完全反应物质各组成微粒的物质的量。 c.计算参加反应的过量物质的物质的量。 d.运用离子反应完成的条件完成反应离子方程式的 书写。
(2009年上海高三十四校联考)下列离子方程式错误 的是( )
【答案】 B
【方法技巧】 判断离子方程式的正误应抓住两 易、两等、两查:
(1)两易:易溶、易电离的物质(可溶性的强电解质 包括强酸、强碱、大多数可溶性盐)以实际参加反应 的离子的符号表示;非电解质、弱电解质、难溶物、 气体等物质用化学式表示。
2.(2008年广东高考)下列化学反应的离子方程式正确 的是( )
答案:A
2.离子的推断 (1)解题思路:依据溶液性质推出溶液中一定含有的 离子(或一定不含的离子),然后依据离子共存,推出一 定不含的离子。
(2)解题技巧 ①先看题干:如溶液颜色、pH值、酸碱性等。 ②再据溶液性质或实验现象推断。
1.下列叙述正确的是( )
①硝酸钾溶液能导电,所以硝酸钾溶液是电解质
②固态氯化钾不导电,但氯化钾是电解质
③氯化氢溶液能导电,所以氯化氢是电解质
④SO2溶于水能导电,所以SO2是电解质 ⑤铁导电,所以铁是电解质
⑥H2不导电,所以H2是非电解质
A.①④
B.②③
C.①②③④
D.④⑤⑥
答案:B
离子方程式的书写及正误判断
书写方法步骤:
a.定义完全反应物质的物质的量为1 mol。 b.找出完全反应物质各组成微粒的物质的量。 c.计算参加反应的过量物质的物质的量。 d.运用离子反应完成的条件完成反应离子方程式的 书写。
(2009年上海高三十四校联考)下列离子方程式错误 的是( )
【答案】 B
【方法技巧】 判断离子方程式的正误应抓住两 易、两等、两查:
(1)两易:易溶、易电离的物质(可溶性的强电解质 包括强酸、强碱、大多数可溶性盐)以实际参加反应 的离子的符号表示;非电解质、弱电解质、难溶物、 气体等物质用化学式表示。
【鲁科版】电解质PPT精美课件1

•
2.“我试图描写一个真正的老人,一 个真正 的孩子 ,真正 的大海 ,一条 真正的 鱼和许 多真正 的鲨鱼 。然而 ,如果 我能写 得足够 逼真的 话,他 们也能 代表许 多其他 的事物 。
•
3.后面一系列的情节都是老人的内心 表白, 一个是 与大海 与大鱼 的对话 ,一个 是自言 自语, 说给自 己听, 一个是 自己心 里的想 法。
•
7.着力追求一种含蓄、凝练的意境。 海明威 曾经以 冰山来 比喻创 作,说 创作要 像海上 的冰山 ,八分 之一露 在上面 ,八分 之七应 该隐含 在水下 。露出 水面的 是形象 ,隐藏 在水下 的是思 想感情 ,形象 越集中 鲜明, 感情越 深沉含 蓄。另 外,为 使“水 下”的 部分深 厚阔大 ,他还 借助于 象征 的手法 ,使作 品蕴涵 深意。
Ca(OH)2(S) Ca2+(aq) + 2OH-(aq)时, 为使氢氧化钙固体的量减少,需加入少量的
(双选)(AD)
A NH4NO3 C CaCl2
B NaOH D NaHSO4
【鲁科版】电解质PPT精美课件1
【鲁科版】电解质PPT精美课件1
当堂训练
2、下列有关AgCl沉淀的溶解平衡的说法中,
【鲁科版】电解质PPT精美课件1
【鲁科版】电解质PPT精美课件1
思考讨论 若要除去溶液中的SO42-离子你选择钙 盐还是钡盐?为什么? 加入可溶性钡盐.因硫酸钡的溶解度 比硫酸钙小,用Ba2+沉淀SO42-更完全
【鲁科版】电解质PPT精美课件1
【鲁科版】电解质PPT精美课件1
当堂训练
1、当氢氧化钙固体在水中达到溶解平衡
•
8.围绕本专题的话题,通过组织讨论 ,要求 学生把 人生积 累和经 验带入 文本, 演绎自 己的认 识,与 文本化 为一体 ,在大 师的思 想沐浴 下真正 得到一 次精神 的洗礼 。最后 ,还可 要求学 生在鉴 赏文章 观点表 达充满 诗意的 基础上 ,也动 手用形 象隽永 的语言 来概括 对本板 块话题 的理性 认识, 并在交 流的过 程中升 华自己 的思想 。
化学课件《电解质》优秀ppt16 鲁科版
91.要及时把握梦想,因为梦想一死,生命就如一只羽翼受创的小鸟,无法飞翔。――[兰斯顿·休斯] 92.生活的艺术较像角力的艺术,而较不像跳舞的艺术;最重要的是:站稳脚步,为无法预见的攻击做准备。――[玛科斯·奥雷利阿斯] 93.在安详静谧的大自然里,确实还有些使人烦恼.怀疑.感到压迫的事。请你看看蔚蓝的天空和闪烁的星星吧!你的心将会平静下来。[约翰·纳森·爱德瓦兹]
[回顾问题1]
溶•• 液、浊液、胶体的本质区别是什么?
• 分• 散系
浊液
胶体
溶液
悬浊>1液0-乳7m浊液 10-7~10-9m <10-9m
[回顾问题2]
溶液、胶体区分方法是什么?
丁达尔效应
CuSO4溶液
Fe(OH)3胶体
课题:电解质
连云港开发区高级中学 高一备课组 2009.9
•【学习目标】
物既不是电解质也不是非电解质。 • 2.电解质的导电是有条件的,盐、碱电解质在水
溶液里和熔化状态下都能导电,而酸电解质只有 在水溶液里才能导电。 • 3.有些非电解质的水溶液也能导电,如CO2、SO2、 NH3等,因为它们与水反应生成了电解质。
CO2+H2O=H2CO3 SO2+H2O=H2SO3
• 【自学探究2】 • 它们为什么导电?
盐酸、硫酸溶液、氢氧化钠溶 液 、食盐水、 硫酸铜溶液
合 物
④金属氧化物、碱、盐的熔融体
熔融的氯化钠、熔融的氧化钠、熔融的氢氧化钠
电解质与非电解质的概念:
{ 化合物
电解质:在水溶液中或者熔融状态下能 ▲
导电的化合物。
非电解质:在水溶液中和▲熔融状态下
均以分子形式存在,
都不能导电的化合物。
• 注意点: • 1.电解质和非电解质都是指化合物,单质和混合
[回顾问题1]
溶•• 液、浊液、胶体的本质区别是什么?
• 分• 散系
浊液
胶体
溶液
悬浊>1液0-乳7m浊液 10-7~10-9m <10-9m
[回顾问题2]
溶液、胶体区分方法是什么?
丁达尔效应
CuSO4溶液
Fe(OH)3胶体
课题:电解质
连云港开发区高级中学 高一备课组 2009.9
•【学习目标】
物既不是电解质也不是非电解质。 • 2.电解质的导电是有条件的,盐、碱电解质在水
溶液里和熔化状态下都能导电,而酸电解质只有 在水溶液里才能导电。 • 3.有些非电解质的水溶液也能导电,如CO2、SO2、 NH3等,因为它们与水反应生成了电解质。
CO2+H2O=H2CO3 SO2+H2O=H2SO3
• 【自学探究2】 • 它们为什么导电?
盐酸、硫酸溶液、氢氧化钠溶 液 、食盐水、 硫酸铜溶液
合 物
④金属氧化物、碱、盐的熔融体
熔融的氯化钠、熔融的氧化钠、熔融的氢氧化钠
电解质与非电解质的概念:
{ 化合物
电解质:在水溶液中或者熔融状态下能 ▲
导电的化合物。
非电解质:在水溶液中和▲熔融状态下
均以分子形式存在,
都不能导电的化合物。
• 注意点: • 1.电解质和非电解质都是指化合物,单质和混合
化学必修鲁科版电解质课件第一课时

阴阳离子、未电离的分 子
存在微粒
实例 方程式
NaCl HCl NaOH NaOH
醋酸 氨水 水
H+
14
Na++OH- CH3COOH +CH3COO-
化合物
一定条件 是否电离
不电离
电离
非电解质
电解质
在水溶液中
全部 电离
部分 电离
强电解质
弱电解质
15
练习:
1、下列物质能导电的是(AB ) A.熔融的氯化钠 B、KNO3溶液 C、硫酸铜晶体 D、无水乙醇 2、下列电离方程式中,不正确的是( ACD ) A、Al2(SO4)3=2Al3++3SO4-2 B、HCl=H++ClC、 CH3COOH =H+ +CH3COOD、Na2CO3=Na++CO3216
移
定向移动
电
动 电子
6
NaCl溶液、熔融NaCl导电的原因:
液体中有离子,且离子能自由移 动 晶体食盐不导电的原因: 离子不能自由移 动 决定溶液导电性强弱的因素:
溶液中自由移动离子浓度的大小
7
2、电解质的电离
Na+
Cl-
食 盐 的 电 离
8
2、电解质的电离
(1)电离: 物质溶于水或受热熔化时,离解成 能够自由移动的离子的过程,称为电离。
BaSO4、AgCl 、CaCO3 NaCl、K2SO4等
完全
②弱电解质:
两者本质区别 电离程度不同
弱酸: H2CO3、CH3COOH、HClO等 弱碱: NH · 3 H2O等
部分
13
总结:
定义 物质类型 电离程度 电离过程
存在微粒
实例 方程式
NaCl HCl NaOH NaOH
醋酸 氨水 水
H+
14
Na++OH- CH3COOH +CH3COO-
化合物
一定条件 是否电离
不电离
电离
非电解质
电解质
在水溶液中
全部 电离
部分 电离
强电解质
弱电解质
15
练习:
1、下列物质能导电的是(AB ) A.熔融的氯化钠 B、KNO3溶液 C、硫酸铜晶体 D、无水乙醇 2、下列电离方程式中,不正确的是( ACD ) A、Al2(SO4)3=2Al3++3SO4-2 B、HCl=H++ClC、 CH3COOH =H+ +CH3COOD、Na2CO3=Na++CO3216
移
定向移动
电
动 电子
6
NaCl溶液、熔融NaCl导电的原因:
液体中有离子,且离子能自由移 动 晶体食盐不导电的原因: 离子不能自由移 动 决定溶液导电性强弱的因素:
溶液中自由移动离子浓度的大小
7
2、电解质的电离
Na+
Cl-
食 盐 的 电 离
8
2、电解质的电离
(1)电离: 物质溶于水或受热熔化时,离解成 能够自由移动的离子的过程,称为电离。
BaSO4、AgCl 、CaCO3 NaCl、K2SO4等
完全
②弱电解质:
两者本质区别 电离程度不同
弱酸: H2CO3、CH3COOH、HClO等 弱碱: NH · 3 H2O等
部分
13
总结:
定义 物质类型 电离程度 电离过程
【鲁科版】电解质PPT课件分析1

SP
1、定义
在一定条件下,难溶性电解质形成饱和溶液,达到溶解 平衡,其溶解平衡常数叫做溶度积常数或简称溶度积.
2.表达式:
AmBn(s)
mAn+(aq)+nBm-(aq)
Ksp, AnBm= [An+]m . [Bm-]n
例:写出下列难溶电解质的溶解平衡关系式和溶度
积表达式。
AgBr
Ag+ + Br-
变
例题(2) 石灰乳中存在下列平衡: Ca(OH)2(s) ≒ Ca2+(aq)+2OH-(aq),加入下列溶液,可使
Ca(OH)2减少的是( AB ) A、Na2CO3溶液 B、AlCl3溶液 C、NaOH溶液 D、CaCl2溶液
【鲁科版】电解质PPT课件分析1
【鲁科版】电解质PPT课件分析1
(6)溶解平衡常数—溶度积KSP
溶解度与溶解性的关系:20℃
难溶 微溶
可溶
0.01
1
易溶
10 S /g
1、问题讨论: Ag+和Cl-的反应能进行到
底吗?
【实验】向盛有2 mL 0.1mol/LAgNO3溶液的试 管中加入2 mL 0.1 mol/L NaCl溶资液料。:化学上通常认
(1)、恰好反应没有?
为残留在溶液中的离 子浓度小于10-5 mol/L
解: Fe(OH)3
Fe3+ + 3OH-
Fe3+ 沉淀完全时的[OH-]为:
[OH-] 3
K sp [Fe3 ]
3
4.0 1039 1105
1.5 1011 mol L1
pOH = 10.8 , pH = 3.2
【鲁科版】电解质PPT课件分析1
鲁科版电解质ppt课件下载完美版2

❖
3.在施工全过程中,严格按照经招标 人及监 理工程 师批准 的“施 工组织 设计” 进行工 程的质 量管理 。在分 包单位 “自检 ”和总 承包专 检的基 础上, 接受监 理工程 师的验 收和检 查,并 按照监 理工程 师的要 求,予 以整改 。
❖
、4.贯彻总包单位已建立的质量控制 、检查 、管理 制度, 并据此 对各分 包施工 单位予 以检控 ,确保 产品达 到优良 。总承 包对整 个工程 产品质 量负有 最终责 任,任 何分包 单位工 作的失 职、失 误造成 的严重 后果, 招标人 只认总 承包方 ,因而 总承包 方必须 杜绝现 场施工 分包单 位不服 从总承 包方和 监理工 程师监 理的不 正常现 象。
❖
5.所有进入现场使用的成品、半成品 、设备 、材料 、器具 ,均主 动向监 理工程 师提交 产品合 格证或 质保书 ,应按 规定使 用前需 进行物 理化学 试验检 测的材 料,主 动递交 检测结 果报告 ,使所 使用的 材料、 设备不 给工程 造成浪 费。
❖
谢谢观看
例如: CO2、 SO2、 SO3、 NH3不是电解质 H2CO3、H2SO3 、 H2S分金属氧化物:CaO、Na2O、Al2O3 ② 酸、碱、盐:HCl、NaOH、BaSO4 ③水
【练习1】判断对错: A 铁能导电,所以铁是电解质 B 氯化钙溶液能导电,所以氯化钙溶液 是电解质
(2)弱电解质
微粒存在: 分子和离子
常见的弱电解质
① 弱酸:
H3PO4、H2CO3 、CH3COOH ② 弱碱:
③水
NH3·H2O、 难溶金属氢氧化物
❖
1.我公司将积极配合监理工程师及现 场监理 工程师 代表履 行他们 的职责 和权力 。
❖
鲁科版高中化学必修一课件化学《电解质》ppt课件.pptx

4、电解质在水溶液和熔融状态下都能导电(× )
【练习2】
下列物质能导电的有( 3、4、7、10 )
其中属于电解质的是( 1、2、3、9
)
属于非电解质的是( 1.液态HCl 2.固体NaCl
6
、3.8熔融NaCl
)
4.KNO3溶液 5.蔗糖溶液 6.CO2 7.铜 8.乙醇 9.纯硫酸 10.氨水
知识总结
A.熔融氢氧化钠
B.石墨棒
C.盐酸溶液
D.固态氯化钾
3、下列电离方程式中,正确的是 ( C )
A. Al2(SO4)3=2Al+3+3SO4-2 B. HClO = H++ClO-
C. HCl = H+ +Cl-
D. Na2CO3=Na++CO32-
4. 下列叙述正确的是( )D
A. 液态HCl、固态NaCl均不导电,所以HCl和 NaCl均为非电解质
NaHSO4能电离出金属阳离子和酸根 阴离子,属于盐。
强电解质:在水溶液里全部电离成离子的电解质
弱电解质: 在水溶液里只部分电离成离子的电解
质
强电解质的电离:H2SO4 = 2H+ + SO42Na2CO3=2Na++CO32HCl = H+ + Cl-
弱电解质的电离:
CH 3COOH
H CH3COO
【反思】:在理解电解质和非电解质的概念 中应注意什么?
①电解质和非电解质是化合物,单质、混 合物既不是电解质也不是非电解质。
②能导电的不一定是电解质;电解质也不 一定能导电。
③必须是在一定条件下,本身发生电离而导电的化合物。
活动·探究
【练习2】
下列物质能导电的有( 3、4、7、10 )
其中属于电解质的是( 1、2、3、9
)
属于非电解质的是( 1.液态HCl 2.固体NaCl
6
、3.8熔融NaCl
)
4.KNO3溶液 5.蔗糖溶液 6.CO2 7.铜 8.乙醇 9.纯硫酸 10.氨水
知识总结
A.熔融氢氧化钠
B.石墨棒
C.盐酸溶液
D.固态氯化钾
3、下列电离方程式中,正确的是 ( C )
A. Al2(SO4)3=2Al+3+3SO4-2 B. HClO = H++ClO-
C. HCl = H+ +Cl-
D. Na2CO3=Na++CO32-
4. 下列叙述正确的是( )D
A. 液态HCl、固态NaCl均不导电,所以HCl和 NaCl均为非电解质
NaHSO4能电离出金属阳离子和酸根 阴离子,属于盐。
强电解质:在水溶液里全部电离成离子的电解质
弱电解质: 在水溶液里只部分电离成离子的电解
质
强电解质的电离:H2SO4 = 2H+ + SO42Na2CO3=2Na++CO32HCl = H+ + Cl-
弱电解质的电离:
CH 3COOH
H CH3COO
【反思】:在理解电解质和非电解质的概念 中应注意什么?
①电解质和非电解质是化合物,单质、混 合物既不是电解质也不是非电解质。
②能导电的不一定是电解质;电解质也不 一定能导电。
③必须是在一定条件下,本身发生电离而导电的化合物。
活动·探究
高中化学鲁科版必修电解质教学课件

Cu2++SO42-+Ba2++2Cl-=BaSO4↓+Cu2++2Cl-
查: 原子是否守恒 ,电荷是否守恒
SO42-+Ba2+=BaSO4↓
高中化学鲁科版必修电解质
高中化学鲁科版必修电解质
问题 探究
1、电流计指针由大到小说明了什么? 2、溶液的颜色为什么由红色变为无色? 3、猜测白色沉淀的成分及形成的由来。 4、H2SO4与Ba(OH)2反应的实质是什么?
高中化学鲁科版必修电解质
高中化学鲁科版必修电解质
问题 讨论
H2SO4与Ba(OH)2分别属于酸、碱类的电解质
4、它有相应的书写方式,即离子方程式。
高中化学鲁科版必修电解质
问题 讨论1 什么是离子方程式?
电解质溶液间的反应实质上是离子 间的反应,顾名思义,离子方程式就是 为真实地反映电解质溶液反应的实质, 而用实际参加反应的离子的符号来表示 离子反应的式子。
问题 讨论2 如何书写离子方程式?
1、要符合反应事实; 2、要符合质量守恒定律; 3.要符合电荷守恒原则。
高中化学鲁科版必修电解质
必考部分
高中化学必修1
第2讲 离子反应
高中化学鲁科版必修电解质
知识 回顾 对电解质的初步了解
1、电解质是具有特定性质的化合物
(在水溶液或熔融状态下能导电)
2、酸、碱、盐是电解质(在水溶液或熔融状态下能导电)
3、酸、碱、盐能发生电离(在水溶液或熔融状态下)
4、电解质溶液的导电能力与溶液中自由 移动的 离子的浓度大小成正比
问题 思考
1、电解质溶液间的反应与离子有 何关系?
2、电解质在水溶液中反应的本质 是什么?
化学课件《电解质》优秀ppt18(4份) 鲁科版1

电解质导电条件的探究 【质疑】:固体氯化钠不导电,而氯化钠溶液和熔融 态的氯化钠都有导电能力是什么原因?
结论
电解质的导电是 需要(填“需要”或“不需要”)条件的
物质
√×
1、完成学案中的判断×正误:
(1)某化合物不是电解质就一定是非电解质。
(2)铜和石墨都能导电,它们×都是电解质;Cl2不能导电,
(2)①④⑩⒁;(3) ②⑦⑿⒀;
(4)⑥⑧;(5)③⑤⑾
85.每一年,我都更加相信生命的浪费是在于:我们没有献出爱,我们没有使用力量,我们表现出自私的谨慎,不去冒险,避开痛苦,也失去了快乐。――[约翰·B·塔布] 86.微笑,昂首阔步,作深呼吸,嘴里哼着歌儿。倘使你不会唱歌,吹吹口哨或用鼻子哼一哼也可。如此一来,你想让自己烦恼都不可能。――[戴尔·卡内基]
87.当一切毫无希望时,我看着切石工人在他的石头上,敲击了上百次,而不见任何裂痕出现。但在第一百零一次时,石头被劈成两半。我体会到,并非那一击,而是前面的敲打使它裂开。――[贾柯·瑞斯] 88.每个意念都是一场祈祷。――[詹姆士·雷德非]
89.虚荣心很难说是一种恶行,然而一切恶行都围绕虚荣心而生,都不过是满足虚荣心的手段。――[柏格森] 90.习惯正一天天地把我们的生命变成某种定型的化石,我们的心灵正在失去自由,成为平静而没有激情的时间之流的奴隶。――[托尔斯泰]
因此电离是电解质导电的前提。
练练: 写出HNO3 、Ca(OH)2 、Al2(SO4)3、 (NH4)2SO4 的电离方程式
多学一点: 电解质可分为强电解质和弱电解质 本质区别:是否完全电离 强电解质包括:强酸、强碱、盐等 弱电解质包括:弱酸、弱碱、水等 电离方程式中的“==”用“ ”代替
完成学案中的例题和电离方程式
化学电解质第一课时课件鲁科版必修[可修改版ppt]
![化学电解质第一课时课件鲁科版必修[可修改版ppt]](https://img.taocdn.com/s3/m/7f8b014cec3a87c24128c455.png)
一 ①HNO3
HNO3=H++NO3-
练
② H2SO4 H2SO4 = 2H+ + SO42-
③KOH
KOH=K++OH-
④Ba(OH)2 Ba(OH)2 = Ba2++ 2OH-
下列叙述正确的是
(D )
A、固体氯化钠不导电,所以氯化钠是非电解质
B、铜丝能导电,所以铜是电解质
C、二氧化碳溶于水能导电,所以二氧化碳是电解质
4、常见的强电解质:强酸、强碱、大多数盐;常见的弱电解质:_____
弱酸、弱碱、水
总结:
强弱电解质比较
强电解质
弱电解质
定义 物质类型 电离程度 电离过程 存在微粒
水溶液全部电离
水溶液部分电离
强酸、强碱、大部分盐 活泼金属氧化物
弱酸、弱碱、水
完全电离
只有部分电离
不可逆
可逆过程
阴、阳离子
阴阳离子、未电离的分子
① 4、N下a2S列O4电离方②程(N式H4中)2S,O4错误的③是Na(HScO4 ) ④ NaHCO3
A.Al2(SO4)3 = 2Al3 + +3SO42B.FeCl3 = Fe3+ + 3ClC. CH3COOH =H+ +CH3COOD.Na2CO3 = 2Na+ + CO32-
下列物质既不是电解质,也不是非电解质的(C )
A、Na2SO4 C、Cl2
B、酒精 D、HCl
[分组讨论]
电解质的导电原理与金属导电有什么不同吗?
电解质在溶液中 存在
熔融态的电解质中
存在
金属内部
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
• 电解质概念、电离方程式的书写
• 【自学探究1】
• 依据你所学的知识或身边生活或查阅 相关资料或网上查询等手段,请尽可 能多地列举出能导电的物质,并给予 分类。
①金属: Cu、Fe、Al等
单
②非金属: 石墨
质
③酸、碱、盐的水溶液:
化
盐酸、硫酸溶液、氢氧化钠溶 液 、食盐水、 硫酸铜溶液
合 物
④金属氧化物、碱、盐的熔融体
事十之八九,如若我们不抱怨,湖涂一些,淡然一点,烦恼就会少些,日子即便是平庸,但也能活得踏实、安稳、快乐。在时间的渡口,我们都是匆匆的过客,多一抹微笑,就会多一个睛朗
走在人生路上,最神奇的是你的微笑。我们生存的空间,本来就单调的,有你的微笑,就能让它变得多姿多彩;我们生活的方式,本来就枯燥的,有你的微笑,能让它变得生动活泼和美好。微笑,会 笑,能淹没心中的痛苦,微笑,还能给人以自信。有一种生活写照叫“笑口常开”,有一种人生观叫“知足常乐”,有一种状态叫“乐在其中”,有一种大度叫“一笑抿恩仇”。人生最重要的,是保特一
{ { 化合物
电解质
强电解质 弱电解质
=
非电解质
,又何必对未知的前方魂牵梦萦?生活中,其实我们每个人都有目标,并且我们的奋斗,都是为了能离它更近。奋斗努力,快步走行,无可厚非,但是我想,人生在路上行走,本应该走走停停,该歇的则 放慢脚步,看看你的身边,看看你的周围,欣赏一下沿途的美丽风景,也许里面就有会你想要的东西。不要为了追求物质财富,不要忙于到达目的地,只顾疲于奔跑,而错过了身边美丽的风景,不要让你
熔融的氯化钠、熔融的氧化钠、熔融的氢氧化钠
电解质与非电解质的概念:
{ 化合物
电解质:在水溶液中或者熔融状态下能 ▲
导电的化合物。
非电解质:在水溶液中和▲熔融状态下
均以分子形式存在,
都不能导电的化合物。
• 注意点: • 1.电解质和非电解质都是指化合物,单质和混合
物既不是电解质也不是非电解质。 • 2.电解质的导电是有条件的,盐、碱电解质在水
有微笑的画卷,这画便会显得亮丽多彩;人生如酒,有微笑的美酒,这酒便能散发出诱人的醇香;人生如歌,有微笑的歌声,这首歌便多了动人的旋律;人生如书,充满着微笑的这本书里,书中篇篇都是快乐的篇章。微笑着,走好自己的路,让一路上留下欢乐和喜悦,同时,你也将会得
春夏秋冬大千世界,芸芸众生,我们每个人就像一粒小小的尘埃,于春夏秋冬的轮回里,在风风雨雨中飘渺,在阳光下微笑人的一生中,会品尝着各种酸甜苦辣的味道,当回眸看看所走过的路程,会让我们渐渐明白一个道理:人需有一颗淡然的心来对待这世间百态,需用一颗平常心简简单单过好生活,因为淡然,会使人简单,简单了,就有快乐。 在忙碌的生活里,谁都会遇到难处,在现实的生活中,谁都有苦楚,人的一生,总是有一些纠结,会让我们无助;总是有太多的奈何,会让我们无可。所以,有些事,可以认真对待,但不可去较真。当然,说说容易,做起来可能就较难,很多时候,我们往往会始终执着一个人,一件事,一段情,这种执着仅仅是一种执念也就罢了,有些封存的往事,只会让你显得落寞和孤寂,将岁月纠结于此,往往让人痛不欲生。岁月静好,可是,你的人生并非安好,许多的事,我们自己是做不了主的,对人生旅途中的风景,我们也没有能力做出选择,但是我们可以对自己的心态进行调整,时不常地换个角度待人看
要怨天怨地怨人怨己,抱怨自己的人生磕磕绊绊,不如人意。要知道很多时候,当在你盲目地追求着你的目标后,当你在怨天怨地怨人怨己时,回过头来看时,可能会发现:许多的美
人的生命总是有限的,时间也不能停滞,但是我们可以驻足。人生路上,一路行走,一路都是风景,路上,你会遇到很多美的人,美的事,美的景。不要忘了经常抬头凝视一会儿蔚蓝的天空和飞翔的 香气。在人生的风景里有春夏秋冬,会有不同景致,春葱茏、夏繁盛、秋斑斓、冬纯净,都显得很美丽,你大凡可尽收眼底。只不过人生的风景画册里,有的柔和,有的热烈,有的凄美,还有的悲壮,只 生就会轻松很多。也许在你放松心境的时候,你就能看见生活的笑容。不同的人生体验,才能让人生多彩丰富。如果太在意目的地,这一路上,心中便会少了很多乐趣。在人生的旅行中,最重要的不是结
③酸、碱、盐的水溶液:
自
由
盐酸、硫酸溶液、氢氧化钠溶 移
液 、食盐水、 硫酸铜溶液
动 的
④金属氧化物、碱、盐的熔融体
离 子
电离:
酸、碱、盐等电解质在溶液中或熔融 状态下产生自由移动的离子过程
电离方程式: 表示电解质电离成自由移动的离子过
程的式子
电离方程式书写步骤:
1、在方程式左边写出化学式
2、在方程式右边书写阴、阳离子符号前面配上系数
溶液里和熔化状态下都能导电,而酸电解质只有 在水溶液里才能导电。 • 3.有些非电解质的水溶液也能导电,如CO2、SO2、 NH3等,因为它们与水反应生成了电解质。
CO2+H2O=H2CO3 SO2+H2O=H2SO3
• 【自学探究2】 • 它们为什么导电?
导电原因
①金属:Cu、Fe、Al等 自由电子定向移动 ②非金属: 石墨
对生活 。
为了在旅途结束时不留下丝毫的遗憾,请把握好旅程中的每一分钟。一路上慢慢地走,别忘了欣赏沿途的风景。
作者简介:谈笑在指尖 原名:张 波文章,诗歌多见于省内外报刊和网络平台。喜欢把日子中的点点滴滴写进文字里,抒写心中之梦,始终保持着乐观心态,过好每一天。滴写进文字里,雀巢冰泣淋裡 形的冰棍我要用它来纪念他们的爱情。
作者简介:谈笑在指尖 文章,诗歌多见于省内外报刊和网络平台。喜欢把日子中的点点滴如同一次旅行,一次不清楚哪里是终点的旅行。在人生的旅程中,有些人走的很从容,一边走一边欣赏着沿途的风景,春天踏青,感受万物复苏时生命的萌动;夏日赏荷,嗅闻花儿的芳香,聆听悠扬的蝉鸣;秋时听风,欣赏落叶在秋风中忘情的舞动;冬日品雪,品味银装素裹的晶莹,让自己的人生如四季绚烂,多姿多彩。有些人却是步履匆匆,他们只顾埋头盯着脚下的道路,拼命的赶完余下的旅程,一路上,只顾疲于奔跑,疲于生存,疲于生,看不见路边花儿的美丽,也注意不到蔚蓝天空中白云的漂浮,一心只忙于到达目的地,一程又一
谢谢欣赏! 四季辗转中,当遇春风,必有柳绿花红,当入夏凉,便能闻荷风送香,当沐浴在秋风里,必能有丰盈的成熟,当见冬雪时,便能够净化灵魂。每天的生活虽然都过得普普通通,可每一段路上我们
走在人生路上,最宝贵的是你的微笑。人的一生会遭遇许多坎坷,经历许多风雨,纵然前面充满荆棘,也必须走下去。微笑着,无论是在平淡的日子里,还是在迷茫低落的时候,都让自己内心尽量靠 你对未来充满着信心,眼前的困难只是暂时的,没什么可畏惧!微笑着,证明了你的意志是无比的坚强,既然确定了目标就去奋斗,一切的阻挠都显得可笑和无力,丝毫都不能让你停顿半步。你脸上的微
笑,就像是那照亮天空的火炬,能使你的眼前永远闪耀着光明与希望;你脸上的微笑,能催你不断奋进向前,让你的生命里充满激情与活力。748219
走在人生路上,最不可少的是你的微笑。人生之路,鲜花和荆棘映衬,坦途和坎坷衔接,艳阳和风雨交织,得志和失意错位。生活给予你的,有精彩,更多的是平淡。人生,不会事事如意,生活,也 事,都不由我们做主。我们最重要的不是要去计较真与伪,得与失,名与利,贵与贱,贫与富,而是要想想,如何好好地快乐度日,并从中发现生活的诗意。尽管日子很平淡,却会有许多的闪光点,尽管
3、检验“=”两边是否守恒(质量、电荷)
• H2SO4=2H++SO42• HCl= H++Cl• NaOH= Na++OH-
• Ca(OH)2=Ca2++2OH• NaCl= Na++Cl• MgCl2= Mg2++2Cl-
书写时注意事项:
1、 适用范围: 电解质的电离。 2、 用的是等号。 3、根据化合价写离子符号。 4、根据右下角系数写离子个数。
• 1.完成下列电离方程式
• (1) Na2CO3 =2Na++CO32• (2)KClO3= K++ClO3• (3)Fe2(SO4)3 = 2 Fe3++ 3 SO42• (4)Ba(OH)2 =Ba2++ 2 OH-
(5)CH3COOH
CH3COO-+H+
(6)NH3·H2O
NH4++OH-
电离方程式:
复习巩固
[回顾问题1]
溶液、浊液 、胶体 的本质区别是什么?
分散系
粒子直径
浊液
悬浊液 乳浊液
>10-7m
胶体 10-7~10-9m
溶液 <10-9m
[回顾问题2]
溶液、胶体区分方法是什么?
丁达尔效应
CuSO4溶液
Fe(OH)3胶体
•【学习目标】
• 掌握电解质的概念, • 并会书写电离方程式
•【学习重难点】
辉和莉是在网络上认识的,莉比辉大5岁。2000年初秋的一天,他们相识了,以后的日子,他们相知了,彼此以姐弟相称。第一次他给她写信是在圣诞节,当时仅仅是 后来,他爱上了她,一个让辉用三生三世都不能忘记的女人。 2001年的2月10日,值得纪念的日子,辉告诉了莉他心裡的想法!因為莉是从艰辛中一路走来身心疲惫的人,深知道爱就要付出什麼,她没有
清弦坠满心事,弹落片片梦幻,我该如何用这弦、这韵去丈量你我天涯的距离,一滴泪上的墨香,如何画下你最爱的睡莲? 清影摇曳,眉眼如水,缓缓来到钢琴前为你弹一曲你最爱的《莫失莫忘》,让我借琴声悄悄告诉天涯的你:今夜,我想喜欢一句话:能让人生灿烂的不只有阳光
每天早上醒来,打开心灵的窗户,让阳光照射进来,你的心中便会亮堂堂,既便是在任何季节,也不会觉得孤单寒凉。每天当你迈开双腿,将微笑挂在脸上,你的步伐便会走的轻松和稳当。携着阳光
凡事都是多棱镜,不同的角度会看到不同的结果。若能把一些事看淡了,就会有个好心境,若把很多事看开了,就会有个好心情。让聚散离合犹如月缺月圆那样寻常,让得失利弊犹如花开花谢那样自然,不计较,也不刻意执着;让生命中各种的喜怒哀乐,就像风儿一样,来了,不管是清风拂面,还是寒风凛冽,都报以自然的微笑,坦然的接受命运的馈赠,把是非曲折,都当作是人生的定数,不因攀比而困惑,不为贪婪而费神,无论欢乐还是忧伤,都用平常心去接受;无论得到还是失去,都用坦然的心去面对,人生原本就是在得与失中轮回的,让一切所有的经历,都化 人的一生说白了,也就是三万余天,贫穷与富贵,都是一种生活境遇。懂得爱自己的人,对生活从来就没有过高的奢望,只是对生存的现状欣然接受。漠漠红尘,芸芸众生皆是客,时光深处,流年似水,转瞬间,光阴就会老去,留在心头的,只是弥留在时光深处的无边落寞。轻拥沧桑,淡看流年,掬一捧岁月,握一份懂得,红尘纷扰,我自心安;书一笔清远,盈一抹恬淡,浮华三千,只做自己;人间有情,心中有爱,携一米阳光,微笑向暖。
• 【自学探究1】
• 依据你所学的知识或身边生活或查阅 相关资料或网上查询等手段,请尽可 能多地列举出能导电的物质,并给予 分类。
①金属: Cu、Fe、Al等
单
②非金属: 石墨
质
③酸、碱、盐的水溶液:
化
盐酸、硫酸溶液、氢氧化钠溶 液 、食盐水、 硫酸铜溶液
合 物
④金属氧化物、碱、盐的熔融体
事十之八九,如若我们不抱怨,湖涂一些,淡然一点,烦恼就会少些,日子即便是平庸,但也能活得踏实、安稳、快乐。在时间的渡口,我们都是匆匆的过客,多一抹微笑,就会多一个睛朗
走在人生路上,最神奇的是你的微笑。我们生存的空间,本来就单调的,有你的微笑,就能让它变得多姿多彩;我们生活的方式,本来就枯燥的,有你的微笑,能让它变得生动活泼和美好。微笑,会 笑,能淹没心中的痛苦,微笑,还能给人以自信。有一种生活写照叫“笑口常开”,有一种人生观叫“知足常乐”,有一种状态叫“乐在其中”,有一种大度叫“一笑抿恩仇”。人生最重要的,是保特一
{ { 化合物
电解质
强电解质 弱电解质
=
非电解质
,又何必对未知的前方魂牵梦萦?生活中,其实我们每个人都有目标,并且我们的奋斗,都是为了能离它更近。奋斗努力,快步走行,无可厚非,但是我想,人生在路上行走,本应该走走停停,该歇的则 放慢脚步,看看你的身边,看看你的周围,欣赏一下沿途的美丽风景,也许里面就有会你想要的东西。不要为了追求物质财富,不要忙于到达目的地,只顾疲于奔跑,而错过了身边美丽的风景,不要让你
熔融的氯化钠、熔融的氧化钠、熔融的氢氧化钠
电解质与非电解质的概念:
{ 化合物
电解质:在水溶液中或者熔融状态下能 ▲
导电的化合物。
非电解质:在水溶液中和▲熔融状态下
均以分子形式存在,
都不能导电的化合物。
• 注意点: • 1.电解质和非电解质都是指化合物,单质和混合
物既不是电解质也不是非电解质。 • 2.电解质的导电是有条件的,盐、碱电解质在水
有微笑的画卷,这画便会显得亮丽多彩;人生如酒,有微笑的美酒,这酒便能散发出诱人的醇香;人生如歌,有微笑的歌声,这首歌便多了动人的旋律;人生如书,充满着微笑的这本书里,书中篇篇都是快乐的篇章。微笑着,走好自己的路,让一路上留下欢乐和喜悦,同时,你也将会得
春夏秋冬大千世界,芸芸众生,我们每个人就像一粒小小的尘埃,于春夏秋冬的轮回里,在风风雨雨中飘渺,在阳光下微笑人的一生中,会品尝着各种酸甜苦辣的味道,当回眸看看所走过的路程,会让我们渐渐明白一个道理:人需有一颗淡然的心来对待这世间百态,需用一颗平常心简简单单过好生活,因为淡然,会使人简单,简单了,就有快乐。 在忙碌的生活里,谁都会遇到难处,在现实的生活中,谁都有苦楚,人的一生,总是有一些纠结,会让我们无助;总是有太多的奈何,会让我们无可。所以,有些事,可以认真对待,但不可去较真。当然,说说容易,做起来可能就较难,很多时候,我们往往会始终执着一个人,一件事,一段情,这种执着仅仅是一种执念也就罢了,有些封存的往事,只会让你显得落寞和孤寂,将岁月纠结于此,往往让人痛不欲生。岁月静好,可是,你的人生并非安好,许多的事,我们自己是做不了主的,对人生旅途中的风景,我们也没有能力做出选择,但是我们可以对自己的心态进行调整,时不常地换个角度待人看
要怨天怨地怨人怨己,抱怨自己的人生磕磕绊绊,不如人意。要知道很多时候,当在你盲目地追求着你的目标后,当你在怨天怨地怨人怨己时,回过头来看时,可能会发现:许多的美
人的生命总是有限的,时间也不能停滞,但是我们可以驻足。人生路上,一路行走,一路都是风景,路上,你会遇到很多美的人,美的事,美的景。不要忘了经常抬头凝视一会儿蔚蓝的天空和飞翔的 香气。在人生的风景里有春夏秋冬,会有不同景致,春葱茏、夏繁盛、秋斑斓、冬纯净,都显得很美丽,你大凡可尽收眼底。只不过人生的风景画册里,有的柔和,有的热烈,有的凄美,还有的悲壮,只 生就会轻松很多。也许在你放松心境的时候,你就能看见生活的笑容。不同的人生体验,才能让人生多彩丰富。如果太在意目的地,这一路上,心中便会少了很多乐趣。在人生的旅行中,最重要的不是结
③酸、碱、盐的水溶液:
自
由
盐酸、硫酸溶液、氢氧化钠溶 移
液 、食盐水、 硫酸铜溶液
动 的
④金属氧化物、碱、盐的熔融体
离 子
电离:
酸、碱、盐等电解质在溶液中或熔融 状态下产生自由移动的离子过程
电离方程式: 表示电解质电离成自由移动的离子过
程的式子
电离方程式书写步骤:
1、在方程式左边写出化学式
2、在方程式右边书写阴、阳离子符号前面配上系数
溶液里和熔化状态下都能导电,而酸电解质只有 在水溶液里才能导电。 • 3.有些非电解质的水溶液也能导电,如CO2、SO2、 NH3等,因为它们与水反应生成了电解质。
CO2+H2O=H2CO3 SO2+H2O=H2SO3
• 【自学探究2】 • 它们为什么导电?
导电原因
①金属:Cu、Fe、Al等 自由电子定向移动 ②非金属: 石墨
对生活 。
为了在旅途结束时不留下丝毫的遗憾,请把握好旅程中的每一分钟。一路上慢慢地走,别忘了欣赏沿途的风景。
作者简介:谈笑在指尖 原名:张 波文章,诗歌多见于省内外报刊和网络平台。喜欢把日子中的点点滴滴写进文字里,抒写心中之梦,始终保持着乐观心态,过好每一天。滴写进文字里,雀巢冰泣淋裡 形的冰棍我要用它来纪念他们的爱情。
作者简介:谈笑在指尖 文章,诗歌多见于省内外报刊和网络平台。喜欢把日子中的点点滴如同一次旅行,一次不清楚哪里是终点的旅行。在人生的旅程中,有些人走的很从容,一边走一边欣赏着沿途的风景,春天踏青,感受万物复苏时生命的萌动;夏日赏荷,嗅闻花儿的芳香,聆听悠扬的蝉鸣;秋时听风,欣赏落叶在秋风中忘情的舞动;冬日品雪,品味银装素裹的晶莹,让自己的人生如四季绚烂,多姿多彩。有些人却是步履匆匆,他们只顾埋头盯着脚下的道路,拼命的赶完余下的旅程,一路上,只顾疲于奔跑,疲于生存,疲于生,看不见路边花儿的美丽,也注意不到蔚蓝天空中白云的漂浮,一心只忙于到达目的地,一程又一
谢谢欣赏! 四季辗转中,当遇春风,必有柳绿花红,当入夏凉,便能闻荷风送香,当沐浴在秋风里,必能有丰盈的成熟,当见冬雪时,便能够净化灵魂。每天的生活虽然都过得普普通通,可每一段路上我们
走在人生路上,最宝贵的是你的微笑。人的一生会遭遇许多坎坷,经历许多风雨,纵然前面充满荆棘,也必须走下去。微笑着,无论是在平淡的日子里,还是在迷茫低落的时候,都让自己内心尽量靠 你对未来充满着信心,眼前的困难只是暂时的,没什么可畏惧!微笑着,证明了你的意志是无比的坚强,既然确定了目标就去奋斗,一切的阻挠都显得可笑和无力,丝毫都不能让你停顿半步。你脸上的微
笑,就像是那照亮天空的火炬,能使你的眼前永远闪耀着光明与希望;你脸上的微笑,能催你不断奋进向前,让你的生命里充满激情与活力。748219
走在人生路上,最不可少的是你的微笑。人生之路,鲜花和荆棘映衬,坦途和坎坷衔接,艳阳和风雨交织,得志和失意错位。生活给予你的,有精彩,更多的是平淡。人生,不会事事如意,生活,也 事,都不由我们做主。我们最重要的不是要去计较真与伪,得与失,名与利,贵与贱,贫与富,而是要想想,如何好好地快乐度日,并从中发现生活的诗意。尽管日子很平淡,却会有许多的闪光点,尽管
3、检验“=”两边是否守恒(质量、电荷)
• H2SO4=2H++SO42• HCl= H++Cl• NaOH= Na++OH-
• Ca(OH)2=Ca2++2OH• NaCl= Na++Cl• MgCl2= Mg2++2Cl-
书写时注意事项:
1、 适用范围: 电解质的电离。 2、 用的是等号。 3、根据化合价写离子符号。 4、根据右下角系数写离子个数。
• 1.完成下列电离方程式
• (1) Na2CO3 =2Na++CO32• (2)KClO3= K++ClO3• (3)Fe2(SO4)3 = 2 Fe3++ 3 SO42• (4)Ba(OH)2 =Ba2++ 2 OH-
(5)CH3COOH
CH3COO-+H+
(6)NH3·H2O
NH4++OH-
电离方程式:
复习巩固
[回顾问题1]
溶液、浊液 、胶体 的本质区别是什么?
分散系
粒子直径
浊液
悬浊液 乳浊液
>10-7m
胶体 10-7~10-9m
溶液 <10-9m
[回顾问题2]
溶液、胶体区分方法是什么?
丁达尔效应
CuSO4溶液
Fe(OH)3胶体
•【学习目标】
• 掌握电解质的概念, • 并会书写电离方程式
•【学习重难点】
辉和莉是在网络上认识的,莉比辉大5岁。2000年初秋的一天,他们相识了,以后的日子,他们相知了,彼此以姐弟相称。第一次他给她写信是在圣诞节,当时仅仅是 后来,他爱上了她,一个让辉用三生三世都不能忘记的女人。 2001年的2月10日,值得纪念的日子,辉告诉了莉他心裡的想法!因為莉是从艰辛中一路走来身心疲惫的人,深知道爱就要付出什麼,她没有
清弦坠满心事,弹落片片梦幻,我该如何用这弦、这韵去丈量你我天涯的距离,一滴泪上的墨香,如何画下你最爱的睡莲? 清影摇曳,眉眼如水,缓缓来到钢琴前为你弹一曲你最爱的《莫失莫忘》,让我借琴声悄悄告诉天涯的你:今夜,我想喜欢一句话:能让人生灿烂的不只有阳光
每天早上醒来,打开心灵的窗户,让阳光照射进来,你的心中便会亮堂堂,既便是在任何季节,也不会觉得孤单寒凉。每天当你迈开双腿,将微笑挂在脸上,你的步伐便会走的轻松和稳当。携着阳光
凡事都是多棱镜,不同的角度会看到不同的结果。若能把一些事看淡了,就会有个好心境,若把很多事看开了,就会有个好心情。让聚散离合犹如月缺月圆那样寻常,让得失利弊犹如花开花谢那样自然,不计较,也不刻意执着;让生命中各种的喜怒哀乐,就像风儿一样,来了,不管是清风拂面,还是寒风凛冽,都报以自然的微笑,坦然的接受命运的馈赠,把是非曲折,都当作是人生的定数,不因攀比而困惑,不为贪婪而费神,无论欢乐还是忧伤,都用平常心去接受;无论得到还是失去,都用坦然的心去面对,人生原本就是在得与失中轮回的,让一切所有的经历,都化 人的一生说白了,也就是三万余天,贫穷与富贵,都是一种生活境遇。懂得爱自己的人,对生活从来就没有过高的奢望,只是对生存的现状欣然接受。漠漠红尘,芸芸众生皆是客,时光深处,流年似水,转瞬间,光阴就会老去,留在心头的,只是弥留在时光深处的无边落寞。轻拥沧桑,淡看流年,掬一捧岁月,握一份懂得,红尘纷扰,我自心安;书一笔清远,盈一抹恬淡,浮华三千,只做自己;人间有情,心中有爱,携一米阳光,微笑向暖。
