98例药品不良反应报告分析
某院578例药品不良反应报告分析

p t ns owecodrta 5 Mot fhm r sl dfo i ihac u tdfr 45 %(7 ae)n u e yp i cone o 3 2 a et wh r le n6 . s o te weer ut m whc co ne . i h e e r v o 6 3 3 3css. d cdb owhc acu tdfr3 . %. i h 2
中图分类号 :R6 . 9 92
文献标识码 :B
文章编号 :1 7— 14 (0 1 1 0 - 3 6 1 8 9 2 1)2 - 18 0 7
An l ss n 5 8Ad e s u a t n Ca eRe o t ay i 7 v r eDr g Re c i s p r o o s
院附属 第九人 民医院 A R 的 发生 以女性 、老年 患者居 多 ,其 临床 表现 多样 ,发生 因素 与 患者年龄 、 给 药途 径 、 药品种 类等 相 关 应加 强 D 对 A R 的监测 及相 关知 识 的 宣传 ,以减 少和避 免 A R 的发生 。 D D
【 关键 词】 药品 不 良反 应 ; 监测
l。・论 7 8
著 ・
Jl2 1,o. N .1 u 1V 1, o y0 9 2
某 院5 8 7例药 品不 良反应报告分析
金 剑 肖忠革 金 芝贵 关 飞华
( 上海交通大学医学院附属第九人 民医院药剂科 ,上海 2 0 1 ) 00 1
【 要】目的 了解 上 海 交通 大 学医 学院 附属 第九人 民医院 药品 不 良反应 ( D ) 的 发生 情况 及 引发 A R 的相 关 因素 。方法 对上 海 交通 摘 A R D 大学 医学 院 附属 第九人 民医 院 2 0 年 1 05 月至 2 1 00年 1 2月收集 到 的 58例 A 7 DR进 行 回顾性 统 计 与分析 。 结果 58例 A R报告 中,女 7 D 性 多于 男性 ,6 5岁以上 老年 惠者 占总例数 的 4 . 8 %。给 药方 式 中,静 脉 滴注 引 发的 A R最 多, 口服 第二 。 涉及 的药品 种类 中 ,抗 感 染药 1 D
曲妥珠单抗不良反应的特点及规律

曲妥珠单抗不良反应的特点及规律周洁车啸天【摘要】目的探讨曲妥珠单抗不良反应特点及规律。
方法选择2018年4月至2020年1月肿瘤患者518例作为研究对象,所有患者均采用曲妥珠单抗治疗,记录所有患者治疗过程中不良反应情况,包括:不良反应类型、不良反应发生时间、药物联合使用情况,分析曲妥珠单抗不良反应特点及规律。
结果518例肿瘤患者均采用曲妥珠单抗治疗,患者治疗过程中98例发生不良反应,发生率为18.9%。
不良反应排在前三位的分别为:消化不良、感冒样症状及背痛,发生率分别为21.4%、15.3%和14.3%;不良反应能发生在不同年龄段人群中,排在前三位为>50岁、41~50岁及31~40岁,分别占:42.9%、25.5%及22.5%;发生不良反应患者中54.1%患者发生在0.5~1h内,而39.8%患者发生在1h后的化疗时间中;曲妥珠单抗不良反应均发生在不同药物联合使用患者中,排在前三位的分别为:托烷司琼+地塞米松+奥美拉唑+胃复安+哌拉西林舒巴坦+左氧氟沙星+门冬氨酸鸟氨酸、顺钳+紫杉醇和卡培他滨+奈达钳,分别占23.5%、15.3%和13.3%)结论曲妥珠单抗临床使用时不良反应发生率较高,具有一定的特点与规律,应及时采取有效的措施进行预防,提高患者用药安全性。
【关键词】抗肿瘤靶向药物;曲妥珠单抗;不良反应Characteristics and regularities of adverse reactions of anti-tumor targeted drug trastuzumab Zhou Jie(Che Xiaotian.Department of Pharmacy,North Campus,Huashan Hospital,Fudan University,Shanghai201907,China 【Abstract】Objectiv To investigate the characteristics and regularities of adverse reactions of trastuzumab. Meth0,s A total of518patients with tumors from April2018to January2020were selected as subjects.All patients were treated with the trastuzumab,and adverse reactions during the treatment of all patients were recorded,including: types of adverse reactions,time of occurrence of adverse reactions,combined use of drugs,analysis of the characteristics and regularities of adverse reactions of trastuzumab in patients.Results All518tumor patients were treated with trastuzumab.During the treatment,98patients had adverse reactions,the incidence rate was18.9%.The top three adverse reactions are:dyspepsia,symptoms of cold medicine and back pain,with incidences of21.4%,15.3%and 14.3%respectively;the adverse reactions can occur in different age groups.Among the population,the top three are> 50years old,41-50years old and31-40years old,accounting for42.9%,25.5%and22.5%respectively;Among patients with adverse reactions,54.1%of them occurred within0.5-1hour,while39.8%of patients occurred within1 hour of chemotherapy.Adverse reactions of trastuzumab occurred in patients who used different drugs in combination, ranking the top three are:tropisetron+dexamethasone+omeprazole+metoclopramide+piperacillin and sulbactam+ levofloxacin+ornithine aspartate,cisplatin+paclitaxel and capecitabine+nidaplatin,accounted for23.5%,15.3% and13.3%respectively.Conclusion The anti-tumor targeted drug trastuzumab has a high incidence of adverse reactions during clinical use,and has certain characteristics and regularities.Effective measures should be taken in time to prevent and improve the safety of patients.【Key words】Anti-tumor targeted drugs;Trastuzumab;Adverse reactions曲妥珠单抗是临床上常用的抗肿瘤靶向药物,属于抗人表皮生长因子受体(Her)-2的单克隆抗体,能通过将自己附着在Her-2上,阻止人体表皮生长因子,从而能阻断肿瘤细胞的增殖、生长[1]o临床研究表明%2&:曲妥珠单抗能刺激自身免疫细胞,从而摧毁肿瘤细胞。
药品不良反应98例分析
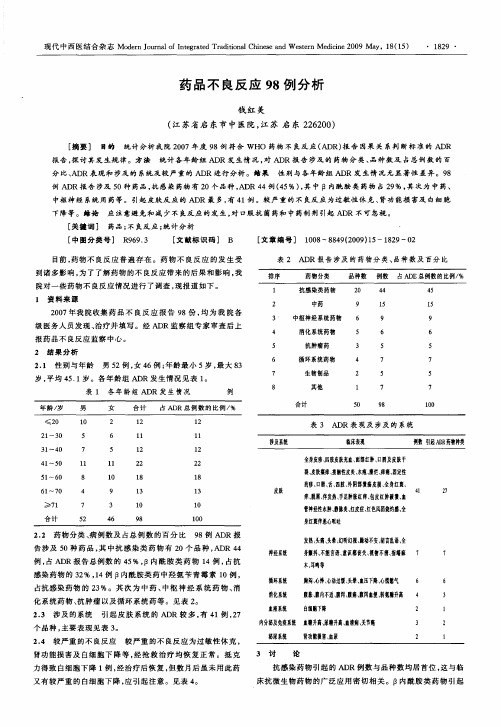
2 4 较严重的不 良反应 .
较严重的不 良反应为过敏性休克 ,
3 讨 论
肾功 能 损 害 及 白细 胞 下 降 等 , 抢 救 治 疗 均恢 复 正 常 。抵 克 经 力 得 致 白细 胞 下 降 1 , 例 经治 疗 后 恢 复 , 数 月 后 虽 未 用 此 药 但 又有 较 严 重 的 白细 胞 下 降 , 引起 注 意 。见 表 4 应 。
2 结 果 分 析
2 1 性 别 与 年龄 .
男5 2例 , 4 女 6例 ; 龄 最 小 5岁 , 大 8 年 最 3
岁 , 均 4 . 。各年龄组 A 平 5 1岁 DR发 生 情 况 见 表 1 。 表 1 各 年 龄 组 A R 发 生 情 况 D 例
涉系 及统
临 表现 床
的 A R1 例 , 1 例 不 良 反 应 是 由 口 服 羟 氨 苄 青 霉 素 弓 4 有 0 表 4 较 严 重 A R 及 其 表 现表 现 D
及药 物 2 7个 品 种 。表 现 为 各 类 皮 疹 , 数 病 例 由皮 肤科 医 生 多
诊 治后 痊 愈 。在 引 起 皮 疹 的 药 物 中 , 生 素 占多数 , 速 发 和 抗 有
排序 药物分类 品种数 例数 占A E总例数的比例/ D %
[ 键 词 】 药品 ; 良反 应 ; 计 分析 关 不 统 [ 图 分 类 号 ] R 6 . 中 993 [ 献标 识码 ] B 文
目前 , 物 不 良反 应 普 遍 存 在 。 药 物 不 良反 应 的 发 生 受 药 到 诸 多 影 响 , 了 了解 药 物 的 不 良反 应 带 来 的 后 果 和 影 响 , 为 我 院 对 一 些 药 物 不 良反应 情况 进 行 了调 查 , 报 道 如 下 。 现 1 资料 来 源 2 0 年 我 院收 集 药 品 不 良反 应 报 告 9 07 8份 , 为 我 院 各 均 级 医 务人 员 发 现 、 疗 并 填 写 。 经 A 治 DR监 察 组 专 家 审 查 后 上 报药 品不 良反 应 监 察 中心 。
98例注射用炎琥宁不良反应分析

9 8例炎琥宁注射剂 药物不 良反应报告进行分 析。结果 关键词 : 注射用炎琥宁 ; 良反应 ; 析 不 分
炎琥宁注射剂 可致消化 、 呼吸 、 肤等 系统 不 良反 应 , 皮 尤以皮肤过 敏为
An ls f 8c s e o t o ayi 0 aerp rs fADR c u e yy n u igijcin s 9 a sd b a h nn et n o
frh l i i ert nl s f rg. e o 9 D a sdb ah nn jco f lS eze op a ip tnsrpr d o ecnc nt i a ueo dusM t d 8A R cue yyn uigi et no l hnhnhsi ln a et eo e t i h ao h n i a t i t f m2 0 o20 eeaaye e op cvl. sl Y n u igi et ncudid c si tr ss m,em tl yss m,i r 0 5t 0 6w r nl dr rset e Reut ah nn jci ol uer pr o yt dr ao g yt d— o z t i y n o n e a y e o e
2 结 果
.
A R在不 同年龄段 的分 布见 表 1 注 射用 炎琥 宁 引起 的 D ;
表 3 炎 琥 宁 注 射 剂 发 生 不 良反 应 时 间
不 良反 应类 型见表 2; 炎琥 宁注 射剂发 生不 良反 应时 间见 表
3 。用 药 剂 量 : 琥 宁 针 剂 成 人 剂 量 一 般 为 4 0~80m , ,L 炎 0 0 g d J
W U “ Bi
( hnhnP amaet a a dMei l ei s vlainCne,hnhn 5 3 ,hn ) S eze hr cui l n dc v e E au t et Seze 0 4 C ia c a D c o r 1 8 AbtatAm T nlz tef tr o D a sdb a h n gi et na dtepeet nadc r mesr Oa fr ai src: i oaaye h cos f R cue yyn u i jci n rvni n ue aue S s oo e b s a A n n o h o s t f s
药品不良反应表格

附表1
药品不良反应/ 事件报告表
首次报告□跟踪报告□编码:
报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□其他□
严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:
1) 导致死亡;
2)危及生命;
3)致癌、致畸、致出生缺陷;
4)导致显著的或者永久的人体伤残或者器官功能的损伤;
5)导致住院或者住院时间延长;
6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
新的药品不良反应:是指药品说明书中未载明的不良反应。
说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
报告时限
新的、严重的药品不良反应应于发现或者获知之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应30日内报告。
有随访信息的,应当及时报告。
其他说明
怀疑药品:是指患者使用的怀疑与不良反应发生有关的药品。
并用药品:指发生此药品不良反应时患者除怀疑药品外的其他用药情况,包括患者自行购买的药品或中草药等。
用法用量:包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2次。
报告的处理
所有的报告将会录入数据库,专业人员会分析药品和不良反应/事件之间的关系。
根据药品风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入警示信息,更新药品如何安全使用的信息等。
在极少数情况下,当认为药品的风险大于效益时,药品也会撤市。
银杏达莫注射液不良反应报告风险分析

银杏达莫注射液不良反应报告风险分析■ 岳红霞(济宁市药品不良反应监测中心药品不良反应监测科)摘 要:目的:分析银杏达莫注射液的安全性风险,为临床合理用药提供参考。
方法:采取回顾性分析研究办法,对2020年1-12月份国家药品不良反应监测系统山东省济宁市数据库中收集上报的99例银杏达莫注射液不良反应报告及文献报道中银杏达莫注射液的药品不良反应数据,分别将不良反应的类型、患者性别与年龄、药品不良反应表现等进行统计和分析。
结果:银杏达莫注射液致新的不良反应37例(占37.37%);严重不良反应(含新的严重的)6例(占6.06%)。
50岁以上的患者居多。
结论:应加强银杏达莫注射液的临床应用监测,及时完善产品说明书,促进药品的合理使用。
关键词:银杏达莫注射液,药品不良反应,分析,合理用药,临床应用监测DOI编码:10.3969/j.issn.1002-5944.2021.18.041Risk Analysis of Adverse Reactions Induced by GinkgoDipyridamole InjectionYUE Hong-xia(Adverse Drug Reaction Monitoring Department of Jining Adverse Drug Reaction Monitoring Center) Abstract: Objective: To analyze the safety risk of ginkgo dipyridamole injection and provide reference for clinical rational drug use. Methods: A total of 99 adverse reaction (ADR) reports of ginkgo dipyridamole injection collected from Jining database of national ADR monitoring system in 2020 were analyzed retrospectively. Results: There were 37 cases (37.37%) of new adverse reactions and 6 cases (6.06%) of serious adverse reactions induced by ginkgo dipyridamole injection. Conclusion: We should strengthen the clinical application monitoring of ginkgo dipyridamole injection, improve the product instructions in time, and promote the rational use of drugs.Keywords: ginkgo dipyridamole injection, adverse drug reaction report, analysis,rationd drug use, clinicd application monitoring医疗医务标准化银杏达莫注射液是一种复方注射液,主要由银杏提取物(银杏总黄酮)和双嘧达莫构成, 临床上主要用来治疗冠心病、血栓阻塞性疾病,对于心血管疾病、脑衰弱综合征、脑动脉硬化和老年性痴呆等常见病具有良好的预防和治疗作用。
心血管内科临床用药常见问题及合理用药分析

心血管内科临床用药常见问题及合理用药分析摘要:目的对心血管内科临床用药常见问题进行总结分析,并探讨合理用药的方式,以期能够提升临床用药安全性。
方法就2020年7月-2022年2月来我院心血管内科就诊患者中随机抽取98例,回顾分析患者在用药过程中存在的常见问题,并探讨帮助患者合理用药的方法,从而提升患者用药合理性与安全性。
结果 98例参与研究的患者中有10例存在用药问题,其中用法用量问题4例,配伍问题2例,抗菌药物应用问题1例,诊断与用药不符问题2例,忽略用药禁忌症1例。
结论通过对患者用药情况分析,我们可以看出心血管内科临床用药中常见问题有用法用量不合理、配伍配药不合理、抗菌药物应用不合理、忽略用药禁忌以及诊断与用药不符,这些问题会对患者病情造成影响。
因此,医务人员应对患者用药进行指导、干预,促使患者用药安全性与合理性得以提升。
关键词:心血管内科;临床用药;合理用药;常见问题引言目前,心血管疾病已经成常见病之一,并且呈现出发病率逐年上涨的趋势。
如果不能合理用药控制,那么就会对患者的身体健康造成威胁。
常见心血管疾病有高血压、冠心病、心肌梗死、心律失常、心肌炎以及心绞痛等,多以药物治疗控制病情。
但当前心血管患者在用药治疗中存在的一些问题,这就影响到用药合理性,不仅降低了用药安全性,同时也无法对患者的病情进行有效控制。
基于此,本次研究就对心血管内科临床用药种常见问题进行探究,随机选取来我院心血管内科就诊患者中的98例,回顾分析用药中常见问题,并对患者用药进行指导与干预。
具体的研究情况如下:1.资料与方法1.1一般资料本次研究对象来自我院心内科2020年7月-2022年8月收治患者,从中随机抽取98例,其中男性患者为51例,女性患者为47例;患者中年龄最小的为38岁,年龄最大的为74岁,平均年龄为(52.149.58)岁;其中高血压患者为16例,心力衰竭患者为23例,心绞痛患者为20例,心肌梗死患者17例,心肌炎患者为19例,心律失常患者为3例。
药品不良反应报告表范例 .doc

药品不良反应报告表范例 .doc
药品不良反应记录
日期:xxxx年xx月xx日
药品名称:xxxx
制剂规格:xxxx
生产企业:xxxx
患者信息:
姓名:xxx
性别:xxx
年龄:xxx
病情/疾病诊断:xxx
不良反应记录:
1.反应名称:xxxx
发生时间:xxxx年xx月xx日xx时xx分
反应描述:患者出现了xxxx的症状,包括xxxx。
症状持续时间约为xx小时/天。
患者对此感到不适,并报告给医生。
处理措施:对患者的症状进行了观察,同时给予了xxxx的治疗。
结果:患者在接受治疗后,症状逐渐缓解,并在xx天后完全消失。
2.反应名称:xxxx
发生时间:xxxx年xx月xx日xx时xx分
反应描述:患者出现了xxxx的症状,包括xxxx。
症状持续时间约为xx小时/天。
患者对此感到不适,并报告给医生。
处理措施:对患者的症状进行了观察,同时给予了xxxx的治疗。
结果:患者在接受治疗后,症状逐渐缓解,并在xx天后完全消失。
备注:
1.患者的不良反应于xx年xx月xx日报告给医生,并得到及时处理。
2.对患者的不良反应进行了详细的记录,包括症状的描述、发生时间、处理措施和疗效结果。
3.患者在接受治疗后的症状得到缓解,并无其他严重不良反应发生。
以上是患者使用该药品期间出现的不良反应的详细记录。
如有进一步需要,请及时与我联系。
医师签名:xxxx
日期:xxxx年xx月xx日。
资料药品不良反应分析报告实例

资料药品不良反应分析报告实例报告编号:XXXX/2024报告时间:2024年X月X日1.引言不良反应是指在正常用药剂量范围内,由于药物的药理作用或其他原因,引起患者出现的有害症状或体征。
及时准确地分析药品不良反应对于制定合理的临床用药方案、保障患者用药安全非常重要。
2.药品信息药品名称:XXX批准文号:XXX生产企业:XXX使用剂量:XXX3.不良反应描述根据患者反馈和医生报道,使用药品XXX后出现不良反应如下:3.1XX不适症状描述不适症状,如头痛,恶心、呕吐等。
3.2XX体征改变描述体征改变,如皮疹、腹泻等。
4.不良反应报告统计统计所有该药品不良反应的发生情况,包括发生率、时间分布等。
4.1不良反应发生率药品使用范围内,不良反应发生率为XX%。
4.2不良反应时间分布不良反应主要发生在用药初期,60%的不良反应在首次使用后48小时内出现。
5.不良反应风险因素分析基于患者特征、药品特征等因素,分析导致不良反应的可能风险因素。
5.1患者特征分析患者的年龄、性别、病情等特征对不良反应的影响。
比如,年龄大于65岁的患者更容易出现不良反应。
5.2药品特征分析药品的药理作用、药代动力学等特征对不良反应的影响。
比如,该药品的副作用与其在肝脏中的代谢机制相关。
6.不良反应处理措施提出针对不良反应的处理措施,包括调整用药剂量、联合用药、停药等。
7.不良反应预防建议提出预防不良反应的建议,包括临床使用上的提示、监测措施等。
8.结论根据以上分析,我院对药品XXX的不良反应进行了全面的分析与统计,并提出了相应的处理和预防建议,以确保患者在用药过程中的安全。
附录:不良反应报告表格表格包括不良反应的具体描述、出现时间、症状严重程度等。
药物不良反应98例分析

表 2 20 20 06— 08药 品不 良反 应 分 类
药物种类
病例数 构成比( ) %
23 严 重 不 良反 应 .
严 重 不 良反 应 1例 , 占总 数 的 10 % 。 .2
注射用 中药注射剂鱼腥草 引起过敏性休克 , 因呼吸衰竭抢救 无效死亡。提示 临床 医生 , 儿童应用中药注射剂应谨慎。
可 以使患者对所用 的药 品治疗有更深的了解 , 提高用药安 全 性 。发现药品不 良反应后 , 药师应积极配合 临床 医护人 员进 行处理 , 将药 品不 良反应造成的损失减少到最低 。 33 中药注射剂所致 不 良反应 . 成分 比较复杂 唯一 1 例死亡病例为 我院 使用 中药制剂鱼腥草注射液所致 , 救无效死亡 。由于中药 抢 , 其所含蛋 白质或 生物大分 子作为过 敏原
与女性患儿发生药 品不 良反应 的 比例 约为 12 :1 .3 。各年 龄组的药品不 良反 应发 生率不 同 , 其年龄 段分 布情 况 见表 1 。按患者性别 、 年龄 、 药物类别 以及不 良反应的临床表现类
型进 行 统 计 分 析 。 表 1 20 20 06— 0 8药 品 不 良反应 发 生 年龄 与例 数
不 良反 应监 测 工作 , 减 少 药品 不 良反 应 的 发 生 。 以
【 关键词】 药物 ; 不良反应 ; 用药 合理
本文对我 院 2 0 0 06— 5—20 0 8—0 5间 9 8例药 物不 良反
应报 告 进 行 分 析 , 旨在 了 解 引 起 不 良反 应 的 药 物 及 临 床 表
・49 ・
全 程 关 注 。 医 院药 师应 该 对 患 者 出现 的 问 题 进 行 专 业 分 析 ,
我院98例药品不良反应报告分析

前 防神 经血 管畸形 药物 , 如叶 酸 , 主要 是促 进胎儿 神
经 系 统 的发 育 , 少 无脑 儿 、 柱 裂 的发生 , 是 如 减 脊 但
展 现 状 及 尚 需 解 决 的 问 题 [] J.中 国 药 房 ,0 4 1 20,5
( 3): 3 — 34 121 .
果 长期 大 剂 量 服 用会 对 孕 妇 和 胎 儿 产 生 不 良 的影 响 , 干扰 孕 妇 的锌 代谢 , 成 胎 儿发 育迟 缓 , 出 如 造 低
收 稿 日期 :000 —1 2 1 — 1 1
作 者 简 介 : 新 文 (9 6 ) 女 , 京 市人 , 管 药师 , 要 从 事 化 学制 药工 作 。 翟 16一 , 北 主 主
文 章 编 号 : 6 1 6 1 2 1 ) 5 - 0 5 —0 1 7 —8 3 ( o 0 0 A- 3 6 3
20 一20 上报的 9 0 7年 0 8年 8例 A DR报 告 按 患者 年 龄 、 别 、 性 引起 A R 的 药 品 及 该 药 品 的种 类 、 药 途 径 、 R 临 床 D 给 AD 表现等方面进行统计 、 分析 。 果 :8例 AD 报 告 中 , 及 药 品 8 5 种 , 中 抗 感 染 药 居 多 (7种 , 5 . 2 )其 结 9 R 涉 类 2 其 2 占 1 9 ,
我院 9 8例 药 品不 良反 应报 告分 析
耿 春梅 , 李德 龙 , 曹妞 香 , 董
( 西 煤 炭 中 心 医 院 , 西 太原 山 山
芳
000) 30 6
摘 要 目的 : 总结 药 品 不 良反 应 ( R) 发 生 情 况 , 讨 A AD 的 探 DR 发 生 的 特 点 及 规 律 , 进 临床 合 理用 药 。方 法 : 促 对
药物不良事件分析讨论记录

药物不良事件分析讨论记录时间:2022年10月15日地点:医院药事科会议室参与人员:药师A、药师B、医生A、医生B、护士A、护士B记录者:药师A主持人:药师A【引言】药师A主持药物不良事件(ADE)分析讨论会议,旨在回顾和分析近期发生的ADE,探讨原因并制定预防措施,以提高药物疗效和患者安全。
【第一例ADE讨论】1. ADE患者信息:- 姓名:李某- 年龄:60岁- 性别:男- 既往病史:高血压、糖尿病、冠心病2. ADE药物信息:- 药物:药物X- 剂量:每日口服150mg,共用药3个月- 途径:口服- 开始时间:2022年8月1日- 停药时间:2022年10月1日3. ADE描述:- 李某出现明显的腹泻和便秘症状,伴有腹部不适感,严重影响生活质量。
- 在用药期间,李某没有出现其它不适症状。
4. ADE分析:- 药师A提出药物X常见的不良反应是腹泻和便秘,与李某的症状相符。
- 李某存在高血压、糖尿病和冠心病等基础疾病,可能增加了药物X的不良反应风险。
- 药师B提出药物X的剂量是否符合规定,是否存在用药错误或剂量过大的可能性。
5. 讨论结果:- 建议检查药物X的剂量是否符合规定,并进一步了解李某的肝功能和肾功能状况。
- 药师B提出需要重视与药物X相互作用的药物,尤其是李某正在接受的其它药物。
【第二例ADE讨论】1. ADE患者信息:- 姓名:张某- 年龄:45岁- 性别:女- 既往病史:哮喘、鼻窦炎2. ADE药物信息:- 药物:药物Y- 剂量:每日鼻喷2次,共用药2周- 途径:鼻腔喷雾- 开始时间:2022年9月15日- 停药时间:2022年9月29日3. ADE描述:- 张某在用药期间出现鼻塞、头痛和流鼻涕等上呼吸道感染症状,严重影响生活质量。
- 张某没有出现其它不适症状,也没有使用其它药物。
4. ADE分析:- 药师B提出药物Y的常见不良反应包括上呼吸道感染和头痛,与张某的症状相符。
- 张某可能对药物Y过敏,加重了上呼吸道感染的症状。
抗凝剂皮下注射不良反应发生率现况调查及其影响因素研究

2021年第7卷第9期Vol.7,No.9,2021中西医结合护理Chinese Journal of Integrative Nursing抗凝剂皮下注射不良反应发生率现况调查及其影响因素研究代莉莉,段艳芹,张梅,朱素芹,陈娟,孙玉玲(安徽省淮北市人民医院,安徽淮北,235000)摘要:目的调查基于循证护理指导下抗凝剂皮下注射不良反应发生率,并进行影响因素分析。
方法采取便利抽样法,对608例患者抗凝剂皮下注射后皮下瘀点瘀斑、硬结等进行记录,计算发生率,对年龄等影响因素进行多元回归分析。
结果通过规范注射,有98例患者发生不良反应,总发生率为16.12%。
年龄、性别、体质量指数、腹部皮肤褶皱厚度、同时使用其他相关药物是其主要影响因素。
D-二聚体、纤维蛋白原水平是特异性指标。
结论规范抗凝剂皮下注射方法,可降低出血相关不良反应。
注射前应全面评估患者,掌握正确的注射方法。
高龄、女性、肥胖、同时使用其他相关药物和D-二聚体、纤维蛋白原降低的患者是高危人群。
关键词:抗凝剂;低分子肝素;皮下注射;影响因素中图分类号:R 473.5文献标志码:A文章编号:2709-1961(2021)09-0039-05Investigation on the incidence of adverse reactions ofsubcutaneous anticoagulant injection andits influencing factorsDAI Lili ,DUAN Yanqin ,ZHANG Mei ,ZHU Suqin ,CHEN Juan ,SUN Yuling(Huaibei People's Hospital ,Huaibei ,AnHui ,235000)ABSTRACT :Objective To investigate the incidence and influencing factors of adverse reac⁃tions of injection site after subcutaneous anticoagulant injection under the guidance of evidence-based nursing Methods Using the convenient sampling method ,608patients with anticoagulant subcutaneous injection were investigated with self-designed general data questionnaire.Results Totally 98patients had hemorrhagic related adverse reactions ,the total incidence was 16.12%.Age ,sex ,body mass index ,abdominal skin fold thickness ,and concomitant other anticoagulants were the main influencing factors.The levels of D-dimer and fibrinogen were specific indexes.Conclusion Standardizing subcutaneous injection method of anticoagulants can reduce the risk of bleeding and other adverse reaction.Patients should be comprehensively evaluated before injec⁃tion and master the correct injection method.Elderly ,female ,obesity ,and the use of other anti⁃coagulant drugs and D-dimer ,fibrinogen decreased in patients are high-risk groups.KEY WORDS :anticoagulant ;low molecular weight heparin ;subcutaneous injection ;influencing factors随着临床医务人员对血栓危害性认识提高,对血栓预防更加重视。
复方丹参注射液不良反应98例分析

复方丹参注射液不良反应98例分析
许明桂;骆渊海
【期刊名称】《湖北民族学院学报(医学版)》
【年(卷),期】2006(023)003
【摘要】复主丹参注射液由丹参、降香两味中药提取精制而成,其临床应用广泛,同时其不良反应报告也日趋增多,有些反应较严重,甚至引起死亡。
本文对复方丹参注射液不良反应共98例进行回顾性分析。
【总页数】1页(P55)
【作者】许明桂;骆渊海
【作者单位】鹤峰县中心医院,湖北,鹤峰,445800;鹤峰县中心医院,湖北,鹤
峰,445800
【正文语种】中文
【中图分类】R2
【相关文献】
1.复方丹参注射液不良反应16例分析 [J], 刘红建;刘鄢妮
2.复方丹参注射液不良反应93例分析 [J], 韩淑萍;孙建宇
3.复方丹参注射液致不良反应69例分析 [J], 朱晓峰;金萍;苗智如
4.复方丹参注射液不良反应85例分析 [J], 高洁婷
5.输血不良反应98例分析 [J], 徐慧英;朱蕾;廖昭平
因版权原因,仅展示原文概要,查看原文内容请购买。
98例参麦注射液不良反应分析

98例参麦注射液不良反应分析
王书杰;王丽萍;李慧
【期刊名称】《中国药业》
【年(卷),期】2006(15)9
【摘要】目的探讨参麦注射液所致不良反应的规律和特点.方法对国内2003年1月至2005年2月应用参麦注射液出现的不良反应报道进行归纳和分析.结果参麦注射液所致不良反应与性别、年龄有关,其出现时间主要集中在用药过程前30 min,临床表现多种多样,主要表现为变态反应,严重者可出现过敏性休克.结论临床医护人员及药师应重视参麦注射液的不良反应,做到合理用药.
【总页数】2页(P51-52)
【作者】王书杰;王丽萍;李慧
【作者单位】中国人民解放军第251医院药剂科,河北,张家口,075000;中国人民解放军第251医院药剂科,河北,张家口,075000;中国人民解放军第251医院药剂科,河北,张家口,075000
【正文语种】中文
【中图分类】R2
【相关文献】
1.154例参麦注射液不良反应分析 [J], 何芳芳
2.参麦注射液的临床应用情况及不良反应分析 [J], 王明昭;齐武强
3.参麦注射液12例不良反应分析 [J], 童丽平
4.2012-2018年景德镇地区参麦注射液不良反应分析 [J], 徐美丽;罗嗣佳妮;邓之江;罗贤宏
5.参麦注射液不良反应分析 [J], 姜芳媛
因版权原因,仅展示原文概要,查看原文内容请购买。
对98例患者应用莫西沙星引发不良反应情况的分析

对98例患者应用莫西沙星引发不良反应情况的分析颜荣【期刊名称】《当代医药论丛》【年(卷),期】2014(000)016【摘要】目的:分析98例患者在应用莫西沙星进行治疗时发生不良反应的情况及其发生不良反应的规律。
方法:将2013年1月至2014年1月我院收治的98例因使用莫西沙星而引起不良反应的患者作为研究对象,对其发生不良反应的情况进行总结性分析。
结果:与其他年龄段的患者相比,本组中年龄>60岁的患者所占的比例较大,差异显著(P<0.05),有统计学意义。
在本组98例患者中,有67例患者进行联合用药治疗,占68.37%;有31例患者单用一种药物进行治疗,占31.63%,二者相比差异显著(P<0.05),有统计学意义。
在本组98例患者中,有27例患者口服药物进行治疗,占27.55%;有71例患者静脉滴注药物进行治疗,占72.45%,二者相比差异显著(P<0.05),有统计学意义。
在本组患者中,与其他各时间段相比,在用药10-90min内发生不良反应的患者所占的比例较大,差异显著(P<0.05),有统计学意义。
结论:患者在应用莫西沙星进行治疗时发生不良反应的几率与其年龄是否偏大、是否联合用药及给药途径等因素有关,其发生不良反应的时间常为用药后10-90min内,具有一定的规律性。
【总页数】2页(P157-158)【作者】颜荣【作者单位】盐城市急救医疗中心江苏盐城 224000【正文语种】中文【中图分类】R978.1【相关文献】1.COPD合并感染性肺炎患者联合应用美罗培南与莫西沙星的疗效及不良反应分析[J], 陈政2.莫西沙星临床应用的不良反应及用药安全性分析 [J], 张远晖3.莫西沙星引发的神经/精神系统不良反应分析 [J], 谷建俐;王书民;秦智彬;张雨晨;闫丽萍;闫抗抗4.莫西沙星联合卷曲霉素治疗耐多药肺结核的临床效果及不良反应发生情况分析[J], 吕月秋;石蕾5.莫西沙星临床应用的不良反应及用药安全性分析 [J], 孙丽娴因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
p H值 见 表 3 含 量 测 定结 果 见 表 4 , 。
形 及 峰 位 均 未发 生 变 化 , 无 杂 峰 出 现 。6h内 外 观 变 化 及 也 表 3 不 同温 度 下 配 伍 液 的 外 观 及 p 值 H
表 4 不 同 温 度 下 配伍 液 中各 药 的 含 量 变 化
保 障 用 药安 全 , 进 合 理 用 药 , 临 床 实 际 工 作 中具 有 重 要 促 在
意义。
本文结合 我 院 20 20 0 4— 05年 发 生 的 9 8例 药 品 不 良反 应进行归类统计和分析, 旨在 发 现 和研 究 不 良反 应 发 生 的 特
婴 幼 儿 占 3. 8 ,1~ 0岁 女 性 占 2 .% 。 87 % 2 3 55 2 2 A R 与 药物 及 用 药 方 式 的 关 系 从 用 药 原 因 方 面 看 , . D 用 于 抗 病毒 感 染 的有 1 7例 , 1. % , 于 抗 细 菌 感 染 的 有 占 73 用
药 物 的使 用 有关 。A R最 常见 表 现 为皮 肤及 其 附 件 损 害 。 结论 应 合 理 使 用 抗 感 染 药 物 , 强对 抗 感 D 加
【 关键 词 】 药 品 不 良反 应 ; 析 ; 感 染 药 分 抗
在 医药 事 业 迅 猛 发 展 和 患 者 维 权 意 识 逐 渐 高 涨 的 当 前 情势下 , 如何 安 全 、 效 、 理 地用 药 已 成 为 临 床 医务 工 作 者 有 合 必 须 面 对 的 重要 课 题 之 一 。对 于 说 明 书 上 标 注 清 楚 的不 良
2 0 1 6. 0 6: 0
3 讨 论
[ ] 李 端 , 明. 理 学 . 民卫 生 出 版社 ,03:0 . 2 殷 药 人 20 4 3 [ ] 刘 亚军, 燕萍. 3 谢 紫外 分光 光 度 法 测 定 利 巴 韦 林 葡 萄 糖 注 射 液
中利 巴韦 林 的 含 量 . 峡 药 学 ,0 0 1 ( ) 3  ̄3 海 2 0 ,2 2 :2 .
[ ] 安 登 魁 . 代 药 物 分 析 选 论 . 国 医 药 科 技 出 版 社 ,0 2 4 现 中 20 :
3 2 3 3 4 .4 .
( 收稿 日期 :0 70 -2 2 0 -60 )
・
临床研究 ・
9 8例 药 品不 良反应 报告 分 析
贾魁 荣
【 要】 目的 了解 我院药品不良反应 ( des du eco , D 发生的特点 , 进临床合 理用 摘 avr rgrat n A R) e i 促
3 I 依 诺 沙 星 、 巴韦 林 在 5 葡 萄 糖 中稳 定 。本 实验 采 用 . 利 % 5 葡 萄糖 作 为 溶 媒 。 % 3 2 实 验表 明 , 诺 沙 星和 利 巴韦林 在 5 葡 萄糖 中 配伍 时 , . 依 %
在 2 ℃ 、  ̄ 时 0~ 5 3C 7 6h内 配伍 液均无 色 、 明 、 澄 无气 体 、 无沉淀 。 3 3 配 伍 液 在 2 0~ 0 m 范 围 内 扫 描 , 形 及 峰 位 均 未 . 0 4 0n 峰 发 生变 化 , 无 杂 峰 出现 。 也
34 依诺沙 星 和利 巴 韦林 的含 量 在 2 ℃时有 所 下 降 , . 5 在
3 C时 基 本 不 变 。 7 ̄
因 此 , 临 床 常用 剂量 下 , 在 两药 可 以配 伍 使 用 。
参 考 文献
[] 1 陈 新 谦 , 有 豫 , 光. 编 药 物 学. 民 卫 生 出版 社, 金 汤 新 人
9 8例 A R报 告 , 用 描 述 性 研 究 方法 , 别 对 9 D 采 分 8例 A R患 D
者 的年 龄 、 别 、 性 家族 病 史 、 患 疾 病 、 药情 况 和 A R进 行 原 用 D 调 查 , 对 上 述 结 果 进 行 分 类 统计 分析 。 并
2 结 果
根据 WH O报 告 , 球 死 亡 人 数 中有 近 17的 患 者 是 死 于 不 全 / 合 理 用 药 。在 我 国 , 有 关 部 门 统 计 , 物 不 良反 应 在 住 据 药
院 患者 中的 发 生率 约 为 2 % J 因此 , 展 A R监 测 工 作 , 0 。 开 D
2 1 A R患 者 年 龄 与 性 别 分 布 . D
9 8例 药 品 不 良 反 应 中 ,
20 04年有 4 0例 ,05年 为 5 20 8例 , 女 比例 为 1 2 3 。其 中 男 : .8
药 。 方法 对 我 院 20 0 4年 1月到 20 0 5年 1 2月 收集 到 的 9 8例 A R报 告从 药 物 种类 、 感染 药 物 类别 、 D 抗 9 8例 AD 中 , 要 与 抗 感 染 R 主 涉及 的器 官 系统 、 药途 径 及 患 者 年龄 、 给 性别 等 方 面 进行 统 计 分 析 。 结 果 染药 物 的质 量监 督 , 以减 少 A R的 发 生 。 D .
维普资讯
中 国临 床实 用 医 学 2 0 0 8年 1月第 2卷 第 1 期
C iaC i P a d Jn 0 7 V 12 N . hn l r Me ,a 2 0 , o. , o 1 n c
・
53 ・
25 结 果 .
6h内配 伍 液 均 无 色 、 明 、 气 体 、 沉 淀 。 峰 澄 无 无
以保 障 患者 的健 康 与 生命 安全 。
1 资 料 与 方 法
ห้องสมุดไป่ตู้
资料来源于我院 20 04年 1月 到 20 0 5年 1 2月 收 集 到 的
反 应 和 禁 忌 证 , 们 往 往 可 以预 见 和 规 避 , 患 者 的 体 质 千 我 但
差 万 别 , 们 往 往 在 合 理 规 范 用 药 以后 , 然 会 出现 一 些 无 我 依 法 控 制 的 与 用药 目的无 关 且 给 用 药 者 带 来 损 害 的 药 品 效 果 。
