第8章 气体动理论
气体动理论作业

第八章气体动理论
8-2 一容器内储有氧气,其压强为1.01105 Pa ,温度 为 27.00 C,求:(1)气体分子的数密度;(2)氧气
的分子质量;(3)分子的平均速率;(4)分子的平均 平动动能。
解: (1)分子数密度 由理想气体物态方程
p nkT
n p kT
1.01105 1.381023 300
分布函数表达式(3)求a与 v0之间 关系;(4)求速率
在 1.5v0 : 2.0v0间隔内的粒子数;(5)求粒子的平均速 率;(6)求 0.5v0 : v0区间内粒子的平均速率。
解:(6) 速率在 0.5v0 : v0 间隔内的粒子数
Nf (v)
N a
N
1 2
v0
a
1 2
v0 2
a 2
3 8
av0
2v0 v
v v N
7 9
v0
习题选解
第八章气体动理论
8-3 在容积为 2.0L 的容器中,有内能为 6.75102 J的 氧气。(1)求气体的压强; (2)若容器中分子总数 为 5.41022 个,求分子的平均平动动能及气体的温度。
解: (1)求气体的压强
内能: E m 5 RT M2
物态方程: pV m RT M
E 5 pV 2
压强: p 2E 1.35105 Pa 5V
习题选解
第八章气体动理论
8-3 在容积为 2.0L 的容器中,有内能为 6.75102 J的 氧气。(1)求气体的压强; (2)若容器中分子总数 为 5.41022 个,求分子的平均平动动能及气体的温度。
平均速率
v vf (v)dv
0
v v0 v a vdv + 2v0 v a dv
气体动理论

第十三章 气体动理论本章从理想气体的微观组成出发,假以统计性假设,推出理想气体的压强和温度公式,揭示了压强和温度的本质;提出了理想气体内能的概念,介绍了理想气体能量按自由度均分原理;阐述了理想气体的麦克斯韦速率分布率。
这称为气体动理论。
气体动理论的产生和发展凝聚了众多物理学家的智慧和心血。
早在1678年,胡克就提出了气体压强是由大量气体分子与器壁碰撞的结果的观点。
之后,在1738年,伯努利根据这一观点推导出压强公式,并且解释了玻意耳定律。
1744年,俄国的罗蒙诺索夫提出了热是分子运动表现的观点。
在19世纪中叶,气体动理论经克劳修斯、麦克斯韦和玻耳兹曼的努力而有了重大发展。
1858年,克劳修斯提出气体分子平均自由程的概念并导出相关公式。
1860年,麦克斯韦指出,气体分子的频繁碰撞并未使它们的速度趋于一致,而是达到稳定的分布,导出了平衡态气体分子的速率分布和速度分布。
之后,麦克斯韦又建立了输运过程的数学理论。
1868年,玻耳兹曼在麦克斯韦气体分子速率分布律中又引进重力场。
第一节理想气体状态方程一、状态参量1.状态参量概念如何描述系统的冷热变化规律,这就需要一些物理量。
假设气体的质量为 m ,其宏观状态一般可以用气体的压强p 、体积V 和温度T 三个物理量来描述。
如果在热力学过程中伴随着化学反应,还需要物质的量、摩尔质量 、物质各组分的质量等物理量来描述。
如果热力学系统处于磁场中,还需要电场强度E 、电极化矢量P 、磁场强度H 和磁化强度M 等物理量来描述。
选择几个描写系统状态的参量,称为状态参量。
2.状态参量分类按照不同的划分标准,状态参量可作如下划分:(1)按状态参量描写系统的性质划分可分为:V P E P H M几何参量:描述系统的空间广延性。
如体积 。
力学参量:描述系统的强度。
如压强 。
化学参量:描述系统的化学组分。
如各组分的质量,物质的量。
电磁参量:描述系统的电磁性质。
如电场强度 ,电极化强度 ,磁场强度 ,磁化强度 。
气体动理论

气体动理论(kinetic theory of gases)是19世纪中叶建立的以气体热现象为主要研究对象的经典微观统计理论。
气体由大量分子组成,分子作无规则的热运动,分子间存在作用力,分子的运动遵循经典的牛顿力学。
根据上述微观模型,采用统计平均的方法来考察大量分子的集体行为,为气体的宏观热学性质和规律,如压强、温度、状态方程、内能、比热以及输运过程(扩散、热传导、黏滞性)等提供定量的微观解释。
气体动理论揭示了气体宏观热学性质和过程的微观本质,推导出宏观规律,给出了宏观量与微观量平均值的关系。
它的成功印证了微观模型和统计方法的正确性,使人们对气体分子的集体运动和相互作用有了清晰的物理图像,标志着物理学的研究第一次达到了分子水平。
《大学物理》第8章气体动理论练习题及答案

《大学物理》第8章气体动理论练习题及答案练习1一、选择题1. 在一密闭容器中,储有A、B、C三种理想气体,处于平衡状态。
A种气体的分子数密度为n1,它产生的压强为p1,B种气体的分子数密度为2n1,C种气体的分子数密度为3n1,则混合气体的压强p为( )A. 3p1;B. 4p1;C. 5p1;D. 6p1.2. 若理想气体的体积为V,压强为p,温度为T,一个分子的质量为m,k为玻尔兹曼常量,R为普适气体常量,则该理想气体的分子数为( )A. pVm⁄; B. pVkT⁄; C. pV RT⁄; D. pV mT⁄。
3. 一定量某理想气体按pV2=恒量的规律膨胀,则膨胀后理想气体的温度( )A. 将升高;B. 将降低;C. 不变;D. 升高还是降低,不能确定。
二、填空题1. 解释下列分子动理论与热力学名词:(1) 状态参量:;(2) 微观量:;(3) 宏观量:。
2. 在推导理想气体压强公式中,体现统计意义的两条假设是:(1) ;(2) 。
练习2一、选择题1. 一个容器内贮有1摩尔氢气和1摩尔氦气,若两种气体各自对器壁产生的压强分别为p 1和p 2,则两者的大小关系是 ( )A. p 1>p 2;B. p 1<p 2;C. p 1=p 2;D. 不能确定。
2. 两瓶不同种类的理想气体,它们的温度和压强都相同,但体积不同,则单位体积内的气体分子数为n ,单位体积内的气体分子的总平动动能为E k V ⁄,单位体积内的气体质量为ρ,分别有如下关系 ( )A. n 不同,E k V ⁄不同,ρ不同;B. n 不同,E k V ⁄不同,ρ相同;C. n 相同,E k V ⁄相同,ρ不同;D. n 相同,E k V ⁄相同,ρ相同。
3. 有容积不同的A 、B 两个容器,A 中装有刚体单原子分子理想气体,B 中装有刚体双原子分子理想气体,若两种气体的压强相同,那么,这两种气体的单位体积的内能E A 和E B 的关系( )A. E A <E B ;B. E A >E B ;C. E A =E B ;D.不能确定。
气体分子动理论

气体分子动理论气体是物质存在的其中一种形态,它的分子运动对于我们理解气体的性质至关重要。
气体分子动理论是一种描述气体性质的科学理论,它通过解释气体分子的运动行为和碰撞规律,为我们提供了对气体行为的深入认识。
1. 分子运动的基本规律气体分子的运动有其基本规律,其中最重要的是玻尔兹曼分布规律。
根据玻尔兹曼分布规律,气体分子的速度分布服从高斯分布,即呈现一个钟形曲线。
这意味着气体分子的速度有一定的平均值,同时也存在一定的速度分散。
这种分布规律的存在,决定了气体的宏观性质,如压强、温度等。
2. 碰撞与压强气体分子之间的碰撞是气体压强产生的主要原因。
当气体分子运动速度较慢,分子之间碰撞不频繁时,气体的压强较低。
相反,当气体分子运动速度较快,分子之间碰撞频繁时,气体的压强较高。
根据气体分子动理论,气体压强与温度呈正相关,其数学关系为压强和温度的乘积与分子间平均速度的平方成正比。
3. 温度与分子速度气体分子运动的速度与气体的温度有着密切的关系。
根据气体分子动理论,气体温度与分子平均动能成正比。
换句话说,温度越高,气体分子的平均动能越大,分子的平均速度也会增加。
这也解释了为什么在相同温度下,不同气体的分子速度可能不同的原因。
例如,氢气分子较轻,根据等温分子速度公式,它的速度较大;而氮气分子较重,其速度相对较低。
4. 分子扩散与扩散速率分子扩散是气体分子运动的另一个重要现象。
根据气体分子动理论,气体分子会自发地从高浓度区域向低浓度区域扩散。
扩散速率受到多种因素的影响,如温度、分子间相互作用力以及分子质量等。
高温下的气体分子动能较大,扩散速率较快;而分子间的相互作用力越大,扩散速率越慢。
5. 分子间相互作用力气体分子间存在一定的相互作用力,这种作用力对气体性质有着重要影响。
分子间相互作用力可以分为吸引力和斥力。
对于吸引力较大的气体分子,它们的运动速度相对较慢,而分子间距离较小。
这种相互作用力称为范德华力。
相反,当气体分子间的斥力较大时,其运动速度较快,分子间距离较大,这种相互作用力被称为排斥力。
第08章气体动理论

nv F (4) P nm ds n i
2 nmvx
平衡态下,分 2 2 2 子速度按方向 vx v y vz 1 v 2 3 分布均匀,即
1 P nm v 2 3
vi
l3
A1
l1
l2
x
22
z
1 2 1 2 P nm v n t v 2 3 3 3
1m 10 l
3 3
8
3.温度T 从热学角度描写气体状态的物理量。
国际单位:绝对温标 T 开,k 常用单位:摄氏温标 t 度, C 4.摩尔数
T t 273.15
气体质量 摩尔质量
M M mol
单位:摩尔,mol 5.普适气体恒量 R
R 8.31 J mol-1 k-1
马略特定律、盖—吕萨克定律、查理定律的气体。
2.理想气体的状态方程
一个热力学系统的平衡态可由四种状态参量确定。 对于一定量的气体,在平衡态下,如果忽略重力的作用,可 以用体积V、压强P、温度T来描述它的状态。 气体状态方程:表征气体平衡态的三个状态参量T、 V、和P之间 存在着的函数关系。
7
M 理想气体状态方程: PV RT RT M mol
如道尔顿板实验,开始黄豆 落入哪个槽是无规律的,但 随着黄豆的增多,黄豆的分 布出现一定的统计规律。
21
三、理想气体的压强公式
压强的微观实质:大量气体分子碰撞器壁的平均结果 (1)取长为 vix 底面积为 ds 体积元,单位体积元内速 率为 vi x的分子数密度为 ni (2)这些分子单位时间对ds的冲量为2mvix×ni vix ds 2 (3)对所有vix>0 求和 F 1 2m ni vixds 2 i y
气体动理论基础

dt
dt
•dt时间内能遇到dA上旳分子数为:
ni ixdtdA
•这些分子在dt时间内对dA总旳冲量:
dIi niixdtdA(2mix )
dA x
•全部分子对器壁旳总冲量:
dI 1 2
2mni
2 ix
dAdt
i
dF
mni
2 ix
dA
i
i dt ix dt
4.理想气体旳压强公式 p dF dA
A
C
若 A 和 B、B 和 C 分别热平衡,
则 A 和 C 一定热平衡。
B
(热力学第零定律)
处于相互热平衡状态旳多种系统拥有某一 共同旳宏观物理性质
——温度 温标:温度旳数值表达措施。
摄氏温标、热力学温标
T t 273.15
8-3 温度旳统计解释
一、温度旳统计解释
pV m RT M
p 1 N RT n R T
p
mni
2 ix
m
ni
2 ix
i
i
2 x
ni 2ix
n
p
nm
2 x
平衡态下
x2
y2
z2123源自p 1 nm 23
t
1 m 2
2
分子旳平均平动动能
p
2 3
n
t
温度旳宏观定义:
表征物体旳冷热程度
初
A
绝热板
A、B 两体系互不影响
态
B
各自到达平衡态
末
A
导热板
A、B 两体系到达共同
态
B
旳热平衡状态
v 8kT 8RT 1.60 RT
m M
第八章 气体分子运动论

《普通物理学》电子教案
第八章
气体动理论
第八章 气体动理论
一、本章要求:
1. 2. 掌握理想气体状态方程,并能熟练的加以应用。 理解理想气体的温度公式和压强公式,了解系统的宏观性质是微观运动的 统计表现。 3. 理解自由度概念, 掌握能量按自由度均分定理, 并能熟练用于理想气体 内能的计算。 4. 理解速率分布函数和速率分布曲线的物理意义, 会计算理想气体平衡态 下的三种特征速率(最概然速率,平均速率,方均根速率)。 5. 理解气体分子平均碰撞频率和平均自由程。
1 2 2 2 根据统计假设,有 v x = vy = v z2 , v x = v 2 ,应用这一关系,从前面的压强 p 的 3
6
电气信息工程学院精品课程
《普通物理学》电子教案
第八章
气体动理论
关系式得到理想气体的压强公式:
1 2 1 2 p = nmv 2 或 p = n( mv 2 ) = nε 3 3 2 3
状态方程:
pv = M
统计平均量:
RT
µ
统计规律
压强公式
p =
2 3
nω
p = nkT
温度公式 T = 速率分布函数:
f (v) = dN Ndv
2ω 3k
能量按自由度均分定 理:
3 2
平均平动动能 ω =
1 2
mv
2
麦克斯韦速率分布律:
f ( v ) = 4π ( m 2πkT )
2
v e
− mv 2
二、知识系统图:
微观模型: 1) 分子视为质点 2) 分子自由运动 3) 分子碰撞是完全弹性的 4) 遵从经典力学规律 宏观量是微观量 的统计平均值
气体动理论公式总结
1.自由度i=t+r
单原子分子 i=t=3
刚性双原子 i=t+r=3+2 刚性三原子i=t+r=3+3
2.分子平均平动动能
t
t 2
kT
3 2
kT
3.分子平均转动动能
r
r 2
kT
4.分子平均动能
k
i kT 2
5.气体内能
E
i RT
2
i pV 2
2
四、麦克斯韦速率分布律
1.速率分布函数: f (v) dN Ndv
3、均匀带电无限长直导线
E 2 0 r
4.半径为R的均匀带电球面
E外
q
4 0r 2
E内 0
q
q
U外 4 0r U内 40R
5.无限大均匀带电平面
E
2 0
15
七、静态平衡时的导体 1. 导体内部场强为0。导体表面附近场强方向与导
体表面垂直。 2.导体为等势体(电势处处相等)。
3. 导体内无电荷,所有电荷分布于表面。
(1)
D dS q0 电场的高斯定律
(2)
E dl
L
S
B
d
S
电 场 的
环路定理
t
(变化的磁场激发电场)
(3) B d S 0
磁场的高斯定律
(4)
S
H dl
L
Ic
d D
dt
Ic
D dS t
磁 场 的 环 路 定 理 (变化的电场激发磁场)
27
第13 章量子物理
一、黑体辐射
v2 b v2 f (v)dv / b f (v)dv
a
气体动理论

2 x
2 y
2 z
1 2
3
二、理想气体的压强公式
对压强的统计解释
气体的压强是由大量分子 在和器壁碰撞中不断给器 壁以力的作用所引起的, 压强是气体分子给容器壁 冲量的统计平均量。
例: 雨点对伞的持续作用。
压强公式的推导:
单位时间内分子a作用在A面上的作用力:
l3 l2 z
y
v a vx A
Fa 2mvx vx 2l
§1 气体的微观图像
一、原子(atom)
“假如在一次浩劫中所有的科学知识都被摧毁, 只剩下一句话留给后代,什么语句可用最少的 词包含最多的信息?我相信,这是原子假说,即 万物由原子(微小粒子)组成.”——费曼
道尔顿确立 了原子概念
原子是化学元素的基本单元
现代的仪器已可以观察和测量原子的大小 以及它们在物体中的排列情况, 例如 X 光 分析仪,电子显微镜, 扫描隧道显微镜等.
引言
气体动理论是从气体分子热运动的观点出发, 运用统计方法研究大量气体分子的宏观性质和统 计规律的科学,它是统计物理学最基本的内容。 本章将根据气体分子模型,研究气体的压强与温 度等宏观性质和分子速率分布规律与能量分布规 律等统计规律,从微观角度揭示这些性质和规律 的本质,同时穿插介绍这些理论的一些应用.
2 x
2 y
2 z
v y
o
vv x
2
2 x
2 y
2 z
v z
12
2 1x
12y
12z
22
2 2x
22y
2 2z
……
N112 N112x N112y N112z N222 N222x N222y N222z
……
气体动理论

0
a vd v Nv0
2 v0
v0
a dv 1 N
2N a 3v0
八 热学
1 N N Nf ( v ) d v a d v av0 2 3 1.5 v0 1 .5 v 0
2 v0 2 v0
a 2 v vf ( v ) d v v dv Nv0 0 0
T ( K),t ( o C)
平衡态
t T 273.15
若某种气体处于热平衡、力学平衡与化学平衡之中, 就说它处在热力学平衡状态。
八 热学
与外界没有能量交换,内部没有能量转换,
也没有外场作用。 气体分子的热运动和相互碰撞永不停息,
在宏观上表现为热动平衡状态——
密度均匀、温度均匀、压强均匀。
M mol N A m
M 代入 pV RT M mol
分子数密度
M Nm
N R p T V NA
N n V
p nkT
R 玻尔兹曼常量 k 1.38 10 23 J/K NA
八 热学 2 理想气体的压强公式和温度公式 分子热运动的统计规律 分子热运动具有无序性与统计性。 气体处在平衡状态时,在容器中密度处处 均匀,因此—— 沿各个方向运动的分子数目相等,分子速 度在各个方向的分量的各种平均值也相等。
8 RT M mol RT 1.60 M mol
八 热学 2)方均根速率2 Nhomakorabeav
0
2
v v 2 f ( v) d v
v
2
3k T m
3RT RT 1.73 M mol M mol
八 热学
3)最概然速率 v p
大学物理第08章温度与气体动理论

理想气体状态方程的另一形式
1 mol 的任何气体都有:
N A 6.023 10 / mol
23
——阿伏伽德罗常量
M Nm M mol N Am
N R M T P RT V NA V M mol
P nkT
n ——分子数密度(m-3) k=R/NA=1.3810-23J/K ——玻尔兹曼(Boltzmann)常量
4
§8.1-4 平衡态 温度 理想气体状态方程 一. 平衡态
热力学系统(热力学研究的对象):
大量微观粒子(分子、原子等)组成的宏观物体。 外界:热力学系统以外的物体。
1.热力学系统分类(按系统与外界交换特点) (1) 孤立系统:与外界无能量和物质交换 (2) 封闭系统:与外界有能量但无物质交换 (3) 开放系统:与外界有能量和物质交换 2.热力学系统分类 平衡态系统
25
(2) 由于碰撞,分子可以有各种不同的速度,速度
取向各方向等概率。
z
i ixi iy j izk
i ix i
i Ni
i Ni
x
2 x
x
y
N x y z 0 N
i i
2 i 2 ix 2 iy
的、确定的规律——统计规律。 统计规律: 大量偶然事件整体满足的规律。
2
三、热学的研究方法 (1)热力学(宏观法): 实验规律→严密的推理(应用数学) 优点:可靠、普遍。缺点:未及微观本质 (2)统计物理学(微观法):
物质的微观结构+统计的方法。 优点:揭示了热现象的微观本质。 缺点:可靠性、普遍性差。
温度的数值表示法
三要素:
(1)测温物质和测温属性; (2)选定点;
大学物理2-1第八章(气体动理论)习题答案

大学物理2-1第八章(气体动理论)习题答案第8 章8-1 目前可获得的极限真空为1.33?10?11Pa,,求此真空度下1cm3体积内有多少个分子?(设温度为27℃)[解] 由理想气体状态方程P?nkT得P?故N?NVkT,N??11PVkT?300 ?61.33?10?1?101.38?10?23?3.21?10(个) 38-2 使一定质量的理想气体的状态按p?V图中的曲线沿箭头所示的方向发生变化,图线的BC段是以横轴和纵轴为渐近线的双曲线。
(1)已知气体在状态A时的温度是TA?300K,求气体在B、C、D时的温度。
(2)将上述状态变化过程在V?T图(T为横轴)中画出来,并标出状态变化的方向。
[解] (1)由理想气体状态方程PV/T=恒量,可得:由A→B这一等压过程中VATAVBVA?VBTB2010 则TB??TA??300?600 (K)因BC段为等轴双曲线,所以B→C为等温过程,则TC?TB?600 (K)C→D为等压过程,则VDTD?VCTCTD?VDVC?TC?2040?600?300 (K)(2)403020100)8-3 有容积为V的容器,中间用隔板分成体积相等的两部分,两部分分别装有质量为m的分子N1 和N2个, 它们的方均根速率都是?0,求:(1)两部分的分子数密度和压强各是多少?(2)取出隔板平衡后最终的分子数密度和压强是多少?[解] (1) 分子数密度n1?N1V1?2N1V8-1 n2?N2V2?2N2V由压强公式:P?13nmV2,132mN1V03VNV?2可得两部分气体的压强为P1?n1mV0?2P2?13n2mV0?22mN2V03V2(2) 取出隔板达到平衡后,气体分子数密度为n?N1?N2V混合后的气体,由于温度和摩尔质量不变,所以方均根速率不变,于是压强为:P?13nmV0?2(N1?N2)mV03V28-4 在容积为2.5?10?3m3的容器中,储有1?1015个氧分子,4?1015个氮分子,3.3?10?7g氢分子混合气体,试求混合气体在433K 时的压强。
气体分子动理论'

例. 扔硬币
单个小球落入位置 少量小球按位置的分布 大量小球按位置的分布 偶然事件 规律不明显 确定的规律 伽尔顿板实验
随机试验: 在相同条件下可重复进行; 每次试验有多种可能结果; 试验结果事先不可预测;
不同试验之间无关联。
(随机试验的每一个可能结果称为一个随机事件。) 伽耳顿板实验中粒子落入的位置 掷色子出现的点数 气体分子的速率、动量、动能等
y
vix
O
z
a
A1
c
I
i 1
N
t
a
v
2 ix
t
a
v
i 1
N
x
b
2 ix
F I t N 2 N 2 p vix V vix S A1 bc abc i 1 i 1
p
V
2 vix i 1
N
1 2 vx N
2 vix i 1
2
例 一容积为 V = 1.0 m3 的容器内装有 N1 = 1.0×1024 个氧分子 N2 = 3.0×1024 个氮分子的混合气体, 混合气体的压强 P = 2.58×104 Pa 。 求 解
(1) 分子的平均平动动能; (2) 混合气体的温度。
(1) 由压强公式 ,有
3 p 3 p 9.68 1021 J 2 n 2 ( N1 N 2 ) V
分子间有相互作用力 f
r0 10
10
m (
平衡位置 )
斥力
r r0 r r0
r0 结论
分子力表现为引力 分子力表现为斥力
合力
O
r0
引力
r
势能
分子有效直径
8-7 气体的运输现象
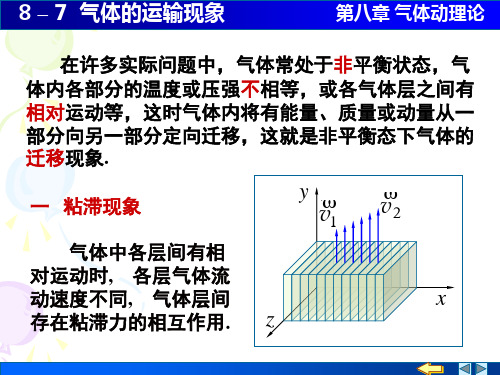
第八章 气体动理论
二 热传导现象
设气体各气层间无相对运动 , 且各处气体分子数
密度均相同, 但气体内由于存在温度差而产生热量从温
度高的区域向温度低的区域传递的现象叫作热传导现
象.
Q T S
t
x
气体热传导现象的微观
称为热导率
Q S T2 T1
本质是分子热运动能量的 T1
定向迁移, 而这种迁移是 *A
1 v CV,m
3
M
扩散系数
D 1 v
3
N S
m' D S
t
x
D 为扩散系数
n1
n2 x
*A
*B
x
8 – 7 气体的运输现象
第八章 气体动理论
气体扩散现象的微观本 质是气体分子数密度的定
n2 n1
N S
Байду номын сангаас
向迁移, 而这种迁移是通 过气体分子无规热运动来 实现的.
n1 *A
n2 x
*B x
四 三种迁移系数
粘度(粘性系数)
1 v
3
热导率
T2 x
*B
通过气体分子无规热运动 来实现的.
x
8 – 7 气体的运输现象
第八章 气体动理论
三 扩散现象
自然界气体的扩散现象是常见的现象, 容器中不 同气体间的互相渗透称为互扩散; 同种气体因分子数 密度不同, 温度不同或各层间存在相对运动所产生的 扩散现象称为自扩散 .
N D n S
t
x
n2 n1
8 – 7 气体的运输现象
第八章 气体动理论
在许多实际问题中,气体常处于非平衡状态,气
体内各部分的温度或压强不相等,或各气体层之间有 相对运动等,这时气体内将有能量、质量或动量从一 部分向另一部分定向迁移,这就是非平衡态下气体的 迁移现象.
气体动理论

第四章气体动理论一、基本要求1. 理解理想气体微观模型。
理解理想气体压强、温度的概念及其微观本质。
掌握理想气体压强、温度的公式并会做相应计算。
通过推导气体压强公式,了解气体动理论的基本研究思想和方法。
2. 理解能量均分定理,掌握理想气体内能的概念、公式及有关计算。
3. 了解麦克斯韦速率分布律、速率分布函数和速率分布曲线的物理意义,了解气体分子热运动三种统计速率。
4. 了解玻耳兹曼能量分布律。
二、内容概要(一)统计概念1.理想气体压强(1)压强概念 垂直作用于器壁单位面积上的压力。
(2)压强公式 p=n 32ε=231_v nm 为分子平均平动动能。
(4-1) (3)适用条件 理想气体(大量分子组成),处于平衡态。
(4)微观本质①由大量气体分子对器壁的碰撞所产生,表示单位时间内气体分子作用于器壁单位面积上的平均冲量。
②一定温度的平衡态下,单位体积内的气体分子数(分子数密度n)越多,或分子平均平动动能(-ε)越大,压强就越高。
-n 、-ε为气体分子微观量的统计平均值。
2. 理想气体温度(1) 温度概念 表征系统处于热平衡态的物理量。
(2) 温度公式 -ε=kT 23 (3) 适用条件 理想气体(由大量分子组成)处于平衡态。
(4) 微观本质 反映了大量分子热运动的剧烈程度,是分子平均平动动能的量度。
(二)统计规律1. 能量均分定理(1) 内容要点物质分子每个自由度的平均动能kT 21 每个分子的平均动能 -k ε=kT i 2vmol 理想气体内能 E=v RT i 2 气体自由度 i=()()()⎪⎩⎪⎨⎧刚性多原子分子刚性双原子分子单原子分子653(2) 适用条件. 式 (4-2) (4-3)----任何物质分子,温度为 T 的平衡态。
式 (4-4)----理想气体,温度为 T (室温附近)的平衡态。
2. 麦克斯韦速率分布律(1) 气体速率分布函数f(v)=Ndv dN (4-6) 表示速率v 在附近单位速率区间内的分子分布概率(即分子数占总分子数的比率)。
气体动理论知识点总结

气体动理论知识点总结气体动理论是研究气体的微观运动状态及宏观性质的一门物理学理论,是现代物理学中较为重要的分支之一。
气体动理论不仅对实际问题的探究有着重要的作用,它的理论体系及方法也为其他学科提供了有力的支持。
下面将围绕着气体运动状态、气体的性质以及气体的热力学定律三个方面,介绍气体动理论中的相关知识点。
一、气体运动状态气体动理论认为,气体分子的运动状态决定了气体的宏观控制状态。
因此,研究气体分子的运动状态对于了解气体的性质及可控性具有重要的意义。
1.分子移动气体分子无序地、自由地运动,并且分子的速度是高度非一致性的。
分子的速度与温度、分子的种类有关。
分子受温度影响,速度随温度的升高而增加。
2.分子运动轨迹气体分子在空间中做无规则运动,但可以将其平均运动速度视为直线运动。
分子的运动具有随机性,在时间、位置上无法精确定位。
3.分子碰撞气体分子之间存在碰撞,碰撞时能量和动量都会发生变化,同时碰撞前和碰撞后分子的速度方向也会发生改变。
二、气体的性质气体的性质不仅涉及气体的物理状态,还涉及气体的化学性质,气体与其他物质的相互作用,气体的电学性质等方面,其中,最为重要的性质包括以下几个方面:1.流动性:气体具有流动性,能够流动并具有一定的流动性质。
2.扩散性:气体分子具有无序运动状态,具有自由的运动方式。
在一定条件下,气体分子能够通过物质间的空隙扩散到其他区域。
3.压缩性:气体分子间的间隔较大,气体分子之间的相互作用力较弱,分子之间可以变形并发生相对位移,气体具有较好的压缩性。
4.热膨胀性:在一定温度下,气体分子具有较大的运动能,随着温度的升高,气体分子之间的反向作用力会减小,会引起体积的增加。
5.气体的状态方程:气体在不同温度下具有不同的压强、体积关系,可以利用理想气体状态方程(P V/ nRT)来描述气体的状态。
三、气体的热力学定律气体动理论依据物理实验,建立了气体的热力学学说体系,包括状态方程、热力学过程、热力学定律等。
大学物理第8章气体分子运动论

23
阿佛伽德罗常数
R=8.31J/mol· 普适气体常数 K
k=R/N =1.38J/K
0
玻尔兹曼常数
四、统计假设
平衡态下: 1、分子数密度相等。 2、分子沿任一方向的运动,机会均等。
那么对于分子的平动速度,有
v v x i v y j vzk
2 2 2 2
vx vy vz
d N Nf ( v ) d v
速率位于 v 1 v 2区间的分子数:
N v N f ( v ) d v 1
v2
C. 速率位于 v 1 v 2 区间的分子数占总数的百分比:
N
N
v2
v1
f ( v )d v
f (v)
N
N
S
o
v1 v2
v
四、 三种速率:
f(v)
1、 最概然速率Vp:
刚体:任意运动时,可分解为质心的平动及绕通 过质心的轴的转动。
y
(x, y, z)
y
b a
(xz
x
刚性双原子: i=5
y
f 刚性多原子: i=6
o
z
x
二、 能量按自由度均分原理
A、 理想气体内能: 分子间相互作 用忽略不计 分子间相互作用势能=0
理想气体的内能=所有分子的热运动动能 之总和。 B、 如果分子有i个自由度,分子的平均 动能: i
2
m 2 x l1
2
m Nx l1
2
i 1
N
m ix
2
l1
第3步:由压强的定义得出结果
y
P
F A1
第8章 气体动理论习题解答

习题8-1 设想太阳是由氢原子组成的理想气体,其密度可当成是均匀的。
若此理想气体的压强为1.35×1014 Pa 。
试估计太阳的温度。
(已知氢原子的质量m = 1.67×10-27 kg ,太阳半径R = 6.96×108 m ,太阳质量M = 1.99×1030 kg )解:mR MVm M mn 3π)3/4(===ρK 1015.1)3/4(73⨯===Mkm R nk p T π8-2 目前已可获得1.013×10-10 Pa 的高真空,在此压强下温度为27℃的1cm 3体积内有多少个气体分子?解:3462310/cm 1045.2103001038.110013.1⨯=⨯⨯⨯⨯===---V kT p nV N 8-3 容积V =1 m 3的容器内混有N 1=1.0×1023个氢气分子和N 2=4.0×1023个氧气分子,混合气体的温度为 400 K ,求: (1) 气体分子的平动动能总和;(2)混合气体的压强。
解:(1)J 1014.41054001038.123)(233232321⨯=⨯⨯⨯⨯⨯=+=-∑N N kT tε(2)Pa kT n p i323231076.21054001038.1⨯=⨯⨯⨯⨯==-∑8-4 储有1mol 氧气、容积为1 m 3的容器以v =10 m/s 的速率运动。
设容器突然停止,其中氧气的80%的机械运动动能转化为气体分子热运动动能。
问气体的温度及压强各升高多少?(将氧气分子视为刚性分子)解:1mol 氧气的质量kg 10323-⨯=M ,5=i由题意得T R Mv ∆=⋅ν25%80212K 102.62-⨯=∆⇒TT R V p RT pV ∆=⋅∆⇒=ννpa 52.0102.631.82=⨯⨯=∆=∆∴-VTR p 8-5 一个具有活塞的容器中盛有一定量的氧气,压强为1 atm 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2)理想气体温标:以理想气体作测温物质 3)热力学温标:不依赖任何具体物质特性的温标
规定:水的三相点 T0=273.16K
16
8.1.3 理想气体状态方程 理想气体:严格遵守四条定律(玻马定律、盖吕萨克定律、查理定律和阿伏伽德罗定律)的 气体其状态方程为:
理想气体的状态方程:
pV RT
p----Pa V----m3
对微观结构提出 统计方法 模型、假设
热现象规律
11
系统状态的描述:
(1)宏观描述法 用一些可以直接测量的物理量(称为宏观量) 来描述系统的宏观性质 例如:p,V,T,M(磁化强度)等 (2)微观描述法 给出系统中每个微观粒子的力学参量(称为宏 观量)来描述系统 例如:分子的质量、速度、直径、动量 微观量与宏观量有一定的内在联系。
P nkT
----理想气体状态方程 的另一形式
18
8.2 理想气体的压强和温度
8.2.1 理想气体的压强 1.理想气体的微观模型和统计假设
(1) 对单个分子个体力学性质的微观假设 a.气体分子当作质点,不占体积; b.分子之间只在碰撞时有力作用(忽略重力) c. 分子之间是完全弹性碰撞
d. 分子的运动规律遵从牛顿力学
R=8.31J/mol· K
T----K
设:m--单个分子质量; μ --摩尔质量;分子数 为N,M为体系内气体的总质量
17
因为 pV RT, N / N A
N R p T nkT V NA
n ----分子数密度(单位体积中的分子数)
k = R/NA = 1.3810 –23 J/K ----玻耳兹曼常数
C
轴
C (x, y, z)
确定质心C, 需知要3个平动 自由度, t =3 (x,y,z) 确定轴的取向,需要2个转 动自由度( , ); r …… 转动自由度, r = 2 ( , )
x
y
总自由度:i=t+r=5
37
3. 刚性多原子分子(可看作刚体)
y
质心, 要3个平动自由度;
10
热力学系统的分类: 孤立系统——和外界无质量、能量交换 封闭系统——和外界无质量交换、有能量交换 开放系统——和外界既有质量交换、也有能量交换 2.热学的研究方法
▲ 热力学(thermodynamics) 逻辑推理
宏观基本实验规律
热现象规律
▲ 统计力学(statistical mechanics)
t =3 (质心坐标 x,y,z) 确定过质心的轴的方位需2 个转动自由度( , );
x
z
确定分子绕轴转动需要1个 转动自由度 ; r = 3 ( , , ) 总自由度: i = t + r=6
38
说明:
以上得到的自由度,我们基于以下 两点: 刚性+质点 一般的n原子分子总的自由度为3n, 也就是3个平动自由度,3个转动自 由度, 3n-6个振动自由度
9
8.1 热学的基本概念
8.1.1 热力学系统 平衡态
1.热学的研究对象及内容
热学: 研究热现象及其规律的学科 宏观:热现象是与温度有关的现象 微观:热现象是与分子热运动有关的现象 对象:宏观物体(大量分子原子的系统) 或物体系 — 称为热力学系统 。
热力学系统以外的物体称为外界。 例:若汽缸内气体为系统,其它为外界。
(1) 如图考虑速度为 vi 的第i
个分子对A面的一次碰撞 因为是弹性碰撞, 分子碰到A面后速度分量
由vix变为–vix 分子的动量增量为
z
A′
y
mvix
y0
A
mvix
z0
x0
x
(– mvix) – mvix= – 2mvix 分子受的冲量为 – 2mvix A面受到的冲量为 2mvix
26
3
规范作业
前三周的周二到周五的上班 时间前往大学物理实验中心
202购买规范作业
考试内容以规范作业为基础;考试不是目的
4
课程规范、要求: 1、课堂出勤。课程每学分不得超过一 次缺勤,每缺勤一次,期末总成绩扣五 分;若缺勤次数超过课程学分数,则取 消该门课程的期末考试资格。本次课程 3.5学分 2、作业。课程作业缺交量超过作业总 量30%及以上的,取消该门课程的期末 考试资格。办理课程免听的学生亦参照 此规定执行。一般12次作业
(2)第i个分子与A面碰撞一次所需时间为: 2x0 / vix
(3) t 时间内第i个分子与A 面碰撞的次数:
vix t / 2 x0
A′
y
mvix
y0 z0 z
N
A
(4) t 时间内A面受到第i个 分子的冲量为
vix t mvix t I i 2mvix 2 x0 x0
y0 z0 z
mvix
x
x0
1 2 定义分子平均平动动能: t 2 mv
1 2 P nmv ----理想气体压强公式 3
2 压强公式又可表示为: p n t 3
28
说明: 1.压强公式是一个统计规律;
压强公式
宏观量 p
微观量的 统计平均值
t
∴压强只有统计意义 2.压强是由于大量气体分子碰撞器壁产生的,它 是对大量分子统计平均的结果。对单个分子无压 强的概念。 3.上述压强公式适用于任意形状的容器
平衡态是热学中的一个理想化状态。
13
描写平衡态下系统宏观属性的一组独立宏观 量,称为状态参量(state parameter)
例如:气体系统的 p、V、T 一组状态参量
描述
对应
一个平衡态
状态参量之间的函数关系称为状态方程,记作:
f ( p, V , T ) 0
14
8.1.2 热力学第零定律 (温度相同的判定原则)
4.无法用实验直接验证
29
8.2.2 理想气体的温度
2 将 p = nkT 代入压强公式得 nkT n t 3
3 t kT 2
1.表示宏观量温度T与微观量的统计平均值之间 的关系----温度的统计意义。 2.温度是大量气体分子热运动剧烈程度的量度 与气体种类无关----温度的微观实质。 3.分子的平均平动动能只与T有关,与气体性 质无关,与整体定向运动速度无关。
Pi xi2
20
统计规律有以下几个特点: a.只对大量偶然的事件才有意义
b.它是不同于个体规律的整体规律
(量变到质变)
个体事件有偶然性,大量偶然事件整体遵守
统计规律
c.总是伴随着涨落 表演实验 伽耳顿板
21
单个粒子行
为--- 偶然
大量粒子行
为--- 必然
22
(3) 对分子集体的统计规律假设 a.平衡态时,在无外场的情况下,分子在各处出 现的概率相同, 即:气体分子在空间的分布是均匀的,分子数密 度处处相同 dN N d V ---体积元 n (宏观小,微观大) dV V b.平衡态时分子的速度按方向的分布是各向等概 率的。
19
(2)统计规律 大量偶然事件从整体上反映出来的一种必然的 规律性。 定义: 某一事件 i 发生的概率为 Pi
Pi lim
N
Ni N
Ni……事件 i 发生的 次数; N……各种事件发生的总次数
2 N x i i i
统计平均值的计算:
x
N i xi
i
N
i
x2
N
i
Pi xi
相同。
35
8.3 能量均分原理
8.3.1 自由度
自由度-确定一个物体的空间位置所需要的独 立坐标数,用i 表示 。 1.单原子分子(如He, Ne, Ar等 ) 可视为质点,确定它在空间的位置需3个独立 坐标,故有3个自由度,称为平动自由度。 i = t =3 t ……平动自由度
36
2. 刚性双原子分子(如 O2 ,H2 ,CO ) 两原子之间成细杆哑铃似的结构, z l γ 0
又
3 t kT 2
2 混合气体的的温度: T t =400K 3k
34
例题 两瓶不同种类的气体,温度、压强相同,但 体积不同,则 (1)它们单位体积中的分子数 相同。 (p=nkT) (2)它们单位体积中的气体质量 不相同。
(=mn)
(3)它们单位体积中的分子平均平动动能的总和
3 3 n t nkT p 2 2
2
32
1 2 t mv 2
2 p n t 3
例 . 在273K时:
3 2 21 3.53 10 eV t kT 5.65 10 J 2
H2分子
v
2
3 8.31 273 1836 m/s 3 2.02 10
O2分子
v
2
3 8.31 273 461 m/s 3 32 10
30
4.运动是绝对的,因而绝对零度不可能达到 5.成立条件:理想气体平衡态。
1 2 t mv 2
3 t kT 2
3kT v m
2
3RT
称为方均根速率
31
总结:
pV RT
P nkT
1 P nmv 2 3
3 t kT 2
3kT 3RT v m
5
课程规范、要求:
6
课件下载方式:
用户名密码为学号 课程:大学物理下 左侧—教学材料 另:qq群:54686531
7
分组安排:
1、环资 --组长?
2、矿业 ---组长?
8
第8章
气体动理论
(The kinetic theory of gas)
