定位效应的解释
轻松获得好人缘!人际交往必知的21个心理学定律

人际交往达人往往都是“心理学家”,每个人在与他人交往的过程中,不仅需要你口若悬河,还需要你善于听话。
换句话说,这需要你与他人进行心理上的沟通与交流。
为此,你需要知道21个心理学定律。
1、破窗效应破窗效应来源于美国斯坦福大学心理学家菲利普·津巴多(Philip Zimbardo)于1969年进行了一项实验,他找来两辆一模一样的汽车,把其中的一辆停在加州帕洛阿尔托的中产阶级社区,而另一辆停在相对杂乱的纽约布朗克斯区。
停在布朗克斯的那辆,他把车牌摘掉,把顶棚打开,结果当天就被偷走了。
而放在帕洛阿尔托的那一辆,一个星期也无人理睬。
后来,辛巴杜用锤子把那辆车的玻璃敲了个大洞。
结果呢,仅仅过了几个小时,它就不见了。
以这项实验为基础,政治学家威尔逊和犯罪学家凯琳提出了一个“破窗效应”理论,认为:如果有人打坏了一幢建筑物的窗户玻璃,而这扇窗户又得不到及时的维修,别人就可能受到某些示范性的纵容去打烂更多的窗户。
久而久之,这些破窗户就给人造成一种无序的感觉,结果在这种公众麻木不仁的氛围中,犯罪就会滋生并蔓延。
破窗效应告诉我们:任何一种不良现象的出现,都会传递出一种负面的能量,这种负能量会导致不良现象的无限扩展。
(比如一条人行道有些许纸屑,不久后就会有更多垃圾,最终人们会视若理所当然地将垃圾顺手丢弃在地上)同时我们也要警惕我们身边看起来“偶然,个别的轻微错误,及时补救和更正,防止损失的无限扩大。
2、詹森效应之前美国有一名叫詹森的运动员,平时训练有素,实力雄厚,但在体育赛场上却连连失利,让自己和他人失望。
不难看出这主要是压力过大,过度紧张所致。
由此人们把这种平时表现良好,但由于缺乏应有的心理素质而导致正式比赛失败的现象称为詹森效应。
詹森效应从心理学角度讲是一种浅层的心理疾病,是人在意识中将现有的困境无限放大,从而产生的异常现象。
我们应该如何避免自己陷入詹森效应呢?以下又三点建议供你参考。
①注重过程,淡化结果。
苯环的定位规则概要

二、定位效应的解释
2、间位定位基的定位效应
存在着:
吸电子诱导效应(-I) 吸电子共轭效应(-C)
O N
O
δ
-
δ
-
间位取代基使苯环上电子云密度下降,苯环钝化,亲电试剂难于进攻。 吸电子基团
B
B 的定位能力次序大致为(从强到弱) -NR3, -NO2, -CF3, -CCl3, -CN, -SO3H, -CHO, -COR,-COOH, -CONH2。
药用基础化学/芳香烃
苯环的定位规则
62%
NO2
浓H2SO4
33%
NO2 NO2
5%
NO2
NO2
+ HNO3(发烟)
ห้องสมุดไป่ตู้90℃
+
NO2
+
1%
NO2
6%
93%
第二个取代基进入的位置是受苯环上原有基团的影响,这种 现象称为定位效应。苯环上原有基团称为定位基。
一、定位效应
1、邻对位定位基
-NHCH3 >–NH2 >– OH >– OCH3 >–R >–X
三、定位效应的应用
1、预测反应产物
(1)两个定位基对于引入第三取代基的定位效应 一致:
三、定位效应的应用
1、预测反应产物
(2)两个定位基对于引入第三取代基的定位效应不一致
a.同类型—定位效应 强的取代基所决定
三、定位效应的应用
1、预测反应产物
(2)两个定位基对于引入第三取代基的定位效应不一致
b.不同类型—由邻 对位定位基决定
2、间位定位基
–N+(CH3)3 >–NO2 >–SO3H >–CHO >–COOH
定位效应的解释

同学们,大家好。
今天要讲的是定位效应的解释。
通过上节课的学习,我们已经知道,有些基团会使苯环的亲电取代反应活性增大,称为活化基;有些基团会使苯的亲电取代反应活性减小,称为钝化基;苯环上的基团还会影响取代位置,根据定位效果分为邻对位定位基和间位定位基。
苯环上原有基团为什么会影响亲电取代活性和取代位置呢?今天我们就来分析并解释这一问题。
大家都知道,苯亲电取代时,亲电试剂靠近苯环生成σ-络合物是整个反应的决速步骤。
同样,取代苯反应的决速步骤也生成σ-络合物,如图,决速步骤中苯与亲电试剂的成键能力与苯环上电子密度有关。
若原有基团是供电子基,苯环电子密度增大,容易受到亲电试剂的进攻,则亲电取代活性增大,该基团就是活化基。
若原有基团是吸电子基,会使苯环电子密度减小,吸引亲电试剂的能力减小,则反应活性减小,该基团是钝化基。
因此判断一个基团是活化基还是钝化基,只需要分析基团与苯环间的电子效应(包括诱导效应和共轭效应)来确定该基团是供电子基还是吸电子基即可。
那么如何分析判断一个基团是邻对位定位基还是间位定位基呢?从反应式可以看出,决速步骤中生成了三种σ-络合物:邻位、间位、对位,这三个平行反应的相对速度决定了最终产物的多少,即决定了取代位置。
这三个平行反应的相对速度可以从两个角度比较。
一方面可以从反应物中邻、间、对三个位置上碳的电子密度相对大小分析。
基团与苯环间的电子效应使邻间对位碳上电子密度不同,电子密度大的碳自然容易受到亲电试剂的进攻而表现出较大的反应活性。
另一方面也可以从三个σ-络合物的稳定性比较。
σ-络合物越稳定,能量越低,生成时经历的过渡态能量越低,反应的活化能越小,反应速度快,相应的σ-络合物生成的就多。
通过以上讲解,大家脑海中要有这样几个概念:第一,分析基团与苯环间的电子效应可以判断基团是供电子基还是吸电子基,从而来确定基团使苯环活化还是钝化;第二,分析基团与苯环间的电子效应可以比较邻间对位碳的电子密度大小,以此判断基团的定位效果;第三,分析σ-络合物的稳定性也可以判断基团的定位效果。
苯环的定位规则概要
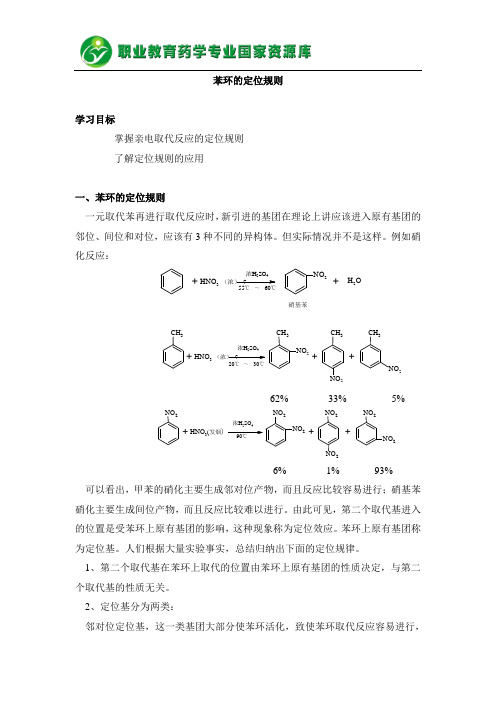
苯环的定位规则学习目标掌握亲电取代反应的定位规则 了解定位规则的应用一、苯环的定位规则一元取代苯再进行取代反应时,新引进的基团在理论上讲应该进入原有基团的邻位、间位和对位,应该有3种不同的异构体。
但实际情况并不是这样。
例如硝化反应:CH 3HNO 3 (浓) ?+NO 2CH 3+浓H 2SO 420℃~30℃CH 3NO 2+CH 3NO 262% 33% 5%NO 2HNO 3(发烟)+NO 2NO 2+ 浓H 2SO 4NO 22NO 2NO 2+6% 1% 93%可以看出,甲苯的硝化主要生成邻对位产物,而且反应比较容易进行;硝基苯硝化主要生成间位产物,而且反应比较难以进行。
由此可见,第二个取代基进入的位置是受苯环上原有基团的影响,这种现象称为定位效应。
苯环上原有基团称为定位基。
人们根据大量实验事实,总结归纳出下面的定位规律。
1、第二个取代基在苯环上取代的位置由苯环上原有基团的性质决定,与第二个取代基的性质无关。
2、定位基分为两类:邻对位定位基,这一类基团大部分使苯环活化,致使苯环取代反应容易进行,HNO 3(浓) ?+ 浓H SO 55℃~60℃NO 2+H 2O硝基苯故又称致活基团;能支配第二个取代基在苯环上主要取代在它的邻位和对位。
常见的邻对位定位基按定位效应强弱次序排列如下:一NR 2、一NHR 、一NH 2、一OH 、一OR 、一NHCOR 、一R 、一X 间位定位基,这一类基团大部分使苯环钝化,致使苯环取代反应较难进行,故又称致钝基团;能支配第二个取代基在苯环上主要取代在它的间位。
常见的间位定位基按定位效应强弱次序排列如下:3、在苯环上有两个取代基,欲引入第三个取代基时,第三个取代基所进入的位置,取决于苯环上原有两个基团的综合效应。
当苯环上原有两个定位基的定位作用一致时,第三个取代基进入的位置由原有两个取代基共同决定。
例如:3H232当苯环上原有两个定位基的定位作用不一致时,有两种情况:一是两个定位基为同一类时,则第三个取代基进入的位置由定位效应强的取代基决定。
苯环的定位规则概要

苯环的定位规则
62%
33%
5%
NO2
+ HN
NO2 +
NO2
+
NO2
6%
1%
NO2 NO2
93%
第二个取代基进入的位置是受苯环上原有基团的影响,这种 现象称为定位效应。苯环上原有基团称为定位基。
一、定位效应
1、邻对位定位基
-NHCH3 >–NH2 >– OH >– OCH3 >–R >–X
b.不同类型—由邻 对位定位基决定
谢
制作人:
谢
石云
2、间位定位基
–N+(CH3)3 >–NO2 >–SO3H >–CHO >–COOH
二、定位效应的解释
H
1、邻对位基的定位效应
--CH3使苯环电子云密度升高,而 活化苯环, 为邻、对位定位基。
HCH
δ
δ-
δ-
A
A 的定位能力次序大致为(从强到弱)
-O , -NR2, -NHR, -NH2, -OH, -OR, -NHCOR -OCOR, -R, -CH3 , -X
给电子基团
二、定位效应的解释
2、间位定位基的定位效应
O
O
N
存在着:
吸电子诱导效应(-I) 吸电子共轭效应(-C)
δ-
δ-
间位取代基使苯环上电子云密度下降,苯环钝化,亲电试剂难于进攻。
吸电子基团
B
B 的定位能力次序大致为(从强到弱)
-NR3, -NO2, -CF3, -CCl3, -CN, -SO3H,
-CHO, -COR,-COOH, -CONH2。
三、定位效应的应用
1、预测反应产物
苯环上亲电取代反应的定位规律

O 2 + 7O2
V2 O5 , K SO4 2 385℃~390℃
2 O
O + 4CO 2 + 4H2O
取代萘氧化时环破裂的规律: 取代基为邻对位定位基,使所在
环活化,氧化时同环破裂;取代基为间位定位基,使所在环钝化, 氧化时异环破裂。
H2 / Ni 150℃ H2 / Ni 200℃
应用:四氢化萘和十氢化萘是两种良好的高沸点溶剂。
2003年9月27日(15-16到此止) 思考题:P864:8,9
2013-6-30
作业:P866习题1的5的c,d;习题3的4,5
18
2013-6-30
10
(2)萘的性质 物理性质
萘为无色片状晶体,熔点80.2℃,沸点218℃,易升华。萘有特 殊的气味,不溶于水,溶于乙醇、乙醚及苯中。
2013-6-30
11
化学性质 ——概况 与苯相似,但芳香性比苯差,更易发生亲电取代反应。 位电子云密度比位高,亲电取代首先在位。但1与8
萘的离域能
254.98kJ•mol –1,稳定,但比两个单独苯环离域能 的总和(300kJ•mol‐1)小,故芳香性比苯差,比苯活泼。
萘衍生物的命名
与多官能团取代苯的母体优先选择次序相同。 常见官能团的优先次序为: ﹣COOH , ﹣SO3H , ﹣COOR , ﹣COX , ﹣CONH2 , ﹣CN , ﹣CHO,﹣CO﹣R,﹣OH,﹣NH2,﹣C≡C﹣, C=C ,﹣OR, ﹣X,﹣NO2。 排在前面的官能团优先选择为母体,后三个官能团以苯为母体:
原因:电子云密度较高的环,较活泼,易被氧化破裂。
苯环的定位效应

苯环的定位效应
苯环的定位效应,也称为取代基定位效应,是指苯环上已有取代基对新引入取代基进入苯环的位置的影响。
这种效应是由于取代基的电子效应和空间位阻效应引起的。
在苯环上引入取代基时,取代基会影响苯环上电子云的分布,从而影响新引入取代基的反应活性和进入苯环的位置。
一般来说,取代基分为两类:给电子取代基和吸电子取代基。
给电子取代基(如甲基、乙基等)会使苯环上的电子云密度增加,从而使亲电取代反应更容易发生,而且新引入的取代基更容易进入苯环上电子云密度较高的位置。
吸电子取代基(如硝基、卤素等)会使苯环上的电子云密度降低,从而使亲电取代反应较难发生,而且新引入的取代基更容易进入苯环上电子云密度较低的位置。
此外,取代基的空间位阻效应也会影响取代反应的位
置。
较大的取代基会阻碍新引入取代基进入苯环上空间位阻较大的位置。
因此,苯环上已有取代基的种类和位置会影响新引入取代基的反应活性和进入苯环的位置,这种效应被称为苯环的定位效应。
有机化学第06章 芳烃(2)
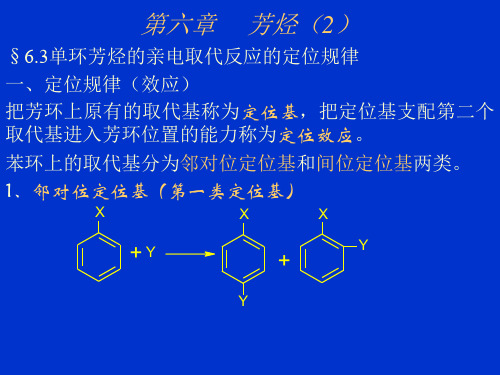
特点:
①这些取代基与苯环直接相连的原子一般都是饱和的或带
有孤电子对或带负电荷(苯环、乙烯基除外);
②大都是给电子取代基,除卤素外,这类定位基均能使苯
环上电子云密度升高,使苯环活化。因此这些定位基又称
活化基;
③这些取代苯(除卤苯外)的亲电取代反应活性比苯高,
反应速度比苯快。
(2)间位定位基 (第二类定位基) X
2
I + 2Cu
+ 2CuI
二、性质
与苯性质相似,将其中的一个苯基看作是另一个苯基的取 代基。
CH3
混酸 Δ
NO2
混酸 Δ
NO2
CH3
NO2+
NO2
+
CH3
NO2 NO2
CH3
若其中一个苯环上含间位定位基时,则发生异环取代; 若是邻对位定位基,则发生同环取代。
6.9稠环芳烃
一、 萘及其衍生物
1、化学性质
Δ ,~90%
O
O 9,10-蒽醌 OO
K2Cr2O7+H2SO4 或CrO3 + HAC
9,10-菲 醌
二、定位规律的理论解释 1、电子效应 1)邻、对位定位基对苯环的影响
δ- H
δ-
2)从共振论观点
进攻邻位 :
CH3H +
E
CH
δ- H
CH 3 H +E
CH3
进攻对位 : +
HE
CH3 +
HE
X
+Y
Y
间位定位能力由强到弱的次序大致如下:
+
NR3
NO2 , CCl3 , CN , SO3H,
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
同学们,大家好。
今天要讲的是定位效应的解释。
通过上节课的学习,我们已经知道,有些基团会使苯环的亲电取代反应活性增大,称为活化基;有些基团会使苯的亲电取代反应活性减小,称为钝化基;苯环上的基团还会影响取代位置,根据定位效果分为邻对位定位基和间位定位基。
苯环上原有基团为什么会影响亲电取代活性和取代位置呢?今天我们就来分析并解释这一问题。
大家都知道,苯亲电取代时,亲电试剂靠近苯环生成二-络合物是整个反应的决速步骤。
同样,取代苯反应的决速步骤也生成一络合物, 如图,决速步骤中苯与亲电试剂的成键能力与苯环上电子密度有关。
若原有基团是供电子基,苯环电子密度增大,容易受到亲电试剂的进攻,则亲电取代活性增大,该基团就是活化基。
若原有基团是吸电子基,会使苯环电子密度减小,吸引亲电试剂的能力减小,则反应活性减小,该基团是钝化基。
因此判断一个基团是活化基还是钝化基,只需要分析基团与苯环间的电子效应(包括诱导效应和共轭效应)来确定该基团是供电子基还是吸电子基即可。
那么如何分析判断一个基团是邻对位定位基还是间位定位基呢?从反应式可以看出,决速步骤中生成了三种一络合物:邻位、间位、对位,这三个平行反应的相对速度决定了最终产物的多少,即决定了取代位置。
这三个平行反应的相对速度可以从两个角度比较。
一方面可以从反应物中邻、间、对三个位置上碳的电子密度相对大小分析。
基团与苯环间的电子效应使邻间对位碳上电子密度不同,电子密度大的碳自然容易受到亲电试剂的进攻而表现出较大的反应活性。
另一方面也可
以从三个;---络合物的稳定性比较。
;「-络合物越稳定,能量越低,生成时经历的过渡态能量越低,反应的活化能越小,反应速度快,相应的二-络合物生成的就多。
通过以上讲解,大家脑海中要有这样几个概念:第一,分析基团与苯环间的电子效应可以判断基团是供电子基还是吸电子基,从而来确定基团使苯环活化还是钝化;第二,分析基团与苯环间的电子效应可以比较邻间对位碳的电子密度大小,以此判断基团的定位效果;第三,分析―络合物的稳定性也可以判断基团的定位效果。
也就是说不论是对活性的影响还是对定位效果的影响都和电子效应有关。
我们知道,甲基是活化基,又是邻对位定位基。
下面就以甲基为
例,通过分析甲基与苯的电子效应解释甲基为什么是活化基?为什么是邻对位定位基?甲基碳是sp3杂化,苯环碳是sp2杂化,因此苯环碳电负性大,电子由甲基向苯环偏移,甲基表现出供电子的诱导效应;甲基中一碳氢键与苯环发生一二超共轭效应,电子由甲基转向苯环,甲基表现出供电子的共轭效应。
供电子的诱导和供电子的共轭使甲基成为供电子基,使苯环上电子密度增大,亲电取代活性增大,因此甲基是活化基。
甲基为什么是邻对位定位基呢?甲基与苯环间的供电子诱导效应在苯环中传递时,如图所示,会使邻位、对位碳带部分负电性,即邻对位碳的电子密度大,间位碳电子密度小。
事实上甲苯中电子密度分布确实如此,如图所示,邻位碳电子密度是 1.017,对位是1.011,而间位只有0.999。
邻对位电子密度大容易受亲电试剂进攻而被取代,主要生成邻对位产物,所以说甲基是邻对位定位基。
甲基的定位效果也可以由匚-络合物的稳定性解释。
甲苯邻位;「-络合物的结构可以用三个极限式表示,其中第3个极限式中正电荷直接与供电子基甲基相邻,有利于正电荷的分散,因此这个极限式能量低,稳定性大。
在间位一络合物的3个极限式中没有类似的稳定的极限式,因此邻位—络合物稳定性大,间位一络合物稳定性小;对位―络合物的3个极限式中,也有一个正电荷直接与甲基相邻的稳定的极限式,所以对位—络合物也很稳定。
因为邻对位二-络合物比间位―络合物稳定,则邻对位一络合物生成的快,生成的多,失去氢离子后得到的邻对位产物就多,所以甲基是邻对位定位基。
甲基的活化能力和邻对位定位效果可以从下面能量示意图进行对
比。
甲苯的邻对位一络合物能量最低,对应过渡态能量也最低,反应最快;苯的匚-络合物能量最高,反应也最慢。
苯反应慢,甲苯反应快,所以说甲基是活化基;邻对位一络合物比间位一络合物生成的快,所以甲基是邻对位定位基。
再来看羟基。
羟基是活化基,又是邻对位定位基。
羟基为什么是活化基呢?氧的电负性大,因此羟基表现出吸电子诱导效应;氧的p 轨道与苯环发生p-二共轭,电子由氧转向苯环,因此羟基表现出供电子的共轭。
诱导效应是吸电子,共轭效应是供电子,二者作用相反,羟基究竟是吸电子基还是供电子基呢?氧和碳都是第二周期的,共轭时,氧的2p轨道和碳的2p轨道能量相近,重叠程度达,共轭效应强,因此氧的共轭效应大于诱导效应,羟基表现出供电子性,是供电子基,使苯亲电取代活性增大,所以羟基是活化基。
羟基为什么是邻对位定位基呢?苯酚的邻位一络合物的极限式中, 第四个极限式所有的原子外层都有8个电子,能量低,稳定性大,而间位一络合物的3个极限式中,带正电荷的碳外层只有6个电子,不稳定,所以邻位—络合物稳定性大,间位—络合物稳定性小。
对位一络合物的极限式中第四个也特别稳定,因此对位一络合物也很稳定。
苯酚的邻对位―络合物比间位―络合物稳定,则邻对位—络合物生成的快,即主要取代邻对位,所以羟基是邻对位定位基。
氯是钝化基,却是邻对位定位基。
为什么呢?与羟基类似,氯的电负性大,表现出吸电子诱导效应;氯的p轨道也与苯环产生供电子的共轭效应,但是氯的p轨道是第三电子层的,与碳的第二电子层的p轨道能量相差大,重叠程度小,共轭效应弱,因此氯的诱导效应大于共轭效应,氯表现出吸电子性,使苯环上电子密度降低,反应活性减小,所以氯是钝化基。
氯苯的邻位一络合物的共振结构可以用四个极限式表示,间位一络合物用这三个极限式表示,对位一络合物可以用四个极限式表示,大家可以看到,氯苯的三个一络合物与上面学习的苯酚的络合物结构类似,邻对位一络合物中都有一个稳定的极限式,而间位没有,所以邻对位一络合物稳定性大,生成速度快,则氯苯的取代产物主要是邻对位取代,因此氯是邻对位定位基。
这个是氯苯和苯的亲电取代能量示意图。
从图中可以看出,氯苯的邻间对位反应速度都比苯小,所以氯是钝化基;氯苯的邻对位反应速度比间位快,所以氯是邻对位定位基。
硝基是钝化的间位定位基。
氮的电负性比碳大,硝基表现出吸电
子诱导效应;如图所示,硝基中的二键和苯环的二键发生二-二共轭电子由苯环转向硝基,硝基表现出吸电子的共轭,吸电子的诱导和吸电子的共轭使硝基成为一个强吸电子基,使苯环的亲电取代活性降低, 所以硝基是强的钝化基。
这是硝基苯的三个一络合物,它们的结构可以用如下极限式表示。
邻位二-络合物的第三个极限式中正电荷直接与强吸电子基硝基相邻,不利于正电荷的分散,能量高,不稳定。
对位中也有一个类似的不稳定的极限式,所以间位―络合物稳定性最大,因此硝基苯主要发生间位取代,硝基是间位定位基。
空间效应也影响取代产物。
例如烷基苯硝化时,主要生成邻对位产物。
但是烷基不同,邻对位产物比例不同。
甲苯、异丙基苯、叔丁基苯硝化的邻对位产物含量如图所示,可以看出,从甲基到异丙基
再到叔丁基,基团体积逐渐增大,邻位产物减少,对位产物增多。
原因是基团体积大,对亲电试剂的空间位阻大,不利于邻位产物的生成。
新引入基团的体积也影响到取代产物。
例如溴苯的氯化和溴化,很明显,溴化时,邻位产物少,对位产物多,这是因为溴的体积大,邻位取代空间位阻大,不利于邻位产物的生成。
从以上例子可以看出,原基团或新引入基团体积大,都不利于邻位产物的生成,邻位产物少, 对位产物多。
反应温度也影响邻对位产物的比例。
例如甲苯的磺化反应,0度时,对位产物百分之五十三,而温度升到100 度时,对位产物增加到百分之七十九,邻位产物只有百分之十三。
可见,温度高,邻位产物少,对
位产物多。
原因是温度高时,基团振动剧烈,对邻位的空间位阻大,不利于邻位的生成。
通过以上学习,大家知道了影响定位效应的因素有电子效应、空间位阻和反应温度。
电子效应决定了取代基是邻对位定位基或间位定位基,是活化基还是钝化基。
供电子基是活化基,吸电子基是钝化基。
而空间位阻和温度影响邻对位产物的相对多少。
基团体积大、空间位阻大,反应温度高,对位产物多,邻位产物少。
当苯环上有两个取代基时,定位效应又如何呢?下面我们来学习二取代苯的定位效应。
当原有的两个基团是同类定位基时,由定位能力强的基团定位,同时还要考虑空间效应。
例如邻氯苯酚中,氯和羟基都是邻对位定位基,羟基的定位能力比氯强,因此由羟基来定位,主要取代羟基的邻位和对位。
对硝基苯甲醛中硝基和甲酰基都是间位定位基,硝基的定位能力强,由硝基定位,主要取代硝基的间位。
3- 甲基乙酰苯胺中甲基和乙酰氨基都是邻对位定位基,乙酰氨基定位能力强,由它来定位,主要取代乙酰氨基的邻位和对位,这个位置也是乙酰氨基的邻位,但是因为两边的基团的空间位阻作用,使该位置很难被取代,因此取代产物主要有两种。
如果原有的两个基团是两类定位基,则由邻对位定位基来定位。
例如甲基是邻对位定位基,硝基是间位定位基,则由甲基定位,对位已有基团,因此主要取代甲基的邻位。
3-硝基乙酰苯胺中硝基是间位定位基,乙酰氨基是邻对位定位基,由乙酰氨基定位,主要取代邻位和对位。
由于空间位阻大,该邻位不易被取代。
关于定位效应的解释今天就讲到这里,再见。
