利用化学方程式的简单计算(练习题)
利用化学方程式的简单计算(题型)

利用化学方程式的计算一、质量比的计算1.丁酸乙酯(C6H12O2)是无色、具有菠萝香味的液体, 常用作食品、饮料的调香剂。
下列正确的()A.丁酸乙酯是由20个原子构成的B.丁酸乙酯中碳元素的质量分数为27.6%C.丁酸乙酯中碳、氢、氧元素的质量比为18: 3: 8D.一个丁酸乙酯分子中, 碳、氢、氧原子的个数比为3:6:22.电解水得到氢气和氧气的质量比为()A.4: 8B.1: 8C.2: 1D.1: 163.磷在氧气中燃烧生成五氧化二磷的化学反应方程式中磷、氧气、五氧化二磷的质量比是()A.31: 16: 142B.4: 5: 2C.124: 160: 284D.31: 32: 71解析: 体会求物质中各元素质量比和化学方程式中求各物质质量比的区别。
二、“相同质量”的计算4.相同质量的下列各种物质, 经完全分解后, 制得氧气质量最多的是()A.HgOB.KMnO4C.H2OD.H2O25、相同质量的下列物质分别在氧气中完全燃烧, 消耗氧气最多的是()A.CB.H2C.FeD.P解析:设相同质量的各物质质量为1g, 方便计算。
三、过量问题6.4g碳在8g氧气中充分燃烧后, 生成二氧化碳的质量是()A.22gB.44gC.11gD.12g7、16克H2与196克 O2充分反应, 求生成水的质量。
第次以后, 生成氧化镁的质量不再增加。
为什么会出现这种情况?解析: 两个已知量, 莫急于代入计算, 需先判断哪个物质过量有剩余, 应用充分反应的量代入计算。
四、反应前后固体质量减少9、15g氯酸钾和二氧化锰的混合物, 充分加热后剩余10.2g固体物质, 则原混合物中二氧化锰的质量为()A.10.2gB.2.75gC.4.8gD.10g10、实验室用加热10g高锰酸钾的方法制取氧气, 实验完毕, 剩余固体为9.2g, 通过计算确定9.2g固体物质中含有那些物质?它们的质量各是多少?11.为测定某石灰石样品中碳酸钙的含量, 取样品10.0g于烧杯中加入稀盐酸50.0g, 恰好完全反应(杂质不反应), 反应后烧杯中物质的总质量为56.7g。
化学方程式的计算练习题40道

化学方程式的计算练习题40道化学方程式的计算练习题40道一、根据化学方程式进行计算1、在一个有6克氧气的密闭容器中,有5克铁粉和足量的硫,加热使之充分反应,问生成多少克固体混合物?2、现有10克氢气和氧气混合气体,点燃使之充分反应,得到5克水蒸气,问原来混合气体中各成分的质量?3、欲制得100千克碳酸钙含量为80%的石头灰,需要煅烧含碳酸钙含量为85%的石灰石多少千克?4、在一定条件下,11.2克金属钠与氧气完全反应,生成16.6克氧化物,求氧化物的化学式。
5、现有硫酸铜溶液20千克,其中含铜的质量分数为6%,现欲采用电解的方法除去其中的水分,问需要除去的水分质量为多少千克?(设水的质量分数为99%)二、物质的量在化学方程式计算中的应用6、在39千克过氧化氢溶液中,加入0.5千克二氧化锰,充分反应后可以得到多少摩尔氧气?61、在标准状况下,11.2升一氧化碳和13.2升氢气混合,充分反应后得到多少克产物?611、一定量的乙醇在氧气不足的情况下燃烧,得到二氧化碳、一氧化碳和水的总质量为50.4克,其中水的质量为25.2克,求二氧化碳的质量。
6111、在一个密闭容器中,有适量铜与一定量氧气反应,生成氧化铜的质量为16克,问消耗氧气的质量为多少?三、有关溶液的计算10、在20℃时,将33克食盐放入100克水中,充分溶解后得到溶液。
已知在该温度下,食盐在水中的溶解度为36克,求所得溶液的质量分数。
101、将58.5克食盐全部溶于200克水中,求该食盐溶液的质量分数。
1011、在20℃时,将40克硝酸钾溶于100克水中,已知在该温度下,硝酸钾在水中的溶解度为60克,求所得溶液的质量分数。
四、综合计算13、工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。
现称取纯碱样品12克,全部溶解在94.7克水中。
当加入稀盐酸73克时,恰好完全反应。
生成的气体全部逸出,所得溶液质量为170.2克。
计算反应后所得溶液中溶质的质量分数。
(完整版)利用化学方程式的简单计算练习(含答案),推荐文档

利用化学方程式的简单计算习题精选一、选择题1.电解水得到的氢气和氧气的质量比是()A.2:1 B.4:8 C.1:8 D.1:162.电解 54 克水,可得到氢气()A.6 克B.3 克C.1.5 克D.8 克3.化学反应:A+2B=C+D,5.6 克 A 跟 7.3 克 B 恰好完全反应,生成12.7 克 C。
现要制得 0.4D,则所需 A 的质量为()A.5.6 克B.11.2 克C.14.6 克D.无法计算4.铝在氧气中燃烧,生成三氧化二铝,在反应中,铝、氧气、三氧化二铝的质量比()A.27:32:102 B.27:16:43 C.4:3:2 D.9:8:175.用氢气还原+2 价金属氧化物 a 克,得到金属 b 克,则该金属的原子量是()A.16b/(a—b)B.4(a—b)/ b C.4b/(a—b)D.b/16(a—b)6.质量相同的下列金属分别与足量盐酸反应时,产生氢气最多的是()A.Mg B.Al C.Zn D.Fe7.铝在氧气中燃烧生成三氧化二铝,在这个反应中,铝、氧气、三氧化二铝的质量比是()A.27:32:102 B.27:24:43 C.4:3:2D.108:96:2048.4 克氧气可跟()克氢气完全反应。
A.1 B.0.5 C.2 D.49.3 克镁在足量的氧气中完全燃烧,可得氧化镁()克A.10 B.6 C.5 D.1210.在化学反应 A2+3B2=2AB3 中,6 克 B2 与足量的 A2 反应后,得到34 可 AB3.则化合物 AB3 中 A,B 两元素的质量比是( )A.17:4 B.14:3 C.14:7 D.14:1711.用铝和铁分别和足量的稀硫酸反应,都得到 2 克氢气,则消耗铝和铁的质量比为()A.1:1 B.27:28 C.9:28 D.3:212.2.3 克钠、2.4 克镁、2.7 克铝分别与足量的盐酸反应,按钠、镁、铝的顺序得到氢气的质量比为()A.1:2:3 B.1:1:1 C.2:3:1 D.3:2:113.相同质量的钠、镁、铝、铁分别跟足量的稀硫酸反应,生成氢气的质量比是()A.1:2:3:2 B.2:3:2:1 C.14.用氢气还原氧化铜的实验中,还原 8 克氧化铜,应该通入氢气的质量是()A.小于 0.2 克 B.等于 0.2 克 C.大于 0.2 克15.托盘天平调至平衡,在两盘烧杯中各盛 98 克 10%的硫酸,向两边烧杯中同时分别加入足量 Mg,Zn 欲使天平仍保持平衡,加入 Mg 和 Zn 的质量分别是()A.3 克 Mg,3 克 Zn B.1 克 Mg,1 克锌C.7 克 Mg,7 克 Zn D.5 克 Mg,5 克Zn16.8 克氢气在氧气中充分燃烧,需要消耗克氧气()A.56 克B.64 克C.72 克D.60 克17.制取 71 克五氧化二磷,需要磷克,需要烧氧气克()A.30 克 30 克B.30 克 40 克C.31 克 40 克D.40 克 31 克二、填空题1.12.25 克 KCl3跟 3.25 克 MnO2共热,反应完全后剩余固体的质量为10.7 克。
(完整版)利用化学方程式的简单计算练习题及答案

第五单元课题3 利用化学方程式的简单计算测试题1.在反应X+2Y====R+2M中,当1.6 g X与Y完全反应后,生成4.4 g R,且反应生成的R和M的质量之比为11∶9,则在此反应中Y和M的质量之比为()A.23∶9 B.16∶9 C.32∶9 D.46∶92.氯酸钾和二氧化锰的混合物共A克,加热完全反应后得到B克氧气和C克氯化钾,则混合物中二氧化锰的质量为()A.(A+B-C)克B.(A-B-C)克C.(A+B+C)克D.(A+C)克3.已知A物质与B物质反应生成C物质,现有12克A与32克B恰好完全反应,则生成C物质的质量是()A.44克B.32克C.22克D.12克4.已知A物质发生分解反应生成B物质和C物质,当一定量的A反应片刻后,生成56克B 和44克C;则实际发生分解的A物质的质量为()A.12克B.44克C.56克D.100克5.只含铜和氧两种元素的固体样品9.0 g,测得铜的质量为8.0 g。
已知铜的氧化物有CuO和Cu2O,下列说法正确的是()A.固体样品的组成只有两种情况B.固体样品一定是CuO与Cu2O的混合物C.固体样品可能是Cu2OD.若固体样品由两种物质组成,则其中一种质量分数为4/96.在2A+B====2C的反应中,1.2 g A完全反应生成2 g C,又知B的式量是32,则C的式量为___________。
7.已知在反应3A+2B====2C+D中,反应物A、B的质量比为3∶4。
当反应生成C和D的质量共140 g时,B消耗的质量为___________g。
8.蜡烛燃烧后的产物有二氧化碳和水,由质量守恒定律可知,石蜡的组成中一定含有_______、_________元素。
(填写元素名称)9.在化学反应3X+4Y====2Z中,已知X和Z的相对分子质量分别是32和102,则Y的相对分子质量为____________。
10.火力发电厂用石灰石泥浆吸收废气中的二氧化硫以防止污染环境,其反应方程式为:2CaCO3(粉末) + 2SO2+ O2====2CaSO4+ 2CO2。
【初中化学】利用化学方程式的简单计算精选习题15道(含答案解析)

1.化学反应在防治环境污染中扮演了重要角色。
某工厂废气中的 SO2,可用以下方式处理:方式一:2SO2 +O2+2CaO=2CaSO4方式二:2SO2 +O2 +4NaOH= aNa 2SO4 +bH2O回答下列问题:(1) CaSO4中有两种元素的质量分数呈整数倍关系,这两种元素是硫元素和_______ (填元素符号)。
(2) 若用方式二处理 9.6tSO2 ,理论上可生成 Na2SO4的质量是____? (写出计算过程,结果精确到 0.1t)2.某兴趣小组用氯酸钾与二氧化锰的混合物制取氧气,试管中固体的质量随时间变化的数据见下表。
(1) 氯酸钾中钾、氯、氧元素的质量比是_______。
(2) 完全反应后,生成氧气的质量为_______g。
(3) 求混合物中氯酸钾的质量是_______。
(根据化学方程式进行计算) 3.实验室用锌与稀硫酸反应制取氢气。
若有 9.8g 硫酸参加反应,生成氢气的质量是多少? (反应化学方程式:Zn+H2 SO4=ZnSO4+H2个)4.氢气是最理想的燃料,具有放热量高、无污染的优点。
计算:分析表中数据,完成下列问题:(1) 10kg 氢气完全燃烧可生成水的质量是多少?(2) 消耗氧气的质量至少是多少?5.碳酸氢钠固体受热易分解生成一种盐和两种氧化物,反应的化学方程式为______;将 10g 碳酸钠和碳酸氢钠的混合物充分加热至固体的质量不再改变,冷却,称量剩余固体的质量为 6.9g,则原混合物中碳酸钠和碳酸氢钠的质量比为______。
6.实验室常用氯酸钾和二氧化锰的混合物制取氧气。
现有氯酸钾和二氧化锰的混合物 50g,完全反应后称量剩余物质的质量为 40.4g。
请计算:(1) 制得氧气的质量为__________。
(2) 混合物中氯酸钾的质量分数。
7.加热氯酸钾和二氧化锰固体混合物来制取氧气时,反应时间和剩余固体质量的关系如图所示。
计算:的质量是___________g。
利用化学方程式的简单计算练习(含答案)汇总

利用化学方程式的简单计算习题精选一、选择题1.电解水得到的氢气和氧气的质量比是()A.2:1 B.4:8 C.1:8 D.1:162.电解54克水,可得到氢气()A.6克B.3克C.1.5克D.8克3.化学反应:A+2B=C+D,5.6克A跟7.3克B恰好完全反应,生成12.7克C。
现要制得0.4D,则所需A的质量为()A.5.6克B.11.2克C.14.6克D.无法计算4.铝在氧气中燃烧,生成三氧化二铝,在反应中,铝、氧气、三氧化二铝的质量比()A.27:32:102 B.27:16:43 C.4:3:2 D.9:8:175.用氢气还原+2价金属氧化物a克,得到金属b克,则该金属的原子量是()A.16b/(a—b)B.4(a—b)/ b C.4b/(a—b)D.b/16(a—b)6.质量相同的下列金属分别与足量盐酸反应时,产生氢气最多的是()A.Mg B.Al C.Zn D.Fe7.铝在氧气中燃烧生成三氧化二铝,在这个反应中,铝、氧气、三氧化二铝的质量比是()A.27:32:102 B.27:24:43 C.4:3:2 D.108:96:2048.4克氧气可跟()克氢气完全反应。
A.1 B.0.5 C.2 D.49.3克镁在足量的氧气中完全燃烧,可得氧化镁()克A.10 B.6 C.5 D.1210.在化学反应A2+3B2=2AB3中,6克B2与足量的A2反应后,得到34可AB3.则化合物AB3中A,B两元素的质量比是( )A.17:4 B.14:3 C.14:7 D.14:1711.用铝和铁分别和足量的稀硫酸反应,都得到2克氢气,则消耗铝和铁的质量比为()A.1:1 B.27:28 C.9:28 D.3:212.2.3克钠、2.4克镁、2.7克铝分别与足量的盐酸反应,按钠、镁、铝的顺序得到氢气的质量比为()A.1:2:3 B.1:1:1 C.2:3:1 D.3:2:113.相同质量的钠、镁、铝、铁分别跟足量的稀硫酸反应,生成氢气的质量比是()A.1:2:3:2 B.2:3:2:1 C.14.用氢气还原氧化铜的实验中,还原8克氧化铜,应该通入氢气的质量是()A.小于0.2克B.等于0.2克C.大于0.2克15.托盘天平调至平衡,在两盘烧杯中各盛98克10%的硫酸,向两边烧杯中同时分别加入足量Mg,Zn欲使天平仍保持平衡,加入Mg和Zn的质量分别是()A.3克Mg,3克Zn B.1克Mg,1克锌C.7克Mg,7克Zn D.5克Mg,5克Zn16.8克氢气在氧气中充分燃烧,需要消耗_______克氧气()A.56克B.64克C.72克D.60克17.制取71克五氧化二磷,需要磷_______克,需要烧氧气_______克()A.30克30克B.30克40克C.31克40克D.40克31克二、填空题1.12.25克KCl3跟3.25克MnO2共热,反应完全后剩余固体的质量为10.7克。
利用化学方程式的简单计算练习 (1)

x
316
1.6克
x
=
32 1.6克 ∴ 答案为A
x = 15.8克
4.下列关于氢气在氧气中燃烧的叙述中正确的是 A.16g 氢气和2g 氧气反应能生成18g 水 B.9g 氢气和9g 氧气反应能生成18g 水 C.1g 氢气和8g 氧气反应能生成9g 水 D.8g 氢气和1g 氧气反应能生成9g 水 思路: 2H2 + O2 ==== 2H2O 4 32 36
例:6克镁粉与8克氧气充分反应后能生成氧化镁多少克? 解:设反应后生成氧化镁的质量为X
点燃
解题指导
2Mg + O2 ==== 2MgO 80 32 48 6克 8克 X
∵48 × 8克 > 32×6克 ∴反应后氧气有剩余 48 80 ∴ = 6克 X X=10克 答:6克镁粉与8克氧气充分反应能生成氧化镁10克。
(5) 简明地写出答案
….………… 答
3.根据化学方程式计算的注意事项: (1)所有代入化学方程计算的量必须是纯净物的质量,如果 是不纯物,则需要转换。 纯物质的质量=不纯物质质量×纯度=不纯物质质量×(1-杂 质的质量分数) (2)气体、液体的体积,要换算成气体、液体的质量。 气体质量(g)=气体体积(L)×密度(g/L) 液体质量(g)=液体体积(mL)×密度(g/mL) (3)若题目中只给出一种物质的质量,则另一种物质的用量 往往用“足量”、“适量”、“过量”或“完全反应”、“恰 好完全反应”等来描述。如果同时知道两种反应物的质量,需 要考虑过量问题。 (4)注意已知质量的单位;设未知数的时候要设×××的质 量为X,而不能设××× X克;整个化学计算过程要带单位, 最后求出的X的值后写上单位。(无说明则保留到小数点后一位)
7、有X、Y两种元素,12gX2与XY3反应生成24gC,若反应 的化学方程式为X2 + XY3 === 3C,则X、Y两元素的相对 原子质量之比为 ( )
九年级上册化学化学方程式计算题

- 解得z = 11g。
- 答:生成二氧化碳的质量是11g。
二、利用化学方程式简单计算(已知一种生成物的质量求反应物质量)
4. 实验室制取二氧化碳,若要得到8.8g二氧化碳,需要碳酸钙的质量是多少?(化学方程式:CaCO_3+2HCl===CaCl_2+H_2O + CO_2↑)
- 解得x = 36g。
- 答:能生成36克水。
2. 加热分解6.3g高锰酸钾,可以得到多少克氧气?
- 解:
- 写出化学方程式:2KMnO_4{}{===}K_2MnO_4+MnO_2+O_2↑。
- 设生成氧气的质量为y。
- 高锰酸钾(KMnO_4)的相对分子质量为158,氧气(O_2)的相对分子质量为32。
- 它们的质量比为100:56。
- 已知m(CaO)=11.2t,列比例式(100)/(m)=(56)/(11.2t)。
- 解得q = 20g。
- 因为石灰石中含杂质20%,所以石灰石的质量为m=(20g)/(1 - 20%)=25g。
- 答:需要这种石灰石的质量是25g。
8. 某赤铁矿(主要成分是Fe_2O_3)样品中Fe_2O_3的质量分数为80%,用该赤铁矿炼铁,若要得到112t纯铁,需要这种赤铁矿的质量是多少?(化学方程式:Fe_2O_3+3CO{高温}{===}2Fe+3CO_2)
- 解:
- 设需要纯净H_2SO_4的质量为s。
-H_2SO_4的相对分子质量为98,氢气(H_2)的相对分子质量为2。
- 在化学方程式Zn + H_2SO_4===ZnSO_4+H_2↑中,H_2SO_4与H_2的质量比为98:2。
初中化学利用化学方程式的简单计算练习题及答案

初中化学利用化学方程式的简单计算练习题及答案一、选择题1.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前、反应中及反应结束前某时刻的各物质的质量(如表)。
表中x、y、m、n分别表示相应物质的质量。
下列数据正确的是()甲乙丙丁反应前质量/g7014610反应中质量/g x11m n反应结束前质量/g42y4010A.x=56 B.y=6 C.m=17 D.n=8解析:A【解析】【详解】A、y=70+14+6+10-42-40-10=8,根据题意有:(70-42):(14-8)=(70-x):(14-11),x=56,该选项说法正确;B、y=8,该选项说法不正确;C、根据题意有:(14-8):(40-6)=(14-11):(m-6),m=23,该选项说法不正确;D、丁反应前后质量不变,则=10,该选项说法不正确。
故选:A。
2.下图是某反应的微观示意图,下列说法不正确的是A.B为单质B.生成物中C和D的分子个数比为1:1C.参加反应的A和B的质量比为17:16D.A中氢元素与硫元素的质量比为1:16解析:C【解析】试题分析:从分子构成看B中只有一种元素所以属于单质,根据配平后的结果看生成物中C和D的分子个数比为1:1;参加反应的A和B的质量比为=34×2:32×3=17:24;;A的化学式为H2S其中氢元素与硫元素的质量比为1:16。
故选C.考点:分子的构成物质之间的质量关系3.如图是某反应的微观示意图,下列说法不正确的是()A.反应物中有单质B.该反应为置换反应C.生成物的分子个数比为1:1D.参加反应的和的质量比为17:24解析:B【解析】试题分析:由图示可知反应前后存在相同的分子,故该图示可转化为如图的反应图示:依据反应前后物质的分子结构可知反应物是氧气和硫化氢生成物是水和二氧化硫,则反应方程式为3O2+2H2S2H2O+2SO2;A、单质是由一种元素组成的纯净物,化合物是由多种元素组成的纯净物,故反应物中氧气属于单质硫化氢属于化合物;B、置换反应要求反应物生成物均是一种单质与一种化合物,而该反应的生成物是两种化合物,所以不是置换反应;C、由图示或方程式都可以看出生成物的分子个数比是1:1;D、由方程式可知参加反应的和的质量比为2×(2+32):6×16=17:24考点:微粒观点及模型图的应用.4.物质X的化学式为H2C2O4,可发生如下反应:aH2C2O4 bH2O↑+cCO2↑+dY↑取45g X,在t℃完全分解,产物通过足量浓硫酸,浓硫酸增重9g,另取45gX,在t℃完全分解,产物通过足量碱石灰(CaO和NaOH的固体混合物),碱石灰增重31g,则下列说法错误的是(已知气体Y不与浓硫酸或碱石灰发生反应)()A.CO2的质量为22g B.气体Y的质量为14gC.化学方程式中b∶c=1∶1D.气体Y可能为甲烷解析:D【解析】A、浓硫酸能吸收反应生成的水,碱石灰既能吸水又能吸收二氧化碳故完全反应分解X生成的二氧化碳的质量为31g﹣9g=22g,正确;B、根据质量守恒定律,反应物X的质量等于生成的水、二氧化碳和Y的质量总和,故生成气体Y的质量为45g﹣31g=14g,正确;C、根据反应的方程式可知,反应中生成水和二氧化碳的质量比为18b:44c=9g:22g,可得b:c=1:1;正确;D、X中H、C原子个数比为1:1,反应生成的水和二氧化碳的分子个数比为1:1,其中氢、碳原子个数比为2:1,则生成y分子中C原子的个数应大于H原子的个数,甲烷中碳原子的个数小于氢原子的个数,错误。
挑战16 计算题(利用化学方程式的简单计算共30题)(解析版)

挑战16 计算题(利用化学方程式的简单计算共30题)1.(2022•呼和浩特)大气污染物二氧化硫主要来源于煤燃烧的烟气。
某煤厂为了减少二氧化硫的排放,向原煤中加入生石灰,燃烧时发生反应:CaO+SO2+O2CaSO4。
请回答下列问题:(1)配平化学方程式: 2 CaO+ 2 SO2+ 1 O2 2 CaSO4。
(2)若该煤厂一次共加入280吨生石灰(含CaO80%),则理论上最多可吸收多少吨?(写出计算过程)【答案】(1)2;2;1;2;(2)256t。
【解答】解:(1)配平化学方程式时,首先设生成物CaSO4的化学计量数是1,则CaO、SO2的化学计量数也是1,则O2的化学计量数为=,然后去分母,各化学计量数同时乘以2,则得到该反应方程式为:2CaO+2SO2+O22CaSO4,即化学计量数分别为2、2、1、2。
(2)氧化钙的质量为:280t×80%=224t,设理论上最多可吸收二氧化硫的质量为x,2CaO+2SO2+O22CaSO4112 128224t x=x=256t答:若该煤厂一次共加入280吨生石灰(含CaO80%),则理论上最多可吸收二氧化硫的质量为256t。
故答案为:(1)2;2;1;2;(2)256t。
2.(2022•西藏)“十四五”期间,我国将独立完成“天宫二号”空间实验室建造。
建造舱段使用的新型铝基碳化硅复合材料是由颗粒状的铝和碳化硅(SiC)复合而成的。
一位科技爱好者自研了一种铝基碳化硅复合材料,为了分析其中铝的质量分数,该科技爱好者取了10g 样品溶于足量稀硫酸,所得实验数据如图所示。
已知:碳化硅既不溶于水和酸,也不与二者反应。
请回答下列问题:(1)当样品中的铝完全反应时,生成的气体质量为 0.6 g。
(2)样品中铝的质量分数为多少?(写出完整解题过程)。
【解答】解:(1)当样品中的铝完全反应时,生成的气体质量为0.6g。
故答案为:0.6。
(2)设参加反应的铝的质量为x。
5.3.2利用化学方程式的简单计算(练习)

第五单元:化学方程式 课题3:利用化学方程式 的简单计算(练习)
首先要勤学勤动脑 然后就熟能生巧
利用化学方程式的简单计算
根据化学方程式的解题步骤: 1.设未知量。
2.写出反应的化学方程式并配平。
3.相应列出已知量和未知量。 4.列出比例式,求解。 5.作答。
利用化学方程式的简单计算
催化剂
利用化学方程式的简单计算
2.某工厂需要100 kg氧气作原料。若用电解水的方法制取这些 氧气,消耗水的质量是多少?同时可以得到的氢气的质量是多 少? 解:设消耗水的质量是x,同时可以得到氢气的质量为y。 2H2O === O2 ↑+ 2H2↑ 4 36 32 x y 100kg 36 x = 100k 32 g 100kg 32 = y 4 x = 112.5 kg y = 12.5 kg
64 92 = x 9.6kg
答:需要N2O4的质量为13.8 kg。
通电
答:消耗水的质量是112.5kg,可以得到氢气的质量为12.5kg。
利用化学方程式的简单计算
3.锌与盐酸(HCl)反应生成氢气和氯化锌。实验室用6.5 g锌与足 量盐酸反应,可制得氢气和氯化锌的质量各是多少?
解:设可制得氢气的质量为x,氯化锌的质量为y。 Zn + 2HCl === ZnCl2 + H2↑ 136 65 2 y x 6.5 g 65 2 = x 6.5g
2KMnO4 === K2MnO4 + MnO2 + 2O2 ↑ 316 (158) 64 (32) 2KClO3 ===== 2KCl + 3O2 ↑ △ (81.6) 245 96 (32) 2H2O === 2H2↑ + O2 ↑ 36 32 显然,相同质量的D. H2O分解后制得氧气最多。
有关化学方程式的简单计算经典23道

有关化学方程式的简单计算经典23道1.冶炼100 kg含杂质2%的生铁,需要含氧化铁80%的赤铁矿石的质量为多少?2.一定量含有氯化钠杂质的氢氧化钠样品,加入25 g水充分溶解后,缓慢加入10%的稀盐酸,当溶液的pH=7时,刚好用去稀盐酸的量为36.5 g。
计算样品中氢氧化钠的质量。
3.将527 g稀盐酸加入盛有50 g碳酸钙的烧杯中,恰好完全反应。
计算反应后所得不饱和溶液中溶质的质量分数。
4.[2019河南25(7)题3分]某潜水艇上有100人,如果每人每分钟消耗氧气为0.001 kg,假如所需要的氧气全部由Na2O2与CO2反应来提供,则该潜水艇一天所需要Na2O2的质量是多少?[提示:2Na2O2+2CO2=== 2Na2CO3+O2]5.[2016河南23(5)题3分]工业上可利用“铝热反应”焊接钢轨、冶炼难熔金属等,其原理是在高温下用铝将某些金属从其氧化物中置换出来。
若用铝与四氧化三铁反应来制取25.2 kg铁,理论上需要消耗铝的质量是多少?6.[2015河南23(5)题3分]铁和钛合金性能优良,广泛用于航空、造船和化学工业中。
工业上常用钠来制取钛,在高温时,钠与四氯化钛(TiCl4)反应生成氯化钠和钛。
若要用该方法制取2.4 kg钛,理论上需要钠的质量是多少?7.[2018河南25(4)题3分]为测定某石灰石样品中碳酸钙的质量分数,称取10 g 石灰石(杂质不参加反应)放入烧杯中,加入100 g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为106.7 g(气体的溶解忽略不计)。
请计算该样品中碳酸钙的质量分数。
8.[2014河南23(4)题3分]某工厂变废为宝,探究用废硫酸等来制取所需产品。
现有废硫酸4.9 t(H2SO4的质量分数为20%),与足量废铁屑反应来制取硫酸亚铁,同时将生成的全部氢气通入足量氧化铜中并加热(H2+CuO =Δ= Cu+H2O),请计算理论上最多可生产铜的质量。
利用化学方程式的简单计算典型例题

利用化学方程式的简单计算典型例题work Information Technology Company.2020YEAR利用化学方程式的简单计算典型例题一、反应物、生成物均为纯净物的计算例1、工业用电解氧化铝的方法制取单质铝,计算电解10t 氧化铝最多生产多少吨铝二、反应生、生成物为不纯物的计算例2、某同学发现养鱼师傅向鱼塘中撒一种微黄色的固体,咨询得知,这种固体的主要成分是过氧化钙(CaO2)是为了解决鱼塘中氧气不足的问题。
他回家后查阅资料,查到过氧化钠与水反应的原理2Na2O2+2H2O=4NaOH+O2,且 CaO2与 Na2O2的化学性质非常相似。
(1)写出该反应的化学方程式:_____ ______。
(2)该同学为测定这种固体中CaO2的质量分数,称取20g样品加入到足量的水中,结果生成3.2g氧气(假设样品中其他成分与水不反应)。
请你帮助计算该样品中CaO2的质量分数。
三、涉及巧解的计算例3、有一种含CaCO3与CaO的混合物,测得其中钙元素的质量分数为50% ,取该混合物16g经高温煅烧后,将剩余固体投入足量水中,固体全部溶解生成Ca(OH)2,则生成Ca(OH)2的质量为()(技巧:元素质量守恒)A 3.7gB 7.4gC 14.8gD 22.2g例4、现有200g澄清石灰水,敞口放在空气中一段时间后,发现液面上产生白膜,称量石灰水质量变为202.2g,求:生成白膜质量为多少克(技巧:差量法)将30g氯酸钾和二氧化锰的混合物加热至没有气体放出,称量剩余固体物质质量为20.4g,求:原混合物种KClO3质量为多少克(不知道任意一种参加反应物质的质量,不能直接用化学方程式的计算,运用质量守恒定律求。
突破口:生成氧气多少克)四、图表型计算例5:(南通市中考)密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:下列说法正确的是( )A.物质C一定是化合物,物质D可能是单质B.反应后密闭容器中A的质量为19.7gC.反应过程中,物质B与物质D变化的质量比为87∶36D.若物质A与物质C的相对分子质量比为197∶158,则反应中A与C的系数之比为l∶2例6、某化工厂生产的纯碱产品中常含有少量氯化钠,工厂的化验员对每批产品进行检测,标出各种成份后才能投放市场。
利用化学方程式的简单计算

利用化学方程式的简单计算例一:加热分解6.3g高锰酸钾,可以制得氧气的质量是多少?例二:火箭升空至少要携带100kg液氢,充分燃烧才能获得足够的能量。
假如你是长征系列火箭推进器的设计师,你会在火箭助燃仓中填充多少千克的液氧?练习:1、工业上,煅烧石灰石(主要成分是CaCO3)可制得生石灰(CaO)和二氧化碳,如果要制取5.6t氧化钙,需要碳酸钙的质量是多少?生成多少二氧化碳?2、100g氢气可与多少氯气恰好完全反应生成氯化氢呢?例三:锌与盐酸(HCl)反应生成氢气和氯化锌。
实验室用6.5g锌与足量盐酸反应可制得氢气和氯化锌的质量各是多少?例四:45g的镁带在标准状况下与11.2L的氧气(密度为1.43g/L)发生燃烧反应,可以生成多少克氧化镁?例五:某化学兴趣小组的同学为检测石灰石中碳酸钙的含量,他们在实验室用6g石灰石样品(主要成分是CaCO3,杂质不参加反应)与19g稀盐酸(HCl)恰好完全反应(其生成物为CaCl2、水喝二氧化碳),测得残留物的质量为22.8g,求:1、生成二氧化碳的质量多少克?2、样品中碳酸钙的质量分数。
例六:高铁酸钠(Na2FeO4)是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为3 NaClO+2Fe(NO3)3+10NaOH==2 Na2FeO4↓+3NaCl+5H2O(1)求高铁酸钠(Na2FeO4)中铁元素和氧元素的质量比。
(2)现要制得830g含杂质20%的高铁酸钠,至少需要次氯酸钠的质量是多少?练习二:1、将18g高锰酸钾加热,当产生1.6g氧气时,固体剩余物是什么?2、某干燥剂含氧化钙的质量为80%(杂质不吸水),理论上14g干燥剂能吸收水的质量是多少?【有关反应的化学方程式为CaO+H2O==Ca(OH)2】3、加热8gKMnO4一段时间后,称得剩余固体质量为7.4g,则剩余物的组成是什么?。
人教版九年级化学上册第5单元课题3《利用化学方程式的简单计算》课时练习题(含答案)

人教版九年级化学上册第5单元课题3《利用化学方程式的简单计算》课时练习题(含答案)一、单选题1.2020年5月5日,配置有氢氧发动机的长征五号B 火箭,搭载我国新一代载人试验飞船顺利升空,飞船成功返回。
从变化观念和平衡思想认识反应: 2222H +O 2H O 点燃。
下列说法正确的是A .氢气和氧气混合生成水B .反应前后元素种类不变、化合价改变C .2g 氢气和1g 氧气反应生成3g 水D .氢气和氧气反应吸收热量2.在化学反应A+2B=C+2D 中,已知16gA 与64gB 恰好完全反应,生成C 和D 的质量比为11:9,又知B 的相对分子质量为32,则D 的相对分子质量为( )A .9B .12C .18D .363.下列化学反应可用如图表示的是( )A .232H CO CO △↑ 2H O +B .232242H SO O =2H SO +C .22HClO 2HCl O +光照↑D .32CaCO CaO CO +高温↑4.将氯化氢转化为氯气的技术是当今化学研究的热点之一,下图是该反应的微观示意图(其中:表示氢原子,表示氧原子,表示氯原子)下列说法正确的是A .该反应涉及两种氧化物B .生成物均由两种元素组成C.参加反应的两种物质的质量比为73:16 D.反应前后分子总数不变5.下列说法正确的是A.根据化学方程式可知道各反应物和生成物的质量比B.物质在空气中加热发生反应后,生成物的总质量必定等于反应物的总质量C.镁条在空气中燃烧后质量减小,说明该反应不遵守质量守恒定律D.24g镁和32g氧气反应,可生成56g氧化镁二、填空题6.已知A、B两种物质反应生成C:A+B→C.用7gA和2gB或4gA和5gB充分反应都可以得到6gC.现取A、B固体混合物共9g,充分反应后得到7.5gC.此混合物中A和B的质量分别是________ .7.下图是某一变化过程的微观示意图,请回答下列问题:(1)该反应的化学方程式是_______;该反应的基本类型为_______。
化学方程式的简单计算(例题)
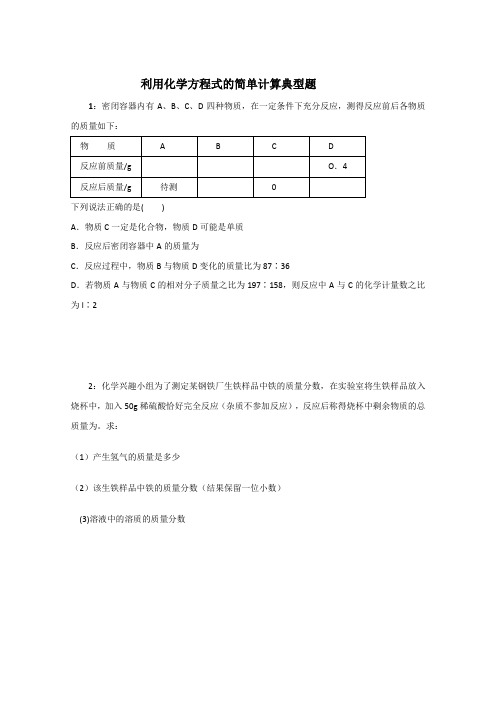
利用化学方程式的简单计算典型题1:密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:下列说法正确的是( )A.物质C一定是化合物,物质D可能是单质B.反应后密闭容器中A的质量为C.反应过程中,物质B与物质D变化的质量比为87∶36D.若物质A与物质C的相对分子质量之比为197∶158,则反应中A与C的化学计量数之比为l∶22:化学兴趣小组为了测定某钢铁厂生铁样品中铁的质量分数,在实验室将生铁样品放入烧杯中,加入50g稀硫酸恰好完全反应(杂质不参加反应),反应后称得烧杯中剩余物质的总质量为。
求:(1)产生氢气的质量是多少(2)该生铁样品中铁的质量分数(结果保留一位小数)(3)溶液中的溶质的质量分数3:单晶硅是重要的半导体材料,是某市的拳头产品,该市某厂生产的单晶硅曾用于制造我国的第一颗人造卫生。
在硅及相关产品的生产中排放的废水含有HCl。
该厂化验员对本厂排放的废水中HCl的质量分数进行测定:将20mL废水(假定其密度为1g/cm3)样品置于锥形瓶中,用质量分数为1%的氢氧化钠溶液进行中和,共用去氢氧化钠溶液8g(假设废水中不含其他能与氢氧化钠溶液反应的物质)。
(1)计算该废水中含HCl的质量分数。
(2)该厂每天产生废水100t,若直接排放将对环境造成污染,必须进行无害化处理后才能进行排放,现准备用氢氧化钙粉末或质量分数为10%的氢氧化钠溶液进行中和。
有关数据如下表所示:你将选择(写化学式)来中和废水中的HCl,请说明理由。
4:为了测定某铜锌合金的组成,某校化学课外活动小组利用该合金粉末与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下:(1) 试计算该铜锌合金中合金锌的质量。
(2) 从上表数据分析,当所取合金与所用稀硫酸的比为时,表明合金中的锌与稀硫酸恰好完全反应。
(3)所用合金与稀硫酸恰好完全反应时所得溶液中溶质的质量分数。
解析和答案:1、解析 由题中所给的数据可知:C 反应后质量没有了,说明是反应物,而B 、D 反应后质量都增加了,说明是生成物,C 反应掉 ,B 、D 共生成的质量只有 ,说明A 也生成物,且生成的质量为 ,则该反应为分解反应,C 一定是化合物,A 、B 、D 可能是化合物,也可能是单质;然后由质量比、相对分子质量比求化学计量数比。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
利用化学方程式计算
1.根据化学方程式计算的步骤
(1)设:根据题意设未知数;
(2)写:书写正确的化学方程式;
(3)找:找出已知量和未知量的质量关系;
(4)列:列出比例式并求解;
(5)答:检查结果,简明作答。
2.根据化学方程式计算应该注意的事项
(1)正确书写化学方程式,准确列出有关反应物或生成物的质量比;
(2)列式时,各物质的质量单位必须统一,对应关系要正确;
(3)反应物、生成物都必须是纯净物,如果是混合物,应该不纯物的质量按题意转化为纯净物的质量;
(4)解题的过程要完整,规范
(5)设未知数是要指明物理量,不要带单位。
例题:某实验室中需要1.6g氧气进行实验。
若用电解水的方法制取这些氧气,需要消耗水多少克?同时可生成氢气多少克?
常见题型
1.利用质量守恒定律的相关信息,如何求反应物的质量及相互质量比?
例1 已知在反应3A+2B=2C+D中,反应物A、B的质量比为3:4。
当反应生成C 和D的质量共140g时,B消耗的质量为_________g。
例2 在化学反应3X+4Y=2Z中,已知X和Z的相对分子质量分别是32和102,则Y的相对分子质量为_____。
2.已知反应物(或生成物)的质量(或密度、体积),如何求另一反应物(或生成物)的质量(或体积)?
例3 中国登山协会为纪念我们首次攀登珠穆朗玛峰成功50周年,再次组织攀登珠峰活动。
阿旺扎西等一行登山运动员于2003年5月21日13:40成功登顶。
假如每位运动员冲顶时消耗自带的液氧4.8g。
求:
(1)这些氧气在标准状况下的体积是多少升?(标准状况下氧气密度为1.43g/L)
(2)若在实验室用高锰酸钾为原料制取相同质量的氧气,需要多少千克的高锰酸钾?
(3)用这种方法给登山运动员供氧,是否可行?简述理由。
3.已知混合物中的一反应物(或生成物)的质量,如何求混合物中另一反应物(或生成物)的质量?
例4 煅烧含碳酸钙80%的石灰石100t,生成二氧化碳多少吨?若石灰石中的杂质全部进入生石灰中,可以得到这样的生石灰多少吨?
4.利用化学反应测定的实验数据,如何进行物质的计算和推断?
例5 小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用了的办法如下:取用8g这种石灰石样品,把40g稀盐酸分4次加入,测量过程所得数据见下表(已知石灰石样品中含的杂质不溶于水,不与盐酸反应)。
请计算:
(1)8g石灰石样品中含有杂质多少克?
(2)样品中碳酸钙的质量分数是多少?
(3
(4
CaCO
3高温
==CaO+CO2↑)
利用化学方程式的简单计算练习题
基础训练
1.为使书写的化学方程式遵守______________定律,要在化学方程式两边的化学式的前面配上适当的______________,使化学方程式等号两边各种原子的____________和_________都相同,这个过程叫配平。
正确的化学方程式应当是配平的,反应物和生成物之间用_________连接,还要标明化学反应发生的______________。
如果______________中无气体,__________中有气体,在______________的气体______________边要注___________号;溶液中的反应,如果生成物中有______________,则在固体物质的化学式的右边要注______________号。
2.在2A+B====2C的反应中,1.2 g A完全反应生成2 g C,又知B的式量是32,则C的式量为___________。
强化训练
1.在反应X+2Y====R+2M中,当1.6 g X与Y完全反应后,生成4.4 g R,且反应生成的R 和M的质量之比为11∶9,则在此反应中Y和M的质量之比为( )
A.23∶9
B.16∶9
C.32∶9
D.46∶9
2.氯酸钾和二氧化锰的混合物共A克,加热完全反应后得到B克氧气和C克氯化钾,则混合物中二氧化锰的质量为( )
A.(A+B-C)克
B.(A-B-C)克
C.(A+B+C)克
D.(A+C)克
3.已知在反应3A+2B====2C+D中,反应物A、B的质量比为3∶4。
当反应生成C和D的质量共140 g时,B消耗的质量为___________g。
4.蜡烛燃烧后的产物有二氧化碳和水,由质量守恒定律可知,石蜡的组成中一定含有_______、_________元素。
(填写元素名称)
5.在化学反应3X+4Y====2Z中,已知X和Z的相对分子质量分别是32和102,则Y的相对分子质量为____________。
巩固训练
1.已知A物质与B物质反应生成C物质,现有12克A与32克B恰好完全反应,则生成C 物质的质量是( )
A.44克
B.32克
C.22克
D.12克
2.已知A物质发生分解反应生成B物质和C物质,当一定量的A反应片刻后,生成56克B 和44克C;则实际发生分解的A物质的质量为( )
A.12克
B.44克
C.56克
D.100克
3.(经典回放)只含铜和氧两种元素的固体样品9.0 g,测得铜的质量为8.0 g。
已知铜的氧化物有CuO和Cu2O,下列说法正确的是( )
A.固体样品的组成只有两种情况
B.固体样品一定是CuO与Cu2O的混合物
C.固体样品可能是Cu2O
D.若固体样品由两种物质组成,则其中一种质量分数为4/9
4.中国登山协会为纪念我们首次攀登珠穆朗玛峰成功50周年,再次组织攀登珠穆朗玛峰活动。
阿旺扎西等一行登山运动员成功登顶。
假如每位运动员冲顶时消耗自带的液氧4.8 g。
求:
(1)这些氧气在标准状况下的体积是多少升?(标准状况下氧气密度为1.43 g·L-1)(2)若在实验室用高锰酸钾为原料制取相同质量的氧气,需要多少千克的高锰酸钾?
5.小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用的办法如下:取用8 g这种石灰石样品,把40 g稀盐酸分4次加入,测量过程所得数据见下表(已知石灰石样品中含的杂质不溶于水,不与盐酸反应)。
请计算:(1)8 g石灰石样品中含有杂质多少克?
(2)样品中碳酸钙的质量分数是多少?
(4)要得到280 kg CaO,需要质量分数为80%的石灰石多少千克?(化学方程式:CaCO3高温CaO+CO2↑)
6.(2005福建福州中考,30)某综合实践活动小组同学,对我市某化工厂排放的污水进行检测,发现主要的污染物为氢氧化钠。
为测定污水中氢氧化钠的含量,取100 g污水于烧杯中,加入36.5 g质量分数为10%的稀盐酸恰好完全反应。
(假设污水中其他成分不与稀盐酸反应,反应的化学方程式为:HCl+NaOH====NaCl+H2O)
求:(1)100 g污水中含氢氧化钠多少克?
(2)污水中所含氢氧化钠的质量分数。
7.火力发电厂用石灰石泥浆吸收废气中的二氧化硫以防止污染环境,其反应方程式为:2CaCO3(粉末) + 2SO2+ O2====2CaSO4+ 2CO2。
(1)若100克废气中含6.4克二氧化硫,则处理100克这种废气需含碳酸钙(CaCO3)的石灰石__________克。
(2)处理上述100克废气,可得到含CaSO4 85%的粗产品_________克。
8.早在17世纪,质量守恒定律发现之前,英国化学家波义耳曾经做过一个实验:在密闭的容器中燃烧金属时,得到了金属灰,然后打开容器盖,称量金属灰的质量,发现比原来金属质量增加了。
(1)试解释金属灰质量比原金属质量增加的原因。
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。
请你改进他的称量方法,以验证质量守恒定律。
