药品报损审批表+销毁表
药剂科药品报损审批表

药剂科药品报损审批表
申请人
职位
部门
报损类别
申请日期
年月日
通用名
商品名
剂型
规格
包装
生产商
批准文号
批号
有效期
报损数量报损金额元Fra bibliotek报损原因:
非质量因素的不合格药品:
□过有效期
□包装破损
□包装污染
□药品外观改变
□改变包装、标签、说明书,旧包装、标签、说明书停用
□退回药品无法确定质量
□其他:
情况简述:
质量不合格的药品:
□假药
□劣药
□国家公布质量不合格的药品
□国家明令禁止销售的药品
□药品监督管理部门抽检不合格的药品
□药剂科抽检不合格的药品
□其他:
情况简述:
药品丢失:
情况简述:
责任人认定:
质量管理员意见:
质量管理员:年月日
药剂科主任意见:
药剂科主任:年月日
备注:
药品报损审批表

药监部门抽检不合格的药品□
药剂科抽检不合格的药品□
其他
原因分析
其他原因
药剂科主任意见
药剂科主任: 年 月 日
分管院长意见
分管院长: 年 月 日
备注
药品报损审批表
报损科室申请日期来自年 月 日药品类别西药□ 中药□
报损品种数量
报损金额
填报人
科室负责人
报
损
原
因
非质量因素的不合格药品
过有效期□
包装破损□
包装污染□
退回药品无法确定质量□
药品外观改变□
改变包装、标签、说明书;旧包装、标签、说明书停用□
其他
原因分析
质量不合格药品
假药□
劣药□
国家公布质量不合格的药品□
报损、过期药品销毁登记表

报损、过期药品销毁登记表一、基本信息1. 登记日期:____年____月____日2. 登记人:_______3. 药品名称:_______4. 生产厂家:_______5. 批准文号:_______6. 生产日期:_______7. 有效期至:_______8. 药品规格:_______9. 药品剂型:_______10. 药品数量:_______二、报损、过期原因1. 报损原因:(1)药品质量问题:由于药品生产、储存、运输等环节出现问题,导致药品无法正常使用。
(2)药品过期:药品在有效期内未销售完,过期后不能继续使用。
(3)药品破损:药品包装破损,导致药品无法正常销售。
(4)其他原因:如药品退市、政策调整等导致药品无法继续销售。
2. 过期原因:(1)库存管理不善:药品库存管理不当,导致药品过期。
(2)市场需求变化:药品市场需求发生变化,导致药品库存积压。
(3)药品采购过量:药品采购过量,导致药品在有效期内无法销售完。
(4)其他原因:如药品质量问题、政策调整等导致药品过期。
三、销毁过程1. 销毁方式:(1)焚烧:将过期、报损药品进行焚烧处理。
(2)填埋:将过期、报损药品进行安全填埋处理。
(3)专业销毁公司处理:委托专业销毁公司对过期、报损药品进行销毁处理。
2. 销毁流程:(1)药品清点:对过期、报损药品进行清点,确保数量准确。
(2)药品搬运:将过期、报损药品搬运至销毁现场。
(3)销毁操作:按照销毁方式对过期、报损药品进行销毁。
(4)销毁记录:记录销毁过程,包括销毁时间、销毁方式、销毁数量等。
(5)销毁证明:销毁完成后,由销毁公司出具销毁证明。
四、销毁结果1. 药品销毁数量:_______2. 销毁时间:_______3. 销毁方式:_______4. 销毁证明:见附件五、处理意见1. 药品报损、过期原因分析:针对本次药品报损、过期情况,进行原因分析,提出改进措施。
(1)加强药品库存管理,合理控制采购量。
药剂科药品报损审批表

药剂科药品报损审批表
申请人
职位
部门
报损类别
申请日期
年月日
通用名
商品名
剂型
规格
包装
生产商
批准文号
批号
有效期
报损数量
报损金额
元
报损原因:
非质量因素的不合格药品:
□过有效期
□包装破损
□包装污染
□药品外观改变
□改变包装、标签、说明书,旧包装、标签、说明书停用
□退回药品无法确定质量来自□其他:情况简述:质量不合格的药品:
□假药
□劣药
□国家公布质量不合格的药品
□国家明令禁止销售的药品
□药品监督管理部门抽检不合格的药品
□药剂科抽检不合格的药品
□其他:
情况简述:
药品丢失:
情况简述:
责任人认定:
质量管理员意见:
质量管理员:年月日
药剂科主任意见:
药剂科主任:年月日
备注:
药学部药品报废审批表

申请人
部门
申请时间
通Hale Waihona Puke 名商品名生产厂家剂型
规格
批准文号
批号
有效期
报损数量
报损金额
报损原因
非质量不合格的药品
□过有效期□包装破损□包装污染
□药品外观变形□退回药品无法确定质量
□改变包装,标签,说明书,旧包装,标签说明书停用
□其他:
质量不合格的药品
□假药□劣药□国家公布质量不合格药品
□国家明令禁止销售的药品□药品监管部门抽检不合格的药品
□药学部额抽检不合格的药品
□其他:
药品丢失
情况简述:
责任人认定:
药学部主任意见:
签字
年月日
分管院长意见:
签字
年月日
麻、精药品空安瓿销毁登记、审批表

麻醉和一类精神药品空安瓿、废贴销毁审批表
医疗机构:ຫໍສະໝຸດ 拟定销毁时间待销毁废贴数量
待销毁空安瓿数量
销毁地点
销毁方式
药剂科
申请意见
意见:
(签章)
年月日
医务科
意见
意见:
(签章)
年月日
药事管理委员会(主任)意见
意见:
(签章/签名)
年月日
麻醉和一类精神药品空安瓿、废贴销毁登记表
医疗机构:
销毁时间
废贴总数量
空安瓿总数量
销毁地点
销毁方式
销毁明细
药品名称
批号
生产单位
规格
数量
监毁人
药事管理委员会
医务科
保卫科
药剂科
注:销毁明细中,不同批号同一药名也要求记录。
精、麻药品销毁情况登记、审批表
科室:
首次登记时间:年月日----末次扥及时间:年月日
(年)麻、精药品销毁情况登记、审批表
医疗机构(公章):年月日
序号
药品名称
批号
生产单位
供货单位
规格
数量
有效期
报损原因
销毁方式
麻醉、一类精神药品管理人员签名
药剂科负责人签名
医院领导签名
卫生健康行政主管部门意见
签章
年月日
卫生健康行政主管部门监毁人员签名
麻醉药品、第一类精神药品报废销毁表
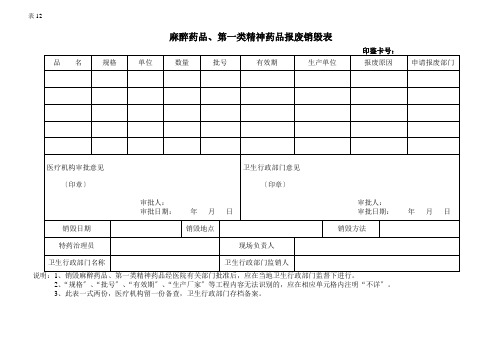
印鉴卡号:
品名
规格
单位
数量
批号
有效期
生产单位
报废原因
申请报废部门
医疗机构审批意见
〔印章〕
审批人:
审批日期:年月日
卫生行政部门意见
〔印章〕
审批人:审批日期:年月日 Nhomakorabea销毁日期
销毁地点
销毁方法
特药治理员
现场负责人
卫生行政部门名称
卫生行政部门监销人
说明:1、销毁麻醉药品、第一类精神药品经医院有关部门批准后,应在当地卫生行政部门监督下进行。
2、“规格〞、“批号〞、“有效期〞、“生产厂家〞等工程内容无法识别的,应在相应单元格内注明“不详〞。
3、此表一式两份,医疗机构留一份备查,卫生行政部门存档备案。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
保管员签字
配送中心负责人签字
质管部意见
质管部负责人签字:时间:年月日
质量负责人意见
质量负责人签字:时间:年月日
总经理意见
总经理签字:时间:年月日销毁执行情况运输源自具运输人员销毁日期
销毁地点
销毁方式
销毁后现场情况
销毁执行人签字
时间:年月日
销毁监督人签字
时间:年月日
药监部门人员签字
时间:年月日
备注
药品报损审批表
填报部门:填报日期年月日部门负责人:填表人:No:
药品编码
药品通用名称剂型
规格
单位
生产企业
供货企业
生产批号
有效期至
报损原因
报损
数量
进价
金额
业务部意见:
时间:
质管部意见:
时间:
主管经理意见:
时间:
金额合计
备注:
药品销毁单
单位或部门:NO:
销毁药品清单号
申请时间
销毁药品品规数
销毁药品总金额
该表后附销毁药品清单(可以是药品报损审批表等)
