第四章 酸碱滴定法
第四章 酸碱滴定法

[H ] [A ] [OH ]
平衡常数代入得:
K a [HA] K w [H ] [H ] [H ]
[H ]2 K a [HA] K w
精确式
第四章
酸碱滴定法
化学分析
若 caKa 20K W 时:可忽略Kw,得:
2 Κ Κ a a 4ca Κ a [H ] 2
(黄与红)
(蓝与黄)
特点: 变色敏锐;变色范围窄。
第四章
酸碱滴定法
化学分析
第三节
酸碱滴定法的基本原理
第四章
酸碱滴定法
化学分析
一、强酸(碱)的滴定
强酸与强碱滴定反应:
H+ + OHKt
H2O
1 1 14 1 . 00 10 [H ][OH ] K w
滴定常数(titration constant),Kt Kt值很大,是水溶液中反应程度最完全的酸碱滴定。
(续前 )
第四章
酸碱滴定法
化学分析
注:
实际与理论的变色范围有差别,深色比浅色灵敏
指示剂的变色范围越窄,指示变色越敏锐
例: pKa 甲基橙 3.4 甲基红 5.1 酚酞 9.1 百里酚酞 10.0 理论范围 2.4~4.4 4.1~6.1 8.1~10.1 9.0~11.0 实际范围 3.1~4.4 4.4~6.2 8.0~10.0 9.4~10.6
2K a 2 0.05 ca K a1
,按一元弱酸(碱)
处理:caKa1(b1)≥20Kw,c/Ka1(b1)≥500,用最 简式:[ H ] cKa1 ;[OH ] cKb1
第四章
酸碱滴定法
化学分析
分析化学酸碱第四章酸碱滴定法

HAc
δ0 δ Ac
Ac
cHAc
δ1 δ 0 δ HAc δ Ac
Ac Ka HAc Ac Ka H H K a 1 Ka H K a H
由上式我们可以看出: 值是H+浓度的函数,而与其 分析浓度无关。有了分布系数及分析浓度即可求得溶 液中酸碱各种存在形式的平衡浓度。
二、 溶剂的质子自递反应和水的质子自递常数
在水分子之间也可以发生质子转移作用, 这种仅在 溶剂分子之间发生的质子传递作用,称为溶剂的质子 自递反应。
H2O H2O H3O O H
该反应称为水的质子自递反应。反应的平衡常数称为水 的质子自递常数,以Kw表示。 [H3O+][OH-]= KW 水合质子H3O+常简写为H+,则 +][OH-]= KW [H 这个常数也称为水的离子积,在25℃时, [H+][OH-] = KW=1.0×10-14, pKW=14
4 4 3
NH NH 1
3 4
2、多元弱酸(碱)溶液中各存在形式的分布分数 (1)、二元酸
例如:草酸H2C2O4,在溶液中存在的形式有: H2C2O4 、HC2O4- 、 C O C2O42-,设其分析浓度为 cH ,三种存在形式的分布系数分别 为:δ 、δ 和 δ 2
H C O 2 2 4 1
[H ]2 Ka 1 Ka 1 Ka 2 [H ]2 [H ]Ka1 Ka 1Ka 2 1 [H ] [H ]2
同法可得:
[HC2O4 ] [H ]Ka1 δ 2 HC O c [H ] [H ]Ka1 Ka1Ka 2 2 4 H 2C 2O 4
第四章 酸碱滴定法 (分析化学人民卫生出版社第8版)

1、强酸(Ca )
HA H2O
H++AH + + OH -
[H+]=[A-]+[OH-]
[A-]=Ca
[H+]=Ca+Kw/[H+]
精确式
《 第四章 酸碱滴定法 1 》
- 6/125页 -
当Ca ≥ 20[OH-],忽略水的解离
[H+] ≈Ca
近似式
pH=-lg [H+]=-lgCa
《 第四章 酸碱滴定法 1 》
理论变色范围 pH=2.4~4.4
《 第四章 酸碱滴定法 1 》
- 35/125页 -
常用酸碱指示剂(P46)
人对不同颜色的敏感程度不同,红色易辨别,实际变色 范围与理论变色范围稍有区别。
《 第四章 酸碱滴定法 1 》
- 36/125页 -
注意 : 1、酸碱指示剂的变色范围不一定正好位于pH=7左右 ,
例:计算0.10 mol/L的邻苯二甲酸氢钾溶液的 pH。 解:查表得邻苯二甲酸的pKa1=2.94, pKa2=5.43
cKa2 ≥ 20Kw c≥ 20Ka1
1 mol/L的邻苯二甲酸氢钾溶液的 pH?
《 第四章 酸碱滴定法 1 》
- 22/125页 -
例:分别计算0.05 mol/L的NaH2PO4和3.33×10-2 mol/L的 Na2HPO4溶液的pH。
溶液的颜色随溶液pH的变化而变化,当pH=pKHIn 时 , [In-]=[HIn],这一点的pH称为理论变色点,溶液显酸 式色和碱式色的混合色。
《 第四章 酸碱滴定法 1 》
- 33/125页 -
由于人眼对颜色的辨别能力有限,在一点上不容易观察出,必须有一
《分析化学》-图文课件-第四章

如果cKa2≥10Kw,c/Ka1≥10,即[HCO3-]≈cHCO3-,则水解 离的H+忽略,Ka1与[HCO3-]相加时可忽略,则上式可简化为
(4-7)
第二节 溶液的酸碱度和pH值的计算
【例4-5】
计算0.10 mol·L-1 NaHCO3溶液的pH值。 解:已知H2CO3的Ka1=4.12×10-7,Ka2=5.62×10-11,符合cKa2≥10Kw, c/Ka1≥10。 根据式(4-7)得
因此,同浓度的NH3和CO3-2的碱性:CO3-2>NH3。
第二节 溶液的酸碱度和pH值的计算
一、 溶液的酸碱度
溶液的酸碱度是指溶液中氢离子、氢氧根离子的活度,常用 pH、pOH表示。它与溶液的浓度在概念上是不相同的,但当溶 液浓度不太大时,可用浓度近似地代替活度。溶液酸碱度的表达 式为
(4-3) 当温度为25 ℃时,水溶液Kw=[H+]·[OH-]=10-14,所 以 pH+pOH=pKw=14。 由此可见,pH值越小,酸度越大,溶液的酸性越强;pH越 大,酸度越小,溶液的碱性越强。同理,pOH越小,碱度越大, 溶液碱性越强;pOH越大,碱度越小,溶液的酸性越强。
实际上,酸碱半反应在水溶液中并不能单独进行,一种酸给 出质子的同时,溶液中必须有一种碱来接受。这是因为质子的半 径很小,电荷的密度比较高,游离的质子在水溶液中很难单独存 在。根据酸碱质子理论,各种酸碱反应实质上是共轭酸碱对之间 水合质子的转移过程。例如:
第一节 酸碱滴定法概述
在上述的反应中,溶剂水接受HAc所给出的质子,形成水合质 子H3O+,溶剂水也就起到碱的作用。同样,碱在水溶液中的解离, 也必须有溶剂水参加。以NH3在水溶液中的解离反应为例,NH3分 子中的氮原子上有孤对电子,可接受质子形成NH4+,这时,H2O 便起到酸的作用给出质子。具体反应如下:
第4章 酸碱滴定法

三种酸强弱顺序:HCl>HAC>H2S 在共轭酸碱对中,如果酸愈易给出质子,酸性愈弱,则其共轭碱对质子的亲和 力就愈弱,就愈不容易接受质子碱性就愈弱。 其共轭碱强弱顺序:Cl-1<AC-<HS2.Ka 和 Kb 之间关系: 共轭酸碱相互依存关系 [H + ][A − ] Ka= , [HA] 例: NH 3 + H 2 O Kb= Ka 和 Kb 之间关系 Ka·Kb=Kw NH + 4 + H 2O Ka= NH 3 + H 3 O +
−
δ1 =
[HC 2 O 4 ] [HC 2 O 4 ] = 2c [H 2 C 2 O 4 ] + [HC 2 O 4 ] + [C 2 O 4 ] K a1 [ H + ] = + 2 [ H ] + K a1 [ H + ] + K a1 K a 2
[C O ] [C 2 O 4 ] δ2 = 2 4 = 2c [H 2 C 2 O 4 ] + [HC 2 O 4 ] + [C 2 O 4 ] = K a1 K a 2 [ H ] + K a1 [ H + ] + K a1 K a 2
注意:Ka 和 Kb 之间的对应关系
§4-2 不同 pH 值溶液中酸碱存在形式的分布情况--分布曲线
引言:上次课上我们对酸碱平衡的基础理论进行简要的讨论,从这节课开始我 们介绍酸碱滴定法的有关理论和应用。这堂课我们学习分布曲线,学习它可帮 助我们深入理解酸碱滴定的过程、滴定误差以及分布滴定的可能性,而且对于 了解络合滴定与沉淀反应条件也是有用的。 任意的离解反应: HB + H 2 O 达平衡时 aq 中存在 [H3O+] H 3O + + B− [HB] [B-]
分析化学第4章 酸碱滴定法

[OH ] [ H ] 1010 104 TE % 100% 100% 0.2% CSP 0.05000
例:同上题,若以酚酞为指示剂,滴定至 pH=9为终点,计算终点误差。 解:已知Cb=0.05000mol/L, 终点溶液pH=9, [H+]=10-9mol/L,则[OH-]=10-14/10-9=10-5 mol/L。
(2)一元弱酸碱滴定
0.1000mol/L NaOH滴定20.00mL 0.1000mol/L HAc
HAC+OH-=AC-+H2O
滴定前:
[ H ] Ca K a
计量点前: HAC-NaAC缓冲系
[ HAC] [H ] Ka [ AC ]
滴入NaOH 19AC ] 20 .00 19 .98
共轭酸碱对概念 例:区分下列物质是酸还是碱?并指出共轭酸碱对
HAc H2CO3 H3PO4 NaAc NaHCO3 NaH2PO4 Na2HPO4 Na3PO4 H2O
NaCO3
酸碱反应的实质
酸碱共轭体系不能单独存在 HAc(酸1)H++Ac-(碱1) H++H2O(碱2) H3O+(酸2)
C C
HAc+OH-
K
b
OH HAc Ac
W
10
14
25C
C
pKa+pKb=pKw
酸的强度与其共轭碱的强度是反比关系。 酸愈强( pKa愈小),其共轭碱愈弱( pKb愈 大 ),反之亦然。
第04章酸碱滴定法

HAc (酸1)+ H2O (碱2)
H3O+(酸2)+Ac- (碱1)
溶剂水起碱的作用
2019年1月26日9时53 分
碱在水溶液中接受质子的过程:
NH3 + H+ H2O NH3 + H2O NH4+ H+ + OH- OH- + NH4+
必须有溶剂水分子参加。在这里,溶剂水起到酸 的作用。 水是一种两性溶剂: H2O + H2O
= 6.80
即
2019年1月26日9时53 分
Kb2=1.6×10 -7
§4.2 不同pH溶液中酸碱存在形式 的分布情况—分布曲线
分布曲线(distribution curve)作用: (1)深入了解酸碱滴定过程; (2)判断多元酸碱分步滴定的可能性。 滴定是溶液pH 与溶液中各物种的量及其比例不断 变化的过程。 分布系数δ (distribution coefficient) :
2019年1月26日9时53 分
例 2:
一元弱酸水溶液,选择HA和H2O为参考水平: HA 的解离反应: HA + H2O 水的质子自递反应: H2O + H2O H3O+ + A-
H3
O+
+ OH
-
质子条件:[H+] = [A- ] + [OH - ]
2019年1月26日9时53 分
例 3:
Na2CO3水溶液,选 CO32- 和 H2O为参考水平: CO3 + H2O
2019年1月26日9时53 分
H3O+ + OH-
水的质子自递常数
在水分子之间存在着的质子传递作用,称为水的 质子自递作用。这种作用的平衡常数称为水的质子自 递常数: Kw = [H3O+][OH-] 或: Kw= [H+][OH-] 在25℃: Kw = 10-14 pKw= 14
4第四章 酸碱滴定法
NH3CH 2COOH的K a1 4.5 103 ; K a 2 2.5 1010 ;
NH 4 a
解:(1) [H ] K a K
Kw Ka Kb
1.8 104 1.0 1014 3.2 107 (mol L1 ) 1.8 105 pH 6.50
•
•
强酸强碱溶液pH值的计算 弱酸弱碱溶液pH值的计算 两性物质溶液(C ) 缓冲溶液pH值的计算
水溶液中[H+]的计算方法: 1. 列出PBE式; 2. 代入有关常数和浓度数据; 3. 计算出[H+]。 注:在计算中可以进行合理的近似处理, 最后用近似式或最简式进行计算。
一、一元酸(碱)溶液的氢离子浓度计算
[ NH ] 4
精确式
[H ] K a1 ( K a 2 K
NH 4 Na H2PO4 Na2HPO4
H
K a1 K a 2 K a1 K a 2
H
H
Ka 2 Ka 3
练习题: (1)计算0.10mol HCOONH4溶液的pH值。 L-1 (2)计算0.10mol L-1氨基乙酸(NH2CH2COOH)溶液的pH 值。 HCOOH的K a 1.8 104 ; NH3的Kb 1.8 105
23 3
2
NH 4 a
[ NH ] 4 [H ] 2- 2[H ] [CO 3 ] 1 1 Ka2 K a1 Kw K
NH 4 a
精确式
[H ] 2 K a 2 K
NH 4 a
最简式***
2. 酸式盐:NH4HCO3
2 [H ] [OH ] [CO3 ] - [H2CO3 ] [NH3 ]
分析化学课件 第四章 酸碱滴定法

[OH-]=(0.1000×0.02)/(20.00+20.02)
= 5.0×10-5 mol·L-1 pOH=4.30, pH=14-4.30= 9.70
2020年11月7日星期六3时
37分22秒
上一页 下一页 返回
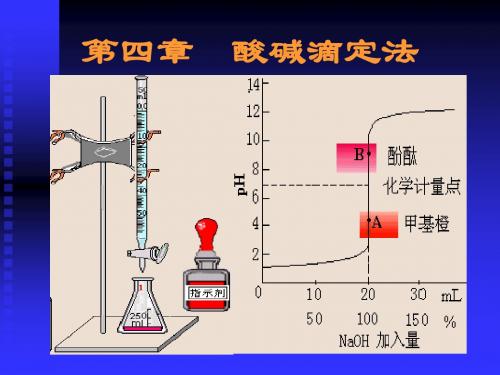
讨论:强碱滴定强酸的滴定曲线
1)滴定前加入18mL,溶液pH变化仅 为:2.28-1=1.28;而化学计量点前 后共0.04 mL(约1滴),溶液pH 变化 为:9.70-4.30=5.40 (突跃)。
碱式色
2020年11月7日星期六3时 37分22秒
上一页 下一页 返回
→甲基橙(methyl orange,MO)-双色
pH≤ 3.1,酸式色,红色; pH 4.4, 碱式色,黄色; pH 3.1-4.4,两种形式共存,为混合色,橙色。
2020年11月7日星期六3时 37分22秒
上一页 下一页 返回
上一页 下一页 返回
若±0.1%误差范围内突跃范围为 4.30~9.70
酚酞(8.0 ~ 10.0):半滴溶液, 无色变粉红。
甲基红(4.4 ~6.2):半滴溶液, 红变橙;
甲基橙(3.1 ~ 4.4):半滴溶液, 橙变黄;
3)选择指示剂的原则:
1.变色范围全部或部分在突跃范围内的指示剂指示
终点,即可保证终点误差在允许的范围。
02.00.102000 1050..130 ~9.87.070
上一页 下一页 返回
5)影响强酸强碱滴定突跃范围大小的因素
酸碱的浓度:浓度变为原1/10,则计量点前后H+、OH-的浓度均 为原来的1/10,所以突跃范围约减小2个pH单位。 故:酸碱滴定中,滴定剂和被测物溶液的浓度不低于~ 0.1mol/L
分析化学 第四章_酸碱滴定法一 图文

H2CO3 H HCO3 H CO32
H3O H H2O H OH
质子条件式为:
H 2CO 3 H 3O
C
O
2 3
O
H
分析化学
第四章 酸碱滴定法
14
• 方法要点:
• 1.从酸碱平衡体系中选取质子参考水准(又称 零水准),它们是溶液中大量存在并参与质子 转移反应的物质。
方法。 • 理论基础: • 酸碱平衡理论及酸碱质子理论。 • 优点: • 方法简单、快速,应用广泛。 • 应用: • 一般酸、碱以及能与酸、碱直接或间接发生质子
转移反应的物质。
分析化学
第四章 酸碱滴定法
2
酸碱质子理论
• 能给出质子的是酸,能接受质子的是碱,酸和 碱是相互依存和相互转化的。酸碱不是彼此独立 的,而是统一在 对质子的关系上。
9
酸碱质子理论的基本要点:
• 1. 能给出质子的是酸,能接受质子的是碱; • 2. 统一在对质子的关系上,共轭酸碱对之间具有
相互依存、相互转换的关系; • 3. 酸或碱的离解常数是物质酸或碱性强弱的定量
指标; • 4. 物质的酸碱性不仅与此物质的本质有关,还与
溶剂的性质有关; • 5. 在溶液中,质子不能单独存及其理论基础 • 第一节 酸碱溶液中氢离子浓度的计算 • 第二节 酸碱指示剂 • 第三节 酸碱滴定法的基本原理 • 第四节 滴定终点误差 • 第五节 非水溶液中的酸碱滴定法
分析化学
第四章 酸碱滴定法
1
• 酸碱滴定法的定义: • 酸碱滴定法是以质子转移反应为基础的滴定分析
分析化学
第四章 酸碱滴定法
12
• (二)电荷平衡
分析化学第四章酸碱滴定

酚酞(PP)
HO OH O- O
OH OH COO
-
-
H+ pKa = 9.1
COO-
Hale Waihona Puke 羟式(无色)醌式(红色)
甲基橙(MO)
(H3C)2
+
-
N
NH
N H
SO3
红色(醌式)
OH H+
1/10
[In-] / [HIn]=1
10
p KHIn +1
理论变色范围
注: 实际与理论的变色范围有差别,深色比浅色灵敏 指示剂的变色范围越窄,指示变色越敏锐
小结:
1)酸碱指示剂的变色范围取决于指示剂常数 值KHIn 2)各种指示剂在变色范围内显示出过渡色 3)指示剂的变色间隔不会大于2个pH单位 4)指示剂加入量影响:适当少些颜色明显 加的多,消耗滴定剂。
强酸)
3.影响滴定突跃的因素和指示剂的选择
影响因素:被滴定酸的性质,浓度 C一定, Ka↓,Kt↓,⊿pH↓ Ka一定,C↓,⊿pH↓(滴定准确性越差) 指示剂的选择: ⊿pH =7.75~9.70,选碱性范围变色的酚酞,百 里酚酞
4.弱酸能被准确滴定的判别式:
Ca •Ka≥ 10-8
讨论:
pH 2.88
(2)Vb < Va :HAc + NaAc
SP前0.1% 时 ,已加入NaOH 19.98mL C AC Cb pH pKa lg pKa lg Ca C HAC
5
3
pH 7.75
第四章酸碱滴定法

第四章酸碱滴定法第四章酸碱滴定法酸碱滴定法(acid-base titrations)是以⽔溶液中的质⼦转移反应为基础的滴定分析⽅法。
⼀般酸、碱以及能与酸碱直接或间接发⽣质⼦反应的物质,⼏乎都可以⽤酸碱滴定法测定。
因此,酸碱滴定法是分析化学的基础内容之⼀。
这个⽅法的关键问题是计量点的确定。
因为酸碱反应通常不发⽣外观的变化,在滴定中需选⽤适当的指⽰剂,利⽤它的变⾊作为到达计量点的标志。
因为不同的指⽰剂的变⾊有其不同的pH,⽽不同类型的酸碱反应的计量点时pH⼜不相同,为了正确地确定计量点,就需要选择⼀个刚好能在计量点时变⾊的指⽰剂。
要解决这个问题,必须了解滴定过程中溶液pH的变化情况。
因此,在学习酸碱滴定时,不仅要了解指⽰剂的变⾊原理和变⾊范围,同时也要了解滴定过程中溶液pH的变化规律和指⽰剂的选择原则,以便能正确地选择合适的指⽰剂,获得准确的分析结果。
基于上述原因,我们先讨论酸碱溶液平衡的基本原理,然后再介绍酸碱滴定中的理论及应⽤。
第⼀节⽔溶液中的酸碱平衡⼀、酸碱的质⼦理论根据质⼦理论,凡能给出质⼦(H+)的物质是酸,能接收质⼦的物质是碱。
酸碱关系可⽤下式表⽰:酸HA与碱A-处于⼀种相互依存的关系中,即:HA失去质⼦转化为它的共轭碱A-,A-得到质⼦后,转化为它的共轭酸HA,则HA与A-被称为共轭酸碱对。
如:由上述酸碱的半反应可知:酸碱可以是中性分⼦,也可以是阳离⼦或阴离⼦,酸碱是相对的。
⼜如:离⼦(H2PO4-)在H3PO4-H2PO4-共轭体系中为碱,⽽在H2PO4--HPO42-共轭体系中为酸。
同⼀物质在某些场合是酸,⽽在另⼀场合是碱,其原因是共存物质彼此间给出质⼦能⼒相对强弱不同。
因此同⼀物质在不同的环境(介质或溶剂)中,常会引起其酸碱性的改变。
既能给出质⼦⼜能接受质⼦的物质称为两性物质。
酸碱质⼦理论认为,酸碱反应的实质是质⼦转移。
例如HAc在⽔中离解,溶剂⽔就起着碱的作⽤,否则HAc⽆法实现其在⽔中的离解,即质⼦转移是在两个共轭酸碱对间进⾏。
第四章酸碱滴定法

第二节 酸碱指示剂
一、指示剂的变色原理
1. 指示剂: a.弱的有机酸(碱); b.酸式体和碱式体颜色不同→指示终点 c.溶液pH变化→指示剂结构改变→指示终点变化
HIn
酸式体
H + + In -
碱式体
2. 常用指示剂的变色原理
二、指示剂的变色范围及其影响因素
1.变色范围 HIn
② 突跃范围:突跃所在的浓度(pH)范围。
③影响突越大小因素 Ca(Cb)越大,突越越大; 对滴定误差的要求。
④ 指示剂的选择原则
凡是变色范围部分或全部落在滴定突跃 范围内的指示剂都可用来指示终点。
4.强酸滴定强碱 形状类似强碱滴定强酸,pH变化相反
二、一元弱酸(碱)的滴定
1.滴定常数
HA + OH-
定义:加入少量酸碱,溶液pH值无显著变化的溶液。 组成:共轭碱(酸)、或浓度较大的强酸(碱)
例: Ca mol/mL HA与Cb mol/mL NaA水溶液
质量: 电荷:
[HA] + [A-] = Ca + Cb [Na+] = Cb [Na+] + [H+]= [A-] + [OH-]
将(2)式带入(3)式,得质子条件式: [A-] = Cb + [H+] - [OH-] (1)
第四章 酸碱滴定法
分析化学教研室
概述
酸碱滴定法: 以酸碱反应(质子转移反应)为基础的定量 分析法。
本章主要内容:
• 各类酸碱溶液的pH值计算方法 • 酸碱滴定曲线和指示剂的选择 • 酸碱滴定及滴定终点误差
酸碱质子理论:
酸——溶液中凡能给出质子的物质
第四章 酸碱滴定法-分析化学

HAc的解离: HAc + H2O
H3O+ + Ac-
质子理论对酸碱的总结:
xie 分 析 化 学 酸碱是相对的,在不同的化学反应中,物质是酸是碱, 取决于反应中该物质对质子亲和力的相对大小。因此 当讨论某一种物质是酸是碱时,不能脱离该物质和其 他物质(包括溶剂)的相互关系。 同一种物质在不同溶剂中可表现出不同的酸碱性。对一 定的酸,溶剂接受质子的能力越强,酸性则越强。 例如:硝酸在水中为强酸,在冰醋酸中酸性减 弱,在浓硫酸中则显碱性。
xie 分 析 化 学
例如:盐酸与氨在水溶液中的反应:
HCl + H2O H3O+ + Cl-
H3O+ + NH3
NH4+ + H2O
NH4+ + Cl-
总式
HCl + NH3
注意:
xie 分 析 化 学 质子论的酸碱中和反应没有盐的生成。因此, 盐的水解反应和电解质的离解过程都是酸碱质子 转移反应。 例如:
pKb=pKw-pKa=14.00-9.21=4.79
xie 分 析 化 学
多元酸在水中分级电离,其水溶液中存在着多
个共轭酸碱对,其共轭关系如下(以三元酸为
例): A3-+H2O HA2-+H2O H2A-+H2O HA2-+OHH2A-+OHH3A+OHKW=Kb1×Ka3 KW=Kb2×Ka2 KW=Kb3×Ka1
3 K a1 K a2 K a3 [ PO4 ] 3 C [ H ]3 K a1 [ H ]2 K a1 K a2 [ H ] K a1 K a2 K a3
第四章酸碱滴定法

解:
NH
4
NH3 H
Ka
Kw Kb
1014 1.8105
cKa 20Kw 但
5.61010 C 500 Ka
[H ] Kac Kw 5.61010 104 1014 2.6107
pH=6.58
例:求0.1mol/L NaCN溶液的pH值。
H2PO4Ka2
HPO42Ka3
H2PO4 - + H+ Kb3
HPO42- + H+ Kb2
PO43- + H+ Kb1
讨论:
多元酸碱在水中逐级离解,强度逐级递减
Ka1 Ka2 Ka3 Kb1 Kb2 Kb3
形成的多元共轭酸碱对中最强酸的解离常数 Ka1对应最弱共轭碱的解离常数Kb3 Ka1 Kb3 Ka2 Kb2 Ka3 Kb1 KW 1.01014
例 .计算0.10mol/LNa2CO3 溶液的pH值 解:已知 H2CO3 的 Ka1 4.2 107 Ka2 5.6 1011
因为
Kb1
Kw Ka2
1.8104
Kb2
Kw K a1
2.4 108
所以 可按一元碱处理 , 又
cKb1 ≥ 20Kw
C 500 Kb1
质子条件式 *
化学平衡关系 [H+]的精确表达式
近似处理 近似式
进一步近似处理
最简式
(一) 强酸(碱)溶液[H+]的计算 → 强酸溶液
质子条件式: 代入平衡关系式
[H+] = [A-] + [OH-]
第四章酸碱滴定法

1
1
K a1 [H ]
Ka1 • Ka2 [H ]2
H 2 H 2 Ka1 H
Ka1 Ka2
即: δ0 δH2C2O4
H 2C2O4 C
H 2 H 2 Ka1 H Ka1 Ka2
同理: δ1 δHC2O4
HC2O4 C
H 6 Ka1 H 5 Ka1 Ka2 H 4 Ka1 Ka2 Ka3 Ka4 Ka5 H Ka1 Ka2 Ka3 Ka4 Ka5 Ka6
第二节 酸碱溶液的pH计算
1. 一元酸(碱)溶液的氢离子浓度计算 2. 多元酸(碱)溶液的氢离子浓度计算 3. 两性物质溶液的氢离子浓度计算 4. 缓冲溶液的氢离子浓度计算
1)
[H ] [HB] [OH ]
[OH
]
Cb
Kw [OH
]
2)
[OH ] Cb Cb2 4Kw
2
(精确式)
3)
[OH - ] Cb
(近似式)
(二)弱酸(碱)溶液的氢离子浓度计算
1. 设一元弱酸(HA)浓度为Ca(mol/L),计算[H+]
HA
H+ +A-
H2O
H + + OH -
小结:
1.MBE、CBE、PBE反映的都是溶液平衡体系中各组分 平衡浓度之间的关系; 2.MBE反映的是总浓度与平衡浓度的关系,组分可以是 离子或中性分子,CBE反映的是体系中所有阴、阳离子平 衡浓度之间的关系,中性分子不包括在内。 3.PBE则反映的是得质子组分与失质子组分平衡浓度之 间的关系,它是处理酸碱平衡体系的基本关系式。
例如,C mol/L的HAc溶液。
参考水准
[H+] 得质子 H2O
第四章 酸碱滴定法(人卫版分析化学)

第四章酸碱滴定法1.基本概念(1)混合指示剂:两种或两种以上指示剂相混合,或一种指示剂与另一种惰性染料相混合。
利用颜色互补原理,使终点颜色变化敏锐。
(2)滴定反应常数(K t):是滴定反应平衡常数。
强碱(酸)滴定强酸(碱):K t=1/K w=1014;强碱(酸)滴定弱酸(碱):K t=K a(b) /K w。
K t值越大,该滴定反应越完全,滴定突跃越大。
(3)滴定曲线:以滴定过程中溶液pH值的变化对滴定体积(或滴定百分数)作图而得的曲线。
(4)滴定突跃:化学计量点附近(±0.1%)pH的突变。
(5)滴定误差:滴定终点与化学计量点不一致引起的误差,与指示剂的选择有关。
(6)质子溶剂:能给出质子或接受质子的溶剂。
包括酸性溶剂、碱性溶剂和两性溶剂。
(7)无质子溶剂:分子中无转移性质子的溶剂。
包括偶极亲质子溶剂和惰性溶剂。
(8)均化效应和均化性溶剂:均化效应是指当不同的酸或碱在同一溶剂中显示相同的酸碱强度水平;具有这种作用的溶剂称为均化性溶剂。
(9)区分效应和区分性溶剂:区分效应是指不同的酸或碱在同一溶剂中显示不同的酸碱强度水平;具有这种作用的溶剂称为区分性溶剂。
2.基本原理(1)酸碱指示剂的变色原理:指示剂本身是一类有机弱酸(碱),当溶液的pH改变时,其结构发生变化,引起颜色的变化而指示滴定终点。
酸碱指示剂的变色范围:pH=pK HIn±1;理论变色点:pH=pK HIn(2)选择指示剂的原则:指示剂变色的pH范围全部或大部分落在滴定突跃范围内,均可用来指示终点。
(3)影响滴定突跃范围的因素:①酸(碱)的浓度,c a(b)越大,滴定突跃范围越大。
②强碱(酸)滴定弱酸(碱),还与K a(b)的大小有关。
K a(b)越大,滴定突跃范围越大。
(4)酸碱滴定的可行性:强碱(酸)滴定一元弱酸(碱):c a(b)K a(b)≥10-8,此酸、碱可被准确滴定。
多元酸(碱):c a1(b1)K a1(b1)≥10-8,c a2(b2)K a2(b2)≥10-8,则两级离解的H+均可被滴定。
第四章 酸碱滴定法

KHIn与温度有关;
如18℃时,甲基橙的变色范围为3.1~4.4,而 100℃时则为2.5~3.7。 滴定宜在室温下进行
返回
不同的溶剂中KHIn值不同; 例如甲基橙在水溶液中pKHIn=3.4,而在甲 醇中pKHIn=3.8。 溶剂中中性电解质的存在增加了溶液的离 子强度,使指示剂的表观离解常数改变, 将影响指示剂的变色范围。 同时某些盐类具有吸收不同波长光的性质, 也会改变指示剂颜色的深度和色调。 返回
第四章 酸碱滴定法
酸碱滴定法(中和滴定法): 以酸碱反应(水溶液中的质子转移反 应)为基础的定量分析法. (非水滴定单独讲解)
本章重点: (1)酸碱平衡理论 (2)各类酸碱溶液的pH值计算方法 (3)指示剂的选择和各类酸碱滴定曲线
第一节 水溶液中的酸碱平衡
一、酸碱的质子理论
凡能给出质子(H+)的物质是酸,能接收 质子的物质是碱。
子条件式中的[OH-]项可忽略,则有:
[H+]=[A-]=Ca
2.一元弱酸
[H+]=[A-]+[OH-]
K a [HA] K w [H ] [H ] [H ]
[H ]2 K a [HA] K w
C a [H ] [HA] Ca δ 0 [H ] K a
NaHCO3溶液 参考物质:HCO3-,H2O
H2CO3 H3O
+
+H +H
+ + HCO3
-H
+ + 2CO3 -
H2O
-H
OH
质子条件式: [H2CO3]+[H3O+]=[CO32-]+[OH-]
(二)一元酸碱溶液的pH计算
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第四章酸碱滴定法(65题)(一)A型题在以下选项中选出一个最符合题意的答案。
1.酸碱滴定法的标准溶液是()。
A.NaOH B.Na2CO3C.HAcD.NH3·H2O E.Na2B4O7·10H2O2.标定HCl溶液的基准物质是()。
A.NaOH B.Na2CO3C.HAcD.NH3·H2O E.KHC8H4O43. 标定NaOH溶液的基准物质是()。
A.HAc B.Na2CO3C.KHC8H4O4D.NH3·H2O E. NaOH4. 测定HAc含量选用的指示剂为()。
A.石蕊 B. 甲基橙 C. 酚酞D.甲基红 E. 中性红5. 用甲基橙为指示剂测定Na2CO3含量,其HCl与Na2CO3反应完全时,物质的量之比为()。
A.2:1 B. 1:2 C. 1:1D.3:1 E. 1:36. NaOH标准溶液测定HAc含量时,用酚酞为指示剂,终点颜色是()。
A.无色 B. 淡红色 C. 红色D.黄色 E. 橙色7. HCl标准溶液测定NH3·H2O含量,应选择的指示剂是()。
A.甲基橙 B. 酚酞 C. 百里酚酞D.中性红 E. 以上均可8. 可用碱标准液直接测定的物质的条件为()。
A.cKa≥10-8的酸 B. cKb≥10-8的碱 C. NaOHD.NH3·H2O E. H2CO39. 可用酸标准溶液直接测定的物质的条件为()。
A.cKa≥10-8的酸 B. cKb≥10-8的碱 C. NaOHD.NH3·H2O E. H2CO310. 测定硼砂含量实践操作正确的是()。
A.左手控制滴定管活塞流速,右手旋摇锥形瓶B. 右手控制滴定管活塞流速,左手旋摇锥形瓶C. 用托盘天平称取硼砂质量D.用移液管移取谁的体积E. 将硼砂加热溶解后立即加入指示剂11. 在用邻苯二甲酸氢钾基准物标定NaOH的实践操作中,正确的是()。
A.用酸式滴定管盛装NaOH溶液B. 排碱式滴定管尖端气泡时,是将胶管中的玻璃珠往上移动C. 用碱式滴定管盛装NaOH溶液D.排碱式滴定管尖端气泡时,是将胶管中的玻璃珠往下移动E. 选用甲基橙指示剂指示终点12.酚酞指示剂的变色范围及颜色是()。
A.8.0(无色)~10.0(红色) B. 8.0(红色)~10.0(无色)C. 3.1(红色)~4.4(黄色) D.3.1(黄色)~4.4(红色)E. 4.4(红色)~6.2(黄色)13. 甲基橙指示剂的变色范围及颜色是()。
A.8.0(无色)~10.0(红色) B. 8.0(红色)~10.0(无色)C. 3.1(红色)~4.4(黄色) D.3.1(黄色)~4.4(红色)E. 4.4(红色)~6.2(黄色)14. 甲基红指示剂的变色范围及颜色是()。
A.8.0(无色)~10.0(红色) B. 8.0(红色)~10.0(无色)C. 3.1(红色)~4.4(黄色) D.3.1(黄色)~4.4(红色)E. 4.4(红色)~6.2(黄色)15. 酸碱指示剂一般属于()。
A. 无机物B. 有机盐C. 有机酸D. 有机碱E. 有机弱酸或弱碱16. 强酸强碱的滴定,化学计量点的酸碱性是()。
A. pH﹤7B. pH﹥7C. pH=7D. 强酸性E. 强碱性17. 强酸滴定弱碱,化学计量点酸碱性是()A. pH﹤7B. pH﹥7C. pH=7D. 强酸性E. 强碱性18. 强碱滴定弱酸,化学计量点酸碱性是()A. pH﹤7B. pH﹥7C. pH=7D. 强酸性E. 强碱性19. 判断二元弱酸能被滴定,并有两个滴定突跃的条件是()A. cKa2≥10-8 B. Ka1/Ka2≥104 C. cKb2≥10-8D. Kb1/Kb2>104 E. cKa2≥10-8;Ka1/Ka2≥10420. 二元弱碱能被滴定,并有两个滴定突跃的条件是( )A. cKa2≥10-8;Ka1/Ka2≥104 B. Ka1/Ka2≥104C. cKb2≥10-8 D. cKb≥10-8;Kb1/Kb2≥104E. Kb1/Kb2>10421. 酸碱指示剂的变色范围是()A. pH=PKHIn ±0.1 B. pH=PKHIn±0.2 C. pH=PKHIn±1D. pH=PKHIn ±2 E. pH=PKHIn±322. 混合指示剂的优点包括,颜色变化敏锐,变色范围()A. 不一定B. 多样C. 宽D. 窄E. 以上均是23. 标定HCl溶液时用Na2CO3为基准物质,称取Na2CO30.6817g,以甲基橙为指示剂,用去HCl溶液26.50ml,HCl溶液的浓度为()mol/L。
(M=105.99)A. 0.4800 B. 0.4854 C. 0.4850D. 0.048E. 0.48624. 在1.000g粗铵盐中加过量NaOH溶液,产生的氨经蒸馏吸收在50.00ml0.5000 mol/L的盐酸中,过量的酸用0.5000 mol/L NaOH标准溶液滴定,用去1.56ml,该样品中的NH3的质量分数为()A. 0.4140B. 0.4141C. 0.4125D. 0.4122E. 0.412425. OH-的共轭酸是()。
A. H+B. H2O C.H3O+D. O2-E. 以上均不是26. 在下列各组酸碱组分中,不属于共轭酸碱对的是()A. HOAc-NaOAcB. H3PO4-H2PO4-C. +NH3CH2COOH-NH2CH2COO- D. H2CO3-HCO3-E. 以上均不是27. 水溶液中共轭酸碱对K a与K b的关系是()A. K a·K b=1B. K a·K b=K wC. K a/K b=K wD. K b/K a=K wE. 以上均不是28. 浓度相同的下列物质水溶液的pH最高的是()A. NaClB. NH4Cl C. NaHCO3D. Na2CO3E. HCl29. 今有一磷酸盐溶液的pH = 9.78, 则其主要存在形式是()(已知H3PO4的解离常数p K a1 = 2.12,p K a2 = 7.20,p K a3 = 12.36)A. HPO42- B. H2PO4- C. HPO42- + H2PO4D. H2PO4-+ H3PO4E. HPO42-+ H3PO430. 以下溶液稀释10倍时pH改变最小的是()A. 0.1 mol·L-1 NH4OAc溶液B. 0.1 mol·L-1 NaOAc溶液C. 0.1 mol·L-1 HOAc溶液D. 0.1 mol·L-1 HCl溶液E. 0.1 mol·L-1HAc溶液31. 以下溶液稀释10倍时pH改变最大的是()A. 0.1 mol·L-1 NaOAc-0.1 mol·L-1 HAc溶液B. 0.1 mol·L-1 NaAc溶液C. 0.1 mol·L-1 NH4Ac-0.1 mol·L-1 HOAc溶液D. 0.1 mol ·L -1 NH 4Ac 溶液E. 0.1 mol ·L -1 NH 4OAc 溶液32. 欲配制pH=9的缓冲溶液,应选用( ) A. NH 2OH(羟氨) (p K b =8.04) B. NH 3·H 2O (p K b = 4.74) C. CH 3COOH (p K a = 4.74) D. HCOOH (p K a = 3.74) E. 以上均不能选用33. 欲配制pH=5的缓冲溶液,下列物质的共轭酸碱对中最好选择( ) A. 一氯乙酸(K a = 1.4×10-3) B. 甲酸(K a = 1.8×10-4) C. 乙酸(K a = 1.8×10-5) D. 氨水(K b = 1.8×10-5) E. 醋酸34. 用NaOH 滴定某一元酸HA ,在化学计量点时,[H +]的计算式是( )A. a HA K c ⋅B. -B HAa c c K ⋅C.a A w -K c K ⋅ D. -A wa c K K ⋅E.-A ac K 35. 配制HCl 标准溶液用( )法。
A. 直接配制法B.间接配制法C. 置换法D. 滴定法E. A 、B 选项均可 36. 配制NaOH 标准溶液用( )法。
A. 直接配法B.间接配制法C. 置换法D. 滴定法E. A 、B 选项均可 37. NaOH 要先配成饱和溶液是因为( )A .由于固体NaOH 易吸收空气中的H 2O 生成Na 2CO 3。
B. 由于固体NaOH 易吸收空气中的H 2CO 3生成Na 2CO 3。
C. 由于固体NaOH 易吸收空气中的CO 2生成Na 2CO 3。
D.由于固体NaOH易吸收空气中的SO2生成Na2SO4。
E. 由于固体NaOH易吸潮。
38. 血浆中CO2结合力的测,可采用()法。
A. 返滴定法B.间接滴定法C. 置换滴定法D. 直接滴定法E. A、B选项均可(二)B型题备选答案在前,试题在后,每组题均对应同一组备选答案,每题只有一个正确答案,每个备选答案可重复选用,也可不选用。
(39~43题共用备选答案)A.NaOH B.HCl C.靛蓝D.甲基橙 E. 酚酞39. 测定碱类化合物的含量,应使用的标准溶液是()。
40. 测定酸类化合物的含量,应使用的标准溶液是()。
41. 测定弱酸含量,选用的指示剂是()。
42. 测定弱碱含量,选用的指示剂是()。
43. 强碱滴定强酸最好的指示剂是()。
(44~48题共用备选答案)A.8.0(无色)~10.0(红色) B. 6.7(黄色)~8.4(红色)C. 3.1(红色)~4.4(黄色) D.2.9(红色)~4.0(黄色)E. 4.4(红色)~6.2(黄色)44. 酚酞指示剂的变色范围及颜色为()45. 甲基橙指示剂的变色范围及颜色为()46. 甲基红指示剂的变色范围及颜色为()47. 酚红指示剂的变色范围及颜色为()48. 甲基黄指示剂的变色范围及颜色为()(三)X型题每题的备选答案中有2个或2个以上正确答案。
少选或多选均不得分。
49. 可作为酸碱滴定法的标准溶液是()。
A.HCL B.NaOH C.HAcD.H2SO4E.NH3·H2O50. 只能用间接方法配制的标准溶液有()A.AgNO3B.NaOH C.NaClD.HCl E.Na2CO351. 影响滴定弱酸的滴定突跃大小因素有()。
A.滴定程序 B. 酸的浓度 C. 酸的电离常数D.指示剂 E. 滴定速度52. 影响指示剂变色范围大小的因素有()A. 速度B. 温度C. 溶剂D.指示剂的用量 E. 滴定程序53. 酸碱滴定法可直接测定哪些物质的含量()。
