第四章谱图解析与化合物结构确定
第4章 四谱综合解析(最初)讲解

第四章 四谱综合解析
§4-2 谱图解析的一般方法
一、摩尔质量和化学式的确定 1. MS法 (1)利用高分辨MS的分子离子峰直接测 定精确的摩尔质量并推断出化学式; (2)用低分辨MS中的分子离子峰及同位 素的M+1、M+2峰和贝农表结合获得摩尔 质量和化学式。
(3)用1H谱获得分子中总H原子数目,与13CNMR谱得到的H数目比较,对无对称性的分 子 1H-NMR 谱 中 获 得 的 H 数 目 减 去 13C-NMR 谱得到的H数目既为与杂原子相连的H数。
第四章 四谱综合解析
(4)用重氢交换法验证与杂原子相连的活 泼氢及其数目;
(5)将1H-NMR谱中获得的各组峰的H数 与13C-NMR谱的基团中H数进行对照调 整,结合摩尔质量,推算出O和其它杂 原子比例。
●MS谱
27
PWBD
§4-3 四谱综合解析示例
解:(1)确定化学式
●将上述4个谱图信息汇总
谱学
C数目
H数目
名称 羰C区:sp2:sp3 总C数 羰C区:sp2:sp3 总H数
13CNMR 1:2:4
7
0:3:9
12
1HNMR 谱图有6组峰 ≥6 (面积)1:2:2:2:2:3 12
IR
谱峰1724、1170、1100cm-1三个峰
m/z
§4-3 四谱综合解析示例
(3)确定结构式
●综合上述分析,该化合物为丁酸烯 丙酯,其结构式为:
H
H
O
C=C
CH3CH2CH2C-O-CH2
核磁共振基本原理和结构鉴定

弛豫(relaxtion)—高能态的核以非辐射的方式回到低能态。
饱和(saturated)—低能态的核等于高能态的核。
在NMR中,弛豫过程有两种方式,即 自旋——晶格弛豫和自旋——自旋弛豫。 自旋——晶格弛豫,又称纵向弛豫,用T1表示; 自旋——自旋弛豫,又称横向弛豫,用T2表示。
第二节 核磁共振与化学位移
h
kT
磁场强度2.3488 T;25C;1H的共振频率与分配比:
共振频率
2
B0
2.68 108 2.3488 100.00MHz
2 3.2434 1.38066
100.00 106 1023 298
J J
s s1 K 1 K
0.999984
两能级上核数目差:1.610-5;
布不均匀,共振吸收复杂,研究应用较少;
(3)I=1/2的原子核
1H,13C,19F,31P 原子核可看作核电荷均
匀分布的球体,并象陀螺一 样自旋,有磁矩产生,是核 磁共振研究的主要对象, C,H也是有机化合物的主要 组成元素。
磁性核在外磁场中的行为 拉莫尔进动
当置于外加磁场H0中时,相对于外磁场,可以有(2I+1)种 自旋取向:I=1/2的核,两种取向(两个能级):
p h I(I 1) 2
自旋量子数(I)与质量数(A)、质子数(Z)、中子数(N)有关:
原子核的磁性
=>
核 磁 矩: p h I (I 1)(:磁旋比) 2
质量数 质子数 (A) (Z)
偶数 偶数
中子数 自旋量子数
(N) (I)
偶数
0
核磁性
实例
无
12C,16O,32S
偶数 奇数
奇数
有机化合物波谱解析第四章 质谱(MS)

电喷雾电离的基本过程 ➢ 电场下的喷雾 ➢ 壳气的作用下 ➢ 电荷的库仑作用 ➢ Rayleigh 极限
Charged Droplets
+ ++
-
+ - -++ -
++
+ +
Evaporation
Rayleigh Limit
Reached
+ +++
+-+--+-- +++
带电雾滴 溶剂的蒸发 带电雾滴的解体 表面张力和库仑斥力的平衡点
• 氩气(Ar)在电离室依靠放电产生氩离子, 高能氩离子经电荷交换得到高能氩原子 流,氩原子打在样品上产生样品离子。 样品置于涂有底物(如甘油)的靶上。 靶材为铜,原子氩打在样品上使其电离 后进入真空,并在电场作用下进入分析 器。
• FAB的优点:
• 电离过程中不必加热气化,因此适合于 分析大分子量、难气化、热稳定性差的 样品。
B + M+
• 加成反应
• BH+ + M
[BHM]+ 或 [BMH]+
ON O N
O
(M.W. 224)
甲糖宁的EI-MS与CI-MS谱比较
化学电离源 分子离子峰
麻黄碱 电子轰击源
• 2.3 场致电离源( Field ionization, FI) • 应用强电场(电压梯度107-108V/cm)诱导样
• 特点:高的灵敏度和专属性
•
可以测定分子量,确定化合物的
分子式。
•
用于推断化合物结构。
第一节 有机质谱仪的工作原理
核磁共振谱图解析与结构确定

对比
2. 谱图解析与结构(1)确定
化合物 C10H12O2
3
2 2
5
8
7
6
5
4
3
2
1
0
谱图解析与结构确定步骤
=1+10+1/2(-12)=5
δ 3.0和δ 4.30三重峰和三重峰 O—CH2CH2—相互偶合峰
δ 2.1单峰三个氢,—CH3峰 结构中有氧原子,可能具有:
δ 7.3芳环上氢,单峰烷基单取代
δ2.3 δ1.2 2H 3H
结构(3)确定过程
化合物 C10H12O2, =1+10+1/2(-12)=5
a. δ 2.32和δ 1.2—CH2CH3相互偶合峰 b. δ 7.3芳环上氢,单峰烷基单取代
c. δ 5.21—CH2上氢,低场与电负性基团相连
哪个正确 a O
b
CH2 C O CH2CH3 A
质子a与质子b 所处的化学环境不 同,两个单峰。 单峰:没有相邻碳 原子(或相邻碳原 子无质子)
质子b直接与吸电子元素相连,产生去屏蔽效应,峰在低 场(相对与质子a )出现。
质子b也受其影响,峰也向低场位移。
谱图解析( 3 )
裂分与位移
谱图解析( 4 )
苯环上的质子在低场出现。为什么? 为什么1H比6H的化学位移大?
最后解析:芳烃质子和其它质子
• 活泼氢D2O交换,解析消失的信号 • 由化学位移,偶合常数和峰数目用一级谱解析
• 参考 IR,UV,MS和其它数据推断解构
• 得出结论,验证解构
1. 谱图解析(1)
6个质子处于完全相同的化学环境,单峰。 没有直接与吸电子基团(或元素)相连,在高场出现。
波谱解析 第四章 碳谱作业参考答案
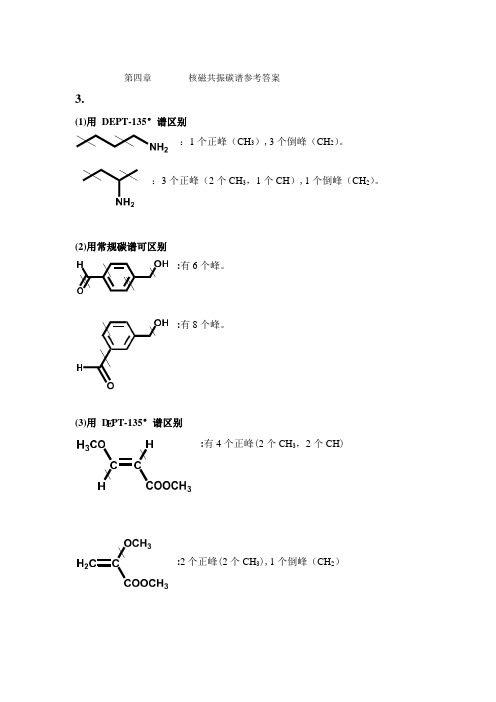
E : (3)用 D PT-135°谱区别 第四章 核磁共振碳谱参考答案3.(1)用 DEPT-135°谱区别:1 个正峰(CH 3),3 个倒峰(CH 2)。
:3 个正峰(2 个 CH 3,1 个CH ),1 个倒峰(CH 2)。
(2)用常规碳谱可区别:有 6 个峰。
有 8 个峰。
:有 4 个正峰(2 个 CH 3,2 个 CH ):2 个正峰(2 个 CH 3),1 个倒峰(CH 2)6.1)由分子式C5H9O2Br 计算不饱和度Ω=1,结构中可能含一个双键或一个环。
2)1H NMR 解析:1.25(t):CH x-CH2- ;2.85(t): 弱吸电子基团-CH y-CH2- ;3.55(t): 弱吸电子基团-CH z-CH2- ;4.20(q): -CO2-CH m-CH3(该基团CH m必定与吸电子基团相连。
根据化学位移和分子式可初步判断是与酯基氧原子相连) 3)13C NMR 解析:共有五条峰,与结构式中碳数一致,说明分子中不含对称元素。
178.2(s): 羧酸或其衍生物的C=O;60.8(t): -CH2-,与氧原子相连37.8(s): -CH2-,可能与弱吸电子原子相连26.5(t): -CH2-,可能与弱吸电子原子相连14.2(q): -CH34)推断过程:碳谱表明分子中有1 个羰基,3 个亚甲基和1 个甲基,因此氢谱中4.20ppm 处必定为亚甲基,所以分子中含CO2CH2CH3片段,再结合氢谱,该片段中CH3出峰应该在1.25ppm 处。
这样一来,可以进一步推断2.85 和3.55ppm 处的信号必然是剩余两个亚甲基,由于都为t 峰,这两个亚甲基必定相连,所以推测出分子含有片段CH2CH2,且两端都连有弱吸电子基团。
至此,分子中含有如下片段:一个B(r(端基),因此该化合物的结构为:端基),一个CH2CH2,一个CO2CH2CH38.1)由分子式C8H5NO2可算出不饱和度Ω=7,结构中可能含有苯环。
红外吸收光谱分析法 红外谱图解析

顺式烯 乙烯基烯 亚乙烯基烯
08:12:21
R1 H R1 H R1 R2
1660cm-1
1660-1630cm-1
中强,尖
总结
ⅰ 分界线1660cm-1 ⅱ 顺强,反弱
ⅲ 四取代(不与O,N等相连)无υ
ⅳ 端烯的强度强
(C=C)峰
ⅴ共轭使υ
下降20-30 cm-1 (C=C)
H C C R R1 C C R2
08:12:21
υ υ
C C
2140-2100cm-1 (弱) 2260-2190 cm-1 (弱)
C C
c)C-H 变形振动(1000-700 cm-1 )
面内变形(=C-H)1400-1420 cm-1 (弱) 面外变形(=C-H) 1000-700 cm-1 (有价值)
R1 H R1 R2 R1 R2 C C R4
O—H,C—O
a)-OH 伸缩振动(>3600 cm-1) b)碳氧伸缩振动(1100 cm-1)
C Cα C Cα′ C C Cα″ β
υ
(C-O)
OH
υ
游 离 仲-OH 醇, 叔-OH 酚 酚-OH 伯-OH
(—OH) 3640cm-1 3630cm-1 3620cm-1 3610cm-1
1050 cm-1 1100 cm-1 1150 cm-1 1200 cm-1
第四章 红外吸收光谱分 析法
infrared absorption spec-troscopy,IR
一、红外谱图解析
analysis of infrared spectrograph
二、未知物结构确定
structure determination of compounds
核磁共振H谱图解析与结构确定
δ 7.3芳环上氢,单峰烷基单取代
ab
Oc
正确结构:
CH 2CH 2OC CH 3
δ3.0 δ 4.30
δ2.1
2020/7/2
谱图解析与结构确定(2)
C7H16O3,推断其结构
9
δ 5.30 1
δ 3.38 δ 1.37 6
2020/7/2
结构确定(2)
C7H16O3,u=1+7+1/2(-16)=0 u=1+n4 + 1/2(n3-n1)
2020/7/2
1H—NMR图谱的解析大体程序为: (1)首先注意检查TMS信号是否正常; (2)根据积分曲线算出各个信号对应的H数; (3)解释低磁场处(δ10~16)出现的—COOH及
具有分子内氢键缔合的—OH基信号; (4)参考化学位移、小峰数目及偶合常数,解释低
级偶合系统; (5)解释芳香氢核信号及高级偶合系统; (6)对推测出的结构,结合化学法或利用UV、IR、
化合物 C10H12O2
3
2
2
5
8
7
6
5
4
3
2020/7/2
2
1
0
谱图解析与结构确定(1)
u=1+10+1/2(-12)=5,
u=1+n4 + 1/2(n3-n1)
δ 3.0和δ 4.30三重峰和三重峰 O—CH2CH2—相互偶合峰
δ 2.1单峰三个氢,—CH3峰 结构中有氧原子,可能具有:
O C CH3
2020/7/2
一、谱图中化合物的结构信息
(1)峰的数目:标志分子中磁不等性质子的种类,
多少种;
(2)峰的强度(面积):每类质子的数目(相对),
有机化学课件 第二版 高占先主编 (第4章 结构的表征)

â × ¸ Æ
Ö Ó Ë ¯ ¹ ¼ ¯ ¢ ñ ¯ ¢ ª ¯ ¢ Ë â ç Ó Ë ¯ È ·×Ô ¶ £ Æ ¶ ¡ Õ ¶ ¡ ׶ ¡ ¹ Í µ ×Ô ¶ µ £ ¾ Ó ¯ Ä ¨Ü ¾ ä ¯ º ¬ ø £ Á ׺ µ £ Ä Á ±º ² Á Ð © ¾ ö Ö Ó Ð º Ü æ Ú º ¨ý ¾ Ä ª à · ·×Ö Ö Ä ´ Ô Ò ¶ Ê Á µ ×é ¯ ¢ ñ ¯ ¡ ç Ó ½ ¨Ü ¶ ¶ ¡ Õ ¶ ¢ µ ×Ô Ç Ä »
4.2.1 基 本 原 理
1. 分子振动的类型 (1)伸缩振动
成键的两原子沿键轴方向伸长和缩短的振动
称为伸缩振动,常用ν 表示。
振动频率(近似地按简谐运动处理)
振动频率ν 与两原子的质量m1、m2、 键的力常数 k 有关:
或用波数σ 表示为:
①键的力常数k与键能有关,键能大,力常数
大,振动频率也大。
d
化学位移
10
6
为什么选用TMS(四甲基硅烷)作为标准物质?
绝大多数吸收峰均出现在它的左边。 (2)结构对称,是一个单峰。 (3)容易回收(b.p低),与样品不反应、不缔合。
(1)屏蔽效应强,共振信号在高场区(δ 值规定为0),
例:在60MHz的仪器上,测得氯仿与TMS间吸收 频率差为437Hz,用δ 表示氢的化学位移为
•
各种官能团的红外吸收频率汇于下表:
4.2.3 红外吸收光谱图及其解析
1. 红外吸收光谱图
cm
1
1
横坐标:波长/λ或波数/cm-1。
m
10
4
A log(
1 T
)
纵坐标:吸光度A或透光率T。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(3) AMX系统
νA
νM
νX
三个相互偶合的核, 各核间的化学位移差
JAX
JMX
JAX
值均远大于任意一个J。 JAM
JAM
JMX
画法1
△AM 》 J AM ,
νA
νM
νX
△ Ax 》 J Ax , (1)有12条谱线, A、M、X各占4条,强度接近。
△ MX 》 J MX , (2)12条谱线有三种和三种J。
(3)每组四重峰的中点为该核的化学位移。
JAM JAX
JAM JMX
JMX JAX
νA 画法2
νM
νX
AMX系统
第四章谱图解析与化合物结构确定
O
HX Ph
X
JMX JAX
HA HM
X = 3. 69,
A
JAM JAX
A = 2. 96 , M = 2. 61
M
JAM JMX
3.5
3.0
2.5
氧化苯乙烯裂分系统
νB
A JAX
X JAX
νA
νX
第四章谱图解析与化合物结构确定
特征: 9条峰,A4条(1-4), B4条(5-8), 一条综合峰;
△ν / J = 2.0 4
3 2 1
νA
56
7 8 9
νB
谱线的位置及相对强度随△ν/ J值的不同而发生变化;
5、6线,7、8线往往合并在一起,呈较宽的单峰。
解析: (a) 读出ν1ν2 ……ν7ν8 (b) JAB =1/3[(ν1-ν4)+ (ν6-ν8)] (c) νA =ν3 (d) νB =1/2(ν5 +ν7 )
第四章谱图解析与化合物结构确定
2、高级谱
△ν/J < 6 时,互相偶合作用强,峰形发生畸变。 高级谱: AB 、AB2、ABX、A2B2、AB3 、A2B3 特点: 和J不能直接量出而要通过计算得到;
谱线数目超出n+1规律的计算数目; 裂分峰的相对强度关系复杂。
JAX
△ν > 6 J
JAX
JAB
△ν =3 J
AB系统
(a) JAB = ν1 -ν2 =ν3 -ν4
A
B
(b) △νAB = [( D +JAB )( D -JAB )]1/2
= [(ν1-ν4 )(ν2-ν3 )]1/2
D D
C = 1/2 [(ν1-ν4 ) - △νAB ]
JAB
JAB
νA = ν1 – C; νB = ν4 + C
ν1
第四章谱图解析与化合物结构确定
(4) AB系统
A
B
D JAB
D JAB
ν1
νA ν2 ν3 νB
ν4
C
C
νAB
A
X
JAX
νA
JAX
νX
特点:四条谱线,A、B各两条,两线间隔等于偶合常数JAB; 四条谱线高度不相等,内侧两条线高于外测两条, νA和νB不在所属两线的中心,需计算求出。
第四章谱图解析与化合物结构确定
νA ν2 ν3 νB
ቤተ መጻሕፍቲ ባይዱ
ν4
C
C
νAB
(c) 峰的强度比
I1=I4 I2=I3
I1 I2
=
I4 I3
= D - JAB D +JAB
= ν 2 -ν3 ν 1 -ν4
注意: 解析 A B 四重峰时谱线不能交叉,即1、2 线属于 A 核, 3、4 线属于B 核,2、3 线不能互换 124
,
第四章谱图解析与化合物结构确定
A
X
JAX
νA
JAX
νX
第四章谱图解析与化合物结构确定
(2)AX2系统
A JAX
νA
X
五条线
JAX
A 三条 1:2:1 X 两条 1:1
三重峰和双峰的裂距大小等
于偶合常数JAX。 各组峰的中心即化学位移。
νX
CH2
Ha Cl C
Cl
HX C Cl HX
CH
6
5
4
CHCl2 CH2Cl的核磁共振
第四章谱图解析与化合物结构确定
常见的AB系统:(偕偶、具有重键的邻偶)
HA
C=C
HB
HB
HA
C=C
HA
HA
C=C
HB
HB
例
第四章谱图解析与化合物结构确定
(5) AB2系统
AX2系统中随着νA 、νB 差值减小,转变成AB2系统
△ν / J = 0.3
4 23 1
νA
△ν / J = 2.0
4
3
2 1
νA
56
7 8
νB
56
7 8 9
JAB
A
X
△ν < J
A
B
△ν =0
第四章谱图解析与化合物结构确定
3、常见 的自旋系统
(1) AX系统
(a) AX系统有四条线, A、X各为两重峰; (b) 两峰之间裂距为偶合常数JAX; (c) 各组双重峰的中点为该核的化学位移; (d) 四条谱线高度相等,峰形无畸变。
(H-F、HC = CF、HCCl2F)
第四章 核磁共振波 谱分析法
第六节 谱图解析与化合物
结构确定
一、核磁共振谱图的类型
二、解析分子谱图的特殊 技术-简化谱图法
三、1H NMR谱图一般步 骤
四、谱图解析与结构确定
第四章谱图解析与化 合物结构确定
一、核磁共振图谱的类型
1.一级谱 (1) 一级谱的条件 (a)一个自旋体系中的两组质子 △ν/J ≥ 6。 (b)在自旋体系中同一组质子的各个质子必须是磁等价的。 (2) 一级谱的规律 (a) 磁等价的质子之间有偶合,但不裂分。 (b) 磁不等价的质子之间有偶合,裂分峰数目符合n+1规律。 (c) 裂分峰强度比相当于 (a+b)n 展开式的系数比 (d) 裂分峰以该质子化学位移为中心,峰形左右对称。 (e) 偶合常数可从图上直接读出来。 (f) 不同类型质子积分面积之比等于质子的个数之比。
421.5, 420.5, 414, 412.5
N
JAB = 1/3[(ν1-ν4)+ (ν6-ν8)] H3C
CH3
= 1/3(15.5+8) = 8Hz
νA = ν3 = 447Hz νB = 1/2(ν5 +ν7 ) = 417.8 Hz
2,6-二甲基吡啶
A = νA /仪器兆周数 = 447 /60 = 7.45 ppm B = νA /仪器兆周数 = 417.8 /60 = 6.96 ppm
谱线间距离的规律: ν1 –ν2 = ν3 –ν4 = ν6 –ν7 ν1 –ν3 = ν2 –ν4 = ν5 –ν8 ν3 –ν6 = ν4 –ν7 = ν8 –ν9
第四章谱图解析与化合物结构确定
吡啶环上三个氢构成典型的AB2系统。8条峰,按由左至右, 频率ν1~ν8
456, 449.5, 447, 440.5,
第四章谱图解析与化合物结构确定
常见的AB2系统:
OH
A OH
B
B
OH
A
B
B
R
R
R
A
B
B
R
N
R
CH - CH2
A B2
B
AB
CH – CH - CH
第四章谱图解析与化合物结构确定
芳香质子偶合系统共振谱
R
大多为高级谱,经验规则:
(1)当单取代苯的取代基无强烈的屏蔽或去屏
蔽效应时,图上出现5个芳氢的单峰。
