硫酸头孢喹肟注射液质量标准
猪肌肉注射硫酸头孢喹肟注射液的安全性试验

猪肌肉注射硫酸头孢喹肟注射液的安全性试验岳永波;吴好庭;杨国辉;杨芳;王德功【期刊名称】《畜牧与兽医》【年(卷),期】2008(40)6【摘要】本试验对硫酸头孢喹肟进行了大、小鼠经口的急性毒性试验和猪肌肉注射硫酸头孢喹肟的安全性研究。
选用SD大鼠和ICR小鼠各30只,其经口LD50均大于5000mg/kg。
随机挑选健康猪12头,分为3组,按2mg/kg、6mg/kg和10mg/kg剂量颈部肌肉注射硫酸头孢喹肟注射液,每日1次,连续5d。
对其给药前后的血常规和血液生化指标分析比较,并每天观察给药后动物临床表现。
试验结果显示:硫酸头孢喹肟注射液在2~10mg/kg剂量范围对猪血液生理生化指标无显著影响(P〉0.05),所有动物给药后采食、行动、呼吸和排泄均未见异常,注射部位未见肿胀结块等现象,除10mg/kg剂量组动物出现短时疼痛反应外,未观察到任何不良反应。
【总页数】3页(P76-78)【关键词】硫酸头孢喹肟;LD50;猪;肌肉注射;安全性【作者】岳永波;吴好庭;杨国辉;杨芳;王德功【作者单位】河北远征药业有限公司,河北石家庄050041;中国兽医药品监察所,北京100081【正文语种】中文【中图分类】S852【相关文献】1.猪单剂量肌注硫酸头孢喹肟注射液的药物代谢动力学 [J], 李生其;杨海峰;陆广富;蒋春茂;朱善元2.HPLC法测定硫酸头孢喹肟注射液中硫酸头孢喹肟含量 [J], 李勇军;杨海峰;蒋春茂;于生兰;张成;金礼琴;朱雄3.硫酸头孢喹肟注射液对猪传染性胸膜肺炎的治疗效果 [J], 刘元秋;王涛;王玉金4.硫酸头孢喹肟注射液在猪体内的药代动力学及生物等效性研究 [J], 郭亚楠;周德刚;李建成;江海洋5.硫酸头孢喹肟注射液在猪体内的生物等效性研究 [J], 李龙飞; 孔梅; 郑莉; 陈玲; 冯言言; 常雪; 崔进; 吴连勇因版权原因,仅展示原文概要,查看原文内容请购买。
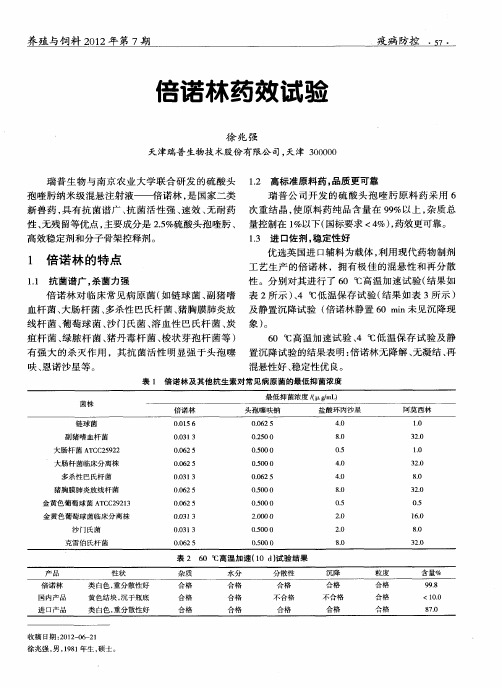
倍诺林药效试验
2 倍 诺 林 的 临 床应 用研 究
一 是使用前认真 阅读产 品说 明书 ;二是使用前 应 充 分摇 匀 ;三 是 对 p一内酰 胺 类抗 生 素 过敏 者 勿
2.1 适应 症
接 触本 品。
1)猪 病 。适 用 于敏感菌 引起 的感 染性 疾病 的预痢 、
好 ,对注射部位 的刺激性更小 ,有效成分更 易于扩
2)牛病 。乳房炎、子宫内膜炎、细菌性肺炎 、肠
散 与 渗透 ,显著 提高 了药 物生物 利用 度 。
道感 染及 全身感 染 性疾病 的预防 和治疗 。
1.5 速 效 与长效 的 完美结 合
2.2 用法 用量
采 用纳 米混 悬 技术 ,改 变药 物 吸收 代谢 过 程 ,
1)猪 。肌 肉注射 ,小猪 0.08 mL/kg体重 ,母猪及
实现速效和长效的完美结合。肌肉注射 l5~60 min 中大猪 0.04 mL/kg体重 ,每 日 1次 ,连用 3 d。
即可达 到 血药 浓 度 峰值 ,并 在靶 部 位 (如肺 脏 、消 化
2)牛 。 治 疗 细 菌 感 染 性 疾 病 ,肌 肉注 射 ,O.04
瑞 普 公 司 开 发 的硫 酸 头 孢 喹 肟 原 料 药 采 用 6
新 兽 药 ,具 有 抗 菌 谱 广 、抗 菌 活性 强 、速 效 、无 耐 药 次重结晶 ,使原料药纯品含量在 99%以上 ,杂质总
性 、无残留等优点 ,主要成分是 2.5%硫 酸头孢喹肟 、 量控 制在 1%以下 (国标要 求 <4%),药效更 可靠 。
高 效稳 定 剂 和分子 骨架 控 释剂 。
1.3 进 口佐 剂 ,稳定 性好
1 倍 诺 林 的特 点
头孢噻呋注射液质量标准、标签和说明书

一、头孢噻呋注射液质量标准、标签和说明书(一)头孢噻呋注射液质量标准头孢噻呋注射液Toubaosaifu ZhusheyeCeftiofur Injection本品为头孢噻呋、大豆油和硬脂酸铝制成的无菌混悬液,含头孢噻呋(C19H17N5O7S3)应为标示量的90.0%~110.0%。
【性状】本品为细微颗粒的混悬液,静置后细微颗粒下沉,振摇后成均匀的灰白色至灰褐色的混悬液。
【鉴别】在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
【检查】有关物质照含量测定项下的方法,取含量测定项下的下层溶液作为供试品溶液;精密量取供试品溶液1ml,置50ml量瓶中,用0.05mol/L醋酸铵溶液稀释至刻度,摇匀,作为对照溶液。
取供试品溶液与对照溶液各20μl注入液相色谱仪,记录色谱图至主峰保留时间的2倍。
供试品溶液的色谱图中如有杂质峰,各杂质峰面积的和不得大于对照溶液主峰面积的1.5倍(3%)。
供试品溶液中任何小于对照溶液主峰面积0.1倍的色谱峰可忽略不计。
粒度取本品,摇匀后,照粒度和粒度分布测定法(附录98页第一法)测定,含15µm 以下的颗粒不得少于90%,不得有50µm以上的颗粒。
沉降体积比取本品适量,用力振摇1分钟,用具塞量筒量取供试品50ml,密塞,用力振摇30秒,记下混悬物的开始高度H0,静置3小时,记下混悬物的最终高度H,沉降体积比(H/H0)应不低于0.90(附录16页)。
无菌取本品适量混匀,分别取30ml和青霉素酶溶液适量(每1mg头孢噻呋加青霉素酶不得少于2万单位)加入到含6%吐温-80的硫乙醇酸盐培养基270ml和含6%吐温-80的改良马丁培养基270ml中,摇匀,置37℃恒温水浴中1小时作为供试品溶液,依法检查(附录137页),结果应符合规定。
其它应符合注射剂项下有关的各项规定(附录6页)。
【含量测定】照高效液相色谱法(附录36页)测定。
动物专用第四代头孢类抗生素——头孢喹肟

兽用第四代头孢菌素-头孢喹肟研究进展邢桂珍浙江海正药业股份有限公司浙江海正药业有限公司研发的硫酸头孢喹肟注射液是目前唯一一个动物专用第四代头孢类抗生素,具有抗菌谱广,抗菌活性强的特点。
其原料和制剂在国内最早被授予国家二类新兽药证书。
本文就该药的抗菌机制、药效、药代、毒理、残留、安全性和临床应用的研究进展做一概述。
1、抗菌机制硫酸头孢喹肟独特的双极性分子结构:头孢母核的7位为甲氧亚胺基-5-氨基噻唑取代基,其为抗菌活性的必需基团,和第三代头孢菌素不同的是其母核的3位有一个季铵盐基团,即头孢喹肟是一个两性离子,头孢核带负电核,四价季铵离子基团带正电核。
硫酸头孢喹肟的结构决定它具有如下特点:(1)可快速穿透革兰氏阴性细菌的外膜;(2)对β内酰胺酶稳定且亲合力低(细菌产生作用于青霉素类和头孢菌素类的β-内酰胺环而使其药效降低);(3)与青霉素结合蛋白(PBPS是药物作用于细菌细胞壁的靶位点,药物与其结合可阻止细菌细胞壁的合成,而起到杀菌作用)亲合力高;(4)其内在抗菌活性强于第三代头孢菌素。
与第三代头孢相比,四代头孢的血浆半衰期长,无肾毒性。
2、药效学中国农大对我公司生产的硫酸头孢喹肟进行了微生物敏感性试验,主要是对几种常见畜禽病原菌的体外抗菌试验。
结果显示硫酸头孢喹肟对金黄色葡萄球菌的最小抑菌浓度(MIC)范围在1~2 μg/mL之间,对氨苄西林和环丙沙星耐药的金黄色葡萄球菌菌株仍有抑制作用,对大肠杆菌的MIC范围在≤0.031~0.25 μg/mL 之间,对链球菌(包括无乳和停乳链球菌)的MIC范围在≤0.031~0.125 μg/mL 之间,对多杀巴氏杆菌的MIC范围在≤0.031~0.5 μg/mL之间,对胸膜肺炎放线杆菌的MIC≤0.031 μg/mL。
硫酸头孢喹肟对上述几种常见畜禽病原菌的抗菌活性较强。
国外也有很多关于头孢喹肟药效学的研究,Guerin-Faudee等研究了头孢喹肟等抗生素对引起奶牛乳房炎的G+菌、G-菌的抗菌活性,结果表明:头孢喹肟对大肠杆菌的MIC范围在≤0.016~0.25 μg/mL之间,对各种链球菌(包括无乳和停乳链球菌)的MIC50值为0.03μg/mL,MIC90值为0.25μg/mL,Rose等研究了头孢喹肟对从牛呼吸系统中分离的107株溶血性巴氏杆菌、117株多杀性巴氏杆菌的抗菌活性,结果显示:头孢喹肟对溶血性巴氏杆菌的MIC50、MIC90值分别为0.03μg/ml和0.06μg/ml,对多杀性巴氏杆菌的MIC50、MIC90值分别为0.03μg/ml和0.5μg/ml。
头孢喹肟的质量鉴别实用方法及最新临床应用价值

猪病防控Swine DiseasePrevention and Control2018年第5期头孢喹肟的质量鉴别实用方法及最新临床应用价值郭建军李凌峰郝小倩李灵娟*(河南牧翔动物药业有限公司国家企业技术中心,河南郑州450000)摘要:头孢类抗生素是兽医临床常用的药物品类之一,目前已经更新至第四代。
其中硫酸头孢喹肟作为第四代头孢类代表药物,药效在第一代基础上显著提升,安全性更好,抗菌谱更广,几乎无过敏反应,对酸和酶的耐受性更强。
混悬注射液是目前市场上的主流剂型;产品的优劣可以通过颜色、气味、溶解泡沫、沉降性、分散性、眼观颗粒、挂壁特征、通针性和包装颜色等特征加以鉴别;除了细菌性感染疾病的治疗外,治疗性诊断也是头孢喹肟重要应用价值之一。
关键词:头孢喹肟;治疗性诊断;鉴别;抗生素中图分类号:S859.7文献标识码:B文章编号院1673-4645(2018)05-0044-03头孢类抗生素在兽医临床领域应用广泛,目前已经 更新迭代至第四代,由于抗菌性能强,对感染性疾病的 治疗效果确切,深受养殖企业的欢迎。
为了让业内更好 认识本类药物,笔者着重以目前应用较多的动物专用第 四代头孢类抗生素一硫酸头孢喹肟为话题做一论述。
1头孢类抗生素头孢类抗生素归属于P-内酰胺类,是一种广谱的 半合成抗生素。
从第一代头孢类药物一头孢噻吩、头 孢氨苄等开始,目前已经发展至第四代。
其中第二代药 物主要有头孢曲松、头孢呋辛等,第三代药物主要有业 内熟知的头孢哌酮和头孢噻呋等,第四代药物主要为头 孢喹肟和头孢吡肟,其中头孢喹肟为动物专用,目前已 得到批准的剂型有混悬注射剂和注射用粉针。
从第一代 发展至第四代,头孢类药物的杀菌力不断增强,抗菌谱 更广,安全性大大提高,过敏反应几率降低,对酸和酶 更加耐受,药效更为确实。
和第一代头孢类药物相比,第四代头孢类药物头孢喹肟的肾毒性几乎消失,除了革兰氏阳性菌外,对致病 性大肠埃希菌、沙门氏菌、副猪嗜血杆菌、巴氏杆菌以 及传染性胸膜肺炎放线菌等革兰氏阴性菌的抗菌作用也 非常卓越,且药物耐酸,对P-内酰胺酶稳定,对动物 少有过敏和应激反应,是目前最新的动物专用头孢类抗 生素。
一种硫酸头孢喹肟注射液及其低温高剪切制备方法[发明专利]
![一种硫酸头孢喹肟注射液及其低温高剪切制备方法[发明专利]](https://img.taocdn.com/s3/m/a57a4a5f65ce0508763213ee.png)
专利名称:一种硫酸头孢喹肟注射液及其低温高剪切制备方法专利类型:发明专利
发明人:廖陶雪,方炳虎,程含波,黄国进
申请号:CN201710518913.6
申请日:20170630
公开号:CN107334730A
公开日:
20171110
专利内容由知识产权出版社提供
摘要:本发明公开了一种硫酸头孢喹肟注射液及其低温高剪切制备方法,该注射液包括如下质量百分比的组分:硫酸头孢喹肟2.25~2.75%、卵磷脂0.9~1.1%、硬脂酸铝1.8~2.2%、余量为油酸乙酯。
制备时,将硫酸头孢喹肟进行低温高剪切得到超细微悬浮液,然后通过胶体磨均质,最终制得硫酸头孢喹肟注射液。
与现有技术相比,本发明采用低温高剪切制备方法,剪切时药液温度控制在
2~8℃,最终得到的产品按照质量标准进行检测,各项检测指标均符合规定,“有关物质”检测项各杂质峰面积的和小于对照溶液主峰面积的3倍(3.0%),且产品收率更高,制备步骤简便,易操作。
申请人:广东温氏大华农生物科技有限公司
地址:527400 广东省云浮市新兴县新城镇东堤北路6号
国籍:CN
代理机构:桂林市华杰专利商标事务所有限责任公司
代理人:杨雪梅
更多信息请下载全文后查看。
一种长效硫酸头孢喹肟注射液及其制备方法[发明专利]
![一种长效硫酸头孢喹肟注射液及其制备方法[发明专利]](https://img.taocdn.com/s3/m/c791c2250a4e767f5acfa1c7aa00b52acec79c41.png)
(19)中华人民共和国国家知识产权局(12)发明专利申请(10)申请公布号 (43)申请公布日 (21)申请号 201710536736.4(22)申请日 2017.07.04(71)申请人 江西傲新生物科技有限公司地址 333100 江西省上饶市鄱阳县芦田轻工产业基地申请人 福建傲农生物科技集团股份有限公司(72)发明人 胡鹏飞 戴多亮 黄静 吴有林 梁世仁 周盛昌 王丽娜 (74)专利代理机构 上海科盛知识产权代理有限公司 31225代理人 王小荣(51)Int.Cl.A61K 9/10(2006.01)A61K 31/546(2006.01)A61K 47/14(2006.01)A61K 47/44(2017.01)A61K 47/38(2006.01)A61K 47/34(2017.01)A61P 31/04(2006.01)(54)发明名称一种长效硫酸头孢喹肟注射液及其制备方法(57)摘要本发明涉及一种长效硫酸头孢喹肟注射液及其制备方法,注射液包括以下组分及重量份含量:硫酸头孢喹肟2-3份、助悬剂2-3份、稳定剂0.5-1份、抗氧化剂0.2-0.4份、聚乳酸-羟基乙酸共聚物0.2-0.4份、交联剂0.3-0.7份、pH稳定剂1-1.5份以及分散媒80-120份;制备时,先将助悬剂、稳定剂、抗氧化剂、聚乳酸-羟基乙酸共聚物、交联剂及pH稳定剂加入至分散媒中,冷却后加入硫酸头孢喹肟,研磨即可。
与现有技术相比,本发明提高了注射液的稳定性及分散性,延长了药效代谢时间,肌肉注射后缓慢释放,血药浓度平稳,一次注射便能够达到同品种常规剂型多次间隔注射的同样效果,减少了用药次数,降低了用药成本及人工成本,避免了应激反应的发生,易于保存。
权利要求书1页 说明书6页CN 107260666 A 2017.10.20C N 107260666A1.一种长效硫酸头孢喹肟注射液,其特征在于,该注射液包括以下组分及重量份含量:硫酸头孢喹肟2-3份、助悬剂2-3份、稳定剂0.5-1份、抗氧化剂0.2-0.4份、聚乳酸-羟基乙酸共聚物0.2-0.4份、交联剂0.3-0.7份、pH稳定剂1-1.5份以及分散媒80-120份。
硫酸头孢喹肟注射液质量标准

硫酸头孢喹肟注射液质量标准硫酸头孢喹肟注射液本品为硫酸头孢喹肟与油酸乙酯等配制而成的混悬注射液。
含头孢喹肟(CHNOS)应为标示量的232465290.0%~105.0%。
【性状】本品为类白色至浅褐色混悬液体;久置分层。
【鉴别】(1)含量测定项下记录的色谱图中,供试品主峰的保留时间应与对照品峰的保留时间一致。
(2)取摇匀后的供试品2 ml,加水5 ml,稀盐酸1 ml,混匀,置超声浴中超声10分钟,弃去有机层,溶液显硫酸盐的鉴别反应(附录15页)。
【检查】有关物质照含量测定项下的方法。
取摇匀后的供试品1.0 ml,加入流动相25.0 ml,置超声浴中超声5分钟,弃去有机层,取水层滤过,取续滤液10µl,注入液相色谱仪,记录色谱图,2,3-环己基吡啶与头孢喹肟相对保留时间为0.20。
按峰面积归一化法计算,2,3-环己基吡啶应不得过3.0%,其他单一杂质应不得过0.50%,杂质总量应不得过4.0%。
水分取本品,照水分测定法(附录58页,第一法)检查,含水分不得过0.2%。
细菌内毒素取摇匀后的供试品2 ml与细菌内毒素检查用水3 ml混匀,分成2等份,振摇30秒,离心15分钟(2000g),吸取水层1 ml,加1 mol/L氢氧化钠溶液0.06 ml调节pH值至6.5~7.5。
用细菌内毒素检查用水按1:10稀释后,照细菌内毒素检查法(附录73页)检查,每1 mg头孢喹肟中含细菌内毒素的量应小于0.1 EU。
6无菌取供试品8瓶,混合均匀,加入含6%吐温-80的蛋白胨缓冲液(1g/L)400ml,混匀,加入800×106单位青霉素酶(每1ml供试品溶液,加2×10单位青霉素酶),充分振摇,将供试品倒置,在37?放置4小时;取供试品溶液,依法检查(附录79页,直接接种法),应符合规定。
分散性取本品1瓶,振摇30秒,将供试品转移置玻璃容器中,不得观察到结块或沉淀物。
沉降取本品1瓶,振摇30秒,取供试品10 ml置刻度试管中(内径1.0~1.5 cm),10分钟内不得沉淀。
一种兽用长效硫酸头孢喹肟注射液及其制备方法[发明专利]
![一种兽用长效硫酸头孢喹肟注射液及其制备方法[发明专利]](https://img.taocdn.com/s3/m/a6ec8231195f312b3069a5dd.png)
专利名称:一种兽用长效硫酸头孢喹肟注射液及其制备方法专利类型:发明专利
发明人:张卫元,陈翠兰,操继跃,刘国庆,张永丹,肖飞,张翠平申请号:CN201110293232.7
申请日:20110929
公开号:CN102319210A
公开日:
20120118
专利内容由知识产权出版社提供
摘要:本发明涉及动物药品技术领域,具体公开了一种兽用长效硫酸头孢喹肟注射液及其制备方法。
每100mL该注射液由2.5-7.5g硫酸头孢喹肟、0.2-0.4g助悬剂、0.4g抑菌剂、0.3g乳化分散剂和余量的溶媒组成。
制备方法为首先将硫酸头孢喹肟加入溶媒中,搅拌使之充分混匀;然后将助悬剂加入90-100℃的溶媒中溶解;将第二步的溶解液冷却至室温后加入正在搅拌的第一步的混悬液中,搅拌均匀;再加入抑菌剂和乳化分散剂至第三步的混悬液中,充分搅拌;最后加入剩余量的溶媒,搅拌混匀,依次过高速剪切分散机和胶体磨,辐照灭菌后制得产品。
猪肌内注射该产品后消除半衰期长,可延长药物在体内的有效作用时间,减少用药次数。
申请人:武汉回盛生物科技有限公司
地址:430042 湖北省武汉市东西湖区张柏路208号
国籍:CN
代理机构:武汉宇晨专利事务所
更多信息请下载全文后查看。
硫酸头孢喹肟注射液质量标准

硫酸头孢喹肟注射液质量标准1. 引言大家好,今天咱们聊聊一个在医学界可是“扛把子”的药物——硫酸头孢喹肟注射液。
听名字就有点拗口,对吧?但是它的作用可是一点都不含糊。
简单来说,这个药物主要用于治疗各种细菌感染,简直就是医院里医生的“神兵利器”。
所以,咱们有必要了解一下它的质量标准,毕竟“药三分毒”,咱可不能让不合格的药物害了自己。
2. 硫酸头孢喹肟的基本信息2.1 药物成分硫酸头孢喹肟,嗯,乍一听就让人觉得有点“高大上”。
它属于头孢类抗生素,主要成分是头孢喹肟。
这个家伙在对抗细菌方面,简直就像超级英雄一样,能够快速消灭各种不速之客,比如说肺炎链球菌、葡萄球菌之类的。
这种药物在体内的作用可不是一时半会儿就能解决的,而是需要在医生的指导下慢慢发挥它的威力。
2.2 使用场合那么,这个药物适合什么样的患者呢?其实啊,它通常用于治疗那些因为细菌感染而引起的肺炎、尿路感染等,简直是“药到病除”的典范。
但有些人一听到“注射液”就打退堂鼓,觉得针头刺得慌,实际上,注射方式能够让药物更快发挥作用,效果更明显。
说到底,打针虽然让人心里发怵,但为了健康,咱们也得勇敢一点,对吧?3. 质量标准的重要性3.1 为什么要有质量标准说到质量标准,大家可能会觉得这是一件“老生常谈”的事。
但真心告诉你,这个标准可重要得很。
没有质量标准,就像没有规矩的方圆,药物的质量可能会参差不齐,直接影响到咱们的身体健康。
想象一下,如果你吃了不合格的药,那可真是“得不偿失”。
所以,国家对药物的质量控制可谓是严格得像“保姆”一样,让每一位患者都能放心用药。
3.2 具体的质量标准具体来说,硫酸头孢喹肟注射液的质量标准包括几个方面。
首先,药品的纯度必须达到一定的比例,通常在95%以上,这样才能确保它的疗效。
其次,药物的稳定性也得过关,避免在运输或者保存过程中变质。
此外,药物的外观、pH值、含量均匀性等都需要符合相关的标准,确保在使用时是“安全无忧”的。
20mL西林瓶对硫酸头孢喹肟注射液质量稳定性影响的研究

摘要:本试验对20mL 硫酸头孢喹肟注射液进行了包材相容性试验考察,通过对各个考察节点检测项检测数据的分析来确定20mL 小容量西林瓶包装对硫酸头孢喹肟注射液质量稳定性是否存在影响。
试验将硫酸头孢喹肟注射液分装于三批包装材料中,分别考察影响因素试验(高温40℃、光照4500±500lx )、加速试验(30±2℃,RH65%±5%)和长期试验(25±2℃,RH60%±10%)条件下对药液稳定性的影响。
通过试验验证,确定20mL 小容量西林瓶包装对药物硫酸头孢喹肟注射液的质量稳定性产生的影响在质量标准控制范围内。
关键词:硫酸头孢喹肟;包材相容性试验;稳定性;质量20mL 西林瓶对硫酸头孢喹肟注射液质量稳定性影响的研究高建峰,王成达,杨琳,段鹏,邓菲*(1.石家庄市藁城区农业农村局石家庄052160;2.华北制药集团动物保健品有限责任公司石家庄052165)收稿日期:2022-11-11作者简介:高建峰,畜牧师,本科,动物医学专业。
*通讯作者:邓菲,女,正高级工程师,硕士,研究方向为新兽药,邮箱:*****************。
华北制药集团动物保健品有限责任公司通过对硫酸头孢喹肟注射液的稳定性考察,确定产品有效期为24个月,目前已上市100mL 规格产品。
为方便中小规模养殖户的使用,拟增加20mL小容量西林瓶包装。
本试验对20mL 硫酸头孢喹肟注射液进行了包材相容性试验考察,为产品注册提供依据。
1头孢喹肟的理化性质和作用机理1.1理化性质硫酸头孢喹肟(C 23H 24N 6O 5S 2·H 2SO 4),分子量626.69,CAS 号为118443-89-3。
性状为类白色至淡黄色粉末,微臭,有引湿性。
在水、甲醇中微溶,在乙醇或丙酮中几乎不溶。
1.2作用机理头孢喹肟是动物专用第四代头孢菌素类抗生素,用于治疗由多杀性巴氏杆菌或胸膜肺炎放线杆菌引起的猪呼吸道疾病,是猪场常用药物之一。
硫酸头孢喹肟注射液的制备工艺研究

学术研究doi:10.3969/j.issn.1008-4754.2014.05.005头孢喹肟是德国赫斯特动物保健品公司率先开发的第一个动物专用的第四代头孢菌素类抗生素,其制剂硫酸头孢喹肟注射液于1993年首次上市,国外已广泛用于猪、牛呼吸系统感染及奶牛乳房炎的临床治疗[1-2]。
目前,国内已有洛阳惠中、河北远征、天津瑞普等单位相继研发并成功申报新药。
本文就硫酸头孢喹肟注射液的制备工艺进行了研究,得到质量可靠的产品,保证临床用药安全。
1仪器与材料1.1材料硫酸头孢喹肟,批号20100901,含量90.5%,洛阳惠中兽药有限公司;油酸乙酯,上海千方油脂有限公司;白矿油,深圳市美凯特科技有限公司;注射用大豆油,龙游县田雨山茶油开发有限公司;茶油(供注射用),龙游县田雨山茶油开发有限公司;硬脂酸铝,河南隆鑫化工有限公司;乙基纤维素,上海三杰生物技术有限公司;失水山梨醇单油酸酯(司盘-80),南京威尔化工有限公司;卵磷脂,天津科密欧试剂有限公司。
1.2仪器设备IKA-RW20DS25高剪切机,德国IKA公司;JMS-50胶体磨,廊坊正端机械有限公司;AH-100D 高压均质机,加拿大ATS工业系统有限公司;UV-P 光学显微镜,北京和众视野公司;YP-150SD药物稳定性试验箱,北京恒泰丰科试验设备有限公司;wa-ters2695高效液相色谱仪,美国沃特斯公司。
2方法与结果2.1检测方法2.1.1含量测定照高效液相色谱法测定。
详细测定方法参照农业部第1085号公告硫酸头孢喹肟注射液质量标准。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂;取一水合高氯酸钠3.45g溶于1 000mL水中,加磷酸12mL和乙腈90mL,用三乙胺调节pH至3.6为流动相;检测波长为270nm。
取头孢噻肟约25mg,溶于100.0mL流动相中,另取头孢喹肟约25mg,置25mL量瓶中,精密加入上述头孢硫酸头孢喹肟注射液的制备工艺研究宋永军1,李向阳2,朱华伟3,付旭东4(1.普莱柯生物工程股份有限公司河南洛阳471000;2.国家兽用药品工程技术研究中心河南洛阳471003;3.洛阳惠中兽药有限公司河南洛阳471013;4.石家庄动物疾病预防控制中心河北石家庄050000)摘要:通过对硫酸头孢喹肟注射液的辅料及分散工艺进行研究,确定了硫酸头孢喹肟注射液的制备工艺。
注射用硫酸头孢喹肟工艺规程

注射用硫酸头孢喹肟工艺规程一、引言注射用硫酸头孢喹肟是一种广泛应用于临床的抗生素,具有广谱抗菌活性。
为了确保药物的质量和安全性,制定了注射用硫酸头孢喹肟的工艺规程。
本文将详细介绍注射用硫酸头孢喹肟的制备工艺。
二、原料准备1. 活性成分:硫酸头孢喹肟原料应符合国家药典规定的质量标准,包括外观、纯度、含量等指标。
2. 辅料:辅料应符合国家药典规定的质量标准,包括溶剂、稳定剂等。
三、工艺流程注射用硫酸头孢喹肟的制备工艺流程如下:1. 粉碎与混合将硫酸头孢喹肟原料粉碎至符合要求的粒度,然后与辅料进行混合,确保辅料均匀分散在原料中。
2. 粉末制备将混合后的原料通过粉碎机进行进一步细磨,直至得到符合要求的颗粒度。
3. 溶解与配制将粉末加入预先配制好的溶剂中,进行充分溶解,并根据配方添加适量的稳定剂,调整药物的pH值和渗透压,以确保药物的稳定性和适宜的温和性。
4. 过滤与灭菌将溶解后的药液进行过滤,去除杂质和微生物。
然后,将药液进行灭菌处理,确保药物的无菌性。
5. 储存与包装将灭菌后的药液进行储存,以确保药物质量的稳定性。
最后,根据规定的包装要求,对药液进行包装,以便于运输和使用。
四、质量控制在注射用硫酸头孢喹肟的生产过程中,需要进行一系列的质量控制,以确保药物的质量和安全性。
1. 原料检验对硫酸头孢喹肟原料进行外观、纯度、含量等指标的检验,确保原料符合要求。
2. 生产过程控制在生产过程中,对粉碎、混合、溶解、过滤等关键步骤进行严格的控制和监测,确保每个步骤的操作符合规范,避免对药物质量的不良影响。
3. 药物质量检验对制备好的注射用硫酸头孢喹肟进行质量检验,包括外观、纯度、含量、pH值、渗透压等指标的测定,确保药物质量符合规定标准。
4. 灭菌效果检验对灭菌后的药液进行菌落总数和无菌检测,确保药物的无菌性。
五、安全与环保措施在注射用硫酸头孢喹肟的生产过程中,应严格遵守相关的安全与环保规定,采取必要的措施,确保工作场所的安全和环境的保护。
硫酸头孢喹肟中4种有机溶剂残留量的测定

硫酸头孢喹肟中4种有机溶剂残留量的测定刘利锋;江善祥【期刊名称】《畜牧与兽医》【年(卷),期】2009()11【摘要】建立以气相色谱法测定硫酸头孢喹肟中乙醇、丙酮、二氯甲烷、甲苯等4种有机溶剂残留的方法。
采用DB-624石英毛细管柱,FID检测器,程序升温:40℃(保持10min)~220℃(保持5min),升温速率为30℃·min^-1,进样口温度为220℃,检测器温度为230℃,流速:5mL·^-1,分流比为20:1。
结果显示:硫酸头孢喹肟原料药中乙醇、丙酮、二氯甲烷、甲苯在所考察的浓度范围内与峰面积比值呈良好的线性关系(r=0.9994~0.9998),检测限分别为1.67,1.89,2.56和2.02μg·min。
(S/N=5),平均加样回收率97.69%-99.42%,RSD均小于5%(n=3)。
本试验建立的色谱方法简便、灵敏、准确、重现性好,适用于硫酸头孢喹肟中有机溶剂残留量的检测。
【总页数】2页(P55-56)【关键词】硫酸头孢喹肟;残留溶剂;毛细管气相色谱法【作者】刘利锋;江善祥【作者单位】南京农业大学动物医学院【正文语种】中文【中图分类】S859【相关文献】1.HPLC法测定硫酸头孢喹肟注射液中硫酸头孢喹肟含量 [J], 李勇军;杨海峰;蒋春茂;于生兰;张成;金礼琴;朱雄2.顶空进样法测定头孢克肟中有机溶剂残留量 [J], 李心泓;茅纯;俞慧丽3.HS-SPME-GC法测定头孢噻肟钠中多种有机溶剂残留量 [J], 黄念桃;李弘弢4.HPLC法测定硫酸头孢喹肟冻干粉针中硫酸头孢喹肟含量 [J], 俞吉杰;余祖功;赵杰;刘利锋;段复康;江善祥5.硫酸头孢喹肟中间体7氨基头孢喹肟氢碘酸盐的合成 [J], 武晓青;赵地顺;尚青;梁策因版权原因,仅展示原文概要,查看原文内容请购买。
HPLC法测定硫酸头孢喹肟冻干粉针中硫酸头孢喹肟含量

HPLC法测定硫酸头孢喹肟冻干粉针中硫酸头孢喹肟含量俞吉杰;余祖功;赵杰;刘利锋;段复康;江善祥
【期刊名称】《畜牧与兽医》
【年(卷),期】2008()9
【摘要】建立高效液相色谱法(HPLC法)测定硫酸头孢喹肟冻干粉针中硫酸头孢喹肟的含量.色谱条件为色谱柱Kromasil C18柱(250 mm×4.6 mm,5 μm),以高氯酸钠-磷酸-三乙胺缓冲液(pH 3.6):乙腈(体积比90∶10)为流动相,流速为0.8 mL/min,紫外检测波长为254 nm.结果表明,硫酸头孢喹肟在0.05~25μg/mL范围内呈良好的线性关系,r=0.99 96,平均回收率为100.34%(n=9),RSD为1.34%.该方法简便快速,结果准确可靠,可用于硫酸头孢喹肟冻干粉的质量控制研究.
【总页数】4页(P31-34)
【关键词】硫酸头孢喹肟冻干粉;硫酸头孢喹肟;HPLC
【作者】俞吉杰;余祖功;赵杰;刘利锋;段复康;江善祥
【作者单位】南京农业大学动物医学院
【正文语种】中文
【中图分类】S859.2
【相关文献】
1.猪组织中硫酸头孢喹肟含量测定和肌注给药残留研究 [J], 刘利锋;覃少华;赵杰;周健;江善祥
2.HPLC法测定硫酸头孢喹肟注射液中硫酸头孢喹肟含量 [J], 李勇军;杨海峰;蒋春
茂;于生兰;张成;金礼琴;朱雄
3.硫酸头孢喹肟中间体3′-碘甲基头孢噻肟的合成 [J], 杨佳宁;
4.长效土霉素、头孢氨苄、硫酸头孢喹肟三种注射液对患病仔猪的疗效观察 [J], 李劲松;韦绍婉
5.硫酸头孢喹肟中间体7氨基头孢喹肟氢碘酸盐的合成 [J], 武晓青;赵地顺;尚青;梁策
因版权原因,仅展示原文概要,查看原文内容请购买。
禽用惠诺威—油苗伴侣

禽用惠诺威—油苗伴侣同时拥有原料药和注射液两大证书的国家二类新兽药一、产品成分1%的硫酸头孢喹肟二、产品特点1、广谱、高效、无耐药。
国家兽药工程技术研究中心研究表明,头孢喹肟分子结构存在两性基团,其独特性在于集对细菌的高度穿透力和对β-内酰胺酶的高稳定性于一体,对目前已分离的G+、G-,耐药菌均具强大的杀灭作用。
2、结晶型原料制作,抗菌活性强,生物利用度高。
头孢喹肟原料存在着普通型和结晶型两种状态,其中普通型原料不稳定,在放置过程中容易降解,抗菌活性差,惠诺威采用结晶型原料精制而成,抗菌活性极强,是普通晶型原料的2-4倍,生物利用度是普通型原料的2倍以上。
3、国内率先采用进口佐剂,佐剂选自台湾百达GTCC,稳定性强,易吸收,对动物无任何刺激。
①采用加速试验测定惠诺威的稳定性将惠诺威放在25±2℃相对湿度60±10%条件下放置两年,于第0、3、6、9、12、18、24月取样,考察性状、有关物质、沉降、粒度、含量等相关项目,与0月的检测结果对比,试验结果如下表:结论:惠诺威的性状、有关物质和含量均无明显变化,说明惠诺威稳定性好。
②静置沉降试验4、触变胶体造就独一无二产品,缓释技术实现速效长效完美统一。
5、安全性高,基本无毒、无残留,无三致作用。
①惠诺威对1日龄雏鸡的安全性试验注:所有试验组均无鸡只伤亡,且对增重无影响。
②惠诺威与油乳剂灭活疫苗的互溶性试验结论:惠诺威注射液和油苗互溶性好,可以一起混合使用,不会影响雏鸡增重,安全系数高。
二、功能主治1、用于预防和治疗雏鸡大肠杆菌、沙门氏菌等单一或混合感染引起的心包炎、肝周炎、气囊炎及鸡白痢等。
2、用于种鸡的大肠杆菌、沙门氏杆菌净化。
3、鸭传染性浆膜炎。
三、用法用量1、商品肉鸡7-10日龄 600-800只/10ml。
----配合油苗注射,减少8-15日龄大肠杆菌药使用,降低口服药对肝肾的损伤,省时省力,提高疗效。
2、种鸡 ----配合油苗注射,净化输卵管,防止垂直传播,有效净化大肠杆菌及沙门氏菌防止垂直感染。
注射用头孢唑肟点评标准(点评指南)

注射用头孢唑肟点评标准适应症敏感菌所致的下呼吸道感染、尿路感染、腹腔感染、盆腔感染、败血症、皮肤软组织感染、骨和关节感染、肺炎链球菌或流感嗜血杆菌所致脑膜炎和单纯性淋病。
说明书:【适应症】敏感菌所致的下呼吸道感染、尿路感染、腹腔感染、盆腔感染、败血症、皮肤软组织感染、骨和关节感染、肺炎链球菌或流感嗜血杆菌所致脑膜炎和单纯性淋病。
用法用量1.成人常用量:一次1~2g(1-2瓶),每8~12小时1次;严重感染者的剂量可增至一次3~4g,每8小时1次。
治疗非复杂性尿路感染时,一次0.5g,每12小时1次。
2.6个月及6个月以上的婴儿和儿童常用量:按体重一次50mg/kg,每6~8小时1次。
3.肾功能损害者:肾功能损害的患者需根据其损害程度调整剂量。
在给予0.5~1g的首次负荷剂量后,肾功能轻度损害的患者(内生肌酐清除率Clcr为50~79ml/分钟)常用剂量为一次0.5g,每8小时1次,严重感染时一次0.75~1.5g,每8小时1次;肾功能中度损害的患者(Clcr为5~49ml/分钟)常用剂量为一次0.25~0.5g,每12小时1次,严重感染时一次0.5~1g,每12小时1次;肾功能重度损害需透析的患者(Clcr为0~4ml/分钟)常用剂量为一次0.5g,每48小时1次,或一次0.25g,每24小时1次,严重感染时一次0.5~1g,每48小时1次,或一次0.5g,每24小时1次。
血液透析患者透析后可不追加剂量,但需按上述给药剂量和时间,在透析结束时给药。
本品可用注射用水、氯化钠注射液、5%葡萄糖注射液溶解后缓慢静脉注射,亦可加在10%葡萄糖注射液、电解质注射液或氨基酸注射液中静脉滴注30分钟~2小时。
说明书:【用法用量】1.成人常用量:一次1~2g(1~2瓶),每8~l2小时1次;严重感染者的剂量可增至一次3~4g(3~4瓶),每8小时1次。
治疗非复杂性尿路感染时,一次0.5g,每12小时1次。
2.6个月及6个月以上的婴儿和儿奄常用量:按体重一次50mg/kg,每6~8小时1次。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
进口兽药质量标准
硫酸头孢喹肟注射液Liusuan Toubaokuiwo Zhusheye Cefquinome sulfate Injection
本品为硫酸头孢喹肟与油酸乙酯等配制而成的混悬注射液。
含头孢喹肟(C
23H
24
N
6
O
5
S
2
)
应为标示量的90.0%~105.0%。
【性状】本品为类白色至浅褐色混悬液体;久置分层。
【鉴别】(1)含量测定项下记录的色谱图中,供试品主峰的保留时间应与对照品峰的保留时间一致。
(2)取摇匀后的供试品2 ml,加水5 ml,稀盐酸1 ml,混匀,置超声浴中超声10
分钟,弃去有机层,溶液显硫酸盐的鉴别反应(附录15页)。
【检查】有关物质照含量测定项下的方法。
取摇匀后的供试品1.0 ml,加入流动相25.0 ml,置超声浴中超声5分钟,弃去有机层,取水层滤过,取续滤液10µl,注入液相色谱仪,记录色谱图,2,3-环己基吡啶与头孢喹肟相对保留时间为0.20。
按峰面积归一化法计算,2,3-环己基吡啶应不得过3.0%,其他单一杂质应不得过0.50%,杂质总量应不得过4.0%。
水分取本品,照水分测定法(附录58页,第一法)检查,含水分不得过0.2%。
细菌内毒素取摇匀后的供试品2 ml与细菌内毒素检查用水3 ml混匀,分成2等份,振摇30秒,离心15分钟(2000g),吸取水层1 ml,加1 mol/L氢氧化钠溶液0.06 ml 调节pH值至6.5~7.5。
用细菌内毒素检查用水按1:10稀释后,照细菌内毒素检查法(附录73页)检查,每1 mg头孢喹肟中含细菌内毒素的量应小于0.1 EU。
无菌取供试品8瓶,混合均匀,加入含6%吐温-80的蛋白胨缓冲液(1g/L)400ml,混匀,加入800×106单位青霉素酶(每1ml供试品溶液,加2×106单位青霉素酶),充分振摇,将供试品倒置,在37℃放置4小时;取供试品溶液,依法检查(附录79页,直接接种法),应符合规定。
分散性取本品1瓶,振摇30秒,将供试品转移置玻璃容器中,不得观察到结块或沉淀物。
沉降取本品1瓶,振摇30秒,取供试品10 ml置刻度试管中(内径1.0~1.5 cm),10分钟内不得沉淀。
粒度取摇匀后的供试品,置显微镜下检查,颗粒直径在5µm以下应不得少于80%,10µm以下不得少于90%,20µm以下不得少于95%,50µm以下不得少于100%。
装量按最低装量检查法(附录67页)检查,应符合规定。
【含量测定】照高效液相色谱法(附录24页)测定。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂;取一水合高氯酸钠3.45g溶于1000 ml水中,加磷酸12 ml和乙腈90 ml,用三乙胺调节pH至3.6为流动相;检测波长为270 nm。
取头孢噻肟约25 mg,溶于100.0 ml流动相中,另取头孢喹肟约25 mg,置25 ml量瓶中,精密加入上述头孢噻肟溶液1 ml,用流动相稀释至刻度。
精密量取10µl 注入液相色谱仪,记录色谱图;计算头孢喹肟与头孢噻肟的分离度,应大于1.0。
对照品溶液的制备精密称取硫酸头孢喹肟对照品适量(约相当于头孢喹肟25 mg),置250 ml量瓶中,用流动相溶解并稀释至刻度,摇匀,即得。
供试品溶液的制备精密量取摇匀后的供试品适量(约相当于头孢喹肟50 mg),精密加入流动相100 ml,置超声浴中超声5分钟,弃去油层,滤过;精密量取续滤液5 ml,置25 ml量瓶,加流动相稀释至刻度,摇匀,即得。
测定法精密量取对照品溶液和供试品溶液各10µl,分别注入液相色谱仪,记录色谱图。
按外标法以峰面积计算,即得。
【作用与用途】抗生素类药。
主要用于治疗大肠杆菌引起的奶牛乳房炎,多杀性巴氏杆菌或胸膜肺炎放线杆菌引起的猪呼吸道疾病
【用法与用量】肌内注射一次量每1 kg体重牛1 mg 一日1次连用2日猪2~3 mg 一日1次连用3日
【休药期】牛 5日;猪 2日;弃奶期 1日。
【规格】 50ml:1.25g
【贮藏】遮光,25℃以下保存。
【有效期】 2年。
【生产企业】英特威国际有限公司(Intervet International GmbH)
注:
蛋白胨缓冲液(1g/L)
蛋白胨(酪蛋白胨或肉蛋白胨) 1g
KH
2PO
4
3.6g
Na
2HPO
4
•2H
2
O 7.2g
NaCl 4.3g 最终pH为7.0±0.2
溶液应无色澄清
来源:中国兽药信息网。
