配位化合物习题答案
配位化合物(习题参考答案)
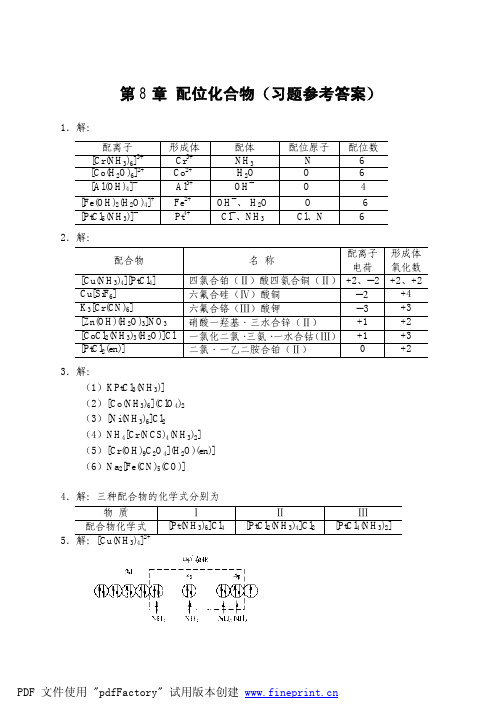
由(2)、(3)计算结果看出,AgCl 能溶于稀 NH3·H2O,而 AgBr 须用浓 NH3·H2O 溶解。 12.解: (1)[HgCl4]2− + 4 I−
K =
ψ
K fψ ([HgI 4 ] 2 − ) K fψ ([HgCl 4 ] )
= 5.78 ×10 14
K ψ 很大,故反应向右进行。
y = 0.49
可见 KCN 可溶解较多的 AgI。 10.解:设 1.0 L 1.0 mol·L−1 氨水可溶解 x mol AgBr,并设溶解达平衡时 c([Ag(NH3)2]+) = x mol·L−1(严格讲应略小于 x mol·L−1)c(Br− ) = x mol·L−1 AgBr(s) + 2NH3·H2O [Ag(NH3)2]+ + Br− + 2H2O 平衡浓度/(mol·L−1) 6.0 − 2 x x x
(2)[Cu(CN)2]− + 2NH3·H2O [Cu(NH3)2]+ + 2CN− + 2H2O
−
Kψ =
K fψ ([Cu(NH 3 ) 2 ] + ) K fψ ([Cu(CN) 2 ] )
= 7.24×10−14
(3)[Fe(NCS)2]+ + 6F−
[FeF6]3− + 2SCN−
+
Kψ =
PDF 文件使用 "pdfFactory" 试用版本创建
[CoF6]3-
[Ru(CN)6]4-
[Co(NCS)4]2―
6.解:已知:[MnBr4]2―μ=5.9 B.M,[Mn(CN)6]3―μ=2.8 B.M。 由: µ= n(n+2) 式求得:
中国药科大学《无机化学》第四章配位化合物习题及答案

中国药科大学《无机化学》第四章配位化合物习题及答案一、选择题1. 对于配合物中心体的配位数,说法不正确的是………………………………………()(A) 直接与中心体键合的配位体的数目(B) 直接与中心体键合的配位原子的数目(C) 中心体接受配位体的孤对电子的对数(D) 中心体与配位体所形成的配价键数2. [Ni(CN)4]2-是平面四方形构型,中心离子的杂化轨道类型和d电子数分别是……()(A) sp2,d7(B) sp3,d8(C) d2sp3,d6(D) dsp2,d8二、填空题3. 配合物[PtCl(NH3)5]Br和[Co(NO2)(NH3)5]2+ 存在的结构异构体的种类和结构简式分别为_______________________________ 和_______________________________________。
4. 已知铁的原子序数为26,则Fe2+在八面体场中的晶体场稳定化能(以△0 =10 Dq表示)在弱场中是_____________ Dq,在强场中是______________ Dq。
5. 对于八面体构型的配离子,若中心离子具有d7电子组态,则在弱场中,t2g轨道上有____个电子,e g轨道上有____个电子;在强场中,t2g轨道上有____个电子,e g轨道上有____个电子。
三、问答题6. 试举例说明π 配合物与π酸配合物的区别。
7. 画出[CoCl2(NH3)2(H2O)2]+配离子的几何异构体。
参考答案一、选择题1. (A)2. (D)二、填空题3. 电离异构体[PtBr(NH3)5]Cl键合异构体[Co(ONO)(NH3)5]2+4. -4 Dq;-24 Dq5. 5,2;6,1三、问答题6.π配合物:由配体提供π电子给中心体原子(离子)的空轨道,形成配位σ 键,例蔡斯盐[PtCl3(C2H4)]-。
Pt – C2H4间存在σ 键及反馈d -π*π键π酸配合物:由CO、NO等一类π酸配体(π受体)与金属原子或d电子较多的过渡金属原子、离子形成的配合物,一方面它们可以提供孤对电子与中心体形成配位σ 健,另一方面,它有空的π轨道可接受来自中心体原子上d轨道上积累的负电荷,配体本身是Lewis 碱,又是Lewis酸。
无机答案第11章 配位化合物

第11章 配位化合物习 题1.给出下列中心金属离子的特征配位数:(a)Cu+;(b)Cu2+;(c)Co3+;(d)Zn2+;(e)Fe2+;(f)Fe3+。
2.按照摩尔导电率的大小将下列配合物排序:(a)K[Co(NH3)2(NO2)4];(b)[Cr(NH3)3(NO2)3];(c)[Cr(NH3)3(NO2)] 3 [Co(NO2)6]2;(d)Mg[Cr(NH3)(NO2)5]。
3.解释为什么EDTA钙盐可作为铅的解毒剂?为什么用EDTA的钙盐而不能用游离的EDTA?4.指出下列配离子中金属元素的氧化态:(1) [Cu(NH3)4]2+;(2) [Cu(CN)2]-;(3) [Cr(NH3)4(CO3)]+;(4) [Co(en)3]2+;(5) [CuCl4]2-;(6) Ni(CO)4.5.命名下列配合物:(1)K3[Co(NO3)6];(2)[Cr(Py)2(H2O)2Cl2];(3)[Cr(H2O)5Cl]Cl2•H2O;(4)K2[Ni(en)3];(5)[Co(NH3)4(NO2)Cl]Cl;(6)K3[Fe(C2O4)3]•3H2O;(7)K2[Cu(C2H2)3];(8)[Pt(Py)4][PtCl4].6.根据下列配合物的名称,写出其化学式:(1)亚硝酸•溴三氨合铂(Ⅱ);(2)一水合二氨•二乙二胺合铬(Ⅲ);(3)溴化硫酸根•五氨合钴(Ⅳ);(4)六氟合铂(Ⅳ)酸钾。
7.画出配离子[Cr(NH3)(OH)2Cl3]2-所有可能的几何异构体。
8.指出下列配合物中配位单元的空间构型并画出它们可能存在的几何异构体:(1)[Pt(NH3)2(NO2)Cl];(2)[Pt(Py)(NH3)ClBr];(3)[Co(NH3)2(OH)2Cl2];(4)K4[Co(NH3)2(NO2)4];(5)[Ni(NH3)3(OH)3];(6)[Ni(NH3)2Cl2].9.配离子[Cr(en)2Cl2]+存在几种几何异构体,哪种异构体可以表现出旋光活性,画出这些异构体。
化学竞赛题库配位化合物答案

ONOOH , ONOOH
NO2 + OH
x=x=1 2 1 3
4x + (+1) ´ 7 + ( -2) ´ 3 = -1 3y + ( -1) ´ 3 + ( +1) ´ 4 = 0
β-PdCl2
Cl Pd Cl
Cl Pd Cl
Cl Pd Cl
Cl Pd Cl
2.该反应的分步反应方程式为 (1) PdCl2 + 2Cl PdCl42PdCl42- + CH2=CH2 [Pd(C2H4)Cl3] + Cl
-
[Pd(C2H4)Cl3] + H2O [Pd(C2H4)(H2O)Cl2] + Cl ………… 总反应方程式为 PdCl2 + C2H4 + H2O (2) Pd2+采取 dsp2 杂化 (3) C2H4 与 Pd2+之间存在 σ 配键与反馈 π 键 Pd + CH3C
-
O H
+ 2HCl
+ +
2
五、1.∵配合物(C)为单核、电中性分子,其分子量为 含 H 原子个数为:
462.85 ´ 0.0523 = 24 (个) 1.008
M Mn 54.69 = = 462.85 0.1187 0.1187
形成(C)的配体是由 2 分子(A)与 1 分子(B)失去 2 分子水后形成的:
CHO
H2N
H H H B C O (A)
H Na
+
H H
B C
O O
Na+ (B)
CH3 O H3C B B O O B CH3 (C) H3C O B
(完整版)配位化合物习题及解析

《配位化合物》作业参考解析1. 下列说法正确的是A. 配合物的内界和外界之间主要以共价键相结合B. 中心原子与配体之间形成配位键C. 配合物的中心原子都是阳离子D. 螯合物中不含有离子键【B】A、D:一般认为配合物的内界和外界之间主要以离子键相结合,因此螯合物中内界和外界之间是可以存在离子键的;C:中心原子可以是阳离子,也可以是中性原子,例如[Ni(CO)4];B:中心原子与配体化合时,中心原子提供杂化过的空轨道,配体提供孤对电子,而形成配位键。
2. 下列配合物命名不正确的是A. [Co(H2O)(NH3)3Cl2]Cl 氯化二氯·三氨·一水合钴(Ⅲ)B. [Cr(NH3)6][Co(CN)6] 六氰合钴(Ⅲ)酸六氨合铬(Ⅲ)C. K[Co(NO2)3Cl3] 三硝基·三氯合钴(Ⅲ)酸钾D. H2[PtCl6] 六氯合铂(Ⅳ)酸【C】根据配体命名顺序,先无机后有机,先阴离子后中性分子,同类配体根据配位原子在字母表中的先后顺序进行命名。
对于C中的配合物而言,NO2-以N原子为配位原子时,命名为硝基,带一个负电荷,氯离子也是阴离子,同类配体,根据配位原子在字母表中的先后顺序,Cl-离子在前,NO2-离子在后,因此该配合物应该命名为“三氯·三硝基合钴(Ⅲ)酸钾”。
3. 下列配离子具有正方形或者八面体形结构,其中CO32-最有可能作为双齿配体的是A. [Co(NH3)4(CO3)]+B. [Co(NH3)5(CO3)]+C. [Pt(en)(NH3)(CO3)]D. [Pt(en)2(NH3)(CO3)]2+【A】根据题意,配离子具有正方形结构时,配位数为4,形成四个配位键;具有八面体结构时,配位数为6,形成6个配位键。
B:[Co(NH3)5(CO3)]+ 配离子中,已有5个氨作为配体,氨是单齿配体,形成5个配位键,因此该配离子中,CO32-离子只能是单齿配体,这样就形成了6个配位键;C:[Pt(en)(NH3)(CO3)] 配合物中,乙二胺(en)为双齿配体,形成2个配位键,氨为单齿配体,形成1个配位键,因此CO32-离子只能是单齿配体,这样就形成了4个配位键;D:[Pt(en)2(NH3)(CO3)]2+ 配离子中,乙二胺(en)为双齿配体,2个en形成4个配位键,氨为单齿配体,形成1个配位键,因此CO32-离子只能是单齿配体,这样就形成了6个配位键;A:[Co(NH3)4(CO3)]+ 配离子中有4个氨为配体,形成4个配位键,因此CO32-离子必须是双齿配体,这样就形成了4个配位键,如果CO32-离子是单齿配体,那么配离子的配位数为5,这与题意不符。
配位化学习题(答案参考)

配位化合物(01)1.历史上记录的第一种人工合成的配位化合物是( D )A.硫酸六氨合钴(II)B.普鲁士蓝C.硫酸四氨合铜(II)D.氯化二氨合银(I)2.配位化学的奠基人是( D)A.阿仑尼乌斯B.路易斯C.鲍林D.维尔纳3.下列说法中错误的是( C)A 配合物的形成体通常是过渡金属元素B 配键是稳定的化学键C 配键的强度可以和氢键相比较D 四面体配合物中,不存在顺反几何异构现象4.下列说法中正确的是(D )A 配位原子的孤电子对越多,其配位能力就越强B 电负性大的元素充当配位原子,其配位能力也强C CH3-C-OH配体是双齿配体D 在[Cu(en)2]2+中,Cu2+的配位数是412.下列说法中错误的是(D )A.对于Ni2+来说,当配位数为6时,无论是强场或弱场配体本位,只能采用SP3d2杂化B.对Ni2+来说,当本位数为4时,随配体的不同可采取dsp2或SP3杂化C.无论中心离子杂化轨道是d2sp2或SP3d2,其构型均为八面体形D.配合物中,由于存在配键,所以配合物都是弱电解质13.下列配体的本位能力的强弱次序为(B )->NH3>NCS->H2O>X-->NH3>NCS->H2O>X-C.X->H2O>CH->NH3>NCS-D.X->CN->H2O>NH3>NCS-14.在配位分子3KNO2.Co(NO3)2中,配位数为(D )A 3B 4C 5D 627.1 共价键和配位共价键的区别是什么?在NH4+离子中分别有多少个共价键和配位共价键?如何对其进行区分?解配位共价键是指一对电子由两个原子共享,且此电子是由其中的一个原子提供的;共价键是指一对共用电子对,一旦形成这两种键就没有区别。
在NH4+离子中有四个共价键,其中有一个是配位共价键。
27.4 求下列配位化合物的中心原子的配位数分别是多少?(a) [Mo(CN)8]4-中的钼(b)Cu(en)22+中的铜(en为乙二胺)解(a) 8 (b) 427.7 指出下列各金属中心离子的特征配为数:(a) CuⅠ(b) CuⅡ(c)AlⅢ(d) CoⅢ(e) ZnⅡ(f) FeⅡ(g) FeⅢ(h) AgⅠ。
配位化学试题及答案

配位化学试题及答案一、选择题(每题2分,共10分)1. 下列哪项不是配位化合物的特点?A. 含有中心原子或离子B. 含有配位键C. 含有离子键D. 含有配体答案:C2. 配位化合物的几何构型通常由什么决定?A. 配体的电荷B. 配体的数目C. 配体的电子排布D. 中心原子的氧化态答案:B3. 配位化学中,路易斯碱是指什么?A. 能够提供电子的分子或离子B. 能够接受电子的分子或离子C. 能够提供空轨道的分子或离子D. 能够接受空轨道的分子或离子答案:B4. 下列哪种配体是单齿配体?A. 乙二胺(en)B. 1,3-丙二胺(pn)C. 环己二胺(cn)D. 四齿配体答案:A5. 配位化合物的命名中,配体的名称通常放在什么位置?A. 中心原子的前面B. 中心原子的后面C. 配位化合物的前面D. 配位化合物的后面答案:A二、填空题(每题2分,共10分)1. 配位化学中,中心原子或离子与配体之间形成的化学键称为______。
答案:配位键2. 一个中心原子或离子最多可以与______个配体形成配位键。
答案:63. 配位化合物的配位数是指______。
答案:中心原子或离子周围配体的数量4. 配位化合物的命名中,配体的数目通常用希腊数字表示,其中“二”表示______。
答案:二5. 配位化合物的命名中,配体的电荷通常用罗马数字表示,其中“Ⅱ”表示______。
答案:+2三、简答题(每题5分,共20分)1. 简述什么是内界和外界,并举例说明。
答案:内界是指配位化合物中中心原子或离子与配体形成的配位单元,外界是指配位单元以外的部分。
例如,在[Co(NH3)6]Cl3中,[Co(NH3)6]是内界,Cl3是外界。
2. 什么是螯合配体?请举例说明。
答案:螯合配体是指能够通过多个配位点与中心原子或离子形成配位键的配体。
例如,乙二胺(en)可以与金属离子形成螯合配位化合物。
3. 配位化合物的稳定性与哪些因素有关?答案:配位化合物的稳定性与中心原子或离子的电荷、配体的类型、配位数以及配体与中心原子或离子之间的配位键强度等因素有关。
无机化学习题-配位化合物答案

化,形成四配位平面四方配离子 5d8 的 8 个 d 电子全部配对, m = n(n + 2) B. M. = 0。
Pt(IV)应为 d2sp3 杂化,形成内轨型六配位八面体配离子。
该配合物实际化学式可能有:
65.39 y + 16 + 59.024 ´ (2 y -1)
81.39 y
= 0.516 解得 y ≈ 4
183.44 y - 102.048
∴(A)的化学式为 Zn4O(CH3COO)6
2.4ZnCO3 + 6CH3COOH
ZnO(CH3COO)6 + 4CO2 + 3H2O
3.Zn2+为 3d10,Zn2+周围有 4 个 O 原子,∴Zn2+离子采取 sp3 杂化
4.2948 + 14.476x = 3.024 + 15.12x, 0.644x = 1.2708, x = 2
∴Al 为+3 氧化态,Al3+采取 sp3 杂化。
H NEt3
NEt3 H
NEt3 H
Al
H
NEt3
H
Al
H
H
Et3N
NEt3 (非极性分子)
Al H
H
因它们都有对称面,所以都不存在对映体。
十六、1.H C
O
H + CH3OH C
O
(B) LiAlH4
(C) SiCl4
(D) (CH3)2NH (E)
6
N (E)为
H2C H3C N H3C
基础化学配位化合物及配位平衡习题解答

13.解答:lgc
K
θ/ ZnY
=7.75>6,可以标定。
14.解答:lgc
K
θ/ ZnY
=9.21>6,可以滴定。
反式-二溴·四氨合钌(III)
顺式-四氨·二水合钴(III) 反式-四氨·二水合钴(III)
11 配位化合物及配位平衡
22.解答:顺式-二氯·二氨·二水合铬(III)结构式:
可能的异构体有:
其中(I)、(II)为反式二氨异构体。 23.解答:配体 en 比配体 F-具有更强的场强,F-引起的中心离子 Co3+d 轨道分裂能
小于 en 引起的中心离子 Co3+d 轨道分裂能。所以电子在[CoF6-]3-的 eg 与 t2g 之间跃迁需要的能量比[Co(en)3]3+的小,即[CoF6-]3-电子跃迁吸收的光波波 长比[Co(en)3]3+的长,[CoF6-]3-显示出的颜色对应的光波波长比[Co(en)3]3+ 的短。所以黄色溶液应该是[Co(en)3]3+的溶液,而[CoF6-]3-溶液成蓝色。 24.解答:(1) [CuBr4]2-、[Cu(H2O)6]2(2) 正 方 形 场 配 合 物 [CuBr4]2- 中 心 离 子 d 轨 道 分 裂 能 比 八 面 体 场 [Cu(H2O)6]2-配合物 d 轨道分裂能小,[Cu(H2O)6]2-的电子跃迁能大于 [CuBr4]2-,[Cu(H2O)6]2-显示的颜色波长大于[CuBr4]2-,[Cu(H2O)6]2-呈淡 蓝色,而[CuBr4]2-呈深紫色。
络合物(配位化合物)(习题及答案)

第九章络合物(配位化合物)一、选择题1.下列离子中属于低自旋的是(C)A.[C oF6]3-B.[FeF6]3-C.[Fe(CN)6]3-D.[MnCl4]2-(μ=5.88)2.下列分子或离子能做螯合剂的是(D)A.H2N—NH2B.CH3COO—C.HO—OH D.H2NCH2CH2NH23.中心原子以sp3杂化轨道形成络离子时,其空间构型为(D)A.直线型B平面四边形C.正八面体D.正四面体4.下列试剂中能溶解Zn(OH)2、AgBr、Cr(OH)3、Fe(OH)3四种沉淀的是(B)A. 氨水B.氰化钾溶液C 硝酸 D.盐酸5.已知Co(NH3)63++e=Co(NH3)62+的Eθ=0.10V , Eθ(Co3+/Co2+)=1.84V,以下叙述正确的是(C)A.K fθCo(NH3)62+]=K fθ[Co(NH3)63+]B. K fθ[Co(NH3)62+]>K fθ[Co(NH3)63+]C. K fθ[Co(NH3)62+]<K fθ[Co(NH3)63+]D.都不对6.[Ni(CN)4]2—为平面四方形构型,中心离子杂化轨道类型和d电子分别是(D)A.sp2,d7B.sp3,d8C.d2sp3,d6D.dsp2,d8二、填空题1.碳酸氯·硝基·四氨合铂(Ⅳ)的化学式为[Pt(NH3)4(NO2)Cl]CO3,配体是NH3、NO2、Cl,配位原子是N、Cl ,配位数是62.氨水装在铜制容器中,发生配位反应,生成了[Cu(NH3)4]2+,使容器溶解。
3.向Cu2++4NH3=[Cu(NH3)4]2+体系中加入NH3,平衡将向正方向移动,加入CN—, 平衡将向逆方向移动(填正、逆)4.实验测得[Fe(CN)6]3-络离子的磁矩为1.7B.M.,则中心离子Fe3+采用了__d2sp3____杂化形式,是_内_轨型络合物。
5.[Ag(S2O3)2]3-的K fθ=a,[ AgCl2]-的K fθ=b则[Ag(S2O3)2]3-+ 2Cl-= [ AgCl2]-+ 2 S2O32-的平衡常数为b/a。
无机及分析化学(习题含答案)-配位化合物

第九章 配位化合物与配位滴定法习题1.是非判断题1-1中心离子的未成对电子数越多,配合物的磁矩越大。
1-2配合物由内界和外界组成。
1-3配位数是中心离子(或原子)接受配位体的数目。
1-4配位化合物K 3[Fe(CN)5CO]的名称是五氰根·一氧化碳和铁(Ⅱ)酸钾。
1-5一般说来,内轨型配合物比外轨型配合物稳定。
1-6配合物中由于存在配位键,所以配合物都是弱电解质。
1-7同一种中心离子与有机配位体形成的配合物往往要比与无机配合体形成的配合物更稳定。
1-8配合物的配位体都是带负电荷的离子,可以抵消中心离子的正电荷。
1-9电负性大的元素充当配位原子,其配位能力强。
1-10在螯合物中没有离子键。
1-11配位物中心离子所提供杂化的轨道,其主量子数必须相同。
1-12配合物的几何构型取决于中心离子所采用的杂化类型。
1-13外轨型配离子磁矩大,内轨型配合物磁矩小。
1-14配离子的配位键越稳定,其稳定常数越大。
1-15氨水溶液不能装在铜制容器中,其原因是发生配位反应,生成[Cu(NH 3)4]2+,使铜溶解。
1-16在配离子[Cu(NH 3)4]2+解离平衡中,改变体系的酸度,不能使配离子平衡发生移动。
1-17已知[HgI 4]2-的4θβ=K 1,[HgCl 4]2-的4θβ=K 2,,则反应[HgCl 4]2-+4I -=[HgI 4]2-+4Cl -的平衡常数为K 1/K 2。
1-18 [Cu(NH 3)3]2+ 的积累稳定常数β3是反应[Cu(NH 3)2]2+ + NH 3⇔[Cu(NH 3)3]2+的平衡常数。
1-19已知θϕ[Fe 3+/Fe 2+]=0.77V ,电极反应[Fe(C 2O 4)3]3-+ e=[Fe(C 2O 4)2]2-+ C 2O 42-,在标准状态时,θϕ的计算式为:θθθθθϕϕc O C c c O C Fe c c O C Fe c Fe F /)(/])([/])([lg 0592.0)/e 2422242334223---+⋅++(= 。
第十一章配位化合物

第十一章 配位化合物 首 页 习题解析 本章练习 本章练习答案 章后习题答案 习题解析 [TOP]例7-1 固体CrCl 3·6H 2O 的化学式可能为〔Cr(H 2O)4Cl 2〕Cl·2H 2O 或〔Cr(H 2O)5Cl 〕Cl·H 2O 或〔Cr(H 2O)6〕Cl 3,今将溶解有0.200gCrCl 3·6H 2O 的溶液流过一酸性阳离子交换柱,在柱上进行离子交换反应: X n+(aq) + n (RSO 3H) (RSO 3)n X + n H +(aq)配合物正离子 阳离子交换树脂 交换后的交换树脂 交换下来的H+ 交换下来的H +用0.100mol·L -1NaOH 标准溶液滴定,计耗去22.50mL ,通过计算推断上述配合物的正确化学式〔已知Mr(CrCl 3·6H 2O)=266.5〕。
析 根据题中条件可知离子的物质的量与配合物的电荷数有确定的关系,因此只要确定离子的物质的量即可求出配离子的电荷,进而求出配合物的化学式。
解 0.200gCrCl 3•6H 2O 的物质的量为1mol 1000mmol mol266.5g 0.200g 1⨯⋅-=0.75mmol 滴定测得 n (H +)=22.50mL×0.100mol·L -1=2.25mmol由交换反应式知:1mol X n+可交换出n mol H +。
因0.75 mmol CrCl 3•6H 2O 交换出2.25 mmol 的H +,由此可得1 :n = 0.75 :2.25 n = 3即X n+为X 3+,所以配正离子只能是[Cr(H 2O)6]3+,配合物为[Cr(H 2O)6]Cl 3。
例7-2(1)根据价键理论,画出[Cd(NH 3)4]2+(μ=0μB )和[Co(NH 3)6]2+(μ=3.87μB )的中心原子与配体成键时的电子排布,并判断空间构型。
配位化合物习题及解析

配位化合物习题及解析————————————————————————————————作者: ————————————————————————————————日期:《配位化合物》作业参考解析1. 下列说法正确的是A.配合物的内界和外界之间主要以共价键相结合B.中心原子与配体之间形成配位键C.配合物的中心原子都是阳离子D.螯合物中不含有离子键【B】A、D:一般认为配合物的内界和外界之间主要以离子键相结合,因此螯合物中内界和外界之间是可以存在离子键的;C:中心原子可以是阳离子,也可以是中性原子,例如[Ni(C O)4];B:中心原子与配体化合时,中心原子提供杂化过的空轨道,配体提供孤对电子,而形成配位键。
2. 下列配合物命名不正确的是A. [Co(H2O)(NH3)3Cl2]Cl氯化二氯·三氨·一水合钴(Ⅲ)B.[Cr(NH3)6][Co(CN)6] 六氰合钴(Ⅲ)酸六氨合铬(Ⅲ)C.K[Co(NO2)3Cl3]三硝基·三氯合钴(Ⅲ)酸钾D.H2[PtCl6]六氯合铂(Ⅳ)酸【C】根据配体命名顺序,先无机后有机,先阴离子后中性分子,同类配体根据配位原子在字母表中的先后顺序进行命名。
对于C中的配合物而言,NO2-以N原子为配位原子时,命名为硝基,带一个负电荷,氯离子也是阴离子,同类配体,根据配位原子在字母表中的先后顺序,Cl-离子在前,NO2-离子在后,因此该配合物应该命名为“三氯·三硝基合钴(Ⅲ)酸钾”。
3. 下列配离子具有正方形或者八面体形结构,其中CO32-最有可能作为双齿配体的是A. [Co(NH3)4(CO3)]+B. [Co(NH3)5(CO3)]+C.[Pt(en)(NH3)(CO3)] D.[Pt(en)2(NH3)(CO3)]2+【A】根据题意,配离子具有正方形结构时,配位数为4,形成四个配位键;具有八面体结构时,配位数为6,形成6个配位键。
B:[Co(NH3)5(CO3)]+配离子中,已有5个氨作为配体,氨是单齿配体,形成5个配位键,因此该配离子中,CO32-离子只能是单齿配体,这样就形成了6个配位键;C:[Pt(en)(NH3)(CO3)] 配合物中,乙二胺(en)为双齿配体,形成2个配位键,氨为单齿配体,形成1个配位键,因此CO32-离子只能是单齿配体,这样就形成了4个配位键;D:[Pt(en)2(NH3)(CO3)]2+ 配离子中,乙二胺(en)为双齿配体,2个en形成4个配位键,氨为单齿配体,形成1个配位键,因此CO32-离子只能是单齿配体,这样就形成了6个配位键;A:[Co(NH3)4(CO3)]+配离子中有4个氨为配体,形成4个配位键,因此CO32-离子必须是双齿配体,这样就形成了4个配位键,如果CO32-离子是单齿配体,那么配离子的配位数为5,这与题意不符。
无机与分析化学第4章_习题答案

第四章配位化合物习题参考解答1•试举例说明复盐与配合物,配位剂与螯合剂的区别。
解复盐(如KCI・MgCl2 6H2O)在晶体或在溶液中均无配离子,在溶液中各种离子均以自由离子存在;配合物K2[HgI 4]在晶体与溶液中均存在[Hgl4]2-配离子,在溶液中主要以[Hgl4]2-存在,独立的自由Hg2+很少。
配位剂有单基配位剂与多基配位剂:单基配位剂只有一个配位原子,如NH3(配位原子是N);多基配位剂(如乙二胺H2N —CH2- CH2- NH2)含有两个或两个以上配位原子,这种多基配位体能和中心原子M 形成环状结构的化合物,故称螯合剂。
2. 哪些元素的原子或离子可以作为配合物的形成体?哪些分子和离子常作为配位体?它们形成配合物时需具备什么条件?解配合物的中心原子一般为带正电的阳离子,也有电中性的原子甚至还有极少数的阴离子,以过渡金属离子最为常见,少数高氧化态的非金属元素原子也能作中心离子,如Si(W )、P(V )等。
配位体可以是阴离子,如X-、OH-、SCN-、CN-、C2O4-等; 也可以是中性分子,如H2O、CO、乙二胺、醚等。
它们形成配合物时需具备的条件是中心离子(或原子)的价层上有空轨道,配体有可提供孤对电子的配位原子。
3. 指出下列配合物中心离子的氧化数、配位数、配体数及配离子电荷。
[CoCl2(NH3)(H2O)(en)]CI Na^AIF 6] K/FeQN"] Na2[Ca Y] [PtCl4(NH3)2]解K 2[PtCI 6] [Ag(NH 3)2]CI [Cu(NH 3)4]SO 4 K 2Na[Co(ONO )6]Ni(C0)4[Co(NH 2)(NO 2)(NH 3)(H 2O)(e n)]CI ©[Z nY]K 3【F e (C N )6】解二硫代硫酸合银⑴酸钠 酸铵; 四氯合铂(II)酸六氨合铂(II) 合铁(III)离子 硫酸一氯 一氨 二乙二胺合铬(III) 解 Na 3[Ag(S 2O 3)2] [Pt(NH 3)6][PtCl 4] [FeCl 2(C 2O 4)(en)] [CrCl(NH3)(en )2】SO 46. 下列配离子具有平面正方形或者八面体构型,试判断哪种配 离四硫氰酸根 二氨合铬(III) 二氯一草酸根一乙二胺NH 4[Cr(SCN )4(NH 3)2]子中的CO32—为螯合剂?[Co(CO3)(NH3)5]+[Co(CO3)(NH 3)4]+[Pt(C O 3)(en)] [Pt(CO3)(NH3)(en)]解[Co(CO3)(NH3)4]+、[Pt(C03)(en)]中CO32-为螯合剂。
配位化学习题答案

配位化学习题答案
配位化学学习题答案
在配位化学中,配位化合物是由中心金属离子和周围的配体组成的。
学习配位
化学需要掌握一定的理论知识和解题技巧。
下面是一些配位化学学习题的答案,希望能帮助大家更好地理解和掌握这一知识点。
1. 问题:写出以下配位化合物的配体名称和化学式:
(a) [Co(NH3)6]Cl3
(b) K4[Fe(CN)6]
(c) [Cu(H2O)4]SO4
答案:
(a) 配体名称:氨
化学式:[Co(NH3)6]Cl3
(b) 配体名称:氰化物
化学式:K4[Fe(CN)6]
(c) 配体名称:水
化学式:[Cu(H2O)4]SO4
2. 问题:计算以下配位化合物的配位数和配体的数量:
(a) [Pt(NH3)4]Cl2
(b) [Co(en)3]Cl3
(c) [Ni(CN)4]2-
答案:
(a) 配位数:4
配体数量:4
(b) 配位数:6
配体数量:3
(c) 配位数:4
配体数量:4
3. 问题:根据配位化合物的性质,判断以下说法的正误:
(a) 配位化合物的颜色与中心金属离子的电子构型有关。
(b) 配位化合物的稳定性与配体的配位能有关。
(c) 配位化合物的磁性与中心金属离子的自旋态有关。
答案:
(a) 正确
(b) 正确
(c) 正确
通过以上学习题的答案,我们可以看到配位化学涉及到配体的命名、配位数的计算以及配位化合物的性质等多个方面。
希望大家在学习配位化学的过程中能够多加练习,加深对这一知识点的理解和掌握。
普通化学 第八章答案
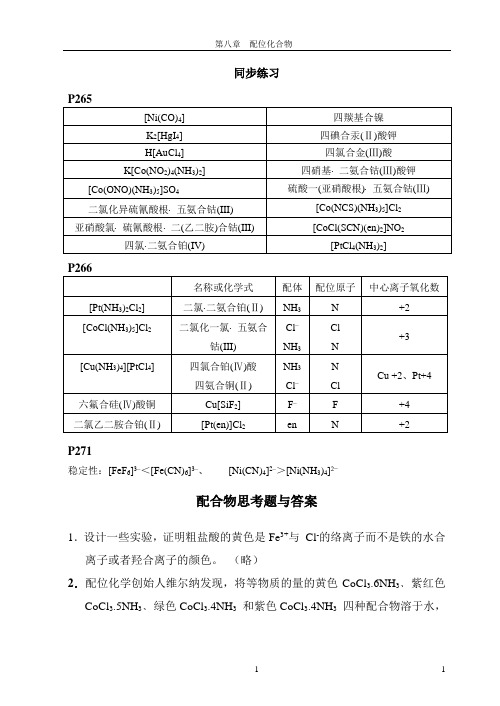
同步练习P265[Ni(CO)4]四羰基合镍K2[HgI4] 四碘合汞(Ⅱ)酸钾H[AuCl4]四氯合金(Ⅲ)酸K[Co(NO2)4(NH3)2] 四硝基⋅二氨合钴(Ⅲ)酸钾[Co(ONO)(NH3)5]SO4硫酸一(亚硝酸根)⋅五氨合钴(Ⅲ) 二氯化异硫氰酸根⋅五氨合钴(III) [Co(NCS)(NH3)5]Cl2亚硝酸氯⋅硫氰酸根⋅二(乙二胺)合钴(III)[CoCl(SCN)(en)2]NO2四氯⋅二氨合铂(IV)[PtCl4(NH3)2]P266名称或化学式配体配位原子中心离子氧化数[Pt(NH3)2Cl2] 二氯⋅二氨合铂(Ⅱ) NH3N +2[CoCl(NH3)5]Cl2二氯化一氯⋅五氨合钴(III) Cl–NH3ClN+3[Cu(NH3)4][PtCl4] 四氯合铂(Ⅳ)酸四氨合铜(Ⅱ) NH3Cl–NClCu +2、Pt+4六氟合硅(Ⅳ)酸铜Cu[SiF2] F– F +4二氯乙二胺合铂(Ⅱ) [Pt(en)]Cl2en N +2P271稳定性:[FeF6]3–<[Fe(CN)6]3–、[Ni(CN)4]2–>[Ni(NH3)4]2−配合物思考题与答案1.设计一些实验,证明粗盐酸的黄色是Fe3+与Cl-的络离子而不是铁的水合离子或者羟合离子的颜色。
(略)2.配位化学创始人维尔纳发现,将等物质的量的黄色CoCl3.6NH3﹑紫红色CoCl3.5NH3﹑绿色CoCl3.4NH3和紫色CoCl3.4NH3四种配合物溶于水,加入硝酸银,立即沉淀的氯化银分别为 3 ﹑2 ﹑1 ﹑1mol,请根据实验事实推断它们所含的配离子的组成。
答:配离子分别是[Co(NH3)6]3+, [Co(NH3)5Cl]2+ , [Co(NH3)4Cl2] +, [Co(NH3)4Cl2] +,颜色不同的原因是有同分异构体。
3.实验测得Fe(CN)64-和Co(NH3) 63+均为反磁性物质(磁矩等于零),问它们的杂化轨道类型。
第六章配位化合物结构与性质习题答案

第六章配位化合物结构与性质习题答案6150(1) [RhCl6]3-(2) [Ni(H2O)6]2+6001分裂成两组, d22yx 和2zd处于高能级,d xy,d yz,d xz处于低能级。
6002X-为弱场配体,CN-为强场配体, NH3介于两者之间。
6003(A)6004否6005(C)6006-2△06007此结论仅在O h场中,中心离子d 电子数n=4--7 时才成立。
6008-0.4△0×6 =-2.4△06009假设填T d空隙LFSE(Td)=[4×(-0.267△)+4×0.178△] = -0.356△假设填O h空隙LFSE(Oh)=[6×(-0.4△)+2×0.6△] = -1.2△Ni2+倾向填入稳定化能大的空隙中,所以NiAl2O4为反尖晶石。
6010小6011参看《结构化学基础》 (周公度编著) p.275 6012(1) t 2g 4 e g 2(2) - 0.4△ (3) │M s │=6π2h(4) μ= 26μβ6013(D) 6014能级次序: d 22y x -最高, 2d z 次之,d xy 再次之,d yz ,d xz 最低。
理由:①因z 方向拉长,相应xy 平面上的 4 个L 靠近,所以d 22y x -能级升高,d z2能级下降; ②因为 d xy 在xy 平面内,受L 的影响大,所以d xy 能级上升,而d yz , d xz 受xy 平面上的 4 个L 排斥小,所以能级下降。
③但因z 方向上方还有 1 个L,加之2z d 的"小环"在xy 平面上,可受到L 的直接作用,所以2d z 能级高于 d xy 能级。
6015O h 点群,说明Jahn-Teller 效应为 0,按强场排:( t 2g )6(e g )0LFSE =-2.4△0 6016(B), (D) 6017否 6018(B)6019(1) [Fe(CN)6]3-: μ= [n(n+2)]1/2μβ; n1= 1[FeF6]3-: n2= 5(2) 中心离子Fe3+为d5结构,配位场为八面体场。
无机化学第九章 配位化合物习题答案

第九章配位化合物习题答案1.命名下列配合物,并指出中心离子的配位数和配体的配位原子。
(1) [Co(NH3)6]C12(2) [Co Cl (NH3)5]C12(3) [Pd (SCN)2(PPh3)2] (4) [Pd (NCS)2(PPh3)2](5) Na3[Ag(S2O3)2] (6) [Ni(C2O4) (NH3)2]答:配合物名称(1)二氯化六氨合钴(II)(2)二氯化一氯·五氨合钴(III)(3)二硫氰酸根·二* (三苯基磷)合钯(II)(4)二异硫氰酸根·二(三苯基磷)合钯(II)(5)二(硫代硫酸根)合银(I)配离子(6)二氯化四氨·二水合镍(II)* 为区别配体数目与配体名称,有时用““二(相当于di-)”字,说成“二硫氰酸根·双(三苯基磷)合钯(II)”。
2.写出下列配合物的化学式:(1) 三硝基·三氨合钴(III)(2) 氯化二氯·三氨·一水合钴(III)(3) 二氯·二羟基·二氨合铂(IV)(4) 六氯合铂(IV)酸钾答:配合物化学式(1)[Co(NO2)3 (NH3)3](2)[Co Cl2 (NH3)3(H2O)]C1(3)[Pt Cl2 (OH)2 (NH3)2](4)K2[PtCl6]9.在[Zn (N H3)4]SO4溶液中,存在下列平衡:[Zn (N H3)4]2+⇌ Zn 2+ + 4NH3分别向溶液中加入少量下列物质,请判断上述平衡移动的方向。
(1)稀H2SO4溶液;(2)NH3· H2O;(3)Na2S溶液;(4)KCN溶液;(5)CuSO 4溶液答:(1)右;(2)左;(3)右;(4)右;(5)右10.在含有2.5⨯10-3 mol·L -1 AgNO 3和0.41 mol·L -1 NaCI 溶液里,如果不使AgCl沉淀生成,溶液中最少应加入CN - 浓度为多少? 已知[Ag(CN)2]- K s (β2) = 1.26 ⨯1021 ,AgCl K sp = 1.56 ⨯10-10解:首先考虑沉淀溶解平衡 Ag + + Cl - = AgCl(s) 根据溶度积规则,有 [Ag +] [ Cl -]= K sp如果不使AgCl 沉淀生成,应满足[Ag +]< K sp / [ Cl -]=1.56 ⨯10-10/0.41=3.80⨯10-10 (mol/L) 然后考虑配位平衡Ag + + 2CN - = Ag(CN)2-初始浓度 2.5⨯10-3 a 0平衡浓度 3.80⨯10-10 a – 2⨯(2.5⨯10-3–3.80⨯10-10) 2.5⨯10-3–3.80⨯10-10 ≈ a –5.0⨯10-3 ≈ 2.5⨯10-3根据配位平衡原理,有 s22K ]CN ][Ag [])CN (Ag [=-+-为使[Ag +]< 3.80⨯10-10 mol/L ,应满足s 2K ]Ag [])CN (Ag []CN [+--> 将平衡浓度代入,得321103100.51026.11080.3105.2a ---⨯+⨯⨯⨯⨯>=7.2⨯10-7+5.0⨯10-3 ≈ 5.0⨯10-3 (mol·L -1)答:溶液中最少应加入CN - 浓度为5.0⨯10-3 mol·L -1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十九章配位化合物
1、[Pt(NH3)2Cl4]
1、配合物:K2PtCl6, Co(NH3)6Cl3, CuSO4·5H2O
螯合物:Ni(en)2Cl2, Cu(NH2CH2COO)2
复盐:(NH4)2SO4·FeSO4·6H2O KCl·MgCl2·6H2O
简单盐:Cu(OOCH3)2
3、(1)六氯合锑(III)酸铵
(2)四氢合铝(III)酸锂
(3)三氯化三(乙二胺)合钴(III)
(4)氯化二氯·四水合钴(III)
(5)二水合溴化二溴·四水合钴(III)
(6)羟·水·草酸根·乙二胺合铬(III)
(7)六硝基合钴(III)配阴离子
(8)氯·硝基·四氨合钴(III)配阳离子
(9)三氯·水·二吡啶合铬(III)
(10)二氨·草酸根合镍(II)
4、(1)[Pt(NH3)2(NO2)Cl] 平面正方形2种异构体
H3N NO2H3N NO2
Pt Pt
H3N Cl H3N Cl (2)[Pt(Py)(NH3)ClBr] 平面正方形3种异构体
Cl Py Cl NH3
Pt Pt
Br NH3 Br Py
Cl 3
Pt
Py Br
(3)[Pt(NH3)2(OH)2Cl2] 八面体5种异构体
3
NH3NH3 NH3
33
OH Cl
(4)[Co(NH3)2(NO2)4]-八面体2种异构体
23
O22O2
NH3NO2
(5)[Co(NH3)3(OH)3] 八面体2种异构体
H3H3
NH3 OH
(6)[Ni(NH3)2Cl2] 四面体无异构体
(7)[Cr(en)2(SCN)2]SCN
[Cr(en)2(SCN)2]-八面体2种异构体
en
SCN en
(8)[Co(en)3]Cl3
[Co(en)3]3+八面体2种异构体
(9)[Co(NH3)(en)Cl3] 八面体2种异构体
(10)[Co(en)2(NO2)2]Cl2
[Co(en)2(NO2)2]2+八面体2种异构体
5、该中心金属离子可能是Fe2+
)2
n
n= 4.90 n = 4
(
即在八面体场中有四个成单电子
八面体强场中磁矩为零,即无成单电子
故Fe2+符合题意
6、高自旋的有:(1),(2),(5),(7)
低自旋的有:(3),(4),(6),(8)
内轨型的有:(3),(4),(6),(8)
外轨型的有:(1),(2),(5),(7)
7、dsp2
8、由软硬酸碱规则:“硬亲硬,软亲软,软硬交界就不管”
9、(1)Al3+与F-的配合物更加稳定,Al3+为硬酸;而碱F-的硬度比Cl-大
(2)Pd2+与RSH配合后更加稳定,Pd2+为软酸,而RSH为软碱,ROH为硬碱。
(3)Cu2+与NH3结合更加稳定。
(4)Cu2+与NH2CH2COOH结合更加稳定,因为前者的配体中有N,后者仅有O,N的配位能力比O强。
10、 解:设[Ag +]为x mol•dm -3
Ag + + 2CN - =Ag(CN)2-
x 2x 0.1-x
2121025.1)2(1.0⨯=-x x x 得:x = 2.7×10-8mol•dm -3 Q = [Ag +][Cl -] = 2.7×10-8×0.10 = 2.7×10-9
Q > Ksp H (AgCl ),因而会有AgCl 沉淀析出
11、解: 设生成 Cu(NH 3)42+后Cu 2+的浓度为xmol•L -1
++⇔+24332)(4NH Cu NH Cu
x 6-4(0.01-x) 0.01-x
4)]
01.0(46[01.0x x x --- = 2.09 × 1013 得: x = 3.79 × 10-19 mol•dm -3
Q = [Cu 2+] – [OH -]2 = 3.79 × 10-19×0.012
= 3.79 × 10-23
Q 小于Ksp H 故铜氨配合物不能被破坏
12、解: K 稳,Fe(SCN)3 = 333]
][[])([-+SCN Fe SCN Fe 633636]
][[][][-+-
-=F Fe FeF FeF K 稳 又 [SCN -] = [F-] = 1 mol•dm -3
3
33636][][][)()(稳稳SCN Fe K SCN Fe FeF K FeF =∴-- [FeF 6]3-/[Fe(SCN)] = 1×1016/2.0×103 = 5×1012
13、解:Ksp H AgI = [Ag +][I -]
3317
75
533
5233523232323232331031.0103.91012.1101101][101])([101][][)(])([]/[]][[][-------+---+++++
∙=∙=⨯⨯⨯⨯⨯⨯=∙⨯=∙⨯=∙=-=cm m ol cm m ol NH cm m ol NH Ag cm m ol I NH NH Ag K NH Ag I AgI Ksp NH Ag NH Ag NH Ag K 稳稳得:)()(θ
14、解:
]lg[059.0/]/[][1]][[][][0.1][][2)(22223
22++-+-+--
----
--+===∙==+⇔+Au Au Au E Au CN Au E Au CN Au CN Au CN Au K dm mol CN CN Au CN Au e CN Au )
()()()()(标准状态时:稳θθθ =1.691 + 0.059lg1/K 稳H
=1.691+0.059lg1/2×1038
=-0.57V
15、解:E H = E H (H+/H 2)- E H [Cu (NH3)42+/Cu] = 0.0300V 即 E H [Cu (NH 3)42+/Cu] = -0.0300V
由 E H [Cu (NH 3)42+/Cu] = E H (Cu 2+/Cu ) + 0.059/2lg[Cu 2+]
12
24
32224
3321049.3lg 2059.034.00300.0/1lg 2/059.034.0]/[/1][]
[14⨯=-
=-+===⇔++++++θθθθθ稳稳稳稳稳得:)(即得:)(K K K Cu NH Cu E K Cu Cu K NH Cu NH Cu 16、解:在水溶液中,
)2/3(++Co Co E θ>)/(22O H O E θ
故Co3+能氧化水
4Co 3++2H 2O=4Co 2+O 2↑+4H +
V OH p O p OH O E OH O E OH e O H O dm m ol OH dm m ol NH V NH Co K NH Co K Co Co E Co Co Co Co
E NH Co NH Co E 45.0)1024.4(1lg 4059.0401.0][/)(lg 4059.0)/()/(4441024.4108.10.1][0.1][04.01058.11038.1lg 059.081.1]
)([])([lg 059.0)2/3(][][lg 059.0)/(])(/)([434222223353335
5
2632632323263363=⨯+=+==++∙⨯=⨯⨯=∙==⨯⨯+==++=+=---
--
------++++++++θθθθ
θθθ则:
设稳稳
])(/)([263363+
+NH Co NH Co E θ<)/(2-OH O E
故 Co (NH 3)63+不能氧化水
17、解:因各级稳定常数都比较小,Cl -过量很多故可以认为:
[Cl -] = 1.0 mol•L -1
[Cl -] + [FeCl 2+] + 2[FeCl 2+] + 3[FeCl 3] + 4[FeCl 4-] =1.0 mol•L -1
[Fe 3+] + [FeCl 2+] + [FeCl 2+] + [FeCl 3] + [FeCl 4-]=0.010 mol•L -1 2.4]
][[][321==-++Cl Fe FeCl k [FeCl 2+] = 4.2[Fe 3+] 3.1]
][[][222==-++Cl FeCl FeCl k [FeCl 2+] = 1.3×4.2[Fe 3+] =5.5[Fe 3+] 040.0]][[]
[233==-+Cl FeCl FeCl k [FeCl 3] = 0.040[FeCl 2+]
= 0.04×1.3×4.2[Fe 3+]
=0.22[Fe 3+]
012.0]
][[][344==--Cl FeCl FeCl k [FeCl 4-]=0.012[FeCl 3] =0.012×0.04×1.3×4.2[Fe 3+]
=0.0026[Fe 3+]
则:[Fe 3+] + 4.2[Fe 3+] + 5.5[Fe 3+] +0.22[Fe 3+] + 0.0026[Fe 3+]=0.010mol•L -1 可得:[Fe 3+]=9.2×10-4 mol•L -1
由此可以得到:FeCl 2+的浓度最大。
