氢原子光谱玻尔氢原子理论
3433第三十四讲氢原子光谱的实验规律玻尔理论

1913年, 28岁的研究生 玻尔将普朗克、爱因斯坦的 量子理论推广到卢瑟福的原 子有核模型中,并结合原子 线光谱的实验规律,提出了 关于氢原子模型的三个假设, 奠定了原子结构的量子理论 基础。为此他获得1922年诺 贝尔物理学奖。
一、氢原子光谱的实验规律 不同原子的辐射光谱特征是完全不同的,研究
原子光谱的规律是为研究原子结构,氢原子是结构 最简单的原子,对氢原子光谱规律研究发现,在可 见光和紫外区氢原子的谱线如图。
连 续
H
紫 H 青 H 深绿 H
红H
氢原子巴耳末系谱线图
一、氢原子光谱的实验规律 1.氢原子光谱 1)是彼此分离的线光谱, 每条谱线有确定波长。
连 续
H
紫 H 青 H 深绿 H
对应一个 m 就构成一个谱线系。
令:
T(m)
R m2
,
T (n)
R n2
称为光谱项。
里兹组合原则: T(m) T(n)
普芳德系 布喇格系 帕邢系
巴耳末系
赖曼系
波长 5.0 4.0 3.0 2.0 1.0
红
外
线
0.8 0.6 0.4 0.2
mm
可见光 紫外线
1
R
1 m2
rn
+e
部分质量都集中于原子核。
M核 me
由牛顿二定律: 由库伦定律:
Fn
Fn
man
m
e2
vn2 rn
4 0rn2
由假设2): L mn rn
nh 2π
e2
4 0rn2
m
氢原子的光谱线解析与理论解释

氢原子的光谱线解析与理论解释光谱线是物质在光的作用下发出或吸收的特定频率的电磁波。
而氢原子的光谱线解析与理论解释,一直以来都是物理学家们研究的热点之一。
本文将从氢原子的光谱线的观测、解析以及理论解释等方面进行探讨。
首先,我们来看氢原子的光谱线的观测。
早在19世纪初,德国物理学家巴尔末发现了氢原子的光谱线,这一发现为后来的研究奠定了基础。
通过将氢气放电于真空管中,巴尔末观察到了一系列明亮的彩色线条。
这些线条经过仔细测量和分类,被分为了几个系列,分别称为巴尔末系列、帕邢系列和卢瑟福系列。
这些系列中的每一个线条都对应着氢原子在特定能级之间跃迁所产生的光。
接下来,我们来解析氢原子的光谱线。
根据量子力学的理论,氢原子的能级是量子化的,即只能取特定的数值。
这就意味着氢原子在不同能级之间的跃迁所产生的光具有特定的频率和波长。
而这些频率和波长正是观察到的光谱线。
例如,巴尔末系列中的线条对应着氢原子的基态到第一激发态之间的跃迁,帕邢系列对应着第一激发态到第二激发态之间的跃迁,而卢瑟福系列则对应着更高能级的跃迁。
那么,为什么氢原子的能级是量子化的呢?这就涉及到氢原子的理论解释。
根据量子力学的理论,氢原子的能级由薛定谔方程给出。
薛定谔方程是描述微观粒子的波函数演化的方程,通过求解薛定谔方程,可以得到氢原子的能级和波函数。
而氢原子的能级量子化的原因是由于氢原子中的电子和质子之间的库仑相互作用。
这种相互作用会导致电子在氢原子中的运动受到限制,从而使得电子只能在特定的能级上存在。
此外,氢原子的光谱线还可以通过波尔模型进行解释。
波尔模型是根据经典力学和电磁学的理论,对氢原子的能级和光谱线进行解释的简化模型。
根据波尔模型,氢原子的电子绕着质子作圆周运动,而电子的能级由其运动半径决定。
当电子从一个能级跃迁到另一个能级时,会吸收或发射特定频率的光子,从而产生光谱线。
波尔模型的成功在一定程度上解释了氢原子的光谱线,但它是建立在经典力学和电磁学的基础上,无法解释一些量子效应。
玻尔理论的基本假设现象氢原子光谱是分立线状

原子的能级结构
回顾
19世纪末20世纪初,人类叩开了微观世界
的大门,物理学家根据研究提出了关于原子
结构的各种模型,卢瑟福的核式结构模型能
够很好
盾.
经典电磁理论
经典电磁理论认为:电子绕核作匀速圆周运动, 绕核运动的电子将不断向外辐射电磁波。由于原子 不断地向外辐射能量,能量 v 逐渐减小,电子绕核旋转的频 e F
Em>En 发射光子, Em<En 吸收光子
能级结构猜想
能级:原子内部不连续的能量称为原子的能级。
数值上等于原子在定态时的能量值。 跃迁:原子从一个能级变化到另一个能级的过程。 在跃迁的过程中,原子辐射(或吸收)光子的能 量为:
hv= Em- En
Em和En分别为跃迁前后的能级
(1)处于高能级的原子会自发
由 T ( m ) T ( n ) 知道,氢原子辐射光谱的波长取决 于两光谱项之差;而hv=Em-En式则揭示出氢原子 辐射光的频率取决于两能级之差。 能级与光谱项之间的关系 最先得出氢原子能级表达式的,是丹麦物理学 家玻尔,他在吸取前人思想的基础上,通过大胆假 设,推导出氢原子的能级满足:
在解决核外电子的运动时 成功引入了量子化的观念
同时又应用了“轨 道”等经典概念和 有关牛顿力学规律
除了氢原子光谱外,在解决 其他问题上遇到了很大的困难.
半经典半量子理论,存在逻辑上的缺点,即把微观粒子看成是遵 守经典力学的质点,同时,又赋予它们量子化的特征。
玻尔理论解决了原子的稳定性和 辐射的频率条件问题,把原子结构的 理论向前推进了一步 .
率也逐渐改变,原子的发射光 谱应是连续谱。由于原子总能 量减小,电子将最终逐渐接近 原子核,而使原子变得不稳定。
高中物理氢原子光谱知识点

高中物理氢原子光谱知识点一、氢原子光谱的发现历程。
1. 巴尔末公式。
- 1885年,巴尔末发现氢原子光谱在可见光区的四条谱线的波长可以用一个简单的公式表示。
巴尔末公式为(1)/(λ)=R((1)/(2^2) - (1)/(n^2)),其中λ是谱线的波长,R称为里德伯常量,R = 1.097×10^7m^-1,n = 3,4,5,·s。
- 巴尔末公式的意义在于它反映了氢原子光谱的规律性,表明氢原子光谱的波长不是连续的,而是分立的,这是量子化思想的体现。
2. 里德伯公式。
- 里德伯将巴尔末公式推广到更一般的形式(1)/(λ)=R((1)/(m^2)-(1)/(n^2)),其中m = 1,2,·s,n=m + 1,m + 2,·s。
当m = 1时,对应赖曼系(紫外区);当m = 2时,就是巴尔末系(可见光区);当m = 3时,为帕邢系(红外区)等。
二、氢原子光谱的实验规律与玻尔理论的联系。
1. 玻尔理论对氢原子光谱的解释。
- 玻尔提出了三条假设:定态假设、跃迁假设和轨道量子化假设。
- 根据玻尔理论,氢原子中的电子在不同的定态轨道上运动,当电子从高能级E_n向低能级E_m跃迁时,会发射出频率为ν的光子,满足hν=E_n-E_m。
- 结合氢原子的能级公式E_n=-(13.6)/(n^2)eV(n = 1,2,3,·s),可以推出氢原子光谱的波长公式,从而很好地解释了氢原子光谱的实验规律。
例如,对于巴尔末系,当电子从n(n>2)能级跃迁到n = 2能级时,发射出的光子频率ν满足hν = E_n-E_2,进而可以得到波长与n的关系,与巴尔末公式一致。
2. 氢原子光谱的不连续性与能级量子化。
- 氢原子光谱是分立的线状光谱,这一现象表明氢原子的能量是量子化的。
在经典理论中,电子绕核做圆周运动,由于辐射能量会逐渐靠近原子核,最终坠毁在原子核上,且辐射的能量是连续的,这与实验观察到的氢原子光谱不相符。
氢原子光谱玻尔氢原子理论

根据电子绕核作圆周运动的模型及角动量 量子化条件可以计算出氢原子处于各定态时的 电子轨道半径。
玻尔的氢原子理论
rn n2 (m0he22 ),n 1,2,3,
r1 0.5291010m 玻尔 半径
电子处在半径为 rn的轨道上运动时,可以计
算出氢原子系统的能量 En为
En
1 n2
பைடு நூலகம்
(8m0e2h4 2 ), n
● 量子化条件的引进没有适当的理论解释。 ● 对谱线的强度、宽度、偏振等无法处理。
氢原子光谱
例题18-6 在气体放电管中,用能量为12.5eV的电子通 过碰撞使氢原子激发,问受激发的原子向低能级 跃迁时,能发射那些波长的光谱线?
解: 设氢原子全部吸收电子的能量后最高能激发到第n
个能级,此能级的能量为
态跃迁到另一能量为 Ek的定态时,就要发射
或吸收一个频率为 kn 的光子。
kn
En
Ek h
玻尔频率公式
玻尔的氢原子理论
(3)量子化条件 在电子绕核作圆周运动中,
其稳定状态必须满足电子的角动量 L等于 h
的整数倍的条件。
2
L n h , n 1,2,3,
2
n为量子数
角动量量子化条件
3. 氢原子轨道半径和能量的计算
§18-4 氢原子光谱 玻尔的氢原子理论
1. 氢原子光谱的规律性
原子发光是重要的原子现象之一, 光谱学 的数据对物质结构的研究具有重要意义。
氢原子谱线的波长可以用下列经验公式表示:
~
R(
1 k2
1 n2
)
~ 1
k 1,2,3, n k 1, k 2, k 3,
波数
R 1.096776 107 m-1 里德伯常量
我们主要研究了氢原子的光谱规律及玻尔的氢原子理论

里n* 称为有效量子数。
从所得的光谱可以计算出各条谱线对应的有效量子数,如表4.1所
示表中的有效量子数 n* 有些接近整数(第一辅线系和柏格曼系)
有些离整数远一些(第二辅线最远,主线系),且都一般都比n略 小,可写成
n* n
Δ 称为量子数亏损,我们注意到,同一线系的Δ 差不多相等。
这是因为同一线系的末态是相同的,而初态的电子轨道角动量量 子数相同。
二、碱金属原子的光 谱在前面讨论氢原子光谱时,我们已知道,氢原子的光谱可表示为
~
RH
1 m2
1 n2
~
RH n2
式中第一项为原子跃迁的终态,决定光谱所在的线系,第二项
为原子跃迁的初态。
在同一线系中(m相同)随着n的增大,谱线的波长越来越短,且 间隔越来越小,最后趋于线系限。
用能级图表示为如图所示(锂原 子):
从图中可以看出,碱金属原子能级与氢原子能级不同。
氢原子的能级只与主量子数n有关,而碱金属原子的能级除了与
主量子数有关外,还与电子的轨道角量子数l有关。 图中把能级按l值分类,l相同的能级画在同一列上。 n相同而l不同的能级有较大差别,l愈小能级越低。 n越小,则不同l的能级差别越大。
玻尔理论无法解释谱线的这种精细结构。
模型的局限性还表现在它缺乏计算原子其它性质的理论方 法例。如不能计算出不同谱线的相对强 度换。言之,处在n=3态上的电子有多少次直接跳到1态上,有多少 次先跳到2再到1上发出两种光。对此玻尔理论无能为力。
其问题出在理论结构本身,它是经典理论与量子条件的结合(所 以又称为旧量子论),其量子条件没有理论根据,缺乏逻辑的统 一性。
第一辅线(漫线系) ~ 2 p nd n 3,4 ~ 3 p nd n 3,4
氢原子的能级与光谱.

氢原子的能级与光谱·爱因斯坦1905年提出光量子的概念后,不受名人重视,甚至到1913年德国最著名的四位物理学家(包括普朗克)还把爱因斯坦的光量子概念说成是“迷失了方向”。
可是,当时年仅28岁的玻尔,却创造性地把量子概念用到了当时人们持怀疑的卢瑟福原子结构模型,解释了近30年的光谱之谜。
§1 氢原子的能级与光谱一、玻尔的氢原子理论(一)玻尔的基本假设1.定态假设:原子只可能处于一系列不连续的能量状态E1, E2, E3,…。
处于这些状态的原子是稳定的,电子虽作加速运动,但不辐射电磁波。
2.频率条件:原子从某一定态跃迁至另一定态时,则发射(或吸收)光子,其频率满足玻尔在此把普朗克常数引入了原子领域。
(二)玻尔的氢原子理论 1.电子在原子核电场中的运动(1)基本情况:核不动;圆轨道;非相对论。
(2) 用经典力学规律计算电子绕核的运动·电子受力:·能量:得f f = - 14πε0 ( )Ze 2r 21 ε0 ( ) Ze2 r = m ( )υ2r1 2E = m υ2 - 1 4πε0 ( ) Ze2 r E = -Ze 28πε0r2.轨道角动量量子化条件玻尔假定:在所有圆轨道中,只有电子的角动量满足下式的轨道才是可能的。
玻尔引进了角动量的量子化。
3.轨道和速度 ·r n = n 2r 1 ,(玻尔半径) r 1= 0.529 Å· υn= υ1/n ,4πε0h 2 r 1 = ( me 2 )( ) 1 Z 4πε0hυ1 = Ze 2)可见, 随n↑⇒r n↑,υn↓4.能级---能量量子化将r n代入前面E式中,有n = 1,2,3,…)R:里德伯常数(见后)基态能量:E1= -13.6 eV可见,随n↑⇒E n↑,∆E n↓*玻尔的理论是半经典的量子论:对于电子绕核的运动,用经典理论处理;对于电子轨道半径,则用量子条件处理。
氢原子光谱的特征

)
1 r 2s in
2θ
2 2φ
]
8π2m
Ze2
h2
(E
)Ψ 0 r
(2)
(2)式即为薛定谔方程在球坐标下的形式。经过坐标变换,
三个变量不再同时出现在势能项中。
如果我们把坐标变换作为解薛定谔方程的第一步,那么变量 分离则是第二步。
解薛定谔方程(2)得到的波函数应是 ( r,, )。
1-3 波函数和原子轨道
波函数 的几何图象可以用来表示微观粒子活动的区域。
1926 年,奥地利物理学家薛定谔(Schodinger ) 提出 一个方程,被命名为薛定谔方程。波函数 就是通过解 薛定谔方程得到的。
薛定谔方程
2 x 2
2 y2
2 z 2
82m h2
(E
我们采取坐标变换的方法来解决(或者说简化)这一问题。 将三维直角坐标系变换成球坐标系。
将直角坐标三变量 x,y,z 变换成球坐标三变量 r,, 。
P 为空间一点
r OP 的长度
(0 — )
z
OP 与 z 轴的夹角 ( 0 — )
OP 在 xoy 平面内的投影 OP′
P
与 x 轴的夹角 ( 0 — 2 )
V)
0
(1)
这是一个二阶偏微分方程
式中 波函数 , E 能量 , V 势能 , m 微粒的质量, 圆周率 , h 普朗克常数
,
,
x
y
z
偏微分符号
2 , x 2
2 , y 2
2 z 2
二阶偏微分符号
解二阶偏微分方程将会得到一个什么结果呢 ?
氢原子光谱、玻尔理论、德布罗意波

~ = R( 1 − 1 ) ν 赖曼系 12 n2 ~ = R( 1 − 1 ) 帕邢系 ν 32 n2 ~ = R( 1 − 1 ) 布喇开系 ν 42 n2 ~ 普芳德系 ν = R( 1 − 1 ) 52 n2
巴尔末系
~ = 1 = R( 1 − 1 ) , v λ 22 n2
态能量 态能量 ( n > 1)
E n = E1 n
2
基态 n =1
−13.6
(47)氢原子光谱、玻尔理论、德布罗意波 47)氢原子光谱、玻尔理论、
玻尔理论对氢原子光谱的解释
hν = Ei − E f
4
E1 En = 2 n
~ = 1 = ν = E1 ( 1 − 1 ) v c hc n 2 n i2 λ f 其中 ni > n f
在可见光范围内的谱线即为所求。 在可见光范围内的谱线即为所求。 可见光的谱线为巴耳末线系。 可见光的谱线为巴耳末线系。 在此为m=4和m=3跃迁到 在此为 和 跃迁到 n=2的两条,波长为: 的两条, 的两条 波长为:
n =4 n =3 n =2 n =1
λ42 = 486.1nm
m λ32 = 656.3n
E m e 1 = 2 3 = .097×107 m−1 ≈ R 里德伯常量) (里德伯常量) 1 hc 8 0 h c ε 氢 n=∞ E∞ = 0 原 n=4 子 与光 布 n=3 能 谱 n=2 级
跃 迁 系
n =1
E
(47)氢原子光谱、玻尔理论、德布罗意波 47)氢原子光谱、玻尔理论、
(1)将一个氢原子从基态激发到 )将一个氢原子从基态激发到n=4的激发态需要 的激发态需要 多少能量? 多少能量?(2)处于 )处于n=4的激发态的氢原子可发出 的激发态的氢原子可发出 多少条谱线? )其中多少条为可见光谱线, 多少条谱线? (3)其中多少条为可见光谱线,其 光波波长各多少? 光波波长各多少? 解: 1)使一个氢原子从基态激发到 ( ) n=4 激发态需提供能量为 E1 ∆E = E4 − E1 = 2 − E1 4 −13.6 = − ( −13.6 ) 2 4 = 12.75eV ≈ 2×10−18 J
第4节氢原子光谱玻尔理论

1第4节 氢原子光谱 玻尔理论一、 氢原子光谱,422-=n n B λ∞=,,5,4,3 nA =7.3645B αH βH γH ∞H ,∞→nB =∞λ巴耳末系,:线系极限∞H =:线系极限波长B =∞λA 7.3645波数:沿波线单位长度内波的个数 ν~cνλν==1~λ )121()121(441(1411~2222222nR n B n B n n B -=-=-=-==λν,5,4,3=n 里德伯公式:里德伯恒量1710096776.14-⨯==m BR 帕邢系:, )131(1~22n R -==λν,6,5,4=n 原子光谱实验规律:“原子光谱都是彼此分立的线状光谱,每一条光谱线的波数由 两个光谱项的差值决定” 里兹并合原理,, )()(~n T k T -=νN k n ∈,k n >、:光谱项)(k T )(n T 氢原子:,2)(k R k T =2)(nRn T =碱金属原子:,2)()(α+=k R k T 2)()(β+=n Rn T 、都给定,给出一条光谱线的波数k n 一定,所有的取值对应的谱线构成一个谱线系 k n 不同,给出不同的谱线系 k二、 玻尔理论1、 原子的有核模型1911,卢瑟夫,粒子散射实验α 有核模型 与经典理论矛盾 按照经典理论: 原子光谱应是连续的,原子是不稳定的2、 玻尔的氢原子理论c2(1) 定态假设:原子只能处在一系列具有不连续能量的 稳定状态:定态,不辐射电磁波 定态1, 定态2,,, , 1E 2E , 轨道1, 轨道2, ,(2) 跃迁假设:的定态的定态 n E →k E 光子频率 hE E nk -=ν <,吸收一个光子,>,放出一个光子n E k E n E k E (3)角动量量子化假设:电子绕核转动的角动量:, n hnL ==π2 ,3,2,1=n:量子数n :约化普朗克常数,SI :=π2h = π2h= Js 341005.1-⨯三、 氢原子结构和氢原子光谱 1、 轨道半径(1) 20224r e r V m πε= (2),n mVr L == ,3,2,1=n (,)V m r P r L⨯=⨯=θθsin sin rmV rP L == ,, 222023141 n r e mr πε=22204n me r ⋅= πε ,3,2,1=n , 1=nA ==529.042201mer πε ,2=n 2122⋅=r r ,3=n2133⋅=r r21n r r n ⋅=<<<321r r r :玻尔半径A =529.01r 结论:电子的轨道半径是量子化的 2、 定态能量,, r e mV E 022421πε-=20224r e r V m πε=r e mV 022821πε= ,210202188n r e re E ⋅-=-=πεπε ,3,2,1=nVm e3,,,1=n eV r e E 6.1381021-=-=πε2=n eV E E 4.32/212-== ,,3=n ,51.13/213eV E E -== 21/n E E n =<<<321E E E 的定态:基态,的定态,激发态 1=n 1>n 结论:氢原子的定态能量是量子化的 每一个定态能量称为一个能级∞=n4=n51.1-3=neV 4.3-2=neV 6.13-1=n3、 氢原子光谱氢原子 ,n E →k E k n >辐射光子频率==h E E k n -=ν)(12121k E n E h -)11(221nk h E -- 波数, ==c νν~11(221n k hc E --k n > 令,, hc E R 1-===λν1~)11(22n k R -k n >= hcER 1-=1710097373.1-⨯m 例:赖曼系中波长最短的谱线光子能量是多少? 答:eV 6.13例:巴耳末系中波长最短的谱线光子能量是多少? 答:eV 4.3例:写出氢原子光谱各谱线系的极限波数表达式解:,, ==λν1~11(22n k R -∞→n 2)(~k R =∞ν赖曼系 (), = 1=k R =∞)(~赖ν1710097.1-⨯m 巴耳末系(), 2=k 1710274.04)(~-⨯==∞m R 巴ν5=n 赖曼系4四、 玻尔理论的缺陷氢原子及 类氢离子光谱 , ,, H +He +2Li +3Be Z= 1, 2, 3, 4碱金属元素的原子光谱,光谱的精细结构 塞曼效应,谱线宽度、强度、偏振逻辑上,玻尔理论自相矛盾 认识原子结构的里程碑 “定态”、“能级”、“跃迁” 例:氢原子由量子数为的定态()的定态 n →1-n 求:(1)辐射光子频率1-→n n ν (2)很大时,n 1-→n n νn ν≈:电子在第轨道上的转动频率n νn 解:(1)= 1-→n n ν22121211)1(12])1([1n n n h E n E n E h h E E n n --⋅-=--=--= ()22102)1(128n n n h r e --⋅πε10218r e E πε-= (2)= () n νn n n n n r mV mV r V ππ222=20224nn n r e r V m πε== (,) 31020214214nh r e n r e n ⋅=⋅πεππε n r mV n n =21n r r n ⋅= 很大时,== n 1-→n n ν22102)1(128n n n h r e --⋅πε310214nh r e ⋅≈πεn ν对应原理:当量子数很大时,量子方程应过渡到经典方程 n 经典理论是量子理论在很大时的极限 n 例:氢原子某谱线系的极限波长为,其中一条谱线A 3647 波长为A 6565求:该谱线对应的氢原子初态和末态的能级能量 ()1710097.1-⨯=m R 解:,,, ==λν1~11(22n k R -∞→n 21k R =∞λ2==∞λR k ,,= =λ1)121(22n R -221211n R -=λR nλ14112-=R R λλ44-344=-=R Rn λλ 初态,3=n eV E E 51.13/213-==末态,2=n eV E E 4.32/212-==。
玻尔的氢原子理论

玻尔的氢原子理论
为此,J.汤姆孙在1904年提出了原子结构的枣糕式模型.该模型认 为,原子可以看作一个球体,原子的正电荷和质量均匀分布在球内, 电子则一颗一颗地镶嵌其中.1909年,J.汤姆孙的学生卢瑟福为了验证 原子结构的枣糕式模型,完成了著名的α粒子散射实验.实验发现α粒 子在轰击金箔时,绝大多数α粒子都穿透金箔,方向也几乎不变,但 是大约有1/8 000的α粒子会发生大角度偏转,即被反弹回来.这样的 实验结果是枣糕式模型根本无法解释的,因为如果说金箔中的金原子 都是枣糕式的结构,那么整个金箔上各点的性质应该近乎均匀,α粒 子轰击上去,要么全部透射过去,要么全部反弹回来,而不可能是一 些穿透过去,一些反弹回来.
玻尔的氢原子理论
二、 原子结构模型
1897年,J.汤姆孙发现了电子.在此之前,原 子被认为是物质结构的最小单元,是不可分的,可 是电子的发现却表明原子中包含带负电的电子.那 么,原子中必然还有带正电的部分,这就说明原子 是可分的,是有内部结构的.执着的科学家就会继 续追问:原子的内部结构是什么样的?简洁的里德 伯光谱公式是不是氢原子内部结构的外在表现?
玻尔的氢原子理论
三、 玻尔的三点基本假设
为了解决原子结构有核模型的稳定性和氢原子光谱的分 立性问题,玻尔提出以下三个假设:
(1)定态假设.原子中的电子绕着原子核做圆周运动, 但是只能沿着一系列特定的轨道运动,而不能够任意转动, 当电子在这些轨道运动时,不向外辐射电磁波,原子系统处 于稳定状态,具有一定的能量.不同的轨道,具有不同的能 量,按照从小到大的顺序记为E1、E2、E3等.
玻尔的氢原子理论
可是这个模型却遭到很多物理学家的质疑.因为按照当时的物 理理论(包括经典力学、经典电磁理论及热力学统计物理),这 样一个模型是根本不可能的,原因有以下两个:
氢原子光谱实验报告

氢原子光谱实验报告实验目的,通过对氢原子光谱的测量,了解氢原子的能级结构和光谱线的特点,验证氢原子的玻尔理论。
实验原理,氢原子的光谱实验是通过光谱仪测量氢原子的光谱线,根据光谱线的位置和强度来确定氢原子的能级结构。
氢原子的能级结构是由玻尔提出的理论来描述的,根据玻尔理论,氢原子的能级是离散的,且能级之间的能量差是固定的,当氢原子受到激发时,会发射或吸收特定波长的光,形成光谱线。
实验仪器,本实验使用的仪器主要有氢原子光谱仪、光源、光栅、光电倍增管等。
实验步骤:1. 调节光源和光栅,使得光线通过光栅后能够分解成光谱。
2. 将氢原子样品放入光谱仪中,调节光谱仪使得光谱线尽可能清晰。
3. 使用光电倍增管测量光谱线的位置和强度,记录下实验数据。
4. 根据实验数据计算氢原子的能级结构和光谱线的特点。
5. 对实验结果进行分析和讨论,验证氢原子的玻尔理论。
实验结果与分析:通过实验测量得到了氢原子的光谱线的位置和强度,根据实验数据计算得到了氢原子的能级结构和光谱线的特点。
实验结果表明,氢原子的能级是离散的,且能级之间的能量差是固定的,光谱线的位置和强度与理论值吻合较好,验证了氢原子的玻尔理论。
结论:本实验通过测量氢原子的光谱,验证了氢原子的玻尔理论。
实验结果表明,氢原子的能级结构是离散的,光谱线的位置和强度与理论值吻合较好。
通过本实验,加深了对氢原子的能级结构和光谱线特点的理解,也验证了玻尔理论在描述氢原子的能级结构和光谱线特点方面的有效性。
通过本次实验,我对氢原子的光谱有了更深入的了解,也对实验操作和数据处理有了更多的经验。
希望通过今后的实验学习,能够进一步提高自己的实验技能和科研能力,为科学研究做出更多的贡献。
波尔的氢原子理论

2 卢瑟福的核式模型
卢瑟福1871年8月13日出生在 新西兰,1894年大学毕业,1895年 到 英 国 剑 桥 大 学 学 习 , 成 为 J.J. 汤 姆孙的研究生。1908年卢瑟福荣获 诺贝尔化学奖,同年在曼切斯特大 学任教,继续指导他的学生进行 粒子散射的实验研究。
卢瑟福的α粒子散射验证了核式模型。
19-1 波尔的氢原子理论
量子物理起源于对原子物理的研究,人们从高能粒子的 散射实验和原子光谱中获得原子内部信息。
3
4
一 玻尔理论的实验基础
1 汤姆逊葡萄干面包模型
1903年,汤姆孙提出原子结构模 型:原子里面带正电的部分均匀地 分布在整个原子球体中,而带负电 的电子镶嵌在带正电的球体之中。 带正电的球体与带负电的电子二者 电量相等,故原子不显电性。
5 6 普芳德(Pfund)系
区域 紫外 可见 可见 红外 红外
此后又发现碱金属也有类似的规律。
日期 1906年 1880年 1908年 1922年 1924年
3 里兹并合原理
~ T(m α) T(n β)
R
光谱项 : T(m) (m )2
R
T (n) (n )2 10
三 经典电磁理论遇到的困难
6
粒子散射
4 2
H
e
,
q 2e, 原子量为4,m 7500me
粒子束射向金箔:
-
(1) 多数 0
+
(2)少数 较大
1 / 8000被反射,
(3)极少数 ,反弹
大部分透过。
7
1911年,卢瑟福提出原子的 “有核结构模型”
原子的核式模型
原子由原子核和核外电子 构成,原子核带正电荷,占据 整个原子的极小一部分空间, 而电子带负电,绕着原子核转 动,如同行星绕太阳转动一样。
玻尔理论推导氢原子能级公式

玻尔理论推导氢原子能级公式
氢原子的能级公式:en=1/n2e1(n=1,2,3,…),其中e1为基态能量。
氢原子能级:原子各个定态对应的能量是不连续的,这些能量值叫做能级。
在氢光谱中,
n=2,3,4,5,…...向n=1光子闪烁构成赖曼线系;
n=3,4,5,6……向n=2跃迁发光形成巴耳末线系;
n=4,5,6,7……向n=3光子闪烁构成帕邢线系;
n=5,6,7,8……向n=4跃迁发光形成布喇开线系,
其中只有巴耳末线系的前4条谱线落到红外线区域内。
能量最低的能级叫做基态,其他能级叫做激发态。
电子“远离”原子核,不再受原子核的吸引力时的状态叫做电离态,电离态的能级为0(电子由基态跃迁到电离态时,吸收的能量最大)。
能级光子首先由波尔(niels bohr)明确提出,但是波尔将宏观规律使用其中,所以除了氢原子的能级光子之外,在对其他繁杂的原子的光子规律的探究中,波尔碰到了非常大的困难。
组成物质的原子中,有不同数量的粒子(电子)分布在不同的能级上,在高能级上的粒子受到某种光子的激发,会从高能级跳到(跃迁)到低能级上,这时将会辐射出与激发它的光相同性质的光。
《氢原子光谱和玻尔的原子模型》教学案

《氢原子光谱和玻尔的原子模型》教学案课标核心素养要求了解氢原子光谱和波尔的原子模型学习目标 1、知道光谱、氢原子光谱的实验规律2、了解波尔的原子模型,能用原子能级图分析问题 学习重点波尔的原子模型、应用原子能级图分析问题学习过程【自主学习】回顾原子的核式结构:【合作学习·难点探究】任务一、了解光谱及氢原子光谱的实验规律 阅读教材梳理:1、把食盐放在火中灼烧,会发出黄色的光2、说明发射光谱形成和种类: 连续谱: 线状谱: 原子特征谱线:3、氢原子光谱巴耳末对氢原子光谱的在可见光区域的谱线进行研究得到了下面的公式:1λ=R ∞⎝ ⎛⎭⎪⎫122-1n 2,n =3,4,5,…,该公式称为巴耳末公式。
【例1】关于光谱和光谱分析,下列说法正确的是( ) A .太阳光谱和白炽灯光谱是线状谱B .霓虹灯和煤气灯火焰中燃烧的钠蒸气产生的光谱是线状谱C .进行光谱分析时,可以利用线状谱,也可以利用连续谱D .观察月亮光谱,可以确定月亮的化学组成【例2】巴耳末通过对氢原子光谱的研究总结出巴耳末公式1λ=R ∞⎝ ⎛⎭⎪⎫122-1n 2,n =3,4,5…,对此,下列说法正确的是( ) A .巴耳末依据核式结构理论总结出巴耳末公式B .巴耳末公式反映了氢原子发光的连续性C.巴耳末依据氢光谱的分析总结出巴耳末公式D.巴耳末公式准确反映了氢原子发光的分立性,其波长的分立值并不是人为规定的任务二、波尔的原子理论1、经典电磁理论的困难(1)无法解释原子的稳定性,(2)无法解释原子光谱的分立特征。
2、玻尔原子理论的基本假设(1)轨道量子化:轨道半径只能够是一些不连续的、某些分立的数值,电子在这些轨道上是稳定的,不产生电磁辐射氢原子的电子轨道最小半径为r1=0.053 nm,其余轨道半径满足r n=n2r1(2)能量量子化:电子在不同轨道上运动时具有不同的能量,即原子的能量是______称为能级,原子中这些具有确定能量的稳定状态,称为______。
17.3 氢原子光谱 玻尔的氢原子理论2
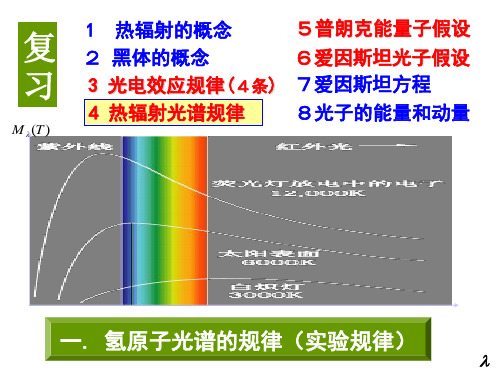
巴尔末( 巴尔末(Balmer)系 ) 赖曼( 赖曼(Lyman)系 ) + 普芳德( 普芳德(Pfund)系 )
n=1 n=2 n=3 n=4 n=5 n=6
帕邢( 帕邢(paschen)系 )
布喇开( 布喇开(Brackett)系 )
三. 弗兰克 — 赫兹实验
按照玻尔(Bohr)理论,在原子内存在一系列分立的能级 分立的能级. ● 按照玻尔(Bohr)理论,在原子内存在一系列分立的能级. 1914年 夫兰克和赫兹(Frank德国物理学家) ● 1914年,夫兰克和赫兹(Frank-Hertz,德国物理学家) 进行了电子轰击汞原子的实验, 进行了电子轰击汞原子的实验, 证明了原子内部的能级的确是分立的。 证明了原子内部的能级的确是分立的。 充汞原子蒸汽 电子由阴级K发出, 电子由阴级K发出, 与栅极G之间有加速电场, K与栅极G之间有加速电场, 与接收极A之间有减速电场。 G与接收极A之间有减速电场。
h 角动量量子化假设 L = mvr = n = nh 2π
r
r v
2、玻尔对氢原子的诠释
1 e v 库仑力提供向心力 2 =m 4πε0 r r 由上两式得, 由上两式得, 第 n 个定态的轨道半径为 ε0h2 ) = n2r1 n = 1,2,3,L rn = n2 ( r2=4r1 πme 2 2 1 e r3=9r1 玻尔半径 r1 = 0.0529 nm E1 = 8πε0 r1 定态能量: 定态能量: 2 E1 -13.6 eV 1 e2 1 2 1 e2 1 e = 2 =− En = mv − =− 2 8πε0 n r1 n 2 4πε0 rn 8πε0 rn
(2) 跃迁假设 )
原子从一个定态跃迁到另一定态, 原子从一个定态跃迁到另一定态,会 E 跃迁到另一定态 k 发射或吸收频率为 的一个光子
第3节 氢原子模型及玻尔的氢原子理论

③.原子核的体积比原子的体积小得多。
3
原子半径~10-10m,原子核半径10-14 ~10-
卢瑟福的原子有核模型可以解释粒子的散射实验: 绝大多数的粒子会穿透原子按原方向进行,只有极 少数的粒子进到核处而产生大角度散射。 后来盖革和马斯顿又仔细地进行了 粒子散射实验,证实了卢瑟福结构模型 的正确性。 原子核式结构模型的建立,只肯定 了原子核的存在,但还不知道原子核外 电子的情况。
6
2
1 ~ 1896年里德伯用波数 来表示谱线,
2 n 波数:单位长度中所包含的波形数目。 B 2 2 n -2 2 1 41 1 1 n 4 ~ 2 - 2 2 B n B 2 n 4 7 -1 里德伯常数 RH 1.097373 10 m 令 RH B
汤姆逊的原子结构模型无法解 释这种现象。 这种大角度散射不可能解释为都是 偶然的小角度的累积—这种可能性要比 1/8000小得多,绝大多数是一次碰撞 的结果。但这不可能在汤姆逊模型那 样的原子中发生。 3. 卢瑟福原子有核模型 ①.原子的中心是原子核,几乎占有原子的全部质量, 集中了原子中全部的正电荷。 ②.电子绕原子核旋转。
10
四、卢瑟福有核原子模型的困难
卢瑟福有核原子模型无法解释 氢原子光谱的规律。 按经典理论电子绕核旋转,作加 速运动,电子将不断向四周辐射电磁 波,它的能量不断减小,从而将逐渐 靠近原子核,最后落入原子核中。
播放动画
11
轨道及转动频率不断变化,辐射电磁波频率也是 连续的, 原子光谱应是连续的光谱。实验表明原子相 当稳定,这一结论与实验不符。实验测得原子光谱是 不续的谱线。 1913年,玻尔在卢瑟福的有核模型的基础上,推 广了普朗克和爱因斯坦的量子概念,并引用到原子中 来。提出了关于原子模型的三个假设。
氢原子光谱和玻尔原子理论

失重状态无关 ,所以 A 、C 、D 错 ,B 正确 .
根据气体压强的微观解释 ,大量气体分子跟容器壁的碰
撞 ,对容器壁形成一个持续的作用力 ,由压强公式 p =
F S
,
气体压强可以说成是“单位面积上的平均作用力” ,E 正确 .
F .气体对器壁的压强就是大量气体分子单位时间作用
在器壁上的平均冲量
解析 由气体分子自身的重力产生的压强很小 ,可忽
略不计 .如果我们在一个很小的容器中加入少量的气体也照
样能获得较大的气压 .同时 ,对处于封闭容器中的气体 ,即使
放到失重的状态下也仍然能保持原有的压强 .气体的压强是
气体分子与器壁碰撞产生 ,与分子间的斥力和分子是否处于
射电磁波 ,辐射的电磁波的频率等于电子做圆周运动的频
率 .那么 ,经典理论至少遇到下面两个困难 :
(1) 由于电子运动时辐射电磁波 ,能量会不断减小 ,从而
导致轨道半径越来越小 ,最终落到原子核上 ,即原子和原子
核的大小是一样的 ,这与卢瑟福核式结构矛盾 .
(2) 由于不断辐射导致轨道半径连续减小 ,频率连续增
1 氢原子光谱
在 1885 年从星体的光谱中观察到的氢光谱线已达 14
条 .巴尔末将这些谱线的波长归纳为 :
λ=
B
n2 n2 -
4
n
=
3
,4
,5
,…
即巴尔末公式 .
随后又发现了氢原子光谱的其他谱线 :即紫外区的赖曼
系 ,红外区的帕邢系 、布喇开系和普丰特系 .如果令 RH =
4 B
,RH 称里德伯常数 ,实验测得其值为
大 ,所以辐射的电磁波的频率应该是连续的 .这与氢原子光
第二章 玻尔氢原子理论

第二章 原子的能级和辐射一、学习要点:1.氢原子光谱:线状谱、五个线系(记住名称、顺序)、广义巴尔末公式)11(~22nm R -=ν、 光谱项()2nR n T =、并合原则:)()(~n T m T -=ν 2.玻尔氢原子理论:(1)玻尔三条基本假设的实验基础和内容(记熟)(2)圆轨道理论(会推导):氢原子中假设原子核静止,电子绕核作匀速率圆周运动02200202220A 529,04,Z Z 4≈===e m a n a n e m r e e n πεπε;13714,Z Z 40202≈===c e n c n e c e n πεααπευ; ()n hcT n hc R n e m E e n --=-=∞22224220Z 2Z )41( πε,n =1.2.3……(3)实验验证:(a )氢原子五个线系的形成)11(Z ~,)4(222232042n m R c h e m R e -==∞∞νπεπ (会推导)非量子化轨道跃迁 )(212n E E mv h -+=∞ν (b )夫-赫实验:装置、.结果及分析;原子的电离电势、激发电势3.类氢离子(+++Li ,He ,正电子偶素.-μ原子等) (1) He +光谱:毕克林系的发现、波数公式、与氢原子巴耳末系的异同等(2)理论处理(会推导):计及原子核的运动,电子和原子核绕共同质心作匀速率圆周运动e e m M m M +⋅=μ, 正负电荷中心之距Ze n r n 22204μπε =. 能量2242202Z )41(n e E n μπε-=,里德伯常数变化Mm R R e A +=∞11 重氢(氘)的发现4.椭圆轨道理论 索末菲量子化条件q q n h n pdq ,⎰=为整数a n nb n e m a n e m E n p e n ϕϕϕπεπε==-==,Z 4,2Z )41(,2220224220 ,n n n ,,3,2,1;,3,2,1 ==ϕn 一定,n E 一定,长半轴一定,有n 个短半轴,有n 个椭圆轨道(状态),即n E 为n 度简并。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
k 1, n 2,3 k 2, n 3,4, k 3, n 4,5,
赖曼系,紫外区 巴尔末系,可见光区 帕邢系,红外区
k 4, n 5,6, 布拉开系,红外区
k 5, n 6,7, 普丰德系,红外区
k 6, n 7,8, 哈弗莱系,红外区
其他元素的光谱也有类似的规律性。
解: 设氢原子全部吸收电子的能量后最高能激发到第n
个能级,此能级的能量为
eV 13.6
n2
,
所以
En
E1
13.6
13.6 n2
把 En E1 12.5eV 代入上式得
n2
13.6 13.612.5
12.36
所以
n 3.5
因为n只能取整数,所以氢原子最高能激发 到 n=3的能级,当然也能激发到n=2的能级.于是 能产生3条谱线。
或吸收一个频率为 kn 的光子。
kn
En
h
Ek
玻尔频率公式
玻尔的氢原子理论
(3)量子化条件 在电子绕核作圆周运动中,
其稳定状态必须满足电子的角动量 L等于 h
的整数倍的条件。
2
L n h , n 1,2,3, 角动量量子化条件
2
n 为量子数
3. 氢原子轨道半径和能量的计算
根据电子绕核作圆周运动的模型及角动量 量子化条件可以计算出氢原子处于各定态时的 电子轨道半径。
氢原子光谱
从n3n1
~1
R(
1 12
)1
32
8 9
R
1
9 8R
9 81.096776107
m
102.6nm
从n3n2
~2
R(
1 22
)1
32
5 36
R
2
36 5R
36 51.096776107
m
656.3nm
从n2n1
~
R(
1 12
)1
22
3 4
R
3
4 3R
4 31.096776107
m
121.6nm
玻尔的氢原子理论
rn n2 (m0he22 ), n 1,2,3,
r1 0.529 1010 m 玻尔 半径
电子处在半径为 rn的轨道上运动时,可以计
算出氢原子系统的能量 En为
En
1 n2
(8m0e2h4 2 ), n
1,2,3,
能量是量子化的。
玻尔的氢原子理论
n 1, E1 13.6eV 基态能级; n 1 的各稳定态称为受激态; n 时 rn En 0
能级趋于连续。
玻尔的氢原子理论
E
0 n4
赖曼系
n 1
氢原子的能级图
玻尔的氢原子理论
根据氢原子的能级及玻尔假设,可以得到氢
原子光谱的波数公式
~nk
me4
8
2 0
h3c
(
1 k2
1 n2
)
与氢原子光谱经验公式是一致的。
R
me4
8
2 0
h3c
1.0973731107
原子光谱线系的规律性深刻地反映了原子内部的规律性
2. 玻尔的氢原子理论
(1)定态假设 原子系统只能处在 一系列不连续的能量状态,在这些
状态中,电子虽然作加速运动,但
并不辐射电磁波,这些状态称为原
子的稳定状态(简称定态),相应
的能量分别为 E1, E2, E3, 。
玻尔
(2)频率条件 当原子从一个能量为 En 的定 态跃迁到另一能量为 Ek的定态时,就要发射
1 1) 2
当 n 很大时
n1,n
me4
8 0 2 h3
2 n3
me4
4
2 0
h3n3
绕转频率为
vn
2rn
mvnrn
2mrn2
nh
4 2mrn2
me4
4 0 2 h3n3
玻尔的氢原子理论
绕转频率为
vn
2rn
mv n rn
2mrn2
nh
4 2mrn2
me 4
4 0 2 h3n3
可见 的值和 n 很大时 n1,n 的值相同。
m-1
R 理论值与实验值符合得很好。
玻尔的创造性工作对量子力学的建立有着深远的影响。
4. 玻尔理论的缺陷
● 玻尔理论仍然以经典理论为基础,定态假设 又和经典理论相抵触。
● 量子化条件的引进没有适当的理论解释。 ● 对谱线的强度、宽度、偏振等无法处理。
氢原子光谱
例题18-6 在气体放电管中,用能量为12.5eV的电子通 过碰撞使氢原子激发,问受激发的原子向低能级 跃迁时,能发射那些波长的光谱线?
玻尔的氢原子理论
例18- 7 计算氢原子中的电子从量子数 n 的状态跃迁
到量子数 k n 1 的状态时所发谱线的频率。试证
明当 n 很大时,这个频率等于电子在量子数 n的圆
轨道上绕转的频率。
解 按玻尔频率公式有
n1,n
me4
8
2 0
h3
(n
1 1) 2
1 n2
me4
8 0 2 h3
2n n2 (n
在量子数很大的情况下,量子理论得到与 经典理论一致的结果,这是一个普遍原则,称 为对应原理。
玻尔的氢原子理论
绕转频率为
vn
2rn
mv n rn
2mrn2
nh
4 2mrn2
me 4
4 0 2 h3n3
可见 的值和 n 很大时 n1,n 的值相同。
在量子数很大的情况下,量子理论得到与 经典理论一致的结果,这是一个普遍原则,称 为对应原理。
