初三化学各单元知识框架图全部汇总
初三化学各单元知识框架图全部汇总
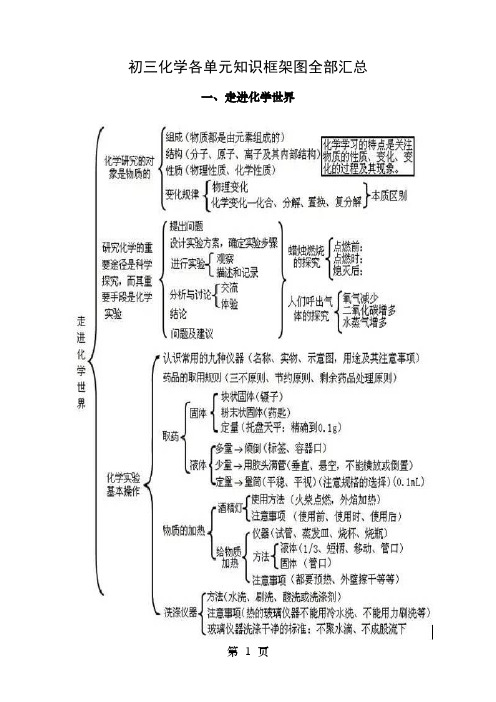
初三化学各单元知识框架图全部汇总一、走进化学世界二、我们周围的空气三、自然界的水四、物质构成的奥秘五、化学方程式六、碳与碳与氧化物七、燃料及期应用八、金属与金属材料九、溶液十、酸碱盐一、化学用语1、电离方程式2、物质的俗称与主要成分:生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4.5H2O;碳酸钠晶体Na2CO3.10H2O;氨水NH3.H2O;二、金属活动性1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
三、酸、碱、盐的溶解性1、常见盐及碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清〞的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-与Cl-时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁四、复分解反响发生的条件反响:有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)(1)不溶性碱只能及酸性发生中与反响(2)不溶性盐,只有碳酸盐能及酸反响(3)KNO3、NaNO3、AgNO3、BaSO4不能做复分解反响的反响物五、溶液的酸碱性及酸碱度的测定1、指示剂---溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱及指示剂无作用;碱性溶液不一定是碱的溶液(特例:碳酸钠的水溶液显碱性)2、pH值---溶液的酸碱度:pH<7溶液为酸性(越小酸性越强);pH=7溶液为中性;pH>7溶液为碱性(越大碱性越强)六、离子的检验Cl-(在溶液中)---在被测溶液中参加硝酸银溶液,如果生成不溶于硝酸的白色沉淀,那么原被测液中含氯离子。
「人教九年级化学」全册单元思维导图,初三学生请收藏
第八单元:金属和金属材料
第九单元பைடு நூலகம்溶液
第十单元:酸和碱
第十一单元:盐 化肥
第十二单元:化学与生活
初中化学有哪些知识点看了此图就知道了各位考生请收藏
「人教九年级化学」全册单元思维导图,初三学生请收藏
初中化学有哪些知识点,看了此图就知道了,各位考生请收藏。
第一单元:走进化学世界
第二单元:我们周围的空气
第三单元:物质构成的奥秘1
第三单元:物质构成的奥秘2
第四单元:自然界的水
第五单元:化学方程式
第六单元:碳和碳的氧化物
纯干货:初中化学各单元知识框架图(收藏)

纯干货:初中化学各单元知识框架图(收藏)第一单元:走进化学世界第二单元:我们周围的空气第三单元:自然界的水第四单元:物质构成的奥秘第五单元:化学方程式第六单元:碳和碳的氧化物第七单元:燃料及其利用第八单元:金属和金属材料第九单元:溶液第十单元:酸碱盐1化学用语1、电离方程式:2、物质的俗称和主要成分:生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4.5H2O;碳酸钠晶体Na2CO3.10H2O;氨水NH3.H2O;3、物质的俗称和主要成分:生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4.5H2O;碳酸钠晶体Na2CO3.10H2O;氨水NH3.H2O。
2金属活动性1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
3酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁4复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物。
九年级化学各单元知识框架图

化学研究的对象是物质的初中化学知识框架图第一单元走进化学世界粗成(物质都星由元素组成的)结构(分手,原子、离子及其内部结构〉〈性质(物理性质、化学性质)化学学习的特点是关注物质的性质、变化、变化的过稈及其现象。
变化规律J物理变化1[化学变化一^合、分解、置换、复分解」"本质区别走逬化学世研究化学的重要途径是科学探究,而其重要手段是化学实验〔提出间题後计实验方案,确症概步曝观察描述和记录「交流L体验进行实验iis f r u■Blilr11前时启燃燃灭点点熄化学实验基本操作分析与讨论・结论<间题艮律议人们呼出气体的探究-氧气减少二氧化碳增多水蒸气增多广认识常用的九种仪器(名称、实物、示盍图*用途及其注盍事项)药品的取用规则(三不原则,节约原则、剩余药品处理原则〉「块状固体(镰子〉取药&固体-粉末状固体(药匙):定量(托盘天平:精确到O.lg)「多墾T倾倒(标签、容器口)I潑体,少壘一用胶头滴管(垂直、悬空,不能横放或倒置)I定壘T童筒(平稳、平视)(注意规格的选择)<0. 5L)侬用方法(火柴点燃,外焰加热).注意事项(使用前、使用时、使用启)•仪器(试管、蒸发皿、烧杯、烧瓶)液体(1/3、短柄、移动、管口)固体(管口)「酒精烁物质的加热.I注意事项(都要笊热、外壁擦干等等)「方法0K矗刷矗酸湍或洗涤剂)洗涤仪器*注意事项(热的玻璃仪器不能用冷水洗、不能用力刷洗等)丄玻璃仪器啟涤干净的标准:不聚水滴*不成股流下第二单元我们周围的空气夢諜勰驚作霹悉囉牖不敬一般稀有气体(氐、帕肛等h 占0.94恥很不活源 作保护气,通电发不同颜色光。
二氧化碳(COD :占0.0带°详见第六单元° 其他气体和杂處:占0. 03% o物理性质: 活有,的>较具剂 比,化常化 {«氧是氧无色,无味、气体,密度比空气略大,不易溶于水。
厂c + 5 瞿CO £ (白光、放如 澄清石灰水变浑浊〉 占瑕 2C + 0£ = 2 COS +°2 = 史2(蓝紫色火焰、放热、刺激性气味气体) 占饿4P+5@ = 2P 205(白光、放热、浓厚白烟、白色固体) 3陀+伦=吗0讥火星四射、放热、黒色固体厳]2 + 0£ = 2虺0 (耀眼白光、放热’白色固体)宓°4A1 +302 =肚1刃3〈耀眼白光、放热、白色固体) 占燃 2H 2 + 02 = 2H £0 2 CO + 02 = 2C02V J CH 4 + 2O 2 =C02+2H 20(淡蓝色或蓝色火焰,放热, 干冷烧杯壁有无水滴,沾石灰 水的烧杯壁是否浑浊)'氧气 (占 2D0 C 工业制祛:分离液态空气,(发生物理变化)((2H 202 2H 20 + 0£ f原理{ 2KMnO 4 = K/ng + Mn02 +0£t 12KC103 竽 2KC1 + 302f 炜半聲晉J 固体加热制駆气体〔棉花>,或 友生叢直]固体与液体舊温下制取气体5验宰制注丿收集奘詈『排水法(氧气不易溶于水) 沁至耐冷恫裁直I向上排空气憧(氧气密度比空气大) 实验步骤:査、装、定、点、收、离、熄* 津音事顼J 加热固体制氧气并用排水法收集完 汪启畢项[毕,应先撤导管,后停止加热等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初三化学各单元知识框架图全部汇总
一、走进化学世界
二、我们周围的空气
三、自然界的水
四、物质构成的奥秘
五、化学方程式
六、碳和碳和氧化物
七、燃料及期应用
八、金属和金属材料
九、溶液
十、酸碱盐
一、化学用语
1、电离方程式
2、物质的俗称和主要成分:
生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4.5H2O;碳酸钠晶体Na2CO3.10H2O;氨水NH3.H2O;
二、金属活动性
1、金属活动性顺序:
K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au
2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:
(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
三、酸、碱、盐的溶解性
1、常见盐与碱的溶解性:
钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁
3、四微溶物:
Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)
Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)
4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁
四、复分解反应发生的条件反应:有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)
(1)不溶性碱只能与酸性发生中和反应
(2)不溶性盐,只有碳酸盐能与酸反应(3)KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物
五、溶液的酸碱性与酸碱度的测定
1、指示剂---溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作用;碱性溶液不一定是碱的溶液(特例:碳酸钠的水溶液显碱性)
2、pH值---溶液的酸碱度:pH<7溶液为酸性(越小酸性越强);pH=7溶液为中性;pH>7溶液为碱性(越大碱性越强)
六、离子的检验
Cl-(在溶液中)---在被测溶液中加入硝酸银溶液,如果生成不溶于硝酸的白色沉淀,则原被测液中含氯离子。
SO42-(在溶液中)---在被测溶液中加入氯化钡(或硝酸钡、或氢氧化钡)溶液,如果生成不溶于硝酸(或盐酸)的白色沉淀,则原被测液中含硫酸根离子。
CO32-(1)(固体或溶液)---在被测物质中加入稀酸溶液,如果产生能使澄清石灰水变浑浊的气体,则原被测物质中含碳酸根离子。
(2)(在溶液中)---在被测溶液中加入氯化钡或硝酸银溶液,如果产生能溶于硝酸的白色沉淀,且同时生成能使澄清的石灰水变浑浊的气体,则原被测溶液中含碳酸根离子。
( 注:1、在鉴别Cl-和SO42-时,用氯化钡溶液,不要用硝酸银溶液,这是因为硫酸银为微溶性物质,使鉴别现象不明显;2、在一未知溶液中加入氯化钡溶液,若产生不溶于硝酸的白色沉淀,则原被测液中可能含银离子也可能含硫酸根离子。
)
七、物质的颜色
1、固体(多为白色)
黑色---CuO、C粉、MnO、2Fe3O4、紫黑色---KMnO4
红色---Cu、Fe2O3 红褐色---Fe(OH)3
蓝色---Cu(OH)2、CuSO4.5H2O 绿色---Cu2(OH)2CO3 2、溶液(多为无色):
浅绿色溶液---(亚铁盐溶液)FeCl2溶液、FeSO4;
黄色溶液--- (铁盐溶液)FeCl3溶液、Fe2(SO4)3 溶液、Fe(NO3)3
溶液蓝色溶液---(铜盐溶液)CuCl2溶液、CuSO4溶液、Cu(NO3)2
溶液蓝绿色溶液-CuCl2溶液(较浓)
八、酸、碱、盐的特性
1、浓盐酸---有挥发性、有刺激性气味、在空气中能形成酸雾。
2、浓硝酸---有挥发性、有刺激性气味、在空气中能形成酸雾,有强氧化性。
3、浓硫酸---无挥发性。
粘稠的油状液体。
有很强的吸水性和脱水性,溶水时能放出大量的热。
有强氧化性。
4、氢氧化钙---白色粉末、微溶于水。
5、氢氧化钠---白色固体、易潮解,溶水时放大量热。
能与空气中的二氧化碳反应而变质。
6、硫酸铜---白色粉末、溶于水后得蓝色溶液(从该溶液中析出的蓝色晶体为五水合硫酸铜CuSO4.5H2O)。
7、碳酸钠---白色粉末,水溶液为碱性溶液(从溶液中析出的白色晶体为碳酸钠晶体Na2CO3.10H2O)
8、氨水(NH3.H2O)---属于碱的溶液
九、酸与碱的通性和盐的性质
1、酸的通性
(1)酸溶液能使紫色的石蕊试液变红,不能使无色的酚酞试液变色。
(2)酸能与活泼金属反应生成盐和氢气
(3)酸能与碱性氧化物反应生成盐和水
(4)酸能与碱反应生成盐和水
(5)(5)酸能与某些盐反应生成新的盐和新的酸
2、碱的通性
(1)碱溶液能使紫色的石蕊试液变蓝,并能使无色的酚酞试液变红色
(2)碱能与酸性氧化物反应生成盐和水
(3)碱能与酸反应生成盐和水
(4)某些碱能与某些盐反应生成新的盐和新的碱
3、盐的性质
(1)某些盐能与较活泼的金属反应生成新的盐和金属
(2)某些盐能与酸反应生成新的盐和新的酸
(3)某些盐能与某些碱反应生成新的盐和新的碱
(4)有些不同的盐之间能反应生成两种新的盐。
