第七章DNA体外重组与基因转移总结
简述dna体外重组的基本过程

简述dna体外重组的基本过程DNA体外重组是一种重要的生物技术方法,用于合成、克隆和改造DNA分子。
它的基本过程包括:DNA提取、DNA片段切割、DNA片段连接、DNA转化和筛选。
进行DNA提取。
DNA提取是从生物样品中分离出DNA分子的过程。
常用的DNA提取方法包括酚/氯仿法、盐水法和商用DNA提取试剂盒。
通过这些方法,可以从细胞或组织中提取纯净的DNA。
接下来,进行DNA片段切割。
DNA片段切割是将DNA分子切割成特定长度的过程,常用的切割酶包括限制性内切酶和脱氧核苷酸转移酶。
限制性内切酶能够识别特定的DNA序列,并在识别位点上切割DNA,产生特定长度的DNA片段。
然后,进行DNA片段连接。
DNA片段连接是将两个或多个DNA 片段通过连接酶连接在一起的过程。
连接酶能够将DNA片段的末端粘性的碱基序列连接起来,形成连续的DNA分子。
连接酶还可以用于连接不同来源的DNA片段,实现重组DNA的构建。
接着,进行DNA转化。
DNA转化是将重组的DNA分子导入到宿主细胞中的过程。
转化方法有多种,常用的方法包括热冲击法、电穿孔法和化学法。
通过转化,重组的DNA可以进入宿主细胞,并在细胞内进行复制和表达。
进行筛选。
筛选是为了筛选出带有所需基因的转化细胞。
常用的筛选方法包括抗生素筛选和荧光筛选。
抗生素筛选是利用转化细胞对特定抗生素的抗性来筛选带有目标基因的细胞。
荧光筛选是利用基因工程技术将目标基因与荧光标记基因连在一起,然后通过观察细胞是否发出荧光来筛选带有目标基因的细胞。
总的来说,DNA体外重组是通过将DNA提取、切割、连接、转化和筛选等一系列操作步骤,将不同来源的DNA片段进行组合和改造,从而获得具有特定功能的重组DNA分子。
这项技术在基因工程、生物医学研究和生物制药等领域发挥着重要作用。
通过不断的改进和创新,DNA体外重组技术将为人类带来更多的科学发展和应用前景。
基因工程重点总结

基因工程重点总结基因工程名词解释:基因工程:重组DNA技术或者基因转移技术,在体外将核酸分子插入病毒、质粒或其他载体分子,构成遗传物质的新组合,并使之渗入到原先没有这类分子的宿主细胞内,而能持续稳定的传递和表达。
报告基因:其编码产物能够被快速测定,常用来判断外源基因是否成功地导入受体细胞(器官或组织)并检测其表达活性的一类特殊用途的基因。
双元载体:由两个分别含有T―DNA和Vir区的相容性突变Ti质粒构成的双质粒载体系统。
受体系统:用于转化的外植体通过组织培养途径或其他非组织培养途径,能高效、稳定地再生无性系,并能接受外源基因的整合,对转化选择抗生素敏感的再生系统。
正负选择法:哺乳动物细胞转染DNA发生随机整合的几率相当高,而同源重组的频率则相当低。
正是由于这种缘故,给哺乳动物细胞的基因定向插入事件的检测造成了很大困难。
用于富集同源重组事件的特殊试验体系,涉及正选择和负选择两个方面。
基因靶标:通过在转染细胞中发生的外源基因与核基因组目标基因之间的DNA同源重组,使外源基因定点地整合到核基因组的特定位置上,从而达到改变系把你遗传特性的目的。
密码子使用的偏爱性:无论是真核基因还是原核基因,一种特定的氨基酸并不是以同等频率使用所有的同义密码子,而主要使用其中的某一两种。
这种密码子使用的非随机性现象选择标记基因:用于鉴别目标DNA的存在,将成功转化了质粒的宿主挑选出来的基因。
主要是一类编码可使抗生素或除草剂失活的蛋白酶基因。
HAT选择法:由于选择TK+细胞的培养基含有次黄嘌呤、氨基蝶呤和胸苷,所以称之为。
生殖细胞浸泡法:将供试外植体如种子、胚、胚珠、子房、花粉粒、幼穗悬浮细胞培养物等直接浸泡在外源DNA溶液中,利用渗透作用把外源基因导入受体细胞并稳定地整合、表达和遗传。
胚囊、子房注射法:使用微量注射器把外源DNA溶液注射到子房或胚囊中,由于卵细胞的吸收使外源DNA进入受精的卵细胞中,从而获得转基因的种子。
DNA的重组

7.2 同源重组
同源重组的概念
同源重组的特点 同源重组的功能 同源重组的机制 细菌的基因转移和重组
7.2 同源重组
同源重组的概念
同 源 重 组是两 条 具 有 同源 序 列 的 DNA靠近时所发生的DNA交换。
真核生物的同源 重组发生在减数 分裂时,姐妹染 色单体间遗传物 质间的交换。
7.2 同源重组
溶菌和溶源状态通过位点特异性重组可 以相互转变且可逆,原先存在的DNA顺 序全部被保存下来,并无丢失。 噬菌体和细菌DNA之间有一段很短的同 源序列,重组交换必须通过其中一个特 定的核苷酸。
7.3 位点特异性重组
l噬菌体整合作用的相关元件
细菌DNA和l-DNA的特异附着位点
l噬菌体特异附着位 点为attP,由POP’ 三部分组成。 细菌特异附着位点 为attB,由BOB’三 部分组成。 重 组 后 位 点 为 attL 和 attR , 分 别 由 BOP’ 和 POB’ 序 列 组成。 attP 和 attB 序 列 中 有 一段相同的核心序列 O,是重组发生的区 域。
7.2 同源重组
细菌的同源重组 发生在接合过程 中,交配的染色 体在两个紧密接 触的细胞中转移, 接合引起重组。
7.2 同源重组
Homologous Recombination
重组修复中也发生同源重组。
7.2 同源重组
同源重组的特点
要求较大的同源DNA片段(﹥75bp) 才能进行交换,同时需要重组酶RecA 参与。 同源片段相同或相近,在任何位点均可 发生重组,但存在重组热点。 整个基因组重组频率不恒定,受综合效 应和局部效应的影响。
7.2 同源重组
切断
Holliday重组模型
交叉
基因工程知识点总结

基因工程知识点总结基因工程,这个在现代生物学中熠熠生辉的领域,正以惊人的速度改变着我们的生活和对生命的认知。
它就像是一把神奇的钥匙,开启了无数未知的大门,为解决人类面临的诸多问题带来了前所未有的希望和可能。
一、基因工程的定义与基本原理基因工程,简单来说,就是按照人们的意愿,将一种生物的基因在体外进行切割、拼接和重组,然后导入另一种生物的细胞内,使之稳定遗传并表达出相应产物的技术。
其基本原理基于三个重要的步骤:首先是获取目的基因,这就像是在茫茫基因海洋中找到我们想要的那一颗珍珠;其次是构建基因表达载体,相当于给这颗珍珠打造一个合适的盒子,使其能够安全、有效地传递;最后是将重组 DNA 分子导入受体细胞,并使其在受体细胞中稳定存在和表达。
二、获取目的基因的方法1、从基因文库中获取基因文库就像是一个巨大的基因仓库,里面存储着各种各样的基因。
我们可以根据已知的信息,从这个文库中筛选出我们需要的目的基因。
2、利用 PCR 技术扩增目的基因PCR 技术就像是一个基因的复印机,能够以极少量的基因片段为模板,快速大量地复制出我们想要的基因。
3、人工合成法如果已知目的基因的核苷酸序列,或者其氨基酸序列,我们可以通过化学方法直接人工合成目的基因。
三、基因表达载体的构建基因表达载体是基因工程的核心部分,它就像是一辆专门运输基因的列车,需要具备多个关键组件。
1、启动子启动子是基因表达的“开关”,它能够控制基因在何时何地开始表达。
2、终止子终止子则是基因表达的“刹车”,告诉基因在何处停止表达。
3、标记基因标记基因就像是一个个小标签,帮助我们筛选出成功导入目的基因的受体细胞。
4、目的基因这是我们最终想要表达的基因片段。
四、将目的基因导入受体细胞1、导入植物细胞(1)农杆菌转化法农杆菌就像是一个天然的基因运输工具,能够将其携带的基因转移到植物细胞中。
(2)基因枪法通过高速的微粒将目的基因直接打入植物细胞。
(3)花粉管通道法利用花粉管通道将目的基因导入植物的受精卵中。
基因转移技术

影响DEAE-葡聚糖的转染效率的主要因素:细胞的数 量、DNA的浓度和DEAE-葡聚糖的浓度最为重要。大 体说来,按每个直径10cm的培养皿中加入 1~10ug的 转染DNA,并使用每毫升培养基含100~400ug DEAE-葡聚糖的溶液,对于绝大多数类型的细胞,都 能得到很好的转染效率。由于DEAE-葡聚糖对有些细 胞具有毒性,因此用低浓度溶液作短时间的接触反类是将目的基因转导入体外培养的细胞或导入从 体内取出的细胞,观察目的基因在细胞中的表达,这 项技术称基因转染(gene transfection )技术。通常情 况下,该技术转入的目的基因不与细胞染色体发生整 合,而是在细胞质呈现暂时性表达,随时间推移而逐 渐减弱或消失。为了使目的基因进入细胞后能与细胞 基因组DNA发生整合、产生永久性的表达,需用病毒 载体将目的基因导入细胞,并发生整合;
.
在1987年,Vlein首先报道了应用此技术将 TMV(烟草花叶病毒)RNA吸附到钨粒表面, 轰击洋葱表皮细胞,经检测发现病毒RNA能进 行复制,并以同样技术将CAT(Chloraphericol acetyltransferase氯霉素乙酰转移酶基因)基因 导入洋葱表皮细胞。现在,该技术已在烟草、 水稻、小麦、黑麦草、甘蔗、棉花、大豆、菜 豆、洋葱、番木瓜、甜橙、葡萄等多种作物上 成功。
.
它是目前基因转移效率较好的一种基因转移方 法, 1.可直接用不含有原核载体DNA片段的外 源基因进行转移; 2.外源基因的长度不受限制, 可达100kb ; 3.实验周期相对比较短。
.
.
二、电穿孔法(Electroporation)
.
电穿孔(electroporation)是指在高压电脉冲的作用下 使细胞膜上出现微小的孔洞。从而导致不同细胞之间 的原生质膜发生融合作用的细胞生物学过程。几乎所 有类型的细胞,包括植物的原生质体、动物的初生细 胞,以及不能用其它方法(诸如磷酸钙或DEAE-葡聚糖 法)转染的细胞,都可以成功地使用电穿孔技术进行基 因转移。此项技术具有操作简便,基因转移效率高等 优点。
DNA体外重组技术介绍

星活性: 酶切反应条件不能满足最适 条件,导致某些酶产生第二活性.
EcoR I*
GAATTC
AATT
酶切反应体系的建立:
标准的酶切体系 1μgDNA,20μl总反应体积,1U酶,推 荐的Buffer和温度,反应1h
酶切体系组成
• 内切酶 根据实验目的选择,保存,使 用,稀释(避免失活与污染)
第五章
DNA体外重组技术
概述
一、DNA重组技术相关概念
克隆(clone) 来自于同一始祖的一群相同分子、细菌、细 胞
或克动 隆物 化((c常lo被ni成ng为) 副本或拷贝)。 获取大量单一拷贝的过程,也称无性繁殖。
DNA克隆(DNA cloning)
应用酶学的方法,在体外将各种来源的遗传 物质(同源的或异源的、原核的或真核的、天然 的或人工的DNA)与载体DNA接合成一具有自我 复制能力的DNA分子。
• 大肠杆菌LacZ基因:编码半乳糖苷酶, 分解X-gal,使菌落为蓝色。
pBR322质粒:一种克隆质粒
结构:
ORI:复制起始点, 保证高拷贝自我复制。
Ampr, Tetr:
Ampr
两个抗性基因用于
Tetr
筛选阳性克隆。
Pst I, BamH I:
两个单酶切位点用于 ORI 插入目的基因
pfxBlue: 克隆质粒
质粒载体
体 酵母人工染色体
粘性载体
二、不同载体的特点与分类 (一)质粒载体 1. 质粒(plasmid)
定义: 细菌染色质以外的双链环状DNA, 能自我复制和表达其携带的遗传信息。
染色质 质粒 细菌培养
大肠杆菌
质粒扩增并表达蛋白质
微生物学理论:基因转移及重组

细菌基因转移和重组的⽅式有转化、接合、转导、溶原性转换和原⽣质体融合。
1.转化受体菌直接摄取供体菌DNA,从⽽获得新的遗传性状的过程称为转化。
2.接合细菌通过性菌⽑相互连接沟通,将质粒或染⾊体的DNA从供体菌转移给受体菌的过程称为接合。
3.转导以噬菌体为媒介,将供体菌DNA⽚段转移到受体菌内,使受体菌获得新的遗传性状的⽅式称转导。
根据转导DNA ⽚段的范围,可分为普遍性转导和局限性转导:①普遍性转导是因供体菌染⾊体或质粒的任何DNA⽚段都有可能被转导,故称为普遍性转导;②局限性转导是前噬菌体从宿主菌染⾊体切离时发⽣偏差,将前噬菌体两旁的基因转移到受体菌,使后者的遗传性状发⽣改变的过程。
4.溶原性转换溶原性细菌因染⾊体上整合有前噬菌体⽽获得新的遗传性状称为溶原性转换。
溶原性转换可使某些细菌发⽣毒⼒变异或抗原性变异。
5.原⽣质体融合是分别将两种细菌经处理失去细胞壁悬于⾼渗培养基中保持原⽣质体状态,然后将两种细菌的原⽣质体混合,滴加聚⼄⼆醇促使原⽣质体融合。
融合后的双倍体细胞可以短期⽣存,在此期间染⾊体之间可以发⽣基因的交换和重组,获得多种不同表型的重组融合体。
融合体经培养重新形成细胞壁,再按其遗传标志选择重组菌。
第七章 基因与基因组学

宣告完成。六国联合体:2001年2 月15日《Nature》 Celera公司:2001年2 月16日《Science》
•2003年4月14日,中、美、日、德、法、英6国科学家
宣布人类基因组序列图绘制成功,人类基因组计划的 所有目标全部实现(弗朗西斯·柯林斯)。温家宝等六 国首脑联名祝贺(标志着后基因组时代来临) 。
(三)第三代基因工程技术——途径工程
第二节 动物基因组学
一、
人类基因组计划(HGP)20世纪人类科技发展史上的三大创举 90年代人类基因组计划 60年代人类首次登上月球
40年代第一颗原子弹爆炸
•1986年,杜尔贝科在《Science》短文《癌症研究
的转折点--人类基因组测序》 。
•1990年,人类基因组计划正式启动,沃森担任
(5)猪的EST专门数据库: /
(6)小鼠单倍型图谱:
/haplotype_map.html (7)QTL在线分析系统:
/ (8)免费医学杂志(含遗传学):
要意义,中国基因组研究中心的测序 能力已跃居世界6大测序大国的16个 测序中心的第7位。
• 以人类基因组和拟南芥基因组为例说明你对生 物基因组全序测定工作的科学意义与社会意义 的认识(8分)
中国科学院2002年 硕士学位研究生入学分子遗传学试题
二、 动物基因组计划
2005年“中-丹家猪基因组计划” 1999年线虫基因组测序 2002年小鼠基因组测序 2005年家蚕基因组测序 2004年斑马鱼基因组测序 2005年绵羊基因组测序 2000年果蝇基因组测序
▪定向测序(Derected or ordered approaches)
▪ 克隆排序(Generate ordered clones ▪ Minimal redundance sequencing) ▪ 引物步移(Primer walking) ▪ 转座子插入(Transposon insertion) ▪ 限制性酶切片段亚克隆(Restriction
第七章重组体克隆的筛选和鉴定总结
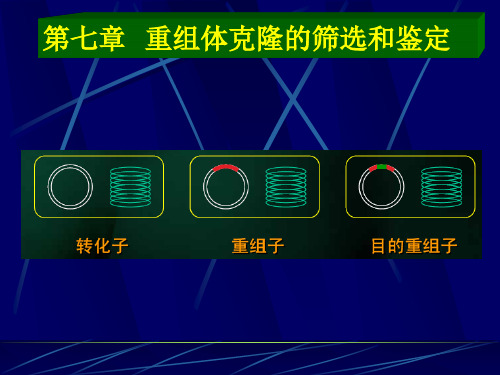
固相支 待测基因 一抗 持滤膜 产物蛋白
125I标记的二抗
125I 标记的二 固相支 待测基因 一抗 二抗 抗结合蛋白 持滤膜 产物蛋白
固相支 持滤膜
待测基因 一抗 产物蛋白
125I标记的二抗
固相支 持滤膜
待测基因 一抗 二抗 产物蛋白
125I
标记的二抗 结合蛋白
2. 放射性抗体检测法过程
3. Broome-Gilbert双位点检测法
Southe rn blot 筛选结 果
酶切前
酶切后
载体
插入片断
4. Northern blotting 用DNA(或RNA) 探针检测RNA样 品。 主要检测插入片 断是否被转录。 从宿主细胞中提 取RNA,再用探 针杂交。
第三节 免疫化学检测法
对表达产物的检测。蛋白——蛋白“杂交”
利用抗体作为“探针”来检测转入受体 菌并且表达出相应的蛋白质的外源基因。 一、放射性抗体检测法 1. 抗体与产物的结合方式 根据第一抗体(一抗)和第二抗体(二抗) 的性质可分为几种作用方式:
四、 核酸分子杂交检测法
1、原理: 1). 核酸杂交 重组克隆与探针杂交。
2). 检测用的探针 与外源DNA插入片断互补的序列。 3). 识别标记 (1)放射性同位素 (2)非放射性标记
32P
荧光素
2、菌落噬菌斑原位杂交筛选 特点: 对应的菌斑或噬菌斑位置不变, 可以直接找出阳性菌落。
3. Southern blotting 用DNA(或RNA)探针检测DNA样品。 从细胞中提取DNA(或质粒载体),再用探 针杂交。 只有带有插入片断的重组载体才能与探针杂 交,在底片上曝光显示。
第七章 重组体克隆的筛选和鉴定
第一节 利用遗传标记的表型特征筛选
基因的体外重组和转化1

提高重组率
(1)连接酶用量:注意甘油浓度
(2)作用时间与温度:12-15℃ (3)DNA分子:酶切完全,回收 (4)底物浓度:载体分子与外源DNA分子 (5)载体分子与外源DNA分子间的比例 1:3-10
二、重组体导入细胞
利用少量连接产物产生大量重组DNA分子(扩增) 便于筛选(纯化) 外源基因表达(表达)
5’
模板 3 ’-
互补序列
GCTAGCCGG
-5’
延伸
5’
3 ’模板 PCR产物 互补序列 GCTAGCCGG
-5’
带酶切位点的PCR产物
5’3’GCAGAATTC CGTCTTAAG EcoRI位点 PCR产物 PCR产物 CGATCGGCC GCTAGCCGG BamHI位点
-3’
-5’
EcoRI
连接效率低
用末端转移酶给平末端DNA片段加尾,连接。
(3)DNA片段末端加衔接物或接头,形成粘性末端后连接
(4)PCR产物的连接
(一)粘性末端的连接
具有粘性末端的两个双链DNA分子在DNA连接酶的作用下, 连接 成为一个杂合双链DNA。
(1) 两DNA片段的连接
依 靠 相 同 的 粘 性 末 端
(2)带酶切位点的引物的结构 3’端15-20bp与模板互补; 5’端6-10bp是某个内切酶的识别序列。 (5’端多余的3-5bp属保护碱基)
!!注意 ①添加保护序列
Primer1: 5' GCGGggatccTATGGTGAGCAAGGGCGAGGA
Primer2: 5‘ GCGGggatccTCTTGTACAGCTCGTCCATGCC
③易于转化或转导
微生物学:第七章微生物的遗传和变异

第二节、微生物的突变
基因突变
染色体畸变
DNA损伤的修复
概念
突变:指遗传物质发生数量或结构变化的现象。 变异:突变导致性状的改变叫变异。 基因突变:指一个基因内部遗传物质结构或 DNA序列的任何变化,包括一对或少数几对的 缺失、插入或置换,导致遗传性状的变化。 基因型:指贮藏在遗传物质中的信息,即DNA 碱基序列。 表型:指可观察或检测到的个体性状或特征,是 特定的基因型在一定环境条件下的表现。
实验室里通过提取获得 双链DNA有转化能力,单链没有.
感受态
受体细胞能接受转化的生理状态称为感受态, 只有处于感受态的细菌才能接受转化因子, 从出现到消失约为40分钟(对数期的中期)
感觉态出现原因
细菌失去部分细胞壁的结果 细菌在细胞表面产生某种E引起
感受态的决定决定因素
细胞遗传性决定 和菌龄有关 环腺苷酸CAMP可提高1000 倍 Ca2+能促使细胞进入感受态
原理 步骤
DNA只含P不含S
Pr 只含S不含P
1:用含同位素S35, P32的培养基培养大肠杆菌 2:让T2感染上述大肠杆菌使其打是S35P32标记
3: 吸附
10分钟后 搅动
离心
上清液 沉淀
结果:上清液中含15%放射击性;沉淀中含85%放射性
植物病毒的重建实验
植物病毒蛋白质和RNA可以人为地分开, 同时又可把它们重新组合成具感染性的病毒.
喷入T1保温
6个平板共353个菌落
6个平板共28个菌落
影印培养试验
原始敏 感菌种
无药 培养基
含药 培养基
基因突变机制
碱基的置换 移码突变
染色体畸变
1 诱变的机制
(1)碱基的置换
基因工程笔记总结

基因工程笔记总结一、基因工程的概念。
基因工程是指按照人们的愿望,进行严格的设计,并通过体外DNA重组和转基因等技术,赋予生物以新的遗传特性,从而创造出更符合人们需要的新的生物类型和生物产品。
又称为DNA重组技术。
(一)基因工程的理论基础。
1. DNA是遗传物质。
- 肺炎双球菌的转化实验和噬菌体侵染细菌的实验证明了DNA是遗传物质,这为基因工程中对DNA的操作提供了理论依据。
2. DNA双螺旋结构和中心法则的确立。
- 沃森和克里克构建的DNA双螺旋结构模型,阐明了DNA的结构特点,为DNA的切割、连接等操作提供了可能。
- 中心法则揭示了遗传信息的传递规律,使得人们能够理解基因表达的过程,从而在基因工程中对目的基因的表达进行调控。
3. 遗传密码的破译。
- 遗传密码的破译使得人们能够根据蛋白质的氨基酸序列推测出相应的DNA序列,反之亦然,这有助于在基因工程中准确获取目的基因并预测其表达产物。
二、基因工程的基本工具。
1. “分子手术刀”——限制性核酸内切酶(限制酶)- 来源:主要从原核生物中分离纯化而来。
- 作用:识别双链DNA分子的某种特定核苷酸序列,并且使每一条链中特定部位的两个核苷酸之间的磷酸二酯键断开。
例如,EcoRI限制酶识别的序列是 - GAATTC -,在G和A之间切开。
- 结果:产生黏性末端(如EcoRI产生的是黏性末端)或平末端。
2. “分子缝合针”——DNA连接酶。
- 类型。
- E.coli DNA连接酶:来源于大肠杆菌,只能将双链DNA片段互补的黏性末端之间连接起来。
- T4 DNA连接酶:来源于T4噬菌体,既可以连接黏性末端,也可以连接平末端。
- 作用:恢复被限制酶切开的两个核苷酸之间的磷酸二酯键。
3. “分子运输车”——载体。
- 种类。
- 质粒:是一种裸露的、结构简单、独立于细菌拟核DNA之外,并具有自我复制能力的双链环状DNA分子,是基因工程最常用的载体。
- λ噬菌体的衍生物:经过改造后可作为基因工程的载体。
第7章基因治疗精品PPT课件
1、内源基因的变异 2、外来生物的入侵
基因致病
基因结构的异常 基因表达的异常
2
基因诊断常用技术
• 核酸分子杂交: • PCR: • 生物芯片: DNA芯片或基因芯片 • 基因测序:
3
血友病A基因诊断
• 病因:factor VIII 基因缺陷 (碱基取代、缺失或插入等), 使凝血因子VIII 无活性或不 稳定,导致凝血障碍。
10
基因治疗的两种途径
ex vivo
靶细胞
载体 目的基因
in vivo
11
基因治疗的总体策略
1、基因矫正(修正)(gene correction):未实现 2、基因置换 (gene replacement): 3、基因修饰(增补)(gene augmentation): 4 、基因激活(gene activation): 5 、基因失活(干预)(gene interference ):反
细胞生长分裂
10天 Gene表达
IL-2刺激C分裂
回输患儿体内
1~2月治疗一次, 10个月 患儿体内ADA水平达正常人的25%
22
基因治疗基本过程 例2
• 逆转录病毒载体 +FⅨcDNA
重组体
5` LTR FⅨ neo SV PSO LTR 3`
①导入仓鼠细胞(CHO )→FⅨ表达;
②导入乙型血友病患者皮肤成纤维细胞(体外培养) →FⅨ表达;
18
7.2 基因治疗的载体
7.2.1 逆转录病毒载体 7.2.2 腺病毒载体 7.2.4 单纯疱疹病毒
19
7.2.1 逆转录病毒载体
• 正链RNA病毒
• 5’ gag- pol-
env 3’
《基因工程》 第七章 重组子选择筛选与分析

第十八页,共四十四页。
③ 卡那霉素 (kanamycin, Kn或 Kan): 含Kan抗性基因菌体转译一种能修饰Kn的 酶,阻碍Kn对核糖体的干扰(gānrǎo)。 四环素(tetracymic, Tc或 Tet): 含Tc抗性基因的菌体转译一种能改变细菌膜的蛋白, 防止Tc 进入细胞后干扰细菌蛋白质的合成。
⑥ 链霉素(strentomycin, Sm或 Str): 含Str 抗性基因的菌体转译一种能修 饰Sm的酶,抑制Sm与核糖体结合。
第三页,共四十四页。
1.根据载体选择标记初步筛选转化子
载体DNA分子上通常携带了一定的选择遗传标记基因,可进行转化 子或重组子初步筛选。做法(zuòfǎ)是将转化处理后的菌液(包括对照处理) 适量涂布在选择培养基上,在最适生长温度条件下培养一定时间,观察 菌落生长情况,即可挑选出转化子。
对于受体细胞而言,通常用LB培养基,在LB 培养基中加入适量的某种 选择物,即为选择培养基。选择物是由载体DNA分子上携带的选择标记基因 所决定。
3) Immunological screening for expressed genes (Western blotting)
4) Analysis of cloned genes (Restriction mapping, DNA sequencing)
2
第二页,共四十四页。
第一节 转基因筛选(shāixuǎn)和选择的方法
(1)抗药性筛选法 (2)插入失活筛选法 (3)插入表达筛选法
第四页,共四十四页。
(1)抗药性筛选
这是利用载体DNA分子上的抗药性筛选标记进行筛选的方法。主要用于 重组质粒DNA分子的转化子筛选。重组质粒DNA分子携带特定的抗药性 选择标记基因,在含有相应选择药物的选择培养基上正常生长。 ① 氨苄青霉素(ampicillin,Ap 或Amp): 含bla基因的菌体能转译 -丙酰胺酶 (-lactarnase),可降解Ap。 ② 氯霉素 (chloramphenicol, Cm 或 Cmp): 含 cat基因的菌体能转译氯霉素乙酰 转酰酶 (chloramphenicol acetyltransferase),使Cm乙酰化而失效。
DNA重组和基因转移

烟草原生质体与Ti质粒转移的共培养法程序为:
①从烟草无菌苗中分离原生质体,并预培养24小时。
②原生质体与农杆菌混合培养,原生质体浓度 l05 / ml 、农杆 菌l07/ml,20℃下保温32小时。
③冲洗去游离的细菌,将原生质体培养在有抗生素(250mg/L 万古霉素, 200mg / L羧苄青霉素, 200mg/ L链霉素 ) 的培养 基中,这些抗生素抑制细菌生长,而对原生质体无毒害。 ④3周后,离心收集细胞团,再培养在无激素培养基上,2周内, 转化的细胞团是激素非依赖性生长细胞团,在该培养基中可快 速生长,而非转化的细胞团则生长很慢,最后变褐死亡。
4、DNA接头连接法 接头的一端是齐平的,而另一端是某种内切酶的粘性末端,先 利用齐平末端连接方法将它与平端的外源DNA连接起来,造成 人工粘性末端,即可再与之互补的粘性末端的载体DNA相连接。
三、载体与DNA片段酶切位点不匹配的连接
所谓载体与DNA片段酶切位点不匹配,指载体与待克隆的 DNA片段上的酶切位点不相同,因而用一种或两种酶切制 造不出可互补的粘性末端。 1、按照平末端连接方法加上接头。
1.杂交抑制转译
要求:被研究的目的基因编码有丰富的mRNA 。 原理: DNA 杂交 提取重组DNA 体外转译 与mRNA总杂交 蛋白电泳放射自显影 (1) 蛋白电泳放射自显影 (2)
筛选出重组菌落 (或噬菌斑)
mRNA
蛋白质
×
步骤:
转化菌落 提取出来 总mRNA
蛋白质
形成DNA-RNA杂种分子
将总mRNA(包括DNA-RNA分子
(二)DNA直接导入法
1、物理方法 (1)基因枪法
80年代末期,由康奈尔大学的Sanford最先提出,主要 是为了克服以往各种基因转化技术的局限。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
退火
5' 5' T GATCC ACTAG G T GATCC ACTAG G T4-DNA ligase 5' 5' TGATCC ACTAGG GGATCA CCTAGT G GATCA CCTAG T G GATCA CCTAG T
5'
5'
5' 5'
TGATCC ACTAGG
GGATCA CCTAGT
Klenow
5' GAATT CTTAA 5' TdT
补平
5' AATTC TTAAG dGTP
补平
GGATC CCTAG 5' dCTP GGATCCCCCCC CCTAG
5'
GAATTGGGGGG AATTC GGGGGGTTAAG CTTAA
退火
BamH I 5' 5'
GAATTGGGGGGGATCC CTTAACCCCCCCTAGG
TG AC
CA GT
5.粘性末端的更换
5' BamHI 5' GGATCC CCTAGG 5'
G CCTAG 5'
Klenow
5' GATCC G
5'
补平
5' GATCC CTAGG
5'
GGATC CCTAG 5'
T4-DNA ligase
5'
GGAATTCC CCTTAAGG
EcoR I
EcoR I linker
GGATC CCTAG 5'
5'
5'
5' GATCC CTAGG
T4-DNA ligase 5' 5' CGATCC GCTAGG GGATCG CCTAGC
5' 5'
CGATCC GCTAGG
GGATCG CCTAGC
4.人工粘性末端的连接 (1)5′突出末端
5' G CTTAA 5' 5' AATTC G EcoR I 5' 5' GATCC G Klenow 5' GATCC CTAGG TdT GATCC CCCCCCCTAGG T4-DNA ligase BamH I BamH I G CCTAG 5'
GCATGCCCCCC 3' C C 3' CCCCCCGTACG
G 3' GGGGGGACGTC
CTGCAGGGGGG 3' G
退火
5' 5'
GCATGCCCCCC G C GGGGGGACGTC GCATGCCCCCC G C GGGGGGACGTC
Klenow Pst I
CTGCAGGGGGG C G CCCCCCGTACG CTGCAGGGGGG C G CCCCCCGTACG
3.不同粘性末端的连接
5' CTGCAG GACGTC PstI 5' CTGCA 3' G G 3' ACGTC 5' 5' GGATCC CCTAGG BamHI 5' GATCC G G CCTAG 5' GGATCC CCTAGG
5'
5'
T4-DNA pol
切平
C G G C
Klenow
补平
GTTTTTTTTTTG CAAAAAAAAAAC GTTTTTTTTTTG CAAAAAAAAAAC
加热
CAAAAAAAAAAC GTTTTTTTTTTG CAAAAAAAAAAC GTTTTTTTTTTG
S1
5' 5'
TTTTTTT T GT TG CAA AC AAAAAAA
AAAAAAA A CA AC GTT TG TTTTTTT
5'
5'
5' Βιβλιοθήκη 'GAATTC CTTAAG
GAATTC CTTAAG
2.同尾酶生产的粘性末端的连接
5' BclI 5' T ACTAG 5' 5' GATCA T TGATCA ACTAGT 5'
5'
GGATCC CCTAGG BamHI 5' GATCC G
GGATCC CCTAGG
5'
5'
G CCTAG 5'
5'
GGATCGGAATTCCGATCC CCTAGCCTTAAGGCTAGG
BamHI的位点已被 破坏
5'
6.重组率
重组率的定义
重组率 = 含有外源DNA的重组分子数 / 载体分子总数 在常规实验条件下,重组率一般为25 - 75%
重组率是衡量连接反应效率的重要指标,较高的重组率可以
大大简化DNA重组的后续操作。
GAATTGGGGGGGATCC CTTAACCCCCCCTAGG
GGATCCCCCCCAATTC CCTAGGGGGGGTTAAG
GGATCCCCCCCAATTC CCTAGGGGGGGTTAAG
5' 5'
4.人工粘性末端的连接 (2)3′突出末端
5' GCATG 3' C TdT C 3' GTACG dCTP Sph I 5' G 3' ACGTC TdT CTGCA 3' Pst I G dGTP
T4-DNA ligase Pst I
5' 5'
5'
5'
GCATGCCCCCCTGCAG CGTACGGGGGGACGTC GCATGCCCCCCTGCAG CGTACGGGGGGACGTC
CTGCAGGGGGGCATGC GACGTCCCCCCGTACG CTGCAGGGGGGCATGC GACGTCCCCCCGTACG
第七章 DNA体外重组与基因转移
一、 DNA的体外重组(切、接) 二、重组DNA分子的转化和扩增(转、增)
第八章 重组子的筛选与鉴定(检) 第九章 外源基因的表达
切
接
转
增 检
一、 DNA的体外重组(切与接)
1.同种内切酶生产的粘性末端的连接 2.同尾酶生产的粘性末端的连接 3.不同粘性末端的连接
4.人工粘性末端的连接
5.粘性末端的更换 6.重组率
1.同种内切酶生产的粘性末端的连接
5' GAATTC CTTAAG EcoRI 5' G CTTAA 5' 5' AATTC G G CTTAA 5' 5' AATTC G GAATTC CTTAAG 5'
5'
退火
5' 5' G AATTC CTTAA G G AATTC CTTAA G T4-DNA ligase 5' 5' GAATTC CTTAAG GAATTC CTTAAG G AATTC CTTAA G G AATTC CTTAA G
5' 5'
4.人工粘性末端的连接 (3)平头末端
5' G 3' C TdT C 3' G dTTP 5' G 3' C TdT C 3' G dATP
GTTTTTTTTTT 3' C C 3' TTTTTTTTTTG
G 3' AAAAAAAAAAC
CAAAAAAAAAA 3' G
退火
5' 5'
T4-DNA ligase
