化学乙醇与乙酸的专项培优练习题附答案
化学 乙醇与乙酸的专项 培优练习题及答案解析

化学 乙醇与乙酸的专项 培优练习题及答案解析一、乙醇与乙酸练习题(含详细答案解析)1.乙烯是来自石油的重要有机化工原料。
结合路线回答:已知:2CH 3CHO+O 2→2CH 3COOH(1)D 是高分子,用来制造包装材料,则反应V 类型是____。
产物CH 2=CHCOOH 也能发生相同类型的化学反应,其化学方程式为:____(2)E 有香味,实验室用A 和C 反应来制取E①反应IV 的化学方程式是____。
②实验室制取E 时在试管里加入试剂的顺序是____(填以下字母序号)。
a .先浓硫酸再A 后Cb .先浓硫酸再C 后Ac .先A 再浓硫酸后C③实验结束之后,振荡收集有E 的试管,有无色气泡产生其主要原因是(用化学方程式表示)____(3)产物CH 2=CH-COOH 中官能团的名称为____(4)①A 是乙醇,与A 相对分子质量相等且元素种类相同的有机物的结构简式是:____、____。
②为了研究乙醇的化学性质,利用如图装置进行乙醇的催化氧化实验,并检验其产物,其中C 装置的试管中盛有无水乙醇。
(加热、固定和夹持装置已略去)(1)装置A 圆底烧瓶内的固体物质是____,C 装置的实验条件是____。
(2)实验时D 处装有铜粉,点燃D 处的酒精灯后,D 中发生的主要反应的化学方程式为____【答案】加聚反应 nCH 2=CHCOOH→3252325ΔCH COOH+C H OH H O+CH COOC H ƒ浓硫酸C233322Na CO +2CH COOH 2CH COONa+H O+CO ═ 碳碳双键、羧基 CH 3-O-CH 3HCOOH 二氧化锰或MnO 2 热水浴 22523ΔO +2C H OH 2H O+2CH CHO →Cu【解析】【分析】由流程知,A 为乙醇、B 为乙醛、C 为乙酸、D 为聚乙烯、E 为乙酸乙酯,据此回答;【详解】(1)D 是聚乙烯,是一种高分子化合物,则反应V 类型是加聚反应,CH 2=CHCOOH 也能发生相同类型的化学反应,即因其含有碳碳双键而发生加聚反应,其化学方程式为:nCH 2=CHCOOH→;答案为:加聚反应;nCH 2=CHCOOH→; (2①反应IV 为乙酸和乙醇在一定条件下发生酯化反应,则化学方程式是3252325ΔCH COOH+C H OH H O+CH COOC H ƒ浓硫酸;答案为:3252325ΔCH COOH+C H OH H O+CH COOC H ƒ浓硫酸;②实验室制取乙酸乙酯时,试剂的添加顺序为乙醇、浓硫酸、乙酸,故选C ; 答案为:C ;③实验结束之后,用饱和碳酸钠收集到的乙酸乙酯内混有乙酸、乙醇,振荡后,有无色气泡产生的主要原因是乙酸和碳酸钠反应产生了二氧化碳气体,化学方程式为:233322Na CO +2CH COOH 2CH COONa+H O+CO ↑═;答案为:233322Na CO +2CH COOH 2CH COONa+H O+CO ↑═;(3)产物CH 2=CH-COOH 中官能团的名称为碳碳双键、羧基;答案为:碳碳双键、羧基;(4)①A 是乙醇,与A 相对分子质量相等且元素种类相同的有机物的结构简式是二甲醚、甲酸,则其结构简式为:CH 3-O-CH 3;HCOOH ;答案为:CH 3-O-CH 3;HCOOH ;②利用如图装置进行乙醇的催化氧化实验,并检验其产物,则其中A 装置用于产生氧气,从C 装置的试管中盛有无水乙醇,在D 装置中乙醇蒸汽和氧气的混合气在D 中发生催化氧化反应;则(1)装置A 圆底烧瓶内的固体物质是二氧化锰,C 装置的实验条件是水浴加热,便于能控制温度便于乙醇持续地挥发;答案为:二氧化锰或MnO 2;热水浴;(2)实验时D 处装有铜粉,点燃D 处的酒精灯后,D 中发生的主要反应为乙醇的催化氧化,则化学方程式为:22523ΔO +2C H OH 2H O+2CH CHO →Cu; 答案为: 22523ΔO +2C H OH 2H O+2CH CHO →Cu。
【化学】化学乙醇与乙酸的专项培优练习题(含答案)及答案解析

【化学】化学乙醇与乙酸的专项培优练习题(含答案)及答案解析一、乙醇与乙酸练习题(含详细答案解析)1.A 、B 、C 、D 、E 均为有机物,其中 B 是化学实验中常见的有机物, 它易溶于水并有特殊香味;A 的产量可衡量一个国家石油化工发展的水平,G 是生活中常见的高分子材料。
有关物质的转化关系如图甲所示:(1)写出 A 的结构式_____;B 中官能团的名称为_____。
(2)写出下列反应的化学方程式:反应③____;反应④____。
(3)实验室利用反应⑥制取 E ,常用如图装置:①a 试管中主要反应的化学方程式为_____。
②实验开始时,试管甲中的导管不伸入液面下的原因是_____;当观察到试管甲中_____时,认为反应基本完成。
【答案】 羟基 u 322322CH CH OH+O 2CH CHO+2H O C ∆→ 22nCH =CH →一定条件3233232ΔCH CH OH+CH COOH CH COOCH CH +H O ƒ浓硫酸防止倒吸 不再有油状液体滴下【解析】【分析】 A 的产量可衡量一个国家石油化工发展的水平,A 是乙烯,结构简式为CH 2=CH 2;B 是化学实验室中常见的有机物,它易溶于水并有特殊香味,根据框图中信息,B 在红热铜丝发生催化氧化,可推知B 是乙醇,根据框图中的转化关系、反应条件和反应试剂可推得, C 是乙醛,D 是乙酸,E 是乙酸乙酯,据此进行解答。
【详解】A 的产量可衡量一个国家石油化工发展的水平,A 是乙烯,结构简式为CH 2=CH 2;B 是化学实验室中常见的有机物,它易溶于水并有特殊香味,根据框图中信息,B 在红热铜丝发生催化氧化,可推知B 是乙醇,根据框图中的转化关系、反应条件和反应试剂可推得, C 是乙醛,D 是乙酸,E 是乙酸乙酯。
(1)由上述分析可知A 的结构式为,B 为乙醇中官能团的名称为羟基,故答案为:;羟基;(2)反应③化学方程式为:u322322CH CH OH+O 2CH CHO+2H O C ∆→ ,反应④化学方程式为:22nCH =CH →一定条件 ,故答案为:u 322322CH CH OH+O 2CH CHO+2H O C ∆→;22nCH =CH →一定条件 ;(3)①反应⑥为乙酸和乙醇的酯化反应,则①a 试管中主要反应的化学方程式为3233232ΔCH CH OH+CH COOH CH COOCH CH +H O ƒ浓硫酸,故答案为:3233232ΔCH CH OH+CH COOH CH COOCH CH +H O ƒ浓硫酸; ②乙酸乙酯中混有的乙酸和乙醇蒸汽易溶于水,为了防倒吸,实验开始时,试管甲中的导管不伸入液面下;由于乙酸乙酯难溶于水,因此当观察到试管甲中不再有油状液体滴下时,反应基本完成,故答案为:防止倒吸;不再有油状液体滴下。
【化学】化学乙醇与乙酸的专项培优易错试卷练习题(含答案)含答案

【化学】化学乙醇与乙酸的专项培优易错试卷练习题(含答案)含答案一、乙醇与乙酸练习题(含详细答案解析)1.医药阿斯匹林的结构简式如图1所示:图1 图2试根据阿斯匹林的结构回答;(1)阿斯匹林看成酯类物质,口服后,在胃肠酶的作用下,阿斯匹林发生水解反应,生成A和B 两种物质。
其中A的结构简式如图2所示,则B的结构简式为__________;B中含有的官能团名称是________________。
(2)阿斯匹林跟NaHCO3同时服用,可使上述水解产物A与NaHCO3反应,生成可溶性盐随尿液排出,此可溶性盐的结构简式是_________________。
(3)上述水解产物A与氢氧化钠溶液反应的化学方程式为__________________。
【答案】CH3COOH 羧基【解析】【分析】(1)阿斯匹林发生水解反应,生成A和B两种物质,由A的结构简式可知B为乙酸;(2)A与小苏打反应,只有-COOH与碳酸氢钠反应;(3)A中-COOH、酚-OH均与NaOH反应。
【详解】(1)阿斯匹林发生水解反应,生成A和B两种物质,由A的结构简式可知B为乙酸,B的结构简式为CH3COOH,含官能团为羧基;(2)A与小苏打反应,只有-COOH与碳酸氢钠反应,则生成盐为;(3)A与足量的氢氧化钠溶液反应的化学方程式为。
2.已知A是来自石油的重要有机化工原料,E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。
根据下图转化关系完成下列各题:(1)A 的分子式是___________,C 的名称是____________,F 的结构简式是____________。
(2)D 分子中的官能团名称是________________,请设计一个简单实验来验证D 物质存在该官能团,其方法是_________________________________________________________。
(3)写出反应②、③的化学方程式并指出③的反应类型:反应②:___________________________________;反应③:___________________________________,反应类型是___________反应。
【化学】化学乙醇与乙酸的专项培优练习题(含答案)含答案

【化学】化学乙醇与乙酸的专项培优练习题(含答案)含答案一、乙醇与乙酸练习题(含详细答案解析)1.医药阿斯匹林的结构简式如图1所示:图1 图2试根据阿斯匹林的结构回答;(1)阿斯匹林看成酯类物质,口服后,在胃肠酶的作用下,阿斯匹林发生水解反应,生成A和B 两种物质。
其中A的结构简式如图2所示,则B的结构简式为__________;B中含有的官能团名称是________________。
(2)阿斯匹林跟NaHCO3同时服用,可使上述水解产物A与NaHCO3反应,生成可溶性盐随尿液排出,此可溶性盐的结构简式是_________________。
(3)上述水解产物A与氢氧化钠溶液反应的化学方程式为__________________。
【答案】CH3COOH 羧基【解析】【分析】(1)阿斯匹林发生水解反应,生成A和B两种物质,由A的结构简式可知B为乙酸;(2)A与小苏打反应,只有-COOH与碳酸氢钠反应;(3)A中-COOH、酚-OH均与NaOH反应。
【详解】(1)阿斯匹林发生水解反应,生成A和B两种物质,由A的结构简式可知B为乙酸,B的结构简式为CH3COOH,含官能团为羧基;(2)A与小苏打反应,只有-COOH与碳酸氢钠反应,则生成盐为;(3)A与足量的氢氧化钠溶液反应的化学方程式为。
2.乙烯是来自石油的重要有机化工原料。
结合路线回答:已知:2CH3CHO+O2→2CH3COOH(1)D 是高分子,用来制造包装材料,则反应V 类型是____。
产物CH 2=CHCOOH 也能发生相同类型的化学反应,其化学方程式为:____(2)E 有香味,实验室用A 和C 反应来制取E①反应IV 的化学方程式是____。
②实验室制取E 时在试管里加入试剂的顺序是____(填以下字母序号)。
a .先浓硫酸再A 后Cb .先浓硫酸再C 后Ac .先A 再浓硫酸后C③实验结束之后,振荡收集有E 的试管,有无色气泡产生其主要原因是(用化学方程式表示)____(3)产物CH 2=CH-COOH 中官能团的名称为____(4)①A 是乙醇,与A 相对分子质量相等且元素种类相同的有机物的结构简式是:____、____。
【化学】化学 乙醇与乙酸的专项 培优练习题及答案

【化学】化学乙醇与乙酸的专项培优练习题及答案一、乙醇与乙酸练习题(含详细答案解析)1.乙醇(CH3CH2OH)是一种重要的有机物(1)根据乙醇分子式和可能结构推测,1mol乙醇与足量钠反应,产生氢气的物质的量可能是________________mol。
(2)实验证明反应的乙醇与产生的氢气物质的量比值是2,该反应的化学方程式是________________________________,乙醇的官能团是_______________。
(3)用如图装置实验,干冷烧杯罩在火焰上,有无色液体产生。
能否据此说明一定有氢气产生,判断及简述理由是_________________________。
(4)乙醇与钠反应比水与钠反应平缓的多,原因是_______________________________ 。
【答案】0.5、2.5、3 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑羟基不能,因为氢气中会含有乙醇蒸汽乙醇分子中羟基上的氢原子没有水中氢原子活泼【解析】【分析】由乙醇的结构简式CH3CH2OH,可知乙醇分子内有三种不同环境下的氢原子,如果钠置换的是羟基氢原子,则1mol乙醇与足量钠反应生成0.5mol氢气,如果钠置换的是乙基上的氢原子,则1mol乙醇与足量钠反应生成2.5mol氢气,如果乙醇中的氢原子都能够被钠置换,则1mol乙醇与足量钠反应生成3mol氢气;乙醇的结构中含有官能团-羟基,能够与金属钠反应置换出氢气,且羟基中氢原子的活泼性小于水中氢原子活泼性,乙醇和钠反应与钠与水比较要缓慢的多,据以上分析解答。
【详解】(1)由乙醇的结构简式CH3CH2OH,可知乙醇分子内有三种不同环境下的氢原子,如果钠置换的是羟基氢原子,则1mol乙醇与足量钠反应生成0.5mol氢气,如果钠置换的是乙基上的氢原子,则1mol乙醇与足量钠反应生成2.5mol氢气,如果乙醇中的氢原子都能够被钠置换,则1mol乙醇与足量钠反应生成3mol氢气;(2)实验证明反应的乙醇与产生的氢气物质的量比值是2,说明钠与乙醇反应置换的是羟基上的氢原子,化学方程式为2C2H5OH+2Na→2C2H5ONa+H2↑;乙醇的官能团为羟基;(3) 图示实验装置不能说明一定有氢气产生,因为乙醇易挥发,乙醇、氢气燃烧都能生成水;(4) 乙醇分子中羟基上的氢原子没有水中氢原子活泼,乙醇与钠反应比水与钠反应平缓的多。
化学乙醇与乙酸的专项培优易错试卷练习题(含答案)附答案

化学乙醇与乙酸的专项培优易错试卷练习题(含答案)附答案一、乙醇与乙酸练习题(含详细答案解析)1.某有机物A,由C、H、O三种元素组成,在一定条件下,由A可以转化为有机物B、C、D、E;C又可以转化为B、D。
它们的转化关系如下:已知D的蒸气密度是氢气的22倍,并可以发生银镜反应。
(1)写出A、D、的结构简式和所含官能团名称A_______、________,D__________、___________(2)写出反应⑤的化学方程式___________________________________;(3)从组成上分析反应⑨是___________(填反应类型)。
(4)F的同分异构体中能与NaOH溶液发生反应的共_______种(包含F),写出其中一种与NaOH溶液反应的化学方程式______________【答案】C2H5OH 羟基 CH3CHO 醛基 2C2H5OH+O2 2CH3CHO+H2O 氧化反应 6 −−→CH3CH2OH+CH3COONaCH3COOC2H5+NaOH∆【解析】【分析】D的蒸气密度是氢气的22倍,则相对分子质量为44,并可以发生银镜反应,说明含有-CHO,则D为CH3CHO;D被氧化生成E为CH3COOH,D被还原生成A为CH3CH2OH;A可以与浓氢溴酸发生取代生成B,B可以与碱的水溶液反应生成A,则B为CH3CH2Br,B可以在碱的醇溶液中反应生成C,则C为CH2=CH2;A与E可发生酯化反应生成F,F为CH3COOC2H5。
【详解】(1)根据分析可知A为CH3CH2OH,其官能团为羟基;D为CH3CHO,其官能团为醛基;(2)反应⑤为乙醇的催化氧化,方程式为2C2H5OH+O2 2CH3CHO+H2O;(3)C为CH2=CH2,D为CH3CHO,由C到D的过程多了氧原子,所以为氧化反应;(4)F的同分异构体中能与NaOH溶液发生反应,说明含有羧基或酯基,若为酯则有:HCOOCH2CH2CH3、HCOOCH(CH3)2、CH3CH2COOCH3,若为羧酸则有:CH3CH(COOH)CH3、CH3CH2CH2COOH,所以包括F在内共有6种结构;酯类与NaOH反应方程式以乙酸乙酯为−−→ CH3CH2OH+CH3COONa,羧酸类:例:CH3COOC2H5+NaOH∆CH3CH2CH2COOH+NaOH=CH3CH2CH2COONa+H2O。
【化学】化学乙醇与乙酸的专项培优练习题及详细答案

【化学】化学乙醇与乙酸的专项培优练习题及详细答案一、乙醇与乙酸练习题(含详细答案解析)1.“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室制取乙酸乙酯。
回答下列问题:(1)浓硫酸的作用是:________________________。
(2)饱和碳酸钠溶液的主要作用是__________________________________________。
(3)通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是_____。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是_________________。
(5)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是_______。
(6)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。
下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)________。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸④正反应的速率与逆反应的速率相等⑤混合物中各物质的浓度不再变化【答案】催化作用和吸水作用吸收随乙酸乙酯蒸出的乙酸和乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到防止倒吸分液防止暴沸②④⑤【解析】【分析】(1)浓硫酸具有脱水性、吸水性及强氧化性;(2)饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;(3)挥发出来的乙酸和乙醇易溶于饱和碳酸钠溶液,导管伸入液面下可能发生倒吸;(4)乙酸乙酯不溶于水;(5)根据可逆反应平衡状态标志的判断依据进行分析。
【详解】(1)乙酸与乙醇在浓硫酸作催化剂加热条件下生成乙酸乙酯,由于反应为可逆反应,同时浓硫酸吸水有利于平衡向生成乙酸乙酯的方向移动,故答案为:催化作用和吸水作用;(2)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,主要是利用了乙酸乙酯难溶于饱和碳酸钠,乙醇与水混溶,乙酸能被碳酸钠吸收,易于除去杂质,故答案为:吸收随乙酸乙酯蒸出的乙酸和乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到;(3)导管若插入溶液中,反应过程中可能发生倒吸现象,所以导管要插在饱和碳酸钠溶液的液面上,目的是防止倒吸,故答案为:防止倒吸;(4)乙酸乙酯不溶于水,则要把制得的乙酸乙酯分离出来,应采用的实验操作是分液,故答案为:分液;(5)①单位时间内生成1mol乙酸乙酯,同时生成1mol水,都表示正反应速率,不能说明到达平衡状态,故①错误;②单位时间内生成1mol乙酸乙酯,同时生成1mol乙酸,说明正逆反应速率相等,反应达到平衡状态,故②正确;③单位时间内消耗1mol乙醇,同时消耗1mol乙酸,都表示正反应速率,不能说明到达平衡状态,故③错误;④正反应的速率与逆反应的速率相等,各组分的密度不再变化,达到了平衡状态,故④正确;⑤混合物中各物质的浓度浓度不再变化,各组分的密度不再变化,达到了平衡状态,故⑤正确;故答案为:②④⑤。
【化学】化学乙醇与乙酸的专项培优练习题及详细答案

【化学】化学乙醇与乙酸的专项培优练习题及详细答案一、乙醇与乙酸练习题(含详细答案解析)1.A 、B 、C 、D 、E 均为有机物,其中 B 是化学实验中常见的有机物, 它易溶于水并有特殊香味;A 的产量可衡量一个国家石油化工发展的水平,G 是生活中常见的高分子材料。
有关物质的转化关系如图甲所示:(1)写出 A 的结构式_____;B 中官能团的名称为_____。
(2)写出下列反应的化学方程式:反应③____;反应④____。
(3)实验室利用反应⑥制取 E ,常用如图装置:①a 试管中主要反应的化学方程式为_____。
②实验开始时,试管甲中的导管不伸入液面下的原因是_____;当观察到试管甲中_____时,认为反应基本完成。
【答案】 羟基 u 322322CH CH OH+O 2CH CHO+2H O C ∆→ 22nCH =CH →一定条件3233232ΔCH CH OH+CH COOH CH COOCH CH +H O ƒ浓硫酸防止倒吸 不再有油状液体滴下【解析】【分析】 A 的产量可衡量一个国家石油化工发展的水平,A 是乙烯,结构简式为CH 2=CH 2;B 是化学实验室中常见的有机物,它易溶于水并有特殊香味,根据框图中信息,B 在红热铜丝发生催化氧化,可推知B 是乙醇,根据框图中的转化关系、反应条件和反应试剂可推得, C 是乙醛,D 是乙酸,E 是乙酸乙酯,据此进行解答。
【详解】A 的产量可衡量一个国家石油化工发展的水平,A 是乙烯,结构简式为CH 2=CH 2;B 是化学实验室中常见的有机物,它易溶于水并有特殊香味,根据框图中信息,B 在红热铜丝发生催化氧化,可推知B 是乙醇,根据框图中的转化关系、反应条件和反应试剂可推得, C 是乙醛,D 是乙酸,E 是乙酸乙酯。
(1)由上述分析可知A 的结构式为,B 为乙醇中官能团的名称为羟基,故答案为:;羟基;(2)反应③化学方程式为:u322322CH CH OH+O 2CH CHO+2H O C ∆→ ,反应④化学方程式为:22nCH =CH →一定条件 ,故答案为:u 322322CH CH OH+O 2CH CHO+2H O C ∆→;22nCH =CH →一定条件 ;(3)①反应⑥为乙酸和乙醇的酯化反应,则①a 试管中主要反应的化学方程式为3233232ΔCH CH OH+CH COOH CH COOCH CH +H O ƒ浓硫酸,故答案为:3233232ΔCH CH OH+CH COOH CH COOCH CH +H O ƒ浓硫酸; ②乙酸乙酯中混有的乙酸和乙醇蒸汽易溶于水,为了防倒吸,实验开始时,试管甲中的导管不伸入液面下;由于乙酸乙酯难溶于水,因此当观察到试管甲中不再有油状液体滴下时,反应基本完成,故答案为:防止倒吸;不再有油状液体滴下。
化学乙醇与乙酸的专项培优练习题(含答案)含详细答案

化学乙醇与乙酸的专项培优练习题(含答案)含详细答案一、乙醇与乙酸练习题(含详细答案解析)1.乙醇(CH3CH2OH)是一种重要的有机物(1)根据乙醇分子式和可能结构推测,1mol乙醇与足量钠反应,产生氢气的物质的量可能是________________mol。
(2)实验证明反应的乙醇与产生的氢气物质的量比值是2,该反应的化学方程式是________________________________,乙醇的官能团是_______________。
(3)用如图装置实验,干冷烧杯罩在火焰上,有无色液体产生。
能否据此说明一定有氢气产生,判断及简述理由是_________________________。
(4)乙醇与钠反应比水与钠反应平缓的多,原因是_______________________________ 。
【答案】0.5、2.5、3 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑羟基不能,因为氢气中会含有乙醇蒸汽乙醇分子中羟基上的氢原子没有水中氢原子活泼【解析】【分析】由乙醇的结构简式CH3CH2OH,可知乙醇分子内有三种不同环境下的氢原子,如果钠置换的是羟基氢原子,则1mol乙醇与足量钠反应生成0.5mol氢气,如果钠置换的是乙基上的氢原子,则1mol乙醇与足量钠反应生成2.5mol氢气,如果乙醇中的氢原子都能够被钠置换,则1mol乙醇与足量钠反应生成3mol氢气;乙醇的结构中含有官能团-羟基,能够与金属钠反应置换出氢气,且羟基中氢原子的活泼性小于水中氢原子活泼性,乙醇和钠反应与钠与水比较要缓慢的多,据以上分析解答。
【详解】(1)由乙醇的结构简式CH3CH2OH,可知乙醇分子内有三种不同环境下的氢原子,如果钠置换的是羟基氢原子,则1mol乙醇与足量钠反应生成0.5mol氢气,如果钠置换的是乙基上的氢原子,则1mol乙醇与足量钠反应生成2.5mol氢气,如果乙醇中的氢原子都能够被钠置换,则1mol乙醇与足量钠反应生成3mol氢气;(2)实验证明反应的乙醇与产生的氢气物质的量比值是2,说明钠与乙醇反应置换的是羟基上的氢原子,化学方程式为2C2H5OH+2Na→2C2H5ONa+H2↑;乙醇的官能团为羟基;(3) 图示实验装置不能说明一定有氢气产生,因为乙醇易挥发,乙醇、氢气燃烧都能生成水;(4) 乙醇分子中羟基上的氢原子没有水中氢原子活泼,乙醇与钠反应比水与钠反应平缓的多。
【化学】化学乙醇与乙酸的专项培优练习题(含答案)附答案解析

【化学】化学乙醇与乙酸的专项培优练习题(含答案)附答案解析一、乙醇与乙酸练习题(含详细答案解析)1.医药阿斯匹林的结构简式如图1所示:图1 图2试根据阿斯匹林的结构回答;(1)阿斯匹林看成酯类物质,口服后,在胃肠酶的作用下,阿斯匹林发生水解反应,生成A和B 两种物质。
其中A的结构简式如图2所示,则B的结构简式为__________;B中含有的官能团名称是________________。
(2)阿斯匹林跟NaHCO3同时服用,可使上述水解产物A与NaHCO3反应,生成可溶性盐随尿液排出,此可溶性盐的结构简式是_________________。
(3)上述水解产物A与氢氧化钠溶液反应的化学方程式为__________________。
【答案】CH3COOH 羧基【解析】【分析】(1)阿斯匹林发生水解反应,生成A和B两种物质,由A的结构简式可知B为乙酸;(2)A与小苏打反应,只有-COOH与碳酸氢钠反应;(3)A中-COOH、酚-OH均与NaOH反应。
【详解】(1)阿斯匹林发生水解反应,生成A和B两种物质,由A的结构简式可知B为乙酸,B的结构简式为CH3COOH,含官能团为羧基;(2)A与小苏打反应,只有-COOH与碳酸氢钠反应,则生成盐为;(3)A与足量的氢氧化钠溶液反应的化学方程式为。
2.X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:元素代号X Y Z M Q R原子半径/nm0.1600.1430.1020.0750.0770.037主要化合价+2+3+6,-2+5,-3+4,-4+1(1)Z在元素周期表中的位置是_________________________。
(2)元素Q 和R 形成的化合物A 是果实催熟剂,用A 制备乙醇的化学方程式是_______________________。
(3)单质铜和元素M 的最高价氧化物对应水化物的浓溶液发生反应的离子方程式为___________________。
【化学】化学乙醇与乙酸的专项培优练习题(含答案)及答案解析

【化学】化学乙醇与乙酸的专项培优练习题(含答案)及答案解析一、乙醇与乙酸练习题(含详细答案解析)1.食品安全关系国计民生,影响食品安全的因素很多.(1)聚偏二氯乙烯()具有超强阻隔性能,可作为保鲜食品的包装材料.它是由________(写结构简式)发生加聚反应生成的,该物质的分子构型是__________________________ 。
(2)劣质植物油中的亚油酸(]324227[CH (CH )CH CHCH CH CH CH )COOH ==含量很低,下列关于亚油酸的说法中,正确的是_________。
A .分子式为18342C H OB .一定条件下能与甘油(丙三醇)发生酯化反应C .能和NaOH 溶液反应D.不能使酸性KMnO 4溶液褪色 (3)假酒中甲醇()3CH OH 含量超标,请写出Na 和甲醇反应的化学方程式:________。
(4)劣质奶粉中蛋白质含量很低.蛋白质水解的最终产物是________。
(5)在淀粉中加入吊白块制得的粉丝有毒.淀粉最终的水解产物是葡萄糖.请设计实验证明淀粉已经完全水解,写出操作、现象和结论:____________________________。
【答案】22CCl CH = 平面型 BC 3322CH OH 2Na 2CH ONa H +→+↑ 氨基酸 取水解后溶液加入碘水,若溶液不变蓝,证明淀粉已完全水解【解析】【分析】(1)链节的主链上只有两个碳原子(无其它原子),将两半链闭合即可;乙烯为平面型分子;(2)根据结构式可分析结果;(3)Na 和甲醇反应生成甲醇钠和氢气;(4)蛋白质是氨基酸通过缩聚反应形成的高分子化合物,水解得到相应的氨基酸;(5)淀粉若完全水解,加入碘水溶液不变蓝色。
【详解】(1)链节的主链上只有两个碳原子(无其它原子),将两半链闭合即可,其单体为22CCl CH =,乙烯为平面型分子,22CCl CH =也为平面型分子,故答案为:22CCl CH =;平面型;(2)A. 由结构式可知分子式为18322C H O ,A 项错误;B.含有羧基能与甘油发生酯化反应,B 项正确;C.含有羧基能与氢氧化钠发生中和反应,C 项正确;D.含有碳碳双键能使酸性4KMnO 溶液褪色,D 项错误,故选:BC ;(3)Na 和甲醇反应生成甲醇钠和氢气,反应方程式为:3322CH OH 2Na 2CH ONa H +→+↑,故答案为:3322CH OH 2Na 2CH ONa H +→+↑;(4)蛋白质是氨基酸通过缩聚反应形成的高分子化合物,水解得到相应的氨基酸,故答案为:氨基酸;(5)淀粉若完全水解,加入碘水溶液不变蓝色,可设计方案为:取水解后溶液加入碘水,若溶液不变蓝,证明淀粉已完全水解,故答案为:取水解后溶液加入碘水,若溶液不变蓝,证明淀粉已完全水解。
化学乙醇与乙酸的专项培优练习题(含答案)含答案解析

化学乙醇与乙酸的专项培优练习题(含答案)含答案解析一、乙醇与乙酸练习题(含详细答案解析)1.食品安全关系国计民生,影响食品安全的因素很多.(1)聚偏二氯乙烯()具有超强阻隔性能,可作为保鲜食品的包装材料.它是由________(写结构简式)发生加聚反应生成的,该物质的分子构型是__________________________ 。
(2)劣质植物油中的亚油酸(]324227[CH (CH )CH CHCH CH CH CH )COOH ==含量很低,下列关于亚油酸的说法中,正确的是_________。
A .分子式为18342C H OB .一定条件下能与甘油(丙三醇)发生酯化反应C .能和NaOH 溶液反应D.不能使酸性KMnO 4溶液褪色 (3)假酒中甲醇()3CH OH 含量超标,请写出Na 和甲醇反应的化学方程式:________。
(4)劣质奶粉中蛋白质含量很低.蛋白质水解的最终产物是________。
(5)在淀粉中加入吊白块制得的粉丝有毒.淀粉最终的水解产物是葡萄糖.请设计实验证明淀粉已经完全水解,写出操作、现象和结论:____________________________。
【答案】22CCl CH = 平面型 BC 3322CH OH 2Na 2CH ONa H +→+↑ 氨基酸 取水解后溶液加入碘水,若溶液不变蓝,证明淀粉已完全水解【解析】【分析】(1)链节的主链上只有两个碳原子(无其它原子),将两半链闭合即可;乙烯为平面型分子;(2)根据结构式可分析结果;(3)Na 和甲醇反应生成甲醇钠和氢气;(4)蛋白质是氨基酸通过缩聚反应形成的高分子化合物,水解得到相应的氨基酸;(5)淀粉若完全水解,加入碘水溶液不变蓝色。
【详解】(1)链节的主链上只有两个碳原子(无其它原子),将两半链闭合即可,其单体为22CCl CH =,乙烯为平面型分子,22CCl CH =也为平面型分子,故答案为:22CCl CH =;平面型;(2)A. 由结构式可知分子式为18322C H O ,A 项错误;B.含有羧基能与甘油发生酯化反应,B 项正确;C.含有羧基能与氢氧化钠发生中和反应,C 项正确;D.含有碳碳双键能使酸性4KMnO 溶液褪色,D 项错误,故选:BC ;(3)Na 和甲醇反应生成甲醇钠和氢气,反应方程式为:3322CH OH 2Na 2CH ONa H +→+↑,故答案为:3322CH OH 2Na 2CH ONa H +→+↑;(4)蛋白质是氨基酸通过缩聚反应形成的高分子化合物,水解得到相应的氨基酸,故答案为:氨基酸;(5)淀粉若完全水解,加入碘水溶液不变蓝色,可设计方案为:取水解后溶液加入碘水,若溶液不变蓝,证明淀粉已完全水解,故答案为:取水解后溶液加入碘水,若溶液不变蓝,证明淀粉已完全水解。
【化学】化学 乙醇与乙酸的专项 培优练习题及答案

【化学】化学 乙醇与乙酸的专项 培优练习题及答案一、乙醇与乙酸练习题(含详细答案解析)1.食品安全关系国计民生,影响食品安全的因素很多.(1)聚偏二氯乙烯()具有超强阻隔性能,可作为保鲜食品的包装材料.它是由________(写结构简式)发生加聚反应生成的,该物质的分子构型是__________________________ 。
(2)劣质植物油中的亚油酸(]324227[CH (CH )CH CHCH CH CH CH )COOH ==含量很低,下列关于亚油酸的说法中,正确的是_________。
A .分子式为18342C H OB .一定条件下能与甘油(丙三醇)发生酯化反应C .能和NaOH 溶液反应D.不能使酸性KMnO 4溶液褪色 (3)假酒中甲醇()3CH OH 含量超标,请写出Na 和甲醇反应的化学方程式:________。
(4)劣质奶粉中蛋白质含量很低.蛋白质水解的最终产物是________。
(5)在淀粉中加入吊白块制得的粉丝有毒.淀粉最终的水解产物是葡萄糖.请设计实验证明淀粉已经完全水解,写出操作、现象和结论:____________________________。
【答案】22CCl CH = 平面型 BC 3322CH OH 2Na 2CH ONa H +→+↑ 氨基酸 取水解后溶液加入碘水,若溶液不变蓝,证明淀粉已完全水解【解析】【分析】(1)链节的主链上只有两个碳原子(无其它原子),将两半链闭合即可;乙烯为平面型分子;(2)根据结构式可分析结果;(3)Na 和甲醇反应生成甲醇钠和氢气;(4)蛋白质是氨基酸通过缩聚反应形成的高分子化合物,水解得到相应的氨基酸;(5)淀粉若完全水解,加入碘水溶液不变蓝色。
【详解】(1)链节的主链上只有两个碳原子(无其它原子),将两半链闭合即可,其单体为22CCl CH =,乙烯为平面型分子,22CCl CH =也为平面型分子,故答案为:22CCl CH =;平面型;(2)A. 由结构式可知分子式为18322C H O ,A 项错误;B.含有羧基能与甘油发生酯化反应,B 项正确;C.含有羧基能与氢氧化钠发生中和反应,C 项正确;D.含有碳碳双键能使酸性4KMnO 溶液褪色,D 项错误,故选:BC ;(3)Na 和甲醇反应生成甲醇钠和氢气,反应方程式为:3322CH OH 2Na 2CH ONa H +→+↑,故答案为:3322CH OH 2Na 2CH ONa H +→+↑;(4)蛋白质是氨基酸通过缩聚反应形成的高分子化合物,水解得到相应的氨基酸,故答案为:氨基酸;(5)淀粉若完全水解,加入碘水溶液不变蓝色,可设计方案为:取水解后溶液加入碘水,若溶液不变蓝,证明淀粉已完全水解,故答案为:取水解后溶液加入碘水,若溶液不变蓝,证明淀粉已完全水解。
化学乙醇与乙酸的专项培优练习题附答案解析
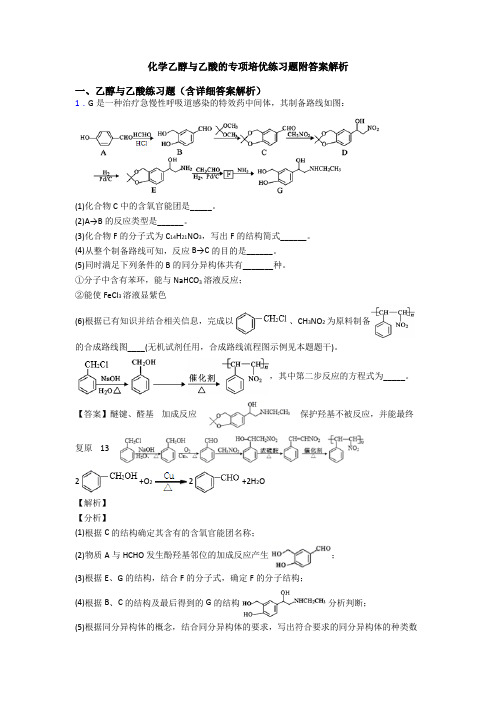
化学乙醇与乙酸的专项培优练习题附答案解析一、乙醇与乙酸练习题(含详细答案解析)1.G是一种治疗急慢性呼吸道感染的特效药中间体,其制备路线如图:(1)化合物C中的含氧官能团是_____。
(2)A→B的反应类型是______。
(3)化合物F的分子式为C14H21NO3,写出F的结构简式______。
(4)从整个制备路线可知,反应B→C的目的是______。
(5)同时满足下列条件的B的同分异构体共有_______种。
①分子中含有苯环,能与NaHCO3溶液反应;②能使FeCl3溶液显紫色(6)根据已有知识并结合相关信息,完成以、CH3NO2为原料制备的合成路线图____(无机试剂任用,合成路线流程图示例见本题题干)。
,其中第二步反应的方程式为_____。
【答案】醚键、醛基加成反应保护羟基不被反应,并能最终复原 132+O22+2H2O【解析】【分析】(1)根据C的结构确定其含有的含氧官能团名称;(2)物质A与HCHO发生酚羟基邻位的加成反应产生;(3)根据E、G的结构,结合F的分子式,确定F的分子结构;(4)根据B、C的结构及最后得到的G的结构分析判断;(5)根据同分异构体的概念,结合同分异构体的要求,写出符合要求的同分异构体的种类数目;(6)与NaOH的水溶液共热发生取代反应产生,该物质被催化氧化产生苯甲醛,苯甲醛与CH3NO2发生加成反应产生,发生消去反应产生,发生加聚反应产生;根据题意,第二步反应为苯甲醇被催化氧化产生苯甲醛。
【详解】(1)根据C的结构简式可知C中含有的含氧官能团为醛基、醚键;(2)物质A酚羟基邻位上断裂C-H键,HCHO分子中断裂C、O双键中的较活泼的键,二者发生加成反应产生,所以A→B的反应类型是加成反应;(3)物质E结构简式为,E与CH3CHO、H2在Pd/C作用下反应产生分子式C14H21NO3的F,则F的结构简式为;(4)B结构简式为,B与反应产生C:。
经一系列反应最后生成,两个官能团又复原,所以从整个制备路线可知,反应B→C的目的是保护羟基不被反应,并能最终复原;(5)B结构简式为,其同分异构体符合条件:①分子中含有苯环,能与NaHCO3溶液反应,说明分子中含有羧基-COOH;②能使FeCl3溶液显紫色,说明分子中含有酚羟基,若含有2个侧链,则为-OH、-CH2COOH,二者在苯环上的位置有邻、间、对三种;若有三个官能团,分别是-OH、-COOH、-CH3,三个官能团位置都相邻,有3种不同结构;都相间,有1种位置;若2个相邻,一个相间,有3×2=6种,因此有三个官能团的同分异构体种类数目为3+1+6=10种,则符合题意的所有同分异构体的种类数目是3+10=13种;(6)一氯甲苯与NaOH的水溶液共热发生取代反应产生,该物质与O2在Cu作催化剂条件下加热,发生氧化反应产生苯甲醛,苯甲醛与CH3NO2发生加成反应产生,发生消去反应产生,发生加聚反应产生,故反应流程为:;根据题意,第二步反应为苯甲醇被催化氧化产生苯甲醛,反应方程式为:2+O22+2H2O。
化学 乙醇与乙酸的专项 培优练习题含答案解析

化学乙醇与乙酸的专项培优练习题含答案解析一、乙醇与乙酸练习题(含详细答案解析)1.乙醇(CH3CH2OH)是一种重要的有机物(1)根据乙醇分子式和可能结构推测,1mol乙醇与足量钠反应,产生氢气的物质的量可能是________________mol。
(2)实验证明反应的乙醇与产生的氢气物质的量比值是2,该反应的化学方程式是________________________________,乙醇的官能团是_______________。
(3)用如图装置实验,干冷烧杯罩在火焰上,有无色液体产生。
能否据此说明一定有氢气产生,判断及简述理由是_________________________。
(4)乙醇与钠反应比水与钠反应平缓的多,原因是_______________________________ 。
【答案】0.5、2.5、3 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑羟基不能,因为氢气中会含有乙醇蒸汽乙醇分子中羟基上的氢原子没有水中氢原子活泼【解析】【分析】由乙醇的结构简式CH3CH2OH,可知乙醇分子内有三种不同环境下的氢原子,如果钠置换的是羟基氢原子,则1mol乙醇与足量钠反应生成0.5mol氢气,如果钠置换的是乙基上的氢原子,则1mol乙醇与足量钠反应生成2.5mol氢气,如果乙醇中的氢原子都能够被钠置换,则1mol乙醇与足量钠反应生成3mol氢气;乙醇的结构中含有官能团-羟基,能够与金属钠反应置换出氢气,且羟基中氢原子的活泼性小于水中氢原子活泼性,乙醇和钠反应与钠与水比较要缓慢的多,据以上分析解答。
【详解】(1)由乙醇的结构简式CH3CH2OH,可知乙醇分子内有三种不同环境下的氢原子,如果钠置换的是羟基氢原子,则1mol乙醇与足量钠反应生成0.5mol氢气,如果钠置换的是乙基上的氢原子,则1mol乙醇与足量钠反应生成2.5mol氢气,如果乙醇中的氢原子都能够被钠置换,则1mol乙醇与足量钠反应生成3mol氢气;(2)实验证明反应的乙醇与产生的氢气物质的量比值是2,说明钠与乙醇反应置换的是羟基上的氢原子,化学方程式为2C2H5OH+2Na→2C2H5ONa+H2↑;乙醇的官能团为羟基;(3) 图示实验装置不能说明一定有氢气产生,因为乙醇易挥发,乙醇、氢气燃烧都能生成水;(4) 乙醇分子中羟基上的氢原子没有水中氢原子活泼,乙醇与钠反应比水与钠反应平缓的多。
化学 乙醇与乙酸的专项 培优练习题及答案

化学乙醇与乙酸的专项培优练习题及答案一、乙醇与乙酸练习题(含详细答案解析)1.CMA(醋酸钙、醋酸镁固体的混合物)是高速公路的绿色融雪剂。
以生物质废液——木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)及白云石(主要成分MgCO3·CaCO3,含SiO2等杂质)等为原料生产CMA的实验流程如图:(1)步骤①发生的反应离子方程式为___________________。
(2)步骤②所得滤渣1的主要成分为____________(写化学式);步骤②所得滤液常呈褐色,颜色除与木醋液中含有少量的有色的焦油有关外,产生颜色的另一主要原因是____________。
(3)已知CMA中钙、镁的物质的量之比与出水率(与融雪效果成正比)关系如图所示,步骤④的目的除调节n(Ca)∶n(Mg)约为____________(选填:1∶2;3∶7;2∶3)外,另一目的是___________________。
(4)步骤⑥包含的操作有____________、过滤、洗涤及干燥。
(5)碳酸镁和碳酸钙与醋酸也可以恰好完全反应得到的混合物制融雪剂,下列有关说法错误的是_____A.该融雪剂中的醋酸钙、醋酸镁均是离子化合物B.该融雪剂还可用于除去煤燃烧产生的二氧化硫C.该融雪剂的水溶液显碱性D.生产该融雪剂所需碳酸盐与醋酸的物质的量之比为1:1【答案】MgCO3·CaCO3+4CH3COOH = Ca2++Mg2++4CH3COO-+2CO2↑+2H2O SiO2实验过程中苯酚被空气中氧气氧化最终产生褐色物质 3∶7 除去过量的乙酸蒸发结晶 D【解析】【分析】根据流程图可知,白云石(主要成分MgCO3•CaCO3,含SiO2等杂质)与木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)反应生成醋酸钙和醋酸镁,过滤得滤渣1为二氧化硅,滤液中主要溶质是醋酸钙和醋酸镁,加入活性炭脱色,除去被氧化的苯酚、焦油等杂质,再加入氧化镁,调节溶液中n(Ca):n(Mg)的值,过滤,除去混合液中固体杂质,得醋酸钙和醋酸镁溶液,将滤液蒸发结晶、过滤、洗涤及干燥得CMA。
【化学】化学 乙醇与乙酸的专项 培优练习题附详细答案

【化学】化学乙醇与乙酸的专项培优练习题附详细答案一、乙醇与乙酸练习题(含详细答案解析)1.乙醇(CH3CH2OH)是一种重要的有机物(1)根据乙醇分子式和可能结构推测,1mol乙醇与足量钠反应,产生氢气的物质的量可能是________________mol。
(2)实验证明反应的乙醇与产生的氢气物质的量比值是2,该反应的化学方程式是________________________________,乙醇的官能团是_______________。
(3)用如图装置实验,干冷烧杯罩在火焰上,有无色液体产生。
能否据此说明一定有氢气产生,判断及简述理由是_________________________。
(4)乙醇与钠反应比水与钠反应平缓的多,原因是_______________________________ 。
【答案】0.5、2.5、3 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑羟基不能,因为氢气中会含有乙醇蒸汽乙醇分子中羟基上的氢原子没有水中氢原子活泼【解析】【分析】由乙醇的结构简式CH3CH2OH,可知乙醇分子内有三种不同环境下的氢原子,如果钠置换的是羟基氢原子,则1mol乙醇与足量钠反应生成0.5mol氢气,如果钠置换的是乙基上的氢原子,则1mol乙醇与足量钠反应生成2.5mol氢气,如果乙醇中的氢原子都能够被钠置换,则1mol乙醇与足量钠反应生成3mol氢气;乙醇的结构中含有官能团-羟基,能够与金属钠反应置换出氢气,且羟基中氢原子的活泼性小于水中氢原子活泼性,乙醇和钠反应与钠与水比较要缓慢的多,据以上分析解答。
【详解】(1)由乙醇的结构简式CH3CH2OH,可知乙醇分子内有三种不同环境下的氢原子,如果钠置换的是羟基氢原子,则1mol乙醇与足量钠反应生成0.5mol氢气,如果钠置换的是乙基上的氢原子,则1mol乙醇与足量钠反应生成2.5mol氢气,如果乙醇中的氢原子都能够被钠置换,则1mol乙醇与足量钠反应生成3mol氢气;(2)实验证明反应的乙醇与产生的氢气物质的量比值是2,说明钠与乙醇反应置换的是羟基上的氢原子,化学方程式为2C2H5OH+2Na→2C2H5ONa+H2↑;乙醇的官能团为羟基;(3) 图示实验装置不能说明一定有氢气产生,因为乙醇易挥发,乙醇、氢气燃烧都能生成水;(4) 乙醇分子中羟基上的氢原子没有水中氢原子活泼,乙醇与钠反应比水与钠反应平缓的多。
【化学】化学乙醇与乙酸的专项培优练习题(含答案)及详细答案

【化学】化学乙醇与乙酸的专项培优练习题(含答案)及详细答案一、乙醇与乙酸练习题(含详细答案解析)1.CMA(醋酸钙、醋酸镁固体的混合物)是高速公路的绿色融雪剂。
以生物质废液——木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)及白云石(主要成分MgCO3·CaCO3,含SiO2等杂质)等为原料生产CMA的实验流程如图:(1)步骤①发生的反应离子方程式为___________________。
(2)步骤②所得滤渣1的主要成分为____________(写化学式);步骤②所得滤液常呈褐色,颜色除与木醋液中含有少量的有色的焦油有关外,产生颜色的另一主要原因是____________。
(3)已知CMA中钙、镁的物质的量之比与出水率(与融雪效果成正比)关系如图所示,步骤④的目的除调节n(Ca)∶n(Mg)约为____________(选填:1∶2;3∶7;2∶3)外,另一目的是___________________。
(4)步骤⑥包含的操作有____________、过滤、洗涤及干燥。
(5)碳酸镁和碳酸钙与醋酸也可以恰好完全反应得到的混合物制融雪剂,下列有关说法错误的是_____A.该融雪剂中的醋酸钙、醋酸镁均是离子化合物B.该融雪剂还可用于除去煤燃烧产生的二氧化硫C.该融雪剂的水溶液显碱性D.生产该融雪剂所需碳酸盐与醋酸的物质的量之比为1:1【答案】MgCO3·CaCO3+4CH3COOH = Ca2++Mg2++4CH3COO-+2CO2↑+2H2O SiO2实验过程中苯酚被空气中氧气氧化最终产生褐色物质 3∶7 除去过量的乙酸蒸发结晶 D【解析】【分析】根据流程图可知,白云石(主要成分MgCO3•CaCO3,含SiO2等杂质)与木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)反应生成醋酸钙和醋酸镁,过滤得滤渣1为二氧化硅,滤液中主要溶质是醋酸钙和醋酸镁,加入活性炭脱色,除去被氧化的苯酚、焦油等杂质,再加入氧化镁,调节溶液中n(Ca):n(Mg)的值,过滤,除去混合液中固体杂质,得醋酸钙和醋酸镁溶液,将滤液蒸发结晶、过滤、洗涤及干燥得CMA。
【化学】化学乙醇与乙酸的专项培优练习题(含答案)及答案解析

【化学】化学乙醇与乙酸的专项培优练习题(含答案)及答案解析一、乙醇与乙酸练习题(含详细答案解析)1.CMA(醋酸钙、醋酸镁固体的混合物)是高速公路的绿色融雪剂。
以生物质废液——木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)及白云石(主要成分MgCO3·CaCO3,含SiO2等杂质)等为原料生产CMA的实验流程如图:(1)步骤①发生的反应离子方程式为___________________。
(2)步骤②所得滤渣1的主要成分为____________(写化学式);步骤②所得滤液常呈褐色,颜色除与木醋液中含有少量的有色的焦油有关外,产生颜色的另一主要原因是____________。
(3)已知CMA中钙、镁的物质的量之比与出水率(与融雪效果成正比)关系如图所示,步骤④的目的除调节n(Ca)∶n(Mg)约为____________(选填:1∶2;3∶7;2∶3)外,另一目的是___________________。
(4)步骤⑥包含的操作有____________、过滤、洗涤及干燥。
(5)碳酸镁和碳酸钙与醋酸也可以恰好完全反应得到的混合物制融雪剂,下列有关说法错误的是_____A.该融雪剂中的醋酸钙、醋酸镁均是离子化合物B.该融雪剂还可用于除去煤燃烧产生的二氧化硫C.该融雪剂的水溶液显碱性D.生产该融雪剂所需碳酸盐与醋酸的物质的量之比为1:1【答案】MgCO3·CaCO3+4CH3COOH = Ca2++Mg2++4CH3COO-+2CO2↑+2H2O SiO2实验过程中苯酚被空气中氧气氧化最终产生褐色物质 3∶7 除去过量的乙酸蒸发结晶 D【解析】【分析】根据流程图可知,白云石(主要成分MgCO3•CaCO3,含SiO2等杂质)与木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)反应生成醋酸钙和醋酸镁,过滤得滤渣1为二氧化硅,滤液中主要溶质是醋酸钙和醋酸镁,加入活性炭脱色,除去被氧化的苯酚、焦油等杂质,再加入氧化镁,调节溶液中n(Ca):n(Mg)的值,过滤,除去混合液中固体杂质,得醋酸钙和醋酸镁溶液,将滤液蒸发结晶、过滤、洗涤及干燥得CMA。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学乙醇与乙酸的专项培优练习题附答案一、乙醇与乙酸练习题(含详细答案解析)1.“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室制取乙酸乙酯。
回答下列问题:(1)浓硫酸的作用是:________________________。
(2)饱和碳酸钠溶液的主要作用是__________________________________________。
(3)通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是_____。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是_________________。
(5)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是_______。
(6)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。
下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)________。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸④正反应的速率与逆反应的速率相等⑤混合物中各物质的浓度不再变化【答案】催化作用和吸水作用吸收随乙酸乙酯蒸出的乙酸和乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到防止倒吸分液防止暴沸②④⑤【解析】【分析】(1)浓硫酸具有脱水性、吸水性及强氧化性;(2)饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;(3)挥发出来的乙酸和乙醇易溶于饱和碳酸钠溶液,导管伸入液面下可能发生倒吸;(4)乙酸乙酯不溶于水;(5)根据可逆反应平衡状态标志的判断依据进行分析。
【详解】(1)乙酸与乙醇在浓硫酸作催化剂加热条件下生成乙酸乙酯,由于反应为可逆反应,同时浓硫酸吸水有利于平衡向生成乙酸乙酯的方向移动,故答案为:催化作用和吸水作用;(2)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,主要是利用了乙酸乙酯难溶于饱和碳酸钠,乙醇与水混溶,乙酸能被碳酸钠吸收,易于除去杂质,故答案为:吸收随乙酸乙酯蒸出的乙酸和乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到;(3)导管若插入溶液中,反应过程中可能发生倒吸现象,所以导管要插在饱和碳酸钠溶液的液面上,目的是防止倒吸,故答案为:防止倒吸;(4)乙酸乙酯不溶于水,则要把制得的乙酸乙酯分离出来,应采用的实验操作是分液,故答案为:分液;(5)①单位时间内生成1mol乙酸乙酯,同时生成1mol水,都表示正反应速率,不能说明到达平衡状态,故①错误;②单位时间内生成1mol乙酸乙酯,同时生成1mol乙酸,说明正逆反应速率相等,反应达到平衡状态,故②正确;③单位时间内消耗1mol乙醇,同时消耗1mol乙酸,都表示正反应速率,不能说明到达平衡状态,故③错误;④正反应的速率与逆反应的速率相等,各组分的密度不再变化,达到了平衡状态,故④正确;⑤混合物中各物质的浓度浓度不再变化,各组分的密度不再变化,达到了平衡状态,故⑤正确;故答案为:②④⑤。
2.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色粘稠液体,易溶于水。
为研究A的组成与结构,进行了如下实验:(1)称取A9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。
则A的相对分子质量为:___。
(2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g。
则A的分子式为:___。
(3)另取A9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。
用结构简式表示A中含有的官能团为:___、__。
(4)A的核磁共振氢谱如图:则A中含有___种氢原子。
(5)综上所述,A的结构简式为___,跟NaHCO3溶液反应的离子方程式为___。
【答案】90 C3H6O3—COOH —OH 4 CH3CHOHCOOH+HCO3-=CH3CHOHCOO-+H2O+CO2↑【解析】【分析】【详解】(1)有机物质的密度是相同条件下H2的45倍,所以有机物质的分子式量为:45×2=90;(2)9.0g物质A的物质的量为0.1mol;浓硫酸增重5.4g,则生成水的质量是5.4g,生成水的物质的量为:5.4g18g/mol=0.3mol,所含有氢原子的物质的量是0.6mol,碱石灰增重13.2g,所以生成二氧化碳的质量是13.2g ,所以生成二氧化碳的物质的量是:13.2g 44g/mol=0.3mol ,所以碳原子的物质的量是0.3mol ,所以有机物中碳个数是3,氢个数是6,根据相对分子质量是90,所以氧原子个数是90-312-616⨯=3,即分子式为:C 3H 6O 3; (3)只有羧基可以和碳酸氢钠发生化学反应生成二氧化碳,0.1molA 可生成2.24LCO 2(标准状况)即0.1mol 二氧化碳,则含有一个-COOH ;醇羟基和羧基可以和金属钠发生反应生成氢气,0.1molA 与足量金属钠反应生成2.24LH 2(标准状况)即0.1mol 氢气,且已知含有一个羧基,则还含有一个-OH ;(4)根据核磁共振氢谱图看出有机物中有4个峰值,则含4种环境的氢原子;(5)综上所述A 的结构简式为;与碳酸氢钠反应生成二氧化碳和水以及相应的钠盐,离子方程式为:CH 3CHOHCOOH+HCO 3-=CH 3CHOHCOO -+H 2O+CO 2↑。
3.2014年中国十大科技成果之一是:我国科学家成功实现甲烷在催化剂及无氧条件下,一步高效生产乙烯、芳烃和氢气等化学品,为天然气化工开发了一条革命性技术。
以甲烷为原料合成部分化工产品流程如下(部分反应条件已略去):(1)乙酸分子中所含官能团名称为_________________。
(2)聚苯乙烯的结构简式为__________________。
(3)图中9步反应中只有两步属于取代反应,它们是____(填序号)。
(4)写出下列反应的化学方程式(注明反应条件):反应③为________________;反应⑤为________________。
【答案】羧基 ⑤⑥ 2CH 3CH 2OH + O 2CuΔ−−→2CH 3CHO + 2H 2O CH 3COOH + CH 3CH 2OH 垐垐垐垎噲垐垐垐浓硫酸ΔCH 3COOC 2H 5+H 2O【解析】【分析】乙烯和苯发生加成反应生成乙苯,和水发生加成反应生成乙醇,乙醇发生催化氧化生成乙醛,乙醛发生氧化反应生成乙酸,乙酸和乙醇发生取代反应或酯化反应生成乙酸乙酯;乙苯发生消去反应生成苯乙烯,苯乙烯发生加聚反应生成聚苯乙烯;溴和苯发生取代反应生成溴苯;据此解答。
【详解】(1)乙酸分子中所含官能团为−COOH ,官能团名称是羧基; (2)聚苯乙烯结构简式为;(3)根据以上分析知,属于取代反应的是⑤⑥;(4)反应③为乙醇的催化氧化反应,反应方程式为2CH 3CH 2OH +O 2CuΔ−−→2CH 3CHO +2H 2O ;反应⑤为乙酸和乙醇的酯化反应或取代反应,反应方程式为CH 3COOH +CH 3CH 2OH 垐垐垐垎噲垐垐垐浓硫酸ΔCH 3COOC 2H 5+H 2O 。
【点睛】本题关键是根据反应前后结构简式的变化确定反应类型,进而判断相应的化学方程式。
4.乙烯是来自石油的重要有机化工原料。
结合路线回答:已知:2CH 3CHO+O 2→2CH 3COOH(1)D 是高分子,用来制造包装材料,则反应V 类型是____。
产物CH 2=CHCOOH 也能发生相同类型的化学反应,其化学方程式为:____(2)E 有香味,实验室用A 和C 反应来制取E①反应IV 的化学方程式是____。
②实验室制取E 时在试管里加入试剂的顺序是____(填以下字母序号)。
a .先浓硫酸再A 后Cb .先浓硫酸再C 后Ac .先A 再浓硫酸后C③实验结束之后,振荡收集有E 的试管,有无色气泡产生其主要原因是(用化学方程式表示)____(3)产物CH 2=CH-COOH 中官能团的名称为____(4)①A 是乙醇,与A 相对分子质量相等且元素种类相同的有机物的结构简式是:____、____。
②为了研究乙醇的化学性质,利用如图装置进行乙醇的催化氧化实验,并检验其产物,其中C 装置的试管中盛有无水乙醇。
(加热、固定和夹持装置已略去)(1)装置A 圆底烧瓶内的固体物质是____,C 装置的实验条件是____。
(2)实验时D 处装有铜粉,点燃D 处的酒精灯后,D 中发生的主要反应的化学方程式为____【答案】加聚反应 nCH 2=CHCOOH→3252325ΔCH COOH+C H OH H O+CH COOC H ƒ浓硫酸C233322Na CO +2CH COOH 2CH COONa+H O+CO ↑═ 碳碳双键、羧基 CH 3-O-CH 3 HCOOH 二氧化锰或MnO 2 热水浴 22523ΔO +2C H OH 2H O+2CH CHO →Cu【解析】【分析】由流程知,A 为乙醇、B 为乙醛、C 为乙酸、D 为聚乙烯、E 为乙酸乙酯,据此回答;【详解】(1)D 是聚乙烯,是一种高分子化合物,则反应V 类型是加聚反应,CH 2=CHCOOH 也能发生相同类型的化学反应,即因其含有碳碳双键而发生加聚反应,其化学方程式为:nCH 2=CHCOOH→;答案为:加聚反应;nCH 2=CHCOOH→; (2①反应IV 为乙酸和乙醇在一定条件下发生酯化反应,则化学方程式是3252325ΔCH COOH+C H OH H O+CH COOC H ƒ浓硫酸;答案为:3252325ΔCH COOH+C H OH H O+CH COOC H ƒ浓硫酸;②实验室制取乙酸乙酯时,试剂的添加顺序为乙醇、浓硫酸、乙酸,故选C ; 答案为:C ;③实验结束之后,用饱和碳酸钠收集到的乙酸乙酯内混有乙酸、乙醇,振荡后,有无色气泡产生的主要原因是乙酸和碳酸钠反应产生了二氧化碳气体,化学方程式为:233322Na CO +2CH COOH 2CH COONa+H O+CO ↑═;答案为:233322Na CO +2CH COOH 2CH COONa+H O+CO ↑═;(3)产物CH 2=CH-COOH 中官能团的名称为碳碳双键、羧基;答案为:碳碳双键、羧基;(4)①A 是乙醇,与A 相对分子质量相等且元素种类相同的有机物的结构简式是二甲醚、甲酸,则其结构简式为:CH 3-O-CH 3;HCOOH ;答案为:CH 3-O-CH 3;HCOOH ;②利用如图装置进行乙醇的催化氧化实验,并检验其产物,则其中A 装置用于产生氧气,从C 装置的试管中盛有无水乙醇,在D 装置中乙醇蒸汽和氧气的混合气在D 中发生催化氧化反应;则(1)装置A 圆底烧瓶内的固体物质是二氧化锰,C 装置的实验条件是水浴加热,便于能控制温度便于乙醇持续地挥发;答案为:二氧化锰或MnO 2;热水浴;(2)实验时D 处装有铜粉,点燃D 处的酒精灯后,D 中发生的主要反应为乙醇的催化氧化,则化学方程式为:22523ΔO +2C H OH 2H O+2CH CHO →Cu; 答案为: 22523ΔO +2C H OH 2H O+2CH CHO →Cu。
