滴定法测定棒酸发酵液中甘油含量
滴定法测定甘油的含量

滴定法测定甘油的含量(仲裁法)本方法等效采用国际标准ISO2879—1975《工业用甘油——甘油含量的测定—滴定法》4.1原理在强酸介质中,甘油被过碘酸钾冷氧化,反应产生的甲酸以PH计指示,用氢氧化钠标准溶液反应式为:CH2OH—CHOH—CH2OH+2NaIO4→HCOOH+2HCHO+2NaIO4+H2O4.2试剂分析过程中,只使用分析纯试剂4.2.1蒸馏水不含CO24.2.2乙二醇稀释溶液:1体积不含甘油的乙二醇,用1体积的水稀释。
用酚酞做指示剂中和过4.2.3硫酸(GB625):(1/2H2SO4)约0.1mol/l4.2.4甲酸钠(NaCHO2)(HG3—966):约1mol//l溶液4.2.5高碘酸钠|(NaIO4)(HG3—1157):60g//l酸性溶液4.2.5.1酸性溶液的配制称取60g(准确至0.1g)高碘酸钠,容于已加入120ml硫酸溶液的(4.2.3)的约500ml 水中,边加入边冷却,转移到1000ML容量瓶中,用水(4.2.1)稀释至刻度并混匀。
如有必要,通过玻璃过滤器过滤。
4.2.5.2溶液的酸度校核空白试验(4.4.4)所以NaOH溶液(4.2.7)的容积,应不少于4.5ml,这与基本反应(4.1)产生酸度相当4.2.5.3溶液的贮存溶液贮存在有磨口玻璃塞的棕色玻璃瓶中。
4.2.6氢氧化钠(GB629)约0.05mol/l的溶液。
4.2.7 氢氧化钠:C(NaOH)0.125mol/l的标准溶液,无二氧化碳。
4.2.8 酚酞(GB10729):5g/l乙醇溶液。
4.3 仪器普通试验室仪器4.3.1滴定管50ml4.3.2PH计:PH计应用两种缓冲溶液校准。
A 苯二钾酸氢钾(GB6857):C﹝C6H4(COOK)(COOH)﹞=0.05mol/l(10.12g/l)溶液,20℃时PH为4.0.B 四硼酸二钠十水合物(GB6856):C(Na2B4O7.10H2O)=0.01mol/l(l3.81g/l)溶液,20℃时PH为9.22.4.4试验程序二氧化碳的存在能引起误差,在放置时间,最好用表面皿盖住含有试液的容器。
甘油检验操作规程

江西欧氏药业有限责任公司GMP文件1 目的:为规范质量检验人员对甘油的检验操作,保证检验结果的准确性和可靠性,特制定本规程。
2 范围:适用于辅料甘油的检验。
3 责任人:QC人员(化验员)对实施本规程负责,QC主任(质量控制实验室负责人)负责监督检查,质量部部长负责抽查执行情况。
4 内容:4.1 检品名称及代码4.1.1 物料名称:甘油4.1.2 物料代码:F0024.2 质量标准编号:STP-ZL-02-002-00。
4.3 取样规程编号:SOP-ZL-03-017-00。
4.4 检验项目及操作方法4.4.1【性状】4.4.1.1仪器与用具:电子天平、锥形瓶4.4.1.2操作方法:4.4.1.3记录:记录观察到的辅料的行状、颜色、色泽,味道、溶解等。
4.4.1.4结果与判定:本品为无色、澄清的黏稠液体;味甜,有引湿性,水溶液(1→10)显中性反应。
本品与水或乙醇能任意混溶,在丙酮中微溶,在三氯甲烷或乙醚中均不溶。
4.4.2相对密度4.4.2.1仪器与用具:电子天平、比重瓶、干燥箱、恒温水浴锅4.4.2.2试液与试剂:纯化水名称甘油检验操作规程编号SOP-ZL-06-002-00码2/74.4.2.3操作方法:取本品,照《相对密度测定法》(编号:SOP-ZL-01-023-00)检查,4.4.2.4记录与计算:记录每次称量数据,并按下述计算公式计算相对密度:相对密度= W1-WW1-W式中:W0为比重瓶重(g);W1为供试品+比重瓶重(g);W2为水+比重瓶重(g)。
4.4.2.5结果与判定:在25℃时不小于1.2569。
4.4.3【鉴别】4.4.3.1仪器与用具:红外分光光度计等4.4.3.2试液与试剂:无水乙醇4.4.3.3操作方法:取本品,照《红外分光光度法》(编号:SOP-ZL-01-013-00)检查,4.4.3.4记录:记录供试品的红外色谱图并附图4.4.3.5结果与判定:本品的红外光吸收图谱应与对照的图谱(光谱集77图)一致。
甘油含量的测定

湖南古杉生物能源有限公司标准GS/ZYP 15甘油含量的测定1、范围1.1、本标准适用于粗甲酯中、冷凝水中、生物柴油中甘油含量的测定。
1.2、本标准规定了甘油含量的分析方法,本法仅限粗略测定。
2、引用标准2.1、AOCS E—III36(79)甘油含量的测定3、原理在酸性条件下,与甘油反应过量的高碘酸以及生成的碘酸被I—还原成I2,再用硫代硫酸钠标液滴定即可计算出甘油含量。
CH2OHCHOH + 2NaIO42H.COOH + 2NaIO3 + H2OCH2OH14H+ + 12I- + IO4- + IO3-7I2 + 7H2OI2+2S2O32- 2 I- + S4O62-4、试剂及仪器所有试剂和溶剂须采用分析纯,水也应为蒸馏水或相当纯净的水。
4.1、过碘酸钾溶液:称取过碘酸钾2.65g溶于100ml的1N的硫酸溶液中,不加热溶解后加水稀释至1000ml。
4.2、10%KI溶液:称取50克的KI溶于450毫升的蒸馏水中。
4.3、20%的盐酸溶液4.4、1%的淀粉指示剂:称取1克的淀粉指示剂,用少量的水调成糊状,加入100毫升刚煮沸的蒸馏水,搅拌均匀,静置15分钟,取上层清液。
4.5、0.1mol/LNa2S2O3标准溶液,准确标定。
4.6、分析天平:精确度为0.0001g4.7、碘量瓶:250ml4.8、移液管:25ml、50ml4.9、棕色滴定管:50ml4.10、容量瓶:500ml4.11、量筒:20ml、50ml5、操作步骤按表1规定准确称取适量(记为W)样品于500ml的容量瓶中,加水至刻度摇匀,用移液管吸取25ml的样品注入碘量瓶中,再加入50ml(用移液管吸取)的过碘酸钾溶液,轻轻摇匀后静止15分钟,如室温低于10℃时,应延长到20~25分钟。
静止后的溶液中加入10%的KI溶液20ml,20%的盐酸溶液20ml和50ml的水,用0.1 mol/LNa2S2O3的Na2S2O3标准溶液滴定至溶液为淡黄色时,加入淀粉指示剂1ml继续滴定至蓝色消失,所消耗的Na2S2O4标准溶液体积数记为V2。
甘油的检测方法汇总

甘油的检测方法汇总甘油的检测方法汇总在发酵行业中,甘油作为底物,是发酵液中生物合成的直接前体,会影响外源蛋白的启动表达效率,其含量的高低直接影响产物的发酵单位,是决定菌种取舍的重要指标,是提高工程菌的发酵密度,提高产品生产率的关键。
在生物柴油生产中,它是副产物,其含量直接影响生物柴油的使用性能,是衡量生物柴油产品品质的重要指标之一。
此外,甘油能与水结合以防止红细胞的冷冻损伤,能延长红细胞的保存期,被普遍用作细胞内冷冻保护剂等。
由于甘油用途很广,因此其含量的测定具有非常重要的意义。
目前国内外甘油含量的测定方法较多,主要有高碘酸氧化法、Cu2 +络合比色法、酶比色法法、紫外-可见分光光度法、高效液相色谱法、气相色谱法、近红外光谱法以及原子吸收法等。
下面将对其进行简要概述:一、高碘酸法二、酶比色法1.原理:它是利用酶的特异性催化反应建立的测定甘油的一种酶学方法,是指甘油在甘油激酶作用下转化为3-磷酸甘油,后者由磷酸甘油氧化酶催化生成磷酸二羟丙酮和过氧化氢,然后过氧化氢和4-氨基安普比林、4-氯酚在过氧化物酶催化下反应生成紫兰色、能在500 nm 左右有特征吸收峰的醌亚胺,通过颜色深浅即吸光度的变化测定所生成的H2O2,甘油的含量与生成的H2O2成正比,这样用比色法就可以测定甘油的含量。
2.操作步骤波长:500nm (480~520nm) 反映温度:37℃比色杯光径:1cm取一定量R1(参看R2瓶签)加入1瓶R2中,溶解后即为工作液,工作液预先保温至测试温度。
三、高效液相色谱法1.原理:高效液相色谱法( HPLC) 的原理是以液体为流动相,采用高压输液系统,将具有不同极性的单一溶剂或不同比例的混合溶剂、缓冲液等流动相泵入装有固定相的色谱柱,利用色谱柱对待测混合物先进行分离,然后再进行检测,从而实现对试样的分析,因而其测量的准确性和精确度较高,目前已成为检测生化分子较常用的一种方法。
2.操作步骤(1)首先用水将发酵液稀释2.5倍,然后加H3PO4调pH至5.5,在转速8000r/min、温度4℃下离心10min,经微孔滤膜过滤用于HPLC分析;(2)将甘油标准系列溶液在最佳色谱条件下进行HPLC分析,以峰面积外标法定量得到甘油标准曲线;(3)按照样品预处理方法处理后进样5微升,记录峰面积,代入线性方程中,计算其测定值。
003甘油检验标准操作规程

003甘油检验标准操作规程甘油检验标准操作规程1 范围本标准建立了甘油的检验标准操作规程。
本标准适用于甘油的质量控制与检验。
2 规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款,其最新版本适用于本标准。
《中华人民共和国药典》 2010版二部《甘油质量标准》编号《微生物限度检查检验标准操作规程》编号3 职责检验人员、复核人员对实施本标准负责。
4 操作规程4.1试剂与试药水、乙醇、丙酮、氯仿、标准氯化钠溶液、稀硝酸、硝酸银试液、氢氧化钠滴定液(0.1mol/L)、10%氢氧化钾溶液、比色用重铬酸钾液、标准硫酸钾溶液、酚酞指示液、盐酸滴定液(0.1mol/L)、比色用氯化钴液、比色用重铬酸钾溶液、硫酸、标准铁溶液、稀盐酸、30%硫氰酸铵溶液、正丁醇、醋酸盐缓冲液(pH3.5)、硫代乙酰胺试液、硫化钠试液4.2设备与仪器比重瓶、烧杯、温度计、纳氏比色管、坩埚、试管、水浴锅、高温电阻炉、碱式滴定管、铁架台、三角锥形瓶、天平、恒温培养箱、干燥器。
4.3 检验项目4.3.1性状4.3.1.1操作方法(1)取本品,在明亮光线下,用目测和口尝法检测;(2)引湿性取本品,加水成水溶液(1?10),观察是否显中性反应(3)取本品,分别用水、乙醇、氯仿、乙醚溶解,观察其溶解情况。
(4)相对密度取本品,在25?时依法操作(《中国药典》2010版二部附录? A 比重瓶法)。
a、取洁净、干燥并精密称定重量的比重瓶,装满供试品(温度应低于20?或各品种项下规定的温度)后,装上温度计(瓶中应无气泡),置20?的水浴中放置若干分钟,使内容物的温度20?,用滤纸除去溢出侧管的液体,立即盖上罩。
然后将比重瓶自水浴中取出,再用滤纸将比重瓶外面擦干净,精密称定,减去比重瓶的重量,求得供试品的重量后,将供试品倒出,洗净比重瓶,装满新沸过的冷水,再照上法测得同一温度时水的重量,按下式计算记得。
b、取洁净、干燥并精密称定重量的比重瓶,装满供试品(温度应低于20?或各品种项下规定的温度)后,插入中心有毛细孔的瓶塞,用滤纸将从塞孔中溢出的液体擦干,置20?恒温水浴中,放置数分钟,随着供试液温度上升,多余的液体将不断从塞孔溢出,随时用滤纸将瓶塞顶端擦干,待液体不再由塞孔溢出,迅速将比重瓶自水浴中取出,照上述a法,自“再用滤纸将比重瓶的外面擦净”起,依法测定,即得。
HPLC检测发酵液中二羟基丙酮和甘油的含量_谢光蓉

HPLC 检测发酵液中二羟基丙酮和甘油的含量
谢光蓉
(中国药科大学生命科学与技术学院,江苏南京 210009)
摘 要:应用高效液相色谱法检测发酵过程中发酵产物二羟基丙酮和底物甘油浓度。在流动相乙腈、纯净水的比例为
72
2013 年第 4 期
4.840 4.836
线性关系良好; 甘油在 0.1-1.0mg/
1
mL 范围内线性关系良好。
1
3.3 DHA 和甘 油 HPLC 检 测 方 法
的精密度
同一日内分别检测 6 次,DHA
检 测 峰 面 积 积 分 值 的 RSD 为
0.38%, 甘油检测峰面积积分值的
RSD 为 0.83% , 结 果 显 示 , 日 内 精
的生成和底物甘油的残留, 以便于对转化过程进行 控制,并根据底物甘油的残留量判断发酵终点。已报 道的 DHA 检测方法有气相色谱法[7],二苯胺法[8]和 薄 层 色 谱 法 [9],这 三 种 方 法 由 于 操 作 复 杂 、 线 性 范 围 窄或者定量准确度差等原因, 难以应用于光 蓉 (1973-),女 ,博 士 生 ,高 级 工 程 师 。研 究 方 向 :药 物 蛋 白 质 工 程 。
密度符合检测要求。
3.529 3.3.568863
4.077 5.329
7.517 7.939
3.4 DHA 和甘 油 HPLC 检 测 方 法
的特异性
3.4.1 不 同 碳 源 和 氮 源 的 培 养 基
3.995 4.117
成分对检测的影响
将含不同碳源和不同氮源配
甘油含量测定方法

资料范本本资料为word版本,可以直接编辑和打印,感谢您的下载甘油含量测定方法地点:__________________时间:__________________说明:本资料适用于约定双方经过谈判,协商而共同承认,共同遵守的责任与义务,仅供参考,文档可直接下载或修改,不需要的部分可直接删除,使用时请详细阅读内容甘油含量的测定实验原理:采用高碘酸氧化还原法仪器及药品:仪器:容量瓶、碘量瓶、锥形瓶药品:NaIO4;KI;H2SO4;淀粉指示剂1.0%淀粉指示液:称取1.0g可溶性淀粉,加10mL水,在搅拌下再注入到90mL水中,微沸2min,放置,取上层清液使用。
试验均要用新配制1.0%的淀粉指示剂。
标准溶液:1. 氢氧化钠:0.5N、0.1N、0.01N(常用)用基准苯二甲酸氢钾标定。
2. 硫代硫酸钠:配制:0.1N称取26克硫代硫酸钠(或16克无水硫代硫酸钠),溶于1000毫升水中,缓缓煮沸10分钟,冷却,放置两周后过滤备用。
(常用)标定:称取0.15克(精确到0.0002克)于120℃烘至恒重的基准重铬酸钾,置于碘量瓶中,溶于25毫升水,加2克碘化钾及20毫升4mol/L的硫酸(3mol/L 25ml),摇匀。
于暗处放置10分钟。
加75毫升水,用0.1N硫代硫酸钠溶液滴定,近终点时加1毫升0.5%淀粉指示剂,继续滴定至溶液由蓝色变为亮绿色。
同时做空白实验。
N=G/0.04903(V1-V2)式中:G——重铬酸钾之重量,克V1——硫代硫酸钠之用量,毫升V2——空白硫代硫酸钠之用量,毫升0.04903——每毫克当量重铬酸钾之克数实验步骤:试样处理精确称取大豆油10.00g(精确到小数点后二位),反应完后,将分层液下层甘油相转入500ml 容量瓶中,并用适量水洗涤上层甲酯层,水相也转入容量瓶中,最后定容,待用。
甘油含量测定准确量取10ml上述甘油溶液,放入250ml碘量瓶中,再加入20ml0.04mol/L NaIO4溶液、10ml 0.6mol/L H2SO4溶液、5ml正己烷,盖好塞盖,摇匀,在室温下于暗处放置 30 min。
甘油转化生产1_3_丙二醇发酵液中甘油含量的测定

甘油转化生产1 ,3 - 丙二醇发酵液中甘油含量的测定王剑锋1 , 修志龙2 , 范圣第1(1 .大连民族学院化工系, 大连116600 ; 2 .大连理工大学生物工程系, 大连116012 )摘要对文献介绍滴定法测定甘油的方法进行了改进,使之能够用于1 ,3 - 丙二醇发酵液中甘油含量测定。
实验表明,化学滴定法测定结果具有较好的准确性和重复性,与酶法和变色酸比色法相比,测定结果接近,化学滴定法测定发酵液中甘油含量是一个较为经济简便的方法。
关键词: 甘油; 1 ,3 - 丙二醇; 发酵液; 含量测定1 ,3 - 丙二醇可作为新型聚酯材料———聚对苯二甲酸丙二酯(简称P T T) ———的单体,较之其它二醇(如乙二醇、1 ,4 - 丁二醇) 形成的聚酯,如聚对苯二甲酸乙二酯( 简称P E T) 、聚对苯二甲酸丁二酯( PB T) , P T T 具有更加独特的性质, 如尼龙样的弹性恢复、在全色范围内无需添加特殊化学品即能呈现良好的连续印染特性、良好的着色性、抗紫外、抗静电、良好的生物降解性1 ,2 。
P T T 这些优良的性质越来越受到关注,因此1 ,3 - 丙二醇的生产也受到了重视。
微生物发酵法生产 1 , 3 - 丙二醇以“绿色化学”为特征,利用可再生资源、生产清洁、对环境友好,符合21 世纪可持续发展需要,因而越来越受到重视。
甘油可以作为底物发酵生产1 , 3- 丙二醇, 发酵液中甘油含量是研究发酵法生产1 ,3 - 丙二醇的重要参数,因此甘油含量测定是非常重要的。
对于发酵液中甘油含量的测定有过报道 3 ,文中对高效液相色谱法、高碘酸氧化比色法、Cu2 + 络合比色法、酶试剂盒法进行了比较。
由于酶试剂的高度专一性,很少受发酵液中所含杂质的影响,因此酶法检测具有较高的准确度4 ,5 , 而其它方法都存在较大的测量误差。
但酶法需要昂贵的试剂,不利于工业应用和大量样品的检测,为此本文将在以往分析方法的基础上加以改进, 寻求一种分析成本低、操作简便、测定结果较为准确的分析方法,以满足科研和生产实际需要。
甘油含量检测方法

甘油含量检测方法
检测甘油含量?这可不是一件难事!咱就来唠唠甘油含量检测方法。
先说说步骤吧!嘿,你想想,就像大厨做菜要有步骤一样,检测甘油含量也有一套流程。
首先,得准备好样品,这就好比要烹饪一道美食,得先有食材不是?然后,选择合适的检测方法,比如色谱法啥的。
接着,进行实验操作,仔细观察数据变化。
哇塞,这过程就像一场神秘的探险,充满了未知和惊喜!
那注意事项呢?哎呀呀,这可不能马虎。
样品的处理要得当,不然结果可就不靠谱啦!实验过程中要严格按照操作规程来,可不能想当然地乱搞。
就像开车得遵守交通规则,检测甘油含量也得守规矩。
安全性和稳定性咋样呢?放心吧!只要操作正确,那是相当安全稳定的。
这就好比走在平坦的大路上,不用担心突然出现大坑。
检测过程中不会有啥危险情况发生,而且结果也比较稳定可靠。
应用场景可多啦!在化妆品行业,得检测甘油含量,确保产品质量。
在医药领域,也少不了对甘油的检测。
这就像一把万能钥匙,可以打开很多领域的大门。
优势也很明显啊,检测方法准确、快速,能为生产和研究提供有力的支持。
来个实际案例咋样?有个化妆品公司,通过检测甘油含量,优化了产品配方,提高了产品质量。
哇,这效果简直杠杠的!就像给汽车加了好油,跑得更快更稳。
咱检测甘油含量的方法就是这么厉害!操作简单,安全稳定,应用广泛,优势明显。
还等啥?赶紧试试吧!。
滴定法测试甘油含量实验方案

滴定法测试甘油纯度实验方案1.实验目的用酚酞作为指示剂,用NaOH滴定,通过计算得到甘油的含量。
2.实验原理用NaIO4氧化甘油,一分子的甘油产生一分子的甲酸,过量的乙二醇溶液除去过量的甲酸,用NaOH滴定甲酸的含量,计算得到甘油的含量。
CH2OH-CH2OH-CH2OH + 2NaIO4——HCOOH + 2HCHO + H20HCOOH + NaOH——H2O + NaCOOH3.实验药品与实验设备实验药品:去离子水(实验前煮沸10min以上除去CO2)乙二醇(1体积乙二醇加入一体积去离子水)硫酸(0.1mol/L,浓硫酸配制)甲酸钠(1mol/L)高碘酸钠(60g/L的0.1 mol/L的硫酸溶液)NaOH(0.05mol/L,0.125mol/L)酚酞5g/L实验仪器:pH计、碱式滴定管、磁力搅拌器、分析天平、容量瓶、烧杯、量筒、移液管、表面皿。
4.实验步骤1)称取0.5g左右的甘油样品,置于500ml的烧杯中,加入蒸馏水至250ml左右,搅拌均匀,加入0.05mol/L的NaOH溶液调节pH至7.9±0.1。
2)准确加入50ml的NaIO4溶液盖上表面皿,在暗处静置30min。
3)加入10ml的50%的乙二醇溶液,在暗处静置20min。
4)加入5ml的1mol/L甲酸钠溶液,加入两滴酚酞溶液,随后用0.125mol/L的NaOH溶液滴定至终点pH为7.9±0.2。
NaOH用量为V1,所加入的甘油质量为m。
5)用50ml的水代替样品做空白试验,加入高碘酸钠前滴定调节PH到6.5,滴定终点pH为6.5。
NaOH用量为V2.5.计算甘油含量X=(9.21*0.125*(V1- V2))/m%6.注意事项1)分析试验注意称量准确2)溶液试剂注意是否过期,溶液是否澄清。
3)提前预判滴定终点,保证滴定终点的准确性。
4)pH计使用前用标准溶液校准。
甘油含量检测方法

甘油含量检测方法1、原理由于甘油是醇类物质,而酸性高碘酸盐氧化糖醇产生甲醛,在Nash试剂参与下生成黄色的化合物,该化合物在412nm下有最大吸收峰。
根据吸光值即可计算出甘油的浓度。
2、试剂①Nash试剂:精确称取15g乙酸铵,蒸馏水溶解,加入0.2ml冰醋酸,0.2ml乙酰丙酮,定容至100ml。
现用现配。
②0.015mol/L高碘酸钠溶液:精确称取高碘酸钠3.2g,用0.12mol/LHCl溶液溶解宾并定容至1000ml。
③0.1%L-鼠李糖:精确称取L-鼠李糖0.5g,溶于蒸馏水中,定容至500ml。
④0.5mg/ml甘油标准溶液:称取甘油0.5g(精确至0.0001g),加水定容至100ml。
摇匀,吸取5ml稀释至50ml,即浓度为0.5mg/ml的甘油标准溶液。
⑤0.12mol/L HCl溶液:量取浓盐酸(12mol/L)20ml,加水定容至2000ml。
3、仪器和设备①漩涡混合器②752分光光度计③恒温水浴锅4、标准曲线绘制①.吸取0.5mg/ml甘油标准溶液各0.5mL、1.0mL、2.0mL、3.0mL、4.0mL,分别定容至50mL。
即配制好0.005mg/ml、0.01mg/ml、0.02mg/ml、0.03mg/ml、0.04mg/ml 的不同浓度的甘油标准液。
②吸取上述各浓度甘油标准液1ml分别置于刻度试管中,然后加入1ml 0.015mol/L的高碘酸钠溶液,混匀,室温放置10min。
然后,加入2ml 0.1%L-鼠李糖溶液,(以除去过多的髙碘酸盐),混匀后加入4ml新鲜配制的Nash试剂,在53℃水浴中加热15min,使其充分显色。
③以空白做参比,在412nm波长下测定其吸光度。
④以甘油浓度(mg/L)为横坐标,OD412为纵坐标绘制标准曲线。
注:空白:用水代替甘油标准稀释液,其余操作同上。
每组样品做2个平行。
15、检测步骤:①称取一定量的甘油样品作适当浓度的稀释。
②吸取1ml稀释液置于刻度试管中,然后加入1ml 0.015mol/L的高碘酸钠溶液,混匀,室温放置10min。
甘油的检测方法汇总

甘油的检测方法汇总在发酵行业中,甘油作为底物,是发酵液中生物合成的直接前体,会影响外源蛋白的启动表达效率,其含量的高低直接影响产物的发酵单位,是决定菌种取舍的重要指标,是提高工程菌的发酵密度,提高产品生产率的关键。
在生物柴油生产中,它是副产物,其含量直接影响生物柴油的使用性能,是衡量生物柴油产品品质的重要指标之一。
此外,甘油能与水结合以防止红细胞的冷冻损伤,能延长红细胞的保存期,被普遍用作细胞内冷冻保护剂等。
由于甘油用途很广,因此其含量的测定具有非常重要的意义。
目前国内外甘油含量的测定方法较多,主要有高碘酸氧化法、Cu2 +络合比色法、酶比色法法、紫外-可见分光光度法、高效液相色谱法、气相色谱法、近红外光谱法以及原子吸收法等。
下面将对其进行简要概述:1、 高碘酸法1.原理:高碘酸氧化法是目前常见用于甘油含量检测的方法,利用高碘酸与甘油发生氧化还原反应,剩余高碘酸及反应生成的碘酸与碘化钾反应生成碘,再用硫代硫酸钠进行滴定,根据消耗的硫代硫酸钠的量来计算甘油的含量。
2.操作步骤准确发酵液10ml于100mL小烧杯中,加少量水溶解,然后转移至100mL容量瓶中,用水稀释至标线,摇匀,静置。
用移液管准确移取10mL上述溶液于碘量瓶中,加入20mL高碘酸钠溶液,混合均匀后,于黑暗中避光静置40min,然后加入碘化钾溶液和20%盐酸溶液各15mL,调节pH值在0.8~1.0之间,然后用硫代硫酸钠标准溶液滴定,近终点时,加入2mL淀粉指示剂溶液,继续滴定至溶液蓝色消失。
同时做试样空白。
3.计算:式中:w——样品中甘油的含量,%;V1——空白试样消耗硫代硫酸钠标准溶液的体积,mL;V2——试样消耗硫代硫酸钠标准溶液的体积,mL;C——硫代硫酸钠标准溶液的浓度,mol/L;M——甘油相对分子质量;2、 酶比色法1.原理:它是利用酶的特异性催化反应建立的测定甘油的一种酶学方法,是指甘油在甘油激酶作用下转化为3-磷酸甘油,后者由磷酸甘油氧化酶催化生成磷酸二羟丙酮和过氧化氢,然后过氧化氢和4-氨基安普比林、4-氯酚在过氧化物酶催化下反应生成紫兰色、能在500 nm 左右有特征吸收峰的醌亚胺,通过颜色深浅即吸光度的变化测定所生成的H2O2,甘油的含量与生成的H2O2成正比,这样用比色法就可以测定甘油的含量。
甘油含量的测定方法国标

甘油含量的测定方法国标【实用版4篇】目录(篇1)1.引言2.甘油含量测定方法的原理3.甘油含量测定方法的实验步骤4.甘油含量测定方法的注意事项5.结语正文(篇1)1.引言甘油是一种重要的化工原料,广泛应用于制药、化妆品、食品等领域。
因此,准确测定甘油含量具有重要的实用价值。
我国国家标准 GB/T 24318-2009《甘油含量的测定方法》规定了测定甘油含量的方法。
2.甘油含量测定方法的原理甘油含量的测定方法基于甘油与硫代硫酸钠反应的原理。
在酸性条件下,甘油与硫代硫酸钠反应生成硫代硫酸甘油酯,同时放出硫化氢。
硫化氢与重铬酸钾反应,产生颜色变化,通过比色定量法测定甘油含量。
3.甘油含量测定方法的实验步骤(1)试样处理:精确称取大豆油 10.00g(精确到小数点后二位),反应完后,将分层液下层甘油相转入 500ml 容量瓶中,并用适量水洗涤上层甲酯层,水相也转入容量瓶中,最后定容,待用。
(2)甘油含量测定:准确量取 10.00mL 试样溶液,加入 5.00mL 硫代硫酸钠溶液,混匀后,加入 1.00mL 重铬酸钾溶液,混匀,静置 30 分钟。
用比色皿取上层清液,以空白硫代硫酸钠溶液为对照,用光电比色计测定吸光度,计算甘油含量。
4.甘油含量测定方法的注意事项(1)试样处理时要保证精确度和准确性,避免试样损失和污染。
(2)在测定过程中,应保持实验环境稳定,避免光线、温度等对实验结果的影响。
(3)比色皿和光电比色计要保持清洁,避免杂质对测量结果的干扰。
5.结语甘油含量的测定方法国标为我国甘油产业的发展提供了重要的技术支持。
目录(篇2)1.甘油含量测定方法的背景和重要性2.国标中甘油含量测定的方法3.甘油含量测定的实验步骤4.甘油含量测定的注意事项5.甘油含量测定方法的优缺点正文(篇2)甘油是一种重要的化工原料,广泛应用于制药、化妆品、食品等行业。
因此,准确测定甘油含量具有重要的意义。
在我国,甘油含量的测定方法有国标规定,以下将为您详细介绍。
滴定法测定棒酸发酵液中甘油含量

第27卷第3期河北工业科技V ol.27,No.32010年5月H ebei Jour nal of Industr ial Science and T echno log yM ay 2010文章编号:1008 1534(2010)03 0189 03滴定法测定棒酸发酵液中甘油含量康 辉,刘桂军,孙凤卿,赵 霞(石药集团河北中润制药有限公司,河北石家庄 050041)摘 要:为了消除发酵液中还原糖的影响,建立了高碘酸钠滴定法测定棒酸发酵液中甘油含量的方法,该方法的回收率为98.5%,RSD 值为1.69%。
本法操作简便,成本低廉,适用于发酵液中甘油含量的测定。
关键词:棒酸发酵液;滴定法;甘油;含量中图分类号:T Q460.7 文献标志码:ADetermination of glycerol content in clavulanicacid fermentation broth by titrationKANG H ui,LIU Gui jun,SU N Feng qing,ZH AO Xia(Hebei Zhong run P har maceutical Company L imited,Shijiazhuang Phar maceutical Gr oup,Shijiazhuang Hebei 050041,China)Abstract:T he met ho d fo r the deter minatio n o f glycero l co ntent in the clavulanic acid ferment ation bro th by so dium per iodatetitr ation is established so as to eliminate the infect ion of reducing sug ar in the bro th.T he averag e recover y r ate is 98.5%,and RSD is 1.69%.T he method is convenient and accurate with low cost.It can be applied t o the deter minatio n of g lycer ol content in the fer mentat ion broth.Key words:clavulanic acid fermentatio n bro th;titration;g ly cer ol;content 收稿日期:2010 01 14;修回日期:2010 03 16责任编辑:张士莹基金项目:国家 十一五 科技支撑计划项目(20007BAI26B00)作者简介:康 辉(1975 ),女,河北石家庄人,工程师,主要从事抗生素研发方面的工作。
甘油含量检测方法

甘油含量检测方法甘油含量是指在其中一种样品中甘油所占的百分比或者质量百分比。
甘油(C3H8O3)是一种无色、无味的有机化合物,被广泛应用于食品、药品、化妆品和烟草等工业中。
一、物理方法物理方法是通过测量样品的特定物理性质来确定甘油含量。
1.折射率法:甘油的折射率与其浓度呈线性关系,所以可以通过测量甘油溶液的折射率来确定甘油的含量。
这种方法需要使用折射仪进行测量,适用于透明溶液或液体。
2.密度法:甘油溶液的密度与其浓度呈线性关系,可以通过测量甘油溶液的密度来确定甘油含量。
这种方法需要使用密度计进行测量,适用于透明溶液或液体。
3.蒸汽压法:甘油的蒸汽压与其浓度呈线性关系,可以通过测量甘油溶液的蒸汽压来确定甘油含量。
这种方法需要使用蒸汽压计进行测量,适用于透明溶液或液体。
二、化学方法化学方法是通过甘油与其中一种化学试剂反应产生可测定的物质或产生其中一种特定的化学性质来确定甘油含量。
1.酶法:甘油酶可以将甘油与辅酶NAD+反应生成甘油醛和还原的NADH,可以通过测量NADH的吸收光谱来确定甘油的含量。
2.磺酸法:甘油与冰醋酸反应生成二甘醇酯,该反应可以通过测量其产物的溶解度或者离子电导率来确定甘油的含量。
3.水合反应法:甘油与氧化亚铜反应生成水合甘油铜离子,可以通过测定其溶解度或者电导率来确定甘油含量。
4.碱滴定法:甘油可以与强碱滴定生成甘油醚,可以通过滴定法来测定甘油的含量。
以上只是常见的甘油含量检测方法,具体选择何种方法还要根据样品的性质和实际需要进行裁定。
另外,随着科学技术的不断发展,新的检测方法也在不断涌现,有望提高检测的准确性和效率。
酶法测定发酵液中甘油含量方法的研究

酶法测定发酵液中甘油含量方法的研究方法一:酒石酸酶法测定发酵液中甘油含量酶法是一种常用的测定甘油含量的方法,它通过酒石酸酶催化甘油生成对应产物,通过检测产物的数量来确定甘油的含量。
下面是一个用酒石酸酶法测定发酵液中甘油含量的步骤。
1.拟定标准曲线:首先准备一系列标准溶液,浓度范围覆盖待测样品的含量范围。
可以通过称取甘油精确配制出不同浓度的标准溶液,也可以购买商用标准溶液。
将每个标准溶液分别加入试管或反应瓶中。
2.加入酒石酸酶:将一定量的酒石酸酶溶液加入每个试管或反应瓶中,混匀后放置在适宜的环境中进行恒温反应。
3.反应终止:在一定的反应时间后,加入适当的反应终止剂,如盐酸、硫酸等,将反应停止。
4.添加试剂:为了产生显色反应,可以添加相应的试剂,如3,5-二硝基水杨酸、间苯二胺等。
5.测定吸光值:将反应溶液转移至比色皿或比色管中,用紫外-可见分光光度计测定吸光值。
根据标准溶液的吸光值绘制标准曲线。
6.测定待测样品:取一定量待测样品,重复上述步骤,得到吸光值。
7.计算甘油含量:根据待测样品吸光值在标准曲线上的位置,利用标准曲线的拟合方程计算出甘油的含量。
此方法的优点是测定条件简单,对样品无特殊要求,测定结果准确可靠。
但是,酒石酸酶法测定的甘油含量仅仅是通过酶催化来确定含量,不能直接测定甘油含量的绝对值。
方法二:酒精脱水法测定发酵液中甘油含量酒精脱水法是一种常用的测定发酵液中甘油含量的方法,它通过将发酵液与酒精进行混合,使甘油与酒精形成共沸体而被脱水,在测定前后甘油的脱水程度来确定其含量。
下面是一个用酒精脱水法测定发酵液中甘油含量的步骤。
1.选择合适的酒精:选择一种纯度较高的酒精,一般使用无水乙醇。
确保酒精的纯度可以满足脱水的要求。
2.预处理样品:将待测样品进行预处理,通常可以通过蒸馏或其他方法去除杂质。
3.混合样品和酒精:将一定量的待测样品和酒精按一定比例混合,如1:1、混合后,对混合液进行搅拌,使其充分接触。
氢氧化钠滴定法测定甘油制剂中甘油的含量

氢氧化钠滴定法测定甘油制剂中甘油的含量
陈芳
【期刊名称】《海峡药学》
【年(卷),期】2009(021)010
【摘要】目的优化洲定甘油制剂中甘油含量的方法.方法采用氢氧化钠滴定法,高碘酸钠定量氧化甘油成甲酸,再用氢氧化钠滴定甲酸,以酚酞作指示剂.结果重复性试验良好,加样回收率高,总加样回收率达到100.53%.结论此方法操作简单,准确,重现性好,可用于测定甘油制剂中甘油含量.
【总页数】2页(P76-77)
【作者】陈芳
【作者单位】浙江省绍兴市越城区绍兴第二医院中药房,绍兴,312000
【正文语种】中文
【中图分类】R927.2
【相关文献】
1.滴定法测定棒酸发酵液中甘油含量 [J], 康辉;刘桂军;孙凤卿;赵霞
2.电位滴定法测定开塞露中甘油含量 [J], 边巴卓玛;尼珍;普普赤;阿萍
3.离子色谱法测定甘油磷酸制剂中的β-甘油磷酸根和L-苹果酸根 [J], 刘玉秀;喻宏伟
4.微量滴定法测定生物医用材料分离油中甘油的含量 [J], 宋春香;吕玉光;石春卉;阎红
5.置换滴定法测定甘油护肤水的甘油含量 [J], 蔡俊;陶欣艺
因版权原因,仅展示原文概要,查看原文内容请购买。
甘油的测定
(B-T)×N×0.02302×100 B = 空白滴定所消耗的体积(ml)
甘油% =
T = 样品滴定所消耗的体积(ml)
W
N = 硫代硫酸钠的浓度(mol/L)
W = 样品的重量(g)
结果保留小数点后面二位
甘油的测定
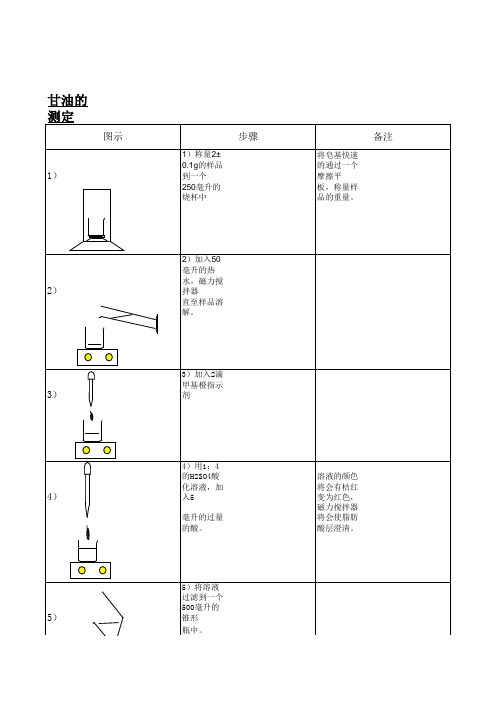
图示 1)
2)
3)
步骤
1)称量2±0.1g的样品到一个 250毫升的烧杯中
备注
将皂基快速的通过一个摩擦平 板,称量样品的重量。
2)加入50毫升的热水,磁力搅拌器 直至样品溶解。
3)加入2滴甲基橙指示剂
4)
4)用1:4的H2SO4酸化溶液,加入5 溶液的颜色将会有桔红变为红色,
毫升的过量的酸。
10) 11)
盖上盖子,摇匀,并在暗橱中保存30 分钟。
移取10毫升10%的KI溶液
12) 13) 14)
加入110毫升的蒸馏水
去除瓶塞,准备加入蒸馏水和滴定 实验
用0.1N的硫代硫酸钠滴定,颜色变为 加水后15分钟内,开始滴定。在滴定
浅黄色
开始前将溶液从暗处拿出。
移取2毫升的指示剂溶液
15)
图示
磁力搅拌器将会使脂肪酸层澄清。
5)
5)将溶液过滤到一个500毫升的锥形
瓶中。
6)
6)用10毫升的热水洗涤带有脂肪酸的
烧杯,重复3次。
7)
7)加入2滴甲基橙指示剂。
图示 8)
9)
步骤
如果溶液是酸性的,用50%的NaOH 溶液中性溶液。
备注
溶液显示轻微的碱性,颜色由粉红 变为桔红色.
移取50毫升的高碘酸
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第27卷第3期河北工业科技V ol.27,No.32010年5月H ebei Jour nal of Industr ial Science and T echno log yM ay 2010文章编号:1008 1534(2010)03 0189 03滴定法测定棒酸发酵液中甘油含量康 辉,刘桂军,孙凤卿,赵 霞(石药集团河北中润制药有限公司,河北石家庄 050041)摘 要:为了消除发酵液中还原糖的影响,建立了高碘酸钠滴定法测定棒酸发酵液中甘油含量的方法,该方法的回收率为98.5%,RSD 值为1.69%。
本法操作简便,成本低廉,适用于发酵液中甘油含量的测定。
关键词:棒酸发酵液;滴定法;甘油;含量中图分类号:T Q460.7 文献标志码:ADetermination of glycerol content in clavulanicacid fermentation broth by titrationKANG H ui,LIU Gui jun,SU N Feng qing,ZH AO Xia(Hebei Zhong run P har maceutical Company L imited,Shijiazhuang Phar maceutical Gr oup,Shijiazhuang Hebei 050041,China)Abstract:T he met ho d fo r the deter minatio n o f glycero l co ntent in the clavulanic acid ferment ation bro th by so dium per iodatetitr ation is established so as to eliminate the infect ion of reducing sug ar in the bro th.T he averag e recover y r ate is 98.5%,and RSD is 1.69%.T he method is convenient and accurate with low cost.It can be applied t o the deter minatio n of g lycer ol content in the fer mentat ion broth.Key words:clavulanic acid fermentatio n bro th;titration;g ly cer ol;content 收稿日期:2010 01 14;修回日期:2010 03 16责任编辑:张士莹基金项目:国家 十一五 科技支撑计划项目(20007BAI26B00)作者简介:康 辉(1975 ),女,河北石家庄人,工程师,主要从事抗生素研发方面的工作。
棒酸是由棒状链霉菌代谢产生的一种 内酰胺酶抑制剂,与 内酰胺类抗生素连用对产生 内酰胺酶的耐药菌有抑制作用,因具有抑制 内酰胺酶的作用,所以棒酸具有可观的医用及经济价值,其年产值可达几十亿元。
由于其具有广泛的药理学特性,所以临床需求量不断增加,棒酸原料药的需求量也在不断增加。
甘油是棒酸生物合成的直接前体,其在发酵过程中的浓度直接影响棒酸的发酵单位。
因此,开发适用于工业化生产的棒酸时,发酵液中甘油的检测分析方法是保证高发酵单位的关键。
精确分析甘油含量的方法有高碘酸氧化法、分光光度法[1]、原子吸收法、气相色谱法、近红外光谱法、高效液相色谱法[2]和甘油激酶法[3]等。
但在微生物培养基和代谢产物成分十分复杂的发酵液中,由于含有其他多羟基醇类的类似产物,故影响了甘油的测定结果,而国际上用来测定发酵液中甘油含量的试剂盒方法价格昂贵,成本较高,故不适合发酵生产过程中对甘油含量的监控。
笔者参照!中国药典∀(2005版)中甘油含量的测定方法[4],根据棒酸发酵液的特性,建立了一种快速、简便、准确测定发酵液中甘油含量的方法,并验证了其检测的精确性。
1 方 法1.1 原理甘油与高碘酸钠发生反应生成酸,剩余的高碘酸钠用乙二醇中和,最后由氢氧化钠滴定生成酸。
由于发酵液中的单糖也和高碘酸钠发生反应生成酸,所以应检测单糖的量,计算其消耗的氢氧化钠的量,再经计算得出甘油消耗的氢氧化钠的量,继而计算得出甘油的含量(全文指质量浓度)。
1.2 试剂配制2.14%(质量分数,下同)高碘酸钠溶液:称取21.4g高碘酸钠,加入978.6g水中,溶解即可;乙二醇(体积分数为50%):将500mL乙二醇加入500mL水中,摇匀即可。
1.3 操作过程1.3.1 还原糖对甘油含量的影响准确称取2.15g葡萄糖,用水定容至100mL 的容量瓶中。
取5mL至碘量瓶中,加入45mL的水,加入25mL质量分数为2.14%的高碘酸钠溶液,摇匀,加盖,于暗处放置15min。
再加入5mL 的乙二醇(体积分数为50%),暗处放置20m in。
然后加入0.5m L酚酞指示剂,用0.1mo l/L的氢氧化钠滴定至溶液由无色变为粉红色,消耗的氢氧化钠的体积为10.159mL。
1m L质量分数为2.15%的单糖消耗氢氧化钠的体积为10.159/5= 2.0318mL;同时进行平行试验,取质量分数为2.15%的葡萄糖溶液1m L,如上操作,消耗氢氧化钠的体积为2.0230mL。
由以上结果可得,1mL质量分数为2.15%的单糖消耗氢氧化钠的体积为(2.0318+2.0230)/2=2.0274mL。
1.3.2 多糖对甘油的影响取淀粉2.0g,加水定容至100m L的容量瓶中,分别取5m L和2mL至碘量瓶中,加入45mL 的水,加入25m L质量分数为2.14%的高碘酸钠溶液,摇匀,加盖,暗处放置15min。
再加入5m L的乙二醇,暗处放置20min。
然后加入0.5m L酚酞指示剂,用0.1mol/L的氢氧化钠滴定至溶液由无色变为粉红色,消耗的氢氧化钠的体积分别为0.1320mL和0.0640mL,计算1mL质量分数为2.0%的多糖消耗的氢氧化钠的体积分别是0.0264 (0.1320/5)mL和0.0320(0.0640/2)mL,平均值为(0.0264+0.0320)/2=0.0292m L。
以上试验表明:多糖消耗氢氧化钠的体积很小,可忽略不计。
1.3.3 棒酸发酵液中甘油含量的测定1)反应原理C3H8O3+2N aIO4=H COOH+2H CH O+ 2NaIO3+H2O,H COOH+N aOH=H COONa+H2O。
2)测定方法精密量取棒酸发酵液(滤液或者上清液)5.0mL 于碘量瓶中,加入45mL的水,精密加入25mL的高碘酸钠溶液,摇匀,加盖,暗处放置15min。
再加入5mL乙二醇溶液,暗处放置20min。
加入酚酞指示剂8~10滴,用0.1m ol/L的标准氢氧化钠溶液滴定至溶液的颜色由无色变为粉红色,消耗的氢氧化钠的体积为V0,同时测定棒酸发酵液中还原糖[2]的含量W(质量浓度),计算出还原糖消耗的氢氧化钠的体积:V1=W#2.0274#5/2.15,甘油消耗的氢氧化钠的体积为V0-V1。
甘油的质量浓度=(V0 V1)#M#9.210.1#5.0。
式中:V0为发酵液消耗的氢氧化钠的体积, m L;V1为还原糖消耗的氢氧化钠的体积,m L;M为氢氧化钠标准滴定液的实际浓度,mo l/L;9.21为1mL氢氧化钠(0.1m ol/L)相当于9.21mg的甘油;5.0为发酵液的取样体积,mL。
2 方法学验证2.1 加样回收率试验称取分析纯甘油1.05g,用棒酸甘油空白发酵液(各种配料均相同,不加甘油)定容至100m L,配成甘油质量浓度为10.5m g/m L的发酵液,用上述方法进行测定,6次测定结果见表1,其中还原糖质量浓度为0.564g/mL;氢氧化钠浓度为0.09831 mol/L;还原糖消耗的氢氧化钠的体积V1=0.564# 2.0274#5.0/2.15∃2.66mL。
表1结果表明该方法的回收率良好。
表1 加样回收率试验结果T ab.1 Recover y r ate result项 目指 标试验次数/次123456 V0/mL8.458.408.458.308.358.35质量浓度/(mg%mL-1)10.5210.3910.5210.0410.3010.30回收率/%100.1098.95100.1095.6298.1098.10平均回收率/%98.50RSD值/% 1.692.2 与甘油酶试剂盒方法检测结果对照试验在2008010批次试发酵试验中,取连续中控发酵液样品,同时用甘油酶试剂盒方法(方法1)与高碘酸钠滴定法(方法2)测定甘油含量,并对照2种方法测定结果,见表2,甘油含量趋势图见图1,甘油酶试剂盒法与高碘酸钠滴定法测定结果对应关系见图2。
190河 北 工 业 科 技 第27卷表2 方法对照结果T ab.2 M ethods co mpar ison result mg%mL-1发酵周期/h7111723293135394347515559方法1 5.39 3.9922.9817.369.91 5.61 1.83 6.58 3.16 1.74 1.72 1.170.82方法2 5.45 4.1120.7015.639.18 5.52 1.85 6.42 2.74 2.54 1.77 1.21 1.10发酵周期/h63677175798387919599103107方法1 1.21 1.300.88 3.95 6.51 6.27 5.25 4.33 3.27 2.65 1.88 1.35方法2 1.160.650.58 3.89 5.11 4.85 3.97 3.45 3.08 2.84 2.01 1.88从表1和图1、图2可见,用2种方法检测甘油的含量(质量浓度),在整个发酵周期结果相差不大,趋势相同,表明用滴定法控制甘油含量可行。
以甘油酶试剂盒法所测定的甘油质量浓度X为横坐标,以高碘酸钠滴定法测定的甘油质量浓度Y为纵坐标,进行线性回归,得到回归方程为Y=0.8875X+ 0.1682,其相关性系数为0.9950。
由于滴定法较甘油酶试剂盒法特异性偏低,因此测定结果略有偏差,但该方法适用于棒酸发酵液中甘油含量的测定,可应用于大规模生产棒酸时发酵液中甘油的分析检测。
2.3 重复性试验取2008010批次75h发酵液样品,以上述方法测定甘油含量,重复测定6次,结果见表3,其中还原糖质量浓度为0.42g/mL,氢氧化钠浓度为0.09831mo l/L,还原糖消耗的氢氧化钠的体积约为2.66mL。
表3结果表明该方法重复性良好。
表3 重复性试验结果T ab.3 Repeatability r esult项 目指 标试验次数/次123456 V0/mL 4.13 4.20 4.25 4.15 4.25 4.10质量浓度/(mg%mL-1)3.89 3.71 3.80 3.62 3.80 3.53质量浓度平均值/(mg%mL-1)3.73RSD值/% 3.563 讨 论1)相对于!中国药典∀测定甘油含量方法,本方法解决了发酵液中存在的单糖被高碘酸钠氧化生成酸,对测量结果产生影响的问题。
