类风湿因子(RF)测定试剂盒(胶乳凝集法)
类风湿因子(RF)检测试剂盒(胶体金法)产品技术要求lanshizi

类风湿因子(RF)检测试剂盒(胶体金法)
适用范围:可定性检测人血清/血浆/全血样本中的类风湿因子,用于类风湿性关节炎的临床辅助诊断。
1.1 条型:单人份/袋;25人份/筒
1.2 板型:单支/袋,10支/袋
1.3 主要组成成分
试剂系由人变性IgG和抗人IgG分别固相于硝酸纤维膜,并与胶体金标记的人变性IgG(固相)制成。
稀释液成分:磷酸盐缓冲液(PBS)0.01 mol/L,pH 7.4。
2.1 物理性状
2.1.1 外观:试纸条整洁完整、无毛刺、无破损、无污染,标签应清晰。
2.1.2 条宽:试纸条宽度应≥2.5 mm。
2.1.3 液体移行速度:液体移速度应≥10 mm/min。
2.2 最低检测限
最低检测限应不高于25 IU/ml。
2.3 特异性
2.3.1 与高胆红素样本的交叉反应:检测含有高胆红素(TBil≤200 μmol/L)的样本,结果应为阴性。
2.3.2 与高脂样本的交叉反应:检测含有高脂(TG≤20 mmol/L)的样本,结果应为阴性。
2.4 重复性
用25 IU/ml的RF重复性参考品平行检测10人份,其反应结果应一致。
2.5 稳定性试验
4℃~30℃条件下放置24个月后两个月内的试纸进行检测,产品的物理性能、最低检测限、特异性和重复性应符合2.1、2.2、2.3和2.4的要求。
2.6 批间差
取3个批号的试纸条,对重复性进行检测,要求反应结果均为阳性,且显色度均一。
类风湿因子(RF)测定试剂盒(胶乳免疫比浊法)产品技术要求shangjing

类风湿因子(RF)测定试剂盒(胶乳免疫比浊法)适用范围:用于体外定量测定人血清中类风湿因子的含量1.1 包装规格试剂1:1×80mL,试剂2:1×20mL;试剂1:50×240μL,试剂2:1×3mL;试剂1:30×240μL,试剂2:1×1.8mL。
1.2 主要组成成分2.1 外观和性状试剂1为清澈透明的液体,无沉淀、悬浮物和絮状物。
试剂2为乳白色悬浮液,无沉淀。
2.2 净含量每瓶试剂的净含量应不少于标示值。
2.3 试剂空白吸光度用纯化水加入试剂作为样品测试时,试剂空白吸光度A应≤1.60。
2.4 分析灵敏度测含已知浓度的类风湿因子(RF)样本时,吸光度差值(ΔA)应≥0.10。
2.5 线性试剂盒在[3,160]IU/mL的线性范围内分析性能应符合如下要求:2.5.1 线性相关系数(r)≥0.990;2.5.2 相对偏差:浓度在(10,160]IU/mL范围内,相对偏差不超过8%;2.5.3 绝对偏差:浓度在[3,10]IU/mL范围内,绝对偏差不超过0.8IU/mL。
2.6 测量精密度2.6.1 重复性用高低两个浓度样本重复测试,所得结果的变异系数(CV)应≤8.0%。
2.6.2 批间差试剂盒的批间相对极差(R)应≤10.0%。
2.7 准确度与已上市产品比对,线性回归方程的相关系数(r)≥0.975,各个浓度点中≤10IU/mL的绝对偏差不超过±0.8IU/mL,各个浓度点中>10IU/mL的相对偏差不超过±10%。
2.8 稳定性2℃~8℃避光贮存,有效期为12个月,取过有效期后一个月内的试剂盒进行检测,试剂盒应仍能符合2.1、2.3、2.4、2.5、2.6.1、2.7要求。
上海捷门生物技术有限公司RF检测试剂盒说明书

上海捷门生物技术有限公司RF检测试剂盒说明书
类风湿因子(RF)科研检测试剂盒组成结构:
1、血清:操作过程中避免任何细胞刺激。
使用不含热原和内毒素的试管。
收集血液后,1000×g离心10分钟将血红细胞迅速小心地分离。
2、血浆:EDTA、柠檬酸盐、肝素血浆可用于检测。
1000×g离心30分钟去除颗粒。
3、细胞上清液:1000×g离心10分钟去除颗粒和聚合物。
4、组织匀浆:将组织加入适量生理盐水捣碎。
1000×g离心10分钟,取上清液。
5、类风湿因子(RF)科研检测试剂盒保存:如果样品不立即使用,应将其分成小部分-70℃保存,避免反复冷冻。
尽可能的不要使用溶血或高血脂血。
如果血清中大量颗粒,检测前先离心或过滤。
不要在37℃或更高的温度加热解冻。
应在室温下解冻并确保样品均匀地充分解冻。
类风湿因子(RF)科研检测试剂盒注意事项
1. 当混合蛋白溶液时应尽量轻缓,避免起泡。
2. 洗涤过程非常重要,不充分的洗涤易造成假阳性。
3. 一次加样时间X好控制在5分钟内,如标本数量多,推荐使用排枪加样。
4. 请每次测定的同时做标准曲线,X好做复孔。
5. 如标本中待测物质含量过高,请先稀释后再测定,计算时请
X后乘以稀释倍数。
6. 在配制标准品、检测溶液工作液时,请以相应的稀释液配制,不能混淆。
7. 底物请避光保存。
8. 不要用其它生产厂家的试剂替换试剂盒中的试剂。
艾威德 类风湿因子(RF)测定试剂盒(胶乳免疫比浊法)说明书

类风湿因子(RF)测定试剂盒(胶乳免疫比浊法)说明书【产品名称】类风湿因子(RF)测定试剂盒(胶乳免疫比浊法)【包装规格】a)试剂1:1×20mL试剂2:1×5mLb)试剂1:2×40mL试剂2:1×20mLc)试剂1:4×60mL试剂2:2×30mLd)试剂1:2×80mL试剂2:2×20mL【预期用途】用于体外定量测定人血清中类风湿因子的含量。
类风湿因子的检测可以作为类风湿性关节炎的诊断依据,也可作为病情进展的指标。
另外有助于诊断系统性红斑狼疮、慢性肝炎等。
测定类风湿因子常用于类风湿性关节炎的辅助诊断依据[1]。
【检验原理】类风湿因子是和人IgG的Fc片段起免疫反应。
用人IgG包被胶乳微粒和样本中RF发生免疫反应,引起微粒凝聚,致使浊度增加,其增加的程度与RF的含量成正相关。
【主要组成成分】试剂1主要组分三羟甲基氨基甲烷缓冲液18.5mmol/L 聚乙二醇(PEG)4% ProClin300适量试剂2主要组分三羟甲基氨基甲烷缓冲液18.5mmol/L 抗原致敏胶乳类风湿因子(RF)抗体适量ProClin300适量注:不同批号试剂盒中各组分未经试验不可互换。
【储存条件及有效期】1.试剂原包装在2~8℃储存,有效期为12个月,生产日期、有效期见标签。
2.开口后的试剂在仪器仓中(2~8℃)可稳定30天。
【适用仪器】艾威德AS-420/AS-660/AS-1200;日立HITACHI7020型/7060型/7180型/7600型/LABOSPECT008AS型;贝克曼AU400/AU480/AU640/AU680/ AU2700/AU5400/AU5800/AU5811/AU5821;佳能TBA-FX8/TBA-120FR/ TBA-2000FR;罗氏cobas8000c702/cobas8000c701/cobas8000c502;西门子SIEMENS ADVIA1800/ADVIA2400;雅培ABBOTT ARCHITECT c8000/ARCHITECT c16000/ARCHITECT ci8200;西森美康SYSMEX BM6010/C;科华KHB卓越310/卓越330/卓越400/卓越450/ZY-1200/ ZY-1280;迪瑞CS-240/CS-T300/CS-300B/CS-380/CS-400A/CS-400B/ CS-600A/CS-600B/CS-800A/CS-800B/CS-1200/CS-1200ISE/CS-1300B/ CS-1400;迈瑞MINDRAY BS-220/BS-330/BS-350E/BS-380/BS-390/ BS-400/BS-430/BS-600/BS-800/BS-2000M;颐兰贝ES-200/ES-380/ES-480;赛诺迈德SUNMATIK-9050型;雷杜Chemray420;英诺华D280;特康TC6010L;锦瑞GS400;普康6066。
类风湿因子测定试剂盒(胶乳免疫比浊法)产品技术要求jiuqiang

类风湿因子测定试剂盒(胶乳免疫比浊法)适用范围:用于体外定量测定人血清中类风湿因子的含量。
1.1 包装规格表1 包装规格试剂1:3×20mL、试剂2:1×20mL试剂1:1×60mL、试剂2:1×20mL试剂1:8×3.8mL、试剂2:4×2.6mL试剂1:2×15mL、试剂2:1×10mL试剂1:6×50mL、试剂2:2×50mL试剂1:12×4.2mL、试剂2:6×2.9mL试剂1:1×45mL、试剂2:1×15mL试剂1:1×15mL、试剂2:1×5mL320测试/盒(试剂1:3×20mL、试剂2:1×20mL)400测试/盒(试剂1:3×20mL、试剂2:1×20mL)480测试/盒(试剂1:3×20mL、试剂2:1×20mL)校准品(液体,4水平或5水平):4×1mL;5×1mL;5×2mL质控品(液体,水平1):1×3mL;1×1mL质控品(液体,水平2):1×3mL;1×1mL1.2 主要组成成分表2 主要组成成分试剂成分浓度试剂1:氨基乙酸缓冲液0.17mol/L试剂2:乳胶颗粒超敏化的变性IgG悬浮液0.17%(w/v)校准品(液体):人血清基质类风湿因子≥10%4水平:水平1:0~20 IU/mL水平2:20~60 IU/mL 水平3:50~100 IU/mL 水平4:100~140 IU/mL5水平:水平1:0~15 IU/mL 水平2:15~30 IU/mL 水平3:30~60 IU/mL 水平4:60~100 IU/mL 水平5:100~140 IU/mL质控品(液体):人血清基质类风湿因子≥10%水平1: 10~30 IU/mL 水平2: 25~50 IU/mL试剂中含有防腐剂。
类风湿因子测定试剂盒(胶乳免疫透射比浊法)产品技术要求新产业
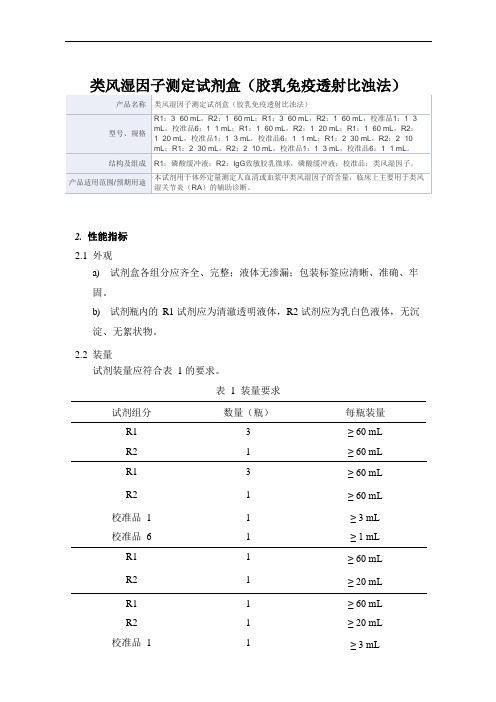
类风湿因子测定试剂盒(胶乳免疫透射比浊法)2.性能指标2.1外观a)试剂盒各组分应齐全、完整;液体无渗漏;包装标签应清晰、准确、牢固。
b)试剂瓶内的R1 试剂应为清澈透明液体,R2 试剂应为乳白色液体,无沉淀、无絮状物。
2.2装量试剂装量应符合表 1 的要求。
表 1 装量要求试剂组分数量(瓶)每瓶装量R1 3 ≥ 60 mLR2 1 ≥ 60 mLR1 3 ≥ 60 mLR2 1 ≥ 60 mL 校准品 1 1 ≥ 3 mL校准品 6 1 ≥ 1 mLR1 1 ≥ 60 mLR2 1 ≥ 20 mLR1 1 ≥ 60 mLR2 1 ≥ 20 mL 校准品 1 1 ≥ 3 mL校准品 6 1 ≥ 1 mL R1 2 ≥ 30 mL R2 2 ≥ 10 mL试剂组分数量(瓶)每瓶装量R1 2 ≥ 30 mLR2 2 ≥ 10 mL 校准品 1 1 ≥ 3 mL校准品 6 1 ≥ 1 mL2.3空白限应≤4.00 IU/mL。
2.4检出限试剂盒检出限不高于 6.00 IU/mL。
2.5线性区间试剂盒线性在[10.00,140.00] IU/mL 区间内,应符合如下要求:a)线性相关系数(r)≥0.990;b)[10.00,14.00] IU/mL 区间内,线性绝对偏差在±1.40 IU/mL 范围内;(14.00,140.00] IU/mL 区间内,线性相对偏差在±10%范围内。
2.6精密度2.6.1重复性试剂盒测试浓度在(15.00±3.00)IU/mL 和(50.00±10.00)IU/mL 范围内的样本时,变异系数(CV)≤10.0%。
2.6.2批间差试剂盒测试浓度在(15.00±3.00)IU/mL 和(50.00±10.00)IU/mL 范围内的样本时,相对极差(R)≤10.0%。
2.7准确度可选用以下方法之一进行验证:a)测试公认参考物质,相对偏差在±10%范围内。
类风湿因子测定试剂盒(胶乳免疫比浊法)产品技术要求zhongshengbeikong

类风湿因子测定试剂盒(胶乳免疫比浊法)适用范围:本试剂用于体外定量测定人血清中类风湿因子的浓度。
1.1包装规格液体双剂型试剂1(R1):60mL×2,试剂2(R2):20mL×2;试剂1(R1):60mL×1,试剂2(R2):20mL×1;试剂1(R1):45mL×1,试剂2(R2):15mL×1;试剂1(R1):75mL×1,试剂2(R2):25mL×1。
1.2主要组成成分1.2.1 试剂1(R1)(液体)甘氨酸100mmol/L 1.2.2 试剂2(R2)(液体)包被变性IgG抗体的胶乳颗粒2mg/mL2.1 外观试剂盒中各组件的外观应满足:2.1.1 试剂1(R1)应为无色或淡黄色透明溶液,无杂质、无絮状物,外包装完整无破损;2.1.2 试剂2(R2)应为乳白色乳浊溶液,无杂质、无絮状物,外包装完整无破损。
2.2 净含量液体试剂净含量应不少于标示值。
2.3 试剂空白吸光度在波长570nm(540nm~600nm)处(光径1cm),试剂空白吸光度(A)应≤1.000。
2.4 准确度测定WHO W1066,相对偏差应不超过±15%。
2.5 分析灵敏度对应于浓度为20 IU/mL 的RF所引起的吸光度差值(△A)的绝对值应在0.010~0.030的范围内。
2.6 重复性重复测定高、低浓度样本,变异系数(CV)应≤ 10%。
2.7 批间差重复测定同一样本,批间差(R)应≤ 10%。
2.8 线性范围在[5,120]IU/mL范围内,线性相关系数(r)应≥0.990,在(20 ,120] IU/mL范围内,线性相对偏差应不超过±10%,在[5,20] IU/mL范围内,线性绝对偏差应不超过±2IU/mL。
2.9 稳定性原包装的试剂盒在2℃~8℃避光贮存,有效期为12个月。
试剂有效期满后3个月以内,试剂性能应符合2.1、2.3、2.4、2.5、2.6、2.8的要求。
类风湿因子(RF)检测试剂盒(胶体金法)产品技术要求lanshizi

类风湿因子(RF)检测试剂盒(胶体金法)
适用范围:可定性检测人血清/血浆/全血样本中的类风湿因子,用于类风湿性关节炎的临床辅助诊断。
1.1 条型:单人份/袋;25人份/筒
1.2 板型:单支/袋,10支/袋
1.3 主要组成成分
试剂系由人变性IgG和抗人IgG分别固相于硝酸纤维膜,并与胶体金标记的人变性IgG(固相)制成。
稀释液成分:磷酸盐缓冲液(PBS)0.01 mol/L,pH 7.4。
2.1 物理性状
2.1.1 外观:试纸条整洁完整、无毛刺、无破损、无污染,标签应清晰。
2.1.2 条宽:试纸条宽度应≥2.5 mm。
2.1.3 液体移行速度:液体移速度应≥10 mm/min。
2.2 最低检测限
最低检测限应不高于25 IU/ml。
2.3 特异性
2.3.1 与高胆红素样本的交叉反应:检测含有高胆红素(TBil≤200 μmol/L)的样本,结果应为阴性。
2.3.2 与高脂样本的交叉反应:检测含有高脂(TG≤20 mmol/L)的样本,结果应为阴性。
2.4 重复性
用25 IU/ml的RF重复性参考品平行检测10人份,其反应结果应一致。
2.5 稳定性试验
4℃~30℃条件下放置24个月后两个月内的试纸进行检测,产品的物理性能、最低检测限、特异性和重复性应符合2.1、2.2、2.3和2.4的要求。
2.6 批间差
取3个批号的试纸条,对重复性进行检测,要求反应结果均为阳性,且显色度均一。
类风湿因子测定试剂盒(胶乳免疫比浊法)产品技术要求shouyi

类风湿因子测定试剂盒(胶乳免疫比浊法)
适用范围:本试剂盒用于体外定量测定人血清中的类风湿因子的含量。
1.1产品型号/规格
1.2产品组成
试剂1:PBS 100mmol/L,PEG 4%。
试剂2:变性IgG 10mg/mL,NaN
0.1%,吐温-20 0.2%。
3
2.1 外观
试剂1为无色透明溶液;试剂2为稍有混浊的透明液体;试剂盒各组分齐全、完整,液体无渗漏,包装标签文字符号清晰牢固不易脱落,外包装完整无破损。
2.2 装量
液体试剂的净含量应不少于标示值。
2.3 试剂空白吸光度
在600nm波长、1cm光径条件下,试剂空白吸光度应不大于0.70。
2.4 分析灵敏度
测定30IU/mL类风湿因子时,吸光度变化在0.0198~0.0786范围内。
2.5准确度
采用比对试验,相关系数r2≥0.95,相对偏差应不超过±10%。
2.6 精密度
2.6.1 重复性
用血清样品或质控样品重复测试所得的变异系数(CV)应不大于8.0%。
2.6.2 批间差
试剂(盒)批间相对极差应不大于10.0%。
2.7线性区间
试剂线性在[15,80]IU/mL区间内:
a) 线性相关系数|r|应不小于0.990;
b) [15,80]IU/mL区间内,线性相对偏差应不超过±10%。
2.8稳定性
原包装试剂2~8℃避光保存有效期12个月,到效期末进行检验,检验结果应符合2.3、2.5、2.7的要求。
类风湿因子RF测定

类风湿因子RF测定1检验目的指导本室工作人员规范操作本检测项目,确保检测结果的准确。
2原理RF是针对自身的变性IgG分子结晶片段的一种自身抗体。
本试剂将人微球蛋白胶合于胶乳微粒,与待测样本中的RF 发生免疫反应,引起微粒的凝集,导致反应体系浊度增加,该浊度的高低在一定量抗体存在时与抗原的含量成正比。
与通过同样处理的标准液比较,即可计算出样本中的RF。
3标本要求3.1使用新鲜血清,不使用血浆.3.2在采集血液后2h分离血清.3.38h内不能及时测定血清可存放于2-80C冰箱保存,3天后测定的血清置-150C―-200C 冰冻保存,但冰冻血清只能复融一次.3.4严重溶血或脂血的标本不能作测定.4试剂4.1试剂:本科使用浙江伊利康生物技术限公司的试剂盒. (浙食药监械(准)字2014第2400384号YZB/浙2314-40-2014)4.1.1试剂盒组成如下:R1三羟甲基氨基缓冲液:20mmol/L叠氮钠:0.95g/LR2:类风湿因子致敏胶乳液:适量叠氮钠:0.95g/L4.1.2 试剂准备:试剂为即用式。
4.1.3 试剂稳定性与贮存:在2~8℃避光、密封的储存条件下,试剂盒自生产之日起有效期为12个月。
4.1.4 变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。
4.1.5 注意事项:试剂中含有稳定剂,可能存在一定的刺激作用和毒性,请勿直接接触皮肤及眼睛。
一旦接触,即用大量清水冲洗。
请勿吞服。
4.2 校准品:使用浙江伊利康生物技术限公司提供的RF校准品对自动分析仪进行校准。
4.3 质控品:使用正常值、病理值复合控制品。
5 仪器AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪6 操作步骤6.1 样品的准备:将标好号的样品离心后放到仪器规定的位置。
6.2 试剂的检测:仪器开机后,检查各种试剂的位置,体积等确认无误后方可进行测定。
类风湿因子(RF)测定(胶乳凝集法)作业指导书

类风湿因子(RF)测定(胶乳凝集法)作业指导书1.原理RF是一种主要发生于类风湿性关节炎患者体内的抗人变性IgG抗体,可与IgG的Fc段结合。
将变性IgG包被于聚乙苯烯胶乳颗粒上,此致敏胶乳在与待测血清中的RF相遇时,即发生肉眼可见的凝集。
2.标本采集2.1 采集前病人准备:受检者应空腹2.2 标本种类:血清2.3 标本要求:采集病人静脉血2ml,室温放置不超过4小时,分离血清备用。
3.标本储存:2-8°C保存不应超过24小时,-20°C不应超过3个月,-70°C长期保存,应避免反复冻融。
4.标本运输:密封,室温运输。
5.标本拒收标准:污染、标本量不足、脂血或严重溶血标本不宜作此项检测。
6.试剂6.1 试剂名称:类风湿因子测定试剂6.2 试剂生产厂家:西班牙BioSystems S.A.6.3 包装规格:60Test/Kit6.4 试剂盒组成:RF胶乳悬液,阳性对照血清,阴性对照血清。
6.5 试剂储存条件及有效期:2-8°C避光保存,有效期6个月。
7.操作步骤7.1 平衡:将试剂盒各组分取出,平衡至室温(18-25°C)。
7.2 分别吸取50μl阳性对照和阴性对照血清均匀铺加在纸卡的两个圆圈中。
7.3 吸取50μl待测血清均匀铺加在纸卡的另一圆圈中。
7.4 加胶乳试剂50μl于上述血清中。
7.5 处分混匀后立即摇动反应板,2分钟内于直射阳光下观察。
8.结果判断:出现明显凝集者为阳性。
9.质量控制:每次测定均做阴阳对照,阴性对照不出现凝集物,阳性对照出现明显凝集。
10. 参考范围:阴性11. 临床意义:RF是一种以变性IgG为靶抗原的自身抗体。
RF阳性常见于类风湿关节炎患者和自身免疫性疾病患者。
少数健康人也会出现阳性结果。
12. 操作性能:灵敏度、特异性高。
13. 方法局限性:检测出的RF主要为IgM类。
14. 注意事项14.1试剂的使用:在大于10°C室温条件下进行;使用前必需充分混匀。
风湿三项检测试剂盒-产品介绍

2020年1月21日星期二
9
(3) 超敏C反应蛋白hs-CRP
超敏C反应蛋白的临床指导作用主要表现在对心血 管疾病,新生儿细菌感染,肾移植等方面。
浓度过大时提示:心肌梗死,缺血卒中危险度,外周 动脉血管性疾病危险度大幅增加。
2020年1月21日星期二
10
风湿三项——常规检测方法
酶联免疫吸附法 胶乳凝集比浊法
机体多种细胞有毒性作用,具有很强的抗原性。 机体被链球菌感染后可产生抗链球菌溶血素O抗体; 检测ASO有助于诊断由溶血性链球菌引起的疾病; 类风湿、急性肾小球疾病、猩红热和扁桃体炎等疾病。
2020年1月21日星期二
7
临床意义
ASO测定诊断A族链球菌感染
ASO测定对于诊断A族链球菌感染很有价值,其存在
2020年1月21日星期二
20
谢谢关注!!
2020年1月21日星期二
21
2020年1月21日星期二
5
类风湿因子(RF)临床意义
其他疾病
自身免疫性疾病诊断: 系统性红斑狼疮、进行性全身性硬化症等的阳性率可达
28.9%~50%。 血管炎、肝病、慢性感染等也可出现RF阳性。
2020年1月21日星期二
6
(2)抗链球菌溶血素O
抗链球菌溶血素O:(ASO)又称抗“O” 是A组链球菌的因子(RF)临床意义
类风湿性关节炎(RA)
美国风湿病学会1987年类风湿性关节炎诊断标准之一1; 70%-90%类风湿性关节炎,RF阳性; 早期诊断:高滴度支持对RA的早期诊断2 ; RA的临床监测;RF的滴度与患者的临床表现呈正相关;
1、2010年中国类风湿关节炎诊疗指南解读[J].浙江医学,2011.11.(30) 2、分析抗CCP、RF、CRP和ASO在类风湿关节炎诊断中的应用价值. 《中国卫生产业》 2013年第10卷第2期 67-68页.
类风湿因子测定试剂盒(胶乳免疫比浊法)产品技术要求haomai

类风湿因子测定试剂盒(胶乳免疫比浊法)适用范围:本试剂适用于体外定量测定人血清中类风湿因子(RF)的含量。
1.1包装规格序号规格序号规格1 试剂1:1×40ml;试剂2:1×10ml。
2 试剂1:2×40ml;试剂2:2×10ml。
3 试剂1:5×16ml;试剂2:5×4ml。
4 试剂1:4L;试剂2:1L。
1.2主要组成成分本试剂由试剂1(R1)和试剂2(R2)组成试剂1(R1):氯化铵缓冲液100mmol/L氯化钠0.95g/L试剂2(R2):Tris缓冲液100mmol/L包被有IgG的胶乳颗粒悬液0.17w/v%2.1 外观试剂盒外观应整洁,文字符号标识清晰;R1为无色液体,R2为白色颗粒悬浊液体。
液体试剂不得有沉淀和絮状物。
2.2 装量试剂瓶内液体装量应不少于标示值。
2.3 空白吸光度以生理盐水为样品,在37℃、660nm波长、1cm光径条件下,吸光度≤1.4。
2.4 分析灵敏度浓度为44IU/ml的样本,吸光度差值△A>0.04。
2.5 准确性回收试验,回收率在90%~110%范围内。
2.6 重复性用不同浓度的两个样本进行检测,各重复检测10次,其批内变异系数(CV)应不超过10%。
2.7 线性2.7.1在(2,160)IU/ml范围内,线性相关系数r应不低于0.990;2.7.2 在(2,16]IU/ml范围内绝对偏差不超过±1.6IU/ml;(16,160)IU/ml范围内相对偏差不超过±10%。
2.8 批间差用三个批号的试剂盒测定同一份样本,试剂盒批间相对极差应不超过15%。
2.9 稳定性试剂盒在2~8℃避光保存,可稳定12个月。
取到效期后的样品检测试剂空白吸光度、分析灵敏度、准确度、重复性、线性范围应分别符合2.3、2.4、2.5、2.6、2.7的要求。
类风湿因子(RF)定量测定试剂盒标准操作程序

类风湿因子(RF)定量测定标准操作程序1.摘要本试剂盒适用于体外临床检验,用于测定人血清中类风湿因子的浓度。
RF的测定对类风湿性关节炎的诊断有一定的参考价值。
2.适用范围程序适用于日立7600自动生化分析仪检测血清、血浆中RF的浓度。
3.职责使用日立7600自动生化分析仪进行测定RF浓度的工作人员要严格按照本SOP程序进行,室负责人监督管理;本SOP的改动,可由任一使用本SOP的工作人员提出,并报经生化室负责人、科主任签字批准生效。
4.检测方法上海科华生物生产的类风湿因子定量测定试剂盒采用的是免疫透射比浊法。
5.原理试剂中的人IgG包被于聚苯乙烯粒子上,样本中RF与试剂中包被于聚苯乙烯粒子上的人IgG结合,形成不溶性免疫复合物,该免疫复合物由于包被的聚苯乙烯粒子而使浊度进一步放大,在人IgG足量的情况下,其浊度与人血清中RF含量成正比,与相同条件下操作的校准品比较,通过剂量/反应曲线求出样品中RF的含量。
6.仪器日立7600自动生化分析仪7.试剂7.1试剂来源:上海科华生物工程股份有限公司提供7.2试剂瓶内主要成分:MOPSO缓冲液(PH7.4)、0.2M、NaN3、包被人IgG的聚苯乙烯粒子7.3试剂稳定性:试剂避光保存于2-8℃,若无污染,可稳定至失效期,本试剂有效期为12个月。
试剂不可冰冻。
R1、R2:打开后冷藏于分析仪中可稳定28天。
7.4试剂准备:试剂为即用式。
8.标准品和质量控制8.1校准程序:使用上海科华生物工程股份有限公司试剂盒内提供的标准品对自动分析仪进行校准。
由a、b、c、d四只组成,浓度见说明书。
按照公司标准品使用要求,使用前用0.5ml的生理盐水复溶,待完全混合均匀后(约30分钟)再使用。
校准后,仪器自动对校准品吸光度通过合适的数学模型绘制校准曲线。
8.2质控品使用某某公司提供的生化复合定值质控血清做为室内质控品。
每日在测定前做一次质控。
该质控品为干粉包装,在2-8℃冰箱可稳定到失效期,使用前用?ml去离子水复溶,待质控物充分溶解(大约30分钟)后使用。
类风湿因子(RF)测定试剂盒(胶乳免疫比浊法)产品技术要求lideman

类风湿因子(RF)测定试剂盒(胶乳免疫比浊法) 适用范围:用于体外定量测定人血清中类风湿因子RF的含量。
1.1规格试剂(R1):2×60mL, 试剂(R2): 2×20mL;试剂(R1):1×45mL, 试剂(R2): 1×15mL;试剂(R1):2×45mL, 试剂(R2): 2×15mL;试剂(R1):1×60mL, 试剂(R2): 1×12mL;试剂(R1):1×60mL, 试剂(R2): 1×15mL;试剂(R1):1×30mL, 试剂(R2): 1×10mL;试剂(R1):2×40mL, 试剂(R2): 2×10mL;试剂(R1):1×15mL, 试剂(R2): 1×5mL;试剂(R1):1×16mL, 试剂(R2): 1×4mL;256T。
校准品(选配):5×1mL;质控品(选配):2×3mL。
1.2 主要组成成分:2.1 外观a)试剂盒各组分应齐全、完整,液体无渗漏;b)包装标签文字符号应清晰;c)R1:无色至淡黄色澄清液体,R2:乳白色液体。
校准品:无色至淡黄色澄清液体。
质控品:冻干品,复溶后为无色至淡黄色澄清液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 试剂空白吸光度在37℃、570nm波长、1cm光径条件下,试剂空白吸光度应在(0.5,2.0)之间。
2.4 分析灵敏度浓度为40IU/mL时,吸光度变化范围应在(0.005,0.3)之间。
2.5 线性试剂线性在(3,120)IU/mL范围内,线性相关系数(r)应不小于0.990;测定结果在(3,40)IU/mL时绝对偏差应在±4IU/mL范围内,在[40,120)IU/mL 范围内的相对偏差应在±10%范围内。
类风湿因子(RF)测定试剂盒(胶乳凝集法)

类风湿因子(RF)测定试剂盒(胶乳凝集法)【产品名称】通用名称:类风湿因子(RF)测定试剂盒(胶乳凝集法)商品名称:类风湿因子(RF)测定试剂盒(胶乳凝集法)英文名称:Rheumatoid Factoid Reagent Kit(Slide Latex Agglutination Test)【包装规格】【临床意义】对血清中RF定性或半定量测定,做辅助诊断用。
【检验原理】本试剂胶乳液是由纯化的人IgG和羧化聚苯乙烯胶乳共价交联而成的抗原胶乳。
RF胶乳的灵敏度调整到20IU/ml,超过上述滴度即出现肉眼可见凝集颗粒,试用本试剂血清标本不需要稀释即可直接测定。
【主要组成成份】胶乳液成份:类风湿因子胶乳、牛血清白蛋白、磷酸盐缓冲液阳性对照成份:羊抗人IgG抗血清、牛血清白蛋白、磷酸盐缓冲液阴性对照成份:牛血清白蛋白、磷酸盐缓冲液不同批号试剂盒中的乳胶液、阳性对照和阴性对照不能混用。
【储存条件及有效期】储藏温度2-10℃,切勿冷冻。
有效期一年。
【适用仪器】手工操作【样本要求】经离心获得新鲜血清样本,贮存于2-8℃,48小时内使用,时间过长须冰冻贮存。
【检验方法】定性实验:试剂使用前,预置达室温;轻轻混匀胶乳试剂;核对阴性和阳性对照;在反应板孔中加一滴未稀释血清(20μl);然后加一滴胶乳试剂在血清中;搅匀、轻轻摇动使其充分混和,二分钟后观察结果。
半定量实验:血清以生理盐水(0.9g氯化钠溶解于蒸馏水中,稀释至100ml)倍比稀释,可参照下法操作。
稀释倍1:2 1:4 1:8 1:16血清100μl生理盐水100μl 100μl 100μl 100μl→100μl→100μl→100μl标本量20μl 20μl20μl20μlmg/L >40 >80 >160 >1320【参考值(参考范围)】正常参考范围:成人<20IU/ml【检验结果的解释】凝集出现可判断样本中RF>20IU/ml阳性;无凝集出现可判断样本中RF<20IU/ml阴性。
类风湿因子测定试剂盒(胶乳免疫比浊法)产品技术要求dimai

类风湿因子测定试剂盒(胶乳免疫比浊法)适用范围:本试剂盒用于体外定量测定人血清中类风湿因子浓度。
1.1规格试剂1:1×40ml;试剂2:1×10ml试剂1:2×40ml;试剂2:1×20ml试剂1:1×60ml;试剂2:1×15ml试剂1:1×80ml;试剂2:1×20ml试剂1:3×80ml;试剂2:3×20ml试剂1:4×60ml;试剂2:3×20ml试剂1:2×80ml;试剂2:2×20ml试剂1:4×60ml;试剂2:4×15ml试剂1:4×60ml;试剂2:1×60ml试剂1:2×40ml;试剂2:2×10ml试剂1:8×60ml;试剂2:2×60ml试剂1:2×60ml;试剂2:2×15ml2.1 外观试剂1应无色澄清、无异物试剂2应呈乳白色、无异物。
2.2 净含量试剂的净含量不少于标称装量。
2.3 试剂空白吸光度用生理盐水作为样本加入试剂测试时,试剂空白吸光度应<1.200A。
2.4 分析灵敏度RF含量为20IU/mL时,测定吸光度差值的绝对值应>0.005△A。
2.5 线性区间试剂(盒)线性在[2,80]IU/mL区间内:2.5.1 线性回归相关系数(r)应≥0.990;2.5.2 线性偏差:[2,10]IU/mL区间内,线性|绝对偏差|≤3IU/mL;(10,80]IU/mL区间内,线性|相对偏差|≤10%。
2.6 精密度2.6.1 重复性用相同批号试剂盒测试两个水平的样本,所得结果的变异系数(CV)应<10%。
2.6.2 批间差用3个不同批号试剂盒测试两个水平的样本,批间相对极差应<10%。
2.7 准确度与已上市的同类产品比对,用40个在[2,80]IU/mL区间内不同浓度的人源样本,用线性回归方法计算两组结果的相关系数(r)不小于0.990;[2,10]IU/mL 区间内,线性绝对偏差不超过±3IU/mL;(10,80]IU/mL区间内,线性相对偏差不超过±10%。
类风湿因子(RF)测定试剂盒(胶乳凝集法)

类风湿因子(RF)测定试剂盒(胶乳凝集法)类风湿因子检测试剂盒(乳胶凝集法)[产品名称]通用名称:类风湿因子检测试剂盒(乳胶凝集法)商品名:类风湿因子检测试剂盒(乳胶凝集法)英文名称:类风湿因子试剂盒(玻片乳胶凝集法)[包装规范]每个包装箱为5毫升;胶水乳液;阳性对照0.5毫升;;阴性对照0.5毫升[临床意义]用于定性或半定量测定血清中的射频,用于辅助诊断。
[试验原理]该试剂胶乳是由纯化的人IgG和羧基化聚苯乙烯胶乳共价交联形成的抗原胶乳乳液射频乳胶的灵敏度调整到XXXX年。
[适用仪器]手动操作[样品要求]通过离心获得新鲜血清样品,并在2-8℃下储存48小时。
如果时间太长,必须冷冻保存。
[试验方法]定性实验:试剂在使用前预设为室温;轻轻混合乳胶试剂;检查阴性和阳性对照;向反应板孔中加入一滴未稀释的血清(20微升)。
然后在血清中加入一滴乳胶试剂。
搅拌均匀,轻轻摇动使其充分混合,2分钟后观察结果。
半定量实验:血清用生理盐水稀释(0.9g氯化钠溶于蒸馏水中,稀释至100ml)倍,可按以下方法操作稀释释放时间1: 2 1: 4 1: 8 1: 16青雪100μl生理盐水100μl 100μl 100μl→100μl→100μl→100μl→100μl标准量为20μ l 20μ l 20μ l在样品中未发现判断RF [试验方法的局限性]本试剂适用于人体内类风湿因子含量的定性和半定量检测。
如果需要定量检测,可以使用类风湿因子定量试剂[产品性能指数]1,灵敏度:20IU/ml阳性2.可测范围:20-60IU/ml[预防措施]1,添加试剂以及阴性和阳性质控品,以确保液滴大小一致2.如果阴阳控制结果异常,则不能使用该试剂。
3.该试剂样品中血清的样品量为20 μ L。
阴阳对照的样品量为对照瓶中的一滴(约50μl)。
4.试剂盒应储存在2-10℃的环境中。
加热会导致试剂的高阳性率。
不要冷冻它5年,阴和阳质控品的乙型肝炎表面抗原、丙型肝炎病毒和艾滋病毒检测结果为阴性,但它们仍需要像患者样本一样小心处理[参考。
类风湿因子测定试剂盒(胶乳免疫比浊法)产品技术要求丹大
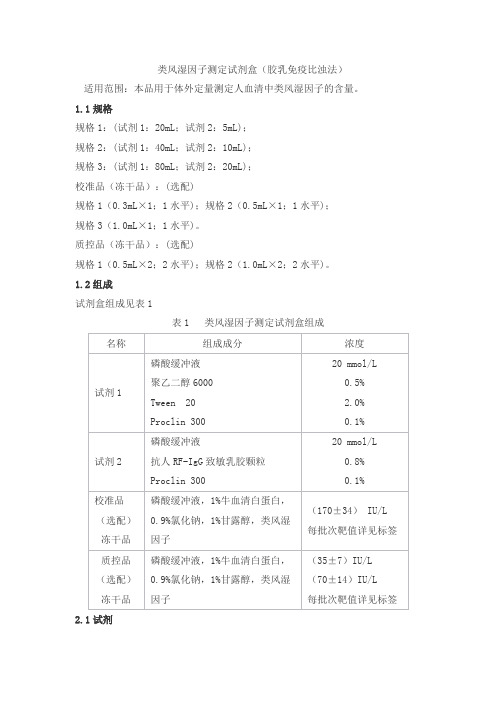
类风湿因子测定试剂盒(胶乳免疫比浊法)适用范围:本品用于体外定量测定人血清中类风湿因子的含量。
1.1规格规格1:(试剂1:20mL;试剂2:5mL);规格2:(试剂1:40mL;试剂2:10mL);规格3:(试剂1:80mL;试剂2:20mL);校准品(冻干品):(选配)规格1(0.3mL×1;1水平);规格2(0.5mL×1;1水平);规格3(1.0mL×1;1水平)。
质控品(冻干品):(选配)规格1(0.5mL×2;2水平);规格2(1.0mL×2;2水平)。
1.2组成试剂盒组成见表1表1 类风湿因子测定试剂盒组成2.1试剂2.1.1外观试剂盒外观应整洁,文字符号标识清晰;试剂1为透明液体,不得有沉淀和絮状物;试剂2为乳白色液体。
2.1.2装量每瓶不少于标示值。
2.1.3试剂空白吸光度用指定的空白样品测试试剂(盒),在光径1cm下,在A600nm处测定试剂空白吸光度A≤1.5。
2.1.4分析灵敏度用指定的空白样品测试试剂(盒),在光径1cm下,测定在20IU/L范围内的样品,吸光度差值△A≥0.005。
2.1.5线性范围2.1.5.1在[2,200] IU/L内,相关系数R≥0.990。
2.1.5.2在[2,20] IU/L内,线性绝对偏差不超过±2 IU/L;(20,200] IU/L 内,线性相对偏差不超过±10%。
2.1.6 重复性重复测试(35±7)IU/L和(70±14)IU/L样本,所得结果的变异系数(CV%)应不大于5%。
2.1.7批间差测定(35±7)IU/L和(70±14)IU/L样本,所得结果的批间相对极差(R)应不大于10%。
2.1.8准确度)中加入一定体积高于200 IU/L的类风湿在正常浓度范围的临床样本(C)或由纯品配制的标准溶液,回收率应在90%-110%范围内。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
类风湿因子(RF)测定试剂盒(胶乳凝集法)
类风湿因子检测试剂盒(乳胶凝集法)
[产品名称]
通用名称:类风湿因子检测试剂盒(乳胶凝集法)商品名:类风湿因子检测试剂盒(乳胶凝集法)
英文名称:类风湿因子试剂盒(玻片乳胶凝集法)
[包装规范]每个包装箱为5毫升;胶水乳液;阳性对照0.5毫升;;阴性对照0.5毫升[临床意义]用于定性或半定量测定血清中的射频,用于辅助诊断。
[试验原理]该试剂胶乳是由纯化的人IgG和羧基化聚苯乙烯胶乳共价交联形成的抗原胶乳
乳液射频乳胶的灵敏度调整到XXXX年。
[适用仪器]
手动操作
[样品要求]
通过离心获得新鲜血清样品,并在2-8℃下储存48小时。
如果时间太长,必须冷冻保存。
[试验方法]
定性实验:试剂在使用前预设为室温;轻轻混合乳胶试剂;检查阴性和阳性对照;向反应板孔中加入一滴未稀释的血清(20微升)。
然后在血清中加入一滴乳胶试剂。
搅拌均匀,轻轻摇动使其充分混合,2分钟后观察结果。
半定量实验:血清用生理盐水稀释(0.9g氯化钠溶于蒸馏水中,稀释至100ml)倍,可按以下方法操作
稀释释放时间1: 2 1: 4 1: 8 1: 16
青雪100μl
生理盐水100μl 100μl 100μl
→100μl
→100μl
→100μl
→100μl标准量为20μ l 20μ l 20μ l在样品中未发现判断RF [试验方法的局限性]
本试剂适用于人体内类风湿因子含量的定性和半定量检测。
如果需要定量检测,可以使用类风湿因子定量试剂
[产品性能指数]
1,灵敏度:20IU/ml阳性2.可测范围:20-60IU/ml
[预防措施]
1,添加试剂以及阴性和阳性质控品,以确保液滴大小一致2.如果阴阳控制结果异常,则不能使用该试剂。
3.该试剂样品中血清的样品量为20 μ L。
阴阳对照的样品量为对照瓶中的一滴(约50μl)。
4.试剂盒应储存在2-10℃的环境中。
加热会导致试剂的高阳性率。
不要冷冻它5年,阴和阳质控品的乙型肝炎表面抗原、丙型肝炎病毒和艾滋病毒检测结果为阴性,但它们仍需要像患者样本一样小心处理
[参考。
]
1,陆胜凯,等:上海医院检验杂志4 (2): 97.1989 2,加林,。
p .等人;临床实验室化验4:73-95(1983)。
