谷胱甘肽还原酶检测试剂盒简介
碧云天谷胱甘肽过氧化物酶检测试剂盒说明书

碧云天生物技术/Beyotime Biotechnology 订货热线:400-1683301或800-8283301 订货e-mail :******************技术咨询:*****************网址:碧云天网站 微信公众号谷胱甘肽过氧化物酶检测试剂盒(NADPH 法)产品编号 产品名称包装 S0056谷胱甘肽过氧化物酶检测试剂盒(NADPH 法)100次产品简介:谷胱甘肽过氧化物酶检测试剂盒(NADPH 法)(Cellular Glutathione Peroxidase Assay Kit with NADPH)是一种简单易行的通过紫外比色来检测细胞、组织或其它样品中谷胱甘肽过氧化物酶(Glutathione peroxidase, GPx)活性的试剂盒。
绝大部分细胞内的谷胱甘肽过氧化物酶都是含硒的,且硒为该酶的活性中心组成部分。
细胞内也有很少量的不含硒的谷胱甘肽过氧化物酶存在。
本试剂盒检测的是最常见的含硒的谷胱甘肽过氧化物酶。
本试剂盒的使用灵活方便,样品用量和检测时间的范围宽,样品用量可以根据样品中GPx 的活力在0.1-50微升之间调整,检测时间可以根据样品中GPx 的活力在5-30分钟内进行调整。
本试剂盒和总谷胱甘肽过氧化物酶检测试剂盒(S0058)配合使用,可以定量检测出样品中不含硒的谷胱甘肽过氧化物酶。
谷胱甘肽过氧化物酶可以清除活细胞内的过氧化物,在保护细胞免受自由基损伤过程中起着关键作用。
细胞内的脂类容易和自由基发生反应,产生脂类过氧化物。
谷胱甘肽过氧化物酶可以利用还原型谷胱甘肽(GSH)还原脂类过氧化物,从而消除自由基的毒害作用。
谷胱甘肽过氧化物酶几乎在所有组织中都有分布。
在一些病理状况下谷胱甘肽过氧化物酶的活力会发生明显上调或下调。
谷胱甘肽过氧化物酶可以利用还原型谷胱甘肽(GSH)催化过氧化氢以及许多有机过氧化物,产生水或有机醇。
但以过氧化氢为底物进行检测会受同样可以分解过氧化氢的过氧化氢酶(Catalase)的影响,因为过氧化氢酶的酶活性会干扰谷胱甘肽过氧化物酶的测定。
谷胱甘肽还原酶(GSR)测定试剂盒 (谷胱甘肽底物法)产品技术要求利德曼
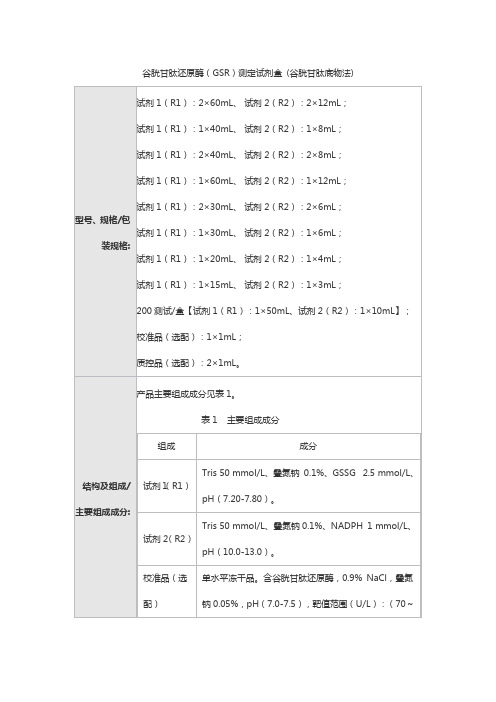
谷胱甘肽还原酶(GSR)测定试剂盒(谷胱甘肽底物法)1.1包装规格试剂1(R1):2×60mL、试剂2(R2):2×12mL;试剂1(R1):1×40mL、试剂2(R2):1×8mL;试剂1(R1):2×40mL、试剂2(R2):2×8mL;试剂1(R1):1×60mL、试剂2(R2):1×12mL;试剂1(R1):2×30mL、试剂2(R2):2×6mL;试剂1(R1):1×30mL、试剂2(R2):1×6mL;试剂1(R1):1×20mL、试剂2(R2):1×4mL;试剂1(R1):1×15mL、试剂2(R2):1×3mL;200测试/盒:【试剂1(R1):1×50mL、试剂2(R2):1×10mL】。
校准品(选配):1×1mL。
质控品(选配):2×1mL。
1.2主要组成成分产品主要组成成分见表1。
表1 主要组成成注:校准品和质控品浓度具有批特异性,具体数值见瓶标签。
2.1外观试剂盒各组分应齐全、完整,液体无渗漏。
包装标签文字符号应清晰。
液体双试剂:试剂1(R1)为无色澄清液体;试剂2(R2)为无色至淡黄色澄清液体。
校准品:冻干品,复溶后为无色至淡黄色澄清液体。
质控品:冻干品,复溶后为无色至淡黄色澄清液体。
2.2 装量液体试剂的净含量不得低于标示体积。
2.3 试剂空白2.3.1空白吸光度在37 ℃、(340 nm±10%)范围内的波长、1cm光径条件下,用纯化水或生理盐水作为样品加入试剂测试时,试剂空白吸光度应≤2.5。
2.3.2空白吸光度变化率在37℃、(340 nm±10%)范围内的波长、1cm光径条件下,用纯化水或生理盐水作为样品加入试剂测试时,空白吸光度变化率(ΔA/min)应≤0.01 。
碧云天谷胱甘肽过氧化物酶检测试剂盒

¾ 谷胱甘肽过氧化物酶可以利用还原型谷胱甘肽(GSH)催化过氧化氢以及许多有机过氧化物,产生水或有机醇。如果以过氧 化氢为底物进行检测,则同样可以分解过氧化氢的过氧化氢酶(Catalase)的酶活性会干扰谷胱甘肽过氧化物酶的测定。本 试剂盒利用了一种间接测定的方法。谷胱甘肽过氧化物酶可以催化GSH产生GSSG,而谷胱甘肽还原酶可以利用NADPH 催化GSSG产生GSH,通过检测NADPH的减少量就可以计算出谷胱甘肽过氧化物酶的活力水平。在上述反应中,谷胱甘 肽过氧化物酶是整个反应体系的限速步骤,因此NADPH的减少量和谷胱甘肽过氧化物酶的活力线性相关。
e. 所有试剂使用前须在水浴中或PCR仪等设备上温育到25℃。
3. 样品测定:
表1
空白对照 (blank)
样品本底对照
样品 (sample)
谷胱甘肽过氧化物酶l
176-184 µl
待测样品
-
2-10 µl
2-10 µl
GPx检测工作液
10 µl
10 µl
10 µl
谷胱甘肽还原酶
0.4 µl
4 µl
8µl
GPx检测工作液体积
10.4 µl
104 µl
208µl
d. 15mM过氧化物试剂溶液的配制。取21.5微升过氧化物试剂(t-Bu-OOH)加入10毫升Milli-Q级纯水,混匀,即配制成
15mM过氧化物试剂溶液。配制好的15mM过氧化物试剂溶液仅限当日使用,且需尽量在冰浴上存放。
产品编号 S0056
谷胱甘肽过氧化物酶检测试剂盒
产品名称 谷胱甘肽过氧化物酶检测试剂盒
谷胱甘肽过氧化物酶(GSH-Px)检测试剂盒(比色法)
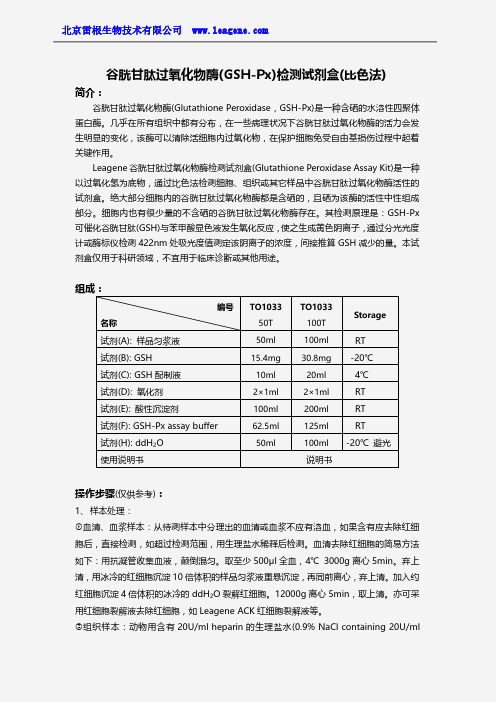
组成:
编号 名称 试剂(A): 样品匀浆液 试剂(B): GSH 试剂(C): GSH 配制液 试剂(D): 氧化剂 试剂(E): 酸性沉淀剂 试剂(F): GSH-Px assay buffer 试剂(H): ddH2O 使用说明书
TO1033 50T 50ml
15.4mg 10ml 2×1ml 100ml 62.5ml 50ml
北京雷根生物技术有限公司
谷胱甘肽过氧化物酶(GSH-Px)检测试剂盒(比色法)
简介:
谷胱甘肽过氧化物酶(Glutathione Peroxidase,GSH-Px)是一种含硒的水溶性四聚体 蛋白酶。几乎在所有组织中都有分布,在一些病理状况下谷胱甘肽过氧化物酶的活力会发 生明显的变化,该酶可以清除活细胞内过氧化物,在保护细胞免受自由基损伤过程中起着 关键作用。
Leagene 谷胱甘肽过氧化物酶检测试剂盒(Glutathione Peroxidase Assay Kit)是一种 以过氧化氢为底物,通过比色法检测细胞、组织或其它样品中谷胱甘肽过氧化物酶活性的 试剂盒。绝大部分细胞内的谷胱甘肽过氧化物酶都是含硒的,且硒为该酶的活性中性组成 部分。细胞内也有很少量的不含硒的谷胱甘肽过氧化物酶存在。其检测原理是:GSH-Px 可催化谷胱甘肽(GSH)与苯甲酸显色液发生氧化反应,使之生成黄色阴离子,通过分光光度 计或酶标仪检测 422nm 处吸光度值测定该阴离子的浓度,间接推算 GSH 减少的量。本试 剂盒仅用于科研领域,不宜用于临床诊断或其他用途。
—
0.1ml
2ml
1ml
4、 GSH-Px 显色反应: 可参考下表设置检测反应体系,依次加入试剂:
Hale Waihona Puke 加入物质空白对照管 本底对照管 测定管
还原型谷胱甘肽(GSH)含量检测试剂盒说明书__ 可见分光光度法UPLC-MS-4486

还原型谷胱甘肽(GSH)含量检测试剂盒说明书可见分光光度法货号:UPLC-MS-4486规格:50T/48S产品组成:使用前请认真核对试剂体积与瓶内体积是否一致,有疑问请及时联系工作人员。
试剂名称规格保存条件试剂一液体50mL×1瓶4℃保存试剂二液体50mL×1瓶4℃保存试剂三液体15mL×1瓶4℃保存标准品粉剂10mg×1支4℃保存溶液的配制:1、标准品:称1mg标准品用1mL蒸馏水溶解,浓度为1mg/mL。
产品说明:谷胱甘肽是由谷氨酸(Glu)、半胱氨酸(Cys)和甘氨酸(Gly)组成的天然三肽,是一种含巯基(—SH)的化合物,广泛存在于动物组织、植物组织、微生物和酵母中。
谷胱甘肽能和5,5’-二硫代-双-(2-硝基苯甲酸)(5,5’-dithiobis-2-nitrobenoic acid,DTNB)反应产生2-硝基-5-巯基苯甲酸和谷胱甘肽二硫化物(GSSG)。
2-硝基-5-巯基苯甲酸为黄色产物,在波长412nm处具有最大光吸收。
技术指标:最低检出限:2.67μg/mL线性范围:3.125-250μg/mL注意:实验之前建议选择2-3个预期差异大的样本做预实验。
如果样本吸光值不在测量范围内建议稀释或者增加样本量进行检测。
需自备的仪器和用品:分析天平、匀浆器/研钵、低温离心机、水浴锅、移液器、可见分光光度计、1mL玻璃比色皿。
操作步骤:一、样本处理(可适当调整待测样本量,具体比例可以参考文献)1、组织处理:新鲜组织首先用PBS冲洗2次,然后称取动物组织或者植物组织0.1g。
加入用试剂一润洗过的匀浆器中(匀浆器提前放冰上预冷);然后加入1mL试剂一(组织/试剂一比例保持不变即可),迅速冰上充分研磨(使用液氮研磨效果更好);8000g,4℃离心10min;取上清液放置于4℃待测,若暂时不能完成测试可放于-80℃保存(可保存10天)。
2、血液处理血浆:将收集的抗凝血于4℃,600g离心10分钟,吸取上层血浆到另一支试管中,加入等体积的试剂一, 4℃,8000g离心10分钟,将上清移入新的试管中放置于4℃待测,若暂时不能完成测试可放于-80℃保存(可保存10天)。
南京建成GPX试剂盒说明书

南京建成GPX试剂盒说明书一、产品简介南京建成GPX试剂盒是一种用于测定谷胱甘肽过氧化物酶(GPX)活性的试剂盒。
谷胱甘肽过氧化物酶是一种重要的抗氧化酶,在生物体内起到清除自由基的作用。
该试剂盒采用酶促反应原理,通过检测GPX酶催化反应的速率,反映样品中GPX活性的强弱。
二、试剂盒组成1.GPX试剂盒2.GPX标准品3.过氧化氢(H2O2)稀释液4.反应底物液5.转化液6.二恶吖啶试剂7.芳醛显色剂液8.脱氧胆酸液三、操作步骤步骤一:样品处理1.将待测样品离心收集沉淀,去除杂质;2.取适量样品,加入过氧化氢(H2O2)稀释液,混匀;3.将处理后的样品转移至离心管,进行离心提取。
步骤二:制备标准曲线1.取GPX标准品不同浓度的工作液,依次加入反应孔;2.使用空白对照孔作为空白对照;3.分别加入转化液和反应底物液,混匀。
步骤三:反应过程1.加入样品提取液和转化液,混匀;2.加入反应底物液,混匀;3.加入二恶吖啶试剂,混匀;4.加入芳醛显色剂液,混匀;5.加入脱氧胆酸液,混匀。
步骤四:测定吸光度使用酶标仪在450nm波长下测定样品、标准品和空白对照的吸光度值。
四、结果判读根据标准曲线,计算出样品中GPX活性的浓度,进行数据分析。
根据浓度值的高低,可以判断出样品中GPX活性的强弱。
五、注意事项1.试剂盒的各组分应在4℃保存,开封后应尽快使用;2.不同批次的试剂盒不能混合使用;3.操作前,必须严格按照说明书操作,确保实验的准确性;4.不同样品的处理方式可能不同,请参照具体样品类型的处理方法;5.操作过程中应佩戴实验手套,避免接触试剂;6.尽量避免阳光直射,保持试剂的保存质量。
六、故障排除1.若标准曲线呈线性上升趋势,则说明实验条件符合要求,结果可信;2.若标准曲线呈非线性趋势,则可能是试剂盒保存不当或过期,需更换新的试剂,重新进行实验;3.若实验结果不符合预期,可能是样品处理不当或操作过程中出错,请检查并重新进行实验。
还原型谷胱甘肽 (reduced glutathione,GSH)含量测定试剂盒使用说明

还原型谷胱甘肽(reduced glutathione,GSH)含量测定试剂盒使用说明产品简介:GSH/GSSG是细胞内最重要的氧化还原对之一。
因此,测定细胞内GSH和GSSG含量以及GSH/GSSG比值,能够很好地反映细胞所处的氧化还原状态。
DTNB与GSH反应生成复合物,在412nm处有特征吸收峰;其吸光度变化与GSH含量成正比。
试验中所需的仪器和试剂:可见分光光度计、低温离心机、水浴锅、可调节移液器、1ml比色皿、双蒸水产品内容:试剂一×1支,充分溶解于100ml双蒸水,4℃保存试剂二×1支,充分溶解于50ml试剂一中,4℃保存试剂三×1支,充分溶解于10ml双蒸水中,4℃避光保存操作步骤:一、样品前处理:取组织约0.1g,加1ml试剂二,冰上充分研磨,8000rpm4℃离心10min,取上清。
(如上清不清澈,再离心3min)GSH测定操作:测定前将试剂一于25℃水浴20min按每100mg组织加入1000µL生理盐水的比例进行匀浆。
8000g4℃离心10分钟,取上清,置冰上待测。
对于非哺乳动物组织:按每100mg组织加入1000µL提取液的比例进行匀浆。
8000g 4℃离心10分钟,取上清,置冰上待测。
(2)血清(浆)样品:直接检测。
二、测定操作表:测定管空白管样本0.1ml/试剂一0.7ml0.7ml蒸馏水/0.1ml试剂三0.2ml0.2ml 迅速混匀,于412nm测吸光值,并记录第60s的OD值GSH含量计算:GSH标准曲线公式:y=0.0015x+0.0818(x为GSH浓度,y为吸光值)液体中GSH(µmol/L)=[(OD测定管-OD空白管)-0.0818]/0.0015×样品稀释倍数组织中GSH计算:①GSH(µmol/mg prot)=[(OD测定管-OD空白管)-0.0818]/0.0015×样品稀释倍数÷样品蛋白浓度(Cpr)②GSH(µmol/g mass)=[(OD测定管-OD空白管)-0.0818]/0.0015×样品稀释倍数÷样品质量(g)注意事项:(1)样品处理等过程均需要在冰上进行,且须在当日测定酶活力,以免影响其活力测定时,除试剂一外,其它试剂均需放置在冰上;(2)样本测定前先取1-2个样做预实验,如吸光值太高(超过标准曲线范围,即y >0.2时),应先用试剂二稀释到适当倍数,使得吸光值在标准曲线范围内。
总谷胱甘肽检测试剂盒
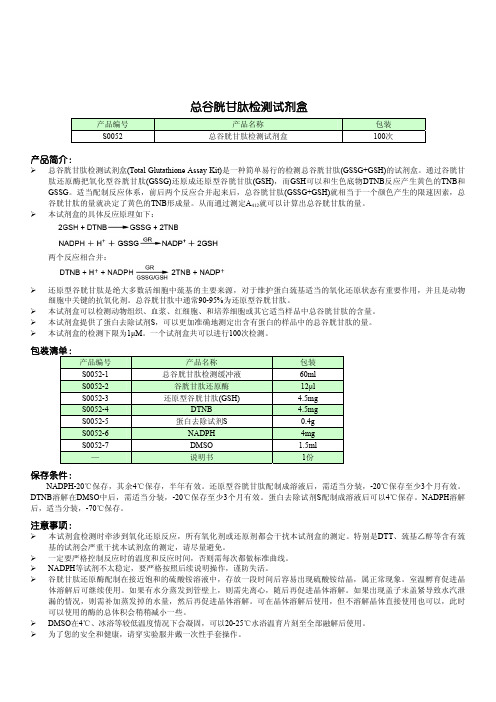
50 μl
50 μl
50 μl
b. 加入50微升0.16mg/ml NADPH溶液,混匀。
c. 立即用酶标仪测定A412,每5分钟测定一次或实时测定,共测定25分钟,测得5个数据。(说明:为了简化实验步骤,可 以在加入NADPH溶液混匀后25分钟,仅测定一次A412)。如果仪器可以设置温度,把温度设置在25℃,否则就在室温
2. Xiao-Long W, Chuan-Ping Y, Kai X, Ou-Jv Q. Selenoprotein W depletion in vitro might indicate that its main function is not as an antioxidative enzyme. Biochemistry (Mosc). 2010;75(2):201-7.
NADPH。每检测一个样品需50微升0.16mg/ml NADPH。
2. 标准品的准备:
把10mM GSH储备液用蛋白去除试剂S溶液稀释成50μM GSH溶液。然后依次稀释成25、15、10、5、2μM GSH溶液。取
50、25、15、10、5、2μM GSH溶液六个点做标准曲线。注意:由于GSH在蛋白去除试剂S溶液中不太稳定,用蛋白去除
b. 细胞样品的准备。请尽量使用新鲜的细胞进行测定,而不要使用冻存的细胞进行测定。PBS洗涤细胞一次,离心收集
细胞,吸尽上清。加入细胞沉淀体积3倍量的蛋白去除试剂S溶液,即如果细胞沉淀为10微升,则加入30微升蛋白去除
试剂S溶液,充分Vortex。(细胞沉淀的体积可以根据细胞沉淀的重量进行估算。收集细胞前后分别对离心管进行称
等处理,而直接加入适量蛋白去除试剂S溶液进行匀浆)。4℃放置10分钟后,10,000g 4℃离心10分钟,取上清用于总
凯基谷胱甘肽过氧化物酶(GSH-PX)测试盒

注意
注 1:空白管、标准管一般只需做 1-2 只。
注 2:最佳取样量及最佳取样浓度因样品种类不同,其 GSH-PX 活力不一。根据酶的百分抑制率与酶的活 力呈抛物线关系,各种测定样品取样量及取样浓度不一样,在每测定一种新的样品前最好选择一个最佳取
样量及最佳取样浓度。
最佳取样浓度的摸索
测试前先预试以确定最佳取样浓度:当您第一次使用本试剂盒测试某一种新的样品时最好先做三只不同浓
4℃或室温保存 6 个月
4℃保存 6 个月 4℃避光保存五天
4℃保存
GSH 的分子量为 307,每次测定前将 1 支 3.07mg 的 GSH 标准品粉剂加到 GSH 标准品的溶剂应用液 中,定容至 10ml 即为 1mmol/L 的 GSH 溶液,现用 现配。
取 1mmol/L GSH 溶液 2ml 加 GSH 标准品溶剂应用 液 18ml 定容至 20ml,作标准曲线用,若不做标准 曲线可以不配。
保存条件 4℃
3 5 7
GSH 应用液的配制: 1mmol/L GSH 溶液
100u mol/L GSH 溶液 20umol/L 的 GSH 标准溶液
试剂二应用液的配制:将已配好的 甲乙两种混合。此为过饱和溶液, 室温静置冷却后,如有结晶,则取 上清进行实验。 加蒸馏水 100ml 溶解 每支加蒸馏水 10ml 溶解 标准品溶剂应用液:GSH 标准品 溶剂贮备液:双蒸水=1:9 即 10 倍稀释配成应用液;按所需量现用 现配。
二.试剂盒的组成和配制
25 Tests (50 Tubes)试剂盒的组成和保存: 试剂编号 1
2
3 4 5
名称 贮备液
甲粉 乙液 粉剂 液体 粉剂
6
GSH 标准品粉剂
谷胱甘肽还原酶测定试剂盒(谷胱甘肽底物法)产品技术要求广州科方生物技术

医疗器械产品技术要求编号:谷胱甘肽还原酶测定试剂盒(谷胱甘肽底物法)2.性能指标2.1试剂盒性能指标2.1.1外观试剂盒各组分应齐全、完整、无液体渗漏;液体试剂应为澄清透明、无絮状物、无肉眼可见颗粒及沉淀的液体;包装标签应清晰,准确、牢固。
2.1.2装量液体试剂的装量应不小于标示量。
2.1.3试剂空白2.1.3.1试剂空白吸光度在温度37℃、波长340nm条件下检测,试剂空白吸光度应≥0.5000(比色杯光径1.0cm)。
2.1.3.2试剂空白吸光度变化率试剂空白吸光度变化率(△A/min)应≤0.0100(比色杯光径1.0cm)。
2.1.4分析灵敏度测定谷胱甘肽还原酶活性为70U/L的样品时,其吸光度变化率(△A/min)应≤0.5000。
2.1.5线性a)线性区间[4,300]U/L,相关系数r应≥0.9900;b)[4,30]U/L区间内绝对偏差应不超过±4.5U/L;(30,300]U/L区间内相对偏差应不超过±15%。
2.1.6精密度2.1.6.1重复性CV应≤10%。
2.1.6.2批间差相对极差(R)应≤10%。
2.1.7准确度以企业参考品为检测样本,测定结果与企业参考品靶值浓度的相对偏差应在±15%范围内。
2.2校准品性能指标2.2.1性状校准品应为无色至淡黄色液体。
2.2.2装量校准品装量应不少于标示值。
2.2.3正确度使用校准物校准后测量参考物质,量值传递的正确度应符合|En|≤1。
2.2.4均匀性a)瓶内均匀性:CV≤10%;b)瓶间均匀性:CV≤15%。
2.3质控品性能指标2.3.1外观质控品应为无色至淡黄色液体。
2.3.2装量质控品装量应不少于标示值。
2.3.3预期结果用校准品校准测量程序后测定质控物,结果应在靶值范围内。
2.3.4均匀性瓶间均匀性:CV应≤15.0%。
谷胱甘肽过氧化物酶(GSH-Px_GPX)活性检测试剂盒说明书__微量法UPLC-MS-4499

谷胱甘肽过氧化物酶(GSH-Px/GPX)活性检测试剂盒说明书微量法注意:本产品试剂有所变动,请注意并严格按照该说明书操作。
货号:UPLC-MS-4499规格:100T/48S产品组成:使用前请认真核对试剂体积与瓶内体积是否一致,有疑问请及时联系工作人员。
试剂名称规格保存条件提取液液体60mL×1瓶4℃保存试剂一粉剂×2瓶4℃保存试剂二液体10μL×1瓶4℃保存试剂三液体30mL×1瓶4℃保存试剂四液体15mL×1瓶4℃保存试剂五液体5mL×1瓶4℃保存标准品粉剂×1支4℃保存稀释液液体20mL×1瓶4℃保存溶液的配制:1、试剂一:临用前加入3.3mL稀释液,充分溶解;2、试剂二:临用前按2μL试剂二:10mL蒸馏水的比例稀释试剂二,现用现配;3、试剂三:瓶底若有结晶可50℃水浴溶解,此溶液为饱和溶液,若底部最终还有结晶,吸取上清使用即可;4、标准品:10mg还原型谷胱甘肽。
临用前加入0.405mL稀释液溶解为80μmol/mL的标准溶液备用。
产品说明:谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px或GPX)是机体内广泛存在的一种重要的过氧化物分解酶。
GPX能够催化还原型谷胱甘肽(GSH)生成氧化型谷胱甘肽(GSSG),使有毒的过氧化氢还原成无毒的羟基化合物。
GPX催化H2O2氧化GSH,产生GSSG,GSH能与DTNB生成在412nm处有特征吸收峰的化合物,412nm下吸光度的下降即可反应GPX的活性。
注意:实验之前建议选择2-3个预期差异大的样本做预实验。
如果样本吸光值不在测量范围内建议稀释或者增加样本量进行检测。
需自备的仪器和用品:可见分光光度计/酶标仪、天平、台式离心机、微量玻璃比色皿/96孔板、可调式移液枪、研钵/匀浆器、EP管。
操作步骤:一、样本处理(可适当调整待测样本量,具体比例可以参考文献)1、组织:按照组织质量(g):提取液体积(mL)为1:5~10的比例(建议称取0.05g组织,加入1mL提取液)进行冰浴匀浆。
谷胱甘肽还原酶检测试剂盒

GSSG。1 U=1000 mU。
c. 对于谷胱甘肽还原酶:1mU/ml=1nmol NADPH/min/ml=(A340/min)/0.00622 即相当于:[检测体系中谷胱甘肽还原酶活力]=[A340/min(sapmle)-A340/min(blank)]/0.00622 注:[检测体系中谷胱甘肽还原酶活力]的单位为mU/ml。
如果A340/min(sapmle)=0.0255,A340/min(blank)=0.0006,那么 [检测体系中谷胱甘肽还原酶活力]= (0.0255-0.0006)/0.00622=4.0mU/ml
[样品中谷胱甘肽还原酶活力]= 4.0mU/mlX10X20/(0.5mg/ml)=1.6U/mg(蛋白)
注意事项:
¾ 本试剂盒检测时牵涉到氧化还原反应,所有氧化剂或还原剂都会干扰本试剂盒的测定。另外,硫酸钠、硫酸铵和铁氰化 物都会干扰本试剂盒的测定。请尽量避免。
¾ 样品可以立即测定,也可以-70℃冻存待以后测定。 ¾ 一定要严格控制反应时的温度,否则会引起较多误差。 ¾ NADPH不太稳定,要严格按照后续说明操作,谨防失活。 ¾ 为了您的安全和健康,请穿实验服并戴一次性手套操作。
产品编号 S0055
谷胱甘肽还原酶检测试剂盒
产品名称 谷胱甘肽还原酶检测试剂盒
包装 100次
产品简介:
¾ 谷胱甘肽还原酶检测试剂盒(Glutathione Reductase Assay Kit)是一种简单易行的通过紫外比色来检测细胞、组织或其它样 品中谷胱甘肽还原酶(Glutathione reductase)活性的试剂盒。谷胱甘肽还原酶可以还原氧化型谷胱甘肽(GSSG)生成还原型谷 胱甘肽(GSH)。谷胱甘肽还原酶在许多组织中都有分布,可以维持细胞内充足的还原型谷胱甘肽(GSH)水平。GSH可以清 除自由基和一些有机过氧化物,或作为谷胱甘肽氧化酶(Glutathione peroxidase)的底物来清除一些过氧化物。
谷胱甘肽还原酶测定试剂盒(谷胱甘肽底物法)产品技术要求jiuqiang

谷胱甘肽还原酶测定试剂盒(谷胱甘肽底物法)适用范围:本试剂盒用于体外定量测定人血清谷胱甘肽还原酶的含量。
1.1 包装规格包装规格见表1。
表1 包装规格1.2 主要组成成分主要组成成分见表2。
表2 主要组成成分2.1 外观试剂1a为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂1b为无色或浅黄色粉末状物质,复溶后为无色或浅黄色液体,目测不得有任何沉淀及絮状悬浮物;试剂2为无色或浅黄色粉末状物质,复溶后为无色或浅黄色液体,目测不得有任何沉淀及絮状悬浮物;质控品为无色或浅黄色粉末状物质,复溶后为无色或浅黄色液体,目测不得有任何沉淀及絮状悬浮物。
试剂盒标签标识清晰,外包装完整无损。
2.2 净含量液体试剂的净含量应不少于标称量。
2.3 试剂空白吸光度2.3.1 试剂空白吸光度A340nm下测定空白吸光度应≤1.5000。
2.3.2 试剂空白吸光度变化率A340nm下测定试剂空白吸光度变化率(ΔA/min)应≤ 0.0100。
2.4 准确度与已上市产品进行比对试验:在[12,184] U/L区间内,相关系数r≥0.975,在[12,50] U/L区间内测定的绝对偏差应不超过±7.5 U/L,在(50,184]U/L区间内测定的相对偏差应不超过±15%。
2.5 分析灵敏度样本浓度为70U/L时,其吸光度变化率应不超过0.5000。
2.6 线性范围在[12,184] U/L区间内,线性相关系数r≥0.990,在[12,50]U/L区间内线性绝对偏差应不超过±7.5U/L,在(50,184] U/L区间内线性相对偏差应不超过±15%。
2.7 测量精密度2.7.1 重复性使用高、低不同浓度的血清样本或质控品重复测定10次,其测定值的变异系数(CV%)应不大于10%。
2.7.2 批间差随机抽取三批试剂盒的批间相对极差(R)应不大于10%。
2.8 瓶间差试剂1b、试剂2、质控品的瓶间差应≤10%。
谷胱甘肽还原酶(GR)活性测定试剂盒说明书

谷胱甘肽还原酶(GR)活性测定试剂盒说明书谷胱甘肽还原酶(GR)活性测定试剂盒说明书微量法100T/96S注意:正式测定之前选择23个预期差别大的样本做猜测定。
测定意义:GR是广泛存在于真核和原核生物中的一种黄素蛋白氧化还原酶,是谷胱甘肽氧化还原循环的关键酶之一(通常昆虫中GR被TrxR取代)。
GR催化NADPH还原GSSG生成GSH,有助于维持体内GSH/GSSG比值。
GR在氧化胁迫反应中对活性氧清除起关键作用,另外GR还参加抗坏血酸—谷胱甘肽循环途径。
测定原理:GR能催化NADPH还原GSSG再生GSH,同时NADPH脱氢生成NADP+;NADPH在340nm有特征汲取峰,相反NADP+在该波长无汲取峰;通过测定340nm吸光度下降速率来测定NADPH脱氢速率,从而计算GR活性。
自备仪器和用品:低温离心机、水浴锅、移液器、紫外分光光度计/酶标仪、微量石英比色皿/96孔板和蒸馏水试剂构成和配置:试剂一:液体120mL×1瓶,4℃保管。
试剂二:粉剂×2支,20℃保管。
临用前加入1.2mL蒸馏水,混匀。
试剂三:粉剂×2支,20℃保管。
临用前加入0.6mL蒸馏水,混匀。
粗酶液提取:1.组织:依照组织质量(g):试剂一体积(mL)为1:5~10的比例(建议称取约0.1g组织,加入1mL试剂一)进行冰浴匀浆。
8000g,4℃离心15min,取上清,置冰上待测。
2.细菌、真菌:依照细胞数量(104个):试剂一体积(mL)为500~1000:1的比例(建议500万细胞加入1mL试剂一),冰浴超声波碎裂细胞(功率300w,超声3秒,间隔7秒,总时间3min);然后8000g,4℃,离心15min,取上清置于冰上待测。
3.血清等液体:直接测定。
操作步骤:1.分光光度计/酶标仪预热30min,调整波长到340nm,蒸馏水调零。
2.试剂一置于25℃(普通物质)或者37℃(哺乳动物)中预热30min。
还原型谷胱甘肽 (reduced glutathione,GSH)含量测定试剂盒使用说明

还原型谷胱甘肽(reduced glutathione,GSH)含量测定试剂盒使用说明产品简介:GSH/GSSG是细胞内最重要的氧化还原对之一。
因此,测定细胞内GSH和GSSG含量以及GSH/GSSG比值,能够很好地反映细胞所处的氧化还原状态。
DTNB与GSH反应生成复合物,在412nm处有特征吸收峰;其吸光度变化与GSH含量成正比。
试验中所需的仪器和试剂:可见分光光度计、低温离心机、水浴锅、可调节移液器、1ml比色皿、双蒸水产品内容:试剂一×1支,充分溶解于100ml双蒸水,4℃保存试剂二×1支,充分溶解于50ml试剂一中,4℃保存试剂三×1支,充分溶解于10ml双蒸水中,4℃避光保存操作步骤:一、样品前处理:取组织约0.1g,加1ml试剂二,冰上充分研磨,8000rpm4℃离心10min,取上清。
(如上清不清澈,再离心3min)GSH测定操作:测定前将试剂一于25℃水浴20min按每100mg组织加入1000µL生理盐水的比例进行匀浆。
8000g4℃离心10分钟,取上清,置冰上待测。
对于非哺乳动物组织:按每100mg组织加入1000µL提取液的比例进行匀浆。
8000g 4℃离心10分钟,取上清,置冰上待测。
(2)血清(浆)样品:直接检测。
二、测定操作表:测定管空白管样本0.1ml/试剂一0.7ml0.7ml蒸馏水/0.1ml试剂三0.2ml0.2ml 迅速混匀,于412nm测吸光值,并记录第60s的OD值GSH含量计算:GSH标准曲线公式:y=0.0015x+0.0818(x为GSH浓度,y为吸光值)液体中GSH(µmol/L)=[(OD测定管-OD空白管)-0.0818]/0.0015×样品稀释倍数组织中GSH计算:①GSH(µmol/mg prot)=[(OD测定管-OD空白管)-0.0818]/0.0015×样品稀释倍数÷样品蛋白浓度(Cpr)②GSH(µmol/g mass)=[(OD测定管-OD空白管)-0.0818]/0.0015×样品稀释倍数÷样品质量(g)注意事项:(1)样品处理等过程均需要在冰上进行,且须在当日测定酶活力,以免影响其活力测定时,除试剂一外,其它试剂均需放置在冰上;(2)样本测定前先取1-2个样做预实验,如吸光值太高(超过标准曲线范围,即y >0.2时),应先用试剂二稀释到适当倍数,使得吸光值在标准曲线范围内。
GR检测线性范围

GR检测线性范围
谷胱甘肽还原酶(GR)测定试剂盒(紫外比色法)试剂盒96T/48T 进口/国产,提供检测试剂盒价格、用途、规格、实验原理、说明书、相关实验操作等详细信息。
谷胱甘肽还原酶(GR)测定试剂盒(紫外比色法)试剂盒产品优点:
1线性范围:0-500U/L(判定依据:r2≥0.995);
2准确度:不准确度≤10%;
3精密度:批内CV<4.0%;批间相对极差<6.0%;
4灵敏度:试剂检测下限≤4.0U/L。
谷胱甘肽还原酶(GR)测定试剂盒(紫外比色法)试剂盒声明
1.限于现有条件及科学技术水平,尚不能对所有原料进行全面的鉴定分析,本产品可能存在一定的质量技术风险。
2.最终的实验结果与试剂的有效性、实验者的相关操作以及当时的实验环境密切相关,请务必准备充足的待测样品。
3.只有全部使用试剂盒内的试剂才能保证检测效果,不能混用其他制造商的产品。
只有严格遵守Antiscience 的实验说明才会得到最佳的检测结果。
4.有效期:6 个月。
5.本操作说明同样适用于48T 试剂盒。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
谷胱甘肽还原酶检测试剂简介
谷胱甘肽还原酶的作用:
一、谷胱甘肽还原酶(GR)在人类细胞中具有极其重要的生理功能,广泛存在于人体肝、肾、心红细胞、单核巨噬细胞等组织细胞中。
它可及时地清除人体代谢过程中产生的氧自由基(OFR),是维持细胞中还原型谷胱甘肽(GSH)含量的主要黄素酶。
对保护肝细胞膜完整具有非常重要的作用意义。
在《临床肝病实验诊断学》和《临床检验诊断解析》中明确标示,血清谷胱甘肽还原酶活性测定可用于协助诊断肝脏疾病,血清谷胱甘肽还原酶活性上升可以辅助诊断肝炎、肝硬化、梗阻性黄疸及相当数量引发的肝肿瘤。
原发性肝细胞癌和广泛转移性肝肿瘤时,血清谷胱甘肽还原酶活性明显升高,急性病毒性肝炎或中毒性肝炎中度升高,而肝硬化是血清GR轻度升高。
二:检测谷胱甘肽还原酶的临床意义
1、急性肝炎早期阶段,血清谷胱甘肽还原酶敏感性最高,可用于肝损的早期检测;
2、急性肝炎患者GR比转氨酶更早增加达到峰值,早早期肝脏损伤判断的首选指标;
3、GR有助于判断亚临床DILI,提高临床DILI的诊断率
4、不同于ALT和AST在肝细胞膜破裂和线粒体破裂时才能检测出来,GR填补肝细胞受损早期自我修复阶段至破裂进程中诊断的空白,将更有利于早期肝炎的诊断和治疗
三、临床解读:
谷胱甘肽和谷丙、谷草在化验单上的具体解读,谷胱甘肽的血清血浆正常值是33-73U/L,共有四种情况。
1、谷胱甘肽指标升高,谷丙和谷草指标正常,提示有肝损伤的风险,建议加强对肝脏的检测频率,有利于发现早期肝损伤。
2、谷胱与谷丙,谷草同时升高,提示进入肝损伤爆发期,建议临床治疗措施干预。
3、谷胱甘肽升高,谷丙、谷草下降,提示正在进行肝损伤修复,可以结合三者评估临床治疗情况。
4、当三者都出现下降,情况有两种极端提示:(1)是修复完成,临床好转。
(2)是重型肝炎出现严重情况,出现胆酶分离现象。
另外一种是红细胞的检测,正常值4.7-13.2U/gHb
红细胞主要针对“蚕豆病”和遗传性伯氨喹溶血病人,谷胱甘肽还原酶降低,红细胞的细胞膜容易被氧化和分解,导致溶血性贫血和溶血性黄疸。
