第六章氨解反应
第六章氨解反应

Cl
NH2
+ 2NH3
+ NH4Cl
NO2
NO2
对硝基氯苯的氨解历程 :
Cl
Cl NH3
NH3
慢
快
+ 2NH3
NO2
N
NO2
OO
NH3
NH2
快
+NH3 , - NH4
NO2
NO2
芳胺与2,4-二硝基卤苯的反应历程:
X NO2
ArNH2 +
NO2
X NH2Ar NO2
N OO
NHAr NO2 + HX
+
HN + H2O
H2N
O
+
布赫勒(Bucherer)反应。
OH + NH3
NaHSO3
NH2 + H2O
主要用于从2-萘酚磺酸制备2-萘胺磺酸。
Bucherer反应羟基被置换难易的规律。
① 羟基处于1位时,2位和3位的磺基对氨解 反应起阻碍作用,而4位磺基促进反应的进 行。
②羟基处于2位时,3位和4位的磺基对氨解 起阻碍作用,而1位磺基则使氨解反应容易 进行。
RY + NH3
胺化
R-NH2 + HY
常见制备方法: 1. 脂肪族伯胺的制备: 醇羟基的氨解和胺化法; 羰基化合物的胺化氢化法; 脂链上卤基氨解法。 脂肪烃基酰胺或脂腈的加氢法。 2. 芳伯胺的制备: 硝化还原法 芳环上取代基的氨解法:卤基的氨解、酚羟基
的氨解、磺基或硝基的氨解。
ArSO3Na + 2NaNH2 ArNHNa + H2O
ArNHNa + Na2SO3 + NH3 ArNH2 + NaOH
第六章_氨解反应

HH NH2 SO3NH4
NH4HSO3
1-2 MPa
6.3.2 酚类的氨解
气相氨解法:
催化剂(硅酸铝),气态酚类与氨进行的气固相催 化反应
液相氨解法:
酚类与氨水在SnCl2,AlCl3,NH4Cl下,在高温高压 下反应
酚类典型的重要的氨解-苯酚的气相氨解法
特点: 可逆 , 放热, 采用较高浓度的氨和 苯酚摩尔比对反应有利。
2-萘酚的氨解
N-苯基-2-萘胺,防老剂丁
6.3.3 亚硫酸盐存在下的氨解
萘酚与萘胺在酸式亚硫酸盐存在下引起的可逆变化, 称布赫尔(Bucherer)反应。
醇式 互变异构 酮式 NH4HSO3
加成
醇式加成物
+NH3 氨解
胺式加成物
-NH4HSO3 消除
萘胺
1.加上两个亚硫酸氢铵 2.与氨发生氨解 3.脱去两个亚硫酸氢铵
•ROH:醇、酚和羟基蒽醌
•反应可逆
•凡是羟基化合物或相应的氨基化合物愈容易变
成酮式或相应的酮亚胺式互变异构体时,则上
述反应愈容易进行。如萘的衍生物比苯的衍生
物易发生反应。
6.3.1 醇类和还氧烷类的氨解
1.醇类的氨解 (制备低级胺常用方法)
ROH
NH3 -H2O
ROH
RNH2 -H2O
ROH
R2NH -H2O
生产实例 (1)硝基苯胺类的制备(非催化)
NH2 NO2
NH2 NO2
NH2 NO2
NO2
NH2
NH2
NO2
Cl
Cl
NO2
(2)2-氨基蒽醌
O
Cl + 2NH3
CuSO4,210-218oC
06 第六章 氨解

1
2、液相氨解法 酚类与氨在氯化锡、三氯化铝、氯化铵等催化剂 存在下于高温、高压下制取胺类
N H 2 O H N H C l 2 H H N
O
OH
O
NH2
NH3
O OH
Na2S2O4或 Zn粉 H3BO3
O NH2
O
NH2
氧化剂
1
O
NH2
3、Bucherer反应 某些萘酚衍生物在酸式亚硫酸盐存在下,在较温 和的条件下与氨水作用转变为萘胺衍生物的反应,称 为布赫勒(Bucherer)反应。Bucherer反应主要用于 从2-萘酚磺酸制备2-萘胺磺酸。其反应可表示如下:
3
二、氨解剂
在反应中提供氨基(或芳胺基)的物质称为氨解剂, 常用的氨解剂有液氨和氨水。 1. 液氨 如果有机化合物在反应温度下是液态的,或者氨 解反应要求在无水有机溶剂中进行,则需要使用 液氨作氨解剂。用液氨进行氨解反应的缺点是: 操作压力高,过量的液氨较难再以液态氨的形式 回收。
4
C l C N N O 2 2 N H + 3
N ( C H 2 C H 2 O H ) 3
2
第三节 羰基化合物的氨解
一、醛酮的氨解
第六章
氨解
Ammonolysis
1
主要氨解方法
• • • • • 卤代烃氨解 羟基化合物氨解 羰基化合物氨解 磺基氨解 硝基氨解 硝基还原
2
胺 制 备 方 法
第一节 概述
一、氨解反应及其重要性
• 氨解指的是氨与有机物发生复分解反应而生成伯 胺的反应。 • 合成胺类化合物目的: • 胺类化合物是一类重要的有机化工产品,具有广 泛的用途,除可用作矿石浮选外,还广泛用于表 面活性剂工业。此外,胺类也是一类重要的有机 中间体,通过它可制得阳离子表面活性剂或相转 移催化剂等,某些芳胺与光气反应制成的异氰酸 酯是合成聚氨酯的重要单体。
精细有机合成单元反应(陈志)06 氨解反应-文档资料

2.卤素衍生物的活泼性
通过取代基的强吸电子作用而对负离子中间物的 稳定效应只能通过共轭效应来产生。
Cl
Cl
~ <<
NO2
Cl
Cl
NO2 O2N
<
<
NO2
NO2
Cl NO2
NO2
3. 溶解度与搅拌: 要求配置良好的搅拌器,保证良好的传热和传质。
否则,因为卤化物密度较大,氨水会上浮。
4. 温度
提高温度可加快氨解反应速度。一般来说,温 度升高10 ℃,反应速度常数将提高 0.6倍左右。
HH OH
SO3NH4
醇式加成物
+NH3 氨解
HH NH2 SO3NH4
NH4HSO3
胺式加成物
-2NH4HSO3
HH
NH 互变异构
NH2
亚胺式
萘胺
6.3 羰基化合物的氨解
氢化氨解
RCHO + NH3 RCHOHNH2 - H2O
RCHOHNH2
+ H2 - H2O
RCH2NH2
RCH NH + H2 RCH2NH2
第六章 氨解反应
(Ammonolysis and Amination)
本章教学目标:
1.熟悉氨解反应的定义、氨化试剂及方法。 2. 掌握卤素的氨解反应理论及影响因素。 3. 熟悉羟基化合物的氨解反应。 4. 掌握羰基化合物的氨解及霍夫曼重排。 5. 了解磺酸基和硝基的氨解以及直接氨解
本章教学重难点:
R=烷基、芳基;Y=OH, Cl, SO3H, NO2
氨解反应的类型
卤素的氨解;羟基化合物的氨解;羰基化合物的氨解; 磺基及硝基的氨解;直接氨解
(优化版)6-胺解反应

+
N H
+
N X
X:C 或 N
哌嗪
(B)
表 N-苄基哌嗪的合成 条件一 卤代芳烃 条件二
27.5 mmol哌嗪
50 mmol哌嗪
A收率
t/min A收率 B收率 总收率 t/min
S 非催化胺化
催化胺化
kOP kOS
T 图 胺化反应选择性随温度的变化
1.2 催化胺解的温度效应
低温有利于胺化反应,高温有利于水解副反应。
2、浓度效应
① 氨(胺)浓度越高越好;
② 水浓度越低越好;
③ 实验表明,卤代芳烃的浓度与选择性无关。 总结:无水条件和氨(胺)%的过量有利于胺解。
三、氨(胺)解反应的影响因素 1、氨(胺) 的浓度
3、原料的回收
若采用胺过量的工艺,一般应以胺易回收为前提。一 般情况下,胺解产物总是质量增大,不易挥发,原料胺如
易挥发,可在碱性条件下用共沸回收胺。
4、反应温度与压力
非催化胺解:胺解可在较宽的温度范围内进行,温度 对选择性影响不大; 催化胺解:升高温度对水解有利,温度过高也会生成 少量二芳胺。故应避免高温。
氨(胺)/水比越大,越有利于氨(胺)解反应。 增加氨(胺)/水的途径: ① 增加氨(胺); ② 减少水;
2、胺的用量与溶剂
以K2CO3、Na2CO3为缚酸剂时,溶剂较重要。胺在不 同介质中稳定性为:碱性>中性>酸性; 极性>非极性。故
用碱性或中性的非质子极性溶剂可避免或减少碳酸盐的分
解而生成水,也就减少了卤代芳烃的水解。 过量胺为溶剂,既增加了胺,又减少了水。
氨解反应

2.芳香卤化物的氨解反应:
需要强烈的条件(高温、催化剂和强氨解 剂)才能进行反应。
芳环上带有吸电子基团时,反应容易进行, 反应的活泼顺序是:F》Cl ≈ Br > I。
3. 卤代衍生物在醇介质中氨解的途径。
C6H13HN
(a)
NO2
Cl NO2 + C6H13NH2
NO2
NO2
OCH3
(b)
O + NH3
NH
HO
+
HN + H2O
H2N
O
+
布赫勒(Bucherer)反应。
OH + NH3
NaHSO3
NH2 + H2O
主要用于从2-萘酚磺酸制备2-萘胺磺酸。
Bucherer反应羟基被置换难易的规律。
① 羟基处于1位时,2位和3位的磺基对氨解 反应起阻碍作用,而4位磺基促进反应的进 行。
Cl 浓 H2SO4
+ NH2OH 120℃,V2O5
Cl NH2
SO3H
当卤苯与羟胺在浓硫酸介质中以V2O5为催 化剂在120℃反应时,环上将同时引入氨基 和磺酸基。如3-氨基-4-氯苯磺酸的制 备(产率84%):
(2)碱式法:在碱性介质中进行反应。
NH2
NH2
+
+ (NH4)2SO4
H2N O
SO3Na
四、羰基化合物的氨解
1. 氢化氨解 醛和酮等羰基化合物在加氢催化剂的存在
下,与氨和氢反应可以得到脂胺。其反应 过程与醇的胺化氢化相同。 对于低级脂肪醛的反应,该反应可以在气 相进行。 对于高沸点醛酮,常在液相进行。
反应过程:
第章氨解反应

H+ 酸化
HO3S
NH2
OH J-酸
• Bucherer反应应用实例2:
OH 发烟硫酸,70~80oC
SO3H OH
二磺化
HO3S G酸
+ HO3S
OH
SO3H R酸
SO3K
KCl
OH
KO3S
G盐
+ KO3S
碱熔 NaOH,250oC
ONa NaO3S
ONa 18%NH3,(NH4)2SO4 氨解
1.非催化氨解 SN2
氨解剂:25%氨水
反应历程:亲核置换反应
非催化氨解:
O2N
Cl 2NH3 aq O2N
NH2
V非催化氨解 = k [ArX] [NH3],因C-X键断裂对反应速度没 有明显影响
Cl
NO2
NH3 aq slow
Cl NH3+ fast -Cl-
-O N+O-
NH3+
NO2
fast +NH3, -NH4+
• Bucherer反应应用实例1:
H2SO4,160oC 磺化
SO3H NaOH 碱熔
ONa H+ 酸化
OH 发烟硫酸 低温磺化
SO3H NH2
发烟硫酸 二磺化
SO3H OH
NH3,NH4HSO3 氨解
SO3H NH2
吐氏酸
HO3S
SO3H NH2
H+
HO3S
NH2
SO3H
水解
SO3H
NaOH 碱熔
1.碱性介质中以羟胺为胺化剂旳直接氨解
2.芳烃用氨旳催化氨解
苯或其他同系物用氨在高温、催化剂存在下可气 相催化氨解为苯胺
第六章 氨解反应

6.3 羟基化合物的氨解
对于某些胺类,如果通过硝基的还原或其他方法来制备并不 经济,而相应的羟基化合物有充分供应时,则羟基化合物的氨解 过程就具有很大的意义。胺类转变成羟基化合物以及羟基化合物 转变成胺类为一可逆过程:
凡是羟基化合物或相应的氨基化台物愈容易转变成酮式或相应的酮
亚胺式互变异构体时,则上述反应愈容易进行。所以,例如荼的
霍夫曼重排反应的过程虽很复杂,但反应产率较高,产物较纯。
例如以邻苯二甲酸酐为原料,通过霍夫曼反应,可制备偶氮染料及
硫靛染料的中间体邻氨基苯甲酸。其反应过程如下:
低温
邻酰氨基苯甲酸钠盐 0℃
邻氨基苯甲酸
例以对二甲苯为原科,经液相空气氧化为对苯二甲酸,再经氨化、霍
夫曼重排得对苯二胺:
反应可在常压、常温下进行,收率达90%,开辟了合成胺类的新原料 来源,而且三废量少,是值得注意的合成对苯二胺的方法。此外,也 可由对硝基苯甲酸制取对硝基苯胺,常压下收率为84%。
由不饱和醛经氢化氨解可制得饱和胺:
利用苯甲醛与伯胺反应,再加氢,此法只生成仲胺。例如N-苄 基对氨基酚的制备:
6.2.2 霍夫曼重排 酰胺与次氯酸钠或次溴酸钠反应,失去羰基,生成减少一个碳 原子的伯胺,这一反应称霍夫曼(Hofmnnn)重排反应,它是出羧酸 或羧酸衍生物制备胺类的重要方法。 霍夫曼重排反应包括了异氰酸酯中间体的生成,其反应历程可 表示如下:
引入磺基是为了提 高氯原子的活泼性 及增加水溶性
6.2 羰基化合物的氨解
6.2.1 氢化氨解 在还原剂存在下,羰基化合物与氨发生氢化氨解反应,分别生 成伯胺、仲胺或叔胺。对于低级脂肪醛的反应,可在气相及加氢催 化剂镍上进行,温度125℃~150℃;而对高沸点的醛和酮,则往往 在液相中进行反应。当醛和氨发生反应时,包括了生成醛-氨的氢化 过程或从醛-氨脱水生成亚胺并进一步氧化的过程,见下式:
(6)氨解反应

25
吐氏酸
α-萘酚经低温磺化,生成2-萘酚-1-磺酸,而1位磺酸基使2位羟 基易氨解。 γ酸 3位磺酸基使1位羟基难氨解,对7位羟基的氨解无影响。
26
6.5 羰基化合物的胺化氢化
羰基化合物的胺化氢化主要用于从丙酮、甲乙酮等制备相 应的脂肪胺。主要用骨架镍或Ni/Al2O3等催化剂,可用气-固 相法或液相法。其过程与醇的胺化氢化相同。
第六章
氨解和胺化
6.1 卤素的氨解 6.2 醇羟基的氨解 6.3 环氧烷类的加成胺化 6.4 芳环上羟基的氨解 6.5 羰基化合物的胺化氢化 6.6 霍夫曼重排 6.7 芳环上磺基、硝基的氨解
第六章
氨解和胺化
利用胺化剂将已有取代基置换成氨基(芳氨基)的 反应称为氨解反应。
R-Y+ NH 3 R-NH 2 + HY ( Y = -OH, -X, -SO 3 H, -NO 2 )
+
O
N H 2O H
N
浓 H 2S O 4
N
34
NH2
13
14
6.2 醇羟基的氨解 醇羟基的氨解是制备C1~C8低碳脂肪胺的主要方 法。
醇羟基的氨解是可逆连串反应,根据市场需 要,调整伯、仲、叔三种胺类的相对产量,可控 制氨和醇的摩尔比和其他反应条件,并将需要量 小的氨循环回反应器。醇羟基不够活泼,需要较 强的氨解条件。 工业上主要有三种方法:气-固相接触催化
11
从氯乙酸制氨基乙酸 α-卤代酸容易与氨水反应生成α-氨基酸。 从氯乙酸制氨基乙酸是连串反应,为了减少仲胺 或叔胺的生成,要用过量很多的氨水,而且要用六 亚甲基四胺等催化剂。
12
6.1.4 芳氨基化 它是以芳胺为胺化剂与卤素衍生物进行胺化,生成 芳胺的反应,反应中常加入缚酸剂MgO、Na2CO3
精细有机合成单元反应06 氨解反应共39页文档

39、没有不老的誓言,没有不变的承 诺,踏 上旅途 ,义无 反顾。 40、对时间的价值没有没有深切认识 的人, 决不会 坚韧勤 勉。
66、节制使快乐增加并使享受加强。 ——德 谟克利 特 67、今天应做的事没有做,明天再早也 是耽误 了。——裴斯 泰洛齐 68、决定一个人的一生,以及整个命运 的,只 是一瞬 之间。 ——歌 德 69、懒人无法享受休息之乐。——拉布 克 70、浪费时间是一桩大罪过。——卢梭
第六章氨解反应讲义

(2)卤素衍生物的活泼性 不同卤素的氨解反应速度有较大的差异, 卤萘中卤原子的活泼性比相应的卤苯要高许多,荼衍生物反应的较大 速度是由其较低的活化能所决定的。而在非催化氨解反应中,氟的置 换反应速度大大超过氯和溴,氯和溴又比碘容易些,卤素衍生物的置 换速度随卤素性质按下列顺序变化:
卤化物上已有取代基对反应速度也有很大影响,通过取代基的强吸电 子作用而对负离子中间物的稳定效应只能通过共轭效应来产生,例
例如邻或对硝基氯苯与氨水溶液加热时,氯被氨基置换,反应按
下式进行:
硝基氯苯的氨解反应属于亲核置换反应,反应分两步进行, 首先是带有未共用电子对的氨分子向芳环上与氯相连的碳原子发 生亲核进攻,得到带有极性的中间加成物,此加成物迅速转化为 铵盐,并恢复环的芳香性,最后再与一分子氨反应,即得到反应 产物;速度决定步骤是氨对氯衍生物的加成。对硝基氯苯的氨解 可用下列方程描述:
(2)催化氨解 氯苯、1-氯荼、1-氯荼-4-磺酸和对氯苯胺等,在没有铜 催化剂存在时,在235℃、加压下与氨都不会发生反应;然而在有铜催 化剂存在时,上述氯衍生物与氨水共热至200℃时,就都能反应生成相 应的芳胺。在氨解反应的动力学研究中已指出:反应速度直接正比于 铜催化剂和氯衍生物的浓度,而与氨水浓度无关,因此,可设想反应 是分两步进行的:第—步是由催化剂和氯化物生成加成产物,即生成 一正离子结合物,这是反应速度决定步骤:
如硝基只对邻位和对位离去基团有作用,氨解反应的活泼性顺序为:
(3)溶解度与搅拌 在液相氨解中,胺化速度取决于反应物质的均一 性,在不采用搅拌时,由于氯化物的密度较大而会沉到加热釜底部, 而氨水溶液却在上面成为明显的一层,反应只会在有限的界面上发 生。影响了反应的正常进行和热量的传递,因此,在间歇氨解的高 压釜中,要求装配良好的搅拌器,在连续管式反应器中,则要求物 料呈现湍流状态,以保证良好的传热和传质。 卤素的氨解反应是在水相中进行的,提高卤素衍生物在氨水中 的溶解度,能加快氨解反应速度,当增加氨水浓度或提高反应温度 时,都可促进溶解。
第六章 氨解反应讲解

如氯苯氨解:
[PhNH 2 ] [PhOH ]
K
[NH 3 ] [OH ]
K k1 k2
NH3的浓度增加,副产物酚和二芳胺都减少。
§6.2 有机卤化物的氨解 § 6.2.1 反应理论 (3)用氨基碱氨解
材料学院·应用化学
Cl
*
KNH2, NH3
-HCl
NH2
* +
* NH2
48%
52%
strong base
CH3 H3C
CH3
Br
Br
I
§6.2 有机卤化物的氨解 反应机理的证明
材料学院·应用化学
实验和光谱证明苯炔中间体的存在。
Diels-Alder反应 O
OH H+ O MeOH
§6.2 有机卤化物的氨解 反应机理的证明
材料学院·应用化学
OCH3
NH2Br -NH3
OCH3
KNH2, NH3
材料学院·应用化学
第六章 氨解反应
§6.1 概述 §6.2 有机卤化合物的氨解 §6.3 羟基化合物的氨解 §6.4 羰基化合物的氨解 §6.5 磺基及硝基的氨解
§6.6 直接氨解
§6.1 概述
引入氨基的方法
材料学院·应用化学
(1)硝化还原
[H]
Ar NO2
Ar NH2
(2)氨解法
Ar Cl Ar OH Ar SO3H Ar NO2 Ar H
不够活泼,需要很强反应条件,用铜盐或亚铜
盐作催化剂。
Cl 200℃
+ 2NH3 CuCl NH2
NH2 + NH4Cl
NH2
§6.2 有机卤化物的氨解 b. 反应机理
第六章氨解反应

NH4Cl
实际应用中:间歇氨解时,氨比为6~15.
连续氨解时,氨比为10~17.
原因:
增加氨水用量能提高氯化物的溶解量,改进
反应物的流动性,减少副产品(如二芳胺)的 生成。 过量胺的存在,可减少生成的NH4Cl对设备 的腐蚀。 但用量太大,会增加回收氨的负荷而降低生 产能力。
非催化氨解反应速度正比于卤素衍生物和氨水
O2N NO2
X
+
HN
O2N NO2
N
X= 相对速度 键能:
F 3300
Cl 4.3
Br 4.3
I 1
C-F > C-Cl > C-Br > C-I
结果说明:C-X键的断裂对反应速度没有明显的影响。
推测机理如下:
O2N
X NO2
+
HN
+
N NO2
O2N NO2 X O2N
+
HN
NH NO2 O2N
(3)Hoffmann降解法
ArCOOH
NH3 -H2O NaBrO
ArCONH2
NaOH
ArNH2
(4)羧酸还原法
NH3 -H2O 还原
ArCOOH
ArCONH2
ArCH2NH2
(5) 环氧乙烷和氨/胺加成
O
+
NH3
HO CH2 CH2 NH2
(6) 含氮环和氨/胺加成
N H
+
NH3
H2N CH2 CH2 NH2
适用活性不强的卤素衍生物 常用铜催化剂
反应可能分两步:
(1)催化剂和氯化物生成加成物―正离子络合物
ArCl + Cu(NH3)2+ ArCl· Cu(NH3)2+
6 氨解反应

(3)用氨基碱的氨解
Cl * KNH2,NH3 - HCl NH2 * * NH2
+
48% 52%
苯炔反应历程:
* X
+
H
NH2
* X - X H3 *
*
+ NH2
-
- NH3
NH2
* NH2 或
*
NH2 +
NH2
(A)支持该理论的直接证据是下列化合物不 与KNH2反应。
CH3 H3C H3C Br CH3 H3C Br CH3 CH3 H3C I CH3
O Cl O
CuSO4 10h
O
NH2
204℃~ 206℃
O
氨比 17.5
yield 90%
6.1.4 脂肪族卤素衍生物的氨解
ClCH2CH2Cl
+ 2 NH3
100℃~ 180℃
H2 NCH2CH2 NH2
ClCH2COOH
NH3 H2NCH2COOH
6.1.5 芳胺基化
以芳胺为胺化剂与卤素衍生物进行胺化的反应。
}
溶解度 ↑
连续式: 管道中流体呈湍流状态。
(4)温度
(A)对反应速度的影响 温度升高,增加ArX在氨水中的溶解度, 同时提高反应速率常数。提高反应速度。 邻硝基氯苯
4682 logk邻 7.20 0.01 T
2-氯蒽醌
4467 logk 6.26 T
(B)温度过高
设备要求高(相应压力高);增加副产物, 出现焦化现象;反应过快,造成危险。
(B)发生Diels-Alder反应。
OH O
+O
H
+
CH3OH
6氨解反应

– 减少副产品二芳胺的生成
– 中和酸性氯化铵减小对设备的腐蚀性 – 用量过大增加回收氨的负荷,降低生产能力。
(B) 浓度
• 动力学表明非催化氨解反应速率正比于氯化物和 氨水的浓度; • 通常用较大浓度,原因: – 提高氯化物溶解度 – 加快反应 – 可以使反应完全,抑制仲胺、叔胺及羟基化合 物生成
k1 K k2
结论:副产物酚的生成随氨浓度的增加而减少!
6.1.1.3 用氨基碱氨解
• 提高胺化剂的亲核能力,可能不用催化剂。 • 例如,用KNH2 在液氨中进行活泼氯代苯的氨解 反应,可以得到约50%的产率。反应为苯炔机理:
CH3 + NH2Cl 液氨 + -33 C NH2 38%(预期) 62%(非预期) CH3 CH3 + ClNH2
ArCOONH2
H2O
ArCONH2
还原
ArCH2NH2
本章内容
6.1 卤素的氨解 6.2 羟基化合物的氨解 6.3 羰基化合物的氨解
6.4 磺基及硝基的氨解
6.5 直接氨解
6.1 卤素的氨解
6.1.1 反应理论
• 按卤素化合物活性可分为:
– 非催化氨解:活泼离去基团 – 催化氨解:不活泼离去基团
H3C I
CH3
• 邻位氢原子是生成苯炔中间体的必要因素。
化学证据
苯炔是高活性中间物; 苯炔类中间物没有真正被分离出来; 已证明苯炔类中间物的存在。
OH Diels-Alder反应 O O H+ MeOH
6.1.2 影响因素
(1)胺化剂
(A)氨比:氨解时所用的氨与芳香氯化物的摩尔比。 原因: – 增加氨水能提高氯化物的溶解度 – 改进反应物料的流动性
06 第六章 氨解

OH
+ NH3
NaHSO3
NH2
+ H2O
1
该反应是可逆反应。其羟基被置换的难易符合以下 规律: • (1)当羟基处于1位时,2位和3位的磺基对氨解 反应起阻碍作用,而4位上存在的磺基则使反应容 易进行; • (2)当羟基处于2位时,3位和4位的磺基对氨解 起阻碍作用,而1位的磺基则能使氨解反应容易进 行; • (3)当羟基与磺基不在同一环上时,磺基对羟基 的氨解影响很小。
RCHO
RCH=NH
RCH2NH2
2
二、酰胺的降解(Hofmann重排)
该反应收率高;产品纯度好,只有伯胺生成,副反 应少。
RCH2CONH2
O R
NaClO 或 Cl2-NaOH
O
RCH2NH2
C
NH2
+X2 - HX
O R
O
C
OH
NHX
-H2O
R
C
N
X
R
C
N
R
N
C
O
+ H2O
RNH2
CO2
2
利用霍夫曼重排反应制胺的优点是:产率高,产物纯。 工业生产中常用于染料中间体的生产。例如
该方法目前应用于苯胺、甲基苯胺的工业生产。相 比硝基还原,该方法投资少,三废少,它与硝基还原法 的比较取决于苯酚的价格。
OH
NH2
催 化 剂 Al2O3 NH3 H2O
1
2、液相氨解法 酚类与氨在氯化锡、三氯化铝、氯化铵等催化剂 存在下于高温、高压下制取胺类
NH2 OH NH2
HCl
H N
O
OH
O
Cl + 2 NH3 NO2
氨解反应
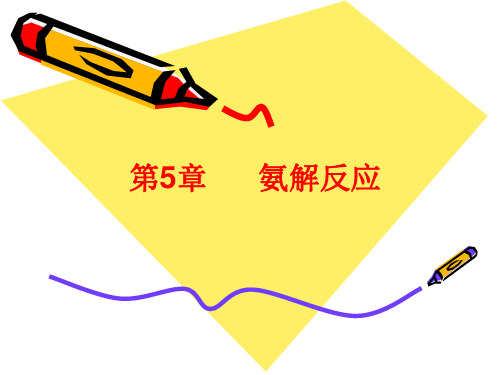
k萘/k苯
171 118 162 11.3
在非催化氨解反应中卤素衍生物的置换反应 速率随卤素性质按以下顺序变化: F>>Cl ,Br>I
⑵搅拌(与溶解度) 无搅拌时相对密度较大的不溶性有机底物沉积在 反应器低部,反应将在两相界面发生。 对间断反应设备,要求安装有效的搅拌装置;对 连续反应设备,控制流速使反应物料形成湍流状态。 对微溶有机物的氨解尤为重要。 ⑶氨水浓度与用量 芳香氯化物氨解时所用的氨的摩尔比称为氨比,理 论氨比为2,实际大大过量。用量提高,对反应有利, 反应物在氨水中的溶解度增加,仲胺副产物下降,设 备腐蚀性减小。通常间断氨解用量6~15mol;连续氨 解用量10~17mol。用量过多,会增加回收负荷,生产 能力降低。
⑴卤化物性质 ①取代基性质:含强吸电子基团,反应活性增加; 含有给吸电基团,反应活性下降。
Cl + 2NH3 Cl + 2NH3 NO2 Cl NO2 + 2NH3 NO2
115~120OC,常压 30%氨水 170~190OC,3~3.5MPa 30%氨水,无催化剂 200~300OC,7MPa 30%氨水,0.1molCu+
NH2 + NH4Cl NH2 + NH4Cl NO2 NH2 NO2 + NH4Cl NO2
②卤素(离去基团)活性
2,4-二硝基卤萘和2,4-二硝基卤苯与苯胺的反应速率
氨解反应

③减少对设备的腐蚀(25℃,pH=4.7)
HX + NH3
腐蚀
NH4X
但太大会增加回收氨的负荷,并降低生产能力。
6.2 卤素的氨解
反应影响因素 (3)温度:
温度升高→反应速度加快 温度升高,压力升高,设备要求跟更高; 氧化副反应速度加快,甚至出现焦化现象; NH3的溶解度降低,反应压力增加。 还会影响氨水的pH值。 (4)搅拌: 非均相反应,加速搅拌有利于传质。
H H ONSHHO23NH4
H
H
H SO3NH4
胺式加成物
HH O
H
H
H SO3NH4
酮式加成物
HH OH
SO3NH4
醇式加成物
+NH3 氨解
HH NH2 SO3NH4
NH4HSO3
胺式加成物
-2NH4HSO3
HH
NH 互变异构
NH2
亚胺式
萘胺
6.3 羟基的氨解
• Bucherer反应应用实例1:
• 醇类的氨解(制备低级胺常用方法)
ROH
NH3 -H2O
ROH
ROH
RNH2 -H2O R2NH -H2O
R3N
工艺方法
气固相接触催化氨解 高压液相氨解 气固相临氢接触催化胺化氢化
6.3 羟基的氨解
• 醇类的氨解(制备低级胺常用方法) • 气固相接触催化氨解法
(1)应用:如甲醇氨解制一甲、二甲和三甲胺; (2)催化剂(脱水):SiO2/Al2O3; (3)温度:350~500℃; (4)压力:0.5~5MPa。
缺点:多某些芳胺溶解度小,有水 解副反应。
其它试剂:氨气、铵盐、有机胺(伯、仲、叔胺)
氨解反应

氨解反应氨解反应是指含各种不同官能团的有机化合物在胺化剂的作用下生成胺类化合物的过程。
氨解反应包括卤素的氨解、羰基化合物的氨解、羟基化合物的氨解、磺基及硝基的氨解和直接氨解。
1定义氨解反应是指含各种不同官能团的有机化合物在胺化剂的作用下生成胺类化合物的过程。
可氨解的基团:-X,―OH,―SO3H,―CO―,Ar―H。
胺化剂:液氨、氨水、尿素、铵盐(NH3的来源)及有机胺。
合成胺类化合物的方法:反应类型,还原、氨解,水解,加成和重排。
芳胺的两大制法,硝基还原(经济、方便)和芳环卤素氨解。
包括:卤素的氨解、羟基化合物的氨解、羰基化合物的氨解、磺基及硝基的氨解和直接氨解。
2卤素的氨解7.2.1 反应理论根据反应物的活泼性的差异,可分为非催化氨解和催化氨解(1) 非催化氨解:对于活泼的卤素衍生物,如芳环上含有硝基的卤素衍生物,用氨水处理时,就可以使卤素被氨基置换。
虽然不含磺基的芳香化合物在氨水中很难溶解,但大多数反应仍能在水相中进行,因为随着温和氨浓度的提高,氯化物在氨水中的溶解度会增大。
ClNO2+NH3NH3ClNOO慢快-ClNH3NO2NH2NO2-H反应历程X +ArNH2NH2ArX NO2NO2NHAr反应属于SN2历程,双分子亲核取代反应,首先是带有未共用电子对的氨分子向芳环与氯相连的碳原子发生亲核进攻,得到带有极性的中间加成物,此加成物迅速转化为铵盐,并恢复环的芳香性,最后脱掉质子,得到产物。
第一步氨基衍生物的生成是决速步骤。
+HXNO2动力学方程式:dc/dt = k c’式中c’为二硝基氯苯的浓度,当NH3大大过量时,为假一级反应。
反应历程的证明:通过一系列具有不同离去基团的卤素衍生物与同一亲核试剂反应反应的速度相比,如2,4-二硝基卤代苯和哌啶反应:XO2NNO2+NHNHO2NNO2X当X为F、Cl、Br、I时,反应相对速率为:3300,4.3,4.3,1.0。
证明C-X键的断裂对反应速率没有影响,否则C-X键的断裂为决速步骤,C-I的键最弱,反应速率为VRI>VBr>VRCl>VF。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4. 温度
升高温度可以加快氨解反应速度。
但温度升高是有限度的:一方面会对设备提出
更高的要求。另一方面温度过高会加剧副反应, 甚至出现焦化现象。
温度还会影响氨水的pH值。(T升高pH降低)
采用碳钢材质的高压釜进行间歇氨解时,反应温度一
般应低于170℃~190℃
三、芳香族卤素衍生物的氨解
非催化卤素氨解在苯系中最广泛应用的是制取硝
的浓度,氨水浓度增加,反应速度加快。
对于催化氨解反应,由于氨浓度增加,提高了
卤化物在氨水的溶解度,因而也加快了反应。 氨水浓度的增加对伯胺有利,可抑制仲胺、叔胺 及羟基化合物的生成。
但是由于受到溶解度的限制,配制高浓
度氨水比较困难。
2.卤素衍生物的活泼性
卤萘中卤原子的活泼性比相应的卤苯要高许多,所以其
O2N NO2
X
+
HN
O2N NO2
N
X= 相对速度 键能:
F 3300
Cl 4.3
Br 4.3
I 1
C-F > C-Cl > C-Br > C-I
结果说明:C-X键的断裂对反应速度没有明显的影响。
推测机理如下:
O2N
X NO2
+
HN
+
N NO2
O2N NO2 X O2N
+
HN
NH NO2 O2N
(3)Hoffmann降解法
ArCOOH
NH3 -H2O NaBrO
ArCONH2
NaOH
ArNH2
(4)羧酸还原法
NH3 -H2O 还原
ArCOOH
ArCONH2
ArCH2NH2
(5) 环氧乙烷和氨/胺加成
O
+
NH3
HO CH2 CH2 NH2
(6) 含氮环和氨/胺加成
N H
+
NH3
H2N CH2 CH2 NH2
H N + H2O
N-苯基-2-萘胺
防老剂丁,橡胶工业中的重要防老剂。
3.亚硫酸盐存在下的氨解
H2SO4 160 C
o
SO3H (1)NaOH
基胺类及其衍生物。
随着芳环上吸电子数目增加,反应条件可由加压和高
温(200℃)而逐步降到常压和100℃左右。
例如:
Cl NO2 氨比 8 170℃~175℃ 7h NH2 NO2
98%
高压管道法生产邻硝基苯胺的流程:
氨比15,225℃~230℃
阳离子染料的重要中间体N-甲基苯胺的制备。
O2N
Cl SO3Na
H2N
OCH3
O2N
H N
OCH3
MgO, 170℃, 0.65MPa
SO3Na
40%H2SO4 ~ 120℃
O2N
H N
OCH3
[H]
H2N
H N
OCH3
安安蓝B色基
反应中常加入缚酸剂MgO(或碳酸钠等)以中和酸性。 引入磺酸(盐)基是为了提高氯的活泼性及增加水溶性。
O Cl Cl ArNH2
+ (CH3)2CHNH2
(CH3)2CHNHCH(CH)2 3
2.环氧烷类的氨解
环氧乙烷、环氧丙烷等在氨作用下采用液相氨
解方法,容易转变成烷基醇胺类。
O + NH3 HO-CH2CH2-NH2
O
+ HO-CH2CH2-NH2
NH(CH2CH2OH)2
O
+ NH(CH2CH2OH)2
N(CH2CH2OH)3
适用活性不强的卤素衍生物 常用铜催化剂
反应可能分两步:
(1)催化剂和氯化物生成加成物―正离子络合物
ArCl + Cu(NH3)2+ ArCl· Cu(NH3)2+
速度决定步骤
(2)正离子络合物提高了氯的活泼性,很快与氨、 氢氧离子或芳胺发生反应
ArCl· Cu(NH3)2
+
+2NH3 k1
NH3上获取质子得到产物
*
+ NH2-
*
NH2
NH3
NH2 + NH2-
两步过程,是一个消除—加成的反应历程。
CH3
+
CH3
CH3
+ + Cl
NH2
液 NH3
Cl
NH2
NH2
从上述历程可知:邻位氢原子是生成苯炔中间体的 必要因素。
在相同条件下,下列卤化物不发生类似反应
Me
Me Me
Me Br
Me
Me Br
Me
Me I
Me
二、影响因素
1.胺化剂
常用的胺化剂可分为各种形式的氨、胺,以
及它们的碱金属盐,尿素、羟胺等。
对于液相氨解反应,氨水仍是应用量最大和应
用范围最广的胺化剂。其浓度和用量对反应有很 大影响。
胺比:卤素衍生物氨解时所用的氨的摩尔比
理论胺比为2.
Cl + 2NH3 NO2 NO2 NH2
ROH:醇、酚和羟基蒽醌 为放热反应
一、醇类和环氧烷类的氨解
1.醇类的氨解
RCH2OH + NH3 RCH2NH2 + H2O
ROH -H2O ROH RNH2 -H O 2
NH3
R2NH
ROH -H2O
R3N
气固相接触催化氨解
工艺方法 高压液相氨解 气固相脱氢接触催化胺化氢化
气固相接触催化氨解法 (1)应用:甲醇氨解制二甲胺; (2)催化剂:SiO2/Al2O3; (3)温度:350~500℃; (4)压力:0.5~5MPa。 高压液相氨解 (1)用于C8~10醇的氨; (2)催化剂:金属合金,如Cu-Al, Ni-Al, Cu-Ni-Al, Cu-Cr-Al等。
§6.1 卤素的氨解
一、反应历程 二、影响因素 三、芳香族卤素衍生物的氨解 四、脂肪族卤素衍生物的氨解 五、芳胺基化
一、反应历程
1. 非催化氨解
Cl + 2NH3 NO2 NO2 NH2
+
NH4Cl
芳环上含有硝基的卤素衍生物,通常以氨水处理时,可 使卤素被氨基置换。
2,4-二硝基卤苯与哌啶反应:
F O2N NH NO2
由于F是非常强的吸电子基,X=F时,使芳 环上连有F的碳原子的正电荷更强,因而更 易于亲核试剂发生反应,另外还有助于稳 定负离子。所以其相对速度达到3300.
卤素的氨解属于亲核置换反应 反应分两步
(1)带有未共用电子对的氨分子向芳环上与氯 相连的C原子发生亲核进攻,得到带有极性的中 间加成物。 (2)加成物迅速转化为铵盐,最后与一分子氨 反应,得到产物。
2HCl
往往得到的是伯、仲、叔胺的混合物,并有多胺生成。
同时会有脱去卤化氢的消除副反应发生。
甘氨酸(氨基乙酸)的合成:
ClCH2COOH
NH3
H2NCH2COOH
五、芳胺基化
以芳胺为胺化剂与卤素衍生物进行胺化,使卤
素转化为芳胺基。属于亲核置换反应。
安安蓝B色基的制备
发烟硫酸
O2N
Cl
115℃
以对硝基氯苯的氨解为例:
Cl
..
+ NH3 NO2
NH3 快
慢
Cl
NH3
O
N
O
快 -Cl-
NH2
+NH3 -NH4+ NO2 NO2
,
速度决定步骤是氨对卤素衍生物的加成。
芳胺与2,4-二硝基卤苯反应也是类似机理:
X ArNH2 + NO2 NO2 慢
X
NH2Ar NO2 N 快
NHAr + NO2 HX
3. 用氨基碱氨解
*
Cl KNH2, NH3 -HCl H *
NH2 + H
*
H
NH2
48%
52%
当氯苯用KNH2在液氨中进行氨解反应时,产物中有将近 一半的苯胺,其氨基是连结在与原来的氨互为邻位的碳 原子上。
首先发生消除反应形成苯炔中间体
*
Cl * + NH2H
X +
NH3
-X-
*
苯炔迅速与亲核试剂加成,产生负碳离子,从
氨比17.5,反应10小时,收率90%。 卤代蒽醌氨解速度与卤素的位置和反应介质极性有关。
四、脂肪族卤素衍生物的氨解
脂肪族卤素衍生物的氨解是制取脂肪胺的重要
方法之一,属亲核置换反应。
二氯乙烷与氨水反应可得到乙二胺:
ClCH2CH2Cl + 2NH3
100℃~180℃
H2NCH2CH2NH2 +
乙醇胺:表面活性剂、农药、医药、石油添加剂中间体、
酸性气体净化剂和水泥增强剂等。
二、酚类的氨解
工业上实现酚类氨解两种方法 A,气相氨解 :Cat(常为硅酸铝)、气态酚 与氨、气固相催化反应 B,液相氨解 :Cat(氯化锡、三氯化铝、氯 化铵等)、酚类与氨水、高温高压
1.苯酚的气相催化氨解
一些季铵盐是优良的阳离子表面活性剂或相转
移催化剂。
高分子材料(如聚氨酯)聚合单体的合成原料 。
4,氨解反应的类型
按被置换基团的不同:卤素的置换、羟基的置换、 磺基的置换、硝基的置换、羰基化合物的氨解和 直接氨解。
5,胺化剂
液氨、氨水、溶解在有机溶剂中的氨、气态的氨、 固体化合物(如尿素)放出的氨、各种芳胺。
OH NH3 NH2 + + H2O
工艺:
固定床绝热式反应器。 硅酸铝催化剂。 苯酚转化率95%,苯胺收率93%.
