第16章 1重氮--2
重氮化反应机理[优质内容]
![重氮化反应机理[优质内容]](https://img.taocdn.com/s3/m/58869a4daa00b52acfc7cad6.png)
(17) 对-甲氧基, 间-氨基苯磺酸
NH2 H3CO
SO3H
(20) 邻-X基联苯胺 [X=H,Cl,OCH3]
X H2N
SO3H X NH2
(18) 对-硝基, 邻-氨基苯甲醚 NH2
H3CO
NO2
(19) 间-硝基, 邻-氨基苯磺酸 NO2
SO3H NH2
精制课件
51
4、苯系中间体的合成途径
SO3H HO3S
SO3H
SO3H
(19) SS-酸
(20) γ-酸
(21) 2D-酸
(22) M-酸
(23) 加买酸
OH NH2 SO3H
SO3H
HO3S
OH
NH2 HO3S
OH
NH2 HO3S SO3H
NH2
OH
HO3S
NH2
OH
(24) J-酸
HO3S
(2)可以进一步合成其他化合物 试剂:脂肪酸、酸酐、酰氯、酯类
精制课件
42
三、氧化反应
两类氧化反应:
在氧化剂存在下,分子中引入氧原子,形成新 的含氧基团;
使有机分子失去部分氢。
CH3 [O]
CH2OH [O]
CHO [O]
COOH
精制课件
43
4,4‘-二氨基二苯乙烯-2,2’-二磺酸(DSD酸)
先引入氨基,然后转化成羟基,常用方法为酸性水 解,重氮盐水解
精制课件
39
(四)异丙基芳烃的氧化-酸解
主要用于生产苯酚。
精制课件
40
第四节 其他反应
一、考尔培反应
酚类化合物的钠盐与二氧化碳反应,在芳环上引 入羧基的反应。
精制课件
徐寿昌《有机化学》(第2版)名校考研真题(重氮化合物和偶氮化合物)【圣才出品】
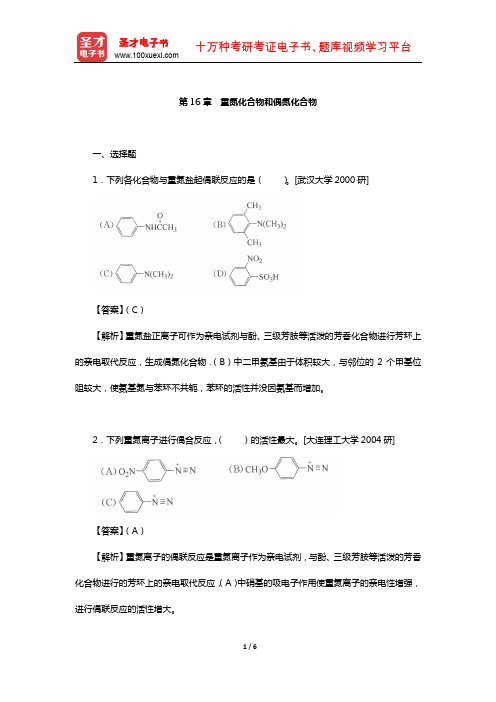
第16章重氮化合物和偶氮化合物一、选择题1.下列各化合物与重氮盐起偶联反应的是()。
[武汉大学2000研]【答案】(C)【解析】重氮盐正离子可作为亲电试剂与酚、三级芳胺等活泼的芳香化合物进行芳环上的亲电取代反应,生成偶氮化合物.(B)中二甲氨基由于体积较大,与邻位的2个甲基位阻较大,使氨基氮与苯环不共轭,苯环的活性并没因氨基而增加。
2.下列重氮离子进行偶合反应,()的活性最大。
[大连理工大学2004研]【答案】(A)【解析】重氮离子的偶联反应是重氮离子作为亲电试剂,与酚、三级芳胺等活泼的芳香化合物进行的芳环上的亲电取代反应,(A)中硝基的吸电子作用使重氮离子的亲电性增强,进行偶联反应的活性增大。
二、填空题1.完成反应式。
[中国科学院-中国科学技术大学2004研]【答案】【解析】重氮甲烷是一较强的甲基化试剂,可与含活泼氢的化合物发生甲基化反应。
2.完成反应式。
[厦门大学2002研]【答案】【解析】重氮盐的偶联反应是重氮离子作为亲电试剂:与三级芳胺进行的芳环上的亲电取代反应。
3.完成反应式。
[上海大学2003研]【答案】【解析】甲氧基苯胺与亚硝酸反应生成重氮盐,重氮盐在次磷酸的作用下,重氮基可被氢原子取代。
4.完成反应式。
[中山大学2003研]【答案】【解析】氢化偶氮苯在酸催化下,发生重排,生成二氨基联苯。
5.完成反应式。
[华中科技大学2004研] 【答案】【解析】对甲苯胺被亚硝酸氧化成重氮盐,重氮盐与CuCN的KCN水溶液作用(桑德迈尔反应),重氮基可被氰基取代,故反应生成对甲苯腈。
6.完成反应式。
[华中科技大学2002研]【答案】【解析】硝基苯被还原成苯胺,苯胺与亚硝酸发生重氮化反应生成重氮盐,重氮盐与吡咯发生偶联反应。
三、问答题1.由指定的原料出发合成:[华中科技大学2001研]答:由苯合成硝基苯,硝基苯被还原成氢化偶氮苯,后者在酸作用下重排成联苯胺,联苯胺与两分子甘油作用即得目标产物。
2.从指定的原料出发合成:[云南大学2004研]答:由苯胺先合成对氨基苯磺酸,再用HN02将其中的氨基氧化成重氮离子,后者与N,N-二甲基苯胺发生偶联反应即得目标产物。
2-重氮-1-萘酚-5-磺酰氯安全技术说明书MSDS

化学品安全技术说明书第一部分化学品及企业标识化学品中文名:2-重氮-1-萘酚-5-磺酰氯化学品英文名:2-diazo-1-naphthol-5-sulphochloride化学品别名:-CAS No.:3770-97-6EC No.:223-211-1分子式:C10H7ClN2O3S第二部分危险性概述| 紧急情况概述固体。
遇热有火灾或爆炸危险。
| GHS 危险性类别根据GB 30000-2013 化学品分类和标签规范系列标准(参阅第十六部分),该产品分类如下:自反应物质和混合物,B型。
| 标签要素象形图警示词:危险危险信息:加热可能起火或爆炸。
防范说明预防措施:远离热源、热表面、火花、明火以及其它点火源。
禁止吸烟。
只能在原包装中存放。
保持低温。
容器和接收设备接地和等势联接。
戴防护手套/穿防护服/戴防护眼罩/戴防护面具。
事故响应:不适用。
安全储存:存放在通风良好的地方。
分开存放。
废弃处置:按照地方/区域/国家/国际规章处置内装物/容器。
| 危害描述物理化学危险在包装件中可发生热爆炸。
健康危害吸入该物质可能会引起对健康有害的影响或呼吸道不适。
意外食入本品可能对个体健康有害。
通过割伤、擦伤或病变处进入血液,可能产生全身损伤的有害作用。
眼睛直接接触本品可导致暂时不适。
环境危害请参阅 SDS 第十二部分。
第三部分成分/组成信息√物质混合物第四部分急救措施| 急救措施描述一般性建议:急救措施通常是需要的,请将本 SDS 出示给到达现场的医生。
皮肤接触:立即脱去污染的衣物。
用大量肥皂水和清水冲洗皮肤。
如有不适,就医。
眼睛接触:用大量水彻底冲洗至少 15 分钟。
如有不适,就医。
吸入:立即将患者移到新鲜空气处,保持呼吸畅通。
如果呼吸困难,给于吸氧。
如患者食入或吸入本物质,不得进行口对口人工呼吸。
如果呼吸停止。
立即进行心肺复苏术。
立即就医。
食入:禁止催吐,切勿给失去知觉者从嘴里喂食任何东西。
立即呼叫医生或中毒控制中心。
重氮盐

+
-
H+
反应机理:
+
C6H5-OH + N2 + H2SO4 (7479%)
N N
-N2
+
H 2O
OH2
+
-H+
OH
讨
论
1. 用重氮硫酸氢盐进行水解反应。 2. 芳基上的取代基对水解速率的影响: 吸电子基团使反应速率减慢。 给电子基团处于邻对位,使反应速率减慢,处于间位 使反应速率加快。 A-C6H4N2+ClA V相对
N H 2
3 / H
2 S O 4
N a N O
2 / H
2 S O 4
N O 2
N 2 H S O 4
4 0 ~ 5 0 % H 2 S O 4 O H
N O 2
N O 2
N O 2
2、被卤原子取代制卤苯:碘苯、氟苯必须用此方 法,特殊氯苯、溴苯必须用此方法。下面举例说明:
有机化合物的分子结构与颜色的关系
1.有机化合物分子中共轭体系的增长导 致颜色的加深。这是因为共轭体系越 长,分子轨道跃迁能量级差越小,越容 易激发。因此,激发光波长移向长波方 向。
2.在有机化合物共轭体系中引入助色基或生色基 一般伴随着颜色的加深。 光谱术语:
① 发色基团(生色团)(Chromophore):共价键不饱和 原子基团能引起电子光谱特征吸收的,一般为带有π电子的 基团。 如: ② 助色基团(Auxochrome):饱和原子基团本身在200nm 前没有吸收,但当它与生色基相连时,它能增长最大吸收峰 的波长并增大其强度。一般为带有p电子的原子或原子团。 如: 助色基被引入共轭体系时,这些基团上未共用电子对参与共 轭体系,提高了整个分子中π电子的流动性(使HOMO能 级上升,能量增加)从而降低了分子的激发能,使化合物吸 收向长波方向移动,导致颜色加深。
《有机化学》徐寿昌-第二版-第16章-重氮化合物和偶氮化合物全文

16.1 重氮化反应—芳香族重氮盐的制备 ◆伯芳胺在低温及强酸(主要是盐酸或硫酸)水溶液
中,与亚硝酸作用生成重氮盐的反应,称为重氮化反应:
NH2 + HONO + HCl <5℃
N2Cl + 2 H2O
(NaNO2+HCl)
氯化重氮苯(重氮苯盐酸盐)
◆反应条件:
料的50%. 偶氮染料种类多,色调鲜艳,广泛应用于 棉、毛、丝、麻以及塑料、印刷、皮革、橡胶、食 品等产品的染色.
◆苏丹红:
苏丹红是一类人工合成的亲脂性偶氮染料,有致癌性和遗传 毒性,在食品中非天然存在,因此在食品中应禁用。
其品种主要包括苏丹红1号、2号、3号和4号,主要用于溶剂、 油、蜡、汽油增色以及鞋和地板等的增光。
◆三线态碳烯是个双游离基, 两个未成键电子分别在 两个原子轨道上,它的加成分两步进行:
由于中间体双游离基的碳碳单键能够旋转,所以最后生 成物有顺、反两种异构体:
例如:
◆ 碳烯与炔烃、环烯烃或苯的加成反应:
例1:
H
例2:
例3:
(2)插入反应
◆单线态碳烯还可插入C—H键之间,发生插入反应:
例如:丙烷与重氮甲烷在光照下作用:
◆重氮盐与伯胺或仲胺发生偶合反应,可以发生苯环上 的氢取代,也可以发生氨基上的氢取代:
重排
对氨基偶氮苯
◆若对位已有取代基,则重排生成邻氨基偶氮苯.
CH3 CH3
NH2
◆若重氮盐与间甲苯胺偶合,则主要发生苯环上的氢被 取代(因为甲基增加苯环的活泼性);重氮盐与间苯二胺 偶合也类似:
偶合发生在活 泼基团的对位
①低温(<5℃):重氮盐高温分解.
(1-重氮基-2-氧代丙基)膦酸二甲酯反应机理

文章标题:深度解析(1-重氮基-2-氧代丙基)膦酸二甲酯反应机理在有机合成领域,(1-重氮基-2-氧代丙基)膦酸二甲酯反应机理是一个备受关注的话题。
这种反应机理的深度和广度,不仅仅体现在化学反应的步骤上,更包括了对化学键断裂、物质转化过程和结构的全面评估。
本文将通过从简到繁、由浅入深的方式,深入探讨(1-重氮基-2-氧代丙基)膦酸二甲酯反应机理,旨在帮助读者更深入地了解这一话题。
**1. (1-重氮基-2-氧代丙基)膦酸二甲酯反应概述**在开始深入探讨反应机理之前,让我们先来总览一下(1-重氮基-2-氧代丙基)膦酸二甲酯反应的基本概念。
这种反应是一种重要的有机合成反应,通常用于合成特定的有机化合物。
它涉及了多个步骤和中间体,在反应过程中需要考虑到反应条件、溶剂选择、催化剂等多种因素。
这种反应具有较高的化学反应活性和特殊的反应机理,因此在有机合成领域中具有重要的应用价值。
**2. 反应机理的步骤**(1-重氮基-2-氧代丙基)膦酸二甲酯反应机理包含了多个步骤,每个步骤都至关重要。
我们需要考虑的是反应的起始物质和基本结构,在了解这些前提条件之后,我们可以更深入地探讨反应机理的步骤。
其中可能涉及到的步骤包括:- 第一步:xxxxxxxxxxxxxx- 第二步:xxxxxxxxxxxxxx- 第三步:xxxxxxxxxxxxxx- ......**3. 中间体的结构和性质**在了解反应机理的步骤之后,我们需要对中间体的结构和性质进行全面评估。
这一步骤涉及到分子结构的变化、键合的形成和断裂、化学键的活化等多个方面。
只有深入了解中间体的结构和性质,我们才能更好地理解这种反应的本质和特点。
**4. 反应条件和影响因素**除了步骤和中间体的结构外,反应条件和影响因素也是决定(1-重氮基-2-氧代丙基)膦酸二甲酯反应机理的重要因素。
在这一部分,我们将着重讨论反应条件对反应机理的影响,包括温度、压力、溶剂选择、催化剂等因素。
重氮化反应

RNH2 HCl NaNO2
ROH N2 NaCl
用途
Ar-N2+X- + Ar’-NH2 偶合 Ar-N=N-Ar’-NH2 Ar-N2+X- + Ar’-OH 偶合 Ar-N=N-Ar’-OH
Ar-N2+X-
NaSO3, NaHSO3
还原
Ar-NHNH2
ArN2X- 重氮基转化 ArY Y=F, Cl, Br, I, CN, OH, H等
NH2 NO2
CH3 NO2
NH2
(1) 有两个或两个以上强吸电基;
(2)不溶于稀酸。
方法:以浓H2SO4或CH3COOH为介质; 亚硝基硫酸法(NO+HSO4-)。
NH2 NO2 Cl
NO2
NH2 NO2
NO2
H3CO
S NH2
N
氨基磺酸或氨基羧酸 特点:(1)易形成内盐,在酸性介质下不溶; (2)可以溶于碱。 方法:碱溶酸析;顺式重氮化法
9.1 重氮化反应
概述 重氮化反应动力学 重氮化反应历程 重氮化反应影响因素 重氮化方法
9.1.1 概述
定义
芳香族伯胺与亚硝酸作用,生产重氮盐的 反应叫做重氮化反应。
ArNH2 2HX NaNO2
ArN2+X- NaX 2H2O
HX=HCl、HBr、浓H2SO4、稀H2SO4 、HNO3等
9.1.5 重氮化方法
碱性较强的芳胺 特点:带供电基,铵盐稳定,不易水解为游离胺
方法: 铵盐溶于水:慢速顺法
NH2
NH2 OCH3
NH2 CH3
NH2 CH3
铵盐不溶于水:快速顺法CH3
H2N
NH2
重氮盐偶联反应

重氮盐偶联反应一、引言重氮盐偶联反应是有机合成中的一种重要反应,可以用于构建碳-碳键和碳-氮键。
该反应以芳香胺或其衍生物为原料,通过氧化亚氮生成重氮盐中间体,再与亲核试剂发生偶联反应。
该反应具有简单易行、高选择性、高效率等优点,在药物合成、材料科学等领域得到广泛应用。
二、机理重氮盐偶联反应的机理主要分为两步:生成重氮盐中间体和与亲核试剂发生偶联反应。
1. 生成重氮盐中间体首先,芳香胺经过亲电取代作用被氧化为亚硝基芳香胺,随后在酸催化下失去水分子形成重氮盐中间体。
2. 与亲核试剂发生偶联反应生成的重氮盐中间体进一步与亲核试剂发生偶联反应。
如与苯乙烯发生偶联反应时,重氮离子上的N-N键断裂,C-N键形成,同时苯环上的双键被还原为单键。
三、影响因素1. 反应物的选择芳香胺的结构和取代基对反应速率和产率有很大影响。
一般来说,含电子供体基团的芳香胺反应活性较高,而含电子吸引基团的芳香胺反应活性较低。
2. 酸催化剂的选择酸催化剂对反应速率和产率也有很大影响。
一般来说,强酸催化剂如硫酸、氯化亚铁等反应速率较快,但容易引起副反应;而弱酸催化剂如硼酸、乙酰氧化铝等则反应速率较慢,但产物纯度高。
3. 温度和溶剂的选择温度和溶剂也是影响重氮盐偶联反应的重要因素。
一般来说,在适当温度下进行该反应可以提高产率;而不同溶剂对该反应也有不同影响,如极性溶剂有利于离子中间体形成,而非极性溶剂则有利于亲核试剂与离子中间体发生偶联。
四、实例分析1. 苯甲醛与N-苯基-1-萘胺的偶联反应首先,N-苯基-1-萘胺在硫酸催化下被亚硝基化生成重氮盐中间体。
随后,重氮盐中间体与苯甲醛发生偶联反应,生成N-(2-苯乙酰基)-1-萘胺。
2. 苯甲醛与N,N-二甲基苯胺的偶联反应首先,N,N-二甲基苯胺在硼酸催化下被亚硝基化生成重氮盐中间体。
随后,重氮盐中间体与苯甲醛发生偶联反应,生成N,N-二甲基-N-(2-苯乙酰基)苯胺。
五、总结重氮盐偶联反应是一种简单易行、高选择性、高效率的有机合成方法,可以用于构建碳-碳键和碳-氮键。
总胆红素化学氧化法和重氮法-概述说明以及解释

总胆红素化学氧化法和重氮法-概述说明以及解释1.引言1.1 概述总胆红素是一种重要的生化指标,其测定方法多种多样。
其中,总胆红素化学氧化法和重氮法是常用的两种方法。
总胆红素化学氧化法通过将总胆红素氧化为胆红素氧化物,再进行光度测定来确定总胆红素含量。
相比之下,重氮法则是通过将总胆红素转化为双重氮化合物,然后进行比色测量来确定总胆红素的含量。
总胆红素化学氧化法在医学、生物化学和临床诊断中有着广泛的应用。
它具有操作简单、结果准确、灵敏度高等优点。
通过这种方法可以快速、准确地检测出总胆红素含量,为疾病的早期诊断和治疗提供重要依据。
然而,总胆红素化学氧化法也存在一些缺点,例如对样品准备要求高、耗时较长、需要使用特定的试剂等。
重氮法是另一种常用的测定总胆红素含量的方法。
它具有操作简单、结果可靠、灵敏度高等特点。
重氮法适用于各种类型的样品,包括血液、尿液和胆汁等。
与总胆红素化学氧化法相比,重氮法更加灵敏,并且可以检测出低浓度的总胆红素。
然而,重氮法也存在一些不足,例如对pH值和温度的要求较高,以及有一定的毒性和危险性。
通过比较总胆红素化学氧化法和重氮法,可以发现它们各自具有一定的优点和局限性。
总的来说,总胆红素化学氧化法在操作简单、结果准确方面具有一定优势;而重氮法则在灵敏度高、适用范围广方面具有一定优势。
根据具体的需求和实际情况,选择不同的方法进行总胆红素的测定,能够更好地满足实验要求和研究需要。
综上所述,总胆红素化学氧化法和重氮法是两种常用的测定总胆红素含量的方法。
它们各自具有一定的优缺点,适用于不同的实验需求。
通过综合评估和比较,可以选择合适的方法进行总胆红素的测定,为相关领域的研究和应用提供可靠的数据支持。
随着科学技术的不断发展,这两种方法仍有进一步改进和完善的空间,有望在未来取得更加广泛的应用。
文章结构部分的内容如下:1.2 文章结构本文将分为5个主要部分来论述总胆红素化学氧化法和重氮法这两种方法。
重氮反应——精选推荐

重氮反应一. 学习目的和要求:1.掌握重氮盐的性质及其在有机合成上的应用。
2.掌握重氮甲烷的结构、性质。
3. 理解α—消除和γ—消除的反应机理,特别是碳烯的形成及应用。
4.了解偶氮化合物及偶氮染料。
5. 了解叠氮化合物及氮烯。
二. 本章节重点、难点:重氮盐的性质及其在合成上的应用;重氮甲烷的结构、性质。
三. 教学内容:引言重氮和偶氮化合物分子中都含有-N=N-官能团,官能团两端都与烃基相连的称为偶氮化合物,只有一端与烃基相连,而另一端与其他基团相连的称为重氮化合物。
重氮盐的结构如图所示:重氮和偶氮化合物的命名阅读P391。
16.1芳香族重氮盐的制备——重氮化反应伯芳胺在低温及强酸水溶液中,与亚硝酸作用生成重氮盐(diazotization)的反应称为重氮化反应。
重氮化反应是制备芳基重氮盐最重要的方法。
强调:1. 重氮盐温度较高时易分解,故重氮化反应常在低温下进行。
2. 亚硝酸的存在会加速重氮盐的分解,故亚硝酸不能过量。
3. 重氮化反应须保持强酸性条件,以避免生成的重氮盐与未起反应的芳胺发生偶合反应。
16.2芳香族重氮盐的性质重氮盐的化学性质非常活泼,它的许多化学反应归纳起来主要有两类:16.2.1取代反应(1)被羟基取代(水解反应)当重氮盐的酸性水溶液加热时,发生水解生成酚并放出氮气。
强调:重氮盐水解成酚时只能用硫酸盐,不用盐酸盐,因盐酸盐水解易发生副反应。
(2)被卤素、氰基取代强调:此反应是将碘原子引进苯环的好方法,但此法不能用来引进氯原子或溴原子。
氯、溴、氰基的引入用桑德迈尔(Sandmeyer)法。
(3)被氢原子取代(去氨基反应)强调:上述重氮基被其他基团取代的反应,可用来制备一般不能用直接方法来制取的化合物。
例由硝基苯制备2,6-二溴苯甲酸:16.2.2还原反应重氮盐可被氯化亚锡、锡和盐酸、锌和乙酸、亚硫酸钠、亚硫酸氢钠等还原成苯肼;如用较强的还原剂则生成苯胺和氨。
阅读:P39616.2.3偶联反应重氮盐与芳伯胺或酚类化合物作用,生成有颜色的偶氮化合物的反应称为偶联反应。
重氮、偶氮和叠氮化合物.doc

重氮、偶氮和叠氮化合物重氮、偶氮和叠氮化合物2010-05-22 10:14重氮化合物的通式为R2C=N2,最简单的重氮化合物是重氮甲烷CH2N2,其结构式为:由此可预见该分子极易脱去一分子氮气形成,即卡宾(carbene)又称碳烯的活性中间体。
9.3.1重氮化合物的制备9.3.1.1重氮甲烷的制备型的化合物与碱作用,可得到重氮甲烷CH2N2,R可为烃基、酰基、磺酰基。
重氮甲烷是有毒的黄色气体,b.p.为-24?,纯重氮甲烷容易爆炸,通常在乙醚稀溶液中使用。
酰氯与重氮化合物反应得到α-重氮酮:α-重氮酮α-重氮酮中羰基与重氮基共轭,故其稳定性高于重氮甲烷。
氨基乙酸酯与亚硝酸反应生成重氮乙酸酯。
重氮乙酸酯为黄色液体,其稳定性也高于重氮甲烷。
9.3.1.2重氮盐的制备在0~5?下,伯胺在强酸存在下与亚硝酸反应,生成重氮盐,称为重氮化反应。
重氮化合物一般不经分离(因为易爆炸)直接进行后续反应。
9.3.2重氮化合物的反应9.3.2.1 CH2N2的反应重氮甲烷中的碳具有一对孤电子,故能作为碱接受质子,又能作为亲核试剂与醛酮、酰氯等反应。
1、与酸的反应重氮甲烷与羧酸作用,放出氮气而生成羧酸甲酯:此反应主要用于一些贵重羧酸的酯化反应,产率可达100%。
例如:重氮甲烷分子中的碳原子有碱性,可以从羧酸中接受质子,转变成甲基重氮离子,随后羧基作为亲核试剂进攻甲基脱去氮气而生成羧酸甲酯:其它的酸,如氢卤酸、磺酸、酚和烯醇都可以与重氮甲烷反应分别生成卤甲烷、磺酸甲酯,酚的甲醚和烯醇甲醚。
醇的酸性太弱,不能直接与重氮甲烷反应,但在Lewis酸催化下,可以与重氮甲烷反应生成甲基醚。
因此,重氮甲烷是一种应用广泛的甲基化试剂。
2、与醛酮的反应重氮甲烷具有亲核性,能与醛酮中的羰基进行亲核加成反应,然后与羰基相连的一个烃基从羰基碳上迁移到原属重氮甲烷的亚甲基上,同时脱去一分子氮气,得到多一个碳原子的羰基化合物。
酮分子中与羰基相连的两个烃基如果不同,则酮与重氮甲烷反应,生成两种异构体。
重氮

被碘原子取代
由于I 原子的亲核活性较高,重氮基比较容易被碘原子取代, 由于 -原子的亲核活性较高,重氮基比较容易被碘原子取代, 而无需催化剂。只要把重氮盐与KI水溶液一起加热 水溶液一起加热, 而无需催化剂。只要把重氮盐与 水溶液一起加热,重氮基即 可被碘原子取代,这是把碘原子引入芳环的好方法。 可被碘原子取代,这是把碘原子引入芳环的好方法。 KI 2 O2N NH2 NaNO + H2SO4 O2N N2HSO4 O2N I 前面已学过,由于 的反应活性不高, 前面已学过,由于I2的反应活性不高,不能用亲电取代反应在 芳环上引入碘原子,只有两种特殊的情况才可以: 芳环上引入碘原子,只有两种特殊的情况才可以:
重氮化反应
(3)加NaNO2要适量。少了,影响产率;多了,会促进重氮盐 加 要适量。少了,影响产率;多了, 的分解;另外影响反应终点的检测; 的分解;另外影响反应终点的检测;甚至会影响到下一步的反 所以一般NaNO2是等摩尔量加入。 是等摩尔量加入。 应。所以一般 反应终点是用KI-淀粉试纸检验,如果未到终点, 反应终点是用 -淀粉试纸检验,如果未到终点, HNO2会将 I- 氧化成 2而使淀粉显蓝色;反应到终点,微量的 氧化成I 而使淀粉显蓝色;反应到终点,微量的HNO2会使 KI-淀粉试纸显蓝紫色。反应结束后,残余的或过量的 -淀粉试纸显蓝紫色。反应结束后,残余的或过量的HNO2 可加入尿素来除去。 可加入尿素来除去。
一、放氮反应
放氮反应就是重氮盐中的重氮基- 、-H、- 放氮反应就是重氮盐中的重氮基-N2X被-OH、- 、- 、 被 、- 、-X、 等原子或原子团取代, -CN等原子或原子团取代,同时放出氮气的反应。因此,又叫 等原子或原子团取代 同时放出氮气的反应。因此, 取代反应。 取代反应。
2-重氮-1-萘酚-5-磺酰氯-危险化学品安全标签

2-重氮-1-萘酚-5-磺酰氯6-diazo-5,6-dihydro-5-oxonaphthalene-2-sulphonyl chloride浓度或浓度范围:2-重氮-1-萘酚-5-磺酰氯:100%危险!易燃固体。
加热可能起火或爆炸。
吞咽有害。
可能导致皮肤过敏反应。
造成严重眼刺激。
对水生生物有害并具有长期持续影响。
【预防措施】远离热源/火花/明火/热表面。
禁止吸烟。
容器和装载设备接地/等势联接。
使用防爆的电气/通风/照明/设备。
戴防护手套/穿防护服/戴防护眼罩/戴防护面具。
只能在原容器中存放。
保持低温。
作业后彻底清洗。
使用本产品时不要进食、饮水或吸烟。
避免吸入粉尘/烟/气体/烟雾/蒸气/喷雾。
受沾染的工作服不得带出工作场地。
避免释放到环境中。
【事故响应】火灾时:使用灭火器灭火。
火灾时:撤离现场。
因有爆炸危险,须远距离灭火。
如误吞咽:如感觉不适,呼叫解毒中心/医生,漱口。
如皮肤沾染:用水充分清洗。
如发生皮肤刺激或皮疹:求医/就诊。
脱掉沾染的衣服,清洗后方可重新使用如进入眼睛:用水小心冲洗几分钟。
如戴隐形眼镜并可方便地取出,取出隐形眼镜。
继续冲洗。
如仍觉眼刺激:求医/就诊。
【安全储存】存放在通风良好的地方。
远离其他材料存放。
【废弃处置】按照地方/区域/国家/国际规章处置内装物/容器。
请参阅化学品安全技术说明书供应商:电话:地址:邮编:化学事故应急咨询电话:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
+ –N2Cl
N N
+ sp杂化 –N2HSO4
¡ ¤ ¡ ¤
重氮苯盐酸盐
重氮苯硫酸盐
第一节 重氮化反应
§16-1 芳基重氮盐 一、芳香族重氮盐的制备——重氮化反应
一级胺与亚硝酸反应,生成重氮盐
C 6H 5NH 2
NaNO2-HCl 0~5 C
O
+ C 6H 5 N
N Cl
能溶于水,水溶液能导电
?
① H3PO2 + H2O ② HCHO + NaOH ③ C2H5OH 邻对位基 练习4: 有副产物“醚” N2X NO2 NH2 Br Br Br Br Br Br Br
Br
Br
§16-2 重氮盐的性质
CH3 CH3
HNO3 H2SO4 Fe+HCl
CH3
练习5:
CH3
CH3COCl Br2
偶合位置
OH NH2
OH (NH2) OH (NH2)
SO3Na
§16-2 重氮盐的性质
偶氮化合物中的重氮部分和偶氮部分:
H2N N N
HO 3S
NO 2
偶联部分
重氮部分 芳香族重氮盐
酚、胺
§16-2 重氮盐的性质 例:由萘、联苯胺为原料合成刚果红。
解:
H2N N N N N
H2N
NH2
H2N
NaO 3S
§16-2 重氮盐的性质
被–OH取代 (重氮盐的水解反应) + –OH –N2HSO4 H2O/H+ + N2↑ △
?
注意问题:①使用硫酸盐,氢卤酸盐会有副产物。 SN1 机理: △ –H+ ②酸性条件,防止苯酚与重氮盐偶联。 + –OH2 + 在不适合磺化碱熔的情况下,引入 H2O 实用价值: –OH。 碱熔条件 + N2↑ NO2 下,–Br pH=8~10 NO2 –N2X + –OH – N=N – – OH Fe+HCl Br2/Fe 会被 –OH HNO3 练习1: H2SO4 取代。 Br 对羟基偶氮苯 –Cl (副产物) N NH2 SO3H SO OH 2HSO 3H 4
HCl + NaNO 2 HCl + ArNH 2
HNO2 ArNH 3Cl
+
还有1molHCl维持反应液的酸性,防止副反应的发 生,并稳定重氮盐
§16-1 芳基重氮盐
注 1: 反应物为芳伯胺。
注 2: 低温条件,重氮盐受热易分解。 强酸条件,否则产物与反应物再发生偶联反应。 注 3:
–NH2 NaNO2/HCl
§16-2 重氮盐的性质
3.保留氮的反应 (1)还原反应
A 弱还原剂
N 2Cl
还原剂
+
NHNH 2.HCl
碱
NHNH 2
还原剂:SnCl2+HCl,Sn+HCl,Zn+HOAc, Na2SO3,NaHSO3
B 强还原剂
N2+ClZn+ HCl
NH2
§16-2 重氮盐的性质
(2)偶联反应
重氮盐 + 芳胺(或酚)
+ Ar N N:
碱 OH-
N:
Ph
Ar N
碱 N OH Ph
N N
Ar N
N O N N
重氮盐的结构:Z,E 稳定性:E>Z 2、放氮反应 (重氮基被取代)——制备芳烃衍生物 +
N2
慢
+ -N2
OH
Y
Y快
3、留氮反应 ——制备偶氮化合物
+ –N2 X
–Y
–Y
去氨基 + N2↑ 反应
重氮基可以被–H、–OH、–X、–CN……取代
ArNH2 + NaNO 2 + HCl (H2SO4)
NH 2 NaNO 2 + HCl 0~5 ℃
0~5 ℃
ArN2 Cl + NaCl + H 2O
N2 Cl
+ NaCl + H 2O
§16-1 芳基重氮盐
1°重氮化反应不能超过5℃,温度高重氮盐易分解。 2°亚硝酸不能过量(亚硝酸有氧化性,不利于重 氮盐的稳定)。HNO2 :ArNH2 = 1 :1 3°重氮化反应必须保持强酸性条件(弱酸条件下 易发生副反应)。芳香伯胺:HCl = 1 :3
三、重氮和偶氮化合物 ——脂肪族不稳定,
(一) 分类、结构和命名 (二) 重氮盐的制备
以芳香族为主。
偶氮基 –N=N–
两端连烃基称“偶氮” 一端连烃基称“重氮” (三) 重氮盐的性质和应用(重点) –N=N–OH –N=N– 偶氮苯 氢氧化重氮苯
–N=N–SO3Na 重氮苯磺酸钠
重点介绍
重氮盐
+ –N≡N X
ArBr / ArCl
- KCN+CuCN + ArN2Cl ArCN
*该反应被认为是 自由基反应,亚铜盐起传递电子 的作用
§16-2 重氮盐的性质
(3)被硝基取代——Gatterman(伽特曼)反应
+ N 2 BF4 NO2
NaNO2,Cu
(4)被氟取代——Schiemann(希曼)反应
+ N 2Cl
学习要点: 反应条件、 实用价值、注意问题。
§16-2 重氮盐的性质
2、重氮基被取代的反应 OH
H2 O △
+ N2
Cl
N2 Cl
+
CuCl 2 2,HCl ℃ 16~60
+
N2
CN
Cu2(CN)2,KCN 90~100℃
+ N2
H3PO2 H2O, △
+
N2
§16-2 重氮盐的性质
(1)被羟基取代——重氮盐的水解,产物为酚
§16-1 芳基重氮盐 二、重氮盐的结构
N N
+
+ Cl R N Ar N: N X N
+
或 Ar-N=N
Ar N N X
+
Ar
N N X
N
N
重氮基正离子,N, N键中有2个π键相互 垂直,有一个σ键。
第二节 重氮盐的性质
§16-2 重氮盐的性质 + (三) 重氮盐的性质和应用 N Ph 1. 酸性 Ph
CH2 N N
1、重氮甲烷(Diazomethane)
N
N
H
N
C H
N
N
Sp2
Sp
Sp
3原子4电子的大键. 电负性: C(2.6) N(3.0) 结构:线状分子 偶极矩不大 b.P -23℃ m.P -145℃ 黄色气体; 剧毒、易挥发,易爆,可溶入乙醚,在乙醚中安定。
§16-3
重氮甲烷和碳烯
(2). 重氮化合物的制备 A N-甲基-N-亚硝基酰胺的碱性分解
NaO 3S
H2N
NH2
NO 2
NaNO2 HCl
Cl-
N
N
+
N
+
N
Cl-
NH2
NH2
HNO3 H2SO4
HCl
Fe
H2SO4
△
SO 3H
H2N N N N N
H2N
NaO 3S
NaO 3S
§16-2 重氮盐的性质
练习6:以甲苯为原料制备 CH3 CH CH3 CH3 CH CH COOH 33 3
CH3 Br
NH2
H3PO2+H2O
NH2 CH3
Br
Br Br H2 O
△
Br
CH3
CH3
Br2/Fe
N2X CH3 Br Br SO3H
Br
SO3H
第三节 重氮化合物
CH2N2重氮甲烷 :CH2 碳烯
§16-3
(1) 重氮甲烷的结构
共振式:CH2N2
H H C N
CH2
重氮甲烷和碳烯
分子式 : CH2N2
NH2
CH3
N2Cl
H+/H2O
CH3
CN
COOH
§16-2 重氮盐的性质
(6)被氢取代
——实用价值:利用–NH2的定位作用。
+ N 2 Cl H3PO2 +H2 O N 2 + H 3PO3+ H Cl + + N 2 Cl HCHO+ 2 NaOH + N2 + HCOON + N 2 Cl HCHO+ 2 NaOH + N2 + HCOONa + NaCl + H2 O
–I
既是反应试剂, 也是催化剂。 ①用其他方式难 以引入的基团。 ②基团位置与定 位规律矛盾。 Cl 伽特曼反应 桑德迈尔反应
–Br –Cl
+ –N +2 X –N2BF4 + –N2 X
如: 伽特曼反应特 –CN 伽特曼反应 Br 点:催化剂用 量少,反应所 –NO2 需温度较低。 –F 希曼反应 但产率不高。 –SO3Na
HNO HNO H 33 2SO 4 H H SO SO 22 44 Fe+HCl KMnO4 NaOH 300℃ NaNO Fe+HCl H+ 2/HX 0~5℃
CH COOH CH 3 3
SO NO H 32 CH3 + N2X 重氮组分 CH3 偶联组分 OH
NH2 NH ONa NO 2 2
O R-C-Cl + CH3NH2 O CH2-H R-C-Leabharlann N=O O RCNHCH3 HNO2
