物理化学第七章 电化学讲解
物理化学课件第七章-电化学
l
S
A
r
r
A
S' E
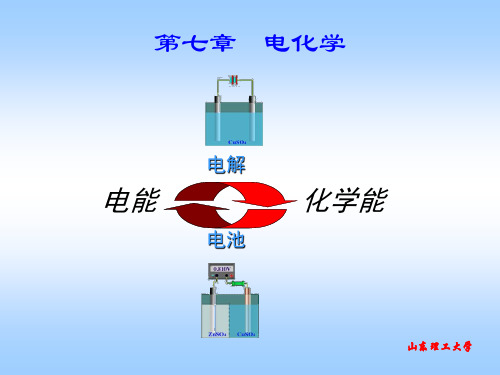
离子的电迁移
山东理工大学 33
Mx N y
c(1 )
xMz yNz
cx cy
设正离子迁移速率为 r ,单位时间向阴极方向通 过任意截面 ss' 的物质的量为 (cx Ar )mol ,所迁移
的电量为 (cx Ar )zF ,因为是单位时间,所以:
Q t
I
(cx Ar )zF
D. 导电总量全部由电子承担
山东理工大学 6
第二类导体又称离子导体,如电解质溶液、熔 融电解质等 第二类导体的特点是:
A. 正、负离子作反向移动而导电
B. 导电过程中有化学反应发生
C. 温度升高,电阻下降
D. 导电总量分别由正、负离子分担(速率,电荷)
*固体电解质,如 AgBr、PbI2 等,也属于离子 导体,但它导电的机理比较复杂,导电能力不高,
dE u ( dl )
u , u 称为正、负离子的
电迁移率,单位 m2 s1 V1。
离子的电迁移率又称为离子淌度(ionic mobility), 相当于单位电位梯度时离子迁移的速率
电迁移率的数值与离子本性、电位梯度、溶剂性 质、温度等因素有关,可以用界面移动法测量。
山东理工大学 30
离子迁移数的定义
2电解质溶液的导电机理 ①正负离子定向迁移;
②界面上分别发生氧化还原反应,电荷转移;
结果实现了化学能和电能之间的转换。
3 电极命名法: 正极(电势高) 负极(电势低)
原电池 阴极(还原反应) 阳极(氧化反应)
电解池 阳极(氧化反应) 阴极(还原反山东应理工)大学 15
法拉第定律的文字表述
物化 第七章 电化学ppt课件

2. 电极过程
电化学过程必须在电化学池中实现,总是伴随着电化学反应和 化学能和电能相互转换发生。
原电池: 化学能转化为电能的装置;干电池,蓄电池,燃料电池等
系统对外做电功
G T,P 0
上一内容
下一内容
回主目录
返回
2. 电极过程
电解池: 电能转化为化学能的装置;电镀装置,电抛光装置等
Q m n M M z F
M-物质的摩尔质量
上一内容 下一内容 回主目录
返回
3. 法拉第定律
已知元电荷电量为
1 . 6 0 2 21 0C
1 9
F=L· e =6.022×1023 mol-1×1.6022×10-19 C
=96484.6 C· mol-1
≈96500 C· mol-1
上一内容
下一内容
回主目录
返回
2018/11/25
2. 电极过程 原电池 将化学能转化 为电能的装置
阳极(负极):
Zn(s)= Zn2+ (aq)+ 2e(氧化反应)
Zn
Cu
阴极(正极):
Cu2+(aq)+ 2e- = Cu(s) (还原反应)
上一内容
下一内容
回主目录
返回
2018/11/25
回主目录
返回
2018/11/25
3. 法拉第定律
Faraday’s Law
⒈ 在电极界面上发生化学变化物质的质量 与通入的电量成正比。 Q m 或 Q n
Michael Faraday ⒉ 通电于若干个电解池串联的线路中,当 (l791-1867) 所取的基本粒子的荷电数相同时,在各个 英国著名的自 学成才的科学家
天大物理化学第五版第七章电化学ppt课件

银库仑计中有0.723 mmol Ag沉积,则在电解池中阳极必有相同数量 的Ag被氧化成Ag+而进入溶液,即 n反应 (Ag ) 0.723 mmol
对Ag+ 物料衡算有 : n电解后
n电解前
n反应 n迁移
t(Ag )n反应
17
t(Ag )
n电解前
n电解后
1
1.007
1.390 1
0.470
n反应
电解质溶液的 :
相距为1m, 面积为1m2
1m2
的两个平行板电极之间充
满电介质溶液时的电导。
1m
(2) 摩尔电导率Λm:
1mol电解质溶液导电能力,即单位浓度下的电导率:
m
/c
(单位为S. m2.mol-1)
20
2. 电导的测定
用惠茨通(Wheatstone)电桥测电导
(实为测电阻,用交流电)
当T=0时: VAD = VAC , I1R1 = I2R3 VDB =VCB , I1Rx = I2R4
m,
均可查表计算
26
5. 电导测定的应用
(1) 计算弱电解质的解离度及解离常数
弱电解质部分电离,例如,醋酸:
解离前
CH3COOH = H+ + CH3COO-
c
0
0
解离平衡时 c(1- ) c c
K
( c /c )2 (1 )c /c
2
1 c /c
m m
测电导可求得
由 可求出 m(= /c)
查表、计算可得 Λm
即:通过1 mol 电子电量时,任一电极上发生得失1 mol 电 子的电极反应。电极上析出或溶解的物质的量与之相应。
物理化学-第七章-电化学

通入的总电量:Q I t 0.23060 360库仑
电极上起化学反应物质的量:
n Q 360 0 00373mol zF 196500
析出Ag的质量: m=n×MAg=0.00373×107.88=0.403g
二、电导、电导率和摩尔电导率
体积与浓度的关系如何呢?
c n V
(mol·m-3)
若n为1mol
Vm
1 c
m
Vm
c
S·m2·mol-1
注意:c的单位:mol﹒m-3
3.电导、电导率和摩尔电导率之间的关系
G 1 R
K l A
G K
m
Vm
c
例: 298K时,将0.02mol·dm-3的KCl溶液放入 电导池,测其电阻为82.4Ω,若用同一电导池充 0.0025mol.dm-3的K2SO4溶液,测其电阻为 326Ω,已知298K时,0.02mol·dm-3的KCl溶液 的电导率为0.2768S.m-1 (1)求电导池常数; (2)0.0025mol.dm-3的K2SO4溶液的电率; (3)0.0025mol.dm-3的K2SO4溶液的摩尔电 导率。
★电池 汽车、宇宙飞船、照明、通讯、 生化和医学等方面都要用不同类型的化学 电源。
★ ⒊电分析 ★ ⒋生物电化学
§7-1 电解质溶液的导电性质 一、电解质溶液的导电机理
1.导体: 能够导电的物体叫导体。
第一类: 靠导体内部自由电子的定向运动而导电的物体
如 金属导体
石墨
性质:
A.自由电子作定向移动而导电
F:法拉第常数,即反应1mol电荷物质所需电量 1F=96500库仑/摩尔
物理化学第7章 电化学

放置含有1 mol电解质的溶液,这时溶液所具有的
电导称为摩尔电导率 Λ m
Λ m
def
kVm
=
k c
Vm是含有1 mol电解质的溶液
的体积,单位为 m3 mol1,c 是电解
质溶液的浓度,单位为 mol m3 。
摩尔电导率的单位 S m2 mol1
注意:
Λ 在 后面要注明所取的基本单元。 m
b、强电解质: 弱电解质:
强电解质的Λ m
与
c
的关系
随着浓度下降,Λ 升高,通 m
常当浓度降至 0.001mol dm3 以下
时,Λ 与 m
c 之间呈线性关系。德
国科学家Kohlrausch总结的经验
式为:
Λ m
=Λm (1
c)
是与电解质性质有关的常数
将直线外推至 c 0
得到无限稀释摩尔电导率Λm
-
- 电源 +
e-
+
e-
阴
阳
极
极
CuCl2
电解池
阳极上发生氧化作用
2Cl aq Cl2(g) 2e
阴极上发生还原作用
Cu2 aq 2e Cu(s)
三、法拉第定律
Faraday 归纳了多次实验结果,于1833年总结出该定律
1、内容:当电流通过电解质溶液时,通过电极 的电荷量与发生电极反应的物质的量成正比;
作电解池 阴极: Zn2 2e Zn(s)
阳极 2Ag(s) 2Cl 2AgCl(s) 2e
净反应: 2Ag(s) ZnCl2 Zn(s) 2AgCl(s)
2.能量变化可逆。要求通过的电流无限小。
二、可逆电极的种类
1、第一类电极
物理化学07电化学
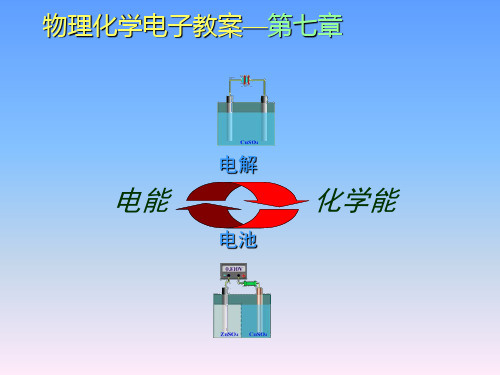
⑴ 通入电量 Q ;
⑵ 通电时间 t ;
⑶ 阳极上放出氧气的物质的量。
解: 1 Au3+ e = 1 Au
3
3
OH
1 4
O2
1 2
H2O e
(1) Q zF 196500197.01.g20mgol-1 /3 Cmol1
⒉ 通电于若干个电解池串联的线路中,当所 取的基本粒子的荷电数相同时,在各个电极 上发生反应的物质,其物质的量相同,析出 物质的质量与其摩尔质量成正比。
Q =n电F
n电:电板反应得失电子的物质的量 F: 法拉第常数在数值上等于1 mol电子的电量。
知元电荷电量为 1.6022 1019 C
F=L·e =6.022×1023 mol-1×1.6022×10-19 C
务各分担2mol,在假想的AA、BB平面上各有2mol正、 负离子逆向通过。
当通电结束,阴、阳两极区溶液浓度相同,但比 原溶液各少了2mol,而中部溶液浓度不变。
1.离子迁移数的定义
1.离子迁移数的定义 2)设正离子迁移速率是负离子的三倍,v 3v ,则
正离子导3mol电量,负离子导1mol电量。在假想的AA、 BB平面上有3mol正离子和1mol负离子逆向通过。
物理化学电子教案—第七章
电解
电能
电池
化学能
第七章 电化学
§7.1 电解池、原电池和法拉第定律 §7.2 离子的迁移数 §7.3 电导、电导率和摩尔电导率 §7.4 平均离子活度因子及德拜-休克尔极限公式 §7.5 可逆电池及其电动势的测定 §7.6 原电池热力学 §7.7 电极电势和液体接界电势 §7.8 电极的种类 §7.9 原电池设计举例
物理化学电子课件第七章电化学基础

第一节 电化学的基本概念
三、离子的电迁移和迁移数
3. 离子迁移数 t有多种测定方法,这里主要介绍希托夫(Hittorf) 法。其原理是:分别测定离子迁出或迁入相应电极区的物质的量及发 生电极反应的物质的量,然后通过物料衡算得到离子迁移数。实验装 置如图7-3所示。
第一节 电化学的基本概念
三、离子的电迁移和迁移数 实验测定中的物料衡算思路为:电解后某离子剩余的物质的量
在电解池和原电池中,一般规定:在电极上发生氧化反应(失电 子)的电极为阳极,发生还原反应(得电子)的电极为阴极;电势较 高的电极为正极,电势较低的电极为负极。下面分别对电解池和原电 池进行讨论。
上述反应发生在电极与溶液的界面处,称为电极反应。电解池中
发生的总的化学反应称为电解反应,此处为
2HCl(l)
第二节 电解质溶液
表7-2 25 ℃时几种浓度KCl水溶液的电导率
第二节 电解质溶液
四、摩尔电导率与浓度的关系
科尔劳施 (Kolrausch)对电解质溶液的摩尔电导率进行了深入的 研究,根据实验结果得出结论:在很稀的溶液中,强电解质的摩尔电 导率Λm与其浓度c的平方根呈直线关系,即科尔劳施经验式:
2. 在稀溶液中,电解质的浓度和价型是影响γ±的主要因素。离子 强度I正是为反映这两个因素的综合影响而提出的,其定义为:
即溶液中每种离子的质量摩尔浓度乘以该离子电荷数的平方,所 得诸项之和的一半称为离子强度。
第二节 电解质溶液
3.德拜-休克尔极限公式 子活度因子 γi及离子的平均活度因子γ±的计算公式:
n电解后=该离子电解前的物质的量n电解前±该离子参与电极反应的物质的 量n反应±该离子迁移的物质的量n迁移,即
式(7-7)中的正负号根据电极反应是增加还是减少该离子在溶 液中的量以及该离子是迁入还是迁出来确定。
物理化学第七章电化学

§7-2 离子的迁移数
通电前后各区域物质的量的变化情况:
上述结果表明: 电解后:三个区域的溶液都是电中性的 电解后,两电极附近的阴极区和阳极区中,浓度变化不相同。
Q u 1 = n阴 Q_ u 3 式中 n阴 、 n阳 分别表示阴极区和阳极区内电解质克当量数(物质 的量)的减少。 2、离子的迁移数 某种离子的迁移数ti是指该离子迁移的电量Q+与通过溶液的总电 n阳
§7-1 电化学的基本概念和法拉第定律
如图所示:
§7-1 电化学的基本概念和法拉第定律
直流电源与两电极相连接,电流方向是电源外电路中由正极流 向负极,而电子流动的方向正好与之相反,是由电源外电路中由 负极流向正极。 电极反应 :电子流到电极上,那么在电极上就会进行有电子得失 的化学反应 规定 :发生氧化反应(也就是失去电子的反应)的电极就称为阳 极 发生还原反应(也就是得到电子的反应)的电极称为阴极。
m
§7—3 溶液的电导率和摩尔电导率
2、电导的测定,电导率和摩尔电导率的计算: 电导是电阻的倒数,因而可 电阻箱电阻 通过测定电解质溶液在某一 电导池中的电阻来确定其电 电可 导变 导,测定电阻可通过惠茨通 池电 电容 (wheatstone)电桥: 容( 如图示: )抵
消
A
D
阻待 测 电
B C
检零器
,这种离子的浓度反而降低了。
电解质实例: 1、两个惰性电极组成的电解池,假想可分为三个部分: 阴极区、中间区、阳极区 2、电解池中的溶液含有16克当量/mol的1—1型电解质。 3、通过电解池的总电量为4F(4mol F) 4、负离子的迁移速度U-是正离子迁移速度U+的3倍。
§7-2 离子的迁移数 如图所示:
物理化学第七章-电化学基础
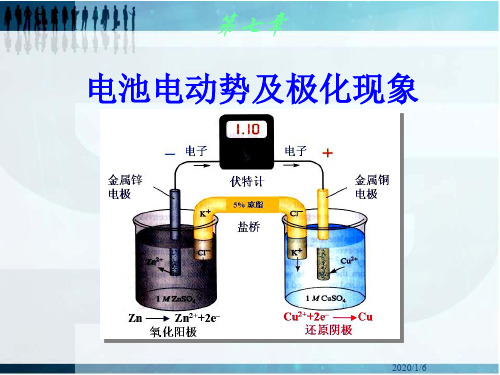
解:Pb+2AgCl=PbCl2+2Ag
ΔrGm=-zFE=-2×96485×0.490=-94555J/mol
rSm
zF
(
E T
)p
296485 (1.8104 )
34.73J K1
mol1
ΔrHm=ΔrGm+TΔrSm=-94555-298×34.73=104905J/mol
7-11 金属的电化学保护 7-12 化学电源
2020/1/6
§7-1 电极电势和电池电动势
一、原电池符号 二、电极电势和电池电动势
2020/1/6
一、原电池符号
2020/1/6
一、原电池符号
与工程化学中学过的一样,负极写作边,正极写右 边,固体或液体与溶液接界用“│”隔开,液体和液 体接界用盐桥符号“‖”隔开。电解质要注明活度,气 体要注明分压,正负即可不注明。如
2020/1/6
一、可逆电池构成条件
1、电池反应互为逆反应 电池反应互为逆反应才能保证系统能够恢复原状。 如铅酸、铜锌等电池皆为可逆电池,而伏达电池、 锌锰干电池等就不能构成可逆电池。
2、电池在充放电时的电流为无穷小 由于电池都有内阻,若有电流通过必然有功转化为 热,而热功转化是不可逆的。
2020/1/6
Qr
zFT
(
E T
)
p
2020/1/6
二、电动势与电池反应热力学函数间的关系
例题:已知25℃时,电池 Pb,PbCl2|KCl|AgCl,Ag 的E=0.490 V, = -1(.8TE0)×p 10-4 V/K。 (1)写出电池反应;
(2)求电池反应的ΔrGm、ΔrSm、ΔrHm、Qr
物理化学下册第七章电化学讲义

m n M z Q F M 2 2 9 0 6 A 5 0 0 2 C 0 m m in o l 1 6 3 .5 g .m o l 1
=7.898gLeabharlann (2) 阳极反应:2Cl- − 2e-→Cl2
n(Cl2)n(Cu)
V n R T 0 .1 2 4 4 m o l 8 .3 1 5 Jm o l 1K 1 2 9 8 K
即:Q=Q++Q-
或: I=I++I-
而: 正离子的运动速度v+ 负离子的运动速度v - QQ , I I
通电 t 时间后,两极附近溶液浓度不同
23 23
§7.2 离子迁移数
离子B的迁移数(transference number):离子B所
运载的电流与总电流之比,用符号tB表示。
def
tB
IB I
如果溶液中只有一种电解质,则:
t t 1
25
电迁移过程示意图
通电前(a): 各区均含有6mol阴离子(-)和阳离子(+) 通电4F电量 : 电极反应(b):阴, 阳极分别发生4mol电子还原及氧化反应。
溶 液 中(c):若υ+=3υ- 中间区电解质物质的量维持不变 阴极区电解质物质的量减少1mol 阳极区电解质物质的量减少3mol
物理化学
Electrochemistry
Copyright © 2007 WUST. All rights reserved.
1
本章基本要求
1 了解电化学研究的主要内容,掌握电解质溶液的导电机理、 法拉第定律、电化学基本概念与术语(电解池、原电池、 阴极、阳极)。
2 掌握电解质溶液的电导、电导率和摩尔电导率、极限摩尔 电导率的概念,掌握电导的测定和电导率、摩尔电导率的 计算,掌握离子独立运动定律及与离子摩尔电导率的关系, 了解无限稀释时离子迁移数、离子的摩尔电导率和离子电 迁移率的关系。
物理化学第七章电化学全解

第七章电化学7.1电极过程、电解质溶液及法拉第定律原电池:化学能转化为电能(当与外部导体接通时,电极上的反应会自发进行,化学能转化为电能,又称化学电源)电解池:电能转化为化学能(外电势大于分解电压,非自发反应强制进行)共同特点:(1)溶液内部:离子定向移动导电(2)电极与电解质界面进行的得失电子的反应----电极反应(两个电极反应之和为总的化学反应,原电池称为电池反应,电解池称为电解反应)不同点:(1)原电池中电子在外电路中流动的方向是从阳极到阴极,而电流的方向则是从阴极到阳极,所以阴极的电势高,阳极的电势低,阴极是正极,阳极是负极;(2)在电解池中,电子从外电源的负极流向电解池的阴极,而电流则从外电源的正极流向电解池的阳极,再通过溶液流到阴极,所以电解池中,阳极的电势高,阴极的电势低,故阳极为正极,阴极为负极。
不过在溶液内部阳离子总是向阴极移动,而阴离子则向阳极移动。
两种导体:第一类导体(又称金属导体,如金属,石墨);第二类导体(又称离子导体,如电解质溶液,熔融电解质)法拉第定律:描述通过电极的电量与发生电极反应的物质的量之间的关系=n=FQξzF电F -- 法拉第常数; F = Le =96485.309 C/mol = 96500C/molQ --通过电极的电量;z -- 电极反应的电荷数(即转移电子数),取正值;ξ--电极反应的反应进度;结论: 通过电极的电量,正比于电极反应的反应进度与电极反应电荷数的乘积,比例系数为法拉第常数。
依据法拉第定律,人们可以通过测定电极反应的反应物或产物的物质的量的变化来计算电路中通过的电量。
相应的测量装置称为电量计或库仑计coulometer,通常有银库仑计和铜库仑计 。
7.2 离子的迁移数1. 离子迁移数:电解质溶液中每一种离子所传输的电量在通过的总电量中所占的百分数,用 tB 表示1=∑±=-++t 或显然有1:t t离子的迁移数主要取决于溶液中离子的运动速度,与离子的价数无关,但离子的运动速度会受到温度、浓度等因素影响。
物理化学_电化学

无论是原电池还是电解池,其共同的特点是, 无论是原电池还是电解池,其共同的特点是,当外 电路接通时: 电路接通时: 在电极与溶液的界面上有电子得失的反应发生; 在电极与溶液的界面上有电子得失的反应发生; 电子得失的反应发生 溶液内部有离子作定向迁移运动 离子作定向迁移运动。 溶液内部有离子作定向迁移运动。 极板与溶液界面上进行的化学反应电极反应 极板与溶液界面上进行的化学反应电极反应 两个电极反应之和为总的化学反应: 两个电极反应之和为总的化学反应: 原电池电池反应; 电解池 电解反应 原电池电池反应; 电解池电解反应 电池反应
AB Ex = EN AB′
9
§7.6 原电池热力学 1. 由E计算∆rGm 计算∆ 计算
例:Zn + CuSO4 === Cu + ZnSO4 恒温、恒压、可逆条件下: 恒温、恒压、可逆条件下: ∆ rGT , p = Wr′ 每摩尔电池反应所做的可逆电功为: 每摩尔电池反应所做的可逆电功为:
∆rGm
电池恒温可逆放电,吸热; 电池恒温可逆放电,吸热;
电池恒温可逆放电,放热。 电池恒温可逆放电,放热。
11
∆r H m = − ZFE + Qr
1) 可逆原电池
反应物
2) 电池外恒压反应
产物
过程(1): 过程
∆H=-ZFE+Qr +
过程(2): 过程 : ∆H=Qp
过程(1)、 是状态函数) 过程 、(2) ∆H 相等 (因H是状态函数 因 是状态函数 与过程有关) 但 Qr ≠ Qp (因Q与过程有关 因 与过程有关 测E 和(∂E/∂T)p 可得到 Qp ∂ ∂
$
RT E=E − ln 2 F aZn2+ ⋅ pH2 / p$ aZn RT ln =E − 2F aZn2+
物理化学第七章 电化学(72)

电解质溶液的电导率可以看着是相距1m的两电极间放置 体积为1m3的电解质溶液的电导。
(3)摩尔电导率m 摩尔电导率---单位浓度的电解质溶液的电导率, 单位为S· 2· -1 m mol
m c
例题:在291K时,浓度为10mol· -3 的CuSO 4 溶液的电导率为 m 0.1434 S· -1,试求CuSO4的摩尔电导率 m (CuSO4 ) 和 ( 1 CuSO4 ) m 2 1 的摩尔电导率 m ( CuSO4 ) 2 解: 0.1434S m1 m (CuSO4 ) 14.34 103 S m2 mol 1 c(CuSO4 ) 10mol m3
1 0.1434S m 1 m ( CuSO4 ) 7.17 103 S m 2 mol 1 1 2 2 10mol m 3 c( CuSO4 ) 2 注意:
1.计算时浓度c的单位应采用mol· -3表示。 m 2. 在使用摩尔电导率这个量时,应将浓度为c的物质的基本 单元置于 m 后的括号内,以免出错。
单位:m 2 · -1· -1 V s
u t u u
u t u u
已知OH-离子的迁移速度是K+离子的3倍。
通电后:
电解质溶液中各区仍保持电中性,中部溶液浓度不变,但是 阴、阳两极部的浓度互不相同,且两极部的浓度比原溶液都 有所下降,但降低程度不同。
离子电迁移过程中的规律:
2 t ( SO4 ) 1 t (Cu 2 ) 0.711
§7.3 电导、电导率和摩尔电Fra bibliotek率• 3.1 定义
(1)电导G 电导---电阻的倒数,单位为S
G 1
R
1S 11
1
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2、电解池 阳极(Anode)
e Zn
Zn2+ SO42-
Cu
阴极(Cathode)
ZnSO4溶液
CuSO4溶液
组成:电解槽、电极和导线(第一类导体),电解质溶液(第二类 ),外加电源。 通电后在电极上的反应:
与电源的正极相连的电极Zn电极:Zn→Zn2++2e (氧化反应 阳极) 与电源的负极相连的电极Cu电极:Cu2++2e→Cu (还原反应 阴极) 电解反应:Zn+Cu2+→Cu+Zn2+
② Faraday定律可以在任何T 和P下使用。
③ 实际电解时,由于存在副反应,如镀锌工艺中,在阴极 除了有Zn析出外,还有H2的生成。所以实际消耗的电量要 比理论电量大,可计算电流效率:
电流效率=理论电量÷实际电量×100%
§7-2离子的迁移数
电解质溶液之所以能导电,是由于溶液中 含有能导电的正、负离子,为了描述电解质溶 液的导电行为,引入了离子电迁移率、离子迁 移数。
1 3
Au(s) 和
1 4
O2 (g)
1 Au( s ) M( )=1/3197.08=65.67 所以 的摩尔质量为: 3 Au(s)
1 3
同样: M( 1 O2 (g) )=1/432=8 4 (a) 由Faraday定律:
Q m M Z F
mZ F 1.20 1 96500 Q 1763C M 65.67
I I I
二、法拉第定律(Faraday Law) Faraday(英国物理、化学家)通过大量电解实验的结果, 于1833年总结出了一条基本规律。
对各种不同的电解质溶液,电解时,每通过1mol电子电 量时,在任一电极上发生得失1mol电子电极反应 1mol电子的电量——Faraday常数
导电机理 电子导体:电子定向运动 离子导体:离子在溶液中定向迁移 电流流经导体 不发生化学变化 发生电解反应 温度升高 导电性下降 导电性上升
原电池和电解池的共同特点: 当外电路接通时在电极与溶液的界面上有电子得失的 反应发生,溶液内部有离子做定向迁移运动。
电极反应:把电极上进行的有电子得失的化学反应. 两个电极反应的总和对原电池叫电池反应,对电解池叫电解 反应。 注意:阴离子在阳极失去电子,失去电子通过外线路流向电源 正极.阳离子在阴极得到电子. 发生氧化反应的电极叫阳极,发生还原反应的电极叫阴极. 正负极依电势高低来定.
1 3
1 2
Au e 1 3 Au(s)
H2O e 1 O (g) H 2 4
3
阳极 :
1 电解反应: 3
1 1 Au3 (aq.) 1 H O ( l ) Au( s ) 2 2 3 4 O2 ( g )
电极反应中得失电子数Z=1,对应电解产物的基本单元:
注意:M和Z的值随所取的基本单元而定。 例:用强度为0.025A的电流通过Au(NO3)3的溶液(Pt作为电 极),当阴极上有1.20g Au(S)析出时,试计算: (a)通过了多少电量? (b)需通电多长时间? (c)阳极上将放出多少氧气(气体在标准状况STP下的体积) 解:若电极反应: 阴极 :
CuSO4溶液 (还原反应) 正极或阴极 (氧化反应) 负极或阳极
在电解池或原电池中,有电流通过时,第一类导体(包 括电极和导线)中的电子和第二类导体中的离子在电场作用 下都作定向移动: 电子: 与电流方向相反 离子: 阳离子(anion)总是向阴极移动 阴离子(cation)总是向阳极移动
在第二类导体中,电流的传导是由阴、阳离子的移动而 共同承担,即:
在STP时,O2(g)的体积为:
V(O2)=4.57×10-3mol×22.4dm3/mol=0.102 dm3
注意:
①Faraday定律中,由基本单元决定的摩尔质量M和得失电子 数Z。本书规定,当电极反应中Z=1时,电解质作为基本单 元,如H2SO4,AgNO3 ,CuSO4: 电极反应分别为: 基本单元
H e 1 2 H2 (g)
Ag e Ag(s)
1 2 2
1 2
H2
Cu
Ag
1 2
Cu
e 1 2 Cu(s)
当通1F电量,在相应的阴极上将析出物质的量分别为: 1mol(½H2)、1mol(Ag) 、 1mol( ½Cu), 它们的质量比为: 1.008:107.9:31.8
F L e 6.0221023 1.6021019 96500C mol1
若电极反应为: MZ++Z+e-→M 通过电解,欲得1mol的M物质,则需通过 Z+F 的电量。 若通过的电量为Q时,可得M的摩尔数n:
n Q Z F
Байду номын сангаас
质量
Q m M Z F
—Faraday定律
一、离子的电迁移现象 在电化学中,常将离子在电场作用下而引起的定向 运动称为电迁移,当电流通过电解质溶液时,发生: ①两个电极上的反应 ②正离子向阴极迁移,负离子向阳极迁移,由正 、 负 离子共同完成导电任务。 由于离子性质不同,它们的迁移速率是不相等的,用图 来讨论离子的电迁移现象:
(b)由电流的定义: I
得:
Q
Q 1763 7.05 10 4 S 19.58hr I 0.025
(c)在阳极上析出的氧气的摩尔数应等于在阴极上析出Au(S) 的摩尔数(前提是所取的基本单元相同)
即:
1 n1 Au n 3 4 O2
1 1 1 1.20 nO 2 n 4 O 2 4.57 10 3 mol 4 4 65.67
3、原电池(primary cell) 与电解池相反,利用两个电极上的反应将化学能转变为电 能的装置,如图: 丹尼尔电池: + Cu - Zn 阳极(Anode) 阴极(Cathode)
Zn2+ SO42-
ZnSO4溶液 原电池的电极反应 Cu极:Cu2++2e→Cu Zn极: Zn→Zn2++2e
第七章 电化学
电化学 —是研究电能和化学能之间相互转化及转化过程中有 关规律的科学。 物理化学中的电化学研究量方面的内容:
1)电能转化为化学能的过程叫电解池 2)化学能转化为电能的过程叫原电池
§7.1 电解质的导电机理和法拉第定律
一、基本概念 1、电导体分为两类:电子导体(第一类导体)和离子导体(第 二类导体) 区别 :
