第八章卤代烃
第八章 卤代烃

CH3CH
CH CH3
CH2CH3
Cl
3-甲基-2-氯戊烷
陈明
CH3
CH
CH
CH2CH3
CH3 Cl
2-甲基-3-氯戊烷
CH3CH CH2 CH3
CH Br
CH3
2-甲基-4-溴戊烷
陈明
H
Cl H (1S,2S)-1-溴-2-氯环己烷
Br
CH2 CH CH CH3
3-甲基- 4 -氯-1-丁烯
CH2 Cl
1)通式:
Nu + R X
亲核试剂 亲核试剂: 底物
-
Nu R + X
产物
-
离去基团
OH-、CH3O-、HS-、X-、CN- ; H2O、NH3、ROH 等;
陈明
2)常见的亲核取代反应
OHR'OR'COOR X -X
o
R-OH R-OR' R-OCOR' R-NR'3 XR-C N R-SH R-C CR'
极性溶剂有利于 SN1 反应的进行
陈明
要强调的是:SN1 和 SN2 反应均受溶剂的很大影响,但 是它们的作用机制不同。 SN2 在质子性溶剂中是不利的,因为亲核试剂被溶剂化 作用降低了反应活性 SN1 反应却是在质子性溶剂中有利的,因为反应中产生 活泼中间体碳正离子的过渡态能被溶剂化作用稳定,生 成的阳离子和阴离子均可被溶剂化作用稳定。
一、分类和命名
根据所含卤素种类,分为氟代烷、氯代烷、溴代烷及碘代烷;
根据所含卤素原子个数,分为一元、二元、多元卤代烷等;
CH3Cl CH3CH2F CH3CH2I CH3CH2Br 2°) 根据卤素所连接饱和碳原子的类型,又可分为伯( 1°)、仲( CH3Cl CH2Cl2 CHCl3 CCl4
有机化学第8章卤代烃

在SN2反应中
进攻试剂是从离去基团的背面进攻碳原子的。 进攻试剂是从离去基团的背面进攻碳原子的。 当Nu与碳原子接近时,C-Nu之间的化学键逐渐形成,而C-X之间的 Nu与碳原子接近时,C Nu之间的化学键逐渐形成,而C 化学键逐渐变弱,三者基本在同一直线上,形成了反应的过渡态,中心 碳由sp 转化为sp 碳由sp3转化为sp2杂化状态, Nu继续接近碳原子并与碳原子完全键合,离去基团完全离去,由过渡状 Nu继续接近碳原子并与碳原子完全键合,离去基团完全离去,由过渡状 态变为产物。
1)被羟基取代 加热 R-X + KOH(NaOH,水溶液) KOH(NaOH,水溶液) 2)被烷氧基取代 R-X + R`ONa R-O-R` +NaX R此反应也称为Wiliamson合成反应 合成反应。 此反应也称为Wiliamson合成反应。 3)被NH3取代 R-X + NH3 R-NH2(胺) + HX 胺是有机碱,它与反应生成的HX成盐 成盐, 胺是有机碱,它与反应生成的HX成盐,RNH3+XR-OH + KX
查依采夫规律
一般叔卤代烷最易消去,而伯卤代烷最难。 一般叔卤代烷最易消去,而伯卤代烷最难。仲或叔卤代烷 氢可以消去,因而产物不同。 有几个β氢可以消去,因而产物不同。 1875年俄国化学家查依采夫根据大量事实指出 年俄国化学家查依采夫根据大量事实指出: 1875年俄国化学家查依采夫根据大量事实指出:在β-消 去反应中主要产物是双键碳原子上烃基最多的烯烃, 去反应中主要产物是双键碳原子上烃基最多的烯烃,即得 到最稳定的烯烃。-- 。--查依采夫规律 到最稳定的烯烃。--查依采夫规律
溴甲烷在NaOH溶液中反应生成甲醇,反应时OH 溴甲烷在NaOH溶液中反应生成甲醇,反应时OH-从背面接近中 心碳原子,必须克服三个氢原子的阻力,同时三个C 心碳原子,必须克服三个氢原子的阻力,同时三个C-H键的偏 转使键角发生变化,因而体系的能量升高。达到过渡状态时,能 量也达到最高点。随着溴离子的进一步离去和C 量也达到最高点。随着溴离子的进一步离去和C-O键的进一步 形成,体系的能量逐渐降低,最后形成产物。
第八章卤代烃

136第八章 卤代烃8.1 绪论烷基卤化物是指烷烃中的氢原子被卤素原子(氟、氯、溴和碘)所取代的化合物。
例如,CH 3Cl 和CH 3CH 2Br 是烷基卤化物,烷基卤化物也被称为卤代烃。
烷基卤化物分为伯卤化物(10)、仲卤化物(20)和叔卤化物(30)。
这种分类是基于卤素直接相连的碳原子。
如果带有卤素的碳原子仅仅与其他一个碳相连,这个碳原子就是伯碳原子,烷基卤化物就属于伯烷基卤化物。
如果带有卤素的碳原子它本身就连有其他两个碳原子,这个碳就是仲碳,该烷基卤化物就是仲卤化物。
如果带有卤素的碳原子它连有其他三个碳原子,那么这个碳就是叔碳,该烷基卤化物就是一个叔烷基卤化物。
下面是伯、仲和叔烷基卤化物的代表。
H CC H H H H10H C C C HH H HCl 20CH 3C CH 3CH 30碳碳碳虽然我们用符号10,20,30,但是我们不能说第一度,第二度,第三度,应该是伯、仲、叔,也可称为一级,二级,三级。
8.2 烷基卤化物的命名卤素取代的烷烃是按照IUPAC 系统命名法来命名的:CH 3CH 2ClCH 3CH 2CH 2F CH 3CHBrCH 3氯乙烷1氟丙烷2溴丙烷当主链上既有卤素又有烷基取代时,不管是卤素还是烷基,从靠近取代基一端向另一端编号。
如果两个取代基到链的末端的距离相等,按照字母的先后顺序从一端编起。
CH 3CHCHCH 2CH 3ClCH 3CH 3CHCH 2CHCH 3ClCH 32-氯-3-甲基戊烷 2-氯-4-甲基戊烷137很多简单卤代烃的习惯命名仍然被广泛应用,然而在这种习惯命名体系中被称为功能性命名,卤代烃被命名为烷基卤化物。
(下面这些命名也被IUPAC 所接受)CH 3CH 2ClCH 3CHCH 3(CH 3)3BrCH 3CHCH 2ClCH 3CCH 2BrBrCH 3CH 3CH 3乙基氯 异丙基溴 叔丁基溴 异丁基氯 新戊基溴8.3 卤化物的结构和物理性质8.3.1卤化物的结构烷基卤化物的卤素原子所连的碳原子是sp 3的,基团的排列围绕碳原子,因此,一般是四面体形。
第八章 卤代烃..

(R=1, 2 , 3 烷基 ; RCH=CH-; RCH=CHCH2-; Ph-. X: I, Br, Cl)
Corey-House合成法——制备烷烃
[CH3(CH2)3]2LiCu + 2CH3(CH2)6Cl
Et2O, 5days 0℃75%
2CH3(CH2)3-(CH2)6CH3 + LiCl +CuCl
无水乙醚
Grignard试剂在醚中有很好的溶解度,醚作为 Lewis碱,与Grignard试剂中的Lewis酸中心镁原子 形成稳定的络合物。
C2H5 C2H5
R O Mg X O
C2H5 C2H5
格氏试剂很易与含活泼H的化合物如 H2O、R-OH、NH3 、 R-NH2 、 HX、 HOOCCH3、炔氢等反应生成相应的烃
卤代烃一般使用伯卤代烃,有时也可使用仲卤 代烃,但仲卤代烃或叔卤代烃在反应条件下往往会发生 消除得到烯烃,不适用于制备。 而乙烯型、苯基型一般都不发生上述反应
1. 水解(被-OH取代): 卤代烃与 NaOH 或 KOH 的水溶液共热,-X被OH取代,产物为醇。这个反应也叫卤代烃的碱性 水解。
R—X + NaOH
伯卤代烃 CH3CH2Cl 2.按C-X键C的类型 仲卤代烃 CH3CHClCH3 叔卤代烃 (CH3)3C-Cl
3.按X的种类 氟代烃(制法和性质特殊) 氯代烃、溴代烃、碘代烃
二、命名
1. 普通命名法: 卤(代)某烃或某烃基卤。 CHCl3 C2H5Cl n-C4H9-Cl 正丁基氯
三氯甲烷
氯乙烷 i-C4H9-Cl 异丁基氯
样作为取代基来命名。 ②编号:根据最低系列原则将主链编号。
③取代基: 优先顺序大的基团后列出。 3 2 1 CH3CHCH2B r CH3 1 H 3C 2 CH 3 CH 4 CH
08卤代烃

2.较复杂的卤代烃按系统命名法命名:
①.卤代烷,以含有卤原子的最长碳链作为主链,将卤原子或其他支链作为 取代基。命名时,取代基按“顺序规则”较优基团在后列出。[烷烃为母体] 例如: 2,3二甲基-6乙基-5-氯 辛烷
CH3CH2CHCHClCH2CHCHCH3 C2H5 CH3CH3
CH3CH2CHCHBrCH2CH3
⑵.与金属锂反应
石油醚
C4H9X + 2Li
C4H9Li + LiX
有机锂化合物的性质与格式试剂很相似,反应性能更为活泼,遇水、醇、 酸等即分解。 有机锂也可与金属卤代物作用生成各种有机金属化合物。
RLi + Cu
R2CuLi +LiI
二烃基铜锂称为铜锂试剂,它是一个很好的烃基化试剂。可以用他合成较复杂的烷烃。
第八章 卤代烃
第一节
卤代烃的分类、命名及同分异构现象
卤代烃:烃分子中一个或多个氢 取代后所生成的化合物。 R-X, X=Cl.、Br、I 、F 卤原子是卤代烃的官能团。 卤代烃的性质:比较活泼,能发生多种化学反应,转化成各种其他类型的化 合物。引入卤原子,往往是改造分子性能的第一步加工,在有机合成中起着桥梁 的作用。 自然界极少含有卤素的化合物,绝大多数是人工合成的。
3.邻近基因的参与
α-溴代烷丙酸负离子按SN1历程进行水解,醇解反应时,其构型完全保持不变。
H OO-
C
CH3 Br
C
OOHຫໍສະໝຸດ -HSN1
C
CH3 OH
C
O
100% 构 型 保 持
这种异常现象的产生,可能是α-溴代丙酸负离子按SN1历程电离产生碳正离子时,分 子内中心碳原子邻近带负电荷的羧基离子,连接溴离子的背面进攻中心碳原子,进行了分 子内的类似于SN2反应,生成不稳定的内酯,产生碳原子的构型发生了转化,此时,羧基 负离子好象在背面固定了碳正离子的构型。当亲核试剂(HO-)进攻时,就只能从原来溴离 子脱离的方向引入,手性碳原子的构型再发生一次转化。经过两次转化,结果使100%保持 原来的构型不变。如下图所示
有机化学 第八章卤代烃

对SN2的影响
空间效应
H2C CH CH2X Ph CH2 X
注意:
H H
Nu H L H
〉SN2反应速度最快
p-π共轭,稳定过渡态, △E活化低快
知识点 苄基 (苯甲基)> 烯丙基 > CH3 > 1º > 2º > 3º
对SN1的影响 SN1的速控步骤:
电子效应 空间效应
RX R+ + X-
R1 2 HO C R R3 R1 R2 C OH R3
第一步生成平面三角形碳正离子, OH-从平面的两边进攻的机会均等。 例:
H3CO + CH3COOH O H2O/O O CH O C CH3 H3CO CH OH SN1
大多亲核取代反应既非完全转化,也非完全外销旋化。
例:
C6H5
CH CH3 + H2O/丙酮 Cl
凡是能稳定C+的因素,也稳定生成它的过渡态。
△E ----反应快( SN1 主要考虑电子效应)
例:
H3CO CH2 X
p-π共轭,稳定C+
空间效应也有影响:
H3C O CH2+
对SN1的影响
电子效应 空间效应
空间效应
3º最拥挤,解除拥挤的要求最强—易形成C+ CH3相反,解除拥挤的要求最小—难形成C+
亲核试剂 Nu
-
R CH2 Nu + X 离去基团
底物
Nucleophilies
反应是由带负电荷(或孤队电子)的试剂进攻带正
电荷的C原子引起的——亲核取代(SN) Substitution Nucleophilic
常见的亲核取代反应:
chapter8 卤代烃

CH2X
3- 甲基 -4- 氯 -1-丁烯 2- 甲基 -1- 氯 -3- 丁烯
×
4 - 甲基 -5- 氯环己烯
或苄基卤( 卤化苄 或苄基卤(氯、溴、碘)
8.3 脂肪族卤代烃的化学性质
C
Nu :
亲核取代
(Nucleophilic Substitution)
选最长碳链为主链, 碳原子数命名为 (1)选择主链 选最长碳链为主链,根据碳原子数命名为 )选择主链—选最长碳链为主链 根据碳原子数 某烷” 注 不是含卤原子最长碳链 不是含卤原子最长碳链) “某烷”;(注:不是含卤原子最长碳链 采用最低秩序原则( (2)碳原子编号 采用最低秩序原则(即从最靠近取代基一 )碳原子编号—采用最低秩序原则 端开始编号,依次标上1, , 等数字),取代基写在 某烷” 等数字),取代基写在“ 端开始编号,依次标上 ,2,3等数字),取代基写在“某烷” 之前,并以半字线连接; 半字线连接 之前,并以半字线连接; (3)主链上的卤原子或取代基按秩序规则顺序排序,并以较 )主链上的卤原子或取代基按秩序规则顺序排序, 优基团列在后(一般卤素为较优基团,应写在后面)。 )。卤素的 优基团列在后(一般卤素为较优基团,应写在后面)。卤素的 秩序是: 秩序是:氟、氯、溴、碘。 CH3-CH-CH-CH3 CH -CH -CH-CH-CH -CH
4. 氰解: 氰解:
R X + NaCN
C2H5OH ( NaCN)
R CN
H3O+
R COOH
增加一个碳原子
该反应的重要意义除可增长碳链外, 该反应的重要意义除可增长碳链外,还可以通过氰 基转化为―COOH、 ―CONH2等官能团。 等官能团。 基转化为 、 该反应与卤代烷的醇解相似, 不能使用叔卤烷, 使用叔卤烷 该反应与卤代烷的醇解相似,亦不能使用叔卤烷, 否则将主要得到烯烃。 否则将主要得到烯烃。
有机化学-第八章卤代烃ppt课件

三、卤代烷的互换
§ 8—3 卤 代 烷的性质
一、物理性质 (略) 二、化学性质
卤代烃的化学性质活泼,且主要发生在C—X 键上。 ① 分子中C—X 键为极性共价键,碳带部分正电荷,易受带负电荷
或孤电子对的试剂的进攻。
CH C CH CH -I CH CH -Cl CH CH -Br 3 3 3 2 卤 代 烷 : 3 2 3 2 1 . 9 1 0 2 . 0 5 2 . 0 3 D 偶 极 矩 μ ( )
R-CH2-X
R-CH=CH-X 乙烯式 R-CH=CH-CH2-X 烯丙式 R-CH=CH(CH2)n-X n≥2 孤立式
X CH 2 X
卤代芳烃
乙烯式 烯丙式
按卤素所连的碳原子的类型
R-CH -X 2
伯 卤 代 烃
R CH-X 2
R C-X 3
仲 卤 代 烃 2 ° 级 卤 代 烃 ( ) 1 一 级 卤 代 烃 ° ( ) 二
CH -CH-CH -CH-CH -CH 3 2 2 3 Cl CH 3
CH -CH -CH-CH-CH -CH 3 2 2 3 Br Cl
3 -氯 4 -溴 己 烷 3 -溴 4 -氯 己 烷 ×
3、卤代烯烃命名时,以烯烃为母体,以双键位次最小编号。
1 -甲 CH = CH-CH-CH -Cl 3 4 -氯 基 丁 烯 2 2 1 -氯 2 -甲 3 CH 基 丁 烯× 3 Cl CH 3
2、与氰化钠反应
醇 R C H C N + N a X R C H X + N a C N 2 2 腈
R COOH CH2 R COOH 1°反应后分子中增加了一个碳原子,是有机合成中增长碳链的方法之一。
2°CN可进一步转化为–COOH,-CH2NH2等基团。
第八章-卤代烃

2 与碱金属的反应
(1) 和钠反应
2RX + 2Na
R R + 2NaX Wurtz反应
(2) 和锂反应 在氮气或氩气的保护作用下,生成有机锂化合物。
C4H9Cl Et2O
C -10 °
C4H9Li
LiCl
有机锂试剂的反应与格氏试剂相似,但比格氏试剂更为活泼。
OCH3 H C4H9Li OCH3 Li C4H10
诺贝尔化学奖 (1912)
RMgX
Grignard试剂
活性:
>
R I R Br
>
R Cl
>
R F
Victor Grignard (1871 ~1935)
溶剂:乙醚、四氢呋喃(THF)
、其他醚类以及苯
溶剂作用:既是溶剂,又与格氏试剂络合成稳定的溶剂化物,是稳 定化剂。 R CH C H
2 5
2 5
离去基团:带着一对电子离去。 1.水解反应 和NaOH或KOH的水溶液共热,生成相应的醇。
RCH2-X + NaOH 水 RCH2OH + NaX
加NaOH是为了加快反应的进行,使反应完全。
2.与醇钠(RONa)反应: (Williamson合成法)
' R-X + RONa R-O R' + NaX 醚
状态: 1C-3C的氟代烷、1C-2C的氯代烷和溴甲烷为气体,其他一卤代
绝大多数卤代烃不溶于水,但能溶于许多常用的有机溶剂, 溶解性:
二、化性:
自身异裂
C X
C
Nu
+ X
亲核取代反应
R
CH2 CH CH
华中科技大学有机化学第八章 卤代烃
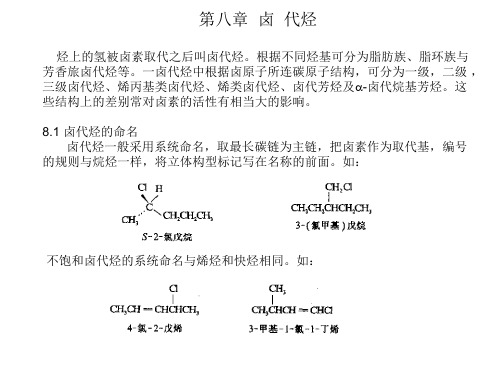
(3) SN1与SN2反应影响因素的比较 它们都属取代反应,但历程不同,因此影响反应速度的因素也各异。 扼要归纳于下表。
如何判断亲核取代反应按SN1还是SN2历程进行,由卤代烃的烃基 部分决定。烃基为伯基或者甲基一般按SN2历程,为叔丁基按SN1历 程,为仲基,烯丙基或者苄基可以是SN1或者SN2。
由实验得知该反应的反应速度与卤代烷和碘负离子的乘积成正比:
同时产物的构型发生转换,即由R转换成S。而叔丁基溴与乙醇加热回流得 到乙基叔丁基醚的反应速度,与乙醇浓度无关,只与叔丁基溴浓度有关。
旅光性的R-2-溴辛烷与水反应得到外消旋的dl-2-辛醇。 从上述实验结果看出,它们用于两种不同的反应过程。推断其历程如下:
这种起始于亲核试剂的进攻而发生的取代反应.称为亲核取代反应, 常用SN来表示(S代表取代反应,N代表亲核试剂进攻)。 亲核取代反应种类很多,在合成上很有用,一些常见的取代反应类 型与取代反应产物的种类如下表。
(1)取代反应历程 SN2与SN1取代反应。反应历程一般是通过测定反应速度与反应物浓度的关 系,以及分析产物构型来推断的。卤代烷与碘化钠在丙酮溶液中的取代反应 是这类反应的典型例子:
从AgX沉淀的速度可以判断此反应的速度,而卤代烷进行SN1与E1反应的 速率为:
NaI-丙酮溶液与卤代烷的反应是按SN2历程进行的, 因此卤代烷的活性次序为:
在卤代烷中加NaI丙酮溶液, 在室温,立即有沉淀产生的为一级溴代烷, 苯甲基卤,烯丙基卤;在50℃,放置3min,有沉淀的为一级氯代烷、二级溴 代烷;50℃,放置长时间出现沉淀的为三级卤代烷、氯代环己烷等。所以, NaI-丙酮与AgNO3-乙醇溶液的测试是很方便的鉴定卤代烷结构的方法。
反应温度升高不利于取代反应。如
有机化学第八章 卤代烃

卤代烷与金属锂反应的活性大小顺序为:R-I > R-Br > R- Cl > R-F 烷基锂在无水乙醚中与碘化亚铜反应生成二烷基铜锂(也叫二 烃基铜锂)。
2RLi + CuI
无水乙醚
0℃
R2CuLi + Li I
二烷基铜锂
二烃基铜锂与卤代烷反应生成各种烃。
R2CuLi
+
R′ X
R′ X 最好是 1°
R-CH=CH2 + NaX + H2O
i) 消除反应的活性:
3°RX > 2°RX > 1°RX
ii)消除方向总是倾向与生成较稳定的共轭烯烃
NaOH Br EtOH
Hβ X X Hβ ' + 2NaOH 乙醇 + 2NaX + 2H2O
iii) 2°、3°RX脱卤化氢时, 遵守扎依采夫(Sayzeff)规则——即主要产物是生成双
×
CH3-CH2-CH-CH2-CH-CH2-CH3 CH3 Cl
CH3-CH-CH2-CH-CH2-CH3 Cl CH3
4-甲基 -2- 氯己烷
3- 氯 -4- 溴己烷 3- 溴 -4- 氯己烷
×
CH3-CH2-CH-CH-CH2-CH3 Br Cl
卤代烯烃命名时,以烯烃为母体,选择含有双键的最长
C2H5 C2H5
R O Mg O X
C2H5 C2H5
和镁反应活性:R-I > R-Br > R-Cl *乙烯卤和芳卤不活泼,要制得Grignard试剂,须改变溶 剂,提高温度。
Br
乙醚 + Mg
H2C
MgBr
CH MgCl MgCl 四氢呋喃
第八章 卤代烃

1、卤代烃的分类§8 -1 卤代烃的分类、异构现象和命名R X CHXR CH XCH 3XCHX 3 CX 4CH 2X 2 卤代烷(饱和卤代烃) 卤代烯烃(不饱和卤代烃)卤代芳烃(芳香族卤代烃)一卤代甲烷 二卤代甲烷 三卤代甲烷 四卤代甲烷X =F 、Cl 、Br 、I第8 章卤代烃南通大学张湛赋RCHR'XRCH 2XRC R'R'X(一级卤代甲烷) (二级卤代甲烷) (三级卤代甲烷)伯卤代烷 仲卤代烷 叔卤代烷2、卤代烷的同分异构现象CH 3CH 2CH 2CH 2CH 2Br CH 3CH 2CH 2CHCH 3CH 3CH 2CHCH 2CH 3BrBr CH 3CH 2CHCH 2BrCH 3CH 3CHCHCH 3Br CH 3CH 3CHCH 2CH 2BrCH 3CH 3CCH 2CH 3CH 3CCH 2BrCH 3CH 3BrCH 33、卤代烃的命名CH 3CH 2CH 2CH 2CH 2Br CH 3CH 2CH 2CHCH 3BrCH 3CH 2CHCH 2CH 3BrCH 3CH 2CHCH 2BrCH 31-溴戊烷2-溴戊烷3-溴戊烷2-甲基-溴丁烷1-CH 3CHCHCH 3BrCH 3CH 3CHCH 2CH 2BrCH 3CH 3CH 2CCH 3BrCH 3CH 3CCH 2BrCH 3CH 33-甲基-1-溴丁烷2-甲基-2-溴丁烷3-甲基-2-溴丁烷2,2-二甲基-1-溴丙烷CH 2C CHCH 3CH 3ClCHCH CH 2CH 2ClCHCH 3CH 3CHCH 2CH 2Cl CH 3CH 2ClCH 32-甲基-3-氯-1-丁烯4-甲基-6-氯-2-己烯3-苯基-1-氯丁烷对甲苯氯甲烷§8 -2 卤代烷的物理性质在常温常压下,氯甲烷、溴甲烷和氯乙烷是气体,其它常见的低级卤代烷都是液体,高级的是固体。
有机化学【卤代烃】

俗名或商品名
Cl CHCl 3 CHI 3 CCl 2F2 Cl Cl Cl Cl Cl 六六六
氯仿
碘仿
氟利昂-1,2
2、卤代烯烃
问题: 试指出下列三个卤代烯烃中氯原子与 双键的相对位置: CH2=CH Cl CH2=CH CH2 Cl CH2=CH CH2 CH2 Cl
(1)卤代烯烃的分类
A.乙烯型卤代烃----卤原子与双键碳原子相连。
CH2=CHCl
B.烯丙基型卤代烃----卤原子与双键相隔一个饱和碳 原子。
CH2=CH-CH2Cl
C.隔离型卤代烯烃----卤原子与双键相隔两个或多个 饱和碳原子。
R-CH=CH(CH2)nX
(2)卤代烯烃的命名
卤代烯烃通常用系统命名法命名。命名 时以烯烃为母体,并以最小位次表示双键的 位置。例如: Br CH3 | | CH2=CH-CH2Cl CH3-CH-CH=C-CH3 3-氯丙烯(烯丙基氯) 2-甲基-4-溴-2-戊烯
(2)与金属钠反应 (武兹(Wurtz)反应)
----只适用于1oRX和某些2oRX 2RX + 2Na R-R + 2NaX
问题: 能否用二种RX反应?
Br
2Na
Cl
+ NaCl + NaBr
武兹-费悌希(Wurtz-Fittig)反应:
Br
CH2CH2CH2CH3
+ CH3CH2CH2CH2Br
(1)水解 :
RX NaOH ROH NaX
H 2O
醇 (2)与醇钠作用 :
RX R' ONa ROR 'NaX
醚
有机化学-卤代烃

X ROH + Mg
(空气)
OH
氧化反应!
30
① 格氏试剂在有机合成上很有用;但它
最忌水、忌活泼氢:否则易分解.
dH+-Od-H
MgX(OH)
d- d+
R-MgX +
H-OR' H-NH2
H-X
H-C CR'
活泼氢
MgX(OR') 合成上无用
RH + MgX(NH2)
定量生成
MgX2 R'C CMgX
C=C + ZnX2
乙醇
-C-CII
C=C + I2
( 双键难加碘的原因)
25
(三) 还原反应
卤代烃发生还原反应产物为烃类化合物。
RX +
Zn + HCl Na + liq.NH3
H2-Pd LiAlH4
RH RH RH RH
(1) 催化氢化: H2 /Pd、Ni 等 (2) 化学还原: LiAlH4 ,NaBH4 ,Zn/HCl ,Na/液NH3 等
叔卤烷(CH3)3CX
1
8.1.2 卤代烃的命名
( 1 ) 普通命名法 “某烃基卤”或“卤(代)某烷”
CH3Cl 甲基氯
CH3CH2Br 乙基溴
C(CH3)3Cl 叔丁基氯
Br 环己基溴
烯丙基溴
氯苯
苄基氯
2
(2)系统命名:(把卤素作为取代基,烃为母体)
①主链:连有卤原子并且支链最多的最长碳链 ②主链编号:取代基编号依次最小 ③列出顺序:较优基团后列出
71%
29%
23
➢ 查依采夫规则的本质:生成最稳定的烯烃产物
第八章 卤代烃 R-X

(
2-戊烯 %
70 52 13 2
1-戊烯 %
30 48 87 98
(2)进攻试剂:
2-戊烯 % 1-戊烯 %
C2H5O(CH3)3CO-
70 27.5
30 72.5
(3)反应物:
2-烯烃 1-烯烃
Br CH3CH2CHCH3
(CH3)3CCH2C(CH3)2 Br
81% 14%
19% 86%
3. 消除反应的立体化学
(b)单分子消除反应历程(E1) CH3 慢 CH3 C X
CH3 CH3 C CH3 OH E1 OH SN 1 CH3 CH3 C CH3 OH
+ X
CH3
CH3 CH3 C CH2 X
V=k C(CH3)3X
有重排(Wagner-Meerwein重排)
CH3 CH3 C CH CH3
H2SO4
Nu: + R
RX RX RX RX RX + + + + +
X
R
Nu + x:
NaOH R’ONa NaCN NaSN AgNO3
ROH + NaX ROR’ + NaX RCN + NaX RSN + NaX RONO2 + AgX↓
进攻试剂是负离子,HO-, RO-, HS-, CN-, NO3-
1,2(β )-消去:
H C C X + CH3CH2ONa CH3CH2OH C C + CH3CH2OH + NaX
1,1(α )-消去 :
Cl Cl C H Cl Cl Cl C : + HCl
1,3 (γ )-消去:
第八章,卤代烃

B H C—C
CH3—CH—CH 2 δX
过渡态
X
顺式消除
C
C
反式消除
B
H C—C X
从立体化学角度考虑,β-消除可能导致两种不同的顺反异构 体。将离去基团X与被脱去的β-H放在同一平面上,若X与βH在σ键同侧被消除,称为顺式消除;若X与β-H在σ键的两侧 (异侧)被消除,称为反式消除。
CH3Cl + OH
-
60oC H2O
CH3OH + Cl-
反应速率 = k2[CH3Cl][OH-]
No
[ CH3Cl ]
[OH-]
Rate(mol L-1 s-1)
1
2
0.0010
0.0020
1.0
1.0
4.9×10-7
9.8×10-7
3
4
0.0010
0.0020
2.0
2.0
9.8×10-7
19.6×10-7
较大的外消旋化百分比说明主要发生了SN1反应。
离子对机制解释:
RX
R+X紧密离子对
R+
X-
R+ + X 自由碳正离子
溶剂分离子对
SN1反应的另一个特点:反应伴有重排。
CH3 CH3 C CHCH3 CH3 CH3 C
+
CH3
H2O
CH3 Br
H2O
SN1
CH3
C CH3
CHCH3 重排 CH3
+
CH3 CH3 C
H HO- + H C Cl H
第8章--卤代烃PPT课件

CH3
C 2H 5O C 2 H 5 OH
CH3
+
C CH
CH3
CH3
CH3 C CH CH3 (SN2)
CH3OC2H5
CH3
CH3 重排
+
CH3 C CH CH3
CH3
C2H5O CH3
CC22HH55OOHCH3 C CH CH3
.
CH3
29
4) SN1 与 SN2反应的比较 (1) 位能曲线
过渡态
C+中间体
.
26
2) 立体化学
(1)外消旋化(构型反转 + 构型保持)
原因:SN1反应第一步生成的碳正离子为平面构型 (正电荷的碳原子为sp2杂化的);第二步亲核 试剂向平面任何一面进攻的几率相等。
R1
C Br R2
R3
R1
C a R2R3 b
HO
R1
R1
HO C
+
C OH
R2 R3
R2 R3
说明:a、形成过渡态,一步反应。 b、反应活性:CH3-X > 1o > 2o >> 3o
.
49
2、单分子消除(E1)
说明:(1)形成C+离子,两步反应。 (2)易发生重排
.
50
例如:
.
51
二、反应取向和立体化学
1、反应取向 Saytzeff 规则和 Hoffmann 规则:
C2H5
CH
CH3
该法是合成不对称醚的常用方法,称为 Williamson(威廉森)合成法。该法也常用于合成 硫醚或芳醚。
.
12
采用该法以伯卤烷效果最好,仲卤烷效果较差, 但不能使用叔卤烷,因为叔卤烷易发生消除反应生成 烯烃。
第八章 卤代烃

亲核试剂的可极化性是指它的电子云在外界电场影响 亲核试剂的可极化性是指它的电子云在外界电场影响 下变形难易的程度。易变形者可极化性大,进攻碳原 子时,其外层电子云易变形而伸向中心碳原子,降低 形成过渡态的活化能,因此,试剂的可极化性越大, 形成过渡态的活化能,因此,试剂的可极化性越大, 其亲核性也越强。如卤离子的可极化性和亲核性次序 其亲核性也越强。如卤离子的可极化性和亲核性次序 为: I- > Br- > Cl- > FCH3S-和CH3O-的可极化性和亲核性次序为: CH3S- > CH3O而碱性为: CH3S- < CH3O-
H H
Nu
C C
H
X
C
H H
② : 离去基团L的影响 离去基团L 仍然是 I > Br > CI 在SN2反应中,形成过渡态使键拉长,因此,离去基 团的离去倾向越大, SN2反应的速度越快。 ③: 亲核试剂Nu的影响 亲核试剂Nu的影响 亲核试剂参与S 亲核试剂参与SN2反应过渡态的形成,试剂的亲核性 越大,越有利于反应的进行。 试剂亲核性的大小,与其所带的电荷、碱性、 试剂亲核性的大小,与其所带的电荷、碱性、体积 和可极化性大小有关。 可极化性大小有关。 凡带有负电荷的试剂比中性试剂的亲核性强,如: 凡带有负电荷的试剂比中性试剂的亲核性强,如: H2O<HO-,H3N<H2N-,ROH<ROROH<
④: 溶剂的影响 一般增加溶剂的极性,对S 反应不利。因为S 一般增加溶剂的极性,对SN2反应不利。因为SN2反 应在形成过渡态时,由电荷较集中的亲核试剂变成 电荷比较分散的过渡态。
δ-
HO- + R-X
[HO
R
X] X]
δ-
HOHO-R + X
(3) SN1和SN2反应的竞争 两种历程在反应中互相竞争,何种为主?影响因素 是多方面的,包括烷基的结构、试剂亲核性大小、 是多方面的,包括烷基的结构、试剂亲核性大小、 溶剂极性以及离去基团的性质等。 烷基结构的影响主要有两个因素:电子效应和空间 烷基结构的影响主要有两个因素:电子效应和空间 效应。试剂亲核性大小对S 效应。试剂亲核性大小对SN1 反应无影响,但对 SN2反应有影响。溶剂极性的变化,是通过对反应 反应有影响。溶剂极性的变化,是通过对反应 的活性中间体(碳正离子和过渡态)的稳定性的影 响而起作用。离去基团对两种历程的反应有相似的 响而起作用。离去基团对两种历程的反应有相似的 影响。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
βα
CC
快
C C +H
卤代烷消除反应的难易与其烃基结构有关,呈现 3°> 2°> 1°(R3CX > R2CHX > RCH2X > CH3X)的变化规律,消除反应的取向遵循扎依采夫(Saytzeff),即在 β-消除反应 中主要产物是双键碳原子上烃基最多的烯烃。
对于 E2 反应而言,一般倾向于反式消除,即进攻基团 RO-从离去基团 X 的背面接近β氢,这时的位阻最小。 5.亲核取代与消除反应的竞争
CC
KOH/ 醇
CC
HX
KOH /水
CC H OH
3
(4)升高反应温度对消除反应有利,因为消除反应与取代反应相比,需要打断得化学键更 多(C—H,C—X)。 6.卤代烃的制备
(1)烃的直接卤代,例如;
CH3CH3
Cl2 光
CH3CH2Cl
用这种方法制备的卤代烃往往选择性较差。
(2)不饱和烃加成,例如:
X RH + Mg
(Y=
OH,—X,—OR,—NH2,— C CR)
Y
例如:
RMgX + D2O
RD + Mg(OH)X
1
这也是在分子中引入氘的一种常用方法。
RMgX CO2
RCOOMgX
H H2O
RCOOH
本反应常用于由卤代烃制备多一个碳原子的羧酸。
有关格氏试剂与醛、酮作用制备醇的反应将在下一章中学习。
8.2 基本内容
1. 卤代烃的结构特点: 卤代烃中与卤素相连的碳原子以 sp3 杂化轨道和卤素 sp3 杂化轨道重叠形成 C—X σ 键,
由于卤素的电负性较大,使成键的一对电子偏向于卤原子一边,因此碳卤键具有极性,表示
δ + δ-
为 C X 。根据与卤原子相连的碳原子不同,卤代烃可以分为:
RCH2X
无影响
利
素
溶剂
非质子溶剂
质子溶剂
离去基团
I > Br > Cl
4.消除反应:
消除反应也有两种历程,一种双分子反应历程(E2), 另一种是单分子反应历程(E1)。
E2 历程表示为:
H
RO-
Cβ αC
X
δRO H
[ Cβ
] αC δBr
CC
+ ROH + X-
E1 历程表示为:
H
βα
慢
CCX
βα
CC
2
H
R2CHX
R3CX
RCH=CH-X
RCH=CH-CH2X
伯卤代烃
仲卤代烃
叔卤代烃
乙烯式卤代烃
烯丙基式的卤代烃
一般来讲,发生化学反应时,烯丙基式的卤代烃最活泼,乙烯式卤代烃最不活泼。
2.卤代烃的性质
(1)亲核取代
通式:Nu: + R X
R Nu + X:
R—X 是受亲核试剂进攻的底物,Nu:代表亲核试剂,X 称为离去基团。
碱性是指基团与 H+的结合能力,亲核性则是亲核试剂上的电子与碳正离子(或碳正中 心)的结合能力。亲核性不仅与其本身碱性有关,还与空间位阻及原子的可极化性有关。如: C2H2O-的碱性大于 OH-, 亲核性也大于 OH-, (CH3)3CO-虽然碱性很强,但亲核性较弱,这 是由于其位阻较大的关系。
在质子性溶剂中,对同族元素而言,随着原子半径的增大,碱性降低,但亲核性增强。
R R' + R'Cu + LiX
3. 影响亲核取代反应的因素
亲核取代反应按照不同的历程可分为 SN2(双分子亲核取代反应)和 SN1(单分子亲 核取代反应),其反应特点及影响因素如下:
反应类型
SN2
SN1
反应历程
慢
Nu + RX
快
δ-
δ-
Nu---R---X
RNu + X
R X慢 R X R Nu 快 R NuNu-] 发生了 Walden 构型转化
V=k1[RX]
生成外消旋产物,可能有重排 产物
烷基结构
CH3X >伯卤代烃 >仲卤代烃 >
影
叔卤代烃
烯丙基卤代烃>叔卤代烃 > 仲 卤代烃 > 伯卤代烃 > CH3X>
乙烯基卤代烃
响
亲核性越强,浓度越高,对反应越有
因 亲核试剂
亲核试剂为富电子基团,常为负离子或含有孤对电子的基团。如:HO-、RO-、CN -、 HS -、NO3¯-、SCN -、I -、AcO –以及 H2O、R‘OH、NH3、RNH2 等。 (2)消除反应(1,2 消除或β-消除)
H
C C X + CH3CH2ONa
CH3CH2OH
C C + CH3CH2OH + NaX
取代反应与消除反应是并存而竞争的反应,试剂进攻底物的中心碳原子则引起亲核取代 反应,进攻 β-氢则引起消除反应。
H
CC
CC
SN2
H
B
E2
SN1
H
B E1
(1)烷基结构对取代反应和消除反应的影响是:
SN越易
30 RX 20RX
10 RX
CH3 RX
E越易 (2)亲核试剂的碱性越强,可极化性差,对消除反应越有利,如 RO-、NH2-等;亲核性强, 碱性较弱的基团,则有利于取代反应,SH –、CN –、 I -、AcO-、H2O 等。
(3)与金属的反应
卤代烃与金属镁在无水溶剂中反应生成 RMgX(Grignard 试剂),简称格氏试剂。
无水乙醚
RX + Mg
RMgX
格氏试剂能与许多含活性氢的物质如水、醇、酸、氨以及末端炔烃反应生成烃,并能与 二氧化碳作用生成羧酸,与醛、酮、酯等多种试剂作用,生成其它的有机化合物。
RMgX + HY
RCH CH2 HX
H+
过氧 化物
RCH CH3 X
RCH2 CH2X
(3)由醇制备,例如:
ROH SOCl2 吡啶 RCl SO2 HCl
(4)卤化物互换,例如:
RBr NaI 丙酮 RI NaBr
4
第八章 卤代烃
8.1 基本要求
1.掌握卤代烃的命名,了解其物理通性。 2.掌握卤代烃的化学性质,包括亲核取代反应、消除反应和活泼金属反应。 3.掌握亲核取代反应(SN1 和 SN2)和消除反应(E1 和 E2)机理。 4.理解卤代烃结构与性质的关系、影响亲核反应和消除反应的各种因素,以及亲核取代反 应与消除反应的竞争。
例如:
F - Cl - Br - I -
碱性减小 亲核性增大
RO -
RS -
碱性减小
亲核性增大
在亲核原子相同的试剂中,碱性大的试剂亲核性也较强,如:RO–> HO–>> RCO2– 。 常见基团的亲核性如下:
SH ¯>CN ¯>I ¯>OH ¯>N3 ¯>Br ¯>CH3COO ¯>Cl ¯>F ¯> H2O (3)在进攻试剂相同的情况下,溶剂极性加大,有利于电荷较为集中的取代反应,不利于 消除反应,例如:
在惰性溶剂中,金属锂与卤代烷反应生成烷基锂。
RX + Li
RLi
两分子烷基锂与一分子卤化亚铜反应生成二烃基铜锂。
2RLi + CuX
RCu + LiX
烷基铜
RCu + RLi
R2CuLi
二烷基铜锂
二烷基铜锂与卤代烷反应制备烷烃是增长碳链的常用的方法,称为 Corey-House 合成。
R'X + R2 CuLi
