全国高考化学物质的量的综合高考真题汇总附答案解析
高考化学物质的量(大题培优 易错 难题)含答案

【详解】
(1)在该反应中,Mn元素化合价由反应前KMnO4中的+7价变为反应后MnCl2中的+2价,化合价降低,得到5个电子,Cl元素化合价由反应前HCl中的-1价变为反应后Cl2中的0价,化合价升高,失去2个电子,电子得失最小公倍数是10,所以KMnO4、MnCl2前的系数是2,HCl前的系数是10,Cl2前的系数是5,根据原子守恒,KCl的系数是2,这样反应中有6个Cl原子未参加氧化还原反应,所有Cl原子都是由HCl提供,因此HCl前的系数为10+6=16,结合H原子反应前后相等,可知H2O的系数是8,用“双线桥”表示电子转移为: ;
②需量取质量分数为98%、密度为1.84 g•cm-3的浓硫酸的体积为______mL。
③配制过程中需先在烧杯中将浓硫酸进行稀释,操作方法是:_______________。
【答案】0.250.4 mo•L-12.240.1532 g•mol-1500mL容量瓶8.2将浓硫酸沿烧杯内壁缓缓注入盛有水的烧杯中并用玻璃棒不断搅拌
(2)在标准状态下,2.24LCl2的物质的量n(Cl2)= =0.1mol。
①根据反应的化学方程式可知:生成0.1molCl2时,参与反应的KMnO4的物质的量为0.1mol× =0.04mol,则参与反应的KMnO4的质量m(KMnO4)=0.04mol×158g/mol=6.32g;
②由反应化学方程式可知,HCl被氧化后生成Cl2,因此根据Cl元素守恒可知:被氧化的HCl的物质的量n(HCl)氧化=0.1mol×2=0.2mol。
(3)在标准状况下,1.7 g氨气所占的体积约为_________L,与_____mol H2S含有相同的氢原子数。
高考化学物质的量综合经典题及答案

高考化学物质的量综合经典题及答案一、高中化学物质的量练习题(含详细答案解析)1.(1)在标准状况下①6.72L CH 4②3.01×1023个HCl 分子③13.6g H 2S ④0.2mol NH 3,体积最大的是____,密最大的是度___,质量最小的是___,氢原子个数最多的是____。
(填写序号)(2)等温等压下,质子数相等的CO 、N 2两种气体,质量之比为____,体积之比为____,摩尔质量之比____。
(3)某物质在一定条件下加热分解,产物都是气体。
分解方程式为:3A =B +3C +2D 。
测得生成的混合气体的平均相对分子质量为2a ,则A 的摩尔质量为____。
【答案】② ② ④ ① 1:1 1:1 1:1 4a g/mol【解析】【详解】(1)①6.72L CH 4中:n(CH 4)= 6.72L 22.4L/mol=0.3mol ,m(CH 4)=0.3mol×16g/mol=4.8g ,ρ(CH 4)= m m M 16==g/L V V 22.4,N(H)=4N(CH 4)=1.2N A ; ②3.01×1023个HCl 分子中:n(HCl)=23233.01106.0210⨯⨯=0.5mol ,V(HCl)=0.5mol×22.4L/mol=11.2L ,ρ(HCl)=m m M 36.5==g/L V V 22.4,m(HCl)=0.5mol×36.5g/mol=18.25g ,N(H)=N(HCl)=0.5N A ; ③13.6g H 2S 中:n(H 2S)=13.6g 34g/mol=0.4mol ,V(H 2S)=0.4mol×22.4L/mol=8.96L ,ρ(H 2S)= m m M 34==g/L V V 22.4,N(H)=2N(H 2S)=0.8N A ; ④0.2mol NH 3中:m(NH 3)=0.2mol×17g/mol=3.4g ,V(NH 3)=0.2mol×22.4L/mol=4.48L ,ρ(NH 3)= m m M 17==g/L V V 22.4,N(H)=3N(NH 3)=0.6N A . 所以:体积最大的是②,密度最大的是②,质量最小的是④,含氢原子数最多的是①; (2)CO 、N 2两种气体涉及的元素有C 、O 、N 质子数分别为6、8、7,所以两种气体的分子的质子数分别为:14、14,质子数相等的CO 、N 2,物质的量相等;CO 、N 2摩尔质量分别为28g/mol 、28g/mol ,故摩尔质量之比1:1;根据m=nM 知:质量之比与摩尔质量成正比为28:28=1:1;根据阿伏伽德罗定律,相同条件下物质的量相等的气体具有相同的体积,故体积之比为1:1;(3)化学方程式系数的意义:表示物质的量。
高考化学 物质的量综合试题及答案

4.(1)1mol H2SO4中含有_____个硫原子,_____mol O。
(2)写出下列物质在水溶液中的电离方程式
HCl:_______________NaHSO4:____________________
【解析】
【分析】
(1)根据物质结构进行计算;
(2)强电解质完全电离;
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气;氢氧化亚铁白色沉淀迅速变为灰绿色,最终变为红褐色为氢氧化亚铁与氧气、水反应生成氢氧化铁;铜与氯化铁溶液反应生成亚铁离子和铜离子;
(4)根据化合价升降法及化合价只靠拢不相交的原则配平;
(5)还原剂,失电子,化合价升高,发生氧化反应,产物为氧化产物;氧化剂得电子,化合价降低,产物为还原产物。
【点睛】
本题考查了物质检验实验方案的设计以及化学方程式的书写、溶质物质的量浓度的计算,明确硫酸根离子、碳酸根离子的性质是解题的关键。
3.按要求完成下列各小题
(1)在同温同压下,相同质量的N2和H2S气体的体积比为____。
(2)0.8molCO和0.4molCO2中电子数目之比为___,含有氧原子物质的量之比为___,相同条件下两物质的密度之比为___。
【解析】
【分析】
根据阿伏伽德罗定律进行分析解答;根据氧化还原反应进行判断。根据溶解规律和离子的特征选择除杂试剂。如Na2SO4中的Na2CO3目的是除去CO32-离子,所以选择H2SO4进行除杂。
【详解】
(1)相同质量的N2和H2S的物质的量之比为 ,根据阿伏伽德罗定律,在同温同压下,气体体积之比等于物质的量之比,因此相同质量的N2和H2S气体的体积比为17:14。答案:17:14;
高考化学物质的量的综合题试题及答案解析
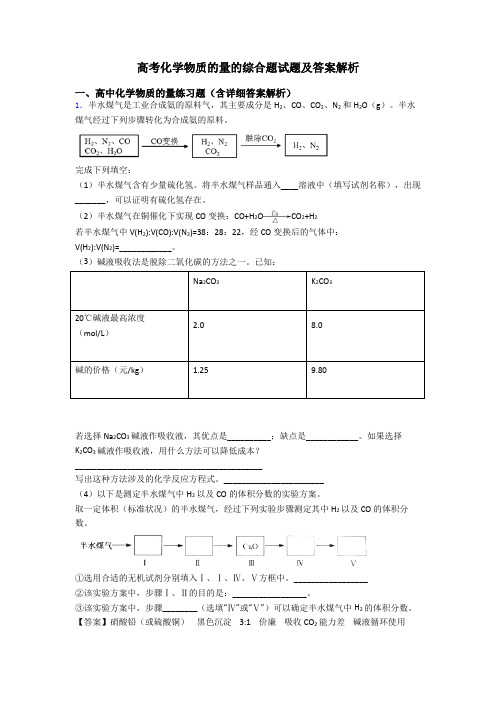
高考化学物质的量的综合题试题及答案解析一、高中化学物质的量练习题(含详细答案解析)1.半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O(g)。
半水煤气经过下列步骤转化为合成氨的原料。
完成下列填空:(1)半水煤气含有少量硫化氢。
将半水煤气样品通入____溶液中(填写试剂名称),出现_______,可以证明有硫化氢存在。
(2)半水煤气在铜催化下实现CO变换:CO+H2O CO2+H2若半水煤气中V(H2):V(CO):V(N2)=38:28:22,经CO变换后的气体中:V(H2):V(N2)=____________。
(3)碱液吸收法是脱除二氧化碳的方法之一。
已知:Na2CO3K2CO320℃碱液最高浓度(mol/L)2.08.0碱的价格(元/kg) 1.259.80若选择Na2CO3碱液作吸收液,其优点是__________;缺点是____________。
如果选择K2CO3碱液作吸收液,用什么方法可以降低成本?___________________________________________写出这种方法涉及的化学反应方程式。
_______________________(4)以下是测定半水煤气中H2以及CO的体积分数的实验方案。
取一定体积(标准状况)的半水煤气,经过下列实验步骤测定其中H2以及CO的体积分数。
①选用合适的无机试剂分别填入Ⅰ、Ⅰ、Ⅳ、Ⅴ方框中。
_________________②该实验方案中,步骤Ⅰ、Ⅱ的目的是:_________________。
③该实验方案中,步骤________(选填“Ⅳ”或“Ⅴ”)可以确定半水煤气中H2的体积分数。
【答案】硝酸铅(或硫酸铜)黑色沉淀 3:1 价廉吸收CO2能力差碱液循环使用2KHCO3→K2CO3+CO2↑+H2O除去半水煤气中的CO2(包括H2S)和H2O IV【解析】【分析】【详解】(1)硫化氢能与重金属生成沉淀,所以将半水煤气样品通入硝酸铅(或硫酸铜)溶液中,出现黑色沉淀可以证明有硫化氢存在。
高考化学物质的量(大题培优)附答案解析

高考化学物质的量(大题培优)附答案解析一、高中化学物质的量1.在实验室里,用足量的浓盐酸与一定量的高锰酸钾反应(不加热),来制取氯气。
反应:2KMnO 4+16HCl=2KCl+2MnCl 2+5Cl 2↑+8H 2O(1)“双线桥法”标出电子转移情况________ 。
(2)若生成2.24L 标准状况时的氯气,请计算(写出必要的计算过程):①理论上需要多少克KMnO 4参加反应?________。
②被氧化的HCl 的物质的量为多少?________。
【答案】 6.32g 0.2 mol【解析】【分析】(1)根据元素化合价升降数目等于反应过程中电子转移数目分析,标出电子转移情况;(2)先计算Cl 2的物质的量,然后根据方程式中KMnO 4、HCl 与Cl 2之间的反应转化关系计算。
【详解】(1)在该反应中,Mn 元素化合价由反应前KMnO 4中的+7价变为反应后MnCl 2中的+2价,化合价降低,得到5个电子,Cl 元素化合价由反应前HCl 中的-1价变为反应后Cl 2中的0价,化合价升高,失去2个电子,电子得失最小公倍数是10,所以KMnO 4、MnCl 2前的系数是2,HCl 前的系数是10,Cl 2前的系数是5,根据原子守恒,KCl 的系数是2,这样反应中有6个Cl 原子未参加氧化还原反应,所有Cl 原子都是由HCl 提供,因此HCl 前的系数为10+6=16,结合H 原子反应前后相等,可知H 2O 的系数是8,用“双线桥”表示电子转移为:;(2)在标准状态下, 2.24LCl 2的物质的量n(Cl 2)=m V 2.24L V 22.4L /mol=0.1mol 。
①根据反应的化学方程式可知:生成0.1molCl 2时,参与反应的KMnO 4的物质的量为0.1mol×25=0.04mol ,则参与反应的KMnO 4的质量m(KMnO 4)=0.04mol×158g/mol=6.32g ; ②由反应化学方程式可知,HCl 被氧化后生成Cl 2,因此根据Cl 元素守恒可知:被氧化的HCl 的物质的量n(HCl)氧化=0.1mol×2=0.2mol 。
高考化学物质的量综合经典题及详细答案

高考化学物质的量综合经典题及详细答案一、高中化学物质的量练习题(含详细答案解析)1.实验室配制500mL0.1mol/LNa2CO3溶液,回答下列问题(1)配制Na2CO3溶液时需用的主要仪器有托盘天平、滤纸、烧杯、药匙、___。
(2)容量瓶上标有刻度线、___,使用前要___。
(3)需用托盘天平称取Na2CO3____g。
(4)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?A.加水时超过刻度线___,B.溶解后未冷却到室温就转入容量瓶___,C.容量瓶内壁附有水珠而未干燥处理___,D.定容时仰视___,E.上下颠倒摇匀后液面低于刻线___。
(5)若实验室中要用浓度为16mol/L的浓硫酸配制480mL2.0mol/L的稀硫酸,则需要量取浓硫酸的体积为___mL。
【答案】500mL容量瓶、玻璃棒、胶头滴管温度、容积检漏 5.3 偏低偏高不变偏低不变 62.5【解析】【分析】配制一定物质的量浓度溶液步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶,分析误差时可根据c=nV判断。
【详解】(1)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、初步摇匀、定容、摇匀、装瓶可知所需的仪器有:托盘天平、烧杯、玻璃棒、药匙、500mL容量瓶和胶头滴管,缺少的仪器:500mL容量瓶、胶头滴管、玻璃棒;(2)容量瓶上标有温度、刻度线、容积;容量瓶带有瓶塞,为防止使用过程中漏液,使用前应查漏;(3)配制500mL 0.1mol/LNa2CO3,需要 Na2CO3的质量为:0.5L×0.1mol/L×106g/mol=5.3g;(4)A.加水时超过刻度线,导致溶液体积偏大,溶液浓度偏低;B.溶解后未冷却到室温就转入容量瓶,冷却后溶液体积偏小,溶液浓度偏高;C.容量瓶内壁附有水珠而未干燥处理,对溶质物质的量和溶液体积都不产生影响,溶液浓度不变;D.定容时仰视,导致溶液体积偏大,溶液浓度偏低;E.上下颠倒摇匀后液面低于刻线,属于正常操作,溶液浓度不变;(5)若实验室中要用浓度为16mol/L 的浓硫酸配制480mL 2.0mol/L 的稀硫酸,应选择500mL 容量瓶,设需要浓硫酸体积为V,则依据溶液稀释过程中溶质物质的量不变得:16mol/L×V=500mL 2.0mol/L,解得V=62.5mL。
全国高考化学物质的量的综合高考真题汇总含答案

全国高考化学物质的量的综合高考真题汇总含答案一、高中化学物质的量练习题(含详细答案解析)1.用98%的浓硫酸(其密度为1.84g/cm3,物质的量浓度为18.4 mol·L-1)配制100mL1.0mol·L-1稀硫酸,现有下列实验仪器备用:A.100mL量 B.托盘天平 C.玻璃棒D.50mL容量瓶 E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶。
请回答:(1)通过计算,需用量筒量取浓硫酸的体积为________mL;(2)实验时选用的仪器有______(填序号),使用容量瓶时第一步的操作是________________;(3)配制过程中,下列情况会使配制结果偏高的是________(填序号);①定容时俯视刻度线观察液面②容量瓶使用时未干燥③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线(4)实验步骤如下:①计算所用浓硫酸的体积②量取一定体积的浓硫酸③溶解④恢复至室温⑤转移、洗涤⑥定容、摇匀⑦装瓶贴标签。
其中,第⑤步中“洗涤”操作的目的是_______________________。
【答案】5.4 CFGEH 检查容量瓶是否漏水①减少溶质损失,减小实验误差【解析】【分析】⑴根据稀释前后溶质物质的量不变进行计算。
⑵配制溶液时需要用到100mL容量瓶、玻璃棒、10mL量筒、胶头滴管、50mL烧杯,使用容量瓶前要检漏。
⑶①定容时俯视刻度线观察液面,溶液体积偏小,溶液溶度偏高;②容量瓶使用时未干燥,与结果无影响;③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线,溶液体积偏大,浓度偏低。
⑷溶质黏在烧杯内壁或玻璃棒上,要洗涤。
【详解】⑴用物质的量浓度为18.4 mol·L-1的浓硫酸配制100mL 1.0mol·L-1稀硫酸,根据稀释前后溶质物质的量不变得到18.4 mol·L−1 ×V= 1.0 mol·L−1×0.1 L,V=0.0054L =5.4mL,因此需用量筒量取浓硫酸的体积为5.4mL;故答案为:5.4。
全国高考化学物质的量的综合高考真题汇总及答案解析

全国高考化学物质的量的综合高考真题汇总及答案解析一、高中化学物质的量1.在实验室里,用足量的浓盐酸与一定量的高锰酸钾反应(不加热),来制取氯气。
反应:2KMnO 4+16HCl=2KCl+2MnCl 2+5Cl 2↑+8H 2O(1)“双线桥法”标出电子转移情况________ 。
(2)若生成2.24L 标准状况时的氯气,请计算(写出必要的计算过程):①理论上需要多少克KMnO 4参加反应?________。
②被氧化的HCl 的物质的量为多少?________。
【答案】 6.32g 0.2 mol【解析】【分析】(1)根据元素化合价升降数目等于反应过程中电子转移数目分析,标出电子转移情况;(2)先计算Cl 2的物质的量,然后根据方程式中KMnO 4、HCl 与Cl 2之间的反应转化关系计算。
【详解】(1)在该反应中,Mn 元素化合价由反应前KMnO 4中的+7价变为反应后MnCl 2中的+2价,化合价降低,得到5个电子,Cl 元素化合价由反应前HCl 中的-1价变为反应后Cl 2中的0价,化合价升高,失去2个电子,电子得失最小公倍数是10,所以KMnO 4、MnCl 2前的系数是2,HCl 前的系数是10,Cl 2前的系数是5,根据原子守恒,KCl 的系数是2,这样反应中有6个Cl 原子未参加氧化还原反应,所有Cl 原子都是由HCl 提供,因此HCl 前的系数为10+6=16,结合H 原子反应前后相等,可知H 2O 的系数是8,用“双线桥”表示电子转移为:;(2)在标准状态下, 2.24LCl 2的物质的量n(Cl 2)=m V 2.24L V 22.4L /mol=0.1mol 。
①根据反应的化学方程式可知:生成0.1molCl 2时,参与反应的KMnO 4的物质的量为0.1mol×25=0.04mol ,则参与反应的KMnO 4的质量m(KMnO 4)=0.04mol×158g/mol=6.32g ; ②由反应化学方程式可知,HCl 被氧化后生成Cl 2,因此根据Cl 元素守恒可知:被氧化的HCl 的物质的量n(HCl)氧化=0.1mol×2=0.2mol 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
全国高考化学物质的量的综合高考真题汇总附答案解析一、高中化学物质的量练习题(含详细答案解析)1.按要求完成下列填空。
(1)在等体积的NaCl、MgCl2、AlCl3三种溶液中,分别加入等量的AgNO3溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为___。
(2)将3.22g芒硝(Na2SO4·10H2O)溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为__g。
(3)在干燥烧瓶中用向下排空气法收集氨气,由于空气不可能排净,所以瓶内气体对氢气的相对密度为9.5,将此瓶气体倒置于水槽中,烧瓶内液面上升的体积占烧瓶总体积的_______。
(4)100mL 0.3mol/L Na2SO4(密度为d1 g/cm3)和50mL 0.2mol/L Al2(SO4)3(密度为d2 g/cm3)混合,所得密度为d3 g/cm3的混合溶液中SO42-的浓度为___________。
(用含d1,d2, d3的式子表示)(5)已知两种碱AOH和BOH的摩尔质量之比为5:7,现将7mol AOH与5mol BOH混合后,从中取出5.6g,恰好可以中和100ml浓度为1.2mol/L的盐酸,则AOH的摩尔质量为_____。
(6)标准状况下,用一定量的水吸收HCl气体后制得浓度为1.0mol/L,密度为1.0365g/cm-3的盐酸。
请计算1体积水吸收_______体积的HCl可制得上述氨水。
【答案】6:3:2 34.2 56(或83.3%) 6d3/(10 d1+5 d2)mol/L 40g/mol 22.4【解析】【详解】(1)设NaC1、MgCl2、A1Cl3的物质的量分别为x、y、z,由分别加入等量的AgNO3溶液,恰好都完全反应,则种溶液中Cl-的物质的量相等,x=y×2=z×3,解得x:y:z=6:3:2,因溶液的体积相同,则物质的量之比等于浓度之比,所以浓度之比为6:3:2;故答案是:6:3:2;(2)3.22g芒硝的物质的量为3.22/322=0.01mol,所以溶液中n(Na+)=2n(Na2SO4·10H2O)=0.01×2=0.02mol,每100个水分子中溶有1个钠离子,所以n(H2O)=100n(Na+)=2mol,0.01mol Na2SO4·10H2O 中含有水的物质的量为0.01×10=0.1mol,所以需要的水的物质的量为2-0.1=1.9mol,所以需要水的质量为1.9mol×18g/mol=34.2g;故答案是:34.2;(3)用排气法收集氨气后,收集到的氨气气体不纯,含有空气;空气的平均相对分子质量为29,混合气体的平均相对分子质量为: 9.5×2=19;设烧瓶的容积为V L,氨气的体积为xL,空气的体积为(V-x)L,则有:[17x/V m+(29×(V-x)/V m)]÷(V/V m)=19,解之得:x=56V;将此瓶气体倒置于水槽中,进入烧瓶的液体体积为氨气体积,即56V,烧瓶内液面上升的体积占烧瓶总体积为:(56V)/V=56(或83.3%);故答案是:56(或83.3%);(4)混合液的质量为(100d1+50d2)g,混合后溶液的体积为:[(100d1+50d2)÷d3]mL=[(100d1+50d2)÷d3]×10-3L;溶液混合后n(SO42-)=(0.1×0.3×1+0.05×0.2×3)=0.06mol;根据c=n/V可知,混合溶液中SO42-的浓度为:0.06÷[(100d1+50d2)÷d3]×10-3=60 d3/(100d1+50d2)mol/L=6d3/(10d1+5d2)mol/L故答案是:6d3/(10d1+5d2)mol/L;(5)设AOH和BOH的摩尔质量分别为5x g/mol和7x g/mol,n(HCl)=n(OH-)=0.1×1.2=0.12mol;7mol AOH与5mol BOH混合物中含有n(OH-)=7+5=12,根据题意可知,5.6g混合碱中含有n(OH-)=0.12mol,则含有n(OH-)=12mol时,混合碱的质量为560g;根据7mol×5x g/mol+5mol×7x g/mol=560g可知,x=8,所以AOH的摩尔质量为40g/mol;故答案是:40g/mol;(6)假设溶液体积为1.00L,1.00L盐酸中含氯化氢的物质的量为:1L×1mol/L=1mol,V(HCl)=1×22.4=22.4L;1.00L盐酸中含水的质量为:m(H2O)=1×1.0365×103-1×36.5=1000g,V(H2O)=1L;标准状况下,1体积水吸收氯化氢的体积为V=[V(HCl)/ V(H2O)]×1L=22.4L;故答案是:22.4。
2.半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O(g)。
半水煤气经过下列步骤转化为合成氨的原料。
完成下列填空:(1)半水煤气含有少量硫化氢。
将半水煤气样品通入____溶液中(填写试剂名称),出现_______,可以证明有硫化氢存在。
(2)半水煤气在铜催化下实现CO变换:CO+H2O CO2+H2若半水煤气中V(H2):V(CO):V(N2)=38:28:22,经CO变换后的气体中:V(H2):V(N2)=____________。
(3)碱液吸收法是脱除二氧化碳的方法之一。
已知:Na2CO3K2CO320℃碱液最高浓度(mol/L)2.08.0碱的价格(元/kg) 1.259.80若选择Na2CO3碱液作吸收液,其优点是__________;缺点是____________。
如果选择K2CO3碱液作吸收液,用什么方法可以降低成本?___________________________________________写出这种方法涉及的化学反应方程式。
_______________________(4)以下是测定半水煤气中H2以及CO的体积分数的实验方案。
取一定体积(标准状况)的半水煤气,经过下列实验步骤测定其中H2以及CO的体积分数。
①选用合适的无机试剂分别填入Ⅰ、Ⅰ、Ⅳ、Ⅴ方框中。
_________________②该实验方案中,步骤Ⅰ、Ⅱ的目的是:_________________。
③该实验方案中,步骤________(选填“Ⅳ”或“Ⅴ”)可以确定半水煤气中H2的体积分数。
【答案】硝酸铅(或硫酸铜)黑色沉淀 3:1 价廉吸收CO2能力差碱液循环使用2KHCO3→K2CO3+CO2↑+H2O除去半水煤气中的CO2(包括H2S)和H2O IV【解析】【分析】【详解】(1)硫化氢能与重金属生成沉淀,所以将半水煤气样品通入硝酸铅(或硫酸铜)溶液中,出现黑色沉淀可以证明有硫化氢存在。
(2)若半水煤气中V(H2):V(CO):V(N2)=38:28:22,经CO变换后H2O转化为氢气,则根据方程式可知所得的气体中:V(H2):V(N2)=(38+28):22=3:1。
(3)根据表中数据可知若选择Na2CO3碱液作吸收液,其优点是价廉,而缺点是吸收CO2能力差。
由于生成的碳酸氢钾受热易分解产生碳酸钾,所以使碱液循环使用可以降低成本,反应的化学方程式为2KHCO3→K2CO3+CO2↑+H2O;(4)①由于半水煤气中含有二氧化碳,所以首先利用碱液除去二氧化碳,干燥后再通过氧化铜反应,利用浓硫酸吸收产生的水蒸气,利用碱液吸收产生的二氧化碳,进而计算体积分数。
所以流程为。
②Ⅰ中KOH吸收CO2和H2S,Ⅱ中浓硫酸吸收水蒸气,干燥气体。
③氢气还原氧化铜生成水蒸气,浓硫酸吸收水蒸气,所以该实验方案中,步骤Ⅳ可以确定半水煤气中H2的体积分数。
【点睛】“教真实的化学,学有用的知识”已成为大家的共识,现在的化学试题强调化学与生活的交融,突出理论联系生产、生活实际和科技前沿,强调学以致用。
试题将真实的问题转化为试题情境,真实问题的复杂性带来了化学试题的综合性,这就要求考生首先读懂并捕捉到全部相关信息,弄清这些信息之间的逻辑关系,特别是确定性信息和未知信息之间的关系,为问题的解决奠定基础。
这显然属于“关键能力”。
对于一个流程的设计和评价,要分析它由几个部分组成,每个部分在整体中处于什么地位、有什么作用,为什么要这样设计,这样设计的优缺点如何,可以如何改进等等,这些都是高考中考查综合能力的重点。
3.按要求完成下列填空I.(1)给定条件下的下列四种物质:a.10g氖气b.含有40mol电子的NH3c.标准状况下8.96LCO2d.标准状况下112g液态水则上述物质中所含分子数目由多到少的顺序是________________(填序号)。
(2)标准状况下,0.51g某气体的体积为672mL,则该气体摩尔质量为______。
(3)将100mL H2SO4和HCl的混合溶液分成两等份,一份中加入含0.2molNaOH溶液时恰好中和完全,向另一份中加入含0.05molBaCl2溶液时恰好沉淀完全,则原溶液中c(Cl-)=____ mol/L。
II.现有以下物质:①铝;②二氧化硅;③液氯;④NaOH溶液;⑤液态HCl;⑥NaHCO3晶体;⑦蔗糖;⑧熔融Na2O;⑨Na2O2固体;⑩CO2。
回答下列问题(用相应物质的序号填写):(1)其中可以导电的有__________。
(2)属于电解质的有_______,非电解质有__________。
(3)写出向⑨与⑩反应的化学方程式___________。
(4)写出①与④的离子方程式_____________。
(5)写出⑤的水溶液与⑥的水溶液反应的离子方程式___________________ 。
(6)写出②与④反应的离子方程式_______________________________ 。
【答案】d>b>a>c 17g/mol 2 ①④⑧⑤⑥⑧⑨②⑦⑩ 2Na2O2 + 2CO2=2Na2CO3 + O2 2Al + 2H2O + 2OH- = 2AlO2- + 3H2 H+ + HCO3- = H2O + CO2 SiO2 + 2OH- = SiO32- + H2O【解析】【分析】I.利用n=mM=ANN=mVV计算。
II.①铝能导电,既不是电解质,也不是非电解质;②二氧化硅不能导电,为非电解质;③液氯不能导电,既不是电解质,也不是非电解质;④NaOH溶液能导电,为混合物,既不是电解质,也不是非电解质;⑤液态HCl不能导电,为电解质;⑥NaHCO3晶体不能导电,为电解质;⑦蔗糖不能导电,为非电解质;⑧熔融Na2O能导电,为电解质;⑨Na2O2固体不能导电,为电解质;⑩CO2不能导电,为非电解质。
