7.2 第4课时 中和反应 课件 2020-2021学年沪教版九年级化学下册优秀课件资料
沪教版九年级下册化学:中和反应
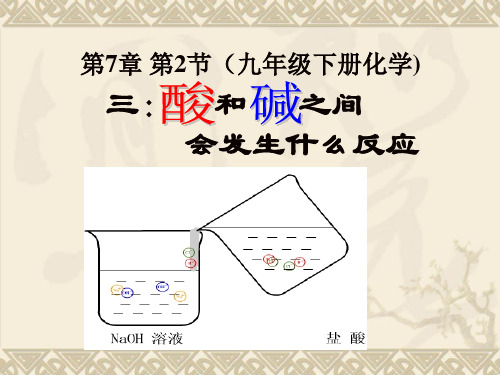
观察现象:无明显现象
结论分析:稀盐酸和氢氧化钠溶液混合后, 试管中的液体仍为无色溶液, 既没有沉淀、也没有气体生成, 所以无法判断反应是否发生
用什么方法可以证 明酸和碱之间可以发生 反应呢?
设计实验2:可以在酸或碱中加入指示剂以
显示它的存在,然后加入碱或酸 直到溶液变为另一种颜色或者褪 色。
1.改变土壤的酸碱性
2.处理工厂的废水 3.用于医药
人的胃液里含有盐酸,可以帮助消化,但是如果饮 食过量时,胃会分泌出大量胃酸,反而造成消化不良. 可以服用某些含有碱性物质的药物,以中和过多的胃 酸.
被蚊虫叮咬后,叮咬处很快肿成大包,如果涂一些含 有碱性物质的药水,如NH3·H2O,就可减轻痛痒.
问题(三)
此药中含有氢氧化铝
试写出胃康—U治胃酸过多的原理。
3HCl+Al(OH)3=AlCl3+3H2O
请同学们回顾本节课的主要内容:
1、中和反应(酸 + 碱 = 盐 + 水)
对于无明显现象的中和反应,通常要借助指示剂 来帮助判断反应的发生。
2、中和反应在实际生活中的应用
A、农业 B、工业 C、医药 D、其他 作业:p66 6、10、13
达出它的原理么?
(说明:此酸雨为硫酸型酸雨)
熟石灰
H2SO4 + Ca(OH)2 = CaSO4 + 2H2O
二、中和反应在实际中的应用:
1.改变土壤的酸碱性 2.处理工厂的废水
工厂生产过程中的污水,需进行 一系列的处理。例如,硫酸厂的污水 中含有硫酸等杂质。可以用熟石灰进 行中和处理。
二、中和反应在实际中的应用:
第7章 第2节(九年级下册化学)
沪教版九下化学 7.2.4复分解反应及其应用 课件 %28共24张PPT%29

• A+B→
A+C→
• A+D→
B+C→白色沉淀
• B+D→
C+D→无色气体
↓
HCl BaCl2 ↓ Na2SO4 Na2CO3
↑
不含CuSO4 试一试,你能行 不含CaCO3
5.有一种固体混合物,可能由CaCO3,CuSO4, B取a该Cl混2,合KC物l,进N行a2如CO下3中实的验一:种或几种B物a不质Cl能2组和同成N时a。2有C现O3
物质之间能发生反应吗?
氧化物
化酸 合 物碱
H2SO4 CO2 NaOH
Na2CO3 HCl CuO
盐
CuSO4 Mg(OH)2
BaCl2
属于复分解反应的有:
♣ 金属氧化物+酸 → 盐 + 水 ♣碱 + 酸 → 盐 + 水 ♣ 盐 + 酸→ 新盐 + 新酸 ♣ 碱 + 盐→ 新碱 + 新盐 ♣ 盐 + 盐→ 新盐 + 新盐
6.有H2SO4、 BaCl2、 NaOH、CuSO4、 NaCl这五种物质,相互之间最多能发生的 反应个数为( )
A. 3个 B. 4个 C. 5个 D. 6个
7. 只需要加入 ①Fe2(SO4)3 ②Na2CO3 ③AgNO3 ④石蕊 四种溶液中的一种,就 能将BaCl2、HCl、NaOH三种无色溶液一 次性鉴别出来的有( )。
学习目标
♫ 知道哪些物质之间能发生复分解; ♫ 掌握复分解反应发生的条件; ♫ 学会正确书写复分解反应的化学方程式; ♫ 掌握利用复分解反应的条件解决具体问题
的思路方法。
想一想,说一说
♪. 什么是复分解反应?
沪教版九下化学 7.2.3中和反应 课件 (共15张PPT)
1】什么是中和反应??????????
自读课本47页最后一段
酸和碱是两类不同的 物质,具有不同的 化学性质。
如果把酸溶液和碱溶液混合,会发生什么现象呢?
请会酸你发的大生三六胆某化山合化些唐预作五之学金诗学岳内者测属反:何谁: 李,性驱为英应白鬼酸峰雄吗质,,碱?相这遇是后碱李,白的会的预化一?测见学,钟藏性情头吗质诗?
什么是中和反应??????????
请大胆预测盐酸和碱溶液的反应的化学方程式
盐酸 +
碱 ----- 水 + 盐酸盐
硫酸 +
硝酸 -碳-- 酸
+ +
碱 碱 碱
------
水? 水?
---- 水?
++ ++ ++
硫?酸盐 硝?酸盐 碳?酸盐
醋- 酸
+
碱 ----- 水? ++ 醋?酸盐
酸 +碱
水+ 盐
酸 +碱
氢氧化钾,化学式为__K_O_H___.。
常见的酸有:盐酸_H__C_l、__H__2O_,硫酸___H_2_S_O_4___, 硝酸____H_N_O__3_____,碳酸H__2C__O_3
1KOH +1HCl 2KOH +1H2SO4 1 KOH +1HNO3
+1-1 1 KCl + 1 H2O +1 -2 1 K2 SO4 + 2 H2O
1】用玻璃棒蘸取实验一所得溶液,加热至蒸干,玻璃棒上出现
白_色__固___体_,有咸味,好像是我们一日三餐必不可少的食盐(氯化钠) 课本盐48酸页实和验氢探氧究1化,钠明确溶实液验步反骤应、生实成验、氯观化察钠、记和录水。
沪教版 九年级下册第七章 第二节 常见的酸和碱 第4课时 《中和反应》说课

《中和反应》实验教学说课稿作者:永春一中刘培飞时间:2021年6月19日各位专家、评委老师:大家好!我是今天说课的题目是:沪教版九年级下册第七章第二节常见的酸和碱第4课时《中和反应》,下面我将从五个方面来展示我的说课内容:一、说教材(一)教材中的地位和作用酸和碱之间发生中和反应是贯穿酸碱盐知识的一个重要纽带,而且,中和反应在实际中有广泛的应用,所以,教材没有简单将它作为酸或碱的性质来介绍,而是专门编成一个课题来说明。
教材根据学生的认知特点,从学生的实验探究开始,让学生自己动手去实验,从实验探究的过程中感悟酸碱中和的结果——酸和碱各自特性都消失;感悟酸碱之间的对立统一;明确中和反应的放热现象,感悟化学变化中的能量变化。
接着,教材通过中和反应的产物引出盐的学习,为下节课的学习打下基础。
为此,我设立了如下教学目标:(二)教学目标知识与技能(1)知道酸与碱之间发生的中和反应。
(2)了解中和反应在实际生活中的应用。
过程与方法(1)通过自主探究,培养学生发现问题、解决问题的能力和动手操作能力。
(2)通过讨论交流,培养学生收集处理信息能力和良好的学习习惯。
情感态度与价值观(1)感受化学与社会生活的关系。
(2)培养学生实事求是的科学态度。
(三)说教学重点、难点重点:酸碱之间的中和反应及中和反应的应用。
难点:中和反应的探究过程。
二、说学情学生已经对常见酸、碱及酸和碱的性质有所了解,但对于酸和碱之间会发生什么反应呢?如何通过具体的实验来探究呢?学生渴望通过自主探究来认识物质,对实验探究表现出极大的兴趣。
所以本节课教学的起点应定位于学生已有的酸碱的知识基础上,设计有利于学生能自主学习的情境。
三、说教法(一)、教学模式我的教法设计模式为:创景设疑——教师演示实验—(转变为)学生分组实验探究——归纳总结——交流讨论――练习实践。
(二)、教学用品药品:Mg(OH)2、Al(OH)3、等碱的固体,NaOH溶液;稀盐酸、稀H2SO4、pH试纸、酚酞试液、紫色石磊试液等。
九年级化学下册习题课件-7.2.4 中和反应-沪教版优品课件PPT

7.【中考·梧州】某校化学兴趣小组利用数字化传感器探 究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶 液的pH随滴加液体体积变化的曲线如图所示。下列 说法错误的是( )
A.图中b点所示溶液中,溶质是NaCl B.向图中c点所示溶液中滴加无色酚酞,溶液不变色 C.该实验是将氢氧化钠溶液逐滴滴入到盛有稀盐酸的
8.【中考·枣庄】向盛有 50 mL稀硫酸的烧杯 中缓慢滴加一定溶质 质量分数的氢氧化钡 溶液至过量,随着氢 氧化钡溶液的滴加, 某些量变化趋势正确 的是( )
【点拨】稀硫酸和氢氧化钡反应生成硫酸钡沉淀和水, 使溶液中的溶质质量减小,恰好反应时溶质质量为0,继 续添加氢氧化钡溶液,溶质质量增大,故A选项不符合 题意;硫酸溶液的pH小于7,氢氧化钡溶液的pH大于7, 向稀硫酸中加入氢氧化钡溶液至过量,溶液的pH由小于 7变化为大于7,但不能一直增大,故B选项不符合题意;
4.【中考·郴州改编】下列没有运用中和反应原理的是 () A.用氢氧化钠溶液洗涤石油产品中的残余硫酸 B.新制的松花皮蛋往往因碱性过重而略带涩味,食 用时可加适量的食醋 C.蚊虫叮咬处涂上肥皂水,可减轻痛痒 D.用生石灰作干燥剂
【点拨】本题采用内涵分析法解答,根据中和反应的定 义进行分析。用生石灰作干燥剂是利用氧化钙能与水反 应生成氢氧化钙,不属于中和反应。
【答案】D
5.中和反应在生活中有着广泛的应用。 (1)小红同学近日常吐酸水,心里非常紧张,医生给她做
了检查后说:“没事,是胃酸过多,吃些药就会好 的。”医生给小红开的药方中有一种含氢氧化镁的药 品,其作用是__中__和__过__多__的__胃__酸____________________, 写出该反应的化学方程式: __M__g_(O__H_)_2_+__2_H_C__l=_=__=_M__g_C_l_2+__2_H__2O_____________;
2020-2021学年沪教版九年级下册化学习题课件7.2.4中和反应

2020-2021学年沪教版九年级下册化学习题课件7.2.4中和反应(2)充分反应后U形管中溶液全部呈⽆⾊,除酚酞外,此时溶液中⼀定含有的溶质的名称为________,可能含有的溶质的化学式为________,写出上述反应的化学⽅程式:_________________________________________。
氯化钠HClNaOH+HCl===NaCl+H2O13.【中考?齐齐哈尔】下列实际应⽤中,利⽤中和反应原理的是()①⽤氢氧化钠溶液洗涤⽯油产品中的残余硫酸②⽤碳酸氢钠治疗胃酸过多③⽤熟⽯灰改良酸性⼟壤④⽤稀氨⽔涂抹在蚊⼦叮咬处(分泌出蚁酸)⽌痒A.①②B.②③④C.②③D.①③④D【⽅法规律】本题采⽤内涵分析法解答,根据中和反应的定义进⾏分析。
⽤碳酸氢钠治疗胃酸过多,是利⽤盐与盐酸之间发⽣的反应,不属于中和反应。
14.【中考?包头】20g溶质质量分数为20%的NaOH溶液与20g溶质质量分数为20%的H2SO4溶液充分反应后,滴⼊紫⾊⽯蕊试液,溶液显()A.蓝⾊B.紫⾊C.红⾊D.⽆⾊A【⽅法规律】根据硫酸与氢氧化钠反应的化学⽅程式,通过计算可知,20g溶质质量分数为20%的氢氧化钠溶液与20g溶质质量分数为20%的稀硫酸反应时,氢氧化钠没有反应完,溶液显碱性,因此滴⼊紫⾊⽯蕊试液,溶液显蓝⾊。
15.【中考?佛⼭】某同学在探究“酸与碱能否发⽣反应”时,⽤稀NaOH溶液、稀盐酸和酸碱指⽰剂进⾏实验的过程见下图。
下图所加试剂①②③分别是()CA.稀NaOH溶液、⽯蕊试液、稀盐酸B.稀盐酸、⽯蕊试液、稀NaOH溶液C.稀NaOH溶液、酚酞试液、稀盐酸D.稀盐酸、酚酞试液、稀NaOH溶液【⽅法规律】本题采⽤标准实验对照法解答。
对照课本中探究氢氧化钠与稀盐酸反应的实验,氢氧化钠溶液与稀盐酸反应没有明显现象,要证明两者发⽣了化学反应需要借助酸碱指⽰剂,为了便于观察,通常是向氢氧化钠溶液中滴加酚酞,溶液变红,再向氢氧化钠溶液中逐滴滴加稀盐酸,溶液由红⾊褪成⽆⾊,证明⼆者发⽣了化学反应。
沪教版九年级下册化学:中和反应(4)

3、酸和碱反应后为什么都有水生成?
中和反应在实际中的应用
• 改变土壤的碱性
中和反应在实际中的应用
• 处理工厂的废水 2NaOH + H2SO4 == Na2SO4 + 2H2O
中和反应在实际中的应用
• 用于医药
治疗胃酸过多
Mg(OH)2 + 2HCl == MgCl2 + 2H2O 蚊虫叮咬
和盐酸反应
思考:这三种物质
CaCl2 + 2H2O
3、氢在氧组化成钠上有什N么aO共H + HCl ==
和盐同酸点反?应
NaCl + H2O
盐
由金属离子和酸根离子
构成的化合物
中与和酸反、碱应有
什么不酸同和?碱作用生成盐和水 的反应
酸+碱→盐+水
讨论:
1、刚才的实验中为什么要使用酚酞? 还可以使用其它物质吗?
练习
• 1. 下列物质之间的反应属于中和反应的是 (D)
A. 2NaOH+CO2=Na2CO3+H2O
B. CaCO3+2HCl=CaCl2+H2O+CO2↑
C. Fe+2HCl=FeCl2+H2↑
D. 2NaOH+H2SO4=Na2SO4+2H2O
• 2、下列化合物中属于盐的是
( C)
A. CO2
玻璃片上有白 色固体生成
结论
氢氧化钠 与盐酸发 生了反应
生成物中 有氯化钠
化学方程式:
NaOH + HCl == NaCl +H2O KOH + HCl == KCl +H2O
下列反应也能发生:
1、氢氧化钾 2KOH + H2SO4 ==
沪教版初中化学九年级下册 7.2.4 中和反应的再研究 课件

中和反应:酸+碱 盐+水
中和反应的微观本质:
H ++ OH _
H2O
知识回顾:
知识回顾:
小知识:
传感器是一种检测装置,能感受到 被测量的信息,并能将信息显示和记录 下来。
利用pH传感器测定酸碱中和 反应溶液的pH变化情况
13.8 , 9.88 13.9 , 7.87 14.0 , 4.30
H2SO4 + Ba(OH)2 == BaSO4↓+ 2H2O
20℃时
硫酸钡的溶解度是2.4×10-4 g
课堂小结:
今天你收获了什么?
拓展提升:
中和反应中除了有 酸碱度 和 温度的变化外,溶液中还有哪些
变化呢?
拓展提升:
H ++ OH _
(离子)
H2O
(分子)
H2SO4 + Ba(OH)2 == BaSO4↓+ 2H2O
拓展提升:
电导率,是描述物质传导电流的能力 的数据。
拓展提升:
实验一:率的变化
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
五、世界上没有比人生更艰难的艺术,因为其他的艺术或学问,到处都有老师。因此,我们要在人生的逆境中学会坚强,拼搏,向上的精神, 不要向困难低头。
4、告诉你一个宝藏的地点,它就在你的生命里。 15、出淤泥而不染,濯清涟而不妖。 7、游手好闲的学习并不比学习游手好闲好。
九自大的、维持不变的、独断的恐龙之所以一夕倒下的原因。 12、人生伟业的建立,不在能知,乃在能行。 3、没有热忱,世间便无进步。 1.成功没有快车道,幸福没有高速路。所有的成功,都来自不倦的努力和奔跑;所有幸福,都来自平凡的奋斗和坚持。 15. 读书改变命运,刻苦成就事业,态度决定一切。 6、有百折不挠的信念的所支持的人的意志,比那些似乎是无敌的物质力量有更强大的威力。 27.意志的出现不是对愿望的否定,而是把愿望合并和提升到一个更高的意识水平上。 36.无论是美女的歌声,还是鬣狗的狂吠,无论是鳄鱼的眼泪,还是恶狼的嚎叫,都不会使我动摇。 23、想不付出任何代价而得到幸福,那是神话。 六、不忘初心,能得始终,永远不要放弃属于自己的梦想,但也不能纠结着坚持着错误的,失去淡然。
