第三章水环境化学
环境化学-第三章-水环境化学-第二节-水中无机污染物的迁移转化知识交流

之,pE越大,电子浓度越低,体系接受电子的倾向就越强。
(2)氧化还原电位E和pE的关系
Ox +ne→Red
(1)
根据Nernst方程
E=E0-(2.303RT/nF)lg[Red]/[Ox] (2) 当反应达平衡时,定义
E0=(2.303RT/nF) lgK
(3)
从上述化学方程式(1),可写出
K= [Red]/{[Ox][e]n }
如果考虑到羟基配合作用,那么金属氧化物或氢氧化物的 溶解度(MeT)表征为:
MeT = [ Mez+ ] +∑[ Me(OH)nz-n ]
固体的氧化物和氢氧化物具有两性的特征,它们和质子或 羟基离子都发生反应,存在一个pH值,在该值下溶解度为最 小值。在碱性或酸性更强的pH值区域内,溶解度都会变得更 大。
因此,在 H2S 和硫化物均达到饱和的溶液中,溶液重金属离子 的饱和浓度为: [Me2+]=Ksp/[S2-]=Ksp [H+]2/Ksp´ =Ksp [H+]2/(0.1K1K2)
3、碳酸盐
——多相平衡,pH通过控制碳酸根浓度影响沉淀平衡
封闭体系: 只考虑固相和液相,把 H2CO3* 当作不挥发酸类处理。
吸附量随粒度增大而减少,并且当溶质浓度范围固定 时,吸附量随颗粒物浓度增大而减少。
温度变化、几种离子共存(竞争作用)等。
3、沉积物中重金属的释放——属于二次污染问题
诱发释放的主要因素有: (1)盐浓度升高:碱金属和碱土金属阳离子可将被吸附在固体颗
粒上的金属离子交换出来。
(2)氧化还原条件的变化:有机物增多,产生厌氧环境、铁锰氧 化物还原溶解,使结合在其中的金属释放出来。
2、它在中性表面甚至在与吸附离子带相同电荷符号的表面 也能进行吸附作用。
环境化学第三章水

二节 气体在水中的溶解性
水的质量特征:
• 酸度和碱度
第一节 概述
• 盐度和氯度:1千克水中碳酸盐转变为氧化物、溴化物 和碘化物转变为氯化物、有机物完全氧化后所含固体 的总克数。
• 硬度 • 溶氧量:25℃时的饱和浓度
[O2 (aq)] = 2.6×10-3 mol/L = 8.32 mg/L
• 清度和色度
化合物直接与 pH值有关,实际涉及到水解和羟基配合物的平
衡过程,该过程往往复杂多变,这里用强电解质的最简单关 系式表述: Me(OH)n(s) → Men+ + nOH根据溶度积表达式 可导出金属离子浓度 等号两边取负对数: Ksp = [Men+][OH-]n [Men+] = Ksp/[OH-]n = Ksp[H+]n/Kwn -lg[Men+] =-lgKsp-nlg[H+] + nlgKw (3-21)
HS- → H+ + S2则总反应: H2S →2 H+ + S2-
K2= 1.3×10-15
K1,2=K1K2=1.16×10-22
三、溶解沉淀平衡
在饱和水溶液中,H2S浓度总是保持在0.1mol/L,则 [H+]2[S2-] = K1,2×[H2S] = 1.16×10-22×0.1 = 1.16×10-23 由于在水溶液中 H 2 S 的二级电离甚微,故可近似认为 [H+] = [HS-],因此可求得溶液中[S2-]浓度:
三、溶解沉淀平衡
第二节 天然水中的平衡
溶解和沉淀是污染物在水环境中迁移的重要途径,一般金
属化合物在水中迁移能力,直观地可以用溶解度来衡量。
溶解度小者,迁移能力小; 溶解度大者,迁移能力大。 在固—液平衡体系中,需用溶度积来表征溶解度。
(完整版)第三章水环境化学答案

第三章水环境化学1、请推导出封闭和开放体系碳酸平衡中[H 2CO 3*]、[HCO 3-]和[CO 32-]的表达式,并讨论这两个体系之间的区别。
解: 开放体系,考虑到CO 2在气液相之间的平衡,[H 2CO 3*] 不变根据亨利定律: [CO 2(aq)] = K H Pco 2 lg[H 2CO 3*] ≈ lg[CO 2(aq)] = lg K H + lg Pco 2 = - 4.9lg[HCO 3-] = lg K 1 + lg [H 2CO 3*] + pH= -11.3 + pHlg[CO 32-] = lgK 1 + lgK 2 + lg[H 2CO 3*] + 2pH= -21.6 + 2pH*][][][*][]][[32133231CO H H K HCO CO H HCO H K +--+==*][][][*][][][32221233223221CO H H KK CO CO H CO H K K +--+⋅==⋅][][][233*32--++=CO HCO CO H C T 是常数。
的总和为各种碳酸化合态浓度假设,T C TC HCO ⎥⎦⎤⎢⎣⎡-=31αTC CO ⎥⎦⎤⎢⎣⎡-=232αTC CO H ⎥⎦⎤⎢⎣⎡*=320α122122][][1(-+++=K H K K H α1211)][][1(-++++=H K K H α122110][][1(-++++=H K K H K α*][][][*][]][[32133231CO H H K HCO CO H HCO H K +--+==*][][][*][][][32221233223221CO H H K K CO CO H CO H K K +--+⋅==⋅][][][][21233*32+--H K K CO HCO C CO H T 和含有的表示式,,为变量表示以:,][],[*],[21023332得到,,代入把αααT C CO HCO CO H --eg oo d 2、请导出总酸度、CO 2酸度、无机酸度、总碱度、酚酞碱度和苛性碱度的表达式作为总碳酸量和分布系数(α)的函数。
中国农业大学_807环境化学与环境监测_《环境化学》课件_环境化学第三章

第一节
水环境中的沉淀溶解反应
3、相互结合的离子半径差别愈小,其离子化合物愈牢固, 即难溶解。 溶解度小于0.01克/100克水的物质叫做“难溶物” 地表水和沉积物的孔隙水中主要阴离子Cl-、SO2-4、HCO-3
还原条件下有H2S衍生的HS-与S2-,碳酸盐、氢氧化物、硫 化物难溶。
第一节
水环境中的沉淀溶解反应
一、氧化物和氢氧化物
金属氢氧化物沉淀有多种形态,它们在水环境中的行为差
别很大。氧化物可看成是氢氧化物脱水而成。金属氢氧化 物的沉淀溶解平衡可以用化学反应的通式表述:
Me (OH)n(s) ==== Me n+ + nOH¯ Ksp = [Me n+][OH–]n [Me n+]= Ksp/[OH–]n = Ksp[H+]n / Knw
pc = ( pKsp – npKw ) + npH (3-1)
第一节
水环境中的沉淀溶解反应
1、pc 与pH成直线关系,即在一定的pH的范围内, pH 越高,金属离子的浓度越低;
2、金属离子的价数就是浓度随pH变化的斜率,其中
lg[Men+] 与pH的关系,斜率分别为 -1、-2、-3。 Ag+、Hg+ 的斜率为 1; Ca2+ 、 Mg2+ 、 Fe2+ 、 Mn2+ 、 Zn2+ 、 Pb2+ 、 Cu2+ 、 Hg2+ 、 Ni2+ 、 Cd2+ 、 Co2+ 的斜率为 2; Al3+、Fe3+、Cr3+ 的斜率为 3; 3、当pc = 0时(-lg[Men+] = 0 即 [Men+] = 1 mol/L), 直线在横轴上的pH值为截距 , 用下式计算:
环境化学第三章水环境化学复习知识点

第三章水环境化学1、水中八大离子:K+、Na+、Ca2+、Mg2+、HCO3-、NO3-、Cl-和SO42-为常见八种离子2、溶解气体与Henry定律:溶解于水中的气体与大气中的气体存在平衡关系,气体的大气分压P G与气体的溶解度的比表现为常数关系,称为Henry定律,该常数称为Henry定律常数K H。
[G(aq)] = K H PG K H-气体在一定温度下的亨利定理常数 (mol/L.Pa) PG -各种气体的分压 (Pa)3、水体中可能存在的碳酸组分 CO2、CO32-、HCO3-、H2CO3 ( H2CO3*)4、天然水中的碱度和酸度:碱度:水中能与强酸发生中和作用的全部物质,即能够接受质子H+的物质总量;酸度:凡在水中离解或水解后生成可与强碱(OH-)反应的物质(包括强酸、弱酸和强酸弱碱盐)总量;即水中能与强碱发生中和作用的物质总量。
5、天然水中的总碱度=HCO3-+2CO32-+ OH- —H+6、水体中颗粒物的类别(1)矿物微粒和粘土矿物(铝或镁的硅酸盐)(2)金属水合氧化物(铝、铁、锰、硅等金属)(3)腐殖质 (4)水体悬浮沉积物 (5)其他(藻类、细菌、病毒等)影响水体中颗粒物吸附作用的因素有:颗粒物浓度、温度、PH。
7、水环境中胶体颗粒物的吸附作用有表面吸附、化学吸附、离子交换吸附和专属吸附。
8、天然水的PE随水中溶解氧的减少而降低,因而表层水呈氧化性环境。
9、吸附等温线:在一定温度,处于平衡状态时被吸附的物质和该物质在溶液中的浓度的关系曲线称为吸附等温线;水环境中常见的吸附等温线主要有L-型、F-型和H-型。
10、无机物在水中的迁移转化过程:分配作用、挥发作用、水解作用、光解作用、生物富集、生物降解作用。
11、PE:pE 越小,电子活度越高,提供电子的倾向越强,水体呈还原性。
pE 越大,电子活度越低,接受电子的倾向越强,水体呈氧化性。
pe影响因素:1)天然水的pE随水中溶解氧的减少而降低;2)天然水的pE随其pH减少而增大。
第三章-水环境化学(第一次课)

ii 表示方法
总含盐量(Total Dissolved Solids-TDS),也称总矿化度: 水中所含各种溶解性矿物盐类的总量称为水的总含盐量。
总含盐量=Σ阳离子+Σ阴离子
iii 测定
重量法
总含盐量=溶解固形物
cT
[H
2 CO
* 3
](1
K1 [H
]
K1K 2 [H ]2
)
0
[H2CO*3
]
1
cT
(1
K1 [H ]
K1K 2 [H ]2
) 1
说明pH决定它们的 含量多少
1
[HCO
3
]
cT
[H ] (
K1
1
K2 [H
) ]
1
2
[CO32 ] cT
([H ]2 K1K 2
[H ] 1)1 K2
lg c2 H • ( 1 1 ) 15.59103 ( 1 1 ) c1 2.303R T1 T2 2.3038.314 298.15 273.15
c2 8.289 1.778 14.74mg / L
0 ℃时的含量14.74mg/L 20 ℃时为9.227mg/L
2.在一个标准大气压下,25℃时CO2在水中的溶解度。已知 CO2在干空气中的含量为0.0314%(体积)。
氧气的分压为
0.9813105 20.95% 0.2056105 Pa
[G(O2) ] KH PG 1.26108 0.2056105 2.590104 mol / L
[G(O2) ] 2.590104 32 8.289mg / L
第三章水环境化学

TDS=[K++Na++Ca2++Mg2+]+[HCO3-+NO3-+Cl-+SO42-
2、天然水的性质
(Characteristic of Natural Waters) (1)碳酸平衡(Balance of H2CO3) 水体中存在四种化合态:
CO2、CO32-、HCO3-、H2CO3
第三章 水环境化学
(Water Environmental Chemistry)
本章重点
1、无机污染物在水体中进行沉淀-溶解、氧化-还原、 配合作用、吸附-解吸、絮凝-沉淀的基本原理;
2、计算水体中金属存在形态;
3、pE计算;
4、有机污染物在水体中的迁移转化过程和分配系数、 挥发速率、水解速率、光解速率和生物降解速率的 计算方法。
农药
有机氯 有机磷
多氯联苯 (PCBS) 卤代脂肪烃 醚
单环芳香族化合物 苯酚类和甲酚类 酞酸酯类 多环芳烃(PAH) 亚硝胺和其他化合物
2、金属污染物 (Metal Pollutant)
Cd、 Hg、 Pb、 As、 Cr、 Cu、 Zn、 Tl、 Ni、 Be
第二节 水中无机污染物的迁移转化
强酸 弱酸 强酸弱碱盐
总酸度= [H+]+ [ HCO3-] +2[H2CO3*] - [ OH-] CO2酸度= [H+]+ [H2CO3*] - [CO32-] - [ OH-] 无机酸度= [H+]- [ HCO3-]-2 [CO32-] - [ OH-]
二、水中污染物的分布及存在形态
1、有机污染物 (Organic Pollutant)
环境化学课件第三章 水环境化学

图 水环境体系(水体)
<返回>
水环境化学是研究化学物质在天然水体中的存在形态、反应机制 、迁移转化和归趋的规律及其化学行为对生态环境的影响。水环 境化学是环境化学的重要组成部分,为水污染控制和水资源的保 护提供了科学依据。
水环境化学研究的领域包括河口、海洋、河流、湖泊等。
研究的特点是: (1)体系非常复杂 离子、分子、胶体微粒 (2)界面现象突出、重要 重金属、有机物附着在胶体微粒面
海湾 海
大洋 海洋沉积物间隙水
DP Dg K
P 0
水循环 Water cycle
1.水的自然循环: 特点:①由降雨量自然循环的大致尺度
②水的性质基本不变 2.水的社会循环 特点:①工业与生活污水的产生与排放是主
要的污染源 ②水的性质不断变化
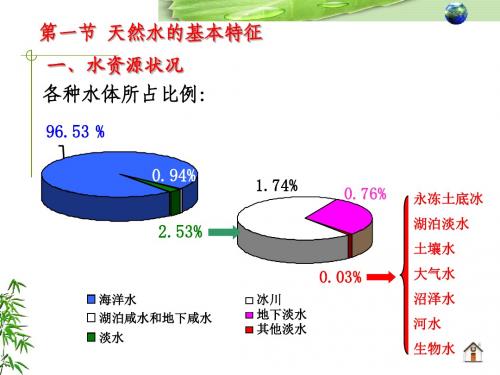
水资源的主要问题
●我国水资源人均和亩均水量少; ●水资源在地区分布上很不均匀,水土资源 组合不平衡 ●水量年内及年际变化大,水旱灾害频繁 ●水土流失严重,许多河流含沙量大; ●我国水资源开发利用各地很不均衡
第三章 水环境化学 Aquatic chemistry
知识点:认识天然水的基本特征和污染物的分布形 态,掌握水中污染物的迁移转化规律,学 会建立水质模型
重 点:水中污染物的迁移和转化规律 难 点:水质模型的建立
水圈:Hydrosphere 1978年.R.A.Horne
环境化学:第三章 水环境化学 1

第一节 天然水的基本特征及污染物的存在形态
②
CO2的溶解度
已知: 干空气中CO2的含量为0.0314%(体积),水
在25℃时蒸气压为0.03167×105 Pa, CO2的亨利定律
常数是3.34×10-7mol/(L·Pa) (25℃), CO2溶于水后发生
的化学反应是:
CO2+H2O = H++HCO3-
CO32-
60
α 40
20
0
2
4
6
8
10
pH
图3-1 碳酸化合态分布图
12
第一节 天然水的基本特征及污染物的存在形态
对于开放体系,应考虑大气交换过程:
[CO 2 (aq)] K H pCO 2
CT [CO 2 (aq)] / 0
1
0
K H pCO 2
1
K1
[HCO ] CT 1
人均水资源量相当于世界人均量的1/4。已经被联合
国列为13个贫水国家之一。
第一节 天然水的基本特征及污染物的存在形态
一、天然水的基本特征
1.天然水的组成
天然水体——包括水、水中的溶解物、悬浮物
以及底泥和水生生物。
天然水的组成按形态分为:可溶性物质和悬浮物质。
悬浮物质包括:
悬浮物、颗粒物、水生生物等。
一般情况下,天然水中存在的气体有O2、CO2、
H2S、N2和CH4等。
表3-2 海水中主要溶解气体的含量范围
气体
含量范围
/mg·L-1
O2
0~8.5
N2
CO2
H2S
Ar
8.4~14.5
(完整版)第三章水环境化学

分布分数:α0 、α1、α2分别表示化合物在总量中的比 例则:
α0=[H2CO3*]/{[H2CO3*]+[HCO3]+[CO32-] } α1 =[HCO3-]/{[H2CO3*]+[HCO]+[CO32-] } α2=[CO32-]/{[H2CO3*]+[HCO3-]+[CO32-] }
2003年我国万元GDP用水量为465m3,是世界平均水平的4 倍;农业灌溉用水有效利用系数为0.4~0.5,是发达国家 的1/2;水的重复利用率为50%,发达国家已达到了85%; 全国城市供水管网漏损率达20%左右。
水危机的出现
根据水利部《21世纪中国水供求》分析,2010年 我国工业、农业、生活及生态环境总需水量在中 等干旱年为6988亿立方米,供水总量6670亿立方 米,缺水318亿立方米。这表明,2010年后我国 将开始进入严重的缺水期。
CT=[H2CO3*]+[HCO3- ]+[CO32- ]
试计算封闭体系和开放体系中各碳酸形态的表示式? (1)封闭体系
总碳酸量不变 (2)开放体系
[H2CO3*]保持不变
封闭体系:
0
H]
k1k2 [H ]2
)1
1
HCO3 CT
(1
[H k1
]
k2 [H
)1 ]
溶解于水中气体的量可能高于亨利定律表示的量。
氧在25℃ ,1.013X105Pa下溶解度计算:
由亨利定律[G(aq)]=KH*pG
不同温度下,气体在水中溶解度的计算:
CO2在25℃ ,1.013X105Pa下溶解度计算
(4)水体富营养化(eutrophication) 由于水体中氮磷营养物质的富集,引起
环境化学(袁加程)第三章-水环境化学

3. 水体污染及水体污染源
主要的水环境污染物
悬浮物 植物性营养物 酸碱污染 难降解有机物 热污染
总碱度 = [HCO3-] + 2[CO32-] + [OH-] – [H+]
2. 天然水体中的化学平衡
酸度是指水中能与强碱发生中和作用的全部物质,亦即放 出H+或经水解能产生H+的物质总量。包括强酸、弱酸、强酸弱 碱盐等。
总酸度 = [H+] + [HCO3-] + 2[H2CO3] – [OH-]
第三章 水环境化学
第一节 水环境化学基础
天然水的基本特性 天然水体中的化学平衡 水体污染及水体污染源 水体的自净作用与水环境容量
1. 天然水的基本特性
1.1 天然水的组成
(1) 天然水的主要离子组成: K+, Na+, Ca2+, Mg2+, HCO3-, NO3-, Cl-, SO42- 为天然水中常 见的八大离子,占天然水离子总量的95-99%。
[HCO
3
]
K1[H2CO3 ] [H ]
[CO32- ]
K1K2[H2CO3 ] [H ]2
0
[H2CO3 ]
[H2CO3 ]
K1[H 2 CO 3 [H ]
]
K1K2[H2CO3 ] [H ]2
(1
K1 [H
]
K1 K 2 [H ]2
) 1
2. 天然水体中的化学平衡
第三章 水环境化学
pKc1
pKc2
结论:
Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ pH<<pKc1 pH=pKc1 pH=pKc2 pH>>pKc2 pH=1/2(pKc1+pkc2) H2CO3* αH2CO3*=αHCO3αHCO3-=αCO32CO32HCO3-
3:开放碳酸体系
= -21.6 + 2pH
由以上方程式作lgc—pH图可看出
3. 碱度的测定:
(原理: 中和滴定法,根据消耗的酸量求出)
c V 1000 碱度(mmol/L ) Vs 单位:mmol[H ]/L
式中:Vs——水样体积)(mL) c——HCl浓度(mol/L) V——HCl体积(mL)
思考:碱度和碱性的区别
例如:若一个天然水的pH为7.0,碱度为1.4mmo1/l, 求需加多少酸才能把水体的pH降低到6.0。
二、水体中的污染物
病原体污染物
耗氧污染物 植物营养物 石油类污染物 放射性物质
酸、碱、盐无机污染物
热污染
有毒污染物
(1)重金属
(2)无机阴离子 (3)有机农药、多氯联苯 (4)致癌物质 (5)一般有机物质
三、水体中的污染物的运动过程
大气降落物 污水排入
1.稀释、扩散过程
3.转化过程
溶解在天然水中的物质
1、主要离子 主要阳离子有: Ca2+、Mg2+、Na+、K+。 主要阴离子有: Cl-、SO42-、HCO3-、CO32-。 这八种离子可占水中溶解固体总量的95%~99%以上。 陆地水中下列成分的含量顺序一般为: HCO3- >SO42- >Cl-,Ca2+ >Na+ >Mg2+ 海水中相应的含量顺序为: Cl- >SO42- >HCO3-,Na+ >Mg2+ >Ca2+。
第三章 水环境化学

6
1、天然水的组成(离子、溶解气体、水生生物) 天然水是含有可溶性物质和悬浮物的一种天 然溶液。可溶性物质非常复杂,主要是岩石风化 过程中,经过水溶解迁移、搬运到水中的地壳矿 物质。
7
(1)天然水中的主要离子组成
天然水中常见的八大离子: K+ 、 Na+ 、 Ca2+ 、 Mg2+ 、 HCO3- 、 NO3- 、 Cl- 、 SO42-。 常见的八大离子占天然水中离子总量的95%-99%。 水中这些主要离子,常用来作为表征水体主要化学特征性指标。 硬 Ca2+ HCO3度 Mg2+ CO32碱 度 酸 H+ OH碱 金 属
1 =0.3086 2.24 1 2.24 =0.6914 2.24 1
[ H 2 CO3 ] [ HCO3 ]
*
所以此时[H2CO3*]=α0CT=0.3086×3×10-3molL-1=0.9258×10-3molL-1 [HCO3-]=α1CT=0.6914×3×10-3molL-1=2.0742×10-3molL-1 加酸性废水到pH=6.7,有0.9258×10-3molL-1的H2CO3*生成,故每升河水中要加入 0.9258×10-3mol的H+才能满足上述要求,这相当于每升河水中加入浓度为1×10-2 molL-1的硫酸废水的量V为: V=0.9258×10-3mol/(2×1×10-2molL-1)=0.0463L=46.3mL。因此相当于每升河水中
100 CO2+H2CO3 HCO3CO32-
80 60 40 20 0
2 4 6 pH 8 10 12
28
碳酸化合态分布图的理解: a、总体分布态势:
资源与环境化学 第三章 第三部分(水污染控制)

《资源与环境化学》 第三章 水环境化学
第8页
《资源与环境化学》 第三章 水环境化学
活性污泥法污水处理工艺流程
第9页
《资源与环境化学》 第三章 水环境化学
B、生物过滤法 在过滤池中,废水被喷淋在表面上覆盖有发达微生物膜的石 块或其他滤料上,这些滤料在化学上是惰性的。 生物膜,实际上是一种胶状膜(Schmutzdecke),其中含有 成熟的微生物,包括细菌、真菌和原生动物等。 在设计生物过滤池时,应考虑其结构能使废水与空气得到充 分的接触,以便生物膜和废水层从空气中吸收氧气。
第11页
(3)三级处理
《资源与环境化学》 第三章 水环境化学
三级处理也称高级处理或深度处理,它是将二级处理未能去 除的部分污染物进一步净化处理,常用超滤、活性炭吸附、离子 交换、电渗析等。其处理内容为去除某些重金属毒物,进一步去 除可溶性无机物(富营养物)、部分有机物以及细菌、病毒等微 生物。经过三级处理后的污水, BOD5去除率在 95%以上,出水 浓度降至5mg/L以下,可直接回用于工业。
三级处理系统
第12页
《资源与环境化学》 第三章 水环境化学
一级处理 二级处理 三级处理
废水
格 栅
沉沙 池
沉淀 池
生物曝气 池或生物 滤池
二次沉淀 池
混凝、过 滤、离子 交换、消 毒等设备
回流污泥 一级处理出水 (排放、灌溉) 二级处理出水 三级处理出水 (排放、灌溉) (排放、再用)
垃圾 处理
沉渣 处理
第14页
《资源与环境化学》 第三章 水环境化学
1、沉淀池的应用 沉淀池通常为径流流经的简易水池。 沉淀池的位臵设臵: 有的沉淀池紧接排水管渠出口,仅比排水管渠更深、更宽 一些。还有的沉淀池就是开挖的深坑或沟渠,其位臵紧挨 着停车场、商场、房屋开发区或高速公路。 沉淀池作用: 由于沉淀池内水流经的横断面积要比排水渠大,径流经 过时流速会下降。这使得径流在流出沉淀池以前就有部分 沉积物沉淀到池底。 城市径流中许多污染物与固体悬浮物相关,因此固体悬 浮物沉淀后可使大量BOD、营养盐、碳氢化合物、金属和 农药得以去除。 * 断流期间,需周期性地将沉淀池内积累的沉积物挖出并装 运填埋。否则可能对地表径流的污染物流量产生影响 。
第三章 水环境化学习题解答

第三章水环境化学一、填空题1、天然水体中常见的八大离子包括:K+、Na+、Ca2+、Mg2+、HCO3-、NO3-、Cl-、SO42-。
2、天然水体中的碳酸平衡体系a0、a1、a2分别表示[H2CO3*]、[HCO3-]、[CO32-]的分配系数,其表达式分别为:(用pH\K1\K2表达):a 0=[H2CO3*]/{[ H2CO3*]+[ HCO3-]+[ CO32-]}=[H+]2/{[H+]2+K1[H+]+K1K2}a 1=[ HCO3-] /{[ H2CO3*]+[ HCO3-]+[ CO32-]}= K1[H+]/{[H+]2+K1[H+]+K1K2}a 2=[ CO32-] /{[ H2CO3*]+[ HCO3-]+[ CO32-]}= K1K2/{[H+]2+K1[H+]+K1K2}。
(注:此三个公式前半段教材119-120页有错误!)a 0+a1+a2=13、根据溶液质子平衡条件得到酸度低表达式:总酸度=[H+]+2[ H2CO3*]+[HCO3-]-[OH-];CO2酸度= [H+]+[H2CO3*]-[CO32-]-[OH-](注:教材121此公式错误),无机酸度= [H+]-[HCO3-]-2[CO32-] -[OH-] 。
4、根据溶液质子平衡条件得到酸度低表达式:总碱度= [OH-] +2[CO32-]+[HCO3-]-[H+];酚酞碱度= [OH-] +[CO32-]-[H+]-[ H2CO3*];苛性碱度= [OH-] -2[ H2CO3*]-[HCO3-]-[H+]。
5、“骨痛病事件”的污染物是镉;水俣病的污染物是汞(或甲基汞)。
6、水体的富营养化程度一般可用总磷(TP)、总氮(TN)、叶绿素a、透明度等指标来衡量。
7、水环境中氧气充足的条件下有机物发生的生物降解称为有氧(或好氧)降解,最终产物主要为二氧化碳和水,有机氮转化为硝酸根,有机硫转化为硫酸根。
水中的有机物在无氧条件经微生物分解,称为厌氧降解,降解产物除二氧化碳和水外,还有小分子的醇、酮、醛、酸等,无机态氮主要以氨氮存在、硫主要以硫化物存在,水体发臭发黑。
环境化学课后答案(戴树桂)主编_第二版(1-7章)

第三章水环境化学1、什么是表面吸附作用,离子交换吸附作用和专属吸附作用并说明水合氧化物对金属离子的专属吸附和非专属吸附的区别.(1)表面吸附:由于胶体表面具有巨大的比表面和表面能,因此固液界面存在表面吸附作用.胶体表面积越大,吸附作用越强.(2)离子交换吸附:环境中大部分胶体带负电荷,容易吸附各种阳离子.胶体每吸附一部分阳离子,同时也放出等量的其他阳离子,这种作用称为离子交换吸附作用,属于物理化学吸附.该反应是可逆反应,不受温度影响,交换能力与溶质的性质,浓度和吸附剂的性质有关.(3)专属吸附:指在吸附过程中,除了化学键作用外,尚有加强的憎水键和范德化力或氢键作用.该作用不但可以使表面点荷改变符号,还可以使离子化合物吸附在同号电荷的表面上.(4)水合氧化物对金属离子的专属吸附与非金属吸附的区别如下表所示.快速可逆请叙述氧化物表面吸附配合模型的基本原理以及与溶液中配合反应的区别。
2、已知Fe3+与水反应生成的主要配合物及平衡常数如下:Fe3+ + H2OFe(OH)2+ + H+ lgK1= - 2.16Fe3+ + 2H2OFe(OH)2+ + 2H+ lgK2= - 6.74Fe(OH)3(s) Fe3+ + 3OH- lgKso= - 38Fe3+ + 4H2OFe(OH)4- + 4H+ lgK4= - 232Fe3+ + 2H2OFe2(OH)24+ + 2H+ lgK= - 2.91请用pc-pH图表示Fe(OH)3(s)在纯水中的溶解度与pH的关系.解:(1)K1=[Fe(OH)2+][H+]/ [Fe3+]=[Fe(OH)2+]KW3/Kso[H+]2p[Fe(OH)2+]=3 lgKW - lgKso + 2 pH - lgK1=2 pH - 1.84(2)K2=[Fe(OH)2+][H+]2/ [Fe3+]=[Fe(OH)2+]KW3/Kso[H+]p[Fe(OH)2+]=3 lgKW - lgKso + pH - lgK2=pH + 2.74(3)Kso=[Fe3+][OH-]3=[Fe3+]KW3/[H+]3p[Fe3+]=3 lgKW - lgKso + 3 pH=3 pH - 4(4)K4=[Fe(OH)4-][H+]4/ [Fe3+]=[Fe(OH)4-][H+]KW3/ Ksop[Fe(OH)4-]=3 lg KW - lgK4 - lgKso - pH=19 - pH(5)K=[Fe2(OH)24+][H+]2/ [Fe3+]2=[Fe2(OH)24+]KW6/ Kso2[H+]4p[Fe2(OH)24+]=6 lg KW - lgK - 2 lgKso + 4 pH=4 pH - 5.09用pc-pH图表示Fe(OH)3(s)在纯水中的溶解度与pH的关系如下4解释下列名词:分配系数;标化分配系数;辛醇-水分配系数;生物浓缩因子;亨利定律常数;水解速率;直接光解;光量子产率;生长物质代谢和共代谢.(1)分配系数:在土壤-水体系中,土壤对非离子性有机化合物的吸着主要是溶质的分配过程(溶解),即非离子性有机化合物可通过溶解作用分配到土壤有机质中,并经过一定时间达到分配平衡,此时有机化合物在土壤有机质和水中含量的比值称为分配系数.(2)标化分配系数:有机化合物在颗粒物-水中的分配系数与颗粒物中有机碳呈正相关,以固相有机碳为基础的分配系数即标化分配系数.(3)辛醇-水分配系数:有机化合物的正辛醇-水分配系数(KOW)是指平衡状态下化合物在正辛醇和水相中浓度的比值.它反映了化合物在水相和有机相之间的迁移能力,是描述有机化合物在环境中行为的重要物理化学参数.KOW与化合物的水溶性,土壤吸附常数和生物浓缩因子等密切相关.(4)生物浓缩因子:有机毒物在生物体内浓度与水中该有机物浓度之比.(5)亨利定律常数:通常可理解为非电解质稀溶液的气-水分配系数.(6)水解速率:反映某一物质在水中发生水解快慢程度的一个参数.(7)直接光解:化合物本身直接吸收太阳能而进行分解反应.(8)光量子产率:分子被活化后,它可能进行光反应,也可能通过光辐射的形式进行"去活化"再回到基态,进行光化学反应的光子数占吸收光子数之比称为光量子产率.(9)生长物质代谢和共代谢:生物降解过程中,一些有机污染物作为食物源提供能量和提供酶催化反应分解有机物,这称为生长物质代谢.某些有机污染物不能作为微生物的唯一碳源与能源,必须有另外的化合物存在提供微生物碳源或能源时,该有机物才能被降解,这种现象称为共代谢.5请叙述有机物在水环境中的迁移,转化存在哪些重要过程.(1)负载过程:污水排放速率,大气沉降以及地表径流引入有机毒物至天然水体均将直接影响污染物在水中的浓度.(2)形态过程:①酸碱平衡:天然水中pH决定着有机酸或碱以中性态存在的分数,因而影响挥发及其他作用.②吸着作用:疏水有机化合物吸着至悬浮物上,由于悬浮物质的迁移而影响它们以后的归趋.(3)迁移过程:①沉淀-溶解作用:污染物的溶解度范围可限制污染物在迁移,转化过程中的可利用性或者实质上改变其迁移速率.②对流作用:水力流动可迁移溶解的或者被悬浮物吸附的污染物进入或排出特定的水生生态系统.③挥发作用:有机污染物可能从水体进入大气,因而减少其在水中的浓度.④沉积作用:污染物被吸附沉积于水体底部或从底部沉积物中解吸,均可改变污染物的浓度.(4)转化过程:①生物降解作用:微生物代谢污染物并在代谢过程中改变它们的毒性.②光解作用:污染物对光的吸收有可能导致影响它们毒性的化学反应的发生.③水解作用:一个化合物与水作用通常产生较小的,简单的有机产物.④氧化还原作用:涉及减少或增加电子在内的有机污染物以及金属的反应都强烈地影响环境参数.(5)生物累积过程:①生物浓缩作用:通过可能的手段如通过鱼鳃的吸附作用,将有机污染物摄取至生物体.②生物放大作用:高营养级生物以消耗摄取有机毒物进入生物体低营养级生物为食物,使生物体中有机毒物的浓度随营养级的提高而增大.请叙述有机物水环境归趋模式的基本原理。
资源与环境化学 第三章 第一部分(天然水组成与化学平衡)

不同温度下气体在水中的溶解度:Clausius-Clapeyron方程
C2 H 1 1 lg ( ) C1 2.303 R T1 T2 C1 , C2 为绝对温度为T1 , T2时气体在水中的溶解度 H 溶解热, J/mol R 气体常数,8.314 J/mol K
《资源与环境化学》 第三章 水环境化学
第三章 水环境化学
Chapter 3. Aquatic Environmental Chemistry
第一部分 天然水的组成与化学平衡
主讲:刘耀驰
中南大学化学化工学院
第1页
《资源与环境化学》 第三章 水环境化学
本章重点
无机污染物在水体中进行沉淀-溶解、氧化还原、配合作用、吸附-解吸、絮凝-沉淀的基 本原理; 计算水体中金属存在形态;
《资源与环境化学》 第三章 水环境化学
(3) 气体在水中的溶解性
亨利定律:大气中的气体与溶液中同种气体间的平衡为:
kH 是各种气体在一定温度 下的亨利定律常数 (mol/L· Pa),pg为分压
[G(aq)] = kH×pg
亨利定律并不能说明气体在溶液中进一步的化学反应 溶解于水中的实际气体量,可以大大高于亨利定律表示的量
K2
2 ] [H ][CO 3 -] [HCO 3
K1[H 2CO3 ] [HCO 3 ] [H ] 2 ] K 2 K1[H 2CO3 ] [CO3 [H ]
第10页
《资源与环境化学》 第三章 水环境化学
(4) 水生生物
生态系统、食物链中的一个重要环节; 生产者、消费者、分解者; 自养生物、异养生物; 生产率、富营养化、C、N、P
第11页
第3章:水环境化学2-1

一、颗粒物与水之间的迁移
1、水中颗粒物的类别
天然水中颗粒物主要包括五大类:矿物、金属水合氧 化物、腐殖质、悬浮物、其他泡沫、表面活性剂等半胶体 以及藻类、细菌、病毒等生物胶体。
(1)非粘土矿物和粘土矿物:都是原生岩石在风化过程 中形成的。
非 粘 土 矿 物 : 天 然 水 中 常 见 为 石 英 (SiO2) 、 长 石 (KalSi3O8)等,晶体交错,结实、颗粒粗,不易碎裂,缺 乏粘结性(例如沙子主要成分为:SiO2)。
第二节、水中无机污染物的迁移转化
一、颗粒物与水之间的迁移 二、水中胶体颗粒物聚集的基本原理和方式 三、溶解和沉淀 四、氧化—还原
五、配合作用
无机污染物,特别是重金属和准金属等污染物,一旦进入 水环境,不能被生物降解;
主要通过吸附—解吸、沉淀—溶解、氧化—还原、配合作 用、胶体形成等一系列物理化学作用进行迁移转化,参与和 干扰各种环境化学过程和物质循环过程; 最终以一种或多种形式长期存留在环境中,造成永久性的 潜在危害。 重点介绍重金属污染物在水环境中迁移转化的基本原理。
在水环境中,配合离子、有机离子、有机高分子和无机高 分子的专属吸附作用特别强烈。例如,简单的Al3+、Fe3+高 价离子并不能使胶体电荷因吸附而变号,但其水解产物却 可达到这种效果,这就是发生专属吸附的结果。 水合氧化物胶体对重金属离子有较强的专属吸附作用,这 种吸附作用发生在胶体双电层的 Stern层中,被吸附的金属 离子进入Stern层后。不能被通常提取交换性阳离子的提取 剂提取,只能被亲和力更强的金属离子取代,或在强酸性 条件下解吸。
粘土矿物:天然水中常见为云母、蒙脱石、高 岭石,层状结构,易于碎裂,颗粒较细,具有粘 结性,可以生成稳定的聚集体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章水环境化学
18
第七节 有机污染物的水环境化学
7.1 有机物污染程度的指标
▪ 溶解氧 DO (dissolved oxygen) 水中溶解的氧的量。
耗氧作用:使 DO 下降,如耗氧有机物分解,生物 呼吸等。
复氧作用:使 DO 增加,如空气中氧的溶解,水生 植物的光合作用。
有机物的氧化分解需要消耗大量的氧,若有机物过多, 会造成水中 DO 量不断减少,可导致有机物缺氧分解而产生 腐败现象。
第三章 水环境化学
第三章水环境化学
1
第六节 水体的氮、磷污染和富营养化
水体营养物增加导致水生植物(主要是浮游植 物和各种藻类)大量繁殖,水体溶解氧下降,水质 恶化,鱼类及其它生物大量死亡的现象。
在湖泊、水库、河口、港湾等水流缓慢的地 区最容易发生,是由氮、磷等化合物过多排入水 体所引发的二次污染现象。
第三章水环境化学
3
在适当的温度、光照和环境酸度下,天然水体中的藻 类进行光合作用,合成本身的藻类原生质。
106 CO2 + 16 NO3- + HPO42- + 122 H2O + 18 H+ + 能量 + 微量元素
C106H263O116N16P (藻类原生质) + 138 O2
藻类的繁殖中成为控制性因பைடு நூலகம்的是无机态的氮 和磷营养物。
第三章水环境化学
8
受蓝藻污染的太湖水
工作人员在打捞蓝藻
第三章水环境化学
9
第三章水环境化学
10
云南滇池的蓝藻污染
第三章水环境化学
11
云南滇池的蓝藻污染
第三章水环境化学
12
赤潮
第三章水环境化学
13
2000 年舟山群岛赤潮
第三章水环境化学
14
珊瑚的坟场
第三章水环境化学
15
6.5 富营养化的防治
第三章水环境化学
4
6.2 N、P 的主要来源
▪ 雨水
NO3-:
0.16 mg/L ~ 1.06 mg/L
NH3、NH4+: 0.04 mg/L ~ 1.70 mg/L
P:
0.01 mg/L
▪ 农业排水:化肥的应用引入氮磷。
▪ 城市污水:排泄物,食品污物, 合成洗涤剂 ( 50~70% 的总磷)等。
▪ 其它:工业废水,水产养殖,地下水,底泥等。
第三章水环境化学
5
6.3 湖水的富营养化程度
▪ 总磷含量:水中的正磷酸盐、聚合磷酸盐、可水解磷酸 盐及有机磷总浓度(可用标准分析法测定)。
▪ 总氮含量:氨氮、亚硝酸盐、硝酸盐、有机氮的总和 ( 可以各自测定后加和)。
▪ 叶绿素a 含量:水中绿色物质含量。 (丙酮萃取后,测 665nm 处吸光度)。
第三章水环境化学
2
6.1 引起富营养化的物质
▪ 营养盐类
C:水中溶解的 CO2,含量稳定。 N:NO3-,NO2-,NH3,NH4+,尿素等。 P:无机态或有机态。
水体富营养化: 无机态氮> 300 mg/m3 总磷 > 20 mg/m3
▪ 微量元素 Fe,Zn,Mn,Cu,B,Mo,Co,I,V 等。 ▪ 维生素,有机物。
RCOOH + CO2 + NH3
II: 2NH3 + 3O2 2HNO2 + O2
2HNO2 + 2H2O 2HNO3
一般指将有机物分解为 CO2,NH3,H2O 的过程 (I)。
BOD20:一般可认为分解在 20 天内完成,用 BOD20 表示。 BOD5: 20oC,5天内可完成 70~80%,称为五日生化需氧 量。
洗衣粉中大多含有 17%左右的三聚磷酸钠,成为造 成富营养化污染的磷的主要来源。
目前世界很多国家已经实行了禁磷措施。 对生活废水进行三级处理是消减水体磷负荷的最有效 途径。
第三章水环境化学
7
▪ 增加给水处理成本
▪ 还原态氮会因硝化作用消耗大量的溶解氧。
▪ 化合态氮对生物和人体具有毒性。
水中氨氮含量超过 1 mg/L 时,会使水生生物血液结 合氧量降低,超过 3 mg/L 时,可于 24~96 小时内使金 鱼、鳊鱼等死亡。饮用氨氮含量超过 10 mg/L 的水,可 以引起高铁血红蛋白症。有机氮亦可经微生物作用转化 为硝酸盐和亚硝酸盐。
第三章水环境化学
16
第三章水环境化学
17
▪ 生物脱氮技术: 利用微生物将含氮化合物最终转化为 N2。
亚硝化细菌
NH4+
NO2-
硝化细菌
反硝化细菌
NO3-
N2
O2
O2
▪ 沉淀法除磷:加入沉淀剂生成难溶物而去除水中的磷。
利用消石灰在 pH=11 时,可以除去 90%的磷,生 成 Ca5(OH)(PO4)3 沉淀。
▪ 透明度
第三章水环境化学
6
6.4 N、P 污染的危害性
▪ 水体富营养化
水体富营养化引起藻类恶性繁殖,产生毒素。藻类 死亡后分解消耗大量溶解氧,严重影响鱼类生存。大量 藻类导致水流变缓。近海发生赤潮、棕潮、绿潮等。
磷污染对水体富营养化的影响更大。藻类的过度繁殖 与磷酸盐的含量之间存在某些平行关系。
21
▪ 化学需氧量 COD (chemical oxygen demand)
水中能被氧化的物质在规定条件下进行化学氧化 所消耗氧化剂的量,以 O2 计,单位为 mg/L。
KMnO4 法(CODMn):测定较清洁水样。 K2Cr2O7 法(CODCr):测定严重污染水样或工业废水。
优点:测量快,不受水质条件限制。 缺点:不能正确反应微生物氧化所需消耗的氧量。
DO 正常值:5 ~ 10 mg/L,海水可达 14 mg/L。
当 DO<4 mg/L时,鱼类将死亡。
第三章水环境化学
19
▪ 生化需氧量 BOD ( biochemical oxygen demand)
水体中微生物分解有机物过程消耗水中溶解氧的 量,单位为 mg/L。
氨基酸的分解:
I: RCH(NH2)COOH + O2
第三章水环境化学
20
优点:能正确反映水中有机物氧化分解时消耗的氧量。 缺点:测量时间长,反映环境问题不及时,受水中有毒
物质影响。
BOD
< 1mg/L: 清洁 > 3~4 mg/L:受到有机物污染
城市生活污水:BOD < 100 mg/L 工业污水: BOD 常大于1000 mg/L
第三章水环境化学
不能把水中有机物全部氧化。
KMnO4 法: 约 60%。 K2Cr2O7 法:80~90%。
水质相对稳定时:
CODCr > BOD20 第>三B章O水D环境5 化>学CODMn
22
▪ 总有机碳 TOC (total organic carbon) 与总需氧量 TOD (total oxygen demand)
