《有机合成讲义》PPT课件
合集下载
有机合成课件6章(缩合反应)(最新版)
NH
CH CH Ph
H3C O2N P2N O NO2
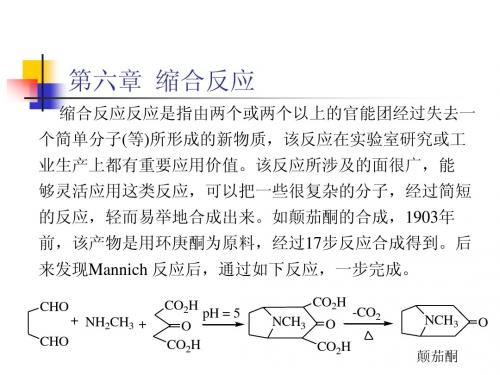
4. Knoevenagel反应: 这类反应的特点是一个亚甲基上连接两个吸电子基团, 使得其氢活性明显提高,反应较易进行。一般使用弱碱(有 机胺)作催化剂即可,甚至不使用催化剂。
第六章 缩合反应
如:
CH2(CN)2
O CH2-C-H
CH3CHO
OH CH3-CH-CH2-CH=O 不稳定,易脱水
CH3CH=CH-CHO
从反应过程来看,应该有两种可能缩合产物。表示如下:
第六章 缩合反应
O CH2-C-H (1) CH3-CH=O CH2=CH-O O H C-CH3 (2) CH3-CH-CH2-CH=O O CH3-CH-CH2-CHO (1) OH H =-16.62KJ/mol
和卤代酸酯的反应(Darzenes) 该反应也要在强作用下完成。如:
O + ClCH2CO2C2H5 t BuOK 83~95% O CO2C2H5
其反应过程为:
ClCH2CO2C2H5 Cl
t BuOK
ClCHCO2C2H5
O
CHCO2C2H5 O O
CO2C2H5
第六章 缩合反应
3,醛(酮)与其它化合物的缩合: 1)硝基化合物:
CHO CHO + NH2CH3 + CO2H O CO2H pH = 5 CO2H NCH3 O CO2H -CO2 NCH3 O
颠茄酮
第六章 缩合反应
一,碳负离子历程的缩合反应
这类反应很多,如羟醛(酮) 缩合,酯缩合等。其反应历程为:
C + C= O C O C 产物
1,醇醛缩合:
CH3CHO NaOH -H2O
CH CH Ph
H3C O2N P2N O NO2
4. Knoevenagel反应: 这类反应的特点是一个亚甲基上连接两个吸电子基团, 使得其氢活性明显提高,反应较易进行。一般使用弱碱(有 机胺)作催化剂即可,甚至不使用催化剂。
第六章 缩合反应
如:
CH2(CN)2
O CH2-C-H
CH3CHO
OH CH3-CH-CH2-CH=O 不稳定,易脱水
CH3CH=CH-CHO
从反应过程来看,应该有两种可能缩合产物。表示如下:
第六章 缩合反应
O CH2-C-H (1) CH3-CH=O CH2=CH-O O H C-CH3 (2) CH3-CH-CH2-CH=O O CH3-CH-CH2-CHO (1) OH H =-16.62KJ/mol
和卤代酸酯的反应(Darzenes) 该反应也要在强作用下完成。如:
O + ClCH2CO2C2H5 t BuOK 83~95% O CO2C2H5
其反应过程为:
ClCH2CO2C2H5 Cl
t BuOK
ClCHCO2C2H5
O
CHCO2C2H5 O O
CO2C2H5
第六章 缩合反应
3,醛(酮)与其它化合物的缩合: 1)硝基化合物:
CHO CHO + NH2CH3 + CO2H O CO2H pH = 5 CO2H NCH3 O CO2H -CO2 NCH3 O
颠茄酮
第六章 缩合反应
一,碳负离子历程的缩合反应
这类反应很多,如羟醛(酮) 缩合,酯缩合等。其反应历程为:
C + C= O C O C 产物
1,醇醛缩合:
CH3CHO NaOH -H2O
有机化学有机合成ppt课件

16
合成路线:
浓 HNO3
浓H2SO4
Br
H2 Fe NO2
NH2 Br
Br2
NaNO2 H3PO2
Br
Br H2SO4 H2O
Br
Br
NH2
17
例四:用苯和二个或二个碳以下的有机原料和无机试剂合成:
OH + N Cl-
逆合成分析:
OH + N Cl-
O
N
OH N
O + HCHO + HN(CH3)2
H+
CH2OH
32
例十一 用苯,苯甲酸和五个碳以下的简单有机原料合成:
Ph O
O Ph
33
逆合成分析:
Ph O
O
Ph CHO
+ PhCH2CH2MgBr
OH Ph
CH2OH
PhCH2CH2Br
Br + CH2O
PhCH2CH2OH
O PhMgBr +
34
合成路线:
Br2
Mg Br anhydrous
7
(3) 碳架的重组;
碳架重组的反应是各种重排反应,包括: *1 Wegner-Meerwein 重排; *2 频哪醇 (Pinacol) 重排; *3 异丙苯氧化重排; *4 Bechmann 重排; *5 Favosky 重排; *6 Baeyer-Villiger 氧化重排; *7 Hofmann 重排; *8 联苯胺重排; *9 Benzilic acid重排;
H2O OH
Br Mg/I2
无水醚
H+
O CH3I O
O
OH
23
例七 用不超过二个碳的简单有机原料或苯合成下列化合物: O
合成路线:
浓 HNO3
浓H2SO4
Br
H2 Fe NO2
NH2 Br
Br2
NaNO2 H3PO2
Br
Br H2SO4 H2O
Br
Br
NH2
17
例四:用苯和二个或二个碳以下的有机原料和无机试剂合成:
OH + N Cl-
逆合成分析:
OH + N Cl-
O
N
OH N
O + HCHO + HN(CH3)2
H+
CH2OH
32
例十一 用苯,苯甲酸和五个碳以下的简单有机原料合成:
Ph O
O Ph
33
逆合成分析:
Ph O
O
Ph CHO
+ PhCH2CH2MgBr
OH Ph
CH2OH
PhCH2CH2Br
Br + CH2O
PhCH2CH2OH
O PhMgBr +
34
合成路线:
Br2
Mg Br anhydrous
7
(3) 碳架的重组;
碳架重组的反应是各种重排反应,包括: *1 Wegner-Meerwein 重排; *2 频哪醇 (Pinacol) 重排; *3 异丙苯氧化重排; *4 Bechmann 重排; *5 Favosky 重排; *6 Baeyer-Villiger 氧化重排; *7 Hofmann 重排; *8 联苯胺重排; *9 Benzilic acid重排;
H2O OH
Br Mg/I2
无水醚
H+
O CH3I O
O
OH
23
例七 用不超过二个碳的简单有机原料或苯合成下列化合物: O
有机合成课件1-2(绪论和氧化反应)

⑴十九世纪上半叶,有机合成只是一般新学科的出现; ⑵十九世纪下半叶开始,英国等老牌资本主义工业的
发展,大大促进了有机合成技术的发展:如染料、 炸药、合成橡胶、医药,等开始进入工业化。
第一章 有机合成化学的地位和任务
2,有机合成化学的历史:
⑶二十世纪开始,有机合成技术进一步得到重视,真正进 入工业化。各国的技术开始进行竞争。
第一章 有机合成化学的地位和任务
3、对等性
合成团(synthon)是有机合成的术语,是指 一般反应可
结合的单位,如与CH3-相当的合成团可以是CH3MgI、
CH3Li等。和CH3C=O相当的合成团可以是CH3COO,
CH3CO2OR等。合成团的对等用
或 表示。
要注意:对等表示作用上的相似,但在反应活性,立体
O
MnO2
H
C
O
O
O
O
第二章 氧化反应
3、高碘酸可使下列单元结构发生C—C键断裂,并 可进行结构鉴定。
OH OH
OH O
O
O
OH OH O
如:
HO2C
CO2H
OH OH
HIO4
2 OHC CO2H + H2O + HIO3
第二章 氧化反应
4、酚的氧化
过硫酸钾碱性溶液把酚氧化成对苯二酚:
OH
OH
K2S2O8
第一章 有机合成化学的地位和任务
3)立体选择性:在反应过程中产生非对映异构,其 一异构体远远超过另一异构体,称为立体选择性。如:
H3C 空阻小
CH3 CH3
O 空阻大
LiAlH4 Et2O
CH3 CH3
OH H3C
90% H
发展,大大促进了有机合成技术的发展:如染料、 炸药、合成橡胶、医药,等开始进入工业化。
第一章 有机合成化学的地位和任务
2,有机合成化学的历史:
⑶二十世纪开始,有机合成技术进一步得到重视,真正进 入工业化。各国的技术开始进行竞争。
第一章 有机合成化学的地位和任务
3、对等性
合成团(synthon)是有机合成的术语,是指 一般反应可
结合的单位,如与CH3-相当的合成团可以是CH3MgI、
CH3Li等。和CH3C=O相当的合成团可以是CH3COO,
CH3CO2OR等。合成团的对等用
或 表示。
要注意:对等表示作用上的相似,但在反应活性,立体
O
MnO2
H
C
O
O
O
O
第二章 氧化反应
3、高碘酸可使下列单元结构发生C—C键断裂,并 可进行结构鉴定。
OH OH
OH O
O
O
OH OH O
如:
HO2C
CO2H
OH OH
HIO4
2 OHC CO2H + H2O + HIO3
第二章 氧化反应
4、酚的氧化
过硫酸钾碱性溶液把酚氧化成对苯二酚:
OH
OH
K2S2O8
第一章 有机合成化学的地位和任务
3)立体选择性:在反应过程中产生非对映异构,其 一异构体远远超过另一异构体,称为立体选择性。如:
H3C 空阻小
CH3 CH3
O 空阻大
LiAlH4 Et2O
CH3 CH3
OH H3C
90% H
有机合成ppt课件公开课

高效合成策略
研究者不断探索更加高效、快速的合成策略,以提高有机合成的效 率和产率,缩短合成路线。
生物催化与转化
利用酶作为催化剂进行有机合成,具有高选择性、高活性和环保的 优点,是当前研究的热点之一。
有机合成面临的挑战
01
02
03
合成路线的复杂性
有机合成涉及众多反应步 骤和条件,如何设计简洁 、高效的合成路线是关键 问题。
产物分离与纯化
在有机合成中,产物往往 与副产物和原料混合在一 起,如何高效地进行分离 和纯化是一个难题。
催化剂的研发
设计高效、稳定且环保的 催化剂是有机合成的核心 问题之一,需要不断进行 研究和改进。
有机合成的未来展望
新反应、新方法的探索
01
随着科学技术的不断发展,未来将有更多新反应、新方法被发
现和开发,推动有机合成的进步。
ERA
有机合成的定义
有机合成是指在有机化学理论 指导下,利用有机反应将简单 有机物或无机物转化为复杂有 机物的进程。
有机合成涉及多种反应类型, 如加成反应、取代反应、消去 反应、氧化还原反应等。
有机合成遵循原子经济性原则 ,旨在实现高效、环保的物质 转化。
有机合成的重要性
有机合成是化学工业的重要支柱,为医药、农药、染料、香料等领域提供关键中间 体和原料。
材料都符合质量标准,并依照正确的比例进行配制。
02
实验场地准备
确保实验场地安全、整洁,透风良好,并配备相应的消防设施。同时,
应远离易燃、易爆物品,并确保电源稳定。
03
实验人员准备
实验人员应具备相应的有机化学知识和实验技能,熟悉实验操作流程和
注意事项。在实验前,应穿着好个人防护装备,如实验服、化学防护眼
研究者不断探索更加高效、快速的合成策略,以提高有机合成的效 率和产率,缩短合成路线。
生物催化与转化
利用酶作为催化剂进行有机合成,具有高选择性、高活性和环保的 优点,是当前研究的热点之一。
有机合成面临的挑战
01
02
03
合成路线的复杂性
有机合成涉及众多反应步 骤和条件,如何设计简洁 、高效的合成路线是关键 问题。
产物分离与纯化
在有机合成中,产物往往 与副产物和原料混合在一 起,如何高效地进行分离 和纯化是一个难题。
催化剂的研发
设计高效、稳定且环保的 催化剂是有机合成的核心 问题之一,需要不断进行 研究和改进。
有机合成的未来展望
新反应、新方法的探索
01
随着科学技术的不断发展,未来将有更多新反应、新方法被发
现和开发,推动有机合成的进步。
ERA
有机合成的定义
有机合成是指在有机化学理论 指导下,利用有机反应将简单 有机物或无机物转化为复杂有 机物的进程。
有机合成涉及多种反应类型, 如加成反应、取代反应、消去 反应、氧化还原反应等。
有机合成遵循原子经济性原则 ,旨在实现高效、环保的物质 转化。
有机合成的重要性
有机合成是化学工业的重要支柱,为医药、农药、染料、香料等领域提供关键中间 体和原料。
材料都符合质量标准,并依照正确的比例进行配制。
02
实验场地准备
确保实验场地安全、整洁,透风良好,并配备相应的消防设施。同时,
应远离易燃、易爆物品,并确保电源稳定。
03
实验人员准备
实验人员应具备相应的有机化学知识和实验技能,熟悉实验操作流程和
注意事项。在实验前,应穿着好个人防护装备,如实验服、化学防护眼
有机合成课件3章(还原反应)

H CO
O
H3C ArCH3
TICl3/K THF
CH3 H3C Ar
还有一个还原关环的方法:
CO2Me
H3C CH3
CH2CO2Me
H3C CH3
Na, NH3(L) H3C
CH3 H3C
OH O
CH3
第三章 还原反应
4.镁:镁与甲醇的混合物可选择性还原α. β-不饱和酯,酰
胺和腈。镁和NH4Cl的混合物可还原酮:
不需加压。
NO2
NH2NH2
NH2
NO2
Pd - C
NH2NH2
NH2
CN Rancy-Ni 98%
CN
H C CH CO2H
NH2NH2
Rancy-Ni 85%
H2 CH2 C CO2H
第三章 还原反应
3.三价磷化合物:
三价磷化合物,Ph3P, (C2H5O)3P 常用于脱氧及脱硫反应:
HH Ph C C COOC2H5
收率高。
OH
OH
NO2 Na2S2O4-OH-
NH2
Cl
Cl
第三章 还原反应
NN OH
SO3H Na2S2O4-OH-
NH2 NH2 OH
2. 肼:
C O NH2NH2
OHC N NH2
CH3 OH
NH2NH2 KOH
CH3 OH
98% CHO
CH3
CH2
SO3H
N2
第三章 还原反应
在Pd-C、或Raney-Ni等催化下,肼的还原更快、
第三章 还原反应
TiCl3可把α,β-不饱和酮的碳碳双键还原:
O CH3-C-CH=CH-CO2C2H5
《有机合成方法》PPT课件

所有的起始原料确定后,再设计全合成路
线。在实施合成时,可以采用逐步合成法或
片段组合法进行合成。
(3)计算机辅助有机合成路线设计
a. 化学信息学和化学信息数据库
与有机合成有关常用数据库: * 现有化学品数据库 * 有机化学反应数据库 * 合成方法和转化数据库 * 合成方法参考文献库 * 保护基团数据库 * 杂环合成数据库
相合成所应用的活化单体。
DMT
OCH 2 O B
H H
O
CH3O P
H H
H
+
C H(C H3)2
NH
C H(C H3)2
Protonated phosphoramidite
氯甲基酮衍生物:
R-COCH2Cl 是良好的烷基化活性中间体,
容易与氨基和巯基等发生烷基化反应。
O
R 1
+
RC C H 2 C l R 2
HH
H
H
OH OH
* 在温和条件下, 仅有极少量的第二醇羟基或碱 基上的氨基与单甲氧基三苯甲基氯作用。 * 用 80% 的乙酸或吡啶-乙酸处理, 即可以除去 这类保护基。
取代的γ-酮酰基 (γ-keto acyl) 保护醇羟基: * 在中性条件下, 用水合肼处理可以方便地除去。
O RC
O
(CH2)2 C OCH2 O Base
a. 氨基保护
O H2 Ph C O C Cl
benzylchloroformate base
+
H2N
H C
CO-O
R
amino acid
O H2 Ph C O C
H HN C
CO-O
R
CBz-amino acid
有机合成培训讲义(第一讲)

对有机合成工作者的基本要求
新试剂、新反应、新方法和新技术的应用使有 新试剂、新反应、新方法和新技术的应用使有 机合成路线更简捷、更有效、更绿色化。 机合成路线更简捷、更有效、更绿色化。 不断学习、掌握、开发和运用有机合成新试剂、 不断学习、掌握、开发和运用有机合成新试剂、 学习 有机合成新试剂 新反应、 新反应、新方法和新技术是对每个有机合成工 作者的基本要求。 作者的基本要求。 在实验过程中必须具备分析判断和应变能力。 在实验过程中必须具备分析判断和应变能力。 分析判断和应变能力
Ha He O CH3
H+
CH3
反应过程规律性研究注意点: 反应过程规律性研究注意点:
抓关键影响因素 抓主要矛盾 遇到矛盾的影响因素要找其平衡点 注意观察反应现象, 注意观察反应现象,认真思考 勤于监控
反应实例 : 烯烃与臭氧加成反应
OH CH3 (CH3)2SO4
NaOH/Benzene
OCH3 CH3
OCH3
NBS / CCl4 U. V. Light
Br OCH3
1) 2)
OH
OCH3
O
O Br
3) NaOH
OCH3
O CH3 1)CF3COOH
2)(CH3)3SiH
OCH3
O CH3
O3 / (CH3O)3P
OCH3
O CH3
OCH3
H OCH3 O
OCH3
烯烃与臭氧加成反应进程
OCH3 OCH3 O CH3 OCH3 O3 H3CO HC O O O C H H O CH3 (CH3O)3P H H3CO O OCH3 O CH3
合成研发是一项系统性、 合成研发是一项系统性、 逻辑性很强的实践活动
有机合成课件5章(金属有机化合物)

H2O C2H5OH (CH3)2CO (CH3)2SO
16 28 20 23
第五章 金属有机化合物
3)金属盐与金属有机化合物的反应
M'X+R-M RM'+MX R2Cd+MgCl2 RCu RLi R2CuLi
如:
CdCl2+RMgX CuI+RLi
4)金属或非金属的化合物与烯烃等不饱和键的加成: 二异丁基铝氢与炔的加成: R
1,2
C
C C C O R' 1,4 RMgX
C C OMgX R'
C C C OMgX R R'
第五章 金属有机化合物
这两种加成是互相竞争的,究竟是哪一种占优势呢?要由R1 和R的相对空间体积大小决定。如:
O Ph C C H H
O Ph C C H H
H + PhMgBr 1,2
CH3 CH CH3
CH3 H3C C CH CH Ph H K CH2Ph
第五章 金属有机化合物
Ph2C CH3SOCH2Na Ph C H2 C CH2SOCH3 CH2 2 Na
因此,一般反应不选择烯烃和炔烃作溶剂。 3,有机锂: 一般为烷烃的溶液,反应溶剂可选择醚,THF等。试验证明,
乙醚中室温保存不久,会分解乙醚。它比RMgX稳定性差。制
OCH3
CO2C2H5
O C-CH3 THF + BrCH2CO2C2H5 + Zn reflux CO2H O H3C CH2CO2C2H5 O
第五章 金属有机化合物
O C CH3 + BrCH2CO2C2H5 + Zn THF reflux CO2C2H5 H3C CH2CO2C2H5 O O
《有机合成》课件 (共48张PPT)

精选版课件ppt
28
例1
CH3 C CH2 CH3
CH2 C COOH CH3
精选版课件ppt
29
Br Br
CH3 C CH2 CH3 C CH2
CH3
CH3
OH OH CH3 C CH2
CH3
OH O CH3 C C H
CH3
精选版课件ppt
CH2
C COOH CH3 30
副产物
副产物
基础原 料
CHOH
精选版课件ppt
21
用化学方法人工合成物质
HO
O O
HO
HO
OH
精选版课件ppt
22
叶绿 素分 子的 结构
式
精选版课件ppt
23
维 生 素
B12 的 化 学 结 构
精选版课件ppt
24
用化学方法人工合成物质
• 修饰 • 自然 • 物质
解热镇痛药物——精选阿版司课件匹ppt林
25
CH3
2.醛.酮加氢气
催化剂
CH3CH=O+H2 Δ
CH3CH2OH
催化剂
(CH3)2C=O+H2 Δ (CH3)2CHOH
3.卤代烃水解
CH3CH2Cl
+H2O
NaOH
△
CH3CH2OH
H2SO4
4.酯的水解 CH3COOCH2CH3+H2O Δ 精选版课C件pHpt 3COOH+CH3CH2O7 H
-X的引入
8
-C=C-或-C=O的引入 官能团
引入
1.醇与卤代烃的消去反应
1)某些醇的消去引入C=C
CH3CH2OH
人教版化学《有机合成》精美课件

13
人 教 版 选 修 五有机 化学第 三章-第 四节有 机合成 56张
• 2、通过加成(加H)或氧化(加O)消除醛基
催化剂
H3CHC=O+H2 Δ
CH3CH2OH
催化剂
2CH3CHO+O2 Δ 2CH3COOH
• 3、通过消去或氧化或酯化等消去羟基
浓硫酸△
CH3CH2OH
CH2=CH2+H2O
Cu △
5
思考与交流
(一)常见引入官能团的方法
1、怎样在有机化合物中引入碳碳双键?
(1)炔烃与氢气 1:1 加成
(2)卤代烃的消去 (3)醇的消去
三种方法
2、怎样在有机化合物中引入羟基?
(1)烯烃与水加成 (2)卤代烃水解
(3)醛/酮加氢 (4)酯的水解
四种方法
6
人 教 版 选 修 五有机 化学第 三章-第 四节有 机合成 56张
2CH3CH2OH+O2
2CH3CHO+2H2O
浓硫酸△
CH3OH+HCOOH HCOOCH3+H2O
人 教 版 选 修 五有机 化学第 三章-第 四节有 机合成 56张
14
人 教 版 选 修 五有机 化学第 三章-第 四节有 机合成 56张
【思考与交流】
【例1】以BrCH2-CH=CH-CH2Br为原料合成药物 CH3OOC-CH=CH-COOCH3的路线为:
官能团的性质
类别
醇
酚 醛 羧酸 酯
官能团 通式
代表物
主要化学性质
—OH
—OH —CHO —COOH —COO—
R—OH CnH2n+2O
CnH2n-6O R—CHO CnH2nO R—COOH CnH2nO2 RCOOR` CnH2nO2
有机合成基本反应ppt课件
反应机理
反应实例
反应实例
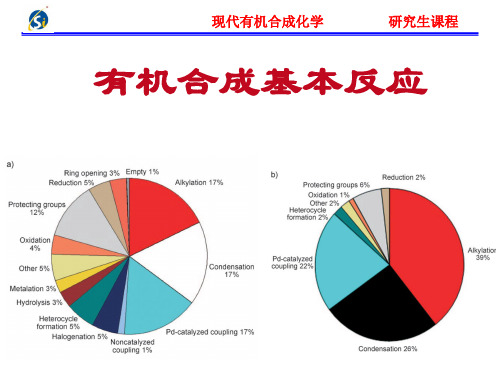
Mannich 反应 含有a-活泼氢的醛、酮与甲醛及胺(伯胺、仲胺或
氨)反应,结果一个a-活泼氢被胺甲基取代,此反应 又称为胺甲基化反应,所得产物称为Mannich碱。
Mannich 反应机理
反应实例
(二)、碳碳双键的形成
• 消除反应 Wittig反应 • (1)卤代烃脱卤化氢
反应实例
Knoevenagel 反应
• 含活泼亚甲基的化合物与 醛或酮在弱碱性催化剂(氨、 伯胺、仲胺、吡啶等有机 碱)存在下缩合得到a,b-不 饱和化合物。
反应实例:
(三)、碳碳叁键的形成
• 二卤代烃脱卤化氢
(四)、碳环的形成
• 环加成反应
Diels—Aider反应
卡宾及卡宾类对烯键的加成
与卤代烃反应:
有机铜化合物的 反应
现代有机合成化学
研究生课程
有机铜化合物的反应
与酰氯作用
现代有机合成化学
研究生课程
与环氧化合物反应
现代有机合成化学
研究生课程
5、活泼亚甲基化合物的反应
• 活泼亚甲基化合物由于吸电子基的吸电子诱导效应,使得 2-碳上的氢具有一定的酸性.可以解离而生成碳负离子,
这类碳负离子通常称为烯醇负离子,此碳负离子因离域而 稳定。下面是一些常见的活泼亚甲基化合物:
研究生课程
催化剂主要为金属卤化物,它们的催化活性大致如下:
现代有机合成化学
研究生课程
原子不同反应活性次序为:
现代有机合成化学
研究生课程
现代有机合成化学
研究生课程
(2) Friedel—Crafts反应酰基化反应
酰基化反应是不可逆的, 也不发生重排,因此酰 基化反应在合成上很有 价值。
反应实例
反应实例
Mannich 反应 含有a-活泼氢的醛、酮与甲醛及胺(伯胺、仲胺或
氨)反应,结果一个a-活泼氢被胺甲基取代,此反应 又称为胺甲基化反应,所得产物称为Mannich碱。
Mannich 反应机理
反应实例
(二)、碳碳双键的形成
• 消除反应 Wittig反应 • (1)卤代烃脱卤化氢
反应实例
Knoevenagel 反应
• 含活泼亚甲基的化合物与 醛或酮在弱碱性催化剂(氨、 伯胺、仲胺、吡啶等有机 碱)存在下缩合得到a,b-不 饱和化合物。
反应实例:
(三)、碳碳叁键的形成
• 二卤代烃脱卤化氢
(四)、碳环的形成
• 环加成反应
Diels—Aider反应
卡宾及卡宾类对烯键的加成
与卤代烃反应:
有机铜化合物的 反应
现代有机合成化学
研究生课程
有机铜化合物的反应
与酰氯作用
现代有机合成化学
研究生课程
与环氧化合物反应
现代有机合成化学
研究生课程
5、活泼亚甲基化合物的反应
• 活泼亚甲基化合物由于吸电子基的吸电子诱导效应,使得 2-碳上的氢具有一定的酸性.可以解离而生成碳负离子,
这类碳负离子通常称为烯醇负离子,此碳负离子因离域而 稳定。下面是一些常见的活泼亚甲基化合物:
研究生课程
催化剂主要为金属卤化物,它们的催化活性大致如下:
现代有机合成化学
研究生课程
原子不同反应活性次序为:
现代有机合成化学
研究生课程
现代有机合成化学
研究生课程
(2) Friedel—Crafts反应酰基化反应
酰基化反应是不可逆的, 也不发生重排,因此酰 基化反应在合成上很有 价值。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
h
22
碳-杂键的形成
碳氧键的形成 碳硫键的形成 碳氮键的形成
h
23
碳氧键的形成
1.卤代烃与醇钠、酚钠反应 2.硫酸酯或磺酸酯与醇钠、酚钠反应 3.卤代烃与羧酸盐反应 4.醇、酸与环氧化合物加成 5.醇、酚分子间脱水 6.醇与烯烃、炔烃加成 7.酸与烯烃、炔烃加成 8.汞化反应
h
24
碳硫键的形成
h
5
α,β-不饱和酮(或酯)的烷基化
类似酮、腈、酯的烷基化
h
6
Michael反应
活泼亚甲基化合物的碳负离子对α,β-不饱和
羰基化合物亲核的1,4-加成反应。
h
7
Wittig反应
Wittig试剂能发生多种有机反应,是有机合成的 重要中间体,广泛用于碳碳双键的形成。
h
8
炔烃的烷基化 利用炔烃与烷基化试剂反应形成新的碳碳键
芳环上的亲电取代反应。
h
17
Friedel-Crafts烷基化反应
MeO MeO
MeSO3H HO NHCOCF3
CH2Cl2
S
M eO M eO
烷基化反应
h
19
Friedel-Crafts烷基化反应
SnCl4
CH2Cl2
OH
O
h
20
Friedel-Crafts酰基化反应
1. Friedel-Crafts烷基化反应 2. Friedel-Crafts酰基化反应 3. Vilsmeier 反应
h
16
Friedel-Crafts烷基化反应
苯环H被烷基取代。
芳烃的烷基化: 烷基化试剂: 卤代烃、烯烃、醇、环氧乙烷、醛、酮等 常用催化剂: 无机酸(如H2SO4 、HCl等)和Lewis酸 (如无水AICl3、FeCl3、BF3、ZnCl2 等)
h
3
活泼亚甲基化合物的烷基化
活泼亚甲基化合物 硝基甲烷 丙二酸酯 乙酰乙酸乙酯 β-二酮 烷基化试剂 卤代烃 磺酸酯 环氧化合物
h
4
酮、腈和酯的烷基化
酮和腈分子中的α-氢酸性比较弱,必须用碱性
比乙醇钠强的碱,使酮和腈差不多全部变成烯醇 盐,可得到较高产率的烃化产物。如氨基钠、氨 基钾、氢化钠、三苯甲基钠、二异丙基胺基锂 (LDA)等。
h
55
h
56
h
57
思考题
h
58
合成子
h
59
h
60
h
61
h
62
h
63
h
64
h
65
h
66
h
67
h
68
h
69
h
70
有机合成中功能团的转化
h
71
复杂化合物的合成
h
72
h
73
h
74
h
75
h
76
h
77
h
78
h
79
h
80
h
81
h
82
h
83
h
84
h
85
h
1.硫化物的烃化 2.硫醇与醛酮的加成 3.亚硫酸氢钠与醛酮的加成 4.芳烃的磺化
h
25
碳氮键的形成
1.氨或胺的酰化 2.卤代烃的氨解 3.酰胺的N-烃化 4.芳烃的硝化
h
26
功能团的转换
h
27
功能团的转换
h
28
功能团的转换
炔烃的偶联反应:
CuCl , NH4Cl , O2
HO
OH
HO
OH
h
h
13
有机锂试剂的反应
有机锂试剂基本上与格氏试剂相同 但是有机锂试剂常常由于碱性强, 会引起消去反应
h
14
有机铜锂试剂的反应
有机铜锂试剂能与多种类型的卤代烃及磺酸酯 反应,获得高产率的取代产物。还可以与不饱和 羰基化合物进行Michael加成,生成新的碳碳键。
h
15
Friedel-Crafts反应
h
12
格氏试剂的反应
格氏试剂是亲核试剂,它可以与醛、酮、羧酸衍生物、二氧化碳 进行亲核加成反应,可以与环氧烷、卤代烃进行亲核取代或偶合 反应。
格氏试剂 + 甲醛: 伯醇 格氏试剂 + 其它醛:仲醇 格氏试剂 + 酮: 叔醇 格氏试剂 + 甲酸酯:仲醇 格氏试剂 + 其它酯:叔醇 格氏试剂 + 碳酸酯:叔醇 格氏试剂 + 酰卤: 酮、叔醇 格氏试剂 + 腈: 酮 格氏试剂 + 二氧化碳: 羧酸 格氏试剂 + 环氧乙烷: 碳链增长2个碳原子的伯醇 格氏试剂 + 活泼的卤代烃:偶合成烃
29
功能团的转换
h
30
功能团的转换
h
31
功能团的转换
h
32
功能团的转换
h
33
功能团的转换
h
34
功能团的转换
h
35
h
36
合成相关的反应
h
37
逆合成分析
h
38
h
39
h
40
h
41
h
42
h
43
h
44
h
45
h
46
h
47
h
48
h
49
h
50
h
51
h
52
h
53
h
54
芳烃及其衍生物通过酰化反应可以制得 酮、醛、羧酸、胺等化合物,但主要用 于酮和醛的合成。
常用酰基化试剂:酰卤、酸酐。
h
21
Vilsmeier反应
OH
+ HCON ( CH3 )2 + POCl3
OH CHO
Vilsmeier反应主要用于苯环上有强的活化基: -OH , -N(CH3)2 , -OR
86
h
87
h
88
有机合成
h
1
碳-碳键的生成
烃化反应 羰基化合物的缩合反应 有机金属试剂的反应 Friedel-Crafts反应
h
2
烷基化反应
1. 活泼亚甲基化合物的烷基化 2. 酮、腈和酯的烷基化
3. α,β-不饱和酮(或酯)的烷基化
4. Michael反应 5. Wittig反应 6. 炔烃的烷基化 7. 烯胺的反应
h
9
烯胺的反应
利用烯胺对羰基邻位碳的活化进行烷基化 Stork 烯胺合成法
h
10
羰基化合物的缩合反应
1. 羟醛缩合反应 2. 酯缩合反应 3. Knoevenagel反应 4. Darzen缩合 5. Mannich反应 6. Perkin反应
h
11
有机金属试剂的反应
格氏试剂 有机锂试剂 有机铜锂试剂 有机锌试剂
