有机化学(四)
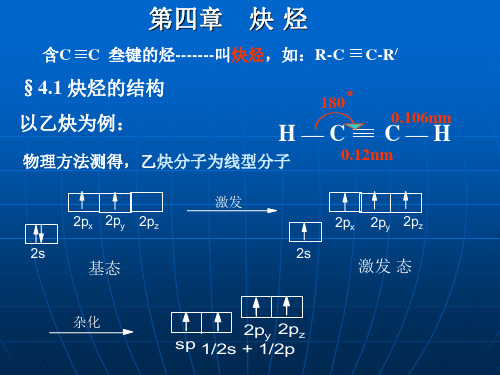
有机化学 第四章 炔烃
R-C
C-Na + NH3↑
R-C≡C-Na + R/X R/X/
6、聚合反应
Cu2Cl2 2 CH CH NH Cl H2O CH2 CH 4
CH CH CH2 CH Cu2Cl2 NH 4Cl H 2O
C CH
C
C CH CH2
增碳
例: 以乙炔为原料合成下列化合物: (1)Z-3-己烯; (3)醋酸乙烯脂; (2)E-3-己烯;
2) 和卤化氢加成
RC
注:
CH
HX
HgCl2
R
C X
CH2 HX
HgCl2
R
X C X
CH3
① 反应可以停留在卤代烯烃阶段; ② 在催化剂汞盐或铜盐存在时,叁键与HX反应 活性比双键大; ③ 不对称炔烃与HX加成符合马氏规则,对于HBr 有过氧化物效应。
3) 和水加成
RC CH + H2O
HgSO4 H 2SO4 ) (稀
5 4 3 2 1
CH3-CH = CH-C
CH
3-戊烯-1-炔
(不叫 2-戊烯-4-炔)
如对称,优先考虑双键。
HC CCHCH=CH 2 CH 3
6 5 4 3 2 1
3-甲基-1-戊烯-4-炔
HC C-CH2-CH2-CH=CH2
1-己烯-5-炔
§4.3 物理性质(自学) §4.4 化学性质 1、氢化反应 1)催化氢化
RC CR' + H2
催化加氢反应活性:炔烃>烯烃
Ni(Pt , Pd)
RCH
CHR'
Ni(Pt, Pd)
H2
RCH2CH2R'
RC
有机化学-4炔烃

CH3C CCHCH2CH CH2 C2H5 4- 乙基 -1-庚烯 -5-炔
HC C CH CH2 CH3C CCHCH2CH CHCH3 CH CH2
1-丁烯 -3- 炔 5- 乙烯基 -2- 辛烯 -6- 炔
二、炔烃的物理性质
û ³ Ã Æ Ò È ² û È ± ² 1-¶ ¡ È ² 1-Î ì È ² 2-Î ì È ² 3-¼ ³ù » -1-¶ ¡ È ² 1-¼ º È ² 1-· ý È ² 1-Ê ® ° Ë Ì ¼ È ² È µ Û ã / C -81.8 -101.5 -122.5 -98 -101 -124 -80.9 22.5 ²µ Ð ã /C -83.4 -23.3 8.5 39.7 55.5 28(10kPa) 71.4 99.8 180(2kPa) ´ ¶ Ï Ô Ü Ã ¶ È (d20 4 ) 0.618 0.671 0.668 0.695 0.713 0.685 0.719 0.733 0.870
AgNO3
(六)聚合
练习: 1、下列烯烃存在顺反异构的是——
A CH2=C(CH3)2 C CH3CH=CHCH3 2、下列化合物发生亲电加成反应的活性最小的是(
A CH2=CH2 C CH2=C(CH3)2 B CH2=CH2-CH3 D CH2=CHNO2
B CH2=CHCH2CH3 )
3、下列碳正离子最稳定的是( A
乙酸乙烯酯
(四)氧化反应
在强烈条件下氧化时,非端位炔烃生成羧酸(盐),端位炔烃生成羧酸(盐)、 二氧化碳和水。
KMnO4 _COOH + CO +H2O C4H9 C CH 2 C H 4 9 H2O ,OH
炔烃用高锰酸钾氧化,可用于炔烃的定性分析,也可用于推测三 键的位置。
有机化学-4-环烃

多环烃
桥环烃:
二、脂环烃的命名
1、 单环脂环烃
(1)根据分子中成环碳原子数目称为“环某烷”;
(2)使取代基的位次尽可能最小(小基团位次最低); (3)环烯(或炔)烃编号时,双(三)键位次最小。
1,3-二甲基环戊烷
1-甲基-3-异丙基环己烷 1,3-二甲基环己烯
(4)对复杂的化合物,可把环看为取代基。
H H H H H H 1
4
6 5 3
H
5 4
2 1
H
H H H
3
6
2
H
5%
95%
(2) 多元取代环己烷中,e键多者为优势构象。
(3) 环上有不同取代基时,最大取代基处于e键上的构象最 稳定。
练习:写出1,2-二甲基取代环己烷的构象式,并排列其稳定性次序:
CH3 CH3
顺式 CH3
CH3 CH3 反式 CH3 CH3 CH3 (Ⅱ) CH3 (Ⅲ)
单环芳烃
H3C CH3
CH3
芳烃 多环芳烃
联苯
多苯代脂烃
CH2
稠环芳烃
2、 芳烃的命名
1) 烃基取代的苯 ①一元取代苯,以苯为母体,烷基为取代基,省略“基”字
甲苯
乙苯
异丙苯
②二元取代苯,可用邻、间、对来表明取代基位置:
CH3 CH3
CH3
H3C
CH3
CH3
邻二甲苯 1,2-二甲苯 O-
间二甲苯 1,3-二甲苯 m-
张力,它的能量比椅型高 30 kJ∙mol-1。
183pm 船 式 H 4 构 H 象
H H H
5 H 3 6
H
H H H
2
1
H H
有机化学题库(4)

第六章 芳烃(习题)一、命名下列化合物1.NO 2COOHBr;2.CHO;3.Br OCH 3;4.NH 2SO 3H ; 5.CH CH 2Br6.NO 2CH 3SO 3H; 7.NH 2COOH; 8.NO 2NH 2Cl; 9.ClC 2H 5CH 3; 10.COOHCl11.NO 2ClCH 3; 12. NO 2BrCl; 13.BrCl ; 14.CH(CH 3)2C 2H 5二、由名称写出结构式1.3,5-二溴-2-硝基甲苯; 2.2-硝基-3-甲氧基甲苯; 3.β-萘磺酸 4.环己烯基苯; 5.间氟苯乙烯;6.邻氨基苯甲酸; 7.3-苯基戊烷; 8.4,4’-二硝基联苯; 9.3-氯-2-萘甲酸; 10.4-氯-2,3-二硝基甲苯 11.2-氯-6-溴苯胺; 12.间氯苯乙烯;13.3-羟基-5-碘苯乙酸 14.4-硝基-2,4’-二氯联苯。
三、完成下列反应式 1.KMnO 4C 2H 5H 3C2.+(CH 3)3C CH 3CH 3AlCl 33.H 2SO 4ClKMnO 4H 3CHNO 3 4.Br 2Cl 2hvH 3CFe5.H 2SO 4+60℃6.CH 2ClCH 3AlCl 3+CO Zn-Hg 浓HCl7.+COOHOHCH 3CH 3HNO 3(2 mol)8.24NO 2NH HNO 3CO9.24△KMnO 4BrC 2H 5HNO 310.△KMnO 4(CH 3)3C11.H 2SO 4HNO 3COO12.Br 2OCH 3COCH 3O13.AlCl 3+14.H 2SO 4CH 2HNO 3O 2 N15.CH 2ClCH 2AlCl 3CO16.CH 2CH 2(CH 3)2C HF17.NO 2Cl 2OCH 3Fe18.H 2SO 4NO 2CH 3OHNO 319.H 2SO 4ClNHCOCH3HNO 320.O 221.H 2SO 4H +KMnO 4HNO 3,22.CH 2ClCH 3AlCl 3+CO C O23.AlCl 3CH 2CH 2CH 2Cl24.+ CH 3CH 2CH 2CH 2ClAlCl 3100CKMnO 425.CH 2COCl326.+CH 2KMnO 4CH 2AlCl 3四、回答问题1.判断下列各化合物或离子中具有芳香性的是( )。
有机化学第四篇芳香烃
第四章芳香烃芳烃,也叫芳香烃,一般是指分子中含苯环结构的碳氢化合物。
现代芳烃的概念是指具有芳香性的一类环状化合物,它们不必然具有香味,也不必然含有苯环结构。
分类:芳香烃按照分子中是不是含有苯环,可分为苯系芳烃和非苯系芳烃。
苯系芳烃按所含苯环的数量和结合方式分为单环芳烃、稠环芳烃和多环芳烃。
1.单环芳烃:指分子中仅含一个苯环的芳烃,包括苯、苯的同系物和苯基取代的不饱和烃。
例如:CH3CH2CH3CH=CH2苯甲苯乙苯苯乙烯2.多环芳烃:指分子中含两个或两个以上苯环的芳烃,多环芳烃按照分子中苯环的连接方式不同分为多苯代脂肪烃,联苯烃和稠环芳烃(1)多苯代脂肪烃:能够看做脂肪烃分子中两个或两个以上氢原子被苯基取代的化合物。
CH2HC CH二苯甲烷1,2-二苯乙烯(1)联苯烃:指两个或两个以上苯环别离以单键相连而成的多环芳烃例如:联苯1,4-三联苯(2)稠环芳烃:两个或两个以上苯环彼此共用两个碳原子而成的多环芳烃,例如:萘蒽菲3.非苯芳烃:指分子中不含苯环的芳香烃,例如:环戊二烯负离子环庚三烯正离子第一节单环芳烃一,单环芳烃的异构现象和命名苯是最简单的单环芳烃。
单环芳烃包括苯、苯的同系物和苯基取代的不饱和烃。
1.异构现象(1)烃基苯有烃基的异构例如:CH2CH2CH3CHCH3CH3(2)二烃基苯有三种位置异构例如:RR'RRR'R'(3)三取代苯有三种位置异构例如: R R'RRR''R''R''R'R'2. 命名(1)苯基的概念芳烃分子去掉一个氢原子所剩下的基团称为芳基(Aryl)用Ar 表示。
重要的芳基有:CH 2(C 6H 5CH 2-)苄基(苯甲基),用Bz 表示苯基, 用Ph 或 表示ф(2)一元取代苯的命名a 当苯环上连的是烷基(R-),-NO 2,-X 等基团时,则以苯环为母体,叫做某基苯。
例如:CH CH 33NO 2Cl异丙基苯叔丁基苯硝基苯氯苯b 当苯环上连有-COOH ,-SO 3H ,-NH 2,-OH ,-CHO ,-CH=CH 2或R 较复杂时,则把苯环作为取代基。
有机化学(第四版)4
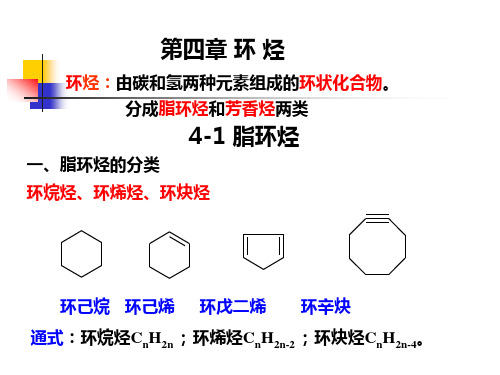
H 3C H
CH3 H
顺-1,2-二甲基环已烷(a e型)
H
H 3C H
CH 3
反-1,2-二甲基环已烷(e e型)
HH
H CH3
CH3 CH3
CH3 H
三、环烷烃的性质 1.物理性质
环烷烃的熔点、沸点和密度都比同碳数的烷烃高。 2.化学性质
一般与烷烃相似,但由于“张力”的存在,小环化合物 (三、四元环)具有一些特殊性质, 易开环。
3.环烷烃的结构
• 稳定性:
<
<
<
• 环丙烷的结构:
• 弯曲键:电子云没有呈轨道轴对称,而是分布在一条曲线上。 • 张力: 角张力:键角偏离正常键角而引起的张力。
• 环丁烷的结构:
蝴蝶式
• 环戊烷的结构:
信封式
• 环己烷的结构:存在两种主要构象。
椅型 船型
56
1
4
3
2
直立键或a键
平伏键或e键
支链化合物比较稳定
(2) 加卤素和加卤化氢
Br2 室温
CH2
CH2
CH2
Br
Br
Br2 加热
CH2 CH2 CH2 CH2
Br
Br
HBr 室温 CH3 CH2 CH2
Br
CH3 CH CH3 HBr C
H2C
CH3
CH3 CH3 CH3 CH C CH3
Br
• 含氢最多的碳原子与含氢最少的碳原子之间断裂; • 氢加在含氢最多的碳原子上。(类似双键加成的马氏规则)
2、苯结构的近代概念
杂化轨道理论:碳sp2杂化,形成6个C-C s-键、6个C-H s-
键。
键。6个p 轨道相互交盖,形成一个“环闭”大p
有机化学4第四章芳香烃

(1)、闭合离域体系
(2)、具有平面结构或接近平 面
(3)、参与共轭的π电子数符合 4n+2
轮烯
[8]轮 烯
HH
[10]轮 烯
HHHH
[14]轮 烯
[18]轮 烯
盆形
不共平面
π电子数8 不符合4n+2
π电子数10 符合4n+2
无芳香性 无芳香性
不共平面
π电子数12 不符合4n+2
无芳香性
共平面
π电子数18 符合4n+2
COCH3
HO
COOH
COOH NH2
HO
CH3CH2CCH2CHCHO O Cl
3-丁烯-2-醇 4-氧代-2-氯乙醛
4-羟基环己烷甲酸
4-羟基-3-甲氧基苯甲醛 2-氨基-5-羟基苯甲酸
3-硝基-4-羟基苯乙酮
官能团的优先顺序 见教材P93
1
α
891
7
2β
6
3
5
10
5
4
α
SO3H
2β
萘 1,5-二甲基萘 2-萘磺酸 或 β-萘磺酸
―O-, ―NH2,―NR2, ―OH(强烈活化) > ―OR,―OCOCH3, ―NHCOCH3(中等活化) > ―R, ―C6H5 >(弱活化) ― F, ―Cl, ―Br, ―I(弱钝化)
2、第二类定位基(间位定位基)
-N+R3, -NO2,-CN, -SO3H, -CF3,-CHO,COCH3,-COOH,-COOCH3, -CONH2(强烈钝化)
Cl
H
Cl
Cl
E
O
δδ
N
有机化学 第四章课后题答案分析

P46 参考1,3-丁二烯的加成反应
P37
烯烃与硫酸加成反应
P72 一元取代萘在进行亲电取代反应时,第二个基团进入环的 位置同样取决于原有基团的性质。 I. 如果环上有一个邻对位定位基时,由于邻对位定位基的致活 作用,所以取代发生在同环。如果第一定位基团在 1 位,那么 第二定位集团优先进入4位;如果第一定位基团在2位,则第二 基团优先进入1位。 II. 如果一个环上有一个间位定位基时,由于间位定位基的致钝 作用,亲代反应主要发生在环的5或8位。
第四章 课后作业
4.7 答案
取代和加成反应的区别 1.烯烃的加成反应。活性次序为 F2>Cl2>Br2>I2.课本P34烯烃与溴的加成, 反应条件是溴的四氯化碳溶液中。由此 类推,如果是烯烃与氯加成,那么反应 条件应该更加简单。
CCl4
不用写上HBr.在有机化 学中大多用箭头,可逆 反应则用可逆符号。而 且多数反应复杂,方程 式不配平,只写出主要 产物即可 2.α-H的取代反应。P40 C=C与卤素的加成一般是按离子(亲 电加成)历程进行的反应,在常温 下,不需要光照即可进行,而烷烃 的卤代反应是按游离基历程(自由 基),需要高温或光照才能进行。 所以烯烃的α-H卤代反应必须在用Br2/CCl4溶液, 后用银氨溶液也 可以。
不能用溴水。原因:环丙烷可以 和溴室温条件下发生开环加成反 应,与高锰酸钾一般不反应P56。
P72 一元取代萘在进行亲电取代反应时,第二个基团进入环的位置同样取决于原有 基团的性质。 I. 如果环上有一个邻对位定位基时,由于邻对位定位基的致活作用,所以取代发生 在同环。如果第一定位基团在1位,那么第二定位集团优先进入4位;如果第一定位 基团在2位,则第二基团优先进入1位。 II. 如果一个环上有一个间位定位基时,由于间位定位基的致钝作用,亲代反应主
有机化学 第四章 立体异构

(二)、旋光仪和比旋光度
Nicol棱镜
旋光仪的工作原理
WXG-4圆盘旋光仪
t: 比旋光度 [ α ]λ
测定温度
比旋光度
[α] t λ=
波长
α
旋光度(旋光仪上的读数)
l × ρ
溶液的浓度(g/ml) 盛液管长度(dm)
质量浓度ρB = 1g/ml的旋光物质溶液,放在l = 1dm长的盛液管中测得的旋光度为这个物质的比
CHO H OH CH2OH COOH [O] HgO H OH CH2OH
D-(+)-甘油醛
D-(-)-甘油酸
If the —OH or —NH2 which attaches to the
chiral carbon atom lies on the right,the
molecule is called ―D‖;if on the left,i H H Cl F H
有对称中心的分子能和它的镜像重合,没有手性
一般来讲,一种分子不能重叠镜像的条件是这 种分子没有对称面,也没有对称中心。
Plane of Symmetry
对映异构体
对映体的物理性质和化学性质一般 都相同,比旋光度的数值相等,但旋光 方向相反;等量对映体的混合物称为外 消旋体(Racemate) ,用dl或(± ) 表示。 Racemic Mixtures
手性分子
Amino acid possesses a carbon with four different attached groups (R, NH2, H, COOH); there is no such carbon in propanoic acid.
大学有机化学 第7章 旋光异构(IV)

尽管手性碳和分子手性没有
必然的关系,但它们有密切的联
系。在大多数情况下,手性分子 中往往存在手性碳原子,而且含
有手性碳的分子肯定有旋光异构
体。
旋光异构
一、物质的旋光性 二、物质的旋光性与分子结构的关系 三、含一个手性碳原子化合物的旋光异构
四、含两个手性碳原子化合物的旋光异构
五、不含手性碳原子化合物的旋光异构 六、环状化合物的立体异构 七、反应中的立体化学
1. 对称面
假设分子中有一平面能把分子切成相
互对称的两半,该平面就是分子的对称面。
具有对称面的分子与其镜像能够重合, 因而无手性,无旋光性,也无旋光异构体 (含手性碳的例外)。
分子的对称面 具有对称面的分子为非手性分子
2. 对称中心:
若分子中有一点 P,通过 P 点画任何直
线,如果在此直线上的P 点两侧,距离 P 点
47
CHO OH H CH2OH
D-(+)-甘油醛 COOH OH H CH3 D-(-)-乳酸
CHO H HO CH2OH L-(-)-甘油醛 COOH H HO CH3 L-(+)-乳酸
规则:在用 DL 表示的 Fischer 投影式中, C* 上羟基像甘 油醛那样处于右侧为D-构型;处于左侧为L-构型。
方法是将这个分子本身以及它的镜像都作成模型,
再来比较实物和镜像是否能完全重合。若不能完
全重合,则该分子有手性,存在对映异构体。 但往往比较麻烦。
物质分子是否有手性(即能否与其 镜象完全重叠),可从分子中有无对称 因素(symmetry of elements)来判断,最常见 的分子对称因素有对称面和对称中心。
三、含一个手性碳化合物的旋光异构
(一)对映体和外消旋体 (二)旋光异构体构型的表示方法 (三)构型的标记和命名 1. D/L相对构型标示法 2. R/S 绝对构型标示法:
有机化学试卷及答案(四)

A、A与G B、A与T C、C与U D、T与U
22、体型结构的塑料具有下列性质:
A、可塑性B、粘流性C、高弹性D、脆性大
23、下列化合物:①、②、③、④
碱性由强到弱的顺序是:
A.①>②>③>④B.②>①>④>③
C.③>④>①>②D.①>③>②>④
24、缩聚反应中单体比例不等于1∶1时,会造成:
七、合成题(每小题5分,共20分)
39、用丙二酸二乙酯和其它必要的试剂合成
40、
41、用合成
42、以甲苯及其它必要的试剂为原料,合
①
序号
XXXX学年第 2 学期考核试卷
课号:EK1G03A 课程名称:有机化学A 试卷编号:A
班级:学号:姓名:
阅卷教师:成绩:
大题号
一
二
三
四
五
六
总分
得分
一.命名下列各化合物或写出结构式(每题1分,共10分)
(5)
(6)
(7)
六、推导题(共5小题,每题6分,任选4题,共24分)
1、A、B两化合物的分子式都是C6H12,A经臭氧氧化并与锌和酸反应后得到乙醛和甲乙酮,B经高锰酸钾氧化只得丙酸,写出A和B的结构式,并写出相关反应方程式。
2、某醇依次与下列试剂相继反应(1)HBr;(2)KOH(醇溶液);(3)H2O(H2SO4催化);(4)K2Cr2O7+H2SO4,最后产物为2-戊酮,试推测原来醇的结构,并写出各步反应式。
六、合成题(每小题5分,共20分)
39、用丙二酸二乙酯和其它必要的试剂合成
40、用邻苯二甲酰亚胺钾和其他必要的试剂合成甘氨酸(H2NCH2COOH)。
初级工-有机化学基础知识(四)

Br
100%
OH
Br 80-86%
+HBr +HBr
三、 醚
醚是醇或酚的羟基中的氢被烃基取代的产物。通式为R-O-R',R和R’可以相同,也可以 不同。相同者称为简单醚或者叫对称醚;不同者称为混合醚。如果R、R'分别是一个有机基团 两端的碳原子则称为环醚。多数醚在常温下为无色液体,有香味,沸点低,比水轻,性质稳 定。醚类一般具有麻醉作用。如乙醚是临床常用的吸入麻醉剂。
1. 与强、浓无机酸形成盐
H2O + HCl ROH + HCl R2O + HCl
H3O+ClROH2+Cl-
R2OH+Cl-
2
PART 02
醛、酮、羧酸及其衍生物
2.1 醛、酮的结构与命名
分子中含有-CHO(醛基)的化合物称为醛,通式为RCHO。R-可以不是烃基,比如羟基乙醛 的R-是HOCH2-;R-也可以是烃基,比如烷基、烯基、芳香基或环烷基。依醛基的数目又可分为 一元醛和多元醛。低级醛为液体,高级醛为固体,只有甲醛是气体。醛的化学性质非常活泼,能 与亚硫酸氢钠、氢、氨等起加成反应,并易被弱氧化剂氧化成相应的羧酸。
6. 叔丁醇
OH
OH 2.
2-环己烯醇
5. CH3CHCH3 OH
1-苯基乙醇
异丙醇
3. HOCH2CH2CH2OH
1,3-丙二醇
CH3
6.
CH3CCH3
ቤተ መጻሕፍቲ ባይዱ
OH
叔丁醇
1.2 醇的物理性质
醇类化合物受羟基的影响,存在分子间的氢键,在水中还有醇分子和水分子间 的氢键。所以,它们的物理性质与相应的烃差异较大。主要表现在熔沸点比较高, 在水中有一定的溶解度等。一般而言,低级的醇类水溶性较好,甲醇、乙醇和丙醇 能与水以任意比例混溶。4~11个碳原子的醇为油状液体,部分溶于水,以后随着碳 原子数增加,烃基对分子的影响越来越大,使高级醇的物理性质更接近于相应的烃。
金属有机化学4

X M M
(iii)卤代芳烃的氧化加成是对芳环的亲核取代。
X PdL4 R R R L3Pd X -L PdL2X
X
R为吸电子基对反应有利,且不同卤素的活性 I > Br > Cl。
(iv)若产物为消旋的,则可能是自由基机理。同时也观 察到单电子转移反应的机理:
M + RX k2 R + Mn+1X [Mn+1]+ [RX]R R + Mn+1R
107 107 102 106 96 98 73
2. 氧化加成和还原消除反应
过渡金属与A-B 型的化合物反应时,A-B键发生断裂, 同时加成到过渡金属上:
A LnM + A B LnM B
其正反应称为氧化加成反应,逆反应称为还原消除反应。 (1)氧化加成反应
LnMm + A LnMm + A
B B
-
NH2
NH3 -Cl
Cl
Pt Cl
NH2
NH2 H2N Pt NH2 NH2
2+
Cl-NH3 H2N
NH2 Pt NH2 Cl
+
NH2
Cl-NH3
Cl
Pt NH2
Cl
(3)配体的立体影响
影响配位和解离的因素主要是配体的立体效应和电子效 应。
对于配体的立体影响,人们在以叔膦为配体的低原子价 络合物的解离平衡方面作了详细的研究。
Y Y L' L M L X Y L' M L L L X L' M L X -L' Y M L L X
即外加配体配位,中间体可以是四方锥形或三角双锥形, 新配体进入离去配体的位置,配合物的构型不变。 反应是高度立体专一的。
《有机化学》练习题(大学)(四)炔烃和二烯烃

《有机化学》练习题(⼤学)(四)炔烃和⼆烯烃第七章炔烃和⼆烯烃⼀.选择题1. ⽐较CH 4(I),NH 3(II),CH 3C ≡CH(III),H 2O(IV)四种化合物中氢原⼦的酸性⼤⼩:(A) I>II>III>IV (B) III>IV>II>I (C) I>III>IV>II (D) IV>III>II>I2. 2-戊炔顺-2-戊烯应采⽤下列哪⼀种反应条件 H 2,Pd/BaSO 4,喹啉 (B) Na,液氨 (C) B 2H 6 (D) H 2,Ni3. 已知RC ≡CH + NaNH 2 ──> RC ≡CNa + NH 3,炔钠加⽔⼜能恢复成炔烃,RC ≡CNa + H 2O ──> RC ≡CH + NaOH,据此可推测酸性⼤⼩为:(A) NH 3>RC ≡CH>H 2O (B) H 2O>RC ≡CH>NH 3 (C) H 2O>NH 3>RC ≡CH (D) HN 3>H 2O>RC ≡CH 4. 制造维尼纶的原料醋酸⼄烯酯由下式合成, 这种加成反应属于:(A) 亲电加成反应 (B) 亲核加成反应 (C) ⾃由基加成 (D) 协同CH 23O CH 3O+CH CH加成5. 区别丙烯、丙炔、环丙烷时鉴别丙炔最好的办法是采⽤:(A) Br 2,CCl 4 (B) KMnO 4,H+(C) 臭氧化 (D) Cu 2Cl 2,NH 3溶液6. Ag(NH 3)2NO 3处理下列各化合物,⽣成⽩⾊沉淀的是:7.产物应是:8. Lindlar 试剂的组成是什么A B CDCrO 3P d -BaSO 4Hg(OAc)2/THF HCl+ZnCl 2//NNC C24HgSO 4CH CO的名称(A )克莱-门森反应(B )库格尔反应(C )科佩奇尼反应(D )库切罗夫反应(B)CH 3CH 2C CH (D)(C)CH 3C CCH 3(A)+H 2Hg +,H+2(B) (CH 3)2CH CH 2CH 2CHO (A) (CH 3)2CHCH 2COCH 3(CH 3)2CHCH 2C CH (C) (CH 3)2CHCH 2C(OH)CH 2(D) CH 3)2CHCH 2CH CHOH10.的CCS 名称是 :(A) (2Z ,4E )-4-叔丁基-2,4-⼰⼆烯 (B) (2E ,4Z )-3-叔丁基-2,4-⼰⼆烯(C) (2Z ,4E )-3-叔丁基-2,4-⼰⼆烯 (D) (2E ,4Z )-4-叔丁基-2,4-⼰⼆烯11. 异戊⼆烯经臭氧化,在锌存在下⽔解,可得到哪⼀种产物 (A) HCHO + OHCCH 2CHO (B) HCHO + HOOCCH 2COOH (C) HCHO + CH 3COCHO (D) CH 3COCHO + CO 2 + H 2O 12. α, β-不饱和羰基化合物与共轭⼆烯反应得环⼰烯类化合物,这叫什么反应(A) Hofmann 反应 (B) Sandmeyer 反应 (C) Diels-Alder 反应 (D) Perkin 反应13.下列化合物中哪⼀个能与顺丁烯⼆酸酐反应,⽣成固体产物(A) 萘 (B) CH 3CH 2CH =CH 2 (C) (D) 对⼆甲苯CH 2C 3CH CH 214.丁⼆烯与溴化氢进⾏加成反应构成什么中间体15. 指出下列哪些化合物的紫外吸收波长最长,并按顺序排列。
有机化学徐寿昌4

**--碘与乙炔的加成--主要为一分子加成产物 HCCH + I2 ICH=CHI (1,2-二碘乙烯) 例2. 选择性加成:
在低温下,缓慢地加入溴,叁键不参加反应:
CH2=HC-CH2-CCH + Br2 CH2BrCHBrCH2CCH
**为什么炔烃的亲电加成不如烯烃活泼?
•烷基碳正离子(中间体)—正碳原子是sp2杂化状态,它的正电荷易 分散到烷基上. •烯基碳正离子(中间体)—sp杂化状态, 正电荷不易分散.所以能量 高,不稳定.形成时需要更高的活化能,不易生成. sp2杂化
(3) 乙炔的键 • C : 2s22p2 2s12px12py12pz1 • 乙炔的每个碳原子还各有两个相互 垂直的未参加杂化的p轨道, 不同碳 原子的p轨道又是相互平行的. • 一个碳原子的两个p轨道和另一个碳原子对应的两 个p轨道,在侧面交盖形成两个碳碳键.
(4) 乙炔分子的圆筒形 电子云 • 杂化轨道理论:两个成键轨道(1, 2),两个反键轨道 (1*, 2*) • 两个成键 轨道组合成了对称分布于碳碳 键键 轴周围的,类似圆筒形状的 电子云.
有机化学 Organic Chemistry
第四章 炔烃 二烯烃 红外光谱
(一) 炔烃
定义:分子中含有碳碳叁键的烃叫做炔烃,它的通 式:CnH2n-2 官能团为: -CC-
4.1 炔烃的异构和命名 (1)异构体——从丁炔开始有异构体. •同烯烃一样,由于碳链不同和叁键位置不同所引起的.
由于在碳链分支的地方不可能有叁键的存在,所以炔
(2) 亲电加成 (A) 和卤素的加成 例1. 炔烃与氯,溴加成: HCCH + Cl2 ClCH=CHCl + Cl2 HCCl2-CHCl2 R-CC-R` + X2 RXC=CXR` + X2 R-CX2-CX2-R` ——炔烃与氯,溴加成,控制条件也可停止在一分子加成 产物上.
有机化学 第4章 环烃

CH3 苯 甲苯
(b) 多环芳烃:分子中含有两个或两个以上苯环
C H 联苯 三苯甲烷
(c) 稠环芳烃:分子中含有两个或多个苯环彼此间通过 共用两个相邻碳原子稠合而成
萘
蒽
菲
二、单环芳烃
(1)苯的结构
ቤተ መጻሕፍቲ ባይዱ
1814年法拉第发现苯
1834年米切利希提出苯这一名称
ph
甲苯基 CH3 CH3 间 CH3 邻 对
(3)单环芳烃的物理性质
苯及其同系物一般为无色液体,相对密度
小于1,但比相对分子质量相近的烷烃和 烯烃的相对密度大。不溶于水,可溶于有 机溶剂。单环芳烃具有特殊气味,有毒
(4)单环芳烃的化学性质 (4.1) 苯环上的亲电取代反应
① 卤代: 在三卤化铁等催化剂作用下,苯与卤素作用生成卤
(代)苯,此反应称为卤化反应
+ CI2 FeCI3 CI + HCI Br + HBr
CH3 + CI2 FeCI3 CI
+
+ Br2
CH3
FeBr3
CH3
CI
卤苯继续卤化,比苯难,邻对位产物为主
Cl Cl + Cl2 Cl Cl + + Cl 邻二氯苯 (39%) Cl 对二氯苯 (55%) (6%) Cl
H C2-C3 H H
H H H
H
HH
H C6-C5
重叠式
构象稳定性:椅式>船式,椅式是环己烷最稳定的构象
(1)椅式构象的画法
加竖键(a键) 加竖键(a键)
H H H H H H
自考有机化学四试题及答案

自考有机化学四试题及答案一、选择题(每题2分,共20分)1. 下列化合物中,哪一个是醇?A. CH₃CH₂OHB. CH₃COCH₃C. CH₃CH₂CHOD. CH₃CH₂COOH答案:A2. 有机化学中的“碳正离子”是指什么?A. 带有一个正电荷的碳原子B. 带有一个负电荷的碳原子C. 带有一个正电荷的氧原子D. 带有一个负电荷的氢原子答案:A3. 以下哪个反应是亲电加成反应?A. 卤化氢与烯烃的反应B. 醇与羧酸的酯化反应C. 烯烃的聚合反应D. 醇的脱水反应答案:A4. 哪种催化剂可以使不饱和烃进行聚合反应?A. 硫酸B. 磷酸C. 金属钠D. 金属铂答案:D5. 下列哪种化合物属于芳香族化合物?A. 环己烷B. 环己烯C. 苯D. 环戊酮答案:C6. 以下哪种反应属于消除反应?A. 卤代烃的水解B. 醇的氧化C. 烯烃的卤化D. 醇的脱水答案:D7. 哪种溶剂最适合进行酯化反应?A. 水B. 甲醇C. 硫酸D. 浓硫酸答案:D8. 下列哪种化合物是手性分子?A. CH₃CH₂CH₃B. CH₃CH(Br)CH₃C. CH₃CHBrCH₂BrD. CH₃CH(OH)CH₃答案:D9. 哪种反应可以用于合成环氧化合物?A. 卤代烃的水解B. 烯烃的卤化C. 醇的氧化D. 烯烃的环氧化答案:D10. 下列哪种化合物是氨基酸?A. H₃N+CH₂COOHB. CH₃COOHC. CH₃CH₂COOHD. CH₃CH₂CH₂NH₂答案:A二、填空题(每空2分,共20分)11. 有机分子中的官能团包括________、________、________等。
答案:羟基、羰基、羧基12. 烷烃的通式为________,其中n是________。
答案:CnH2n+2,正整数13. 芳香烃的典型代表是________,其分子式为________。
答案:苯,C₆H₆14. 在有机化学中,碳原子的杂化轨道类型有________、________和________。
金属有机化学(4)

2. 醛酮的氢化硅烷化反应 醛和酮的氢化硅烷化反应比相应的烯烃更容易
原因:硅对氧的亲合性比对碳的亲和性大
O C Ph CH3 [RhL2(S)2]
+
OSiEtMe2 CH Ph CH3
H3O+ Ph
OH CH CH3
Me2EtSiH
反应历程:
α,β-不饱和羰基化合物
• 可以发生1,4-加成,也可以发生1,2-加成;
对简单烯烃无催化活性
一些Cr、Mo等金属的络合物也能选择性氢化 共轭烯烃
四、醛、酮的氢化反应 回顾:
还 原 成 醇 还 原
催化还原(H2 / Ni、Pb、Pt) (特点:无选择性 C=O、C=C、-CN、-NO2等都可被还原) 氢化铝锂(LiAlH4) (特点:还原能力强,
选 择 性 还 原
HNEt2
NEt2 Rh(S)Binap2ClO4 NEt2
H 3O
CHO
ZnBr2 OH
H2 OH
药物:
80-90年(20世纪) Non-Chiral Racemic Racemic Optically Pure Optically Pure 21世纪 Non-Chiral
2.反应条件温和,-最希望常温常压 3.催化
Rh(I)ClL3 NVE 16
Rh(I)ClL2 + L 14
L=PPh3
制法: i)PPh3还原法
RhCl3(H2O)X + 4PPh3 C2H5OH RhCl(PPh3)3 + O PPh3
既是配位体, 又是还原剂
此法限于制备三苯膦或某些三芳膦的Wilkinson 催化剂
ii)二聚法
MeOH/H2O Cl
有机化学 第四章 环烃

苯结构的表达
1. Kekulé苯
Kekulé苯结构式能解释
(a) 苯的一取代物只有一种
Br
Br
Br
(b) 苯可以加氢还原为环己烷
催化剂
+ H2
Kekulé苯结构式却不能解释
(a) 苯容易发生取代反应,却难于发生加成和氧化反应
(b) 按照Kekulé结构式,邻位二取代苯应该有两个异构体, 但实际上只有一个
5
2
2'
1 1'
6 6'
3' 4'
CH3
5'
4,4'-二 甲 基 联苯
23
1
4
6
5
1,4- 联三 苯
65
1
4
2
3
1,3- 联三 苯
(2)多苯代脂肪烃:可看作脂肪烃分子中氢原子被苯取代:
CH2
CH
CH CH
二苯 甲 烷
三苯 甲 烷
二苯 乙 烯
(3)稠环芳烃:并联:两个或两个以上苯环共用两个相邻碳原子。
CH3
1
6
2
5
3
4
CH3
1,4-二甲基环己烷
CH3
3
4
2
5
6 1 CH3
1,3-二甲基环己烷
CH3
1
6
2
5
3
4
CH
CH3 CH3
1-甲基-4-异丙基环己烷
3. 当环上连有取代基及不饱和键时,即为环烯(炔)烃时, 不饱和键以最小的号数表示。
4-甲基环已烯
CH3
4
5
3
6
2
1
4. 某些情况下,如当简单的环上连有较长的碳链时,也 可将环当作取代基,如:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高纲1125江苏省高等教育自学考试大纲03035有机化学(四)南京中医药大学编江苏省高等教育自学考试委员会办公室一、课程性质及其设置目的与要求(一)课程性质和特点有机化学(四)课程是中药学专业的一门重要专业基础课,它是本专业必须具备的基础,它的任务是为学生提供必要的有机化学基本知识、基础理论和基本操作技能,并训练他们应用这些理论和技能去研究各类有机化合物,从而为以后学习中药化学等专业课程,以及将来从事中药研究工作奠定良好的化学基础。
本课程的内容分成“有机化学基本概念”和“各类有机化合物”两部分。
基本概念部分阐述学习有机化学所必须掌握的一些基本理论知识;各类有机化合物则介绍有机化合物的结构、命名、性质、制法和有关反应历程等。
同时,还加强了与中药化学等课程有密切关系的“糖类”、“含氮有机化合物”、和“杂环化合物”等三章以及立体化学方面的内容。
(二)课程的基本要求通过本课程的学习,自学应考者应达到以下要求:1.掌握有机物的一般命名方法。
2.掌握各类有机化合物的基本结构;能解决一些立体结构问题。
3.掌握各类化合物的基本性质,了解一些重要的化学反应历程。
(三)本课程与相关课程的联系本课程是中药化学的基础,同时也为生物化学、药理学、中药鉴定学等课程提供基础。
二、课程内容与考核目标第一章绪论(不作考试要求)第二章有机化合物的结构和化学键一、课程内容本章主要介绍共价键形成的两个重要理论(价键理论和分子轨道理论)、共价键的属性、分子间作用力对物质物理性质的影响、共振论、电子效应理论。
二、学习目的与要求通过对有机分子的相关结构理论及分子间作用力知识的学习,为各类化合物的结构研究提供理论支持,为化学性质的分析提供理论基础。
三、考核知识点与考核要求1.领会:价键理论、共价键的属性、共振论及场效应理论。
2.掌握:分子间作用力和氢键对有机物物理性质的影响。
3. 熟练掌握:诱导效应和共轭效应理论。
第三章立体化学基础一、课程内容本章主要介绍立体化学的一些基本概念,分子模型的表示方法,顺反异构、对映异构和构象异构。
二、学习目的与要求确立有机分子的立体概念。
理解有机化合物的三大立体异构现象,并能够标示出化合物的构型,学会对烷烃进行构象分析,能正确分析环己烷的构象。
理解并掌握各种异构体的命名方法。
三、考核知识点与考核要求1.领会:立体化学中的一些基本概念,不含手性碳的分子的旋光异构。
2.掌握:锯架投影式和纽曼投影式的表达方式,烷烃的构象和环己烷的构象。
3.熟练掌握:含一至两个双键分子的顺反异构和构型表示方法;含一至两个手性中心分子的旋光异构和构型表示方法。
第四章烷烃一、课程内容本章主要介绍烷烃的结构、定义、同系列、通式的等基本概念,烷烃的命名原则烷烃的异构和物理性质,烷烃的卤代反应及卤代反应的历程。
二、学习目的与要求理解同系列、通式、同分异构现象的基本概念,理解并掌握烷烃的命名原则,掌握烷烃化学性质,并了解烷烃卤代反应历程。
三、考核知识点与考核要求1.领会:同系列和同分异构现象,烷烃的物理性质,卤代反应历程。
2.掌握:卤代反应规律及自由基的稳定性。
3.熟练掌握:烷烃的系统命名。
第五章烯烃一、课程内容本章主要介绍烯烃的基本概念、命名、物理性质、化学性质、亲电加成反应历程以及制备。
二、学习目的与要求理解烯烃的一些基本概念,学会烯烃的系统命名,通过烯烃的结构分析理解加成反应、α-H 的卤代反应,通过烯烃的加成反应历程理解烯烃的加成反应择向规律,理解氧化反应与烯烃结构的关系,了解烯烃的物理性质及常用制备方法。
三、考核知识点与考核要求1.领会:烯烃的结构、异构和物理性质2.掌握:烯烃的α-H 的卤代反应、催化加氢、硼氢化反应。
3.熟练掌握:烯烃的系统命名和亲电加成反应及氧化反应。
第六章炔烃和二烯烃一、课程内容本章主要介绍炔烃的结构、命名和异构,炔烃的物理性质、化学性质,二烯烃的分类、命名、结构和特性反应。
二、学习目的与要求理解炔烃基本结构,学会炔烃的系统命名,了解炔烃的物理性质,通过炔烃的结构分析理解加成反应及与烯烃异同、择向规律,理解炔烃的活泼氢反应,理解氧化反应。
通过共轭二烯烃的结构理解共轭二烯烃的加成反应,理解双烯合成反应。
三、考核知识点与考核要求1.领会:炔烃基本结构与亲核加成反应,共轭二烯烃的特性、双烯合成反应。
2.掌握:端基炔氢的酸性,炔烃的氧化反应,共轭二烯烃的加成反应。
3.熟练掌握:炔烃的命名和亲电加成反应。
第七章脂环烃一、课程内容本章主要介绍脂环烃的分类和命名,脂环烃的化学反应,环烷烃的结构和稳定性,环烷烃的立体异构现象。
二、学习目的与要求学会脂环烃的命名,对照烯烃和烷烃化学性质及环烷烃的稳定性理解环烷烃的化学性质,理解环烷烃的立体异构现象。
三、考核知识点与考核要求1.领会:脂环烃的分类和化学反应。
2.掌握:脂环化合物的顺反异构和对映异构现象,取代环己烷的构象异构。
3.熟练掌握:脂环烃的命名。
第八章芳烃一、课程内容本章主要介绍苯的分子结构理论,芳烃的命名和物理性质,苯的取代反应及反应历程、氧化反应,萘的结构和性质,蒽和菲结构,非苯芳烃的概念。
二、学习目的与要求通过对苯的结构研究理解芳香性概念,学会芳香烃的命名,结合反应历程理解苯环的亲电取代反应与亲电取代定位规则,理解苯及其同系物的氧化反应。
理解常见的多环芳烃的萘、蒽和菲的基本结构与命名,理解萘的主要化学性质,理解休克尔规则。
三、考核知识点与考核要求1.领会:芳香烃的分类、物理性质,蒽的结构和性质,菲的结构。
2.掌握:单环芳烃的加成反应,萘的氧化还原反应,休克尔规则。
3.熟练掌握:芳香烃的命名、单环芳烃亲电取代反应及定位规则,单环芳烃的氧化反应,萘及萘的衍生物亲电取代反应。
第九章卤烃一、课程内容本章主要介绍卤烃的结构、命名、分类,卤烃的物理性质、化学性质及制备。
二、学习目的与要求学会命名卤烃,通过亲核取代反应历程理解卤烃的取代反应及影响取代反应的因素,通过消除反应历程理解卤烃的消除反应及影响消除反应的因素,理解卤烃与金属镁的反应及反应生成的格氏试剂的性质,理解二烃基铜锂试剂的生成与性质,理解卤烃的还原反应,理解卤烃的常用制备方法。
三、考核知识点与考核要求1.领会:卤烃分类、物理性质,有机钠和有机锂的生成及性质,卤烃的还原反应,卤烃的制备方法。
2.掌握:卤烃系统命名、格氏试剂的生成与性质,双键位置对卤素活泼性的影响。
3.熟练掌握:卤烃的亲核取代反应与消除反应。
第十章醇、酚、醚一、课程内容本章主要介绍醇、酚和醚三类化合物的结构、命名、分类,物理性质、化学性质及制备方法。
二、学习目的与要求学会醇、酚、醚的系统命名,理解醇、酚、醚的结构和物理性质,理解醇羟基官能团的特性以及相应的化学性质,从酚羟基的特性理解酚羟基的反应及苯环上的亲电取代反应,理解醇和酚的氧化反应,理解醚的化学性质。
三、考核知识点与考核要求1.领会:醇、酚、醚的结构、分类、物理性质和常用制备反应,酚的氧化反应。
2.掌握:醇和酚的酸性,醇的氧化反应,酚酯的形成与重排,酚与三氯化铁的反应,醚与强酸的反应。
3.熟练掌握::醇、酚、醚的命名,醇的亲核取代反应和脱水反应;酚的卤代、磺化、硝化反应。
第十一章醛、酮、醌一、课程内容本章主要介绍醛、酮、醌的结构、命名,醛和酮的物理性质、制备、化学性质与亲核加成反应历程,α,β-不饱和醛酮的反应,醌的性质。
二、学习目的与要求学会醛、酮的系统命名,理解醛、酮的结构和物理性质,根据醛、酮的结构特点理解醛、酮的化学性质,根据α,β-不饱和醛酮的结构特点理解其主要化学性质,理解醛、酮的常用制备方法,理解醌的结构和命名。
三、考核知识点与考核要求1.领会:醛、酮的结构和物理性质,醛、酮与水和醇的加成反应,醛、酮的常用制备方法,醌的结构、命名和性质。
2.掌握:醛酮的氧化和还原反应,α,β-不饱和醛酮的主要化学性质。
3.熟练掌握:醛、酮的系统命名,醛、酮的亲核加成反应,醛、酮的α-卤代和羟醛缩合反应。
第十二章羧酸及其衍生物一、课程内容本章主要介绍羧酸、酰卤、酸酐、酯和酰胺的结构、命名和分类,羧酸的物理性质、化学性质、制备方法,二元羧酸的特性反应,酰卤、酸酐、酯和酰胺的主要化学性质,羧酸衍生物的水解、醇解、氨解的反应活性的比较。
二、学习目的与要求理解羧酸及其衍生物的基本结构,学会羧酸及其衍生物的系统命名,理解羧酸的物理性质和化学性质,理解二元羧酸的特性反应,理解羧酸衍生物的性质。
三、考核知识点与考核要求1.领会:羧酸及其衍生物的基本结构,羧酸的物理性质,羧酸及其衍生物的还原反应,羧酸的制备方法,羧酸的脱羧反应、α-H卤代反应。
2.掌握:二元羧酸的特有反应,酯缩合反应,羧酸衍生物与格氏试剂的反应,异羟肟酸铁反应,霍夫曼降解反应,酰胺的酸碱性。
3.熟练掌握:羧酸及其衍生物的系统命名,羧酸的酸性大小,羧基上羟基的取代反应,羧酸衍生物的水解、醇解、氨解反应。
第十三章取代羧酸一、课程内容本章主要介绍卤代酸、醇酸、酚酸、羰基酸和氨基酸的结构、命名及化学性质;乙酰乙酸乙酯的结构理论、性质、制备和在合成上的应用。
二、学习目的与要求学会取代羧酸的系统命名,理解多官能团化合物的结构特点和官能团之间的相互影响,理解乙酰乙酸乙酯的两种分解方式和互变异构的基本理论。
三、考核知识点与考核要求1.领会:取代羧酸的分类,酚酸的化学性质,氨基酸的两性与等电点,羰基酸的性质。
2.掌握:氨基酸的受热反应,乙酰乙酸乙酯的互变异构,乙酰乙酸乙酯的酸式分解和酮式分解。
3.熟练掌握:取代羧酸的命名,卤代酸与碱的反应,醇酸的脱水反应。
第十四章糖类一、课程内容本章主要介绍糖的定义、分类,己醛糖和己酮糖的结构,单糖的物理性质、化学性质,双糖的定义、分类、结构和还原性,多糖的结构。
二、学习目的与要求理解糖的定义、分类,理解并掌握单糖的结构和化学性质,理解双糖的结构与还原性,理解淀粉多糖的特性。
三、考核知识点与考核要求1.领会:糖的定义、分类,D-果糖的链状结构和环状结构,单糖的颜色反应,常见的还原性双糖和非还原性双糖的结构特点与性质,淀粉的特性。
2.掌握:单糖的差向异构化反应、氧化反应、与溴水反应、成苷反应、成脎反应。
3.熟练掌握:D系己醛糖的链状结构和环状结构(Haworth式、构象式)。
第十五章含氮有机化合物一、课程内容本章主要介绍胺的结构、命名和分类,胺类的物理性质和化学性质,季铵盐的性质及反应,重氮盐的结构、制备及性质。
二、学习目的与要求理解胺类的结构、命名、重要的化学性质及其应用,理解芳香重氮盐的结构、重要的化学性质。
三、考核知识点与考核要求1.领会:胺的结构、分类、物理性质和制备,芳香重氮盐的留氮反应。
2.掌握:胺的烷基化反应、酰化反应、亚硝酸反应,芳香胺的卤代、硝化、磺化反应,芳香重氮盐的放氮反应。
