染色质免疫共沉淀 ChIP Protocol及crosslink 的原理
免疫共沉淀技术原理

免疫共沉淀技术原理免疫共沉淀技术(Immunoprecipitation,简称IP)是一种常用的分析蛋白质相互作用的方法。
该技术基于抗体对目标蛋白质的高度选择性结合能力,使得能够富集含有目标蛋白质的复合物,并进一步用于蛋白质相互作用的研究。
接下来将介绍免疫共沉淀技术的原理和实验过程。
免疫共沉淀技术的原理是利用特异性抗体与目标蛋白质结合形成免疫复合物,然后通过沉淀技术将免疫复合物从细胞裂解物中分离出来。
通常,实验者需要先对目标蛋白质进行抗体的免疫标记,常用的方法包括对抗体进行染色标记、酶标记或放射性标记。
免疫标记后的抗体与目标蛋白质结合,形成免疫复合物。
免疫共沉淀技术可以分为直接法和间接法。
直接法是将抗体固定在沉淀材料(如蛋白A或蛋白G的琼脂糖糖珠)上,与细胞裂解物中的目标蛋白质共沉淀。
间接法是在细胞裂解物中,先将目标蛋白质与一种特异性抗体结合,然后再将这种结合后的复合物与固定在沉淀材料上的第二抗体结合。
实验过程中,首先将细胞裂解并制备成可用于免疫共沉淀的样品。
然后加入预先标记的抗体,与目标蛋白质结合形成免疫复合物。
接下来,将沉淀材料添加到样品中,如蛋白A或蛋白G的琼脂糖糖珠。
这些材料能够与抗体的Fc区结合,从而沉淀下免疫复合物。
混合物经过洗涤步骤后,免疫复合物得以纯化。
在纯化后,可以通过不同的方式进一步分析目标蛋白质的亚细胞分布、蛋白质相互作用或修饰状态。
例如,可以使用Western blotting检测特定的蛋白带来确定免疫共沉淀的效果。
此外,还可以使用质谱分析技术对免疫共沉淀的蛋白质进行鉴定。
免疫共沉淀技术的应用广泛,可以用于研究蛋白质复合物的组成、相互作用以及功能。
这项技术在研究细胞信号传导、基因调控和疾病发生机制等领域都有重要的应用。
通过免疫共沉淀技术,研究者可以了解目标蛋白质在细胞中的功能以及与其他蛋白质的相互作用关系,有助于深入理解生物学过程和寻找新的治疗靶点。
综上所述,免疫共沉淀技术是一种重要的蛋白质相互作用分析方法,其原理主要依赖于抗体与目标蛋白质的特异性结合能力。
染色质免疫沉淀技术及其应用

染色质免疫沉淀技术及其应用染色质免疫沉淀(ChIP)技术是一种用于研究染色质蛋白相互作用的关键技术,它可以帮助我们理解基因组上的DNA结构与功能之间的关系。
本文将介绍染色质免疫沉淀技术的原理、步骤和应用。
染色质免疫沉淀技术的原理基于特定抗体与染色质上的目标蛋白结合的能力。
通过将染色质与细胞核蛋白一起交联,然后使用适当的酶切酶切割DNA,将与目标蛋白结合的DNA 片段与抗体结合,最后通过沉淀纯化和逆交联来获取与目标蛋白相互作用的DNA片段。
这些DNA片段可以通过PCR扩增或高通量测序来分析,从而确定目标蛋白与基因组上的特定DNA区域的相互作用。
1. 细胞处理:选择适当的细胞类型和处理条件,如细胞状态(正常、疾病或处理后)、细胞密度和处理时间等。
2. 细胞交联:给细胞添加交联剂(一般为福尔马林)来固定细胞核内蛋白与DNA的相互作用。
3. 核提取:裂解交联细胞,将细胞核提取出来。
核提取过程中添加蛋白酶抑制剂来防止蛋白降解。
4. 酶切:使用适当的酶切酶切割DNA,产生与目标蛋白结合的DNA片段。
5. 免疫沉淀:将抗体与目标蛋白特异性识别的DNA结合起来。
可以使用预包被蛋白G 或蛋白A纯化好的抗体,并将其加入核提取物中。
这样就可以使抗体与特定蛋白结合,并形成免疫复合物。
6. 沉淀纯化:使用磁珠或其他材料将免疫复合物与其他非特异性结合物分离。
通过洗涤等步骤去除非特异性结合物。
7. DNA释放:对免疫复合物进行逆交联,从而释放出与蛋白相互作用的DNA。
8. DNA分析:通过PCR扩增或高通量测序等方法对所得到的DNA片段进行分析。
可以使用特定的引物或在全基因组范围内进行扩增。
染色质免疫沉淀技术已经广泛应用于生物医学研究中,特别是在基因调控和表观遗传学领域。
以下是染色质免疫沉淀技术的主要应用:1. 转录因子与基因调控:通过分析转录因子与染色质上的相互作用,可以研究转录因子对基因的调控机制。
可以确定转录因子的结合位点,并研究其对基因的表达水平和活性的影响。
免疫共沉淀实验原理及详细步骤

免疫共沉淀实验原理及详细步骤免疫沉淀(immunoprecipitation,简称IP)是一种广泛应用于生物学和生物化学研究中的实验方法,用于检测和分离复合物中的特定蛋白质。
它结合了特异性抗体与蛋白质-抗体相互作用的原理,利用抗体选择性地沉淀出目标蛋白质,并与其相关的复合物。
本文将详细介绍免疫共沉淀实验的原理及步骤。
免疫共沉淀实验利用抗体与目标蛋白质相互结合的特异性,通过该特异性结合,将目标蛋白质及其相关的复合物选择性地沉淀出来。
该实验主要包括以下几个步骤:1.抗体与抗原的结合:在实验中,需要选择特异性的抗体与目标蛋白质结合。
2.抗体与蛋白质-抗体复合物的沉淀:将抗体结合的蛋白质与复合物从样本中沉淀。
3.洗涤:洗涤沉淀的复合物,去除非特异性结合的蛋白质和杂质。
4.释放目标蛋白质:将目标蛋白质从抗体中释放出来,以进行后续的下游分析。
1.细胞预处理:在进行免疫共沉淀实验之前,需要将细胞或组织进行必要的处理,例如刺激剂的刺激或疾病模型的建立。
可以选择不同条件下的实验处理组和对照组进行对比。
同时,还需要对实验样本进行适当的裂解,以确保目标蛋白质的充分释放。
2.抗体选择:选择特异性的抗体与目标蛋白质结合。
抗体可以是单克隆抗体或多克隆抗体,也可以是特异性抗体。
此外,需要选择适当的免疫沉淀试剂盒,确保实验的准确性。
3.抗原结合:将适当的抗体与目标蛋白质结合,形成抗原-抗体复合物。
这一步骤可以在实验前进行或将其加入样本中进行。
为确保抗原-抗体结合的充分性,可以进行一定的反应时间和反应温度。
4.免疫沉淀:将抗原-抗体复合物选择性地沉淀出来。
可以采用多种方法进行免疫沉淀,例如蛋白A/G琼脂糖,特效筛选柱等。
通过离心或过滤等方式从沉淀中收集复合物。
5.洗涤:洗涤步骤用于去除非特异性结合的蛋白质和杂质。
洗涤液的组成可以根据实验需要进行调整。
洗涤步骤需要进行多次,确保洗涤得到干净的复合物。
6.释放目标蛋白质:将目标蛋白质从抗体中释放出来,以进行后续的下游分析。
染色体免疫共沉淀介绍

免疫学方法
在保持组蛋白和DNA联合的同时,通过运用对 在保持组蛋白和DNA联合的同时,通过运用对 应于一个特定组蛋白标记的生物抗体,染色质被 切成很小的片断,并沉淀下来。IP是利用抗原蛋 切成很小的片断,并沉淀下来。IP是利用抗原蛋 白质和抗体的特异性结合以及细菌蛋白质的 A”特异性地结合到免疫球蛋白的FC FC片 “protein A”特异性地结合到免疫球蛋白的FC片 段的现象活用开发出来的方法。目前多用精制的 protein A预先结合固化在argarose的beads上,使之 A预先结合固化在argarose的beads上,使之 与含有抗原的溶液及抗体反应后,beads上的 与含有抗原的溶液及抗体反应后,beads上的 protein A就能吸附抗原达到精制的目的。在免疫 A就能吸附抗原达到精制的目的。在免疫 沉淀之前,通过甲醛作用使DNA和蛋白质发生 沉淀之前,通过甲醛作用使DNA和蛋白质发生 共价连接,通过离心就可以得到DNA共价连接,通过离心就可以得到DNA-蛋白复合 体。染Fra bibliotek体免疫共沉淀的应用
CHIP可以检测体内反式因子与DNA的动态作用 CHIP可以检测体内反式因子与DNA的动态作用 CHIP与其他方法的结合,扩大了其应用范围: CHIP与其他方法的结合,扩大了其应用范围: CHIP与基因芯片相结合建立的 CHIP-on-chip方法 CHIP与基因芯片相结合建立的 CHIP-on-chip方法 已广泛用于特定反式因子靶基因的高通量筛选; CHIP与体内足迹法相结合,用于寻找反式因子的 CHIP与体内足迹法相结合,用于寻找反式因子的 体内结合位点; RNA-CHIP用于研究RNA在基因表达调控中的作 RNA-CHIP用于研究RNA在基因表达调控中的作 用
染色体免疫共沉淀
关于染色质免疫共沉淀ChIP实验原理及实验总结

关于染色质免疫共沉淀ChIP实验原理及实验总结ChIP实验原理在活细胞状态下固定蛋白质-DNA复合物,并将其随机切断为一定长度范围内的染色质小片段,然后通过免疫学方法沉淀此复合体,特异性地富集目的蛋白结合的DNA片段,通过对目的片断的纯化与检测,从而获得蛋白质与DNA相互作用的信息。
可以利用ChIP研究转录因子(transcription factor, TF)与启动子(promoter)的关联性。
由于ChIP采用甲醛固定活细胞或者组织的方法,所以能比较真实的反映细胞内TF与Promoter的结合情况。
这个优势是EMSA这个体外研究核酸与蛋白相互结合的实验方法所不能比拟的。
当用甲醛处理时,相互靠近的蛋白与蛋白,蛋白与核酸(DNA或RNA)之间会产生共价键。
细胞内,当TF与Promoter相互结合(生物意义上的结合)时,它们必然靠的比较近,或者契合在一起,这个时候用甲醛处理,能使它们之间产生共价键。
一般ChIP的流程是:甲醛处理细胞——收集细胞,超声破碎——加入目的蛋白的抗体,与靶蛋白-DNA复合物相互结合——加入Protein A,结合抗体-靶蛋白-DNA复合物,并沉淀——对沉淀下来的复合物进行清洗,除去一些非特异性结合——洗脱,得到富集的靶蛋白-DNA复合物——解交联,纯化富集的DNA-片断——PCR分析。
ChIP实验步骤第一天:(一)、细胞的甲醛交联与超声破碎。
1、取出1平皿细胞(10cm平皿),加入243ul 37%甲醛,使得甲醛的终浓度为1%。
(培养基共有9ml)2、37摄氏度孵育10min。
3、终止交联:加甘氨酸至终浓度为0.125M。
450ul 2.5M甘氨酸于平皿中。
混匀后,在室温下放置5min即可。
4、吸尽培养基,用冰冷的PBS清洗细胞2次。
5、细胞刮刀收集细胞于15ml离心管中(PBS依次为5ml,3ml和3ml)。
预冷后2000rpm 5min收集细胞。
6、倒去上清。
按照细胞量,加入SDS Lysis Buffer。
chip seq原理

ChIP-seq(Chromatin Immunoprecipitation followed by sequencing)是一种用于研究染色质上特定蛋白质与DNA相互作用的技术。
它结合了染色质免疫沉淀(ChIP)和高通量测序技术。
ChIP-seq的基本原理如下:
1. 交联:首先,细胞或组织中的染色质与蛋白质相互作用需要被交联,通常使用甲醛进行交联。
2. 染色质免疫沉淀(ChIP):交联后的细胞或组织被裂解,染色质与特定的抗体结合,形成染色质-抗体复合物。
这些复合物可以通过抗体的亲和力选择性地富集。
3. DNA解交联:染色质-抗体复合物被洗脱,并通过加热或酶解去除交联。
4. DNA测序:富集的DNA被提取,并通过高通量测序技术进行测序。
这可以产生大量的短序列片段。
5. 数据分析:测序数据经过质量控制和预处理后,可以通过比对到参考基因组上,确定染色质-抗体复合物结合的位置。
通过统计分析,可以确定特定蛋白质与DNA相互作用的区域。
ChIP-seq技术的优势在于可以高分辨率地确定特定蛋白质与DNA相互作用的位置,从而帮助研究人员理解基因调控、表观遗传学和疾病发生机制等方面的问题。
CHIP原理

关于染色质免疫共沉淀ChIP实验原理及实验总结ChIP实验原理在活细胞状态下固定蛋白质-DNA复合物,并将其随机切断为一定长度范围内的染色质小片段,然后通过免疫学方法沉淀此复合体,特异性地富集目的蛋白结合的DNA片段,通过对目的片断的纯化与检测,从而获得蛋白质与DNA相互作用的信息。
可以利用ChIP研究转录因子(transcription factor,TF)与启动子(promoter)的关联性。
由于ChIP采用甲醛固定活细胞或者组织的方法,所以能比较真实的反映细胞内TF与Promoter的结合情况。
这个优势是EMSA这个体外研究核酸与蛋白相互结合的实验方法所不能比拟的。
当用甲醛处理时,相互靠近的蛋白与蛋白,蛋白与核酸(DNA或RNA)之间会产生共价键。
细胞内,当TF与Promoter 相互结合(生物意义上的结合)时,它们必然靠的比较近,或者契合在一起,这个时候用甲醛处理,能使它们之间产生共价键。
一般ChIP的流程是:甲醛处理细胞——收集细胞,超声破碎——加入目的蛋白的抗体,与靶蛋白-DNA复合物相互结合——加入Protein A,结合抗体-靶蛋白-DNA复合物,并沉淀——对沉淀下来的复合物进行清洗,除去一些非特异性结合——洗脱,得到富集的靶蛋白-DNA复合物——解交联,纯化富集的DNA-片断——PCR分析。
ChIP实验步骤第一天:(一)、细胞的甲醛交联与超声破碎。
1、取出1平皿细胞(10cm平皿),加入243ul37%甲醛,使得甲醛的终浓度为1%。
(培养基共有9ml)2、37摄氏度孵育10min。
3、终止交联:加甘氨酸至终浓度为0.125M。
450ul2.5M甘氨酸于平皿中。
混匀后,在室温下放置5min即可。
4、吸尽培养基,用冰冷的PBS清洗细胞2次。
5、细胞刮刀收集细胞于15ml离心管中(PBS 依次为5ml,3ml和3ml)。
预冷后2000rpm5min收集细胞。
6、倒去上清。
按照细胞量,加入SDS Lysis Buffer。
免疫共沉淀技术原理

免疫共沉淀技术原理
免疫共沉淀技术是一种在生物学实验中常用的技术,是由免疫学和共沉淀技术两种方法结合构成的。
免疫共沉淀技术基本原理为:首先用抗体(抗原特异性免疫球蛋白)和抗原(蛋白质、多糖类或核酸分子)结合,形成抗原-抗体复合物,然后将抗原-抗体复合物及抗原混合悬浮液置于离心机或离心管中,进行离心,将复合物沉淀在管底,抗原在此过程中被抑制,经离心或超滤操作从抗原-抗体复合物中抽提出抗体,最后可用SDS-PAGE或ELISA技术鉴定抗体的纯度。
该技术在抗原和抗体可溶性、亲和力足够强的情况下,可大规模地制备抗体。
02 CHIP染色质免疫共沉淀实验方法简介

Ago----argonaute蛋白
谢 谢!
概述 原理 方法 比较 举例
Saleh A, Alvarez-Venegas R, Avramova Z. An efficient chromatin immunoprecipitation (ChIP) protocol for studying histone modifications in Arabidopsis plants. Nat Protoc. 2008;3(6):1018-1025.
概述
原理 染色质免疫沉淀实验(CHIP)
方法 比较
举例 ➢ 研究体内DNA-蛋白质相互作用的重要 工具。 它不仅可以灵敏地检测目标蛋 白与特异DNA 片段的结合情况,还可以 用来研究组蛋白与基因表达的关系。
概述
原理 CHIP原理
方法
比较 在活细胞状态下固定蛋白质-DNA复合物
举例
将其随机切断为一定长度范围内的染色质
概述
原理 应用举例
方法
比较
举例
Mantovani F, Tocco F, Girardini J, et al. The prolyl isomerase Pin1 orchestrates p53 acetylation and dissociation from the apoptosis inhibitor iASPP. Nat Struct Mol Biol. 2007 Oct;14(10):912-920.
方法
比较
举例
条 超声波破碎条件的选择
件 选
抗体量的选择
择 PCR反应条件的选择
对 Input对照
照 设
阳性对照:如组蛋白抗体
置 阴性对照:阴性引物
chip-seq染色质免疫共沉淀原理

1. 概述chip-seq技术1.1 chip-seq是一种用于研究染色质蛋白与DNA相互作用的技术 1.2 蛋白与DNA的相互作用对于基因表达和细胞功能非常重要1.3 chip-seq技术的原理是利用染色质免疫共沉淀(ChIP)和高通量测序(sequencing)相结合2. ChIP-seq技术的步骤2.1 细胞或组织的交联2.2 细胞或组织的裂解和核的提取2.3 免疫共沉淀2.4 DNA纯化2.5 测序和数据分析3. 染色质免疫共沉淀原理3.1 免疫共沉淀是指利用特异性抗体将靶蛋白与DNA结合并进行共沉淀3.2 抗体的具体选择非常重要,需要保证抗体能够特异性结合到目标蛋白3.3 免疫共沉淀的原理是利用抗体与靶蛋白的特异性结合来将靶蛋白与DNA结合物沉淀下来3.4 靶蛋白和DNA结合物的提取可以通过酸碱或酶的方法进行4. ChIP-seq技术的应用4.1 在研究基因表达调控中的应用4.2 在研究细胞分化和组织发育中的应用4.3 在研究疾病发生和发展中的应用4.4 在药物研发中的应用5. ChIP-seq技术的优势和局限性5.1 优势包括高灵敏度、高特异性和全基因组覆盖5.2 局限性包括实验操作复杂、数据分析费时费力6. 结语6.1 chip-seq技术作为一种重要的分子生物学技术,在基因组学和表观遗传学研究中发挥着重要作用6.2 虽然其原理复杂,但结合高通量测序技术,能够为科研工作者提供丰富的信息资源6.3 随着技术的不断发展和完善,chip-seq技术在生命科学领域的应用前景将更加广阔。
7. ChIP-seq 技术在生物学研究中的应用ChIP-seq 技术在生物学研究中展现出了广泛的应用价值,特别是在基因表达调控的研究中发挥了重要作用。
通过 ChIP-seq 技术,研究人员可以对特定转录因子与 DNA 的结合位点进行高通量测序,从而获得全基因组范围内的转录因子结合位点的信息。
这种技术的应用可以帮助研究人员更深入地理解基因表达调控的机制,发现新的转录因子结合位点以及破解染色质的三维结构和动态变化。
ChIP试剂盒染色质免疫共沉淀全套解决方案

ChIP试剂盒染色质免疫共沉淀全套解决方案染色质免疫沉淀-芯片试剂盒染色质免疫沉淀(芯片)的完整溶液是研究体内DNA与蛋白质相互作用的最佳方法。
其基本原理是将蛋白质-DNA复合物固定在活细胞状态,将其随机切割成一定长度范围内的小染色质片段,然后通过免疫学方法沉淀复合物,特异性富集与靶蛋白结合的DNA片段。
通过目标片段的纯化和检测,可以获得关于蛋白质和DNA之间相互作用的信息。
芯片不仅可以检测体内反式因子与DNA的动态相互作用,还可以研究组蛋白的各种共价修饰与基因表达的关系。
此外,芯片与其他方法的结合扩大了其应用范围:通过芯片与基因芯片的结合建立的芯片-芯片法已广泛用于高通量筛选特异的反式因子靶基因;芯片结合体内足迹法寻找反式因子的体内结合位点;核糖核酸芯片用于研究核糖核酸在基因表达调控中的作用因此,随着ChIP的进一步完善,它必将在基因表达调控研究中发挥越来越重要的作用。
就目前国内研究状况而言,教师在研究领域有分化、转录、发育、诱导多能性、肿瘤干细胞、表观遗传学等。
会做ChIP实验,一些老师会自己购买抗体,手动配置试剂。
然而,因为实验本身具有复杂的实验步骤,并且其中许多步骤非常关键,需要更多的试剂,所以很容易导致配置之间的错误,并且实验周期长。
如果没有设置阴性和阳性对照,结果就无法分析,从而导致无休止的混乱。
经典染色质免疫沉淀(ChIP)试剂盒(p-2002):提供细胞样品上染色质免疫沉淀反应所需的所有试剂此外,试剂盒包含阳性对照抗体(核糖核酸聚合酶2抗体)、阴性对照抗体(正常小鼠的IgG)和GAPDH引物(可用作阳性对照,以确保试剂盒中的试剂和操作步骤没有问题)在大多数生长中的哺乳动物细胞中,核酸聚合酶II富集在GAPDH基因启动子上,为启动转录做准备,因此启动子可以与核酸聚合酶II进行免疫沉淀反应,但不能与正常的小鼠IgG进行免疫沉淀反应。
在该染色质免疫沉淀反应中,细胞与甲醛偶联以提取其中的染色质染色质被适当破坏,然后加入微孔中,与吸附在微孔表面的抗体反应特异性结合在微孔上的DNA从抗体-捕获蛋白-DNA复合物中释放出来,通过我们公司专门设计的高速离心柱进行翻转和纯化。
免疫共沉淀实验原理及方法

免疫共沉淀实验原理及方法免疫共沉淀实验(immunoprecipitation)是一种常用的分子生物学实验方法,用于检测免疫反应的可视化。
该实验基于免疫学反应的原理,通过特异性抗体与目标分子结合,将目标分子从复杂的混合物中沉淀出来,以便进一步分析。
免疫共沉淀实验的原理是基于抗体与抗原之间的特异性结合。
首先,需要选择与目标分子特异性结合的抗体,并对抗体进行纯化和标记,常用的标记物有酶、放射性同位素、荧光素等。
然后,将标记的抗体与样品中的目标分子充分混合,在适当的条件下,使抗体与目标分子发生结合反应。
接下来,通过添加沉淀剂,例如蛋白A/G磁珠、蛋白G琼脂糖或亲和素等,将抗体/目标复合物与其他组分一起沉淀下来。
通过离心将沉淀物分离出来,然后用缓冲液洗涤,以去除非特异性结合的物质。
最后,将洗涤后的沉淀物进行破碎、蛋白质酶解等处理,并使用电泳、免疫印迹、质谱等技术对目标分子进行分析和鉴定。
在免疫共沉淀实验中,关键步骤包括抗体的选择和标记、样品的制备与处理、抗体与目标分子的结合、沉淀物的分离与洗涤以及沉淀物的分析和鉴定。
1.抗体的选择和标记:选择特异性结合目标分子的抗体,并对抗体进行纯化和标记。
例如,使用蛋白A/G或蛋白G将抗体结合于磁珠或琼脂糖上,再通过标记物的共价偶联(如酶、放射性同位素、荧光素等)对抗体进行标记。
2.样品的制备与处理:根据实验要求,选择适当的样品组织或细胞,将其裂解并得到包含目标分子的混合物。
裂解缓冲液的组成需要根据目标分子的特性进行优化,以保持目标分子的稳定性和活性。
可以加入适量的蛋白酶抑制剂、磷酸酯酶抑制剂和甲基化酶抑制剂等保护目标分子。
3.抗体与目标分子的结合:将标记的抗体加入到样品中,与目标分子发生特异性结合反应。
可以在低温(4℃)下进行反应,以减少非特异性结合。
4.沉淀物的分离和洗涤:通过添加适当的沉淀剂,将抗体/目标复合物与其他组分一起沉淀下来。
常用的沉淀剂有通过蛋白A/G磁珠、蛋白G琼脂糖或亲和素等。
chip—seq原理

chip—seq原理Chip-seq(Chromatin Immunoprecipitation Sequencing,染色质免疫沉淀测序)是一种用于研究染色质上的转录因子结合位点和组蛋白修饰的方法。
该方法首先对细胞进行染色质交联,使得DNA与染色质蛋白交联在一起。
然后使用适当的抗体选择性地免疫沉淀目标转录因子或组蛋白修饰。
接下来,将沉淀物中的DNA进行解交联,并通过DNA纯化获取目标DNA片段。
之后,对目标DNA片段进行测序。
通过高通量测序技术,可以得到很多短序列片段,这些片段对应于染色体上的不同位置。
这些测序片段可以与参考基因组进行比对,从而确定它们在基因组上的位置。
最后,通过对比实验组和对照组的测序数据,可以鉴定转录因子结合位点或组蛋白修饰位点的位置和富集情况,进而研究染色质的功能和调控机制。
总结起来,Chip-seq的原理可以简化为以下几个步骤:1. 染色质交联:将DNA与染色质蛋白交联在一起。
2. 免疫沉淀:使用抗体选择性地沉淀目标转录因子或组蛋白修饰。
3. DNA解交联:将沉淀物中的DNA解除交联,并进行纯化。
4. DNA测序:对纯化后的DNA片段进行高通量测序。
5. 数据分析:通过比对测序数据,确定DNA片段在基因组上的位置,并进行ChIP峰检测和差异分析等。
当使用Chip-seq技术进行染色质免疫沉淀测序时,还可以进一步进行数据分析来获得更多的信息。
1. Peak calling(峰检测):通过对测序数据进行分析和统计,可以识别出在特定条件下与目标蛋白结合的区域,称为峰。
峰通常表示转录因子结合位点或组蛋白修饰位点。
2. Motif analysis(基序分析):对峰区域进行进一步分析,可以识别出其中的共有序列模式,称为基序。
这些基序可能与特定转录因子的结合相关,从而可以推断特定转录因子在染色质上的结合位点。
3. Differential binding analysis(差异结合分析):比较不同实验条件下的Chip-seq数据,可以发现转录因子的结合差异。
关于染色质免疫共沉淀ChIP实验原理及实验总结

关于染色质免疫共沉淀ChIP实验原理及实验总结ChIP实验原理在活细胞状态下固定蛋白质,DNA复合物,并将其随机切断为一定长度范围内的染色质小片段,然后通过免疫学方法沉淀此复合体,特异性地富集目的蛋白结合的DNA片段,通过对目的片断的纯化与检测,从而获得蛋白质与DNA相互作用的信息。
可以利用ChIP研究转录因子( transcription factor, TF)与启动子(promoter)的关联性。
由于ChIP采用甲醛固定活细胞或者组织的方法,所以能比较真实的反映细胞内TF与Promoter的结合情况。
这个优势是EMSA这个体外研究核酸与蛋白相互结合的实验方法所不能比拟的。
当用甲醛处理时,相互靠近的蛋白与蛋白,蛋白与核酸(DNA或RNA)之间会产生共价键。
细胞内,当TF与Promoter 相互结合(生物意义上的结合)时,它们必然靠的比较近,或者契合在一起,这个时候用甲醛处理,能使它们之间产生共价键。
一般ChIP的流程是:甲醛处理细胞——收集细胞,超声破碎——加入目的蛋白的抗体,与靶蛋白-DNA复合物相互结合——加入Protein A,结合抗体-靶蛋白-DNA复合物,并沉淀——对沉淀下来的复合物进行清洗,除去一些非特异性结合——洗脱,得到富集的靶蛋白-DNA复合物——解交联,纯化富集的DNA-片断——PCR 分析。
ChIP实验步骤第一天:(一)、细胞的甲醛交联与超声破碎。
1、取出1平皿细胞(10cm平皿),加入243ul 37,甲醛,使得甲醛的终浓度为1,。
(培养基共有9ml)2、37摄氏度孵育10min。
3、终止交联:加甘氨酸至终浓度为0.125M。
450ul 2.5M甘氨酸于平皿中。
混匀后,在室温下放置5min即可。
4、吸尽培养基,用冰冷的PBS清洗细胞2次。
5、细胞刮刀收集细胞于15ml离心管中(PBS依次为5ml,3ml和3ml)。
预冷后2000rpm 5min收集细胞。
6、倒去上清。
按照细胞量,加入SDS Lysis Buffer。
染色质免疫共沉淀技术ChIP介绍

染色质免疫共沉淀技术ChIP介绍
1.ChIP的分类
ChIP-Seq:将ChIP与**代测序技术相结合的技术,能够高效地在全基因组范围内检测与组蛋白、转录因子等相互作用的DNA区段。
ChIP-chip:将ChIP与DNA芯片相结合的技术,主要用于特定反式因子靶基因的高通量筛选以及组蛋白修饰和染色体重建。
RIP:RNA结合蛋白**沉淀技术,是研究细胞内RNA与蛋白质相互作用的一项技术。
主要用于研究RNA在基因表达调控中的作用。
ChIP-Re-ChIP:在次ChIP的基础上不解交联,而继续进行另一个目的蛋白的**沉淀,从而得到与两种目的蛋白都结合的DNA序列。
2.染色质免疫共沉淀测序技术优势:
检测覆盖范围广:全基因组范围内扫描目标区域;
检测分辨率高:更利于定位目标区域;
样本需要量低:需要的**沉淀后的DNA量可低至5-10ng;
可靠性好:避免了非特异性杂交,背景低;
性价比高:花费较少即可检测全基因组,获取准确丰富的信息。
3.ChIP试剂盒的选择
由于ChIP实验的操作繁琐、每一步反应需要注意的细节很多,常常需要花费实验者很长的时间才能完成整个实验,而且回收得到的DNA片段可能出现各种各样的问题。
因此,为了帮助广大科研用户解决这些问题,许多商业化的ChIP试剂盒问世。
染色质免疫共沉淀(ChIP)实验

染色质免疫共沉淀(ChIP)染色质免疫共沉淀可以:(1)组蛋白修饰酶的抗体作为“生物标记”;(2)转录调控分析;(3)药物开发研究;(4)DNA损失与凋亡分析。
1实验方法原理:在保持组蛋白和DNA联合的同时,通过运用对应于一个特定组蛋白标记的生物抗体,染色质被切成很小的片断,并沉淀下来。
IP是利用抗原蛋白质和抗体的特异性结合以及细菌蛋白质的“prorein A”特异性地结合到免疫球蛋白的FC片段的现象活用开发出来的方法。
目前多用精制的prorein A预先结合固化在argarose的beads上,使之与含有抗原的溶液及抗体反应后,beads上的prorein A就能吸附抗原达到精制的目的。
2实验材料、试剂、仪器耗材:细胞样品甲醛、甘氨酸、PBS、SDS、Lysis Buffer、洗脱液、RNaseA、蛋白酶K、omega胶回收试剂盒等离心管、超声仪、电泳仪、离心机等3实验步骤:一、细胞的甲醛交联与超声破碎(第一天)1. 取出1平皿细胞(10 cm平皿),加入243 ul 37%甲醛,使得甲醛的终浓度为1%(培养基共有9 ml)。
2. 37℃孵育10 min。
3. 终止交联:加甘氨酸至终浓度为0.125 M。
450 ul 2.5 M甘氨酸于平皿中。
混匀后,在室温下放置5 min即可。
4. 吸尽培养基,用冰冷的PBS清洗细胞2次。
5. 细胞刮刀收集细胞于15 ml离心管中(PBS依次为5 ml,3 ml和3 ml)。
预冷后2 000 rpm 5 min收集细胞。
6. 倒去上清。
按照细胞量,加入SDS Lysis Buffer。
使得细胞终浓度为每200ul含2×106个细胞。
这样每100 ul溶液含1×106个细胞。
再加入蛋白酶抑制剂复合物。
假设MCF7长满板为5×106个细胞。
本次细胞长得约为80%。
即为4×106个细胞。
因此每管加入400 ul SDS Lysis Buffer。
ChIP_原理及实验方法
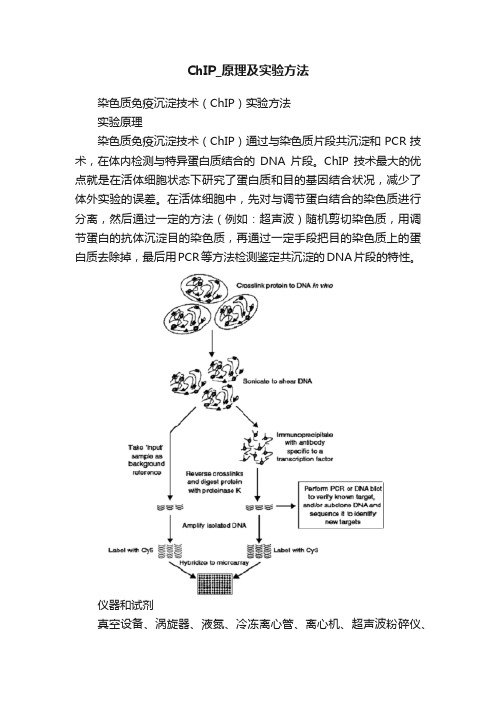
ChIP_原理及实验方法染色质免疫沉淀技术(ChIP)实验方法实验原理染色质免疫沉淀技术(ChIP)通过与染色质片段共沉淀和PCR技术,在体内检测与特异蛋白质结合的DNA片段。
ChIP技术最大的优点就是在活体细胞状态下研究了蛋白质和目的基因结合状况,减少了体外实验的误差。
在活体细胞中,先对与调节蛋白结合的染色质进行分离,然后通过一定的方法(例如:超声波)随机剪切染色质,用调节蛋白的抗体沉淀目的染色质,再通过一定手段把目的染色质上的蛋白质去除掉,最后用PCR等方法检测鉴定共沉淀的DNA片段的特性。
仪器和试剂真空设备、涡旋器、液氮、冷冻离心管、离心机、超声波粉碎仪、miracloth 37%甲醛,2M甘氨酸,ddHO,剪切的鲑精DNA/protein A琼脂糖珠(Sant cruz),2蛋白酶K(14mg/ml),RNaseA,酚:氯仿:异戊醇(25:24:1),氯仿,无水乙醇,提取缓冲液1(EB1):0.4M蔗糖;10mM Tris-HCl,pH8.0;5mM β-ME;0.1mM PMSF;蛋白酶抑制剂混合物(aprotinin、pepstain A、Leupeptin、Antipain、TPCK、Benzamidine)提取缓冲液2(EB2):0.25M 蔗糖;10mM Tris-HCl,pH8.0;10mM MgCl2;1%Triton X-100(聚乙二醇辛基苯基醚);5mM β-ME;0.1mM PMSF;蛋白酶抑制剂混合物(同上)提取缓冲液3(EB3):1.7M蔗糖;10mM Tris-HCl,pH8.0;0.15%Triton X-100;2mM MgCl;5mMβ-ME;0.1mM PMSF;蛋白酶抑制剂混合物(同上)2核裂解缓冲液(NLB):50mM Tris-HCl,pH8.0;10mM EDTA;1%SDS;PMSF和蛋白酶抑制剂混合物(同上)ChIP稀释缓冲液(ChIP DB):1.1%Triton X-100;1.2mM EDTA;16.7 mMTris-HCl,pH8.0;167mM NaCl;PMSF和蛋白酶抑制剂混合物(同上)洗脱缓冲液(EB):1%SDS;0.1M NaHCO3(现配)低盐洗脱液:150mM NaCl;0.1%SDS;1%Triton X-100;2mM EDTA;20mM Tris-HCl,pH8.0高盐洗脱液:500mM NaCl;0.1%SDS;1%Triton X-100;2mM EDTA;20mM Tris-HCl,pH8.0LiCl洗脱液:0.25M LiCl;1%NP-40;1%脱氧胆酸钠;2mMEDTA;20mM Tris-HCl,pH8.0TE缓冲液:1mM EDTA;10mM Tris-HCl,pH8.0实验方法植物材料的准备(以拟南芥为例)1.在覆盖有保鲜膜的土里播上拟南芥的种子。
染色质免疫共沉淀(ChIP)原理及注意事项

染色质免疫共沉淀(ChIP)原理及注意事项【前言】早期,人们就发现在细胞的生命活动中,DNA复制、mRNA转录与修饰以及病毒的感染等,都涉及基因-蛋白质相互作用,很多生理学家都探讨了这种现象的发生过程。
近年来,随着研究的深入,很多医学研究者已经将目光投向了基因-蛋白相互作用,期望在此水平上,另辟蹊径,深入分析癌症、心血管疾病、中央神经系统紊乱等疾病的主要代谢通路和发生机制。
染色质免疫共沉淀(ChIP)作为目前为止唯一的研究体内DNA与蛋白质相互作用的实验方法,深得人心。
很多人都希望接触和掌握此实验技术,希望从组蛋白修饰、转录调控、凋亡等角度深入研究病变机制,进而开发相应的药物。
总之,ChIP是一个有效且重要的实验技术。
下面就来聊聊它。
【正文】能够与DNA结合的蛋白有多种,主要分为组蛋白和非组蛋白。
一方面,染色体是由组蛋白和DNA构成的,组蛋白作为染色体的结构蛋白,可以与DNA形成核小体,组蛋白与DNA的结合关系是固定存在的,因此组蛋白的修饰作用成为研究的关键。
NaCl可解除组蛋白和DNA的交联关系。
(核小体结构图)另一方面,非组蛋白多是参与DNA复制、mRNA转录过程的一些功能蛋白,包括解链酶、切割酶、转录激活蛋白等等,它们与DNA、mRNA的结合关系是瞬时的,发挥完作用可能就及时脱离开了。
ChIP实验原理:在活细胞状态下,通过甲醛固定DNA-蛋白质复合物后,采用微球菌核酸酶(Micrococcal Nucleas)(注:早期使用的超声已经被淘汰了,不推荐使用)随机切断DNA,形成一个个一定长度范围内的染色质小片段,随后通过抗原-抗体特异性结合反应富集、沉淀这些小片段,然后通过对NaC、蛋白酶K解除蛋白质和DNA的交联,分离蛋白,纯化DNA,最后采用PCR检测DNA的序列信息,获取更多信息。
从上面的原理就可以看出,ChIP实验步骤大致可分5步:(1)1%甲醛处理使蛋白质与 DNA 交联;(2)细胞裂解,采用微球菌核酸酶消化形成染色质小片段;(3)抗原-抗体反应,促进免疫沉淀反应;(4)NaCl、蛋白酶 K 处理,解除DNA-蛋白交联;(5)DNA 纯化回收;(6)采用1.8%琼脂糖凝胶电泳、RT-PCR对DNA作进一步分析。
chip原理及实验方法

C h I P原理及实验方法本页仅作为文档封面,使用时可以删除This document is for reference only-rar21year.March染色质免疫沉淀技术(ChIP)实验方法实验原理染色质免疫沉淀技术(ChIP)通过与染色质片段共沉淀和PCR技术,在体内检测与特异蛋白质结合的DNA片段。
ChIP技术最大的优点就是在活体细胞状态下研究了蛋白质和目的基因结合状况,减少了体外实验的误差。
在活体细胞中,先对与调节蛋白结合的染色质进行分离,然后通过一定的方法(例如:超声波)随机剪切染色质,用调节蛋白的抗体沉淀目的染色质,再通过一定手段把目的染色质上的蛋白质去除掉,最后用PCR等方法检测鉴定共沉淀的DNA片段的特性。
仪器和试剂真空设备、涡旋器、液氮、冷冻离心管、离心机、超声波粉碎仪、miracloth 37%甲醛,2M甘氨酸,ddH2O,剪切的鲑精DNA/protein A琼脂糖珠(Sant cruz),蛋白酶K(14mg/ml),RNaseA,酚:氯仿:异戊醇(25:24:1),氯仿,无水乙醇,提取缓冲液1(EB1):0.4M蔗糖;10mM Tris-HCl,;5mM β-ME;0.1mM PMSF;蛋白酶抑制剂混合物(aprotinin、pepstain A、Leupeptin、Antipain、TPCK、Benzamidine)提取缓冲液2(EB2):0.25M 蔗糖;10mM Tris-HCl,;10mM MgCl2;1%Triton X-100(聚乙二醇辛基苯基醚);5mM β-ME;0.1mM PMSF;蛋白酶抑制剂混合物(同上)提取缓冲液3(EB3):1.7M蔗糖;10mM Tris-HCl,;%Triton X-100;2mM MgCl2;5mMβ-ME;0.1mM PMSF;蛋白酶抑制剂混合物(同上)核裂解缓冲液(NLB):50mM Tris-HCl,;10mM EDTA;1%SDS;PMSF和蛋白酶抑制剂混合物(同上)ChIP稀释缓冲液(ChIP DB):%Triton X-100;1.2mM EDTA;16.7 mM Tris-HCl,;167mM NaCl;PMSF和蛋白酶抑制剂混合物(同上)洗脱缓冲液(EB):1%SDS;0.1M NaHCO3(现配)低盐洗脱液:150mM NaCl;%SDS;1%Triton X-100;2mM EDTA;20mM Tris-HCl,高盐洗脱液:500mM NaCl;%SDS;1%Triton X-100;2mM EDTA;20mM Tris-HCl,LiCl洗脱液:0.25M LiCl;1%NP-40;1%脱氧胆酸钠;2mM EDTA;20mM Tris-HCl,TE缓冲液:1mM EDTA;10mM Tris-HCl,实验方法植物材料的准备(以拟南芥为例)1.在覆盖有保鲜膜的土里播上拟南芥的种子。
