常用酸碱试剂的浓度与相对密度(20℃)
盐酸、硫酸、液碱、次氯酸钠的应急预案

事故应急救援预案(盐酸、硫酸、液碱、次氯酸钠)一、目的为了更加有效地处置工作过程中酸碱泄漏事件。
防止由此引发的爆炸、中毒、烫伤、化学品灼伤、环境污染等种类事故的发生,保证生产和员工人身安全,特制定本预案。
二、适用范围本预案适用于本部门内工作环节中一旦发生泄漏,即可能对生产、员工人身安全和环境安全构成威胁的酸、碱。
三、事故处置程序1、四、化学品种类及特性1、硫酸硫酸分子量98.08,相对密度 1.83(95.0~98.0%),纯品无色。
是一种强酸。
在空气中白色的雾,产生许多液体水合物。
健康危害侵入途径:吸入、食入。
? 健康危害:对皮肤、粘膜等组织有强烈的刺激和腐蚀作用。
对眼睛可引起结膜炎、水肿、角膜混浊,以致失明;引起呼吸道刺激症状,重者发生呼吸困难和肺水肿;高浓度引起喉痉挛或声门水肿而死亡。
口服后引起消化道的烧伤以至溃疡形成。
严重者可能有胃穿孔、腹膜炎、喉痉挛和声门水肿、肾损害、休克等。
慢性影响有牙齿酸蚀症、慢性支气管炎、肺气肿和肺硬化。
毒性:属中等毒性。
危险特性:与易燃物(如苯)和有机物(如糖、纤维素等)接触会发生剧烈反应,甚至引起燃烧。
能与一些活性金属粉末发生反应,放出氢气。
遇水大量放热,可发生沸溅。
具有强腐蚀性。
?? 燃烧(分解)产物:氧化硫。
2、盐酸盐酸分子量36.46,相对密度 1.19(37~38%)、1.15(30%)、1.13(25%),氯化氢的水溶液,纯品无色,因含杂质而呈黄色。
商品浓盐酸含氯化氢37~38%,是一种强酸。
除金、银、铂、铌和某些金属外,盐酸能溶解大多数金属。
强氧化剂能氧化盐酸生成氯。
工业盐酸中含有砷杂质。
在空气中白色的雾,产生许多液体水合物。
与氯化物接触立即产生剧毒气体氰化氢。
空气最高容许浓度 15mg/m3中毒表现:患者可感到头痛、头昏、恶心、眼部刺痛、羞明流泪、咽喉灼痛、声音嘶哑、咳嗽(有时痰中带血)、呼吸困难、胸闷、胸痛。
检查可见眼结膜、鼻、咽部粘膜红肿,角膜混浊,两肺可有散在干罗音,严重者可有肺水肿表现。
常用化学品安全操作说明书(硫酸碱液盐酸三氯化铁次氯酸钠焦亚硫酸钠片碱硫酸铝)

常用化学品安全操作说明书1、硫酸2、碱液3、盐酸4、三氯化铁5、次氯酸钠6、焦亚硫酸钠7、聚丙烯酰胺(PAM)8、片碱9、硫酸铝10、氩气一、浓硫酸分类与特性概述:外观及性状:纯品为无色油状液体,工业品因含杂呈黄色或棕色,无味。
中文名浓硫酸分子式H2SO4相对分子质量98.07CAS号7664-93-9危险性类别:8.1 类强酸性腐蚀品侵入途径:吸入、食入、皮肤接触。
最高容许浓度:车间空气中有害物质的最高容许浓度2mg/m3健康危害:刺激鼻、喉,引起打喷嚏、肺水肿、支气管粘膜发火、气阻、胸痛、呼吸短促、鼻和牙床出血,严重时灼伤鼻、口,引起肺水肿、慢性肺炎、皮炎,并灼痛眼睛,引起角膜损伤,甚至失明;过量食入导致流涎,极度口渴、吞咽困难、休克、牙龈损害、口腔、咽喉、胃及食管烧伤、恶心、呕吐物有咖啡粒状物、胃肠穿孔,肾损害;长期暴露症状相同甚至更严重。
危险特性 与碱发生中和反应并放热。
具有强烈的吸水性能和氧化性,对水猛烈结合放出大 量热。
对棉麻织物、木材、纸张等碳水化合物因脱水而炭化。
二、浓硫酸储存条件及方式:存在密闭容器中,置于凉爽、干燥、通风处,避免接触氯酸盐、铬酸盐、碳化物、雷酸盐、硝酸盐,金属粉未;防水,避免光照;储存区地面应为耐酸、耐腐蚀的坚固水泥地面,严禁烟火;储存处应使用防爆电器设备;禁用金属容器储存 三、使用时的注意事项:操作人员必须经过上岗培训,严格遵守操作规程和操作卡。
严禁烟火;戴防护镜,穿防护服;选用适当呼吸器。
避免与碱性物质和水接触。
搬运时要轻装轻卸,防止包装及容器损坏。
配备泄漏应急处理设备。
倒空的容器可能残留有害物。
稀释或制备溶液时,应严格遵守在搅拌下将硫酸缓慢加入水中,以免沸腾和飞溅。
工程控制 密闭操作。
提供安全淋浴和洗眼设备。
呼吸系统防护 可能接触其粉尘时,必须佩戴头罩型电机动送风过滤式 呼吸器。
必要时,佩戴空气呼吸器。
眼睛防护:戴化学安全防护面罩。
身体防护 穿耐酸碱橡胶皮靴,穿工作服(防腐材料制作)。
SDS溶液(20%,pH7.2)
北京雷根生物技术有限公司
SDS 溶液(20%,pH7.2)
简介:
SDS 即Sodium dodecyl sulfate ,中文名为十二烷基磺酸钠,也称十二烷基硫酸钠。
SDS solution(20%,pH7.2)是生化试剂,用途广泛,可以用于SDS-PAGE 、细菌碱裂解等。
组成:
操作步骤(仅供参考):
1、根据具体实验要求操作。
注意事项:
1、 如遇环境温度较低,溶液易产生沉淀,可以温浴加热促溶。
2、 Leagene SDS 溶液对人体有一定刺激性,请注意防护。
3、 为了您的安全和健康,请穿实验服并戴一次性手套操作。
有效期: 12个月有效。
相关:
编号 名称 R00171 Storage SDS solution(20%,pH7.2) 100ml RT 使用说明书 1份
编号 名称 CC0005 磷酸缓冲盐溶液(1×PBS,无钙镁) DC0032 Masson 三色染色液 IH0143
PBS 磷酸盐缓冲液(0.1mol/L,pH7.2-7.4) PE0080
Tris-HCl 缓冲液(1mol/L,pH6.8) PT0013
考马斯亮蓝快速染色液 PW0040
Western blot 一抗稀释液 TO1013 丙二醛(MDA)检测试剂盒(TBA 比色法)。
常用酸碱浓度表

盐酸 HCl 质量 百分数 1 2 4 6 8 10 12 14 16 18 20
20 密度 d 4 / g.cm-3
100mL 水溶 液中含 HCl/g
HCl 质量 百分数 22 24 26 28 30 32 34 36 38 40
20 密度 d 4 / g.cm-3
100mL 水溶液 中含 HCl/g
1.004 2.018 3.044 4.080 5.128 10.54 16.26 22.30 28.67 35.40 42.49 49.85 57.52 65.50 73.66 82.00
1.3931 1.4134 1.4337 1.4521 1.4686 1.4826 1.4850 1.4873 1.4892 1.4912 1.4932 1.4952 1.4974 1.5008 1.5056 1.5129
氢氧化钠
NaOH 质 量百分数 1 2 4 6 8 10 12 14 16 18 20 22 24
20 密度 d 4 / g.cm-3
100mL 水溶液 中含 NaOH/g
NaOH 质 量百分数 26 28 30 32 34 36 38 40 42 44 46 48 50 碳酸钠
20 密度 d 4 / g.cm-3
100mL 中 游离 SO3/g
1.860 1.865 1.870 1.875 1.880 1.885 1.890 1.895
2.8 5.0 8.0 10.2 12.1 13.7 15.4 17.7
1.900 1.905 1.910 1.915 1.920 1.925 1.930 1.935
19.1 20.1 21.8 25.5 30.6 35.9 41.2 49.6
255种国标试剂

255种国标试剂255种国标试剂是一种广泛应用于化学实验室和科研领域的试剂,它们具有多种不同的化学成分和用途。
这些试剂的使用范围广泛,可以用于分析、合成、测定和检测等多个实验过程。
本文将从几个不同的角度介绍一些常见的国标试剂以及它们的特点和用途。
一、氢氧化钠(NaOH)氢氧化钠是一种强碱性试剂,常用于酸碱中和反应和沉淀反应中。
它具有腐蚀性,需小心操作,避免接触皮肤和眼睛。
二、盐酸(HCl)盐酸是一种强酸性试剂,常用于酸碱中和反应和沉淀反应。
它具有刺激性气味,需在通风良好的环境下操作。
三、硫酸(H2SO4)硫酸是一种常用的酸性试剂,具有强酸性和强腐蚀性。
它常用于酸碱中和反应、氧化还原反应和沉淀反应中。
在操作时需小心防护,避免与皮肤和眼睛接触。
四、氯化银(AgCl)氯化银是一种无机盐,常用于沉淀反应中。
它具有白色固体的外观,溶于浓盐酸和氨水。
氯化银可用于银离子的检测和分析。
五、硫酸铜(CuSO4)硫酸铜是一种常用的无机盐,常用于溶液的制备和氧化还原反应中。
它具有蓝色结晶的外观,可用于铜离子的检测和分析。
六、氯化钾(KCl)氯化钾是一种常用的无机盐,常用于溶液的制备和沉淀反应中。
它具有白色结晶的外观,可用于钾离子的检测和分析。
七、硫酸钠(Na2SO4)硫酸钠是一种常用的无机盐,常用于溶液的制备和沉淀反应中。
它具有无色结晶的外观,可用于钠离子的检测和分析。
八、硝酸(HNO3)硝酸是一种常用的无机酸,具有强氧化性和强腐蚀性。
它常用于氧化反应和酸碱中和反应中。
在操作时需小心防护,避免与皮肤和眼睛接触。
九、醋酸(CH3COOH)醋酸是一种常用的有机酸,常用于酸碱中和反应和沉淀反应中。
它具有刺激性气味,需在通风良好的环境下操作。
255种国标试剂涵盖了各种常见的无机盐和有机酸碱,它们在化学实验和科研中扮演着重要的角色。
合理使用这些试剂,遵守操作规程和安全要求,可以确保实验的准确性和安全性。
希望本文对读者对国标试剂有所了解,并能正确使用它们进行实验。
化工化学试剂使用指南

乙酸乙酯乙酸乙酯(ethyl acetate)又称醋酸乙酯。
分子式C4H8O2,相对分子质量为88.11。
结构式为:物化性能无色透明有芳香气味的液体。
熔点-83.6℃。
沸点77.06℃。
相对密度(d420)0.902。
折射率(d420)1.3719。
闪点-3℃。
自燃温度426℃。
在空气中爆炸极限2.2%~9%。
溶于氯仿,乙醇、乙醚,微溶于水。
与水形成沸点为70.4℃的共沸物,与乙醇形成沸点为71.8℃的共沸物。
蒸气压73×133.3Pa(20℃)。
主要用途是重要的香料添加剂,可用作调香的组分,还可用作为特殊改性酒精的香味萃取剂。
是一种极发了的工业溶剂,可用于硝酸纤维、乙基纤维、氯化橡胶和乙烯基树脂、乙酸纤维素酯、纤维素乙酯丁酯和合成橡胶,也可用于复印机用液体硝基纤维墨水。
可用作粘接剂的溶剂,喷漆的稀释剂。
是制造染料及药物的原料。
实验室制法将装有25mL乙醇的250mL圆底烧瓶置于冰水冷却下,缓慢加入25mL浓硫酸。
烧瓶口通过塞子装上一分液漏斗,其下端浸入液体中,同时在塞子上再插一个与直形冷凝管相连接的弯玻管。
将烧瓶置油浴上加热至140℃,并于此温度下滴加200mL乙醇和200mL乙酸混和物,其滴加速度和蒸出速度相同。
反应持续6h。
馏出液用2% Na2CO3溶液中和,然后与50g CaCl2和50mL水溶液振荡,用30g无水CaCl2干燥24h,然后蒸馏提纯乙酸乙酯(77℃),产量约205g,产率67%。
生产原理工业上用硫酸为催化剂,使乙酸与乙醇发生酯化反应。
工艺流程原料配比(kg/t)乙酸(98%) 610乙醇(95%) 615硫酸(95%) 4主要设备酯化釜洗涤锅过滤器精馏釜(精馏塔) 分液器贮槽操作工艺将400kg乙酸、375kg乙醇、3kg浓硫酸加入到搪瓷反应釜中,搅拌、加热、回流6h,将釜中的粗乙酸乙酯蒸出放到水洗锅中,用配制的5%氯化钠溶液洗涤,再用氢氧化钠和氯化钠的混和水溶液调节锅内物料的pH值为8。
酸碱指示剂的酸碱度范围选择和溶液浓度

酸碱指示剂的酸碱度范围选择和溶液浓度酸碱指示剂是一种常用于酸碱滴定反应中的物质,它可以通过改变颜色来指示溶液的酸碱性质。
在进行滴定实验时,选择合适的酸碱指示剂是十分重要的,因为它能够准确地反映溶液的酸碱度范围和浓度。
本文将探讨酸碱指示剂的酸碱度范围选择和溶液浓度对实验结果的影响。
酸碱指示剂的酸碱度范围选择是根据其酸碱性质和PH范围来确定的。
常见的酸碱指示剂有苏丹红、溴酚蓝、甲基橙等,它们分别对应着酸性、中性和碱性溶液。
首先是苏丹红,它是一种酸性指示剂,可以将酸性溶液的颜色变为红色。
苏丹红的酸碱度范围为PH 0-3,因此适用于酸性溶液的滴定实验。
对于酸碱中性或碱性溶液,苏丹红的指示效果较差。
其次是溴酚蓝,它是一种中性指示剂,会使中性溶液的颜色变为蓝色。
溴酚蓝的酸碱度范围为PH 6.0-7.6,因此适用于中性溶液的滴定实验。
对于酸性或碱性溶液,溴酚蓝的指示效果较差。
最后是甲基橙,它是一种碱性指示剂,可以将碱性溶液的颜色变为橙色。
甲基橙的酸碱度范围为PH 3.1-4.4,因此适用于碱性溶液的滴定实验。
对于酸性或中性溶液,甲基橙的指示效果较差。
除了酸碱度范围的选择,溶液浓度也对酸碱指示剂的使用产生影响。
一般来说,指示剂在浓度较低的溶液中呈现出较明显的颜色变化,而在浓度较高的溶液中颜色变化较为模糊。
例如,在进行酸碱滴定实验时,如果溶液浓度过高,就会导致指示剂颜色变化不明显,难以准确判断等价点。
因此,在实验中应当尽可能使用相对较低浓度的溶液,以确保可观察到明显的颜色变化。
此外,酸碱指示剂的选择还应考虑其化学稳定性和溶解性。
指示剂应具有良好的稳定性,不易受到光、热或其他因素的影响而发生变化。
溶解性也是一个重要的考虑因素,以确保指示剂能够充分溶解在溶液中,不会出现沉淀现象。
综上所述,选择合适的酸碱指示剂对于酸碱滴定实验的准确性和可靠性至关重要。
在选择酸碱指示剂时,应根据需求确定所需的酸碱度范围,并考虑溶液的浓度、化学稳定性和溶解性等因素。
实验室常用的酸碱和基本特性

名称 化学式 含量 基本性质
氟硼酸 HBF4 40% 常压沸点为 130℃(分解),在密闭容器中不需要高压就能获得比氢氟酸更 高的温度,且酸不分解。特别适宜消解那些需要分解硅酸盐和需高温条件 的含有无机基体的样品。 适用范围 硅酸盐,地质样品 名称 化学式 含量 基本性质 王水 HCl:HNO3 3:1 沸点 112℃,在 0.7MPa 下温度可达 145℃。一种有效的氧化剂,能产生氯 化亚硝酰。王水需现配现用。王水可用来溶解许多金属和合金,也可从硅 酸盐基质中酸洗出部分金属,但无法有效的加以完全溶解。除王水外,硝 酸和盐酸还常以另外的比例混合在一起使用,所谓的乐福特王水,也叫逆 王水,是三份硝酸与一份盐酸的混合物。常用来溶解氧化硫和黄铁矿。 适用范围 适用于无机物,特别是金矿、铂矿,快速分解硫化物、砷化物、硒化物以 及锑氧化物;也常用此消化废水,植物样品。
实验室常用酸/碱的配制和基本特性
名称 化学式 含量 基本性质 浓硝酸 HNO3 65%~70% 常压下的沸点为 120℃。在 0.5MPa 下温度可达 176℃,它的氧化电位显著 增大,氧化性增强。能对无机物及有机物进行氧化作用。金属和合金可用 硝酸氧化为相应的硝酸盐,这些硝酸盐通常易溶于水。部分金属元素,如 Au、Pt、Nb、Ta、Zr 不被溶解。Al 和 Cr 不易被溶解。硝酸可溶解大部分 的硫化物。 适用范围 食品、化妆品及生物组织样品的首选用酸。广泛用于消解有机样品,如饮 料、碳水化合物、植物试样、工业废水、糖果、各类调味品、蛋白质、淀 粉、油脂、酒类、生活垃圾、一些颜料和有机聚合物等;常用消化易溶于 硝酸的金属元素和化合物;也可酸洗土壤、沉积物等;含量高的发烟硝酸 适宜消解极难分解的高碳量的试样。 名称 化学式 含量 基本性质 浓盐酸 HCl 36%~38% 常压沸点为 108℃,在 0.7MPa 下温度可达 140℃,HCl 不属于氧化剂,通 常不用来消解有机物。HCl 在高压与较高温度下可与许多硅酸盐及一些难 溶氧化物、硫酸盐、氟化物作用,生成可溶性盐。 溶解弱酸性的盐类:碳酸盐、磷酸盐、硅酸盐和无机氧化物(如 Fe 系氧化 物),以及比氢更容易还原的金属或合金(如 Al);对于水溶液中的胺和 生物碱与某些有机金属化合物,也是一种良好的溶剂;将其同硝酸联合使 用,应用更加广泛。
常用酸碱指示剂配制

常用酸碱指示剂配制注:下列70余种指示剂按pH变色域由小到大顺序排列。
圆括号中列出的是其pH变色域。
左边系酸型色,右边系碱型色。
变色pH域可因观察者对颜色敏感程度不同而存在差异,它还受离子强度、温度、溶剂等因素影响,因而列出的数据为近似值。
配制下列指示剂凡是用0.02 mol/L及0.05 mol/L氢氧化钠溶液或乙醇溶解的,应将指示剂全部溶解后,然后稀释至—定的体积。
所用乙醇均指95%(体积分数)乙醇,应呈中性。
苦昧酸(三硝基苯酚)(无色0.0—1.3黄) 0.10 g溶于100 mL水。
结晶紫(龙胆紫)(绿0.0—2.0紫) 0.20 g溶于100 mL水。
孔雀绿(黄0.0—2.0绿) 0.3 g溶于100 mL冰乙酸。
《说明》孔雀绿的第二变色域是:绿11.0~13.5无色。
亮绿(黄0.0—2.6绿) 0.5 g溶于100 mL冰乙酸。
甲基紫(黄0.1—1.5蓝) 0.25 g溶于l00 mL水。
《说明》甲基紫的第二pH变色域是:蓝1.5~3.2紫。
每100 mL滴定液加3~5滴。
邻甲酚红(红0.2—1.8黄) 0.05~0.1 g溶于l00 mL 20%乙醇。
《说明》邻甲酚红第二pH变色域是:黄7.2—8.8红紫。
间胺黄(红1.2—2.3黄) 0.5 g溶于100 mL水。
《说明》每l00 mL滴定液加3~5 mL。
间甲酚紫(红1.2—2.8黄) 0.1 g溶于13.6 mL0.02 mol/L氢氧化钠中,用水稀释至250 mL。
对二甲苯酚蓝(红1.2—2.8黄) 0.10 g溶于250 mL乙醇。
百里(香)酚蓝(麝香草酚蓝)(红1.2— 2.8黄) ①0.10g溶于10.75 mL0.02 mol /L氢氧化钠中,用水稀释至250 mL。
②0.1 g溶于4.3 mL 0.05 mol/L氢氧化钠中,用水稀释至200 mL。
《说明》百里酚蓝第二变色域:黄8.0—9.6紫蓝。
《说明》每l00 mL滴定液加1~3滴。
实验室常用试剂缓冲液配制方法一览表

实验常用试剂、缓冲液的配制方法1、1M Tris-HCl□组份浓度1 M Tris-HCl(pH7.4,7.6,8.0)□配制量1L□配置方法1. 称量121.1gTris置于1L烧杯中。
2. 加入约800mL的去离子水,充分搅拌溶解。
3. 按下表量加入浓盐酸调节所需要的pH值。
pH值浓HCl7.4 约70mL7.6 约60mL8.0 约42mL4. 将溶解定容至1L。
5. 高温高压灭菌后,室温保存。
注意:应使溶液冷却至室温后再调定pH值,因为Tris溶液的pH 值随温度的变化差很大,温度每升高1℃,溶液的pH值大约降低0.03个单位。
2、1.5 M Tris-HCl□组份浓度1.5 M Tris-HCl(pH8.8)□配制量1L□配置方法1.称取181.7gTris置于1L烧杯中。
2. 加入约800mL的去离子水,充分搅拌溶解。
3. 用浓盐酸调pH值至8.8。
4. 将溶液定容至1L。
5. 高温高压灭菌后,室温保存。
注意:应使溶液冷却至室温后再调定pH值,因为Tris溶液的pH值随温度的变化差异很大,温度每升高1℃,溶液的pH值大约降低0.03个单位。
3、10×TE Buffer□组份浓度100 mM Tris-HCl,10 mM EDTA (pH 7.4,7.6,8.0)□配制量1L□配置方法1. 量取下列溶液,置于1L烧杯中。
1 M Tris-HCl Buffer(pH7.4,7.6,8.0)100mL500 mM EDTA(pH8.0)20mL2. 向烧杯中加入约800mL的去离子水,均匀混合。
3. 将溶液定至1L后,高温高压灭菌。
4. 室温保存。
4、3 M 醋酸钠□组份浓度3 M 醋酸钠(pH5.2)□配制量100mL□配置方法1. 称取40.8gNaOAc•3H2O置于100~200mL烧杯中,加入约40mL的去离子水搅拌溶解。
2. 加入冰乙酸调节pH值至5.2。
3. 加入去离子水将溶液定容至100mL。
2024年高考化学实验常用试剂性质总结

2024年高考化学实验常用试剂性质总结一、酸碱中和反应试剂性质总结:1. 盐酸(HCl):性质:无色液体,有刺激性气味,易溶于水,能与金属反应产生氢气。
主要用途:用于测试金属的活动性、进行酸碱中和反应等。
2. 硫酸(H2SO4):性质:无色液体,有强烈的腐蚀性,能吸湿,可溶于水,具有酸性,加热时能发生分解反应。
主要用途:用于制备酸性溶液、进行酸碱中和反应等。
3. 碳酸氢钠(NaHCO3):性质:白色结晶粉末,具有碱性,能与酸发生中和反应,能释放出二氧化碳气体。
主要用途:用于中和酸性溶液、进行气体的产生与收集等。
4. 氢氧化钠(NaOH):性质:固体为白色结晶体,吸湿性强,具有碱性,溶于水时会产生热,具有腐蚀性。
主要用途:用于制备碱性溶液、进行酸碱中和反应等。
5. 苯酚(C6H6O):性质:无色结晶体,有刺激性气味,溶于醇、醚等有机溶剂,能与稀碱溶液发生酸碱中和反应。
主要用途:用于酸碱中和反应、制备酚酞指示剂等。
二、氧化还原反应试剂性质总结:1. 高锰酸钾(KMnO4):性质:紫红色结晶,能被还原剂还原,在酸性溶液中能氧化有机物,酸性溶液下加热可分解放氧气。
主要用途:用作氧化剂,进行氧化还原反应等。
2. 硫酸亚铁(FeSO4):性质:蓝色结晶或绿色晶体,具有还原性,能够还原高锰酸钾等氧化剂。
主要用途:用作还原剂,参与氧化还原反应等。
3. 硫酸铜(CuSO4):性质:蓝色结晶,具有氧化性,能作为强氧化剂氧化还原反应中的还原剂。
主要用途:用作还原剂,参与氧化还原反应等。
4. 氢氧化钾(KOH):性质:白色结晶粉末,有吸湿性,具有强碱性,可溶于水,能与酸反应产生中和反应。
主要用途:用作氧化剂或还原剂,参与氧化还原反应等。
三、沉淀反应试剂性质总结:1. 氯化银(AgCl):性质:白色结晶粉末,不溶于水,微溶于浓盐酸,溶于氨水,阳离子(Ag+)和阴离子(Cl-)结合产生的沉淀是白色的。
主要用途:用于检测氯离子的存在,进行有机物的沉淀反应等。
亚硫酸氢钠安全技术说明书

亚硫酸氢钠安全技术说明书第一部分:化学品名称化学品中文名称:亚硫酸氢钠化学品俗名:酸式亚硫酸钠化学品英文名称:hydrogen sulfite sodium第二部分:成分/组成信息有害物成分含量亚硫酸氢钠≥40%第三部分:危险性概述侵入途径:吸入、食入、经皮吸收。
健康危害:对皮肤、眼、呼吸道有刺激性,可引起过敏反应。
可引起角膜损害,导致失明。
可引起哮喘;大量口服引起恶心、腹痛、腹泻、循环衰竭、中枢神经抑制。
环境危害:对环境有危害,对水体可造成污染。
燃爆危险:本品不燃,具腐蚀性,可致人体灼伤。
第四部分:急救措施皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗。
就医。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。
就医。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
食入:饮足量温水,催吐。
就医。
第五部分:消防措施危险特性:具有强还原性。
接触酸或酸气能产生有毒气体。
受高热分解放出有毒的气体。
具有腐蚀性。
有害燃烧产物:氧化硫、氧化钠。
灭火方法:尽可能将容器从火场移至空旷处。
喷水保持火场容器冷却,直到灭火结束。
第六部分:泄漏应急处理应急处理:隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘口罩,穿防酸服。
不要直接接触泄漏物。
小量泄漏:避免扬尘,小心扫起,收集于干燥、洁净、有盖的容器中。
大量泄漏:收集回收或运至废物处理场所处置。
第七部分:操作处置与储存操作注意事项:密闭操作,局部排风。
防止粉尘释放到车间空气中。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿橡胶耐酸碱服,戴橡胶耐酸碱手套。
避免产生粉尘。
避免与氧化剂、酸类、碱类接触。
配备泄漏应急处理设备。
倒空的容器可能残留有害物。
储存注意事项:储存于阴凉、通风的库房。
远离火种、热源。
防止阳光直射。
包装密封。
应与氧化剂、酸类、碱类分开存放,切忌混储。
锰的化合物有哪些

锰的化合物有哪些锰的化合物主要有氧化物、氢氧化物、锰盐等三大类。
一、锰的氧化物锰的氧化物主要有一氧化锰(MnO)、二氧化锰(MnO2)、三氧化二锰(Mn203)、四氧化三锰(Mn3O4)、亚锰酸酐(Mn2O5)、锰酸酐(Mn03)和高锰酐(Mn2O7).Mn2O5和MnO3不能以游离状态存在,只能以亚锰基和锰酸基形式存在。
自然界中最常见的锰的氧化物有软锰矿(MnO2)、硬锰矿(mMnO·MnO2·nH20)、偏锰酸矿(MnO2·nH2O)、水锰矿[MnO2·Mn(OH)2]、褐锰矿(Mn203)、黑锰矿等。
含锰天然氧化物见表1。
表1 含锰天然氧化物MnO,Mn203,Mn304,MnO2等不溶于水,锰的各种氧化态,随氧化价的升高,碱性减弱,酸性增强,低价的MnO,Mn2O3属碱性;4价的MnO2属中性;高价的MnO3,Mn207为酸性。
(一)一氧化锰一氧化锰又称为氧化亚锰(MnO),分子量70.94,呈草绿色或灰绿色粉末,为碱性氧化物,在空气中易氧化,在大气中加热至不同温度时可以生成Mn304,Mn203,MnO2.常温下不溶于水,易溶于酸而生成玫瑰色的二价锰盐。
结晶水合物和Mn2+盐溶液的玫瑰色是因为存在[Mn(H20)6]2+离子的缘故。
MnO密度为5.43~5.46g/cm3,硬度为5~6,熔点1784℃.Mn0主要用于生产硫酸锰,因为生产硫酸锰的主要原料是软锰矿(Mn02),MnO2不溶于稀酸,必须预先还原成MnO。
纯度较高和重金属离子含量低的MnO可直接用于作肥料和饲料添加剂。
工业上生产MnO的方法主要是在回转窑或反射炉加碳还原软锰矿粉制得,也有报导可在多层移动炉、沸腾炉生产。
除采用软锰矿外还可用Mn(OH)2和MnCO3在隔绝空气条件下加热制得。
(二)四氧化三锰(Mn304)Mn304矿物学中又称之为黑锰矿,分子量228.82,理论含锰量72.03%,离子结构为Mn2+[Mn23+]O4,复合分子式为MnO·Mn203,属四方(斜方)晶系,是普通尖晶石结构。
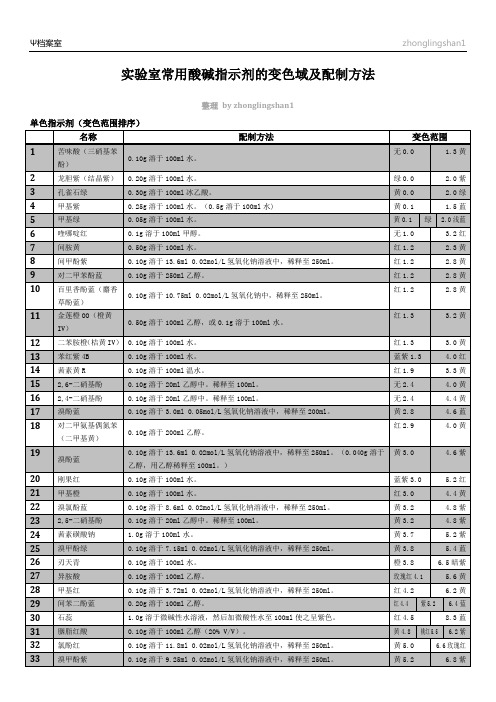
实验室常用酸碱指示剂的变色域及配制方法
无5.6
7.4黄
37
松色素
1.0g溶于乙醇。
无5.8
7.8红紫
38
溴百里香酚蓝(溴麝香草酚蓝)
0.10g溶于8.0ml 0.02mol/L氢氧化钠溶液中,稀释至250ml。
黄6.0
7.6蓝
39
儿茶酚紫
0.10g溶于100ml水。
黄6.0
7.0紫
40
姜黄
饱和水溶液。
黄6.0
13
苯红紫4B
0.10g溶于100ml水。
蓝紫1.3
4.0红
14
茜素黄R
0.10g溶于100ml温水。
红1.9
3.3黄
15
2,6-二硝基酚
0.10g溶于20ml乙醇中。稀释至100ml。
无2.4
4.0黄
16
2,4-二硝基酚
0.10g溶于20ml乙醇中。稀释至100ml。
无2.4
4.4黄
17
溴酚蓝
0.10g溶于3.0ml 0.05mol/L氢氧化钠溶液中,稀释至200ml。
黄2.8
4.6蓝
18
对二甲氨基偶氮苯(二甲基黄)
0.10g溶于200ml乙醇。
红2.9
4.0黄
19
溴酚蓝
0.10g溶于13.6ml 0.02mol/L氢氧化钠溶液中,稀释至250ml。(0.040g溶于乙醇,用乙醇稀释至100ml。)
黄3.0
4.6紫
20
刚果红
0.10g溶于100ml水。
蓝紫3.0
5.2红
1
13*
2g/L甲基红乙醇溶液
1
红紫
不明显蓝色
