肺癌分期第八版
肺癌TNM第八版分类中文版

辅助治疗
在手术后,患者可能需要接受化疗 或放疗等辅助治疗,以杀死可能残 留的癌细胞。
局部治疗
对于无法手术的患者,可以采用局 部治疗的方式,如放疗或射频消融 等。
第三期治疗策略
综合治疗
化疗
对于第三期的肺癌患者,通常采用综合治疗 的方式,包括化疗、放疗和免疫治疗等。
第三期的患者通常需要接受多程的化疗。
第三期(t1n2m0,t2n1m0,t3n0m0)
要点一
总结词
要点二
详细描述
生存期更短,预后更差。
T1是指肿瘤最大径线≤3cm,未侵犯周围组织。N2是 指肿瘤侵犯淋巴结,但未侵犯远处组织。M0是指无远 处转移。T2是指肿瘤侵犯周围组织,但未侵犯肺叶。 N1是指肿瘤侵犯淋巴结,但未侵犯远处组织。M0是指 无远处转移。T3是指肿瘤侵犯肺叶或周围组织,但未 侵犯胸膜或纵膈。N0是指无淋巴结转移。M0是指无远 处转移。
tnm分期的历史与发展
TNM分期最初由美国癌症联合会(AJCC)提出,经过多次修订和完善,目前已 经发展到第八版。
随着医学技术的不断进步,TNM分期也在不断改进和完善,以更好地满足临床需 求。
新版的TNM分期更加注重病理学诊断和分子标志物在分期中的价值,以提供更准 确的预后评估和治疗方案建议。
02
第四期(任何t,任何n,m1)
总结词
最晚期的肺癌,生存期最短,预后最差。
详细描述
任何T是指无论肿瘤大小、侵犯范围等。任何N是指无论淋巴 结转移情况如何。M1是指已发现远处转移。
04
tnm分期与治疗策略
第一期治疗策略
01
02
03
手术治疗为主
对于第一期的肺癌患者, 通常建议进行手术治疗, 以切除肿瘤并清除周围的 淋巴结。
肺癌TNM第8版分类中文版

肺上沟癌
下一例为不能手术切除的肺上沟癌,增强 矢状位T1WI图
臂丛明显受累(白箭),锁骨下动脉包绕 (A)
N分期
区域淋巴结分级系统 淋巴结分期依据美国胸科协会绘制模式图进行。 锁骨上淋巴结群: 1、下颈部、锁骨上和胸骨隐窝淋巴结 上纵隔淋巴结群: 2、上段气管旁:主动脉弓以上,锁骨以下 3A、血管前:不包括第2站,即非气管临近的血管前淋巴结 3P、椎体前:非气管临近的、食管后椎体前的淋巴结 下纵隔淋巴结群: 4、下段气管旁(包括奇静脉淋巴结):主动脉弓上缘以下水平至主支气管水平 主动脉淋巴结群: 5、主动脉下(主肺动脉窗):动脉韧带旁淋巴结。这些淋巴结不位于主动脉和肺动脉干之间,但位于这些血管旁。 6、主动脉旁(升主动脉或膈):位于长主动脉和主动脉弓前侧和外侧。 隆突下淋巴结群: 7、隆突下 下纵隔淋巴结群: 8、食管旁(隆突以下) 9、肺韧带:位于肺韧带内的淋巴结 肺淋巴结群: 10-14、N1淋巴结:位于纵隔外
例如,cT1N0(分期 IA)五年生存率为7792%。
分期的另一端,任何M1c患者(分期IV B)五年生存率为0%。
有如下情况者,肺叶切除总的来说是不可能: 跨肺裂生长 肺血管浸润 主支气管侵犯 上叶和下叶支气管受累 影像报告中应该特别强调这些内容。
应用薄层图像和三维重建来最清晰证实病变与相邻结 构的关系。
>3,<=4厘米 >4,<=5厘米 >5,<=7厘米(最大径) 侵犯胸壁,侵犯心包,侵犯膈神经,同一肺叶见卫星结节灶 肿瘤大于7厘米(最大径),侵犯纵隔、膈肌、心脏、大血管、喉返神经、隆突、气管、食管、脊柱或同侧肺多 个肿瘤 同侧支气管周围和/或肺门淋巴结,肺内淋巴结 同侧纵隔和/或隆突下淋巴结 对侧纵隔或肺门;同侧/对侧斜角肌/锁骨上淋巴结 远处转移 对侧肺或胸膜、心包结节/恶性浸润 单发胸外转移,包括单发非局部淋巴结 一个或多发器官的多发胸外转移
肺癌TNM第八版分类中文版

转移灶大小
转移灶数目
测量转移灶的最大直径,了解转移灶的大小 ,对判断患者的预后和制定治疗方案具有重 要意义。
了解转移灶的数目,有助于判断患者的预后 和治疗方案的制定。
综合分析
将肿瘤、淋巴结和远处转移的情况进行综合分析,根据tnm 分期标准,确定患者的分期,如Ⅰ期、Ⅱ期、Ⅲ期、Ⅳ期等 。
根据患者的分期,制定合适的治疗方案,如手术切除、放疗 、化疗等。
应的治疗方案。
根据TNM分期,患者可分为早期、中 期和晚期,不同阶段的治疗方案存在
差异。
对于早期患者,可采用手术切除或局 部放疗等局部治疗手段,以提高治愈 率和生存率;对于中晚期患者,则需 采取综合治疗措施,包括手术、放疗
、化疗、免疫治疗等手段。
ቤተ መጻሕፍቲ ባይዱ
肺癌的预后评估和随访
TNM分期是评估肺癌预后的重要因素,不同分期的患者预后存在差异 。
淋巴结数量
了解淋巴结的数量,有助于判断是 否存在多发转移。
淋巴结转移情况
通过病理学检查,了解淋巴结转移 情况,如转移个数、转移灶大小等 。
确定远处转移的情况
远处转移部位
远处转移形态
通过CT、MRI、PET-CT等检查,确定远处 转移的部位,如脑、肝、骨等。
观察远处转移的形态,是否规则、有无钙化 等,对判断转移灶的性质和程度具有重要意 义。
TNM分期与预后密 切相关
TNM分期与其他临 床评估指标(如病 理类型、年龄等) 有一定关系
TNM分期与治疗策 略选择密切相关
04
tnm分类的局限性和不足
tnm分类的缺陷和不足
肿瘤异质性
同一病理类型的肿瘤具有不同的生物学特性和临床表现,因此仅依靠病理类型进行分类存在局限性。
肺癌第8版TNM分期 PPT

IA 细分为 IA1、IA2、IA3;T1a~ bN1 由 IIA 变为 IIB;T3N1 由 IIB 变 为 IIIA 期;T3N2 由 IIIA 期变为 IIIB 期;T3~4N3 变为 IIIC。B。
x:无法评估;N0:无; 1:同侧支气管周围和 / 或同侧肺门淋巴结以及肺内淋巴结有转 移(10-14站) 2:同侧纵隔内和 / 或隆突下淋巴结转移。(2-9站) 3:对侧纵隔、对侧肺门、同侧或对侧前斜角肌及锁骨上淋巴结 转移。
Mx:无法判断;M0:无; M1:有。当有远处转移,即 M1 时,无论 T、N 如何均为 IV 期。
第七版分期中将肿瘤累及主支气管距离隆突≥2cm归 为T2,累及主支气管且距离隆突<2cm但未累及隆突 者为T3。而研究却发现,在所有的研究人群中,累及 主支气管且距离隆突≥2cm与其他因素T2预后一致, 生存差异并无统计学意义,而累及主支气管且距离隆 突<2cm但未累及隆突者,预后明显好于其他因素T3 ,因此新版分期对于主支气管受累,只要未侵犯隆突
肺癌第8版TNM分期
(1)将T1分为T1a(≤1cm),T1b (> 1至≤2cm),T1c(> 2至≤3cm); (2)T2分为T2a(> 3≤4cm)和T2b (> 4至≤5cm);(3)重新分类大于 5cm且小于或等于7cm的肿瘤分为T3;(4) 重新分类超过7cm或更大的肿瘤为T4;(5) 支气管受累距隆突小于2cm,但不侵犯隆突, 和伴有肺不张/肺炎则归为T2;(6)侵犯膈 肌分为T4;(7)删除纵隔胸膜浸润这一T分 期术语。
Rami-Porta学者研究发现肿瘤大小是影响肺癌患者预 后的重要因素。根据NSCLC患者原发肿瘤大小不同, 将其分为≤1cm,1~2cm,2~3cm,3~4cm, 4~5cm,5~6cm,6~7cm这7个组别观察其术后预后 差别,研究发现对于≤5cm的前五组,每增加1cm, 各组的5年生存率存在明显差异(P<0.001),而最 后两组生存差异不大,因此将其合并为T3(肿瘤最大 径>5cm,≤7cm)。由于肿瘤最大径≤3cm及> 3cm生存差异很大(P<0.001),因此将3cm仍作为 T1、T2的分界点,前三组T1又依次分为T1a、T1b、 T1c,中间两组T2分又为T2a及T2b,每个分期间隔为 1cm。同时研究发现肿瘤最大径>7cm患者预后与七 版分期的T4患者生存率类似,因此新版将>7cm归为 T4。
肺癌分期AJCC第8版

T2:肿瘤最大径>3 cm,≤5 cm;侵犯主支气管(不常见的表浅扩散型肿瘤,不 论体积大小,侵犯限于支气管壁时,虽可能侵犯主支气管,仍为T1),但未侵及 隆突;侵及脏层胸膜;有阻塞性肺炎或者部分或全肺肺不张。符合以上任何一个条 件即归为T2。
T2a:肿瘤最大径>3 cm,≤4 cm; T2b:肿瘤最大径>4 cm,≤5 cm;
4. 侵犯膈肌及纵隔胸膜的T分期调整
第七版TNM分期将肿瘤直接侵犯膈肌及纵隔胸膜均归为T3。 最新研究发现膈肌浸润患者要比其他pT3患者预后更差,类似于pT4患 者,因此新版TNM分期将侵犯膈肌归为T4。 对于纵隔胸膜浸润,研究者认为需要进行手术切除或胸腔镜活检后才 能进一步确认,和壁层胸膜不同,纵隔胸膜受累没有明显征象,当发 现纵隔胸膜受累时往往肿瘤已越过胸膜侵犯到胸膜内组织或脏器,而 且病理界定有一定困难,在病理分期中极少见仅单独纵隔胸膜受侵而 没有浸润到纵隔内组织的情况,因此将纵隔胸膜浸润纳入临床分期并 不可靠,故而在新版分期中删除了纵隔胸膜受累的T分期因素。
对于那些直径≤5 cm的患者,肿瘤至今每增加1 cm,其预后明显下降(P < 0.001),而对于肿瘤最大径 > 5 cm,≤7 cm的患者生存率变化不大,因此 将其统称为T3。 由于肿瘤最大径≤3 cm及 > 3 cm生存差异很大(P < 0.001),因此将3 cm 仍作为T1、T2的分界点,前三组T1又依次分为T1a、T1b、T1c,中间两组 T2分又为T2a及T2b,每个分期间隔为1 cm。 同时研究发现肿瘤最大径 > 7 cm患者预后与七版分期的T4患者生存率类似, 因此新版将 > 7 cm归为T4。
肺癌第8版TNM分期

第七版TNM分期将肿瘤导致的部分肺不张或阻塞性肺炎归为T2, 若导致全肺不张则归为T3。而在所有研究人群中发现:合并部分 肺不张或阻塞性肺炎患者预后与其他因素T2预后一致,但合并全 肺不张或阻塞性肺炎患者预后明显好于其他因素T3,因此新版分 期无论肺不张或阻塞性肺炎范围大小、累及全肺与否均归为T2。
Rami-Porta学者研究发现肿瘤大小是影响肺癌患者预后的重要因素。根 据NSCLC患者原发肿瘤大小不同,将其分为≤1cm,1~2cm,2~3cm, 3~4cm,4~5cm,5~6cm,6~7cm这7个组别观察其术后预后差别, 研究发现对于≤5cm的前五组,每增加1cm,各组的5年生存率存在明显 差异(P<0.001),而最后两组生存差异不大,因此将其合并为T3(肿 瘤最大径>5cm,≤7cm)。由于肿瘤最大径≤3cm及>3cm生存差异 很大(P<0.001),因此将3cm仍作为T1、T2的分界点,前三组T1又 依次分为T1a、T1b、T1c,中间两组T2分又为T2a及T2b,每个分期间 隔为1cm。同时研究发现肿瘤最大径>7cm患者预后与七版分期的T4患 者生存率类似,因此新版将>7cm归为T4。
第七版肺癌TNM分期标准 是2009年颁布的
新版分期包含了1999-2010年间94708例肺癌患者,来自16个国 家的35个数据库,其中NSCLC所占的比例明显增加,亚洲病例数明 显增加。
将T1分为T1a(≤1cm),T1b(> 1至≤2cm),T1c (> 2至≤3cm);(2)T2分为T2a(> 3≤4cm)和T2b (> 4至≤5cm);(3)重新分类大于5cm且小于或等于 7cm的肿瘤分为T3;(4)重新分类超过7cm或更大的肿瘤 为T4;(5)支气管受累距隆突小于2cm,但不侵犯隆突, 和伴有肺不张/肺炎则归为T2;(6)侵犯膈肌分为T4;(7) 删除纵隔胸膜浸润这一T分期术语。
最新肺癌TNM分期(第8版)

最新肺癌TNM分期(第8版)出版⽇期:2017年12⽉9⽇。
这是对肺癌TNM第8版的总结,这是⾃2017年1⽉1⽇以来⾮⼩细胞肺癌分期的标准。
它由IASLC(国际肺癌研究协会)颁发,取代了TNM第7版。
表中显⽰了第8版TNM分类的⾮⼩细胞肺癌,与第七版的不同之处⽤红⾊表⽰。
符合以前的版本有三个组成部分,描述肿瘤的解剖范围:T为原发肿瘤的程度,N为淋巴结受累,M为转移性疾病。
使⽤CT进⾏T分类,使⽤CT和PET-CT进⾏N分类和M分类。
可⽤于术前影像学和临床分类iTNM / cTNM,但也可⽤于明确的病理分期pTNM,治疗后yTNM 再分期和复发rTNM的分期。
第七版与第⼋版的区别在新的TNM第8版中,⼏个T类别的⼤⼩有所下降,并引⼊了⼀些新的基于病理学的类别。
此外,还介绍了关于胸外转移性疾病的新M类别。
肺实质病灶的⼤⼩被定义为肺窗三个正交平⾯中任何⼀个的最⼤直径。
在亚组织病变中,T分类由固体组分的直径定义,⽽不是完整的⽑玻璃病变的直径。
第8版TNM在肺癌中的肺癌分期T,N和M类别的亚组分为⼀些阶段,因为这些患者的预后相似[1]。
例如,cT1N0疾病(IA期)具有77-92%的5年存活率。
另⼀⽅⾯是任何M1c疾病(IVB期),其5年⽣存率为0%。
肺癌在冠状和⽮状⾯重建上具有明显的穿透⾎管⽣长(Transfissural); 肺叶切除不再是可能的如果存在以下情况,通常不可能进⾏肺叶切除术:Transfissural增长。
肺⾎管侵袭。
主⽀⽓管⼊侵。
涉及上下叶⽀⽓管。
这些是要报告的具体项⽬。
为了最好地展⽰与周围结构的关系,薄层图像和三平⾯重建是必要的。
在不确定⼊侵的情况下,多学科肿瘤委员会应根据个案和合并症来决定是否给予怀疑。
T-分类T0:影像学上没有原发肿瘤Tis:原位癌,不论⼤⼩;这只能在切除肿瘤后才能诊断出来。
T1肿瘤 - 左下叶典型的T1肿瘤,完全被肺实质包围。
T1肿瘤⼤⼩≤3cm;肿瘤≤1cm=> T1a;肿瘤> 1cm但≤2cm=> T1b;肿瘤> 2cm但≤3cm=> T1cT1a(mi)病理确诊来源于“微创”的,与⼤⼩⽆关。
肺癌TNM新分期及解读 (1)

研究人群
• 亚洲地区(日本、韩国、中国)贡献了最大量的患者,占数据库的79% • 腺癌患者比例明显增多,约占总体的2/3
11
25
地理区域 总计 南北美洲 澳洲 欧洲 亚洲 总共 75 1375 cT1 31 752 M0 总计 2577 1032 M0
临床分期
64
腺癌 鳞癌 其他
cT2 36 429
第7版和第8版T分期调整对比
第7版
新截点:1cm T1a: ≤2cm
升期
第8版
T1a: ≤1cm T1b: >1cm, 但≤2cm T1c: >2cm, 但≤3cm
T1b: >2cm, 但≤3cm
T2a: >3cm, 但≤5cm
新截点:4cm
T2a: >3cm, 但≤4cm T2b: >4cm, 但≤5cm
Asamura H, et al. J Thorac Oncol 2015;10:1675-1684.
第8版肺癌N分期:小结
•推荐:
•目前保留与之前相同的描述 •提出以下用于前瞻性检验的新的描述: -pN1a:包括单个pN1结节站 -pN1b:包括多个pN1结节站 -pN2a1:包括单个pN2结节站(非pN1)(跳过pN2) -pN2a2:包括单个pN2结节站(及pN1) -pN2ab:包括多个pN2结节站
cT3 8 146
cT4 0 48
pT1 1364 454
pT2 994 460
pT3 194 112
pT4 25 6
9
1268 10294 13012
383 5934 7100
456 3318 4239
2518
2571
745
肺癌TNM新分期及解读

第7版和第8版T分期调整对比
第7版
T1a: ≤2cm T1b: >2cm, 但≤3cm T2a: >3cm, 但≤5cm T2b: >5cm, 但≤7cm
T3: >7cm
新截点:1cm 升期
新截点:4cm 升期 升期
第8版
T1a: ≤1cm T1b: >1cm, 但≤2cm T1c: >2cm, 但≤3cm
P值 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001
第8版T分期调整
•3cm临界值明显区分了T1和T2 •最大径1cm到5cm的肿瘤,每增加1cm,患者 预后便明显不同 •>5-7cm肿瘤的预后等同于T3,>7cm肿瘤的预 后等同于T4 •支气管侵犯<2cm以及完全肺不张/肺炎,预后 相当于T2 •隔膜侵犯患者的预后相当于T4 •纵膈胸膜侵犯这一描述很少使用,予以删除
208 39 77,156
Rami-Porta R, et al. 2015 WCLC Abstract PLEN02.02.
治疗类型
化疗:9.3%
化疗+放疗 4.7%
放疗:1.5%
三联 4.4%
化疗+手术 21.1%
放疗+手术 1.5%
手术:57.7%
Rami-Porta R, et al. 2015 WCLC Abstract PLEN02.02.
N=16644 (%) 75 9 10 56 29 21 33 25 34
手术 HR(95% CI) 2.06(1.87, 2.28) 2.24(2.01, 2.50) 2.58(2.36, 2.83) 1.70(1.57, 1.83) 1.47(1.31, 1.65) 0.98(0.87, 1.10) 1.45(1.21, 1.74) 1.82(1.52, 2.18) 2.43(2.04, 2.90)
肺癌的分期

T分期(T2)
部分肺不张
完全肺不张
T分期(T3)
6.6cm • T3:肿瘤最大径>5cm,≤7cm;直接侵犯以下任何一个器官,包括:胸壁(包含
肺上沟瘤)、膈神经、心包;同一肺叶出现孤立性癌结节。符合以上任何一个条件 即归为T3。
T分期(T4)
• T4:肿瘤最大径>7cm;无论大小,侵及以下任何一个器官,包括:纵隔、心脏、大血 管、隆突、喉返神经、主气管、食管、椎体、膈肌;同侧不同肺叶内孤立癌结节。
• 8区:食管旁淋巴结,是3P向下的延续,自隆突下沿食管延伸至膈肌食管裂孔。 • 9区:肺韧带淋巴结,位于肺韧带区,包括下肺静脉后壁及下方淋巴结。
纵隔淋巴结分区(10-14区)
• 10区:肺门淋巴结,包括临近主支气管与肺门血管淋巴结。在右侧自 奇静脉下缘至叶间区域,左侧自肺动脉上缘至叶间区域。
• 11区:肺叶间淋巴结 12区:肺叶淋巴结。 • 13区:肺段淋巴结 14区:肺亚段淋巴结。
M分期(M1b)
Mlb:远处器官单发转移灶。
M分期(M1c)
M1c:多个或单个器官多处转移
IASLC第八版TNM分期
小结
IASLC第八版TNM分期
谢谢
右肺肿瘤N分期:
• N1:同侧支气管周围和/或肺门淋巴 结10R-14R。
• N2:同侧纵隔和/或隆突下淋巴结 2R,3aR,3p,4R,7,8R,9R。
• N3:对侧纵隔和/或肺门,以及任何 锁骨上淋巴结。
• 1,2L,3aL,4L,5,6,8L,9L, 10L-14L。
左肺肿瘤N分期:
• N1:同侧支气管周围和/或肺门淋巴 结10L-14L。
• M分期:
• MX:远处转移不能被判定。 • M0:无远处转移。 • M1:远处转移。 • M1a:局限于胸腔内,包括胸膜播散 (恶性胸腔积液 、心包积液或
分期手册AJCC第8版原发性支气管肺癌TNM分期图谱
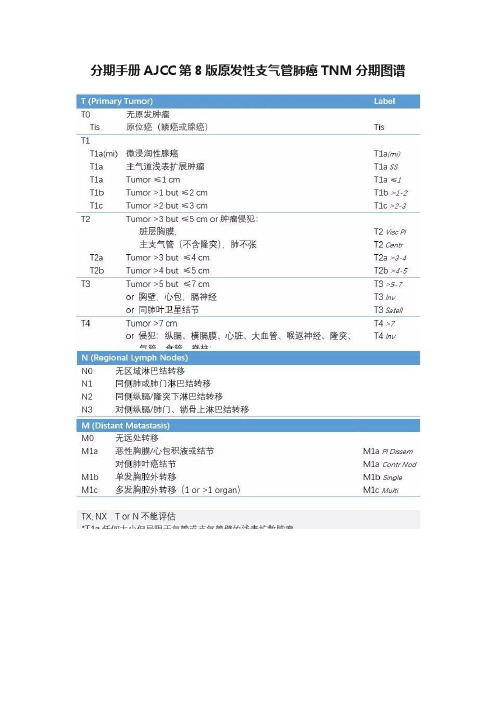
分期手册AJCC第8版原发性支气管肺癌TNM分期图谱
纵膈淋巴结分区
AJCC第八版肺癌分期图谱
8th VS 7th
1
T分期
◆T1分为T1a:≤1cm;T1b:>1cm到≤2cm;T1c:>2cm到≤3cm;
◆T2分为T2a:>3cm到≤4cm;T2b:>4cm到≤5cm;
◆T3为>5cm、≤7cm的肿瘤;
◆T4为≥7cm的肿瘤;
◆支气管受累距隆突小于2cm,但未侵犯隆突、伴有肺不张或肺炎的肿瘤由T3期变为T2期;
◆侵犯膈肌改为T4期;
◆纵隔胸膜浸润T分期去除。
2
N分期
◆提出了转移淋巴结位置、站数和跳跃式转移的概念;
◆将N1分为pN1a(单站)、pN1b(多站);
◆N2分为pN2a1(单站,跳跃式转移无N1淋巴结)、pN2a2(单站N2有N1转移)、pN2b(多站N2转移)。
3
M分期
◆将M1分为M1a(局限于胸腔,包括胸膜播散)、M1b(远处器官单发转移灶)和M1c(单个或多个器官的多处转移)。
4
TNM分期
◆IA期分为IA1、IA2、IA3期;
◆T1a-bN1M0从ⅡA期改为ⅡB期;
◆T3N1M0由ⅡB期改为ⅢA期;
◆T3N2M0由ⅢA期改为ⅢB期;
◆M1a和M1b改为ⅣA期,M1c改为ⅣB期。
参考文献:
[1]Detterbeck FC, Boffa DJ, Kim AW, Tanoue LT, The 8th Edition Lung Cancer Stage Classification, CHEST (2016), doi: 10.1016/j.chest.2016.10.010.
编辑 | 陈海石。
肺癌第8版TNM分期PPT课件

主支气管受累距隆突的距离不再 作为T分期的依据
第七版分期中将肿瘤累及主支气管距离隆突≥2cm归 为T2,累及主支气管且距离隆突<2cm但未累及隆突 者为T3。而研究却发现,在所有的研究人群中,累及 主支气管且距离隆突≥2cm与其他因素T2预后一致, 生存差异并无统计学意义,而累及主支气管且距离隆 突<2cm但未累及隆突者,预后明显好于其他因素T3 ,因此新版分期对于主支气管受累,只要未侵犯隆突
16
Mx:无法判断;M0:无; M1:有。当有远处转移,即 M1 时,无论 T、N 如何均为 IV 期。
17
18
M分期调整---将寡转移引入肺癌 分期
新版们M分期对第七版的M1b进行了较大调整,使之更加细化 ,与第七版分期最大区别在于引入了远处寡转移病例,其研究 结果主要来自西德癌症医学中心Eberhardt等的研究[4]。他们 对225例单一远处器官出现的单一转移病灶、229例单一远处 器官出现的多发转移病灶以及247例远处多个器官出现的多发 转移三组患者进行预后分析,发现远处单个器官的单发转移组 中位生存时间为11.4月,明显好于其余两组的6.3月,显示转 移灶数目与患者预后密切相关,而且转移灶数目比转移器官数 更有预后价值。因此新版分期将转移器官及转移灶数目纳入分 期系统,七版的M1b重新调整为M1b(单个远处器官的单发转 移,即寡转移)和M1c(单个器官多发转移或多个器官多发转 移)。对于M1a,由于研究发现胸腔内单发转移与多发转移预 后无统计学差异,因此仍然沿用原来的M1a分期。新的TNM 分期中M1b的预后与M1a类似,明显由于M1c。
7
强调肿瘤大小对预后的影响
Rami-Porta学者研究发现肿瘤大小是影响肺癌患者预 后的重要因素。根据NSCLC患者原发肿瘤大小不同, 将其分为≤1cm,1~2cm,2~3cm,3~4cm, 4~5cm,5~6cm,6~7cm这7个组别观察其术后预后 差别,研究发现对于≤5cm的前五组,每增加1cm, 各组的5年生存率存在明显差异(P<0.001),而最 后两组生存差异不大,因此将其合并为T3(肿瘤最大 径>5cm,≤7cm)。由于肿瘤最大径≤3cm及> 3cm生存差异很大(P<0.001),因此将3cm仍作为 T1、T2的分界点,前三组T1又依次分为T1a、T1b、 T1c,中间两组T2分又为T2a及T2b,每个分期间隔为 1cm。同时研究发现肿瘤最大径>7cm患者预后与七 版分期的T4患者生存率类似,因此新版将>7cm归为 T4。
肺癌第8版TNM分期

Mx:无法判断;M0:无; M1:有。当有远处转移,即 M1 时,无论 T、N 如何均为 IV 期。
M分期调整---将寡转移引入肺癌
分期
新版们M分期对第七版的M1b进行了较大调整,使之更加细化 ,与第七版分期最大区别在于引入了远处寡转移病例,其研究 结果主要来自西德癌症医学中心Eberhardt等的研究[4]。他们 对225例单一远处器官出现的单一转移病灶、229例单一远处 器官出现的多发转移病灶以及247例远处多个器官出现的多发 转移三组患者进行预后分析,发现远处单个器官的单发转移组 中位生存时间为11.4月,明显好于其余两组的6.3月,显示转 移灶数目与患者预后密切相关,而且转移灶数目比转移器官数 更有预后价值。因此新版分期将转移器官及转移灶数目纳入分 期系统,七版的M1b重新调整为M1b(单个远处器官的单发 转移,即寡转移)和M1c(单个器官多发转移或多个器官多发 转移)。对于M1a,由于研究发现胸腔内单发转移与多发转移 预后无统计学差异,因此仍然沿用原来的M1a分期。新的 TNM分期中M1b的预束 感谢各位的批评指导!
谢 谢!
让我们共同进步
第七版肺癌TNM分期标准是2009年颁 布的
背景
新版分期包含了1999-2010年间94708 例肺癌患者,来自16个国家的35个数据 库,其中NSCLC所占的比例明显增加,亚 洲病例数明显增加。
T-原发肿瘤
改变
(1)将T1分为T1a(≤1cm),T1b(> 1 至≤2cm),T1c(> 2至≤3cm);(2) T2分为T2a(> 3≤4cm)和T2b(> 4至 ≤5cm);(3)重新分类大于5cm且小于或 等于7cm的肿瘤分为T3;(4)重新分类超 过7cm或更大的肿瘤为T4;(5)支气管受 累距隆突小于2cm,但不侵犯隆突,和伴有 肺不张/肺炎则归为T2;(6)侵犯膈肌分为 T4;(7)删除纵隔胸膜浸润这一T分期术语。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2、新版TNM分期主要变更内容
2.1 T分期
(1)将T1分为T1a(≤1cm),T1b(>1至≤2cm),T1c(>2至≤3cm);(2)T2分为T2a(>3≤4cm)和T2b(>4至≤5cm);(3)重新分类大于5cm且小于或等于7cm的肿瘤分为T3;(4)重新分类超过7cm或更大的肿瘤为T4;(5)支气管受累距隆突小于2cm,但不侵犯隆突,和伴有肺不张/肺炎则归为T2;(6)侵犯膈肌分为T4;(7)删除纵隔胸膜浸润这一T分期术语。
2.2 N分期
继续使用原N分期方法。
但提出了转移淋巴结的位置:nN(单站与多站),存在和不存在跳跃式淋巴结转移,pN1a,pN1b,pN2a1,pN2a2和pN2b可能对预后的评价更为精确。
2.3 M分期
将M1分为Mla,M1b和M1c:(1)Mla局限于胸腔内,包括胸膜播散 (恶性胸腔积液、心包积液或胸膜结节)以及对侧肺叶出现癌结节归为Mla;(2)远处器官单发转移灶为M1b;(3)多个或单个器官多处转移为M1c。
2.4 TNM分期
(1)IA起分为IA1,IA2和IA3;(2)T1a,bN1由IIA期改为IIB期;(3)T3N1由IIB期改为IIIA期;(4)T3N2 由IIIA期改为IIIB期;(5)T3-4N3 更新为IIIC期;(6)M1a和M1b 更新为IVa, M1c更新为IVb。
3、新版TNM分期调整部分详细解读
3.1 T分期解读及修改依据
3.1.1更加强调肿瘤大小对预后的影响Rami-Porta学者研究发现肿瘤大小是影响肺癌患者预后的重要因素[2]。
根据NSCLC患者原发肿瘤大小不同,将其分为≤1cm,1~2cm,2~3cm,3~4cm,4~5cm,5~6cm,6~7cm这7个组别观察其术后预后差别,研究发现对于≤5cm的前五组,每增加1cm,各组的5年生存率存在明显差异(P<0.001),而最后两组生存差异不大,因此将其合并为T3
(肿瘤最大径>5cm,≤7cm)。
由于肿瘤最大径≤3cm及>3cm生存差异很大(P <0.001),因此将3cm仍作为T1、T2的分界点,前三组T1又依次分为T1a、T1b、T1c,中间两组T2分又为T2a及T2b,每个分期间隔为1cm。
同时研究发现肿瘤最大径>7cm患者预后与七版分期的T4患者生存率类似,因此新版将>7cm 归为T4。
3.1.2 主支气管受累距隆突的距离不再作为T分期的依据第七版分期中将肿瘤累及主支气管距离隆突≥2cm归为T2,累及主支气管且距离隆突<2cm但未累及隆突者为T3。
而研究却发现,在所有的研究人群中,累及主支气管且距离隆突≥2cm与其他因素T2预后一致,生存差异并无统计学意义,而累及主支气管且距离隆突<2cm但未累及隆突者,预后明显好于其他因素T3,因此新版分期对于主支气管受累,只要未侵犯隆突,无论距离隆突多远均归为T2。
3.1.3 肺不张/阻塞性肺炎的范围不再作为T分期依据第七版TNM分期将肿瘤导致的部分肺不张或阻塞性肺炎归为T2,若导致全肺不张则归为T3。
而在所有研究人群中发现:合并部分肺不张或阻塞性肺炎患者预后与其他因素T2预后一致,但合并全肺不张或阻塞性肺炎患者预后明显好于其他因素T3,因此新版分期无论肺不张或阻塞性肺炎范围大小、累及全肺与否均归为T2。
3.1.4 侵犯膈肌及纵隔胸膜的T分期调整第七版TNM分期将肿瘤直接侵犯膈肌及纵隔胸膜均归为T3。
最新研究发现膈肌浸润患者要比其他pT3患者预后更差,类似于pT4患者,因此新版TNM分期将侵犯膈肌归为T4。
对于纵隔胸膜浸润,研究者认为需要进行手术切除或胸腔镜活检后才能进一步确认,和壁层胸膜不同,纵隔胸膜受累没有明显征象,当发现纵隔胸膜受累时往往肿瘤已越过胸膜侵犯到胸膜内组织或脏器,而且病理界定有一定困难,在病理分期中,极少见仅单独纵隔胸膜受侵而没有浸润到纵隔内组织的情况,因此将纵隔胸膜浸润纳入临床分期并不可靠,故而在新版分期中删除了纵隔胸膜受累的T分期因素。
3.2 关于N分期---增加了病理亚分期
由于以往不同N分期之间生存率差异已经能够很好地反映肺癌患者分期与预后的关系,因此新版分期建议继续沿用原来第七版N分期。
但研究却发现对于同一级别的N分期中,临床分期与病理分期生存率差异较大[3],而病理分期往往更能够反映真实的分期情况,研究发现淋巴结转移站数及是否存在跳跃性转移对预后会产生重要影响,伴有多站转移及存在跳跃性转移患者预后明显变差,因此推荐将原来的N1细分为N1a(单站转移)和N1b(多站转移);N2分为N2a1(无N1转移,直接跳跃到N2的淋巴结)、N2a2(有N1淋巴结转移,同时发生单站N2淋巴结转移)和N2b(多站N2淋巴结转移)。
3.3 M分期调整---将寡转移引入肺癌分期
新版们M分期对第七版的M1b进行了较大调整,使之更加细化,与第七版分期最大区别在于引入了远处寡转移病例,其研究结果主要来自西德癌症医学中心Eberhardt等的研究[4]。
他们对225例单一远处器官出现的单一转移病灶、229例单一远处器官出现的多发转移病灶以及247例远处多个器官出现的多发转移三组患者进行预后分析,发现远处单个器官的单发转移组中位生存时间为11.4月,明显好于其余两组的6.3月,显示转移灶数目与患者预后密切相关,而且转移灶数目比转移器官数更有预后价值。
因此新版分期将转移器官及转移灶数目纳入分期系统,七版的M1b重新调整为M1b(单个远处器官的单发转移,即寡转移)和M1c(单个器官多发转移或多个器官多发转移)。
对于M1a,由于研
究发现胸腔内单发转移与多发转移预后无统计学差异,因此仍然沿用原来的M1a 分期。
新的TNM分期中M1b的预后与M1a类似,明显由于M1c。
3.4 TNM分期更加细化
新版TNM分期将原来的IA期进一步细分为IA1、IA2及IA3期,T1a,bN1由IIA期改为IIB期;T3N1由IIB期改为IIIA期;T3N2 由IIIA期改为IIIB 期;T3-4N3 更新为IIIC期;M1a和M1b 更新为IVa, M1c更新为IVb,相对更复杂更细致的临床分期使判断预后更加准确,对选择合理的个体化治疗更有针对性。
总之,修订后的TNM分期能够更好的显示患者的预后,在当前精准医学理念的大背景下,新分期标准使肺癌的诊断、治疗以及预后判断更加精准。
4、新版TNM分期的局限性
虽然第八版TNM分期较第七版更加全面,能够更好的反应患者的预后,但仍然存在一些问题。
4.1 新版分期数据采集的局限性新版分期虽然增加了亚洲人群比例,但主要为日本病例,中国作为肺癌大国,病例数较少,而且主要为上海和广东病例,不具备代表性。
另外虽然首次将南美病例纳入研究,但仍然缺乏非洲、俄罗斯及印度患者的数据。
同时由于欧亚人种的个体差异性较大,对治疗的反应及耐受性存在一定差异,其生存率也受到一定影响,例如研究发现对于pN0分期的患者,5年生存率就存在明显的地域性差异,亚洲患者预后最好,5年生存率高达79%,而欧洲患者预后最差,仅为54%,之间相差了25个百分点,然而新的分期并没有考虑到人群特征及地域性差异,也没有进行人群特征校正分析,更没有在本次N分期中体现,虽然这种差异随着pN分期的增加而最终消失,但是对于不同地域患者生存率及预后判断可能存在一定偏差。
4.2 肺癌驱动基因状态及肺癌分子分型并未在新分期中体现近年来肺
癌分子遗传学研究取得了显著进展,基于遗传特征的分子分型的广泛应用于临床,使中晚期肺癌的治疗步入了个体化分子靶向治疗时代,大大改善了部分中晚期肺癌患者的预后,提高了患者远期生存率。
然而体现靶向治疗敏感性的肺癌驱动基因(EGFR、ALK及ROS1等)状态,PD-1表达水平等分子生物学标志均未在第八版分期中有所体现。
除此之外,由于地域发展不平衡及样本量的限制,部分病例在统计肿瘤大小、淋巴结转移状况、转移灶器官及个数以及治疗方案的选择方面都存在一定偏差,加上放化疗病例数偏少,由此也导致数据统计上的偏差。
另外虽然PET-CT 已在大多数国家及地区应用于临床,但由于价格昂贵并没有作为常规检查项目,因此其研究结果也并未纳入新版分期。
尽管如此,新版分期相比UICC第七版分期还是有了明显的改善和提高,更能适应目前的临床需求。
