从海水中获得的化学物质
2020年浙江高考化学复习:专题十从海水中获得的化学物质
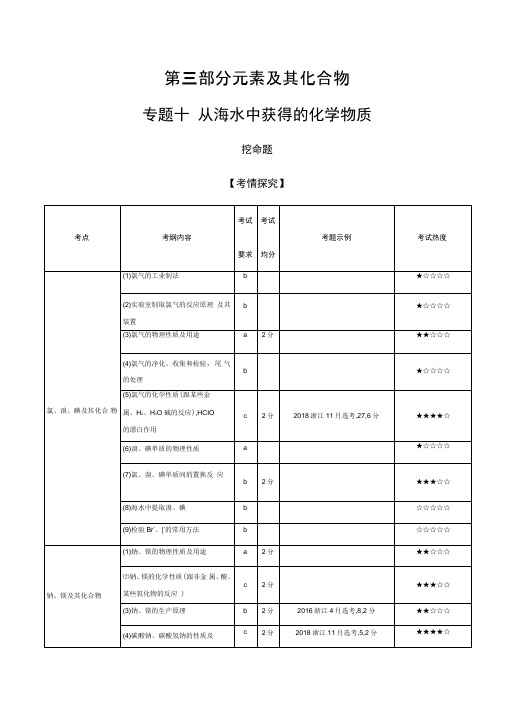
第三部分元素及其化合物专题十从海水中获得的化学物质挖命题【考情探究】分析解读本专题选择题重点考查点有二:一是氯气的性质及用途;二是钠、碳酸钠和碳酸氢钠的性质及用途,试题难度不大。
主观题部分单独命题的可能性不大 ,通常以元素化合物知识为载体,融离子反应、氧化 还原反应、反应速率与化学平衡、电化学及盐类的水解与电离等知识于一体进行考查。
预计今后高考对本 专题内容的考查方式基本不变。
【真题典例】--------------------------------------------------------- 於-(2018^11月选夸.27・6分}已知化讣物耳甫1种无武蛆盛*莘学习小範 进行丁如下实验:① 飙适贲X.加水完全瀋解.无气体产生*擀浚呈喊性;进甘焰色反应、 进过蓝色姑玻璃现泉到火焰呈購色 ②詳溥十水* iDA^HClO^OOftnol 的盐戕恰好屮狗;屮和右闸得蒂權与硝酸战化的过駄曲阻間液反逼•穆^14305曲色观金 谓岡答* 1(悄中3神无素是 _________ (用元素挣号表加)◎肚宾与比反应的化学片程式尼 __________________________________________[3JX 中-种尤我对应的单匮,可与足童的屉落襪反应谓到(斗打马川厦 反应的化学方程式;破考点 【考点集训】考点一 氯、溴、碘及其化合物1.(2019届浙江宁波镇海中学高一单元测试 ,6)下列离子方程式正确的是( )① 氯气与水反应:Cl 2+H — 2H ++CI+CI0-; ② 氯气与氢氧化钠溶液反应:Cl 2+2OHCl -+CIO+HO;■o itfflX'F 暂評屯虜.■ Q 長鸣儿耳TvK 乂匚兀。
为认 KCH*丄乂虫T.飆』o 檢心當点I, 物庫曲址的肖誥计卑 ♦甜LR 其去突此合输的性虜❷能力要求卄显时踪合论他力、力利恢 1受新知训及扶临有恢偵嵐繼力的考畫. @解题思路⑴根谣①和M 综合拆斷十135诅和木反 应生廣0E mnl SI 和n.H2 rnJ K 〔Hi ・曲*厂 <\ II II.-I^KIJ ■…. .|-I II : wl- ''ll| ] Z \ i' 恻 EX 刑ClgUU ind K ?9 肿iud+A5,脚叔”I flfil niDixlJad :由”化含辆、祁种元議 ffljR'W t 览合將中可舐飭扛元竄咸耙 元札Hff 9UK^AM«元轧K*廉的量为QDlnd*所口负为£00〔期L K 反应的化爭方程式为血H.U = 2K0H+Kd«(3)1CL+H J1O= 2IKI +CLO , 2Xd.CO J +2UU^^2\.^i j+2XdllU). HlhliW 2O S +2N^C0^M 3O=^!NJ1C0J +4 2\da+u,o "❹易信谆示勉引问屮色输35解液足ht.姑訴 月星式蜡写肖2“尹制屮1%^=1珂f +4 2Xd (J+< 1J ).❺答案(1M <X 0aiK/304^ ----------- BKOfbKi I(3)2N^C01+2O 1+H 1Q^-€l ]p4lNflH(:O.+2Nut3❺规律总结 几柑"瘪礼曲:牡徳闌息凰略_ (龙族Hi 实益議探中晡冇息山及魁] 谭赵卜T 估£1-什小时乩忡珀样屮附 e\~^救辿,衍nt W>5 p $疋逍L .2•「172.-5 于 4 I'' I'- I'f . 样丈霽直班叩Vr 域的愛邑*所毎辆 甩冷:咛F ;屮吋詁I <t-r i i(t<.- 址吐枠冷一馭Fhi.EL 4 n 餐盜CT * 山Z'.M iq, Bfi 册 厲、抻立M 豪.大IHfltt,金ID# ^iirffiriio (Viwn 跡 质的无盍,期股的化学KlUJtAOi f7'.>ntt'":详式△③浓盐酸与二氧化锰共热:MnC2+4HCI(浓)Mn2++2CI+Cl2 f +2H0;④漂白粉溶液中通入少量的二氧化碳气体:Ca2++2CIO +HO+C — CaCO J +2HCIQA. ①③B.②④C.②③D.①④答案B2. (2019届浙江温州瑞安中学单元检测,3)下列与含氯化合物有关的说法正确的是()A. HCIO是弱酸,所以NaCIO是弱电解质B. 向沸水中逐滴加入少量饱和FeCb溶液,可制得Fe(OH)3胶体C. HCI溶液和NaCI溶液均通过离子导电,所以HCI和NaCI均是离子化合物D. 电解NaCI溶液得到22.4 L H 2(标准状况),理论上需要转移N A个电子(N A表示阿伏加德罗常数)答案B3. (2018浙江武义一中高一期末,12)已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图所示装置进行氯、溴、碘的性质实验。
2021_2022学年新教材高中化学专题3从海水中获得的化学物质第三单元第2课时从海水中提取镁和从海

第2课时
海洋化学资源的综合利用
从海水中提取镁和从海带中提取碘
课标定位素养阐释
1.能够从模型认知视角掌握从海水中提取镁、碘单质的工
艺流程。
2.能够从实验探究角度掌握镁、碘及其化合物的性质。
自主预习·新知导学
一、从海水中提取镁和从海带中提取碘
1.从海水中提取镁。
(1)提取流程:
海水
MgCl2
,理由是
。
答案:(1)B (2)Fe3+ Br2 FeBr3 Br2的氧化性大于Fe3+
FeI2 Fe3+的氧化性大于I2 (3)不能 Br2的氧化性大于I2
解析:(1)根据还原剂的还原性大于还原产物,可确定还原性
强弱顺序应为I->Fe2+>Br-,氧化性强弱顺序应为Br2>Fe3+>I2。
第(2)小题是对第(1)小题的深化和应用。根据氧化性、还原
C.①③⑤②④ D.③①②⑤④
答案:A
解析:向海带灰中加水后进行过滤,然后利用氧化还原反应
的原理使滤液中的碘从化合态变成游离态,最后用有机溶剂
萃取出碘单质并分液。
3.世界上60%的镁是从海水中提取的,其提取步骤如下:①把
贝壳烧制成生石灰;②向海水中加入生石灰,过滤,洗涤沉淀物;
③将沉淀物与盐酸反应,结晶、过滤;④在氯化氢热气流中加
I2
棕黄色→棕褐色
紫色→深紫色
2、Br2、I2的化学性质。
(1)相似性:
①都能与绝大多数的金属化合;
②都能与H2反应生成HX(X=Cl、Br、I,下同),HX都易溶于
水且都是强酸;
③都能与水和碱液反应:X2+H2O══HX+HXO,
高中化学专题3从海水中获得的化学物质第1单元第1课时氯气的发现与制备教学案苏教版第一册

第1课时氯气的发现与制备发展目标体系构建1。
能运用发展的、相互联系的、对立统一的观点理解化学变化,培养变化观念与平衡思想的化学核心素养.2.初步掌握实验探究元素及其化合物性质的基本方法,掌握氯气的制备方法,培养科学探究与创新意识的化学核心素养.1.氯气的发现1774年瑞典化学家舍勒把浓盐酸与软锰矿(主要成分是MnO2)混合在一起加热,意外地发现了一种具有强烈刺激性气味的黄绿色气体——氯气.2.氯气的实验室制法(1)反应原理:MnO2+4HCl(浓)错误!MnCl2+Cl2↑+2H2O。
(2)实验装置①A装置为气体发生装置,作用是制备气体。
②B装置为收集装置,作用是收集气体.③C装置为尾气处理装置,作用是吸收多余Cl2。
3.氯气的工业制法以电解饱和食盐水为基础制取氯气、烧碱等产品的工业称为氯碱工业.(1)氯气的制备原理:反应的化学方程式为2NaCl+2H2O错误! 2NaOH+H2↑+Cl2↑.(2)实验室电解饱和食盐水①实验装置:②实验操作a.接通电源,观察铁棒和石墨棒上发生的现象。
通电一段时间后,将小试管套在a管上,收集U形管左端产生的气体。
2 min 后,提起小试管,并迅速用拇指堵住试管口,移近点燃的酒精灯,松开拇指,检验收集到的气体.b.取一支小试管,用向上排空气法收集从b管导出的气体,观察收集到的气体的颜色。
c.关闭电源,打开U形管左端的橡皮塞,向溶液中滴加1~2滴酚酞溶液,观察溶液颜色的变化。
②实验分析实验现象结论a出现爆鸣声a管中气体为氢气b产生黄绿色的气体b管中气体为氯气c铁棒端溶液变红、石墨棒端溶液不变色U形管左端溶液显碱性、U形管右端溶液不显碱性③实验结论根据实验推断电解饱和食盐水的产物是H2、Cl2、NaOH溶液。
1.判断正误(正确的打“√”,错误的打“×”。
)(1)自然界中既有游离态的氯又有化合态的氯气单质。
(×)(2)瑞典化学家舍勒发现了氯气. (√)(3)工业上制取氯气的化学方程式为MnO 2+4HCl(浓)错误!MnCl 2+Cl 2↑+2H 2O 。
专题二从海水中获得的化学物质

其他有机物质
其他有机物质
除了烃类化合物、氨基酸和蛋白质外, 海水中还含有其他多种有机物质,如 糖类、醇类、酚类等。这些物质在生 物体中具有重要的生理功能,并具有 广泛的应用前景。
提取方法
对于其他有机物质的提取,通常采用 吸附、萃取、膜分离等方法。这些方 法可根据不同有机物的性质和含量进 行选择和应用。
总结词
开发挑战
随着技术的不断进步和全球气候变化的压力增加,核 能资源的开发和利用有望得到进一步发展,成为未来
能源供应的重要部分。
前景展望
核能开发面临一些挑战,如处理核废料和确保核安全 等。此外,核能开发还受到政治因素的制约,如国际 核不扩散条约的限制。
其他能源物质
01 总结词
除了甲烷水合物和核能资源外 ,海水中还含有其他具有开发 潜力的能源物质。
02
详细描述
海水中含有丰富的化学物质, 如锂、钾、镁等,这些物质可 以用于制造燃料电池、电动汽 车电池等新能源产品。此外, 海水中还含有一些稀有元素, 如铀、钍等,可用于核能开发 。
03
开发挑战
04
从海水中提取这些物质面临一些 技术挑战,如分离和纯化过程复 杂、成本较高。此外,一些物质 在海水中的浓度较低,需要高效 的提取技术才能实现商业化利用 。
镁
海水中镁的含量也相当丰富,是制造耐火材料、合金、轻质建材等的重要原料。
钾
海水中的钾元素是植物生长所需的微量元素之一,钾肥可以提高土壤肥力,促进农作物 生长。
非金属元素
氯
海水中含有大量的氯元素, 主要以氯化钠的形式存在。 氯是制造漂白粉、氯气、盐
酸等的重要原料。
溴
海水中的溴被广泛用于制造 各种含溴化合物,如溴化物
从海水中获得的化学物质PPT课件

收集装置
尾气吸收装置
分组讨论 :1、这样收集到的氯气是否纯净 ? 交流与讨论 :这个装置可分为几个部分?各部分所起的 作用分别是什么? 2、该分别用什么除去这些杂质气体?
MnO2 + 4HCl(浓) === MnCl2 +Cl2 +2H2O
除去HCl
除去水 蒸气
发生装置
净化装置
收集装置
尾气吸收 装置
电解饱和食盐水装置的结构
直流电源
石 墨 铁 棒
饱和食盐水
实验现象
1
结论
通电后有气体物 质生成 有氯气生成
两极均产生气泡
碳棒附近有黄绿色、刺激 2 性气味的气体产生,能使 湿润的淀粉碘化钾试纸变 蓝
3
铁棒周围的颜色变红 有碱性物质生成 有氢气生成
将铁棒上方收集到的气体 4 靠近火焰,有爆鸣声
电解饱和食盐水装置的结构
专题 2
从海水中获得的化学物质
永强 ——永嘉场 ——永嘉盐场
含量/g
30 25 20 15 10 5 0
0.712 1.11 5.11 27.2
KCl
CaCl2 2
MgCl2 2
NaCl
每千克海水中几种氯化物的含量
氯气的生产原理
思考:你知道通过电解水可以获得哪些物质吗
回忆联想:水的电解
水通电反应的化学方程式:
直流电源 石
墨
铁 棒
饱和食盐水
NaOH 溶液
氯气的发现史
1774年,瑞典化学家舍勒发现氯气。
1810年,英国化学家戴维研究后得出这 种气体仅由一种元素组成。我国早年译 文将其译成“绿气”,后改为氯气。
戴维
分液漏斗 圆底烧瓶
浓盐酸
苏教版化学必修一2.1.2 从海水中获得的化学物质-《氯气》教学设计与反思

《氯气》教学设计与反思一.教材分析和学生情况分析1.教材的地位和作用本节学习化学特有的科学方法“结构决定性质,性质影响其存在制备和应用”,对以后研究其它非金属及其分合物具有指导意义。
从教育目的看,氯及其化合物在生活、生产上具有广泛的应用,研究它更具有现实意义。
2.教学重点、难点重点:氯气的化学性质,氯水的成分,氯气与强碱的反应。
难点:探究氯气与水反应的产物以及次氯酸的漂白作用。
3.学生起点能力分析(1)知识准备:知道氢气、钠、铁能在氯气里燃烧;(2)技能准备:能独立进行简单的实验操作;(3)态度:好奇心强,但探究意识淡薄,易将科学神化;4.教学目标的制定新课程倡导“用教材教”,而非“教教材”。
因此,只有准确理解和把握教材内容及其呈现方式所体现的课程目标和教育,深入分析和究掘教材内容的认知价值和情意方式,深刻感悟和领会教材内容背后所蕴含的思想、观点和方法等,才能在化学教学设计时确定适合的教学目标。
(1)知识与技能①能描述氯气的物理性质②掌握氯气与金属,非金属,与水以及碱的反应③知道氯气是一种很活泼的非金属④通过探究实验,培养分析问题的能力,设计并完成实验的能力(2)过程与方法①通过实验录像观察、分析、归纳燃烧的定义②通过观看相像,学会筛选信息进行交流③经历氯气漂白实验演示,对氯气与水反应的产物以及次氯酸的漂白作用的探究,学习科学探究的基本方法,提高科学探究能力。
(3)情感、态度与价值观①感受舍勤的成就和遗憾,体会质疑是科学研究的重点品质。
②经历人类认识燃烧的三个阶段,体会科学的历史和本质。
③关注氯气泄漏事件,能够对化学有关的社会和生活问题做出合理的判断。
二.教法和学法分析教学方法是以教学目标为导向,以学生情况为依据,以教学内容为基础,以培养学生素养为目的来选择。
本节元素化合物知识内容的教学,就不能孤立地死记硬背有关物质的性质,而要突出化学学科以实验为基础的特点,加强对典型反应和现象的感知,注重与社会、生活实际的联系,最终使学生形成“结构决定性质,性质影响其存在、制备和应用”的思维方式,掌握元素化合物知识的内在联系。
高中化学专题3从海水中获得的化学物质2.2碳酸钠碳酸氢钠2教案苏教版1

碳酸钠碳酸氢钠本节课学习内容是苏教版高中化学必修1专题3第二单元第2节中《碳酸钠碳酸氢钠》,在本节所介绍的碳酸钠的性质和应用中,大多数都在水溶液中进行的,如碳酸钠与酸反应、碳酸钠转化为碳酸氢钠等,这些反应的本质都是离子反应,为后面离子反应的学习做好铺垫。
1.通过实验探究方法对比研究了解碳酸钠、碳酸氢钠的性质,并知道它们在生产生活中的用途。
2.通过实验探究碳酸钠、碳酸氢钠的化学性质,初步形成基于物质构成对物质性质进行预测和检验的认识模型。
3.通过体验实验探究和问题讨论的过程,了解实验研究化学物质的一般方法,初步形成分析推理、综合归纳的能力,培养科学探究与创新意识核心素养。
4.通过对侯氏制碱法的学习,培养科学态度与社会责任核心素养.实验探究碳酸钠碳酸氢钠性质差异1.资料收集、幻灯片制作2.化学实验准备①通入CO 2②适量H +板书设计碳酸钠 碳酸氢钠一、碳酸钠 碳酸氢钠物理性质比较二、碳酸钠 碳酸氢钠化学性质比较三、碳酸钠 碳酸氢钠相互转化四、碳酸钠 碳酸氢钠用途五、侯氏制碱法NaCl+NH 3+CO 2+H 2O==NaHCO 3+NH 4ClNa 2CO 3 NaHCO 32NaHCO3∆==Na2CO3+ CO2↑+ H2O本节课的教学内容《碳酸钠碳酸氢钠》,在九年级化学下册第十一单元课题1《生活中常见的盐》中已经部分的接触,当时主要了解了碳酸钠、碳酸氢钠的俗名、化学式、物理性质,并通过实验得出碳酸钠的几点化学性质.鉴于此,本节课教学中要认真处理新知识的学习与旧知识的衔接以及教学内容的升华呢.重点应在碳酸钠、碳酸氢钠性质的差异,利用两者在性质方面的差异选择合适的方法鉴别碳酸钠和碳酸氢钠。
本节课主要以探究实验探讨碳酸钠与碳酸氢钠性质的差异,在学生做探究实验过程中,教师指导学生实验,对存在的不足及时提醒,并要求学生改正。
新苏教版高中化学必修1课件1:3.3.2 从海水中提取镁、从海带中提取碘

(4) 实验室从海带中提取单质碘的方法是:取样→灼烧→溶解→过滤→萃
取。
( ×)
2.海带中含有丰富的碘,有人设计如下步骤:
①将海带灼烧成灰,在灰中加水搅拌;②加四氯化碳充分振荡静置;③通入氯
气;④过滤;⑤用分液法分离液体混合物。合理操作的先后顺序是( D )
A.①②③④⑤
B.①④②③⑤
C.①②④③⑤
、 、 ;
镁与水反应的剧烈程度 弱 于钠与水反应,说明镁的还原性 弱 于
钠。
能力提升
一、海水提镁及海带中碘元素的检验
[问题探究] 问题 1.海带中的碘元素主要以 I-的形式存在,怎样设计实验证明海带中含 有碘? 提示:①用剪刀剪碎海带,用酒精湿润,放入坩埚中。②灼烧海带至完全成 灰,停止加热,冷却。③将海带灰加蒸馏水溶解,搅拌、煮沸、过滤。④在 滤液中滴加稀 H2SO4 及 H2O2,然后加入几滴淀粉溶液。如果淀粉溶液变蓝 色则证明海带中含有碘元素。
通电 ③MgCl2(熔融)=====Mg+Cl2↑。
知识点拨:由 MgCl2·6H2O 加热制取无水 MgCl2 时,要不断通入干燥的 HCl 气 体,防止 MgCl2 水解生成 Mg(OH)2。
3.镁的性质 (1)镁的原子结构
镁的原子结构示意图为:
原子最外层有 2 个电子,在化学反应中容
易应原理:2H++2I-+H2O2===I2+2H2O。 (2)实验步骤及证明方法
【对点训练】
1.已知 MgO、MgCl2 的熔点分别为 2 800 ℃、604 ℃,将 MgO、MgCl2 加热
熔融后通电电解,都可得到金属镁。从海水中提取金属镁,正确的方法是( D )
二、从海带中提取碘
1.海带中提碘 (1)流程:干海带→浸泡→氧化→过滤→提纯→碘单质。 (2) 以 氯 气 为 氧 化 剂 , 制 取 碘 单 质 的 化 学 反 应 方 程 式 为 : ___C_l2_+__2_K__I=_=__=_2_K_C_l_+__I_2___。
专题3从海水中获得的化学物质复习 高一上学期化学高中化学苏教版(2020)必修第一册

③关闭电源,打开U形管左端的橡皮塞,向溶液中滴加1~2滴酚酞溶液,观察溶 液的颜色。
(2)现象与推理
实验现象 ① 出现爆鸣声 ② 产生黄绿色的气体
结论 a管中的气体为氢气 b管中的气体为氯气
③
铁棒端溶液变红,石墨棒端溶液不 U形管左端溶液显碱性,右端溶液不
5.含氯消毒剂的合理使用 (1)漂白粉应密封、避光保存,并置于阴凉干燥处。 (2)含氯漂白剂与洁厕剂(含有盐酸)不能混合使用,因为两者混合会反应生成氯气。 (3)新型灭菌消毒剂——二氧化氯:杀菌、消毒能力比氯气强。
次氯酸(HClO)的性质及应用
1.弱酸性 HClO是一种比H2CO3还弱的弱酸。 写出下列化学方程式: HClO与NaOH反应:HClO+NaOH=NaClO+H2O。 HClO与Ca(OH)2反应:2HClO+Ca(OH)2=CaCl2+2HClO。
粗盐提纯的思路
溶解
过滤
除去可溶性杂质
过滤
蒸发结晶
可溶性杂质的去除
杂质离子 Na2SO4 MgCl CaCl2
除杂试剂 __B_a_C__l2_溶__液 _N__a_O_H__溶_ 液
N_a_2_C_O__3_溶液
离子方程式 B_a_2_+_+__S_O_24_-_=_=_=_B__aS__O_4_↓____ _M_g_2_+_+__2_O__H__-_=_=_=_M__g_(_O_H__)_2↓_ C_a_2_+_+__C_O_23_-_=_=_=_C__aC__O_3_↓___
②氧化钠溶于盐酸:Na2O+2HCl===2NaCl+H2O; ③氧化钠与CO2反应:Na2O+CO2===Na2CO3 5.(1)过氧化钠与水反应的化学方程式是2Na2O2+2H2O===4NaOH+O2↑。 (2)过氧化钠与二氧化碳反应的化学方程式是2Na2O2+2CO2===2Na2CO3+O2, (3)与氧气反应
从海水中获得的化学物质公开课一等奖优质课大赛微课获奖课件

含有离子:
Cl-、
+
H
请思考:
如何检查也许含有Cl-和H+呢?
请设计最合理试验方案。
氯水的化学性质.swf
第35页
氯水
检查Cl-离子试验设计:
往氯水中滴加AgNO3溶液和稀HNO3溶 液,假如有白色浑浊或沉淀出现,则阐明 氯水中含有Cl-离子。
试验现象:有白色浑浊出现
试验结论:氯水中含有Cl-离子
BD)
B.氯水 D.CuCl2溶液
第52页
巩固练习:
5.用自来水养鱼时,将氯水注入鱼缸前需在阳光
下曝晒一段时间,主要目的是( B )
A.起杀菌作用
B.使水中HClO分解
C.提升水温
D.增长水中O2含量
第53页
巩固练习:
6.漂白粉制取原理反应方程式
是 2Cl2+2Ca(OH)2=====CaCl2+Ca(ClO)2+2H2O ;
溶剂
因此,氯气是一个主要化工原料。
第47页
总结
一、物理性质
氯气是一个黄绿色有刺激性气味气体,有毒,密
度比空气大,能溶于水,易液化。
二、化学性质 1、与金属单质反应 Cu +
点燃
Cl2
=
光照
CuCl2
2、与非金属单质反应 H2 + Cl2
2HCl
3.与水反应: Cl2+H2O 4.与碱反应
HCl+HClO
第10页
阳离子互换膜电解槽
离子互换膜作用: (1)预防氯气和氢气混合而引起爆炸 (2)避免氯气与氢氧化钠反应影响氢氧化钠产量
第11页
厂址选择:当代化工生产要求有较大生产规模;
调查研究 厂址选择涉及原料、水源、能源、土地供应、市场
海水中获得的化学物质

【资料MgCl2(熔融) 通=电Mg+Cl2 卡】
英国化学家戴维
资料:1808年戴维建造了更巨大的电池 组,电解苦土(含镁化合物)从中发现 了镁元素,后来工业上通过电解熔融的 MgCl2来制取Mg.
在工业上制备一种物质需要解决哪些方面 的问题?
解决三个问题:原料——原理——工艺流程
解决问题的基本原则:丰富易得、科学可行、经济环保
从海水中获得化学物质,来 源于自然,服务于人类,人 与自然和谐相处,保护环境, 从你我做起。
海水中获得的 化学物质
一.每千克海水中几 种氯化物的 含量
含量/g
20 15 10 -
1.8×1015吨
5.11g/Kg 0.511%
5-
KCl CaCl2 MgCl2 NaCl 每千克海水中几种氯化物的含量
电解时氯化钠要熔融,氯化钠的熔点为801 ℃,比较高。所以用熔融温度约为580 ℃的 40%氯化钠和60%氯化钙的低共熔物可降低 电解时所需的温度,降低了钠的蒸气压。电 解时,氯气在阳极放出,当电流通过熔盐时, 金属钠和金属钙同时被还原出来,浮在阴极 上方的熔盐上面,从管道溢出。把熔融的金 属混合物冷却到105 ℃~110 ℃,金属钙成 晶体析出,经过滤就可以把金属钠跟金属钙 分离。
学考复习从海水中获得的化学物质

2Na + H2 = 2NaH NaH + H2O = NaOH + H2 ;NaH是强的还原剂。
钠及其化合物知识网络:
(3)工业制钠:
电解熔融的NaCl 2NaCl(熔融) 通电 2Na + Cl2↑。
(4)钠的用途:
①作强还原剂,在熔融的条件下钠可以制取一些 金属,如钛、锆、铌、钽等;
一、氯及其化合物
1、氯气的工业制法
原料:氯化钠、水。
主要以海盐为原料。海盐中含硫酸钙、
硫酸镁、氯化镁等杂质,要净化后制成饱
和食盐水再电解。
原理:电解饱和食盐水。
装置:阳离子隔膜电解槽。
反应式:
2NaCl
+
2H2O
通电
== 2NaOH
+
H2↑
+Cl2↑
例题: 在电解食盐水之前,需要提纯食盐 水。为了除去粗盐中的Ca2+、Mg2+、SO42- 及泥沙,可将粗盐溶于水,然后进行下列五
A、熔成小球并在液面上游动 B、有气体生成 C、溶液底部有银白色物质生成 D、溶液变浑浊
解析:将一小块钠投入饱和澄清石灰水中,钠与水剧烈反应,所 以首先观察到钠与水反应的一系列现象。随着2Na+2H2O=2NaOH+H2↑反 应的进行,水被消耗,溶液的温度升高,由于Ca(OH)2的溶解度随温度 的升高而降低,所以溶液中的Ca(OH)2有部分析出,可以观察到溶液变 浑。
从海产品中提取碘:
水
氯气
碘
海带 浸泡 氧化 过滤 提纯
单
质
Cl-、Br-、I-的检验:AgNO3─HNO3法 Ag+ + Cl- == AgCl↓ 白色沉淀 Ag+ + Br- == AgBr↓ 浅黄色沉淀 Ag+ + I- == AgI↓ 黄色沉淀
高中化学专题3从海水中获得的化学物质第3单元第1课时粗盐提纯从海水中提取溴教学案苏教版第一册

第1课时粗盐提纯从海水中提取溴发展目标体系构建1。
初步了解海洋化学资源的分布,了解粗盐的提纯及海水中提取溴的基本原理和方法,能依据物质性质及其变化综合利用资源。
2。
认识化学理论与技术在资源利用中发挥的积极作用,培养科学态度与社会责任的化学核心素养。
一、粗盐提纯1.不溶性杂质的除去2.粗盐中可溶性杂质的除去杂质加入的试剂化学方程式Na2SO4BaCl2溶液Na2SO4+BaCl2===BaSO4↓+2NaCl MgCl2NaOH溶液MgCl2+2NaOH===Mg(OH)2↓+2NaClCaCl2Na2CO3溶液CaCl2+Na2CO3===CaCO3↓+2NaCl 在除去上述粗盐中可溶性杂质的过程中,是否考虑除杂试剂用量问题除杂试剂是否会引入新的杂质?[提示]除杂试剂应稍过量,这样才能使杂质离子完全变成沉淀,通过过滤除去,但过量的除杂试剂又成为新的杂质。
二、从海水中提取溴1.溴的提取海水提取粗食盐后的母液,通入氯气将其中的溴离子转化为单质溴。
2.海水提溴的工艺流程3.含溴化合物的应用(1)含溴物质用于制备药物、感光剂等。
(2)溴是制造农药杀虫剂、阻燃剂的原料。
1.判断正误(正确的打“√”,错误的打“×”。
)(1)粗盐提纯实验中,加入足量碳酸钠溶液的作用只是为了除去Ca2+. (×)(2)粗盐提纯实验中,加入足量盐酸的作用是除去多余的OH-和CO错误!。
(√)(3)要除去氯化钠溶液中含有的氯化镁,可加入适量的氢氧化钠溶液后过滤。
(√)(4)海水中提取溴的过程中不发生氧化还原反应. (×)2.在“粗盐提纯”的实验中,下列做法正确的是()A.把浑浊的液体倒入蒸发皿内加热B.开始析出晶体后用玻璃棒搅拌C.加入试剂的顺序为Na2CO3、BaCl2、NaOH、HClD.用过滤法除去粗盐中的泥沙D[未过滤即蒸发,不能除去泥沙,所以A项错误;加热过程中应用玻璃棒不断地搅拌,所以B项错误;应先加入BaCl2,再加Na2CO3以除去过量的Ba2+,所以C项错误。
从海水中获得的化学物质

实验注意: 实验注意:一贴二低三靠 ①“一贴”是指滤纸折叠角度要与漏斗内壁口径吻合, ①“一贴”是指滤纸折叠角度要与漏斗内壁口径吻合,使 一贴 湿润的滤纸紧贴漏斗内壁而无气泡, 湿润的滤纸紧贴漏斗内壁而无气泡,因为如果有气泡会影响过 滤速度. 滤速度. ②“二低”是指滤纸的边缘要稍低于漏斗的边缘,二是在 ②“二低”是指滤纸的边缘要稍低于漏斗的边缘, 二低 整个过滤过程中还要始终注意到滤液的液面要低于滤纸的边缘。 整个过滤过程中还要始终注意到滤液的液面要低于滤纸的边缘。 这样可以防止杂质未经过滤而直接流到烧杯中, 这样可以防止杂质未经过滤而直接流到烧杯中, ③“三靠 一是指待过滤的液体倒入漏斗中时, 三靠” ③“三靠”一是指待过滤的液体倒入漏斗中时,盛有待过 滤液体的烧杯的烧杯嘴要靠在倾斜的玻璃棒上, 滤液体的烧杯的烧杯嘴要靠在倾斜的玻璃棒上,防止液体飞溅 和带过滤液体冲破滤纸;二是指玻璃棒下端要轻靠在三层滤纸 和带过滤液体冲破滤纸; 处以防碰破滤纸; 处以防碰破滤纸;三是指漏斗的颈部要紧靠接收滤液的接受器 的内壁,以防液体溅出。 的内壁,以防液体溅出。
钠的化学性质
钠原子的最外层只有1个电子,很容易失去。因此, 钠原子的最外层只有 个电子,很容易失去。因此,钠的化学 个电子 性质非常活泼,主要表现在: 性质非常活泼,主要表现在: 1.钠跟氧气的反应 钠跟氧气的反应 观察演示实验: 观察演示实验:钠与氧反应 在常温时 在常温时4Na+O2=2Na2O + = 在点燃时 淡黄色) 在点燃时2Na+O2Na2O2(淡黄色 + 淡黄色 过氧化钠) (过氧化钠 过氧化钠 过氧化钠比氧化钠稳定。 过氧化钠比氧化钠稳定。 2.钠跟硫等非金属的反应 钠跟硫等非金属的反应 钠除了能跟Cl2直接化合外,还能跟很多其它非金属直接化合, 直接化合外, 钠除了能跟 直接化合外 还能跟很多其它非金属直接化合, 如跟硫化合时甚至发生爆炸。 如跟硫化合时甚至发生爆炸。 2Na+S=Na2S + = 硫化钠) (硫化钠 硫化钠
海水中获得的化学物质

收集
尾气吸收
防止倒吸,吸 收易溶于水的 气体 如HCl、NH3、 SO2等
问:如何利用图示装置实现氢气、二氧化碳、 氨气等气体的收集? a b
请思考图示的装置都有哪些用途?
2、氯气的性质--物理性质 ⑴黄绿色、刺激性气味、气体、有毒 -1 3.17g· L ⑵标况下的密度= ,密度比空气大 向上排空气法收集 液氯为黄绿色 ⑶易液化 工业上液化后保存在钢瓶中 (干燥氯气不与Fe反应) ⑷能溶于水,1体积水可溶解2体积氯气 (1体积水可溶解500体积HCl,700体积NH3) 氯气泄漏该如何处理?
⑺氯气的用途:消毒、制盐酸、漂白粉、 氯仿等有机溶剂 3、HCl性质
△ 制备:NaCl +H2SO4 (浓) ==NaHSO4+HCl 固体 4、ClO2
3、溴、碘的性质
(1)生产原理 溴
粗盐提取后的母液
通Cl2
2KBr+Cl2=2KCl+Br2 溶解于水中的Br2 热空气 水蒸气 Br2蒸气 冷 凝 粗溴 精制 提纯 高纯溴
原料:海水
2.提取碘
干海带
加水浸泡
过 滤 含I-的溶液 通Cl2 过滤 粗碘
提纯
滤渣
2KI+Cl2=2KCl+I2
碘单质
原料:海产品
灼烧后的海带
加水浸泡
过 滤 含I-的溶液 通Cl2 2KI+Cl2=2KCl+I2 碘水
加CCl4萃取分液
滤渣
实验 从海带中 提取碘
I2的CCl4溶液
蒸馏
I2
(3)物理性质
⑶在工业生产中,电解食盐水常在电解槽中进行。 为避免电解产物之间发生反应,常用阳离子交换 膜将电解槽分隔成两部分。
从海水中获得的化学物质 (2)

专题2 从海水中获得的化学物质
(3)酸式盐的电离:多元强酸酸式盐与多元弱酸酸式盐的阴离 子电离情况不同。 如 NaHSO4 溶液中:N__a_H_S_O__4_=_=_=_N_a_+_+__H__+_+__S_O__24-__________; NaHCO3 溶液中:N__a_H_C__O_3_=_=_=_N__a_+_+__H_C__O_3-______________、 HCO- 3 H++CO23-。
栏目 导引
专题2 从海水中获得的化学物质
写出氯化铵、次氯酸在水溶液中的电离方程式: ______________________、______________________。 答案:NH4Cl===NH4++Cl- HClO H++ClO-
栏目 导引
专题2 从海水中获得的化学物质
电离方程式书写的思维模型
栏目 导引
专题2 从海水中获得的化学物质
2.下列物质中,属于电解质的是________,属于非电解质的 是________;属于强电解质的是________,属于弱电解质的 是________。(填序号) ①硫酸 ②氯气 ③硫酸钡 ④酒精 ⑤铜 ⑥醋酸 ⑦氯化氢 ⑧蔗糖 ⑨氨气 ⑩CO2
栏目 导引
(2)多元弱酸的电离分步书写,多元弱碱的电离一步写完。如 H2CO3 : _H__2C__O_3____H__+_+__H_C__O_3-________________________ , __H__C_O__- 3____H__+_+__C_O__23-_____________________ ; Fe(OH)3 : __F__e(_O__H_)_3____F_e_3+_+__3_O__H_-________________。
高中化学专题3从海水中获得的化学物质第三单元海洋化学资源的综合利用第二课时从海水中提取镁从海带中提取

第二课时从海水中提取镁从海带中提取碘必备知识基础练进阶训练第一层知识点一海水提镁1.海水中含有MgCl2,是镁的重要来源之一。
从海水中提取镁,可以按照如下步骤:①把贝壳制成石灰乳;②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥产物;④将所得产物熔融后电解。
关于提取镁,下列说法不正确的是()A.此法的优点之一是原料来源丰富B.进行①②③步操作的目的是从海水中提取MgCl2C.第④步电解会产生Cl2D.以上提取镁的过程中涉及到的反应有分解反应、化合反应和置换反应知识点二镁的性质2.下列物质的转化不能通过一步反应实现的是()A.Mg→MgO B.MgO→Mg(OH)2C.MgO→MgCl2D.MgCl2→Mg(OH)23.下列有关说法正确的是()A.镁燃烧发出耀眼的红光,因此常用来制造信号弹和焰火B.自然界中的镁主要以单质的形式存在于地壳和海水中C.镁着火可用泡沫灭火器扑灭D.电解熔融的MgCl2可得到金属镁4.镁条在二氧化碳中剧烈燃烧,瓶壁有黑色和白色粉末,不能说明()A.二氧化碳显氧化性B.二氧化碳中含有碳元素C.二氧化碳是酸性氧化物D.助燃和不助燃是相对的知识点三海带提碘5.海带中含碘元素,有人设计了以下步骤来提取碘:①通足量氯气 ②将海带烧成灰,向灰中加水搅拌 ③加入CCl 4,振荡 ④过滤 ⑤用分液漏斗分液合理的操作顺序为( )A .②④①③⑤B .②①③④⑤C .①③⑤②④D .③①②⑤④6.从海带中提取碘的实验过程中,涉及下列操作,其中正确的是( )知识点四 加碘盐中碘元素的检验7.加碘食盐中碘元素以碘酸根(IO -3 )的形式存在。
已知在酸性条件下,IO -3 离子能跟碘离子(I -)发生反应生成碘(I 2),碘能使淀粉变色。
现提供下列试剂和生活中常见的物质:①碘化钾溶液(溶液中含有I -);②白醋;③白糖;④白酒;⑤纯碱;⑥淀粉。
欲通过实验证明加碘食盐中存在碘酸根离子,必须选用的试剂和物质是( )A .①②③B .①②⑥C .①⑤⑥D .②④⑤关键能力综合练 进阶训练第二层一、选择题:每小题只有一个选项符合题意。
从海水中获得的化学物质

•海水中的成分可以划分为五类:
•1.主要成分(大量、常量元素):指海水中浓度大于 1×106mg/kg的成分。属于此类的有阳离子Na+,K+,Ca2+, Mg2+和Sr2+ 五种,阴离子有Clˉ,SO42ˉ,Brˉ,HCO3ˉ(CO32ˉ ),Fˉ五种,还有以分子形式存在的H3BO3,其总和占海水盐分 的99.9%。所以称为主要成分。
• 蒸发,结晶
•实验注意:一贴二低三靠
• ①“一贴”是指滤纸折叠角度要与漏斗内壁口径吻合,使湿 润的滤纸紧贴漏斗内壁而无气泡,因为如果有气泡会影响过滤 速度. • ②“二低”是指滤纸的边缘要稍低于漏斗的边缘,二是在整 个过滤过程中还要始终注意到滤液的液面要低于滤纸的边缘。 这样可以防止杂质未经过滤而直接流到烧杯中, • ③“三靠”一是指待过滤的液体倒入漏斗中时,盛有待过滤 液体的烧杯的烧杯嘴要靠在倾斜的玻璃棒上,防止液体飞溅和 带过滤液体冲破滤纸;二是指玻璃棒下端要轻靠在三层滤纸处 以防碰破滤纸;三是指漏斗的颈部要紧靠接收滤液的接受器的 内壁,以防液体溅出。
实验操作
1.溶解
2.过滤 过滤时漏斗里的液面不要高于滤纸边缘
•3.蒸发 •把得到的澄清滤液倒入蒸发皿.把蒸 发皿放在铁架台的铁圈上,用酒精灯 加热(图). •同时用玻璃棒不断搅拌滤液(晶体析 出时,防止固体飞溅). 等到蒸发皿中出现较多量固体时,停 止加热.利用蒸发皿的余热使滤液蒸 干.
•4.用玻璃棒把固体转移到纸上,称量 后,回收到教师指定的容器.比较提 纯前后食盐的状态并计算精盐的产率 .
与酸反应:NaHCO3+HCl=NaCl+H2O+CO2↑
与碱反应:NaHCO3+NaOH=Na2CO3+H2O
(新教材适用)高中化学专题3从海水中获得的化学物质第3单元海洋化学资源的综合利用第2课时从海水中提取

第2课时从海水中提取镁和从海带中提取碘基础巩固1.由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。
其先后顺序正确的是( )。
A.②④⑤③①B.③②④①⑤C.③④②⑤①D.②④③⑤①答案:D解析:由海水中提取镁可知,先在海水中加入熟石灰,使Mg2+变成Mg(OH)2沉淀,过滤得到Mg(OH)2,然后再加盐酸溶解、浓缩结晶,在一定条件下脱水干燥,最终得到无水氯化镁。
2.镁粉是焰火、闪光粉中不可缺少的原料,工业制造镁粉是将镁蒸气在气体中冷却。
下列气体能用作镁蒸气冷却气的是( )。
A.空气B.CO2C.H2D.N2答案:C解析:镁能与O2、CO2、N2发生化学反应,但与H2不反应,故H2能作为镁蒸气的冷却气。
3.将氯水加入KI溶液中,用力振荡,再加入四氯化碳,振荡后静置,看到的现象是( )。
A.液体为紫红色B.液体为无色C.液体分两层,上层为紫红色,下层接近无色D.液体分两层,上层接近无色,下层为紫红色答案:D解析:Cl2将I氧化生成I2,I2被CCl4萃取,所以上层接近无色,下层为紫红色。
4.下列不能使淀粉碘化钾试纸变蓝的物质是( )。
A.碘水B.溴水C.氯水D.溴化钠溶液答案:D解析:因氧化性:Cl2>Br2>I2,则加入氯水、溴水,均可将I氧化为I2,淀粉遇碘变蓝;另外直接加入碘水,试纸也变蓝;而NaBr溶液与碘化钾不反应,不能使试纸变色。
5.稀碘水和稀溴水的颜色非常浅,近乎无色。
检验稀碘水和稀溴水时,所用的最佳试剂是( )。
A.淀粉溶液B.氯水C.NaOH溶液D.NaBr溶液答案:A解析:氯水、NaBr溶液与溴水、碘水都不反应,均不能区分;NaOH溶液与溴水、碘水都反应,能使溴水、碘水都褪色,现象相同,不能区分;淀粉溶液遇I2变蓝色,可以区分。
6.已知溴易挥发 ,碘易升华,向含有NaBr和KI的混合溶液中通入过量氯气充分反应后将溶液蒸干,并灼烧所得物质,最后剩余的固体是( )。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
查阅有关资料了解人们 是如何从海水中获得氯 化钠和使用氯化钠的。
氯化钠的应用:
生活----维持生命运动必需的物质, 防腐、食品腌制等等。
医疗----生理盐水。 工业----纯碱、烧碱、氯气、盐酸等。
氯气的生产原理
(一)氯气的工业制法 1、电解饱和食盐水
回忆联想:水的电解
1.电极名称
2.电极反应产物
水的化学方程式?
实验现象
结论
1
两极均产生气泡
通电后有新的气体 物质生成
2
将铁棒上方收集到的气体靠 近火焰,有轻微的爆鸣声
有氢气生成
黄绿色、刺激性气味的气体 3 产生,湿润的淀粉碘化钾试
纸变蓝
有氯气生成
4
铁棒周围的颜色变红
有碱性物质生成
实验原理:
氯化钠和水发生电解反应,在阳极生成氯气, 在阴极生成氢气和氢氧化钠。
轻元素,如氘、氚的聚变,在一定的条件下,它们的原子核可以相互碰撞 聚变成为一种新的—氦核,同时将蕴藏于其中的巨大能量释放出来。1千克氘 燃料,至少可以抵得上4千克铀燃料或者10000吨优质煤燃料。
氘在海水中分布甚广,储量巨大。海水中氘的含量为十万分之一,即每升 海水中含有0.03克的氘,海水中氘的总储量竟达几百亿吨,可为人们提供上亿 年的能源消费。
科学家预测,核聚变技术和海洋氘—氚提取技术在最近20年内将有望获得 重大突破,这给人类摆脱能源危机的前景带来了无限生机。
浙江:国内最大海水淡化工程在玉环电厂启动
中国宁波网消息(05年11月04日):我国目前最大的海水淡化工 程——浙江华能玉环电厂海水淡化系统工程正式启动。该工程可日 产淡水近3.5万吨,而此前国内在建的其他海水淡化工程最大日处 理能力仅为1万吨。
海水中的核能──人类未来最有希望的能源
人类利用核能的方式,主要有重元素的裂变与轻元素的聚变。重元素,如铀的 裂变,其基本的原理是采用人工方法轰击铀的原子核,使之分裂,从而释放出 巨大的能量。1千克的铀裂变时所释放出的热量,相当于2500吨优质煤燃烧释 放出的全部热能。
在那浩瀚无际、神奇莫测的海洋中,却溶解有超过陆地储量几千万倍的铀。 1000吨海水中含3克铀,人们用吸附法、共沉法、气泡分离法和藻类生物浓缩 法等从海水中提炼铀。
2、阳离子交换膜电解槽
氯气
阳
极
浓盐
阴 氢气 极
稀碱
膜
Na+
稀盐
浓碱
阳离子交换膜电解食盐水的微观过程
氯碱工业:
以电解食盐水为基础制取氯气等产品的工业。
电 NaOH 解 饱 和 Cl2 食 盐 水
H2
有机合成、造纸、玻璃、肥皂、纺织、印染
NaClO 消毒液
有机合成、氯化物合成、农药
HCl
盐酸
有机合成、金属冶炼
海水晒盐
把海水引入 盐田,利用日光、 风力蒸发浓缩海 水,使其达到饱 和,并进一步使 食盐结晶出来, 这种方法称为太 阳能蒸发法,又 称为盐田法。
含量/g
30
27.2
25
20
15
10
5.11
5 0.712
1.11
0 KCl
CaCl2
MgCl2
NaCl
每千克海水中几种氯化物的含量
元素 浓 度 / 元素 mg.L-1
3.水通电反应的化学 方程式
若向水中加入氯化钠,通电后两个电极上可能 会得到什么物质?
实验:
观察与思考:
按下图装置进行饱和食盐水电解: 1.电解饱和食盐水的实验
装置与电解水有何不同?
2.电解过程中两电极产生
的气体分别是什么?
3.实验中颜色有什么变化?
4.电解过程中产生了什么
新物质?
5.如何书写电解饱和食盐
电极反应式:
阳极:2Cl--2e- = Cl2↑ (氧化反应) 阴极 :2H+ + 2e - = H2↑(还原反应)
电解氯化钠溶液的化学方程式:
通电
2NaCl+2H2O === 2NaOH +H2↑+ Cl2↑
思考:
1.水电解时得到H2和O2,而饱和食盐水电 解时得到H2和Cl2。为什么?
2.由于① Cl2能与NaOH反应生成NaCl 和NaClO;②H2与Cl2混合气体光照会发 生爆炸。工业上电解饱和食盐水时应注意 哪些问题?
浓度/ mg.L-1
氯
19350
溴
67
Cl
Br
钠
10770பைடு நூலகம்
锶
8
Na
Sr
镁
1290
硼
4.6
Mg
B
硫
885
锂
0.17
S
Li
钙
400
铷
0.12
Ca
Rb
钾
380
碘
0.06
K
I
元素
浓度/ mg.L-1
钡
0.03
Ba
钼
0.01
Mo
铀
0.003
U
镍
0.002
Ni
钴
0.0005
Co
金 0.000004 Au
谢谢您的关注
专题 2
从海水中获得的化学物质
你知道浩瀚的大海中究竟蕴藏 着哪些物质吗?请查阅有关资料 了解海水中主要含有的物质和各 元素的含量。
海水中含有80多种元素
海洋,生命的摇篮----丰富的生物资源 海水,占地球上97%的水 ----海水淡化 海水,能源的宝库----潮汐能、化学能、核能 海水,经济发展的支柱----氯化钠
