结构化学课件..
合集下载
结构化学课件

1.
1900年,Planck假设
n
e =hn
66261034J· s
能量量子化
2. 光电效应和光子学说
e =hn
p =h /l
光的波粒二象性
3. 实物微粒的波粒二象性 de Broglie 电子衍射
阴极 栅极
K
E =hn p =h /l
多晶 薄膜
Cs
G
U
高压
屏P
de Broglie 波的物理意义 几率波 粒子的波性是和微粒行为的统计性相联系 一个粒子 通过晶体到达底片的位置不能准确预测
y (q1, q1, q3 ,..., qn ) = y (q1, q1, q3 ,..., qn )
y (q1 , q1 , q3 ,..., qn ) = 0
因为一个任意的函数都可以被一组 完整函数的集合展开
y = cy c y c y = cy ,
1 1 2 2 n n i i i
c , c ,c 为任意常数。
1 2 n
组合系数ci的大小反映yi贡献的多少。
例如:为适应原子周围势场的变化,原 子轨道通过线性组合,所得的杂化轨道 (sp,sp2,sp3等)也是该原子中电子可 能存在的状态。
2
• 量子力学需用线性自轭算符,是为了使和 算符对应的本证值能为实数。
若干物理量及其算符
物理量 位置
动量的 x 轴分量 角动量的 z 轴分量 动能
算符 x
px
x=x
= ih px 2p x
= ih x y Mz 2p y x
Mz= xpy − ypx
ih ih = x y 2p x 2p y
1900年,Planck假设
n
e =hn
66261034J· s
能量量子化
2. 光电效应和光子学说
e =hn
p =h /l
光的波粒二象性
3. 实物微粒的波粒二象性 de Broglie 电子衍射
阴极 栅极
K
E =hn p =h /l
多晶 薄膜
Cs
G
U
高压
屏P
de Broglie 波的物理意义 几率波 粒子的波性是和微粒行为的统计性相联系 一个粒子 通过晶体到达底片的位置不能准确预测
y (q1, q1, q3 ,..., qn ) = y (q1, q1, q3 ,..., qn )
y (q1 , q1 , q3 ,..., qn ) = 0
因为一个任意的函数都可以被一组 完整函数的集合展开
y = cy c y c y = cy ,
1 1 2 2 n n i i i
c , c ,c 为任意常数。
1 2 n
组合系数ci的大小反映yi贡献的多少。
例如:为适应原子周围势场的变化,原 子轨道通过线性组合,所得的杂化轨道 (sp,sp2,sp3等)也是该原子中电子可 能存在的状态。
2
• 量子力学需用线性自轭算符,是为了使和 算符对应的本证值能为实数。
若干物理量及其算符
物理量 位置
动量的 x 轴分量 角动量的 z 轴分量 动能
算符 x
px
x=x
= ih px 2p x
= ih x y Mz 2p y x
Mz= xpy − ypx
ih ih = x y 2p x 2p y
结构化学课件第四章第一节

分子结构模型
80%
原子模型
原子是化学元素的最小单位,由 原子核和绕核运动的电子构成。
100%
分子模型
分子由两个或更多原子通过化学 键连接而成,是物质的基本单位 。
80%
空间构型
分子中原子在空间的排列方式, 包括线性、平面、立体等构型。
化学键类型及特点
01
02
03
离子键
由正负离子间的静电引力 形成,具有高熔点、硬而 脆等特点。
波尔模型
电子只能在一些特定的轨道上运动,在这些轨道上 运动的电子既不吸收能量,也不放出能量。
原子核外电子排布
电子层
核外电子经常出现的区域称电 子层。电子层可用n(n=1、2、 3…)表示,n=1表明第一层电 子层(K层),n=2表明第二电 子层(L层),依次n=3、4、5 时表明第三(M层)、第四(N 层)、第五(O层)。
04
配合物结构与性质
配合物组成和命名
配合物组成
配合物由中心原子(或离子)和 配体组成,中心原子通常是金属 元素,配体可以是无机或有机分 子或离子。
配合物命名
配合物的命名遵循一定的规则, 包括中心原子、配体和配位数的 标识,以及配合物类型的区分。
配合物空间构型和异构现象
配合物空间构型
配合物的空间构型取决于中心原子和 配体的排列方式,常见的空间构型有 直线型、平面三角形、四面体型等。
金属晶体
由金属阳离子和自由电子通过 金属键结合形成的晶体,具有 良好的导电性、导热性和延展 性。
晶体中粒子间作用力
离子键
正负离子之间的静电吸引力,作用力强,无方向 性和饱和性。
分子间作用力
分子间的相互作用力,包括范德华力和氢键等, 作用力较弱。
结构化学PPT课件

1 c1 o.5 0 s o 4 0 0.20
解得: c22 0.20
c2 0.45
c1210.80 c1 0.89
据此,可计算出H2O 中,两个孤对电子所在轨道的成分 ( α=0.30 ,β=0.7),夹角(θ=115.4o )
CHENLI
19
例 2. NH 3
实验测定 NH3 分子属C3v 点群。3个 N—H 键 中 s 、p 成分相同。∠HNH=107.3o。
D∞h D3h Td
D4h D3h C4v Oh
CO2 , N3BF3 , SO3
CH4
Ni(CN)42PF5 IF5 SF6
CHENLI
13
• 杂化轨道满足正交性、归一性
例: i aisbip
由归一性可得: i *id1 ai2 bi2 1
由正交性可得: i*jd0
i j
★根据这一基本性质,考虑杂化轨道的空间分布及 杂化前原子轨道的取向,就能写出杂化轨道中原子轨道的 组合系数。
b0 .5p 5 x0 .7Cp H0 y EN L0 I .4s5
18
若不需区分 px 和 py ,只需了解杂化轨道中 s成分和 p 成分,
可按
cos 计算夹角。
对于 H2O 中的 O 原子只有 s 轨道和 p 轨道参加杂化。
设 s 成分为 α, p 成分β=1- α
则:
1 c o s 0
y H
0 .6c 1 1 p x 0 .7c 1 9 p y c2 s
根据原子轨道正交、归一条件,可得: 解之,得 c12 0.80 c1 0.89
x
{ c12 c22 1 0 .62c 1 1 2 0 .72c 9 1 2 c 2 2 0
结构化学课件

第四章 分子对称性
Chapter 4. Molecular Symmetry and Introduction to Group Theory
第四章.分子的对称性
对称 是一种很常见的现象。在自然界
我们可观察到五瓣对称的梅花、桃花,六瓣 的水仙花、雪花、松树叶沿枝干两侧对称, 槐树叶、榕树叶又是另一种对称……在人工 建筑中,北京的古皇城是中轴线对称。在化 学中,我们研究的分子、晶体等也有各种对 称性,有时会感觉这个分子对称性比那个分 子高,如何表达、衡量各种对称?数学中定 义了对称元素来描述这些对称。
in ={E n为偶数,i n 为奇数}
依据对称中心进行的对称操作为反演 操作,处于坐标原点的对称中心的反演操 作i的表示矩阵为:
由此可见,从分子中任一原子至对称 中心连一直线,将此线延长,必可在和对 称中心等距离的另一侧找到另一相同原子。
如果每一个原子都沿直线通过分子中心移动,达到这
个中心的另一边的相等距离时能遇到一个相同的原子,那
位置再反映到H3的位置……整个分子图形不变,n次映转轴
可用符号Sn来表示,即旋转角度(
)再平面反映。
S1 h ; S2 i ; S3 C3 h ; S4独立,包含C2 ; S5 C5 h ; S6 C3 i
即只有 是独立的点群,其余Sn 可化为 或 有些教科书定义的是反轴In,即先进行旋转再进行反演的联合 操作。与Sn点群相同,也只有 是独立点群。它们之间既有 联系,又相互包含,故只需选择一套就够了,对分子多用Sn群, 对晶体多用In群。Sn群与In群的关系如下:
各种对称操作相当于坐标变换 , 可用坐标变换矩阵表示对称操作。C n 轴通过原点和 z 轴重合的k次对称操作 的表示矩阵为:
数学上,对三维空间绕Z轴逆时针转动角度的旋转,可用一个 三维矩阵表示,即:
Chapter 4. Molecular Symmetry and Introduction to Group Theory
第四章.分子的对称性
对称 是一种很常见的现象。在自然界
我们可观察到五瓣对称的梅花、桃花,六瓣 的水仙花、雪花、松树叶沿枝干两侧对称, 槐树叶、榕树叶又是另一种对称……在人工 建筑中,北京的古皇城是中轴线对称。在化 学中,我们研究的分子、晶体等也有各种对 称性,有时会感觉这个分子对称性比那个分 子高,如何表达、衡量各种对称?数学中定 义了对称元素来描述这些对称。
in ={E n为偶数,i n 为奇数}
依据对称中心进行的对称操作为反演 操作,处于坐标原点的对称中心的反演操 作i的表示矩阵为:
由此可见,从分子中任一原子至对称 中心连一直线,将此线延长,必可在和对 称中心等距离的另一侧找到另一相同原子。
如果每一个原子都沿直线通过分子中心移动,达到这
个中心的另一边的相等距离时能遇到一个相同的原子,那
位置再反映到H3的位置……整个分子图形不变,n次映转轴
可用符号Sn来表示,即旋转角度(
)再平面反映。
S1 h ; S2 i ; S3 C3 h ; S4独立,包含C2 ; S5 C5 h ; S6 C3 i
即只有 是独立的点群,其余Sn 可化为 或 有些教科书定义的是反轴In,即先进行旋转再进行反演的联合 操作。与Sn点群相同,也只有 是独立点群。它们之间既有 联系,又相互包含,故只需选择一套就够了,对分子多用Sn群, 对晶体多用In群。Sn群与In群的关系如下:
各种对称操作相当于坐标变换 , 可用坐标变换矩阵表示对称操作。C n 轴通过原点和 z 轴重合的k次对称操作 的表示矩阵为:
数学上,对三维空间绕Z轴逆时针转动角度的旋转,可用一个 三维矩阵表示,即:
《结构化学》课件

《结构化学》ppt课件
contents
目录
• 结构化学简介 • 原子结构与性质 • 分子的电子结构与性质 • 晶体结构与性质 • 结构化学实验结构化学的定义
总结词
结构化学是一门研究物质结构与 性质之间关系的科学。
详细描述
结构化学主要研究原子的排列方 式、电子分布和分子间的相互作 用,以揭示物质的基本性质和行 为。
晶体的电导率、热导率等性质取决于其内 部结构,不同晶体在这些方面表现出不同 的特性。
晶体的力学性质
晶体材料的应用
晶体的硬度、韧性等力学性质与其内部原 子排列密切相关,这些性质决定了晶体在 不同工程领域的应用价值。
晶体材料广泛应用于电子、光学、激光、 半导体等领域,如单晶硅、宝石等。了解 晶体的性质是实现这些应用的关键。
分子的选择性
分子的选择性是指分子在化学反应中对反应物的选择性和对产物的选择性。选择性强的分 子可以在特定条件下优先与某些反应物发生反应,产生特定的产物。
04
晶体结构与性质
晶体结构的基础知识
晶体定义与分类
晶体是由原子、分子或离子在空 间按一定规律重复排列形成的固 体物质。根据晶体内部原子、分 子或离子的排列方式,晶体可分 为七大晶系和14种空间点阵。
电子显微镜技术
• 总结词:分辨率和应用 • 电子显微镜技术是一种利用电子显微镜来观察样品的技术。相比光学显微镜,
电子显微镜具有更高的分辨率和更大的放大倍数,因此可以观察更细微的结构 和组分。 • 电子显微镜技术的分辨率一般在0.1~0.2nm左右,远高于光学显微镜的分辨 率(约200nm)。因此,电子显微镜可以观察到更小的晶体结构、病毒、蛋 白质等细微结构。 • 电子显微镜技术的应用范围很广,例如在生物学领域中,可以用于观察细胞、 病毒、蛋白质等生物样品的结构和形态;在环境科学领域中,可以用于观察污 染物的分布和形态;在材料科学领域中,可以用于观察金属、陶瓷、高分子等 材料的表面和断口形貌等。
contents
目录
• 结构化学简介 • 原子结构与性质 • 分子的电子结构与性质 • 晶体结构与性质 • 结构化学实验结构化学的定义
总结词
结构化学是一门研究物质结构与 性质之间关系的科学。
详细描述
结构化学主要研究原子的排列方 式、电子分布和分子间的相互作 用,以揭示物质的基本性质和行 为。
晶体的电导率、热导率等性质取决于其内 部结构,不同晶体在这些方面表现出不同 的特性。
晶体的力学性质
晶体材料的应用
晶体的硬度、韧性等力学性质与其内部原 子排列密切相关,这些性质决定了晶体在 不同工程领域的应用价值。
晶体材料广泛应用于电子、光学、激光、 半导体等领域,如单晶硅、宝石等。了解 晶体的性质是实现这些应用的关键。
分子的选择性
分子的选择性是指分子在化学反应中对反应物的选择性和对产物的选择性。选择性强的分 子可以在特定条件下优先与某些反应物发生反应,产生特定的产物。
04
晶体结构与性质
晶体结构的基础知识
晶体定义与分类
晶体是由原子、分子或离子在空 间按一定规律重复排列形成的固 体物质。根据晶体内部原子、分 子或离子的排列方式,晶体可分 为七大晶系和14种空间点阵。
电子显微镜技术
• 总结词:分辨率和应用 • 电子显微镜技术是一种利用电子显微镜来观察样品的技术。相比光学显微镜,
电子显微镜具有更高的分辨率和更大的放大倍数,因此可以观察更细微的结构 和组分。 • 电子显微镜技术的分辨率一般在0.1~0.2nm左右,远高于光学显微镜的分辨 率(约200nm)。因此,电子显微镜可以观察到更小的晶体结构、病毒、蛋 白质等细微结构。 • 电子显微镜技术的应用范围很广,例如在生物学领域中,可以用于观察细胞、 病毒、蛋白质等生物样品的结构和形态;在环境科学领域中,可以用于观察污 染物的分布和形态;在材料科学领域中,可以用于观察金属、陶瓷、高分子等 材料的表面和断口形貌等。
结构化学课件

d 轨道与配体间的作用
八面体场中d轨道能级分裂
配合物离子的颜色
所吸收光子的频率与分裂能大小有关。 颜色的深浅与跃迁电子数目有关。
•
配 合 物 的 颜 色
影响o的因素(中心离子,配位体,晶体场)
1 中心M离子:电荷Z增大, o增大
主量子数n增大, o增大
o /cm-1
o /cm-1
2 配位数为 4 的配合物
[BeX4]2-四面体
四 配 位 的 平面正方形,μ=0 配 合 物
四面体,μ=2.83B.M.
3 六配位的配合物
μ=2.4B.M. μ=5.90B.M.
内轨形 外轨形
价键理论小结:
价键理论的优势:直观明了,使用方便, 很好地解释了配合物的空间构型、磁性、稳 定性。
3.分子轨道理论
配位化合物饿分子轨道理论是用分子轨道理论 的观点和方法处理金属离子和配位体的成键作用。
4. 配位场理论
配位场理论是晶体场理论的发展,其实质是配 位化学物的分子轨道理论。在处理中心金属原子 在其周围配位体所产生的电场作用下,金属的原 子轨道能级发生变化时,以分子轨道理论方法为 主,根据配位场的对称性进行简化,并吸收晶体 场理论的成果,阐明配位化合物的结构和性质, 它与纯粹的分子轨道理论有一定的差别,故称配 位场理论。
排布原则: (1)能量最低原理
(2)Hund规则
(3)Pauli不相容原理
电子成对能(P):两个电子进入同一轨
道时需要消耗的能量。
强场:o > P
弱场:o < P
八面体场中电子在t2g和eg轨道中的分布
八面体场中电子在t2g和eg轨道中的分布
例:
o /J
P/J 场
八面体场中d轨道能级分裂
配合物离子的颜色
所吸收光子的频率与分裂能大小有关。 颜色的深浅与跃迁电子数目有关。
•
配 合 物 的 颜 色
影响o的因素(中心离子,配位体,晶体场)
1 中心M离子:电荷Z增大, o增大
主量子数n增大, o增大
o /cm-1
o /cm-1
2 配位数为 4 的配合物
[BeX4]2-四面体
四 配 位 的 平面正方形,μ=0 配 合 物
四面体,μ=2.83B.M.
3 六配位的配合物
μ=2.4B.M. μ=5.90B.M.
内轨形 外轨形
价键理论小结:
价键理论的优势:直观明了,使用方便, 很好地解释了配合物的空间构型、磁性、稳 定性。
3.分子轨道理论
配位化合物饿分子轨道理论是用分子轨道理论 的观点和方法处理金属离子和配位体的成键作用。
4. 配位场理论
配位场理论是晶体场理论的发展,其实质是配 位化学物的分子轨道理论。在处理中心金属原子 在其周围配位体所产生的电场作用下,金属的原 子轨道能级发生变化时,以分子轨道理论方法为 主,根据配位场的对称性进行简化,并吸收晶体 场理论的成果,阐明配位化合物的结构和性质, 它与纯粹的分子轨道理论有一定的差别,故称配 位场理论。
排布原则: (1)能量最低原理
(2)Hund规则
(3)Pauli不相容原理
电子成对能(P):两个电子进入同一轨
道时需要消耗的能量。
强场:o > P
弱场:o < P
八面体场中电子在t2g和eg轨道中的分布
八面体场中电子在t2g和eg轨道中的分布
例:
o /J
P/J 场
《结构化学》PPT课件

(2)反键轨道具有和成键轨道相似的性质,每一轨道也可 按Pauli不相容原理、 能量最低原理和Hund规则安排电子, 只不过能级较相应的成键轨道高,轨道的分布形状不同。
(3)在形成化学键的过程中,反键轨道并不都是处于排斥 的状态,有时反键轨道和其他轨道相互重叠,也可以形成 化学键,降低体系的能量,促进分子稳定地形成。利用分 子轨道理论能成功地解释和预见许多化学键的问题,反键 轨道的参与作用常常是其中的关键所在,在后面讨论分子 的化学键性质时,将会经常遇到反键轨道的作用问题。
方程
i i
ii
分子体系总能量 E = ∑Ei
2.分子轨道是由分子中原子的原子轨道线性组合(li near combination of atomic orbitals, LCAO)而成。
由n个原子轨道组合可得到n个分子轨道,线性组合 系数可用变分法或其它方法确定。由原子轨道形成 的分子轨道,能级低于原子轨道的称为成键轨道, 能级高于原子轨道的称为反键轨道,能级等于或接 近原子轨道的一般为非键轨道。 3.两个原子轨道要有效地组合成分子轨道,必须满 足对称性匹配,能级相近和轨道最大重叠三个条件。 其中对称性匹配是先决条件,其它影响成键的效率。 4.分子中电子按 Pauli不相容原理、 能量最低原 理和Hund规则排布在MO上
三键 三键
CO、NO的电子组态分别如下: CO [( 1σ)2 ( 2σ)2 ( 3σ)2 (4σ)2 (1π)4 (5σ)2 ] NO [( 1σ)2 ( 2σ)2 ( 3σ)2 (4σ)2 (1π)4 (5σ)2 (2π)1 ]
CO :
CO与N2是等电子体,
一样也是三重键:一个σ键, 二个π键,但是与N2分子不 同的是有一个π键为配键, 这对电子来自氧原子。(如 右图所示)CO作为一种配 体,能与一些有空轨道的 金属原子或离子形成配合 物。例如同ⅥB,ⅦB和Ⅷ 族的过渡金属形成羰基配 合物:Fe(CO)5、Ni(CO)4 和Cr(CO)6等。
(3)在形成化学键的过程中,反键轨道并不都是处于排斥 的状态,有时反键轨道和其他轨道相互重叠,也可以形成 化学键,降低体系的能量,促进分子稳定地形成。利用分 子轨道理论能成功地解释和预见许多化学键的问题,反键 轨道的参与作用常常是其中的关键所在,在后面讨论分子 的化学键性质时,将会经常遇到反键轨道的作用问题。
方程
i i
ii
分子体系总能量 E = ∑Ei
2.分子轨道是由分子中原子的原子轨道线性组合(li near combination of atomic orbitals, LCAO)而成。
由n个原子轨道组合可得到n个分子轨道,线性组合 系数可用变分法或其它方法确定。由原子轨道形成 的分子轨道,能级低于原子轨道的称为成键轨道, 能级高于原子轨道的称为反键轨道,能级等于或接 近原子轨道的一般为非键轨道。 3.两个原子轨道要有效地组合成分子轨道,必须满 足对称性匹配,能级相近和轨道最大重叠三个条件。 其中对称性匹配是先决条件,其它影响成键的效率。 4.分子中电子按 Pauli不相容原理、 能量最低原 理和Hund规则排布在MO上
三键 三键
CO、NO的电子组态分别如下: CO [( 1σ)2 ( 2σ)2 ( 3σ)2 (4σ)2 (1π)4 (5σ)2 ] NO [( 1σ)2 ( 2σ)2 ( 3σ)2 (4σ)2 (1π)4 (5σ)2 (2π)1 ]
CO :
CO与N2是等电子体,
一样也是三重键:一个σ键, 二个π键,但是与N2分子不 同的是有一个π键为配键, 这对电子来自氧原子。(如 右图所示)CO作为一种配 体,能与一些有空轨道的 金属原子或离子形成配合 物。例如同ⅥB,ⅦB和Ⅷ 族的过渡金属形成羰基配 合物:Fe(CO)5、Ni(CO)4 和Cr(CO)6等。
结构化学课件

此外,他还把价键理论进一步扩展到金属和金属 络合物方面,并且阐明和发展了有关原子核结构和裂 变过程本质的理论。 他的研究工作涉及面较广,尤其是他的化学键理 论,解释和阐明了许多复杂化合物的空间构型和本质 特征,从而解决了过去长期未能解决的分子结构方面 的许多问题。50年代后,他的工作主要是把理论上的 研究成果进一步应用于生物学和医学等方面。他的研 究成果不仅对化学的各个基本领域产生巨大影响,而 且深深扩展到生物学、生理病理学和医学等领域,也 为分子生物学的崛起和发展做出了积极贡献。 由于他在化学方面,特别是化学键的性质和复杂 分子结构方面的贡献,1954年获得诺贝尔化学奖,又 由于对世界和平事业所作出的贡献,1962年获得诺贝 尔和平奖。
二、化学键理论简介
从二十世纪初发展至今,化学键理论已形成三 大流派:分子轨道理论(Molecular Orbital)、价键 理 论 (Valence Bond) 和 密 度 泛 函 理 论 (Density Functional Theory)。
1. 分子轨道理论:
从 20 世 纪 30 年 代 初 , 由 Hund , Mulliken , Lennard-Jones 开创 , Slater, Hü ckel, Pople发 展 至今。该方法的分子轨道具有较普通的数学形式, 较易程序化。六十年代以来,随着计算机的发展, 该 方 法 得 到 了 很 大 的 发 展 。 如 Pople 等 研 制 的 Gaussian从头算程序, 已成为当今研究化学键理论 的主流方法,以后我们将主要介绍该方法。
The Nobel Prize in Chemistry 1998
"for their theories, developed independently, concerning the course of chemical reactions"
结构化学课件
4
化学学院 结构化学
第二章
5
化学学院 结构化学
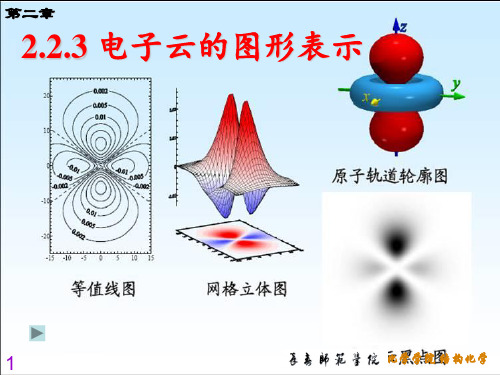
第二章 C. 径向分布函数 2R2n,l(r)~r图 径向分布函数r 图
6
化学学院 结构化学
第二章
球极坐标与笛卡儿坐标的关系
7
化学学院 结构化学
第二章
☆1s态:核附近D为0;r=a0时,D极大。表 1s态 核附近D 极大。 明在r 附近,厚度为dr的球壳夹层内 明在r=a0附近,厚度为dr的球壳夹层内 找到电子的几率要比任何其它地方同样厚 度的球壳夹层内找到电子的几率大。 度的球壳夹层内找到电子的几率大。 ☆每一 n 和 l 确定的状态,有n-l个极大值 确定的状态, 值为0的点。 和n-l-1个D值为0的点。 ☆n相同时:l越大,主峰离核越近;l越小, 相同时: 越大,主峰离核越近; 越小, 峰数越多,最内层的峰离核越近; 峰数越多,最内层的峰离核越近; l相同时:n越大,主峰离核越远;说明n小 相同时: 越大,主峰离核越远;说明n 的轨道靠内层,能量低; 的轨道靠内层,能量低; 电子有波性,除在主峰范围活动外, ☆电子有波性,除在主峰范围活动外,主量 子数大的有一部分会钻到近核的内层。 子数大的有一部分会钻到近核的内层。
25
化学学院 结构化学
10
第二章
11
化学学院 结构化学
第二章
12
化学学院 结构化学
第二章
13
化学学院 结构化学
第二章
14
化学学院 结构化学
第二章 (3) 空间分布 )
ψ −r 和 ψ2 −r图 ★ s态的 态的
Z 3 − a0 1 −r ψ1s = 3 e ⇒ψ1s = e πa π 0
3 1 Z ψ 2s = 2πa3 4 0 1/ 2 r − Zr − 2a0 1 1 2 2 − e ⇒ψ 2s = (2 − r)e a0 4 2π Zr
结构化学

绪论
3 学习结构化学的方法
结构化学课程是在学过高等数学,普通物理,无机化 学,分析化学等课程的基础上,进一步讲授微观物质的运 动规律。由于该课程需要的数理基础知识多,概念又比较 抽象,所以,初学者在开始学习时常有雾里看花,无所适 从之感。针对结构化学课程的特点,必须探索出适合自己 的学习方法,作为学习结构化学普遍性的学习原则,应注 意以下几点。
2.2.3 新材料、新药的合成
7
结构化学精品课程
绪论
2.2.1 反应机理的研究
反应机理研究是一个既古老而又有很多问题尚不清楚 的学科。美国 R.Hoffmann 和日本 Kenich Fukui分别提出 了分子轨道对称守恒原理和提出前线轨道理论,为此他们 获得了1981 年诺贝尔化学奖。由李远哲教授等创立的交叉 分子束反应是研究微观反应机理的重要实验手段,为此他 们获得了1986年诺贝尔化学奖。
3.3 广泛联系无机、有机、物化中遗留的问题
由于该课程涉及的数理公式多,概念抽象,很容易使初学者 感到枯燥、无味,失去学习的兴趣。因此,在学习过程中必须广 泛联系无机、有机、物化中遗留的问题,用结构化学的观点、知 识分析解决这些问题是提高学习兴趣的有效方法。
全满、半满的稳定性: 例如:
各种效应:
离域效应、量子力学隧道效应、红移效应、取代基团的定位效应
14
结构化学精品课程
绪论
超导材料: YBa2Cu3O7的结构 (Y:Ba:Cu=1:2:3规则)
以钙钛矿型结构为基本单元, 通过原子的空缺、置换、位移变 形、堆叠组合等多种型式,可以 描述多种氧化物超导相的结构. 例如,钇钡铜氧高温超导体就是 一种缺氧钙钛矿型三倍超格子结 构,属正交晶系.
15
Cu O Ba Y
结构化学 绪论 ppt

结构化学告诉你 —— “为什么”!
24
绪论
参考书目
1. 周公度,段连运,结构化学基础(第四版),北京大学出版社, 2008 2. 西北大学《结构化学》精品课程网站 /jghx 3. 周公度,段连运,结构化学习基础题解析(第四版),北京大学 出版社,2008 4. 徐光宪,物质结构(第二版),高等教育出版社,1987 5. 李炳瑞编著,结构化学,北京:高等教育出版社,2004 6. 林梦海等编,结构化学(第二版),北京:科学出版社,2008 7. R. McWeeny, C.A. Coulson著,原子价,余敬曾译,科学出版 社,1986 8. 徐森,物质结构目标教学辅导,上海科技文献出版社,32开, 1989(推荐)
基本知识已广泛地应用于化学的各个领域。特别是:当
今化学早已进入纳米空间(10-9m)、飞秒时间(10-15s)时 代,结构化学知识越显重要,很多学科领域都与结构化 学知识密切相关。 2.2.1 反应机理的研究 2.2.2 人工模拟生物固氮催化剂的合成
2.2.3 新材料、新药的合成
7
绪论
2.2.1 反应机理的研究 反应机理研究是一个既古老而又有很多问题尚不清楚 的学科。美国 R.Hoffmann 和日本Kenich Fukui分别提出 了分子轨道对称守恒原理和前线轨道理论,为此他们获得 了1981 年诺贝尔化学奖。由李远哲教授等(李远哲,D. R. Herschbach,J. Polanyi)创立的交叉分子束反应是研 究微观反应机理的重要实验手段,为此他们获得了1986年 诺贝尔化学奖。 常规的宏观动力学方法有时很难确定一些反应的具体 微观机理,只能是一种推断。 8
m 1
过渡态
400
300
209 389
结构化学课件.ppt

发展简史:
“物质结构”这门学科是在十九世纪末叶逐步发 展起来的。当时由于生产力的不断提高,实验技术 有了很大的发展。有一些物理学家观察到许多现象, 用当时已经非常成熟、理论体系已经非常完整的经 典物理学理论无法加以说明,甚或与其推论完全相 反。最主要的发现有:电子的发现、元素的天然放 射现象的发现、黑体辐射现象的规律的发现等。这 就迫使人们对经典物理学的体系提出革命性的见解, 并逐步发展新的理论体系。
量子力学基础知识、原子的结构和性质、分子 的结构和性质、化学键理论、晶体化学、研究结构 的实验方法等。
结构化学是在原子、分子水平上研究物质分子构 型与组成的相互关系,以及结构和各种运动的相互影 响的化学分支学科。它是阐述物质的微观结构与其宏 观性能的相互关系的基础学科。
结构化学是一门直接应用多种近代实验手段测定 分子静态、动态结构和静态、动态性能的实验科学。 它要从各种已知化学物质的分子构型和运动特征中, 归纳出物质结构的规律性;还要从理论上说明为什么 原子会结合成为分子,为什么原子按一定的量的关系 结合成为数目众多的、形形色色的分子,以及在分子 中原子相互结合的各种作用力方式,和分子中原子相 对位置的立体化学特征;结构化学还要说明某种元素 的原子或某种基团在不同的微观化学环境中的价态、 电子组态、配位特点等结构特征。
当对很多个别具体对象进行测量后,再总结成 规律。当然这些测试方法的原理,也是以量子理论 为基础的。其中有一种称做原子参数图示方法或键 参数函数方法,可以总结出对冶金、化工等科学技 术上有实际意义的规律。这些规律对于发展化学健 理论也有其价值。
两条途径中,前者主要是量子化学的主要内容, 后者主要是物理测试方法等的内容。当然这两部分 内容彼此间还是有密切联系的。前者的基本理论都 是来源于实践,在由实践总结成基本理论时,归纳 法也起了很重要的作用。后者又依靠前者作为理论 基础,在由基本理论指导新实验技术的建立和发展 时,演绎法也有重要的作用。
结构化学晶体学基础ppt课件
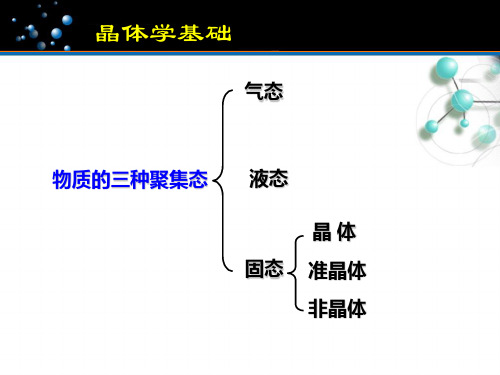
晶体学基础
气态
物质的三种聚集态 液态 晶体
固态 准晶体 非晶体
晶体学基础
• 非晶体
在它们内部原子或分子的排列没有周期性的结构 规律,像液体那样杂乱无章地分布,可以看作过冷 液体,称为玻璃体、无定形体或非晶态物质。
玻璃体的结构特点
晶体学基础
• 准晶体
准晶是一种介于晶体和非晶体之间的固体。准晶具有 完全有序的结构,然而又不具有晶体所应有的平移对称性, 因而可以具有晶体所不允许的宏观对称性。准晶体的发现, 是20世纪80年代晶体学研究中的一次突破。
金刚石中的滑移面
晶体的微观对称性
7.3.2 230个空间群 空间群符合一般用熊夫利和国际符号联合表示
晶体结构的周期性和点阵理论
3 晶体具有确定的熔点
晶体结构的周期性和点阵理论
4 晶体的对称性和对X射线的衍射
晶体的理想外形具有特定的对称性,这是内 部结构对称性的反映。晶体结构的周期大小和X 射线的波长相当,使它成为天然的三维光栅,能 够对X射线产生衍射。而晶体的X射线衍射,成 为了解晶体内部结构的重要实验方法。
晶胞
• 晶胞的两个基本要素:
晶胞
• 分数坐标
OP = xa + yb + zc
x, y, z为P原子的分数坐标。 x, y, z为三个晶轴方向单位 矢量的个数(是分数)(晶轴 不一定是相互垂直)。 x, y, z一定为分数
晶胞
• 凡不到一个周期的原子的坐标都必须标记,分 数坐标,即坐标都是分数,这样的晶胞并置形 成晶体。
点阵结构
2. 从晶体点阵结构中抽象出点阵 例1. 等径圆球排列形成的一密置列直线点阵
一个点阵点代表一个球 重复周期为a a = 2r
气态
物质的三种聚集态 液态 晶体
固态 准晶体 非晶体
晶体学基础
• 非晶体
在它们内部原子或分子的排列没有周期性的结构 规律,像液体那样杂乱无章地分布,可以看作过冷 液体,称为玻璃体、无定形体或非晶态物质。
玻璃体的结构特点
晶体学基础
• 准晶体
准晶是一种介于晶体和非晶体之间的固体。准晶具有 完全有序的结构,然而又不具有晶体所应有的平移对称性, 因而可以具有晶体所不允许的宏观对称性。准晶体的发现, 是20世纪80年代晶体学研究中的一次突破。
金刚石中的滑移面
晶体的微观对称性
7.3.2 230个空间群 空间群符合一般用熊夫利和国际符号联合表示
晶体结构的周期性和点阵理论
3 晶体具有确定的熔点
晶体结构的周期性和点阵理论
4 晶体的对称性和对X射线的衍射
晶体的理想外形具有特定的对称性,这是内 部结构对称性的反映。晶体结构的周期大小和X 射线的波长相当,使它成为天然的三维光栅,能 够对X射线产生衍射。而晶体的X射线衍射,成 为了解晶体内部结构的重要实验方法。
晶胞
• 晶胞的两个基本要素:
晶胞
• 分数坐标
OP = xa + yb + zc
x, y, z为P原子的分数坐标。 x, y, z为三个晶轴方向单位 矢量的个数(是分数)(晶轴 不一定是相互垂直)。 x, y, z一定为分数
晶胞
• 凡不到一个周期的原子的坐标都必须标记,分 数坐标,即坐标都是分数,这样的晶胞并置形 成晶体。
点阵结构
2. 从晶体点阵结构中抽象出点阵 例1. 等径圆球排列形成的一密置列直线点阵
一个点阵点代表一个球 重复周期为a a = 2r
结构化学课件7

共五十九页
图 7.19 腺嘌呤和胸腺嘧啶生成由两个(liǎnɡ ɡè)氢键联结的互补对的示意图
共五十九页
图 7.20 胞嘧啶和鸟嘌呤生成(shēnɡ chénɡ)三个氢键联结的互补对的示意图
共五十九页
氢键(qīnɡ jiàn)
共五十九页
HF
HCl HBr HI
沸点/℃
19.9 -85.0 -66.7 -
共五十九页
4、氢键对物质性质(xìngzhì)的影响:
氢键广泛存在,如水、醇、酚、酸、羧酸、氨、胺。 氨基酸、蛋白质、碳水化合物等许多化合物都存在氢键。 氢键对物质的影响也是多方面的。
(1)对物质熔、沸点的影响。 分子间形成氢键使物质的熔沸点升高。如图7-32。
这是由于(yóuyú)要使液体气化或使固体液化都需要能 量去破坏分子间氢键的缘故。
35.4
极化率Biblioteka 小大色散作
用
弱
强
沸
点
低
高
HF的沸点反常的高?
原因:存在氢键。
HF分子中,共用电子对强烈偏向电负性大的F原子
一侧。在几乎裸露的H原子核与HF分子中F原子的
某一孤对电子之间产生的吸引作用称为氢键。 共五十九页
除了分子间氢键外,还有分子内氢键。例如(lìrú):
硝酸的分子内氢键使其溶沸点降 低。
共五十九页
2、氢键 的特点: (qīnɡ jiàn)
(1)氢键具有(jùyǒu)方向性。它是指Y原子与X-Y形成氢键 时,尽可能使氢键的方向与X-H键轴在同一条直线上,这 样可使X与Y的距离最远,两原子电子云间的斥力最小,因 此形成的氢键愈强,体系愈稳定。
(2)氢键具有饱和性。它是指每一个X-H只能与一个Y原
图 7.19 腺嘌呤和胸腺嘧啶生成由两个(liǎnɡ ɡè)氢键联结的互补对的示意图
共五十九页
图 7.20 胞嘧啶和鸟嘌呤生成(shēnɡ chénɡ)三个氢键联结的互补对的示意图
共五十九页
氢键(qīnɡ jiàn)
共五十九页
HF
HCl HBr HI
沸点/℃
19.9 -85.0 -66.7 -
共五十九页
4、氢键对物质性质(xìngzhì)的影响:
氢键广泛存在,如水、醇、酚、酸、羧酸、氨、胺。 氨基酸、蛋白质、碳水化合物等许多化合物都存在氢键。 氢键对物质的影响也是多方面的。
(1)对物质熔、沸点的影响。 分子间形成氢键使物质的熔沸点升高。如图7-32。
这是由于(yóuyú)要使液体气化或使固体液化都需要能 量去破坏分子间氢键的缘故。
35.4
极化率Biblioteka 小大色散作
用
弱
强
沸
点
低
高
HF的沸点反常的高?
原因:存在氢键。
HF分子中,共用电子对强烈偏向电负性大的F原子
一侧。在几乎裸露的H原子核与HF分子中F原子的
某一孤对电子之间产生的吸引作用称为氢键。 共五十九页
除了分子间氢键外,还有分子内氢键。例如(lìrú):
硝酸的分子内氢键使其溶沸点降 低。
共五十九页
2、氢键 的特点: (qīnɡ jiàn)
(1)氢键具有(jùyǒu)方向性。它是指Y原子与X-Y形成氢键 时,尽可能使氢键的方向与X-H键轴在同一条直线上,这 样可使X与Y的距离最远,两原子电子云间的斥力最小,因 此形成的氢键愈强,体系愈稳定。
(2)氢键具有饱和性。它是指每一个X-H只能与一个Y原
相关主题
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
课程简介
结构化学---内容提要
物质结构(结构化学)是在原子、分子水平上, 深入到电子层次,研究物质的微观结构及其宏观性能 关系的科学。其内容涉及用量子力学原理与方法研究 化学问题,进而建立物质结构理论;提出与创造结构 分析方法;剖析以生物在分子为主的复杂物质的结构。 这一门课我们采用的是北京大学出版社出版的《结构 化学基础》一书。这本书是北京大学化学院结构化学 (即物质结构)基础教材。内容主要包括: 量子力学基础知识、原子的结构和性质、分子 的结构和性质、化学键理论、晶体化学、研究结构 的实验方法等。
结构化学的产生与有机物分子组成的 研究密切相关。有机化学发展的初期,人 们总结出许多系列有机物分子中碳原子呈 四面体化合价的规律。为解释有机物组成 的多样性,人们提出了碳链结构及碳链的 键饱和性理论。随后的有机物同分异构现 象、有机官能团结构和旋光异构现象等研 究,也为早期的结构化学研究提供有力的 实验证据,促使化学家从立体构型的角度 去理解物质的化学组成和化学性质,并从 中总结出一些有关物质化学结构的规律性, 为近代的结构化学的产生打下了基础。
结构化学是在原子、分子水平上研究物质分子构 型与组成的相互关系,以及结构和各种运动的相互影 响的化学分支学科。它是阐述物质的微观结构与其宏 观性能的相互关系的基础学科。
结构化学是一门直接应用多种近代实验手段测定 分子静态、动态结构和静态、动态性能的实验科学。 它要从各种已知化学物质的分子构型和运动特征中, 归纳出物质结构的规律性;还要从理论上说明为什么 原子会结合成为分子,为什么原子按一定的量的关系 结合成为数目众多的、形形色色的分子,以及在分子 中原子相互结合的各种作用力方式,和分子中原子相 对位置的立体化学特征;结构化学还要说明某种元素 的原子或某种基团在不同的微观化学环境中的价态、 电子组态、配位特点等结构特征。
近代测定物质微观结构的实验物理 方法的建立,对于结构化学的发展起了 决定性的推动作用。X射线衍射方法和 原理上相当类似的中子衍射、电子衍射 等方法的发现与发展,大大地丰富了人 们对物质分子中原子空间排布的认识, 并提供了数以十万种计的晶体和分子结 构的可靠结构数据。此外,通过晶体衍 射的研究,使人们能够从分子和晶体结 构的角度说明这些物质在晶态下的物理 性质。
结构化学的信息工程的研究能充分利用电 子计算机的高速、高效率,充分发挥结构化 学数据库的作用,对于新的半经验理论和新 的结构化学理论的提出将有重大的影响。有 关方法的建立将对于“分子设计”的实现起 着重要的作用。 目前,结构化学已成为一门不但与其他化 学学科联系密切,而且与生物科学、地质科 学、材料科学等各学科的研究相互关联、相 互配合、相互促进。由于许多与物质结构有 关的化学数据库的建立,结构化学也越来越 被农学家和化工工程师所重视。
结构化学的研究方法和学习方法
研究方法: 其一 演绎法, 理论到实验。
其二 归纳法, 实验到理论。 学习方法: 1.重视理论与实践之间的密切联系; 2.要学会用抽象思维和运用数学工具来处理问 题方法; 3.要恰当的运用类比,模拟,对比和其它方法; 4.要理论联系实际。
发 展 史: 1900 — 至今 (简介之)
1905年爱因斯坦(A. Einstein)提出相对论,在 高速运动的物体的力学方面对经典力学提出重要修正 与补充。过后他又在量子论和相对论基础上以光电现 象作为实验基础,提出光的量子论,把对微观世界物 质运动的规律的研究又推进了一大步。 1913年玻尔(N.Bohr)则把他们的理论与卢瑟福 (E.Rutherford)的原子有核模型巧妙地结合起来,第一 次提出原子结构的量子理论,首次提出原子内部电子 运动状况具有不连续性即量子化特性的思想,又提出 定态的概念,并成功地把氢原子光谱现象与氢原子内 电子运动的定态相联系起来,为运用光谱现象研究原 子的内部结构提供了理论基础与成功的经验。玻尔理 论的发展,使化学键的电子理论得以建立,使得化学 基础理论的发展进入一个新的阶段。
研究对象:
结构化学是研究原子 、分子和晶体的微观结 构,研究原子和分子运动规律,研究物质的结构 和性能关系的科学,是化学的一个重要分支。 这里所指的结构和运动规律,涉及原子和分 子层次的空间排布,涉及微观粒子所遵循的量子 力学规律,它包括原子中电子的分布和能组合、 分子的化学组成、分子的空间构型和构象、分子 中电子的分布、化学键的性质和分子的能量状态、 晶体中原子的空间排布、晶体的能量状态等内容。 结构化学根据结构决定性能、性能反应结构的基 本原则,探讨物质的结构与性能间的关系。
表面结构和表面化学反应的研究与工 业生产上的非均相催化反应关系极为密切, 有关的研究对于工业催化剂,尤其是合成 氨等工业生产用的新型催化剂的研制具有 理论指导的作用。 激光光谱学和激光化学的研究,对于 快速动态结构和快速化学反应动态过程等 研究方法的建立有着深远的影响,并且可 能导致新的结构化学研究手段的建立。激 光作用下的化学反应过程更具有独特之处。
近代实验物理方法的发展和应用,为结 构化学提供了各种测定物质微观结构的实 验方法;量子力学理论的建立和应用又为 描述分子中电子和原子核运动状态提供了 理论基础。有关原子结构特别是原子中电 子壳层的结构以及内力、外力引起运动变 化的理论,确立了原子间相互作用力的本 质,也就从理论上阐明了化学键的本质, 使人们对已提出的高子键、共价键和配位 键加深了理解有关杂化轨道的概念,也为 众多化合物的空间构型作出了合理的阐明 甚至预测。
另一类测定结构的方法是谱学方法。谱学方 法在提供关于分子能级和运动的信息,尤其是更 精细的和动态的结构信息方面起着重要的作用。 如分子振动光谱是鉴定物质分子的构成基团的迅 速和有力的工具。因而被称为化学物质的“指 纹”,与电子计算机高速信息处理功能结合起来, 人们已能通过计算机的检索和识别很快地查明未 知物样品的分子结构。红外喇曼光谱的理论处理, 还能提供有关振动力常数等有关化学键特征的一 些数据。其他谱学法有:核磁共振谱、顺磁共振 诺、电子能谱、质谱、穆斯堡尔谱学、可见—紫 外光谱、旋光谱、圆二色性谱以及扩展 X射线吸 收精细结构等。
物质的某些物理常数的测定,也能提供有关分 子结构的某些整体信息,如磁化率、折射率和介电 常数的测定等。此外,高放大率、高分辨率的电子 显微镜还能提供有关物质表面的结构化学信息,甚 至已能提供某些分子的结构形象。 量子化学是近代结构化学的主要理论基础。量 子化学中的价键理论、分子轨道理论以及配位场理 论等,不但能用来阐明物质分子构成和原子的空间 排布等特征,而且还用来阐明微观结构和宏观性能 之间的联系。由于量子化学计算方法的发展和逐步 提高完善,加上高速电子计算机的应用,有关分子 及其不同聚集状态的量子化学方法已有可能用于特 殊材料的“分子设计”和制备方法的探索,把结构 化学理论推向新的高度。
当今结构化学主要研究新构型化合物 的结构化学,尤其是原子簇结构化学和金 属有机化合物。这一类研究涉及“化学模 拟生物固氮”等在理论研究上极其重要的 课题,以及寻找新型高效的工业催化剂等 与工农业生产息息相关的应用研究课题。 稀土元素的结构化学与中国丰富的稀 土元素资源的综合利用的关系非常密切。 有关的研究对于中国稀土工业的发展具有 重要的意义。
另一方面,从结构化学的角度还能阐明物 质的各种宏观化学性能,和各种宏观非化学性 能与微观结构之间的关系及其规律性。在这个 基础上就有可能不断地运用已知的规律性,设 法合成出具有更新颖、结构特点更不寻常的新 物质,在化学键理论和实验化学相结合的过程 中创立新的结构化学理论。与此同时,还要不 断地努力建立新的阐明物质微观结构的物理的 和化学的实验方法。 与其他的化学分支一样,结构化学一般从 宏观到微观、从静态到动态、从定性到定量按 各种不同层次来认识客观的化学物质。演绎和 归纳仍是结构化学研究的基本思维方法。
发展简史:
“物质结构”这门学科是在十九世纪末叶逐步发 展起来的。当时由于生产力的不断提高,实验技术 有了很大的发展。有一些物理学家观察到许多现象, 用当时已经非常成熟、理论体系已经非常完整的经 典物理学理论无法加以说明,甚或与其推论完全相 反。最主要的发现有:电子的发现、元素的天然放 射现象的发现、黑体辐射现象的规律的发现等。这 就迫使人们对经典物理学的体系提出革命性的见解, 并逐步发展新的理论体系。 1900年普朗克(M.Planck)提出量子论,是在微观 领域内对经典物理学第一次强有力的冲击,且为以 后量子力学理论的建立作了良好开端。
很明显,物质的动态结构的研究要以研究 静态结构所得成果为基础,其内容也比较复杂。 本课程作为一门基础课将主要探讨物质的静态 结构。
研究途径:
研究物质结构主要采取两条途径: 其一是以演绎的方法为主,即是从微观 质点运动的普遍规律,即量子力学规律出发, 先研究原子内电子运动的规律,其中包括电 子和原子核以及电子之间相互作用的规律, 由此推论原子的性质,特别要阐明元素周期 律的本质。进而研究原子是如何组成分子或 如何组成晶体的。为此,要探讨分子中电子 在两个或多个原子核作用下以及相互作用下 其运动的规律,由此探讨化学键的本质。
如要研究动态结构,还要研究在整个 化学反应过程中电子状态如何随着原子核 的相对运动而发生变化,并讨论这种变化 如何制约着化学反应的进行。 其二是以归纳为主的方法,主要用一 些物理测试的手段,如X射线结构分析、 原子光谱、分子光谱、电学及磁学性质的 测定、核磁共振、电子自旋共振等方法来 研究物质内部原子的排列及运动状况、原 子和分子中电子的运动状态等。
当对很多个别具体对象进行测量后,再总结成 规律。当然这些测试方法的原理,也是以量子理论 为基础的。其中有一种称做原子参数图示方法或键 参数函数方法,可以总结出对冶金、化工等科学技 术上有实际意义的规律。这些规律对于发展化学健 理论也有其价值。 两条途径中,前者主要是量子化学的主要内容, 后者主要是物理测试方法等的内容。当然这两部分 内容彼此间还是有密切联系的。前者的基本理论都 是来源于实践,在由实践总结成基本理论时,归纳 法也起了很重要的作用。后者又依靠前者作为理论 基础,在由基本理论指导新实验技术的建立和发展 时,演绎法也有重要的作用。
