盐酸林可霉素稳定性实验报告
林可霉素可行性研究报告

林可霉素可行性研究报告
一、研究背景
林可霉素是一种广谱抗生素,常被用于治疗呼吸道感染、皮肤感染、尿道感染等疾病。
然而,随着抗生素耐药性的增加,林可霉素的疗效逐渐减弱,导致临床治疗效果不佳。
因此,有必要对林可霉素进行进一步研究,以提高其疗效,减少副作用,并延长其在临床上的应
用价值。
二、研究目的
本研究旨在评估林可霉素在临床应用中的可行性,探讨其安全性、有效性和剂量效应关系,为临床医生提供更多关于林可霉素应用的指导。
三、研究方法
1. 研究设计:本研究采用随机对照试验设计,将患者分为实验组和对照组,分别接受林可
霉素治疗和常规治疗。
2. 研究对象:本研究将招募符合入组标准的患者作为研究对象,共计100例。
3. 治疗方案:实验组患者接受林可霉素治疗,对照组患者接受常规治疗。
治疗期间监测患
者的临床症状、生化指标等。
4. 数据统计与分析:采集患者的临床资料,进行统计分析,比较两组患者的治疗效果及不
良反应发生率。
四、研究意义
通过本研究,可以评估林可霉素在临床应用中的可行性,为临床医生提供更多关于林可霉
素的治疗指导,提高其在临床应用中的效果,减少治疗风险。
五、预期结果
我们预期本研究可以为临床医生提供更多有关林可霉素治疗的实用信息,提高其在临床应
用中的可行性,减少副作用,提高疗效。
六、结论
通过本研究对林可霉素的可行性进行评估,为其在临床应用中的合理使用提供了一定的参
考依据。
我们相信,随着对林可霉素疗效和安全性的进一步研究,它将在临床上发挥更大
的作用。
采用高效液相色谱及旋光法测定盐酸林可霉素注射液含量的对比实验

南
垒 囊
2 0 1 5 罐 ( 第 3 6 卷 ) 第 9 期
他产品的过程中 , 会 担忧 网购 产 品 的落 地 服 务 得 不 到 保
础 。任你网络推广做得天花乱坠, 也不如养殖户用料的具
体 效 益 来 得 实 在 。在 电商 时 代 , 如 何 让 用户 利用 社 交 网 络, 分 享 真实 用 料情 况 , 迄 今 为止 还 缺乏 行 之有 效 的 展现
表 3 盐 酸林 可霉 素注 射液 的稳 定性 试 验结 果
2 - 4 两种含 量测 定 方法 的 比较
取批 号 为 1 0 1 2 1 1 、 1 1 0 2 0 3 、 1 1 0 5 0 8 的盐 酸林 可霉 素 注 以旋 光 度 ( A ) 为纵 坐 标 , 浓度 ( C ) 以林 可 霉 素 计 为 横 坐标 进 行 线 性 回归 , 得 回归 方 程 为 A = 3 1 8 . 2 9 C 一 0 . 0 2 8 1 , r = 1 . 0 。结 果 表 明 , 在0 . 0 1 - 0 . 0 5 ( g ・ m l ) 的 浓度 范 围 内 , 浓 度 射液 , 精 密 量取 5 m l , 分别 置 于 5 0 m l 量瓶中 , 用 水 稀 释 至
可霉素注射液 的含量测定采用《 中国兽药典) ) 2 O L O 年版一 部高效液相色谱法 , 操作繁琐 , 检验时间长 , 对兽药厂半成
品 质量 控 制来 说 , 其 检 验方 法 并 不理 想 。因此 , 笔 者 根据
2 . 5 g 各2 份, 分别置于 5 0 m l 容量瓶中, 按处方量加入其他 辅料 , 加水 溶解 并稀 释至 刻度 , 制 成浓 度分 别 为 O . 0 1 、
度, 制成浓度分别为 0 . 0 l 、 0 . 0 2 、 0 . 0 3 、 0 . 0 4 、 0 . 0 5 ( g ・ ml ) 的
盐酸林可霉素

3年
生产日期
DATE OF MANUFACTURE
依据
ACCORDING TO
B.P2002&E.P.(V)
报告日期
DATE OF ANALYSIS
检验项目
Items
标准规定
Criteria
检验结果
Results
性状
Characteristics
应为白色或几乎白色结晶性粉末
A white or almost white crystalline powder
水分
Water
3.1~4.6%
4.3%
细菌内霉素
Bacterial endotoxins
Not more than 0.5I.U.of endotoxin per milligram
符合规定
Complies
含量测定
Assay
Anhydrous substance 82.5~93.0%
89.1%
结论本品依据BP2002和E.P.(V)检验其结果符合规定
4.2
比旋度
Specific optical rotation
4%(W/V)Water solution+135~+150°
+145°
林可霉素B
Lincomycin B
≤5.0%
3.8%
重金属
Heavy metals
≤5PPM
符合规定
Passed
硫酸化灰分
Sulphated ash
≤0.5%
0.1%
Conclusion MEETS THE STANDARD OF BP2002 AND E.P.(V)
019盐酸林可霉素检验记录
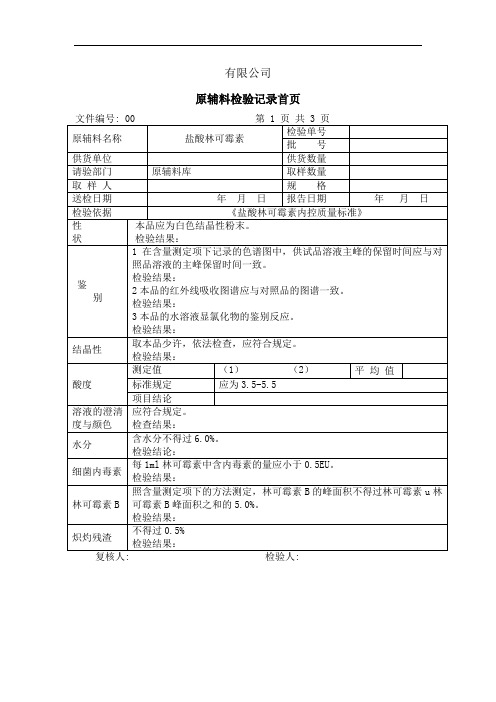
原辅料检验记录首页
文件编号: 00第 1 页 共 3 页
原辅料名称
盐酸林可霉素
检验单号
批 号
供货单位
供货数量
请验部门
原辅料库
取样数量
取 样 人
规 格
送检日期
年 月 日
报告日期
年 月 日
检验依据
《盐酸林可霉素内控质量标准》
性
状
本品应为白色结晶性粉末。
检验结果:
鉴
别
1在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液的主峰保留时间一致。
对照品制备:另取林可霉素对照品,同上法制得 。
样品编号
内 容
1
2
样品取量Vs(g)
样品峰面积As
对照品取量Wc(g)
对照品峰面积Ac
计算公式:
As×Wc×N N(对照品含量)=
X = ×100%
Ac×Vs×S S(样品标示量)=
按无水物计,样品含量X(%)
含 量 平 均 值(%)
A-B
相对偏差 ×100%主要Fra bibliotek分析仪器
名 称
型 号
精度
柱温
测定用波长
编 号
分 析 天 平
BT25S
0.00001
____
_______
MHT-007
高效液相色谱仪
UV200II
----
30℃
254nm
MHT-008
色谱柱
C-18
流动相:0.05mol/L硼砂溶液-甲醇(4:6)
样品制备:取本品约50mg,精密称定,置25ml量瓶中,加流动相溶解并稀释至刻度,摇匀,精密量取10ul,注入液相色谱仪 。
盐酸林可霉素原料药稳定性研究

盐酸林可霉素是一种高效的抗革兰阳性菌的抗生素,在体 内分布广。可进入骨髓和骨组织,临床广泛用于呼吸系统骨髓 炎及软组织感染等病症的治疗,尤其适用于对青霉素和红霉素 过敏的病人 [1]。本研 究 采 用 极 限 试 验 法 加 快 盐 酸 林 可 霉 素 中 组分的分解变化,以高效液相色谱(HPLC)法测定其含量变化, 考察盐酸林可霉素产品在运输过程中产品的稳定性。
每个样进样 3次,记录峰面积。取每个样品平均值,以峰面积 为纵坐标,浓度为横坐标进行线性回归,得回归方程:Y=7.0× 10-5X-0.0199,相关系数 R2 =0.99983,r=0.9991。结果表明 盐酸林可霉素在 0.0003~3.0mg/mL的范围内有良好的线性 关系。 2.1.5 精密度试验
将供试样品溶液每小时进样一次,考察 24h内溶液的稳定 性,主成分盐酸林可霉素的峰面积以 RSD值计算(RSD不得大 于 0.85%),林可霉素 B和其他有关物质的含量的绝对值在 ± 0.1%,并不得检查 出 新 的 杂 质,否 则 认 为 溶 液 不 稳 定,需 要 在 溶液变化发生之前进样。对 24次进样结果分析后,主成分盐 酸林可霉素 RSD为 0.23%,杂质 A绝对值 0.0%,杂质 B绝对 值 0.0%,总杂质绝对值 0.0%,林可霉素 B绝对值 0.0%。说 明盐酸林可霉素供试液在 24h内是稳定的。液相色谱图如图 1。
1.2 试剂
乙腈,甲醇,氨水,超纯水,盐酸林可霉素标准品批号 n○3, 杂质鉴别标准品 n○1(来 源 EDQM),盐 酸 林 可 霉 素 样 品 批 号 A1、A2、A3(天方药业有限公司)。
2 方法和结果 2.1 稳定性考察指标
2.1.1 色谱条件 色谱柱:250mm ×4.6mm ×5μm,SUPELCOSILLC-8-
盐酸林可霉素溶析结晶工艺优化研究 Ⅰ.盐酸林可霉素在丙酮-水体系中的介稳区性质研究

盐酸林可霉素溶析结晶工艺优化研究.盐酸林可霉素在丙酮-水体系中的介稳区性质研究赵茜Ξ 高大维33 陈永泉 李秉滔333(华南农业大学食品科学系, 广州510642) 摘 要 本文研究了在丙酮-水体系中盐酸林可霉素的介稳区性质,建立了介稳区宽度的数学模型。
测定了一定条件下的溶解度曲线和超溶解度曲线,为工业生产选择适宜的结晶过饱和度提供了依据。
关键词 盐酸林可霉素; 溶析; 结晶; 介稳区 盐酸林可霉素(lincom ycin hydroch lo ride)由M a2 son等于1962年得到,Hoek sem a等于1964年确定结构,是临床上应用较广的一种抗生素[1]。
在临床上它主要用于治疗败血症、呼吸道感染、骨和关节感染等,其用药特点是副作用少,控制感染快,适用于对青霉素及红霉素有过敏的病人[2]。
由于它们对革氏阴性菌抗菌活性较差,近年来半合成了各种林可霉素衍生物。
目前国际市场上对高质量(主要是纯度、粒度分布)的盐酸林可霉素需求较大,除直接用于临床外,还用于半合成林可霉素衍生物,因此盐酸林可霉素是一种可供出口创汇的医药产品。
但实际生产中,成品质量常常达不到出口标准,主要问题是粒度不均,细晶多。
晶体质量的好坏是与结晶工艺密不可分的,目前国内盐酸林可霉素等抗生素的溶析结晶过程还停留在凭经验操作水平上,没有一套完善的溶析结晶理论指导实际操作,结晶常常在不稳区进行,致使操作失败。
优化溶析结晶工艺须分两步进行,第一步是进行物系的介稳特性研究,第二步是进行最佳操作程序的研究。
本文对盐酸林可霉素在丙酮-水体系中的介稳特性进行了研究,现报道如下。
1 材料与方法1.1 实验药品与设备盐酸林可霉素(中国药品生物制品检定所);丙酮(分析纯);氦氖激光器(上海玻璃仪器一厂);磁力搅拌器(HANNA in strum en ts公司);W ZZ21型旋光仪(上海物理光学仪器厂);超级恒温水浴(重庆试验设备厂);电子分析天平(Sarto riu s公司);多功能电子蠕动泵(浙江象山石浦海天电子仪器厂)。
盐酸林可霉素滴眼液的HPLC法测定

注射用盐酸克林霉素方法学研究原始记录

检验人:复核人:
检验人:复核人:
方法学研究测定原始记录
检验人:复核人:
方法学研究测定原始记录
方法学研究测定原始记录检验人:复核人:
方法学研究测定原始记录检验人:复核人:
方法学研究测定原始记录
第页共页检验人:复核人:
方法学研究测定原始记录
检验人:复核人:
检验人:复核人:
检验人:复核人:
方法学研究测定原始记录
检验人:复核人:
检验人:复核人:
方法学研究测定原始记录检验人:复核人:
方法学研究测定原始记录
方法学研究测定原始记录
检验人:复核人:
方法学研究测定原始记录
检验人:复核人:
方法学研究测定原始记录
方法学研究测定原始记录
检验人:复核人:
方法学研究测定原始记录
检验人:复核人:
方法学研究测定原始记录
检验人:复核人:
方法学研究测定原始记录
检验人:复核人:
检验人:复核人:日期:日期:。
紫外分光光度法测定盐酸林可霉素葡萄糖注射液半成品中林可霉素的含量

对照品稀释 / ml·100 ml - 1
C / mg·L - 1
A (λ= 214 nm)
2
47. 72
0. 166
3
71. 58
0. 246
4
95. 44
0. 334
5
119. 30
0. 413
6
143. 16
0. 498
表 2 供试品溶液不同浓度的紫外吸收
供试品稀释 / ml·100·ml - 1
ABSTRSACT To deveolp a UV met hod for lincomycin in t he halt2product of lincomycin hydrocholride and glucose injection. The sol2 vent was aqueous purified. And t he detection wavelengt h was at 214 nm. The calibration curve was linear in t he range of 48~144μg ·ml - 1 of lincomycin (r = 019992) . The average recovery rate was 100117 % wit h relative standard deviation of 011 % ( n = 5) . The
盐酸林可霉素葡萄糖注射液 (本厂产品 ,规格 : 250 ml∶ 016 g) ;盐酸林可霉素对照品 (国家标准品) ;硼砂 :分析纯 ;甲 醇 : HPL C 级 ;乙腈 : HPL C 级 。
3 试验步骤 3. 1 试验条件 紫外 :环境温度 20 ℃,检测波长 214 nm ,吸 收池 1 cm ,高效 :环境温度 20 ℃,流动相 :0105 mol·L - 1 硼砂 - 甲醇 - 乙腈 (60 ∶34 ∶4) ,检测波长 214 nm ,流速 110 ml· min - 1 ,进样量 20μl 。 3. 2 对照品及样品溶液的制备 供试品溶液的制备 :精密量 取供试品溶液 2 、3 、4 、5 、6 ml 分别置 100 ml 量瓶中 ,加水稀释 至刻度 ,摇匀 ,取得 5 个不同浓度的供试品溶液 。
盐酸林可霉素检验记录

结果:
检验人:复核人:
检查
(4)水分
仪器名称与型号:ZSD-2型自动水分滴定仪仪器编号:0310-04-103
测定温度:
费休氏试液的标定:
F……………为每1ml费休氏试液相当于水的重量(mg)
W…………为称取重蒸馏水的重量(mg)
A……………为滴定所消耗费休氏试液的容积(ml)
B……………为空白所消耗费休氏试液的容积(ml)
W1=mg W2=mg W3=mg
A1=ml A2=ml A3=ml
B=ml
计算得:F1=F2=F3=
F平均值为相对平均偏差=
供试品测定:供试品中水分含量X=
W…………为称取供试品的重量(mg)
计算:含量X
…………为称取对照品的重量(g) …………为对照品峰面积
…………为称取供试品的重量(g) …………为供试品峰面积 ……………为对照品含量
MR=
Mx1=Mx2=
AR1=AR2=
AX1=AX2=
X1=X2=
检验人:复核人:
含量测定
平均值:
含量(按干品计)为
结果:
检验人:复核人:
(2)测定:取本品约50mg,精密称定,置25ml量瓶中,用适量流动相溶解并稀释至刻度,摇匀,精密量取10μl注入液相色谱仪,记录色谱图;另取盐酸林可霉素对照品适量,同法测定。按外标法以峰面积计算供试品中C18H34N2O6S的含量。
(3)含量
对照品来源:对照品批号:
对照品规格:对照品含量:
对照品溶液配制:精密称取盐酸林可霉素对照品,置于25ml量瓶中,用适量流动相溶解并稀释至刻度。
注射用盐酸林可霉素0.6工艺验证报告

验证报告编号:2305·429-00注射用盐酸林可霉素工艺验证报告起草人:日期:年月日审核人:日期:年月日批准人:日期:年月日海南霞迪药业有限公司注射用盐酸林可霉素(0.6g规格)生产工艺验证方案目录1.概述 (3)2.验证目的 (3)3.验证范围 (3)4.验证小组成员及职责范围 (3)4.1验证小组成员 (3)4.2 验证小组成员职责范围 (3)5.验证进度计划 (4)6.验证规程号 (4)7.粉针主要生产设备一览表 (4)8.生产洁净区的划分及工艺流程 (5)9.生产和检验标准文件的引用 (6)10.产品生产工艺过程综合指标确认 (7)11.验证内容 (10)12.验证条件监控 (22)12.1人员监控情况 (22)12.2关键工艺参数监控情况 (23)12.3生产环境监控情况 (23)12.4处理程序 (23)13.偏差报告 (23)14.拟订验证周期 (23)15.验证结果评价和结论 (24)16.验证会签 (24)1 概述:本公司生产的注射用盐酸林可霉素,其规格为0.6g/瓶。
为了证明在执行SP-MF-000-000-00注射用盐酸林可霉素生产工艺规程的情况下,能稳定地生产出符合质量标准的产品。
在这之前验证小组已对空调净化系统、纯化水和注射用水系统,以及在线设备分别进行了验证,同时对生产线也进行了验证合格,所以本报告主要就该产品生产工艺规程及其生产过程和最终产品质量等进行验证并作出评价。
2目的:为了证明在执行SP-MF-000-000-00注射用盐酸林可霉素生产工艺规程的情况下,连续生产三批,最终产品的稳定性、可靠性并符合标准要求。
3 范围: 本验证报告适用于粉针车间的厂房、设施、设备、工艺条件下注射用盐酸林可霉素(0.6g规格)的生产,当上述条件发生改变时,应重新验证。
4 验证小组成员及职责范围:4.1验证小组成员:部门职务姓名生产技术部组长质量部组员工程部组员物控部组员QA 组员QC 组员岗位操作组员4.2.1生产技术部:负责起草验证方案和有关规程,按批准的验证方案起草验证方案,组织培训考核人员,组织实施验证并同时收集验证资料,会签验证报告。
不同pH值的盐酸可霉素输液稳定性

不同pH值的盐酸可霉素输液稳定性王胜浩;林芳;等【期刊名称】《浙江省医学科学院学报》【年(卷),期】2002(013)001【摘要】目的考察不同pH条件对盐酸林可霉素输液的影响。
方法分别制备pH值为6.0、6.5、7.0的林可霉素输液,于低温(4℃)、高温(60℃)及强光照射(4500Lx,25℃)条件下考察各输液的稳定性。
HPLC测定了所考察样品的含量及降解产物等。
结果 pH为7.0样品的外观及澄明度不合格,高温10天的含量下降8%左右;而pH为6.0样品的外观、澄明度药物含量、色普降解产物均无明显变化;pH6.5样品的考察结果介于两者之间。
HPLC含量方法回收经:99.8%±0.8;标准曲线:Cmg/ml=1.846829X-0.085526,r=0.996;最低检出限:6ng。
结论盐酸林可霉素输液的pH为6.0时,样品在强光、高温、低温等条件下均稳定。
因此,输液的pH上限为6.0为宜。
【总页数】3页(P9-11)【作者】王胜浩;林芳;等【作者单位】药物研究所310013;药物研究所310013【正文语种】中文【中图分类】R978.1【相关文献】1.pH值对复方卡那霉素口服液中盐酸普鲁卡因稳定性的影响 [J], 马倩;夏运岳2.微生物法考察乳糖酸红霉素在不同输液中的稳定性 [J], 宁霞;钟洁莲3.盐酸头孢吡肟在不同输液中的配伍稳定性 [J], 刘萍4.盐酸左氧氟沙星注射液在不同pH值液体中的稳定性研究 [J], 吴洲;武风云5.盐酸林可霉素与硫酸丁胺卡那霉素注射液在四种输液中配伍的稳定性探讨 [J], 陈红因版权原因,仅展示原文概要,查看原文内容请购买。
反相离子对高效液相色谱法测定盐酸林可霉素注射液中乙二胺四乙酸二钠的含量

Waters 2695-2996 高效液相色谱仪,二极管阵 列 检 测 器 ,Empower 化 学 工 作 站 ( 美 国 Waters 公 司);梅特勒 AG135 电子天平(梅特勒-托利多仪器 有限公司);PHS-25 型酸度计 (北京华瑞博远科技 发展有限公司)。
盐酸林可霉素注 射 液 (规 格 为 2 mL:0.6 g,批 号 :0912232、1009242、1001245,山 东 方 明 药 业 股 份 有 限 公 司 ); 乙 二 胺 四 乙 酸 二 钠 (EDTA-2Na, 上 海 中 试 化 工 总 公 司 , 批 号 :20080925, 纯 度 :97.0%, 分 析
作者简介 屈蓉,女,主管中药师,研究方向:药物分析 E-mail: qurong81@
收稿日期 2012-05-13 修回日期 2012-05-28
372
纯);甲醇为色谱纯;氯化铁、四丁基氢氧化铵、甲酸 均为分析纯;水为超纯水。
2 方法和结果
2.1 色谱条件和系统适用性试验 色谱柱:Waters Symmetry C18(4.6 mm×150 mm,
参考文献
[1] 刁岩忠,韩继永,陈祥峰. HPLC 法测定注射用泮托拉 唑 钠 中 乙 二 胺 四 乙 酸 二 钠 的 含 量 [J]. 药 物 分 析 杂 志 ,
2011,31(2):282. [2] 黄 建 ,李 文 仙 ,霍 军 生. 反 相 离 子 对 高 效 液 相 色 谱 法
测 定 果 味 饮 料 中 的 乙 二 胺 四 乙 酸 二 钠 [J]. 中 国 食 品 工 业 ,2009(6):56. [3] 耿 志 旺 ,刘 蔚 ,刘 茜 ,等. HPLC 法 测 定 丙 泊 酚 注 射 液中乙二胺四乙酸二钠含量[J]. 药物分析杂志,2011,31 (3):588.
注射用盐酸林可霉素工艺验证报告0.6g

验证报告编号:2305·429-00注射用盐酸林可霉素工艺验证报告起草人:日期:年月日审核人:日期:年月日批准人:日期:年月日海南霞迪药业有限公司注射用盐酸林可霉素(0.6g规格)生产工艺验证报告目录1.概述 (3)2.验证目的 (3)3.验证范围 (3)4.验证小组成员及职责范围 (3)4.1验证小组成员 (3)4.2 验证小组成员职责范围 (3)5.验证进度计划 (4)6.验证规程号 (4)7.粉针主要生产设备一览表 (4)8.生产洁净区的划分及工艺流程 (5)9.生产和检验标准文件的引用 (6)10.产品生产工艺过程综合指标确认 (7)11.验证内容 (10)12.验证条件监控 (22)12.1人员监控情况 (22)12.2关键工艺参数监控情况 (23)12.3生产环境监控情况 (23)12.4处理程序 (23)13.偏差报告 (23)14.验证周期 (23)15.验证结果评价和结论 (24)16.验证会签 (24)1 概述:本公司生产的注射用盐酸林可霉素,其规格为0.6g/瓶。
为了证明在执行SP-MF-000-000-00注射用盐酸林可霉素生产工艺规程的情况下,能稳定地生产出符合质量标准的产品。
在这之前验证小组已对空调净化系统、纯化水和注射用水系统,以及在线设备分别进行了验证合格,同时对生产线也进行了验证合格,所以本验证主要就该产品生产工艺规程及其生产过程和最终产品质量等进行验证并作出评价。
2目的:为了证明在执行SP-MF-000-000-00注射用盐酸林可霉素生产工艺规程的情况下,连续生产三批,最终产品的稳定性、可靠性并符合标准要求。
3 范围: 本验证报告适用于粉针车间的厂房、设施、设备、工艺条件下注射用盐酸林可霉素(0.6g规格)的生产,当上述条件发生改变时,应重新验证。
4 验证小组成员及职责范围:4.1验证小组成员:部门职务姓名生产技术部组长质量部组员设备部组员物控部组员QA 组员QC 组员岗位操作组员4.2.1制造部:负责起草验证方案和有关规程,按批准的验证方案起草验证方案,组织培训考核人员,组织实施验证并同时收集验证资料,会签验证报告。
盐酸林可霉素稳定性实验报告

盐酸林可霉素稳定性实验报告取100g盐酸林可霉素溶于250ml 纯化水中,待其稳定后用自动旋光仪测量,结果为: pH3.28(28.3℃)、176019u/ml。
然后分为三份考察其在不同条件下的稳定性,其结果如下:1.pH0.71 条件下不同温度、不同时间的结果室温55℃70℃0min165075u/ml————100min164690u/ml163926u/ml157665u/ml340min164425u/ml160625u/ml137620u/ml430min164614u/ml159761u/ml133202u/ml再过 15hr163952u/ml144386u/ml85587u/ml2.pH1.78 条件下不同温度、不同时间的结果室温55℃70℃0min175174u/ml————100min174744u/ml173072u/ml175792u/ml340min174833u/ml177130u/ml180450u/ml430min174934u/ml178026u/ml182564u/ml再过 15hr175129u/ml182027u/ml179516u/ml3.pH3.61 条件下不同温度、不同时间的结果室温55℃70℃0min176714u/ml————100min175634u/ml175729u/ml177622u/ml340min175685u/ml178815u/ml187443u/ml430min185830u/ml179768u/ml188908u/ml再过 15hr176329u/ml189040u/ml192802u/ml结果分析:从以上实验数据可以看出:①盐酸林可霉素在 pH1.78 以上是稳定的,无论室温或是高温均无什么影响。
生产工艺上控制在 pH1.5 以上,对盐酸林可霉素应该没有什么破坏;②盐酸林可霉素在 pH0.71 时会受到破坏,随着温度的升高和时间的延长破坏程度明显加强。
盐酸林可霉素原料药稳定性探究

盐酸林可霉素原料药稳定性探究【摘要】目的:探究盐酸林可霉素产品在运输过程中产品的稳定性分析。
方法:采用分组对比的方式,采取极限实验与长期实验两种方式,考察盐酸林可霉素产品在运输过程中产品的稳定性。
结果:极限实验实施开展时间为2个月,实验结束后,经过数据分析结果显示,相关物质无明显变化,采用Minitab 计算水分含量合格回归方程为:0.0407 + 0.000833 月,极限条件推测下,水分不合格现象的出现将会在3.8月时间段,约 8.9 月盐酸林可霉素含量合格。
结论:实验结束后数据分析得出:盐酸林可霉素相关物质及水分在极限实验条件下,性质没有发生变化,稳定性较好。
【关键词】盐酸林可霉素; 抗生素; 原料药; 极限环境; 稳定性盐酸林可霉素(洁霉素),一种药品,可治疗各种感染。
本品为白色结晶性粉末;有微臭或特殊臭;味苦。
本品在水或甲醇中易溶,在乙醇中略溶。
本品为窄谱抗生素,作用与红霉素相似,对革兰阳性球菌有较好作用,特别对厌气菌、金葡菌及肺炎球菌有高效。
其作用机制和红霉素相似,属抑菌剂。
本研究采用极限试验法加快盐酸林可霉素中组分的分解变化,以高效液相色谱( HPLC) 法测定其含量变化,考察盐酸林可霉素产品在运输过程中产品的稳定性。
1、仪器和材料1.1仪器HWS - 250 智能型恒温恒湿箱、仪器 CP225D 天平、电热恒温水浴锅、KQ5200B 型超声波清洗器、DL31 卡尔菲休氏水分滴定仪、Agilent1200 高效液相色谱仪。
1.2试剂乙腈,甲醇,氨水,超纯水,盐酸林可霉素。
2、方法2.1溶液稳定性试验对24h内的溶液稳定性进行考察,观察期间,需要每小时都对供试样品溶液进行观察,RSD 值计算主成分盐酸林可霉素的峰面积,其中,RSD 不得大于0.85% 。
在溶液变化发生之前进样,确保不会检查出新的杂质的基础上,必须要保障林可霉素 B 和其他有关物质的含量的绝对值在±0.1% ,如果符合实验数据标准,将被认定为溶液不稳定。
注射用盐酸克林霉素在2种注射液中配伍的稳定性考察

注射用盐酸克林霉素在2种注射液中配伍的稳定性考察郑芳;李鹏;朱雪松【摘要】目的考察室温下,注射用盐酸克林霉素分别与5%转化糖注射液、5%转化糖电解质注射液配伍的稳定性.方法按临床常用浓度配置盐酸克林霉素与5%转化糖注射液、5%转化糖电解质注射液配伍液,采用反相高效液相色谱法测定配伍液中盐酸克林霉素0~8 h内的含量变化,并观察配伍液的外观及pH值变化.结果注射用盐酸克林霉素与5%转化糖注射液及5%转化糖电解质注射液8 h内配伍液外观、pH值及含量均无明显变化.结论在室温下,注射用盐酸克林霉素分别与5%转化糖注射液、5%转化糖电解质注射液8 h内可配伍使用.【期刊名称】《实用药物与临床》【年(卷),期】2013(016)010【总页数】3页(P937-939)【关键词】盐酸克林霉素;转化糖注射液;转化糖电解质注射液;反相高效液相色谱法;配伍;稳定性【作者】郑芳;李鹏;朱雪松【作者单位】湖北医药学院附属东风医院药学部,湖北,十堰,442008;湖北医药学院附属东风医院药学部,湖北,十堰,442008;湖北医药学院附属东风医院药学部,湖北,十堰,442008【正文语种】中文盐酸克林霉素(Clindamycin hydrochloride)主要用于治疗革兰阳性球菌和各种厌氧菌引起的感染,临床常用于治疗扁桃体炎和咽炎、肺部感染、骨关节感染等。
转化糖注射液是由等量的葡萄糖与果糖混合制成的输液剂,临床常用做药物稀释剂、能量补充剂和各类需水分和能量的患者的补液治疗。
转化糖电解质注射液是由葡萄糖与果糖等分子混合制成的同时含有电解质的复方制剂,主要用于提供水、电解质及能量,并产生利尿作用和代谢性碱化作用。
注射用盐酸克林霉素分别与5%转化糖注射液和5%转化糖电解质注射液配伍稳定性的研究较少,笔者查阅资料,参照有关文献[1-3],模拟临床用药浓度,在室温[(20 ±1)℃]、不避光条件下,对其配伍稳定性进行了考察,旨在为临床合理用药提供依据。
盐酸林可霉素凝胶的稳定性考察

盐酸林可霉素凝胶的稳定性考察
王文清;汪秋兰;黄泽中;施春阳;汤杰;方建国
【期刊名称】《医药导报》
【年(卷),期】2005(024)004
【摘要】目的研究不同条件下盐酸林可霉素凝胶的稳定性.方法采用高效液相色谱法测定盐酸林可霉素凝胶中林可霉素的含量,考察影响因素(光照、温度)实验、加速实验和长期留样试验对其稳定性的影响.结果盐酸林可霉素凝胶对强光照射不敏感,对高温(≥60℃)稳定性较差.结论盐酸林可霉素凝胶在生产和贮藏过程中光照无影响,在室温条件药物无变化,该药的有效期暂定为2 a.
【总页数】2页(P332-333)
【作者】王文清;汪秋兰;黄泽中;施春阳;汤杰;方建国
【作者单位】华中科技大学同济医学院附属同济医院药学部,武汉,430030;华中科技大学同济医学院附属同济医院药学部,武汉,430030;华中科技大学同济医学院附属同济医院药学部,武汉,430030;华中科技大学同济医学院附属同济医院药学部,武汉,430030;华中科技大学同济医学院附属同济医院药学部,武汉,430030;华中科技大学同济医学院附属同济医院药学部,武汉,430030
【正文语种】中文
【中图分类】R927.2
【相关文献】
1.苦参碱口腔生物黏附凝胶的体内外释放模型研究及初步稳定性考察 [J], 严俊;陈晓瑾;余舒莹;王萍萍;廖莉
2.HPLC法测定复方盐酸林可霉素凝胶中盐酸林可霉素的含量 [J], 周小红;黄巧玲
3.复方盐酸林可霉素凝胶的研究 [J], 朱全刚;王增福
4.盐酸林可霉素胶囊稳定性考察 [J], 刘雅华;史蕙;黄蓓
5.用RP-HPLC法测定盐酸林可霉素眼用温敏凝胶中盐酸林可霉素的含量 [J], 施启红
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
精选文档
盐酸林可霉素稳定性实验报告
取100g盐酸林可霉素溶于250ml纯化水中,待其稳定后用自动旋光仪测量, 结果为:pH3.28 (283C)、176019u/ml。
然后分为三份考察其在不同条件下的稳定性,其结果如下:
1.pH0.71条件下不同温度、不同时间的结果
2.pH1.78条件下不同温度、不同时间的结果
3.pH3.61条件下不同温度、不同时间的结果
结果分析:
从以上实验数据可以看出:
精选文档
①盐酸林可霉素在pH1.78 以上是稳定的,无论室温或是高温均无什么影响。
生产工艺上控制在pH1.5 以上,对盐酸林可霉素应该没有什么破坏;
②盐酸林可霉素在pH0.71 时会受到破坏,随着温度的升高和时间的延长破坏程度明显加强。
③在pH1.78和pH3.61的条件下,效价有所升高,系在高温条件下,溶液蒸发所致。
结论:
盐酸林可霉素在pH值较低的情况(pH<1.5)下是不稳定的,pH越低其稳定性越差,且随着温度的升高和时间的延长,盐酸林可霉素受到的破坏程度将随着加强。
(专业文档是经验性极强的领域,无法思考和涵盖全面,素材和资料部分来自网
络,供参考。
可复制、编制,期待你的好评与关注)。
