美罗培南中间体的合成与结构表征_马红梅
(完整版)美罗培南合成反应
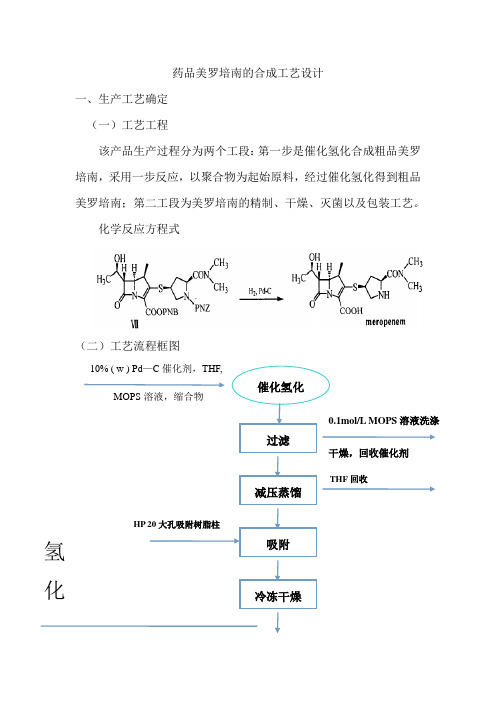
药品美罗培南的合成工艺设计一、生产工艺确定 (一)工艺工程该产品生产过程分为两个工段:第一步是催化氢化合成粗品美罗培南,采用一步反应,以聚合物为起始原料,经过催化氢化得到粗品美罗培南;第二工段为美罗培南的精制、干燥、灭菌以及包装工艺。
化学反应方程式(二)工艺流程框图10% ( w ) Pd —C 催化剂,THF,MOPS 溶液,缩合物0.1mol/L MOPS 溶液洗涤干燥,回收催化剂过滤减压蒸馏吸附冷冻干燥催化氢化THF 回收HP 20大孔吸附树脂柱大孔吸附树脂柱氢化(三)生产工艺过程叙述本设计工艺将工艺分为氢化和精制两个工段实施,现将生产工艺叙述如下。
1. 氢化反应工段 (1)工艺规程①投料 将聚合物、催化剂加入氢化反应釜中,打开MOPS 溶液以及甲醇计量罐阀门,向釜中加入液体,使聚合物(kg ):催化剂(kg ):MOPS 溶液(L ):THF(L)=1:1:6:5开动搅拌,使之溶解②氢化反应 向反应釜中通入氢气,保持压力在70 psi (约482.65kPa )左右,温度保持在20℃-25℃内,反应6h 。
水/丙酮(1:1)洗脱水/丙酮回收精制③过滤停止搅拌,打开泄压阀是气压下降至当地大气压,回收过量的氢气。
将溶液将加入到压滤罐中,打开压缩空气进口阀,使压滤罐内压力为0.25MPa~0.30MPa,压滤后,滤液全部到分子蒸馏器中,滤渣用少量MOPS溶液洗涤后回收。
④减压过滤溶液进入蒸馏器后开始加热并开启真空泵蒸馏出的THF分尽水层,抽入计量罐在下次生产中回收套用。
⑤吸附以一定的流速把上述残液加到经过预处理的大孔吸附树脂柱的上端进行吸附。
2.精制过程①洗脱先用水清洗以除去树脂表面或内部还残留的杂质。
然后用洗脱液(水:丙酮=1:1)在一定的温度下以一定的流速进行洗脱。
将洗脱液转入脱色罐中【注】a.吸附树脂的预处理:吸附树脂预先用乙醇浸泡24h,用乙醇洗至流出液与水1:5不浑浊。
然后用水洗至无醇味,再用5%HCl通过树脂柱,浸泡2-4h,水洗至中性。
(完整版)美罗培南合成反应

药品美罗培南的合成工艺设计一、生产工艺确定 (一)工艺工程该产品生产过程分为两个工段:第一步是催化氢化合成粗品美罗培南,采用一步反应,以聚合物为起始原料,经过催化氢化得到粗品美罗培南;第二工段为美罗培南的精制、干燥、灭菌以及包装工艺。
化学反应方程式(二)工艺流程框图10% ( w ) Pd —C 催化剂,THF,MOPS 溶液,缩合物0.1mol/L MOPS 溶液洗涤干燥,回收催化剂过滤减压蒸馏吸附冷冻干燥催化氢化THF 回收HP 20大孔吸附树脂柱大孔吸附树脂柱氢化(三)生产工艺过程叙述本设计工艺将工艺分为氢化和精制两个工段实施,现将生产工艺叙述如下。
1. 氢化反应工段 (1)工艺规程①投料 将聚合物、催化剂加入氢化反应釜中,打开MOPS 溶液以及甲醇计量罐阀门,向釜中加入液体,使聚合物(kg ):催化剂(kg ):MOPS 溶液(L ):THF(L)=1:1:6:5开动搅拌,使之溶解②氢化反应 向反应釜中通入氢气,保持压力在70 psi (约482.65kPa )左右,温度保持在20℃-25℃内,反应6h 。
水/丙酮(1:1)洗脱水/丙酮回收精制③过滤停止搅拌,打开泄压阀是气压下降至当地大气压,回收过量的氢气。
将溶液将加入到压滤罐中,打开压缩空气进口阀,使压滤罐内压力为0.25MPa~0.30MPa,压滤后,滤液全部到分子蒸馏器中,滤渣用少量MOPS溶液洗涤后回收。
④减压过滤溶液进入蒸馏器后开始加热并开启真空泵蒸馏出的THF分尽水层,抽入计量罐在下次生产中回收套用。
⑤吸附以一定的流速把上述残液加到经过预处理的大孔吸附树脂柱的上端进行吸附。
2.精制过程①洗脱先用水清洗以除去树脂表面或内部还残留的杂质。
然后用洗脱液(水:丙酮=1:1)在一定的温度下以一定的流速进行洗脱。
将洗脱液转入脱色罐中【注】a.吸附树脂的预处理:吸附树脂预先用乙醇浸泡24h,用乙醇洗至流出液与水1:5不浑浊。
然后用水洗至无醇味,再用5%HCl通过树脂柱,浸泡2-4h,水洗至中性。
美罗培南中间体的合成与结构表征

MA Ho g me ,HU n- i ANG S u - h n h n z o g,L Ho g c a g, WANG Xio c e I n-hn a - h n, Z UHe g h a,XU Z o g y H n-u hn-u
( co l f h r ay at hn nvri f cec n eh o g ,S a g a 2 0 3 ,C ia Sh o o am c ,E s C iaU ies yo i ea dT c nl y h nh i 0 2 7 hn ) P t S n o
A s a t (S 4 )- Dme ya ioab n l 4- ra t 1一 4- io e zlxero y) yrl ie w s b t c : 2 ,S 2- i t lm n eroy - mecpo- ( nt b ny y ab n1p r i n a r h r o od
mir wa e ra i t n a d t s h r a to tme c o v ir d a i n hu t e e c i n i wa s o tn d n ir g n r t ci n imis d o s h re e a d n to e p oe to d s se .Th tr e e agt c mp u d a n e e a e r de tfe t H o o n nd i t r dit swe e i n i d wih m i NM R, I R, MS a d OR. n
h d oy i y r l ss
1 前
言
要 使用 四水醋 酸镍 、正三 丁基膦 、三 苯膦 、偶 氮化 合物 和氯 甲酸 异丙酯 等反应 试剂并 需惰 性气体 保护 反 应条 件 等 。笔者 综合 考 虑原 料 来 源 、操作 难 易 、 转化 率 以及 后处 理等 多种 因素 ,选 择如 下所示 的路 线合 成 目标 化合 物 1 。
药物合成-美罗培南(华理药物合成)

小组成员
杨志平 陈朦皎 谢木青 蔡剑锋 许钦昌 刘朝阳
2 双环母核的合成
1 单环β-内酰胺的合成
Fujimoto K , Iwano Y, Hirsi K,et al.From penicillin to penem and carbapenemVII.Synthesis and antibacterial activity of penem derivafives[J].Chem Pharm Buff,1986,34(3):999—1014.
药典标准
适应症
用于敏感菌引起的下列感染:脑膜炎、 败血症、蜂窝组织炎、淋巴结炎、扁桃 体周围脓肿、肛门周围脓肿、骨髓炎、 关节炎、外伤创口感染、烧伤创面感染、 手术切口感染、慢性支气管炎、慢性呼 吸系统疾病继发感染、肺炎、肺浓脓疡、 脓胸肾盂肾炎、发作性膀胱炎、胆囊炎、 胆管炎、肝脓疡、腹膜炎、子宫附件炎、 子宫内感染、中耳炎、副鼻窦炎、眼科 感染、颌骨及周围蜂窝组织炎等。
第三种路线
MatsumuraH,Bando T,Sunagawa M.An efficient synthesis of (2S.4s)-2substituted 4-mereaptopy rolidinederivatives[J].Heterocycles.1995,41(I):147159.
Meropenem
美罗培南
Content
第一部分 第二部分 第三部分 药物简介 合成路线 总结概述
物质结构
通用名称:meropenem,美罗培南 化学名称:(5R,6S) -2-[(3S,5S) -5- (二甲基甲 酰基)吡咯烷-3-基硫]-6- [(R)-1-羟乙基]-1-甲基碳 青霉-2-烯-3-羧酸三水合物 分子式:C17H31N3O8S 分子量:437.20 结构式:
美罗培南化学结构

美罗培南化学结构
美罗培南是一种强效的抗生素,属于β-内酰胺类。
它的化学结构是一种环状的β-内酰胺,由6个成分组成。
这6个成分包括一个氨基苯甲酸、一个N-甲基-L-丙氨酸、一个L-半胱氨酸、一个D-谷氨酰胺、一个1,2-环己二胺和一个D-丙氨酸。
美罗培南的化学结构使其能够有效抑制细菌的生长,特别是对于耐药性较强的革兰阴性杆菌有很好的效果。
美罗培南的临床应用广泛,但也存在一些副作用和限制。
因此,在使用美罗培南时应该严格遵循医生的指示,避免滥用和误用。
- 1 -。
一种用于合成美罗培南侧链的中间体的制备方法[发明专利]
![一种用于合成美罗培南侧链的中间体的制备方法[发明专利]](https://img.taocdn.com/s3/m/f4ebb48125c52cc58ad6be7b.png)
专利名称:一种用于合成美罗培南侧链的中间体的制备方法专利类型:发明专利
发明人:杨兆钰,孟宪强,房正薇,梁寒冰,吕玲玉
申请号:CN201911392664.6
申请日:20191231
公开号:CN111763219A
公开日:
20201013
专利内容由知识产权出版社提供
摘要:本发明属于医药中间体制备技术领域,具体涉及一种合成酮的方法,将顺式‑4‑羟基‑L‑脯氨酸溶解于碱的水溶液中,‑5~10℃下,滴加对硝基氯甲酸苄酯溶液,调节pH至8.5~10.5;将制得的浊液在‑5~10℃下保温2~7h,分层得溶液;采用无机酸调节溶液的pH至1~1.5,控制温度0~10℃,析晶,过滤,烘干等,得产品,本发明产率高,产品质量好。
申请人:山东金城柯瑞化学有限公司
地址:255000 山东省淄博市淄博高新区四宝山办事处东张村
国籍:CN
更多信息请下载全文后查看。
美罗培南新脂溶性前药的合成和药物动力学研究

美罗培南新脂溶性前药的合成和药物动力学研究李静;崔玉彬【期刊名称】《国外医药(抗生素分册)》【年(卷),期】2011(032)004【摘要】为了提高美罗培南口服吸收,本课题合成并研究了一系列在其羰基和吡咯烷基上引入脂溶性修饰基前药.在这些前药中,对特戊酰甲氧基-(1R,5S,6S)-2-[(3S,5S)-5-(N,N-二甲氨基甲酰基-1-(异丁酰氧甲氧基羰基)吡咯烷-3-硫代-6-[(1R)-1-羟乙基]-1-甲基羧苄青霉素-2-烯-3-羧酸酯(4)和1-吡咯烷氧羰基氧甲基(1R,5S,6S)-2-[(3S,5S)-5-(N,N-二甲基氨基甲酰基)-1-(异丁酰氧甲基氧羰基)吡咯烷-3-硫代]-6-[(1R)-1-甲基羧苄青霉素-2-烯-3-羧酸酯(8)作了深入研究.研究发现,在鼠和犬的动物实验中,口服前药4和8,其生物利用度为18.2%~38.4%,且对包括耐青霉素肺炎链球菌和β-内酰胺酶阴性耐氨苄西林流感嗜血杆菌在内的各种病原体均有效.【总页数】7页(P165-171)【作者】李静;崔玉彬【作者单位】中国医药集团总公司,四川抗菌素工业研究所,成都,610052;中国医药集团总公司,四川抗菌素工业研究所,成都,610052【正文语种】中文【中图分类】R978.1+9【相关文献】1.含喹诺酮类药物的高分子前药的合成及表征的初步研究 [J], 温志国;叶艳秋;黄剑华;郑巧燕;董声雄;李春艳2.含有环丙沙星高分子前药物的合成 [J], 连鸿丹;叶艳秋;董声雄3.双重响应两亲性聚前药的合成及其在药物控释方面的应用 [J], 韩克;张国颖4.一种基于亮氨酸氨基肽酶前药分子的中间体合成及其药物缓释机制设计 [J], 曾繁明;宋振升;王飞翼;马超;杨桂春5.分析DOX抗癌药物前药的合成及表征 [J], 姜兵兵[1];曾银海[1]因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1前言
美罗培南(meropene型肾脱氢肽酶耐受 性 好 的 新 型 β - 内 酰 胺 类 抗 生 素 , 由 Dainippon Sumitomo Pharma 研 发 , 于 1995 年 首 次 在 意 大 利 上市, 在临床上主要用于治疗威胁人类生命的腹腔 感染、 泌尿系感染等重症感染, 应用剂型包括静脉 注射剂、 肌肉注射剂 2 种 。 [1-3]
基-1-(4-硝基苯甲氧羰基)吡咯烷(4)的合成 将 2.00 g (6.5 mmol) (2S,4R)-2-羧 基-4-羟 基-1-(4-硝基苯甲氧羰基)吡咯烷(3)和 37.5 mL 二 氯甲烷与 2.45 g(24.3 mmol)三 乙 胺 溶 液 混 合 , 降 温 至-15℃, 于该温度下逐滴加入 2.55 g(22.3 mmol) 甲磺酰氯后搅拌反应 1 h, 加入 1.45 g(17.8 mmol)盐 酸二甲胺和 2.50 g (24.8 mmol)三乙胺, 加毕在相 同温度下继续搅拌反应 1 h。 反应毕, 依次 用 1 mol / L 盐酸、 1 mol / L 氢氧 化 钠 和 氯 化 钠 溶 液 洗涤, 有机层用无水硫酸镁干燥后浓缩, 以甲醇 / 正己烷(v∶v=1∶1)重结晶得 2.20 g 白色固体 4, 收率 82.0%, m.p.116.0~116.2℃ (文献[4]值: 收率 73%, m.p. 115~116℃); IR (KBr, v / cm-1): 3 316, 2 954, 1 737, 1 666; 1H NMR ( CDCl3) , δ: 2.30 ~2.58 (2H, m) , 2.86 (1H, s) , 2.99 ( 3H, s) , 3.05 ( 3H, s) , 3.16 ( 2H, s) , 3.91 ~3.96 ( 2H, m) , 4.85~4.95 (1H, 2×t, J=7.68 Hz), 5.20~5.27 (2H, dd, J=13.55 Hz), 5.36 (1H, s), 7.44~7.52 (2H, dd, J=8.5 Hz), 8.21~8.23(2H, d); [α]D20=-1.85° (c 1.000, CH3Cl)。 2.2.3 (2S,4S)-2-二甲氨基甲酰基-4-乙酰硫基-1
经相应的 1H NMR、 IR、 MS 以及 OR 进行了结构表征。
关键词: 反式-4-羟基-L-脯氨酸; 微波化学合成; 构型翻转; 合成; 水解
中图分类号: O626.13
文献标志码: A
文章编号: 1009-9212(2010)03-0029-03
Synthesis and Characterization of Meropenem Intermediate MA Hong-mei, HUANG Shun-zhong, LI Hong-chang, WANG Xiao-chen, ZHU Heng-hua, XU Zhong-yu* (School of Pharmacy, East China University of Science and Technology, Shanghai 200237, China) Abstract: (2S,4S) -2 -Dimethylaminocarbonyl -4 -mercapto -1 -(4 -nitrobenzyloxycarbonyl)pyrrolidine was synthesized from trans -4 -hydroxy -L -proline in overall yield of 40.9% in few steps including N -acylation, sulfonylation, amidation, inversion of configuration and hydrolysis. The configuration inversion was assisted by microwave irradiation and thus the reaction time was shortened and nitrogen protection dismissed. The target compound and intermediates were identified with 1H NMR, IR, MS and OR. Key words: trans -4 -hydroxy -L -proline; microwave -assisted synthesis; configuration inversion; synthesis; hydrolysis
羰基)吡咯烷(3)的合成 将 2.00 g (0.015 mol) 反-4-羟基-L-脯氨酸溶 解于 16.5 mL (2 mol / L) 氢氧化钠溶液中, 降温至 0~5℃, 滴加到含 3.6 g (0.017 mol) 氯甲酸对硝基 苄 酯 的2.9 mL 二氯甲烷溶液, 滴加完毕, 0~5℃下 搅拌反应 3 h。 反应毕, 加入 3.6 mL(2 mol / L)氢氧 化钠溶液分层, 水层用 10 mL 二氯甲烷洗涤, 之后 再用浓硫酸酸化析晶。 经过滤、 水洗、 真空干燥后 即 可 得 到 3.4 g 化 合 物 3, 收 率 73.0% , m.p.134~ 135℃ ( 文 献 [4] 值 : 收 率 93% , m.p.134~135.5℃ ) ; IR (KBr, v / cm-1): 3 411, 1 720, 1 681, 1 608; 1H NMR (MeOD), δ: 2.06~2.12 (1H, m), 2.32~
-(4-硝基苯甲氧羰基)吡咯烷(5)的合成 将 2.40 g (5.78 mmo1) (2S,4R)-2-二甲氨基甲 酰基-4-甲磺酰氧基-1-(4-硝基苯甲氧羰基) 吡咯 烷(4)、 1.32 g(11.58 mmo1)硫代乙酸钾加入到适量 N,N-二甲基甲酰胺中溶解, 置于微波催化合成仪 中, 搅拌升温至60~65℃反应 30 min。 反应毕, 向 反 应 液 中 分 别 加 入 10 mL 水 和 10 mL 乙 酸 乙 酯 萃 取分离。 分出有机层, 用饱和氯化钠溶液洗涤, 干 燥, 浓缩, 得到 1.89 g 目标化合物 5, 收率 83.0%, m.p.115.0 ~116.2℃ ( 文 献 [4] 值 : 收 率 96% , m.p. 115.5 ~119℃ ) ; 1H NMR (CDCl3), δ: 1.85 ~1.92 ( 1H, m) , 2.34 ( 3H, s) , 2.68 ~2.85 ( 1H, m) , 2.99 ( 3H, s) , 3.10 ( 3H, s) , 3.46 ~3.49 ( 1H, t) , 3.99 ~4.13 ( 2H, m) , 4.75 ( 1H, m) , 5.01 ~ 5.34 (2H, m) , 7.46~7.52 (2H, dd, J =8.0 Hz) , 8.19~8.23(2H, d, J=8.0 Hz);[α]2D0=7.57°,(c 0.370,
2 实验部分
2.1 仪器与试剂 仪器: XH-100B 微波催化合成 / 萃取仪 (北京
祥鹄)、 WRS-1B 数字熔点仪 (温度未经校正, 上 海精科)、 DRX500 核磁共振仪 (四 甲 基 硅 烷 为 内 标, 德国布鲁克公司)、 IR200 红外光谱 仪 (溴 化 钾压片 , 美 国 热 电 ); Micromass GCT 质 谱 仪 (英 国 质 谱 公 司 )、 Agilent 1200 高 效 液 相 色 谱 仪 (美 国 Agilent 公司)、 Autopol Ⅲ自动旋光仪 (美国鲁 道夫公司)。
(2S,4S)-2-二甲氨基甲酰基-4-巯基-1-(4-硝 基苯甲氧羰基)吡咯烷(1)是合成碳青霉烯类抗生素 的重要中间体和合成砌块, 关于该中间体的合成, 文献 报 [4-9] 道了多种方法, 均以反式-4-羟基-L-脯 氨酸为原料经酰化等多步反应制备目标化合物, 需
要使用四水醋酸镍、 正三丁基膦、 三苯膦、 偶氮化 合物和氯甲酸异丙酯等反应试剂并需惰性气体保护 反应条件等。 笔者综合考虑原料来源、 操作难易、 转化率以及后处理等多种因素, 选择如下所示的路 线合成目标化合物 1。
2.33 ( 1H, m) , 3.56 ~3.64 ( 2H, m) , 4.40 ~4.49 (2H, 2×t, J=8.09 Hz), 5.15~5.33 (2H, 2×dd, J= 13.85 Hz) , 7.56 ~7.74 ( 2H , m ) , 8.20 ~8.24 (2H , t ) ; [α ]D20=-44.60° (c 1.000, CH3OH)。 2.2.2 (2S,4R)-2-二 甲 氨 基 甲 酰 基-4-甲 磺 酰 氧
第 40 卷第 3 期 2010 年 6 月
!!!!!!!!!!!
医药及中间体
精细化工中间体
FINE CHEMICAL INTERMEDIATES
Vol. 40 No. 3 JUNE 2010
!!
!!
!!!!!!!!!!!
美罗培南中间体的合成与结构表征
马红梅, 黄顺忠, 李红昌, 王晓晨, 祝衡华, 徐仲玉 *
第3期
马红梅, 等: 美罗培南中间体的合成与结构表征
31
acetone)。 2.2.4 (2S,4S)-2-二甲氨基甲酰基-4-巯基-1-(4-
硝基苯甲氧羰基)吡咯烷(1)的合成 将 2.2 g (5.6 mmo1) (2S,4S)-2-二甲氨基甲酰 基-4-乙 酰 硫 基-1-(4-硝 基 苯 甲 氧 羰 基 ) 吡 咯 烷 (5)加至适量甲醇中, 搅拌溶解, 冷却至-10℃, 滴 加 1.1 mL (4 mol / L) 氢 氧 化 钠 溶 液 , -10℃ 反 应 40 min, 反应毕, 以 4 mol / L 氢氧化钠溶液调反应 液 pH 值为 10, 二氯甲烷提取, 水层用 4 mol / L 盐 酸调 pH 值为 1, 乙酸乙酯提取, 有机层用饱和氯 化钠溶液洗涤, 干燥, 浓缩后得 1.67 g 淡红色固体 粉末 1, 收率 85.0 %, m.p.118~120℃, [α]2D0=+9.53° ( c1.012, CH3Cl) { 文 献 [4] 值 m.p.118.5 ~119.5℃ , [α]D20+9.60° (c 1.01, CH3Cl) } ; EI-MS m / Z 354.1 (M+1)。
