芳香烃PPT下载1
合集下载
新课标人教选修 芳香烃全部PPT课件
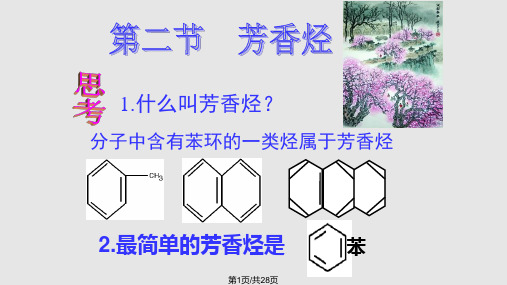
A
B
C
D
第12页/共28页
(1)长导管的作用:导气兼起 冷凝回流作用,防止苯和溴的 挥发
(2)锥形瓶内导管不插入液面 以下的原因:防止倒吸
第13页/共28页
2Fe + 3Br2 = 2FeBr3
+ Br2 FeBr3
实验步骤:按左图连 接好实验装置,并检 验装置的气密性.把 少量苯和液态溴放 在烧瓶里.同时加入 少量铁粉.在常温下, 很快就会看到实验 现象.
第20页/共28页
二、苯的同系物
1.定义: 苯环上的氢原子被烷基取代的产物
通式: CnH2n-6(n≥6)
结构特点: 只含有一个苯环,苯环上连结烷基.
1.比较苯和甲苯结构的异同点,推测甲苯的化 学性质. 2.设计实验证明你的推测.
第21页/共28页
1.取苯、甲苯各2分别注入2支试
管中,各加入3滴KMnO4酸性溶 液,充分振荡,观察现象。
第9页/共28页
1)苯的氧化反应:在空气中燃烧 2C6H6+15O2 点燃 12CO2+ 6H2O 但不能使酸性高锰酸钾溶液褪色
产生 浓烟
2)苯的加成反应 (与H2、Cl2)
+ H2 Ni
环己烷
H l H Cl
+ 3Cl2
催化剂
第10页/共28页
Cl
H
H
Cl
Cl H
H Cl
3)苯的取代反应(卤代、硝化、磺化)
第19页/共28页
1.配制浓硫酸与浓硝酸混和酸时,是否可以将 浓硝酸加入到浓硫酸中?为什么? 2.步骤③中,为了使反应在50-60℃下进行,常 用的方法是什么? 3.步骤④中洗涤、分离粗硝基苯使用的主要 仪器是什么? 4.步骤④中粗产品用5%NaOH溶液洗涤的目的 是什么? 5.敞口玻璃管的作用是什么?浓硫酸的作用是 什么?
《芳香烃》 课件1

设计制备溴苯实验方案——改进 苯与溴的反应
液溴、苯、铁粉
硝酸银溶液
两者相比,后一装置有哪些优点?
2
(氯苯) +HCl
设计苯的硝化反应实验方案 ②硝化 (苯分子中的 H原子被硝基取代的反应)
+ HO- NO2
浓 H2SO4 50℃ 3; H2O
【资料】硝基苯,无色,油状液体,苦杏仁味,有毒, 密度大于水,难溶于水,易溶于有机溶剂。硝基苯 蒸气有毒性。
甲苯
C7H8
萘 C10H8
蒽 C14H10 苯
最简单的芳香烃:
一、苯(benzene)的结构与化学性质
1、苯的物理性质
(1) 无色、有特殊气味的液体。 (2) 密度比水小(0.88g/ml),不溶于 水,易溶于有机溶剂。(常用做有机溶剂) (3) 熔点为5.5℃,沸点为80.1℃。熔沸点 低,易挥发,用冷水冷却,苯凝结成无色 晶体 (4) 苯有毒。
H C C H C H
3、苯的化学性质
稳定性。易取代,难加成,可燃烧,不氧化。
反应的化学方程式
苯与溴发生 C6H6+Br2 取代反应 苯与浓硝酸 发生取代反 应
反应条件
C6H5Br+HBr 液溴. 铁粉做催化剂 50℃~60℃水浴加 热、浓硫酸做催化 剂吸水剂
苯与氢气发 生加成反应
C6H6+3H2
(苯磺酸) 苯磺酸:无色针状或片状晶 体,易溶于水,乙醇,微溶 于苯,不溶于乙醚、二硫化 碳。
3)苯的加成反应 (与H2、Cl2)
+3 H2
Ni
加热加压
(环己烷) H Cl H Cl
+ 3Cl2
紫外线
Cl H
H
芳香烃PPT人教版1

12CO2+ 6H2O
但不能使酸性高锰酸钾溶液褪色
产生 黑烟
在乙烯、乙炔、苯分子中,含碳的质量分数较甲烷等 烷烃高,乙炔、苯分子中含碳的质量分数又比乙烯高。乙 烯、乙炔、苯在空气中燃烧不完全,易产生黑烟,乙炔、 苯的黑烟更浓。
(2)苯的加成反应
(1)苯的氧化反应:在空气中燃烧
点燃
2C6H6+15O2
(1)结构式
H
(2)结构简式
(3)比例模型:
C
HC
CH
HC
CH
C
H
➢回顾2.苯的结构特点 2.组成与结构: 分子式: C6H6
(1)结构式
H
(2)结构简式
(3)比例模型:
C
HC
CH
HC
CH
C
H
(苯的凯库勒式)
➢回顾2.苯的结构特点 2.组成与结构: 分子式: C6H6
(1)结构式
H
(2)结构简式
点燃
2C6H6+15O2
12CO2+ 6H2O
但不能使酸性高锰酸钾溶液褪色
产生 黑烟
在乙烯、乙炔、苯分子中,含碳的质量分数较甲烷等 烷烃高,乙炔、苯分子中含碳的质量分数又比乙烯高。乙 烯、乙炔、苯在空气中燃烧不完全,易产生黑烟,乙炔、 苯的黑烟更浓。
(1)苯的氧化反应:在空气中燃烧
点燃
2C6H6+15O2
2.各个键角都是120°
(4)结构特点 苯分子具有平面正六边形结构。 1.6个碳原子、6个氢原子均在 同一平面上。
2.各个键角都是120° 3.苯分子中的6个碳原子之间的
键完全相同,是一种介于单键和双键之间的独特的 键。因此常用 来表示苯分子。苯的结构使苯的
化学课件《芳香烃》优秀ppt优秀ppt9 人教课标版

5/19/2019
③温度计的位置,必须悬挂在水浴中。 ④不纯的硝基苯(显因黄为色溶有NO2)而纯净硝 基苯是无色,有苦杏仁味,比水重,油 状液体。 ⑤为提纯硝基苯,一般将粗产品依次用
蒸馏水和NaOH溶液洗涤。
5/19/2019
(3)磺化(苯分子中的H原子被磺 酸基取代的反应)
+ HO-SO3H 70℃~80℃
5/19/2019
(1)卤代反应---苯跟溴的反应
问题1:导管口为什么在液面上? 溴化氢易溶于水,防止倒吸。
问题2:什么现象说明发生了取代反应?
导管口有白雾。锥形瓶里滴入硝酸银溶液后 生成浅黄色沉淀,说明苯跟溴反应时苯环上 的一个氢原子被溴原子取代,生成溴化氢。
问题3:怎样除去无色溴苯中所溶解的溴?
联苯或多联苯:苯环之间通过碳碳单键直接相连
—
联苯(C12H10)
稠环芳烃:苯环之间通过共用苯环的若干环边
而形成
萘(C10H8)
蒽(C14H10)
5/19/2019
三、芳香烃的来源及其应用
芳香烃对健康的危害
是黏合剂、油性涂料、油墨等的常用有机溶剂
操作车间空气中苯的浓度≤40mg·m-3
苯 居室内空气中苯含量平均每小时≤0.09mg·m-3
未褪色
2mL甲苯 3滴高锰酸钾酸性溶液
用力振荡
褪色
实验 结论:
苯不能被KMnO4酸性溶液氧化, 甲苯能被KMnO4酸性溶液氧化
5/19/2019
二、苯的同系物
甲苯被氧化的是侧链,即甲基被氧化,该
反应可简单表示为:
CH3
KMnO4、H+
COOH
(苯甲酸)
这样的氧化反应,都是苯环上的烷烃基被 氧化,说明了苯环上的烷烃基比烷烃性质活泼。 这活泼性是苯环对烷烃基影响的结果。
③温度计的位置,必须悬挂在水浴中。 ④不纯的硝基苯(显因黄为色溶有NO2)而纯净硝 基苯是无色,有苦杏仁味,比水重,油 状液体。 ⑤为提纯硝基苯,一般将粗产品依次用
蒸馏水和NaOH溶液洗涤。
5/19/2019
(3)磺化(苯分子中的H原子被磺 酸基取代的反应)
+ HO-SO3H 70℃~80℃
5/19/2019
(1)卤代反应---苯跟溴的反应
问题1:导管口为什么在液面上? 溴化氢易溶于水,防止倒吸。
问题2:什么现象说明发生了取代反应?
导管口有白雾。锥形瓶里滴入硝酸银溶液后 生成浅黄色沉淀,说明苯跟溴反应时苯环上 的一个氢原子被溴原子取代,生成溴化氢。
问题3:怎样除去无色溴苯中所溶解的溴?
联苯或多联苯:苯环之间通过碳碳单键直接相连
—
联苯(C12H10)
稠环芳烃:苯环之间通过共用苯环的若干环边
而形成
萘(C10H8)
蒽(C14H10)
5/19/2019
三、芳香烃的来源及其应用
芳香烃对健康的危害
是黏合剂、油性涂料、油墨等的常用有机溶剂
操作车间空气中苯的浓度≤40mg·m-3
苯 居室内空气中苯含量平均每小时≤0.09mg·m-3
未褪色
2mL甲苯 3滴高锰酸钾酸性溶液
用力振荡
褪色
实验 结论:
苯不能被KMnO4酸性溶液氧化, 甲苯能被KMnO4酸性溶液氧化
5/19/2019
二、苯的同系物
甲苯被氧化的是侧链,即甲基被氧化,该
反应可简单表示为:
CH3
KMnO4、H+
COOH
(苯甲酸)
这样的氧化反应,都是苯环上的烷烃基被 氧化,说明了苯环上的烷烃基比烷烃性质活泼。 这活泼性是苯环对烷烃基影响的结果。
芳香烃实用ppt人教版
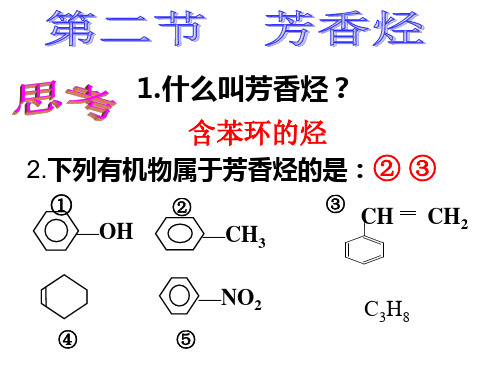
|
酸性高锰酸钾溶液
O || C—OH
|
烷基上与苯环直接相连的碳上 连有氢原子
2、取代反应 A:卤代
CH3
+Cl2 光照
CH2Cl+HCl
CH3
+Cl2 FeBr3
CH3
—Cl
+HCl
或 Cl—
CH3
+HCl
B:硝化
CH3
CH3
浓硫酸 O2N
NO2
+ 3HNO3 △
+ 3H2O
NO2
三硝基甲苯(TNT)
3、苯的邻位二元取代只产生一种取代 产
物 —— 6个碳原子和6个氢原子等效
巩固训练
1、下列各组中互为同分异构体的是
Cl
CD
A.
Cl
Cl
Cl
B.
Cl Cl
Cl
Cl
C.Cl
D. Cl
Cl
Cl
2.下列物质中所有原子都有可能在同一
平面上的是 (BC )
Cl
A.乙烷 B.乙烯 C.
CH3
D.
3.能通过化学反应使溴水褪色,又能
1、氧化反应 A:燃烧 现象与苯类似
B:与酸性高锰酸钾
现象
结论
苯+酸性
苯不能被酸性高
高锰酸钾 溶液不褪色 锰酸钾氧化
甲苯+酸性 溶液褪色 高锰酸钾
甲苯能被酸性 KMnO4溶液 氧化
①甲苯被氧化的是侧链,即甲基被氧化, 该反应可简单表示为:
CH3
KMnO4、H+
COOH
(苯甲酸)
苯环上的烷烃基被氧化。
•
3. 辞官归隐田园后融入大自然怀抱里的悠 闲自得 ,忘却 了荣辱 得失, 尽享田 园生活 之恬淡 。
酸性高锰酸钾溶液
O || C—OH
|
烷基上与苯环直接相连的碳上 连有氢原子
2、取代反应 A:卤代
CH3
+Cl2 光照
CH2Cl+HCl
CH3
+Cl2 FeBr3
CH3
—Cl
+HCl
或 Cl—
CH3
+HCl
B:硝化
CH3
CH3
浓硫酸 O2N
NO2
+ 3HNO3 △
+ 3H2O
NO2
三硝基甲苯(TNT)
3、苯的邻位二元取代只产生一种取代 产
物 —— 6个碳原子和6个氢原子等效
巩固训练
1、下列各组中互为同分异构体的是
Cl
CD
A.
Cl
Cl
Cl
B.
Cl Cl
Cl
Cl
C.Cl
D. Cl
Cl
Cl
2.下列物质中所有原子都有可能在同一
平面上的是 (BC )
Cl
A.乙烷 B.乙烯 C.
CH3
D.
3.能通过化学反应使溴水褪色,又能
1、氧化反应 A:燃烧 现象与苯类似
B:与酸性高锰酸钾
现象
结论
苯+酸性
苯不能被酸性高
高锰酸钾 溶液不褪色 锰酸钾氧化
甲苯+酸性 溶液褪色 高锰酸钾
甲苯能被酸性 KMnO4溶液 氧化
①甲苯被氧化的是侧链,即甲基被氧化, 该反应可简单表示为:
CH3
KMnO4、H+
COOH
(苯甲酸)
苯环上的烷烃基被氧化。
•
3. 辞官归隐田园后融入大自然怀抱里的悠 闲自得 ,忘却 了荣辱 得失, 尽享田 园生活 之恬淡 。
《芳香烃》课件(新人教版选修5)

㈢ 苯的同系物加成反应
苯的同系物也和氢气可以发生加成反应
CH3 + 3H2
催化剂
CH3
三、芳香烃的来源及其应用 1、来源:
a、煤的干馏 b、石油的催化重整 应用:简单的芳香烃是基本的有机化工原 料。
课外研究活动:
生活中的苯及其同系物或衍生物
加成
3、苯的化学性质
(1).加成反应(与H2、Cl2,不能与溴水)
Ni
+ 3H2
C6H6
H2C 己烷
△
C6H12
3
C6H6Cl6
(2).取代反应 ①溴代反应
H
FeBr3
+ Br2
Br
+ HBr
注意: 反应物:苯和液溴(不能用溴水) 反应条件:催化剂(FeBr3或Fe) 溴苯不溶于水且密度大于水无色油状物
2.如何提纯硝基苯? 5%NaOH溶液洗涤,最后再用蒸馏水洗涤.将 用无水CaCl2干燥后的粗硝基苯进行蒸馏, 得到纯硝基苯
(3).氧化反应—燃烧
2C6H6 + 15 O2
点燃
12CO2+6 H2O
①现象:火焰明亮并伴有大量的黑烟
②注意:不能被高锰酸钾氧化使其褪色
苯的化学性质:
(易取代、 能氧化、难加成)
迁移
苯的同系物的苯环易发生取代反应。
从上组反应中我们看到甲基受苯环影响使 得甲基易被氧化;那么苯环的化学性质有没有 受到甲基的影响呢?
甲苯的硝化反应比苯更容易进行
阅读课本P 38 实验以下的内容填表
温度 苯 甲苯
50℃- 60℃
生成物 硝基苯
邻、对位硝 基甲苯
30℃
比较苯和甲苯与KMnO4溶液的作用, 以及硝化反应的条件产物等,你从中得到 什么启示? 【结论】 侧链和苯环相互影响: 侧链受苯环影响易被氧化; 苯环受侧链影响易被取代。
芳香烃的主要化学性质PPT资料(正式版)

E
两类定位基团 (1) 第一类定位基(邻对位定位基)
NR2 NHR NH2 OH OR NHCOR OCOR
R
C6H5
X
(2). 第二类定位基(间位定位基)
N3R N2O CC 3 l CN SO 3H CHOCORCO 2R CON 2 H
定位规律的应用
(1)
N2O
A : (1)硝 化(2)氯 代
B:(1)氯 代(2)硝 化 Cl
HNO3 H2SO4
NO 2 C2l FeCl3
NO 2 Cl
C H 3
(2)
C O 2H A:(1)硝化(2)氧化 B:(1)氧化(2)硝化
N2O
CH3
HNO3 H2SO4
CH3 KMnO4
CO2H
NO2
NO2
二. 醇、酚、醚的主要反应
(一) 醇的主要反应反应
(A) 烷基化 Friedel—Crafts反应
V2O5 + O2 400 ~ 500 ℃
O + CO2 + H2O
(A) 烷基化
醇、酚、醚的主要反应
O
Getterman—Koch反应
(一) 醇的主要反应反应 Getterman—Koch反应
顺丁烯二酸酐
Maleic anhydride
侧链氧化
CH 3
反 应 活 性 : F2 > C l2 >FeB r3 或 Fe
+ HBr
80%
B rom obenzene
Cl
+ C l2
FeC l3 或 Fe
+ HCl
86%
C hlorobenzene
Friedel—Crafts反应 (A) 烷基化
化学课件《芳香烃》优秀ppt优秀ppt16 人教课标版1

二、苯分子的结构式及结构简式
分子式 :C6H6 (不饱和) 结构特点:
结构简式: 或
H
C
结构式: H C
CH
HC
CH
C
H
(1)苯分子是平面六 边形的稳定结构;
(2)苯分子中碳碳键 是介于碳碳单键与碳
碳双键之间的一种独 特的键;
(3)苯分子中六个碳 原子等效,六个氢原 子等效。
空间构型:平面正六边形
94.对一个适度工作的人而言,快乐来自于工作,有如花朵结果前拥有彩色的花瓣。――[约翰·拉斯金] 95.没有比时间更容易浪费的,同时没有比时间更珍贵的了,因为没有时间我们几乎无法做任何事。――[威廉·班] 96.人生真正的欢欣,就是在于你自认正在为一个伟大目标运用自己;而不是源于独自发光.自私渺小的忧烦躯壳,只知抱怨世界无法带给你快乐。――[萧伯纳]
苯的化学性质小结
苯环结构比较稳定,易发生取代反应, 而破坏结构的加成反应和氧Байду номын сангаас反应比较困 难。
(易取代、 能氧化、难加成)
二、苯的同系物
1.定义: 苯环上的氢原子被烷基取代的产物
通式: CnH2n-6(n≥6)
结构特点: 只含有一个苯环,苯环上连结烷基.
一 CH3 甲苯
一CH3 一CH3
邻二甲苯
高二化学选修5章烃和卤代烃
节芳香烃
思 考
1.什么叫芳香烃?
分子中含有苯环的一类烃属于芳香烃
2.最简单的芳香烃是?
苯
3.什么叫苯的同系物,代表物有哪 些?
一、苯的物理性质
1.无色,有特殊芳香气味的液体
2.密度小于水 3.不溶于水易溶于有机溶剂 4.熔点5.5℃, 沸点80.1℃ 5.易挥发(密封保存) 6.苯蒸气有毒
第五章芳香烃ppt课件

所以,也可用下式表示苯的结构:
6
第二节 单环芳烃的异构与命名
1.一元取代苯“某苯”
甲苯
乙苯
(toluene)
( ethylbenzene
) 有些取代基,有专门名称,将取代基和苯一 起作为母体。如苯酚 苯胺 苯甲酸 苯磺酸
7
2.二元取代苯的命名
邻二甲苯(1,2 间二甲苯(1,3 对二甲苯(1,4
一、取代反应
1. 卤代反应
16
烷基苯的卤代
苯氯甲烷 苯二氯甲烷 苯三氯甲烷
反应条件不同,产物也不同。原因是两者 反应历程不同,前者(铁粉或FeCl3作催化剂) 为离子型取代反应,光照卤代为自由基历程。
17
侧链较长的芳烃 ,光照卤代主要发生
在α碳原子上。
18
✓自由基的稳定性增加顺序:
<
<
(甲基自由基 < 伯自由基 < 仲自由
间位定位基则对苯环起吸电子作用,使苯 环电子云密度降低,因而不利于苯环的亲电取 代反应,即起钝化作用。
38
三、取代定位效应的应用 1. 指导选择合成路线
例1:
必须先氧化后硝化
39
例2:
40
例3:
41
第六节 稠环芳香烃
一、结构和命名 稠环芳香烃是由两个或两个以上苯环共用 两个邻位碳原子稠合而成的多环芳香烃。
蒽
菲
48
第三节 芳香性:4n+2规则
判断芳香性的规律:在一单环多烯化合物 中,具有共平面的离域体系,其 π 电子数等于 4n+2(n=0,1,2,3…) ,此化合物就具有芳香性。 此 规律称为Hückel 规律,又叫做4n+2规则。
π 电子数 4
有机化学第08章 芳香烃(共201张PPT)

再比较 4式和5式
4
催化 剂
+ H2 压 力, 溶剂
112.3KJ mol-1
5
催 化剂
+ H2
压力 ,溶 剂
按上面的计算和结论,5 式若为共轭三烯结构,当加一 分子氢时,氢化热应为-112.3-(-7.2) = -105.1 KJ mol -1。
催化剂
+ H2 压力,溶剂
(Z)
H?
(Z)
- 105.1 KJ mol -1
4 苯具有特殊的稳定性---从氢化热数据看苯的内能。
环己烯 环己二烯
环己三烯
苯
氢化热(kJ / mol) 119.5 (测定)
231.8 (测定)
119.53=358.5 208.5 (根据假设计算) (测定)
每个C=C的平均氢化热 119.5
115.9
119.5
69.5
(kJ / mol)
从整体看: 苯比环己三烯的能量低 苯比环己二烯的能量低
119.5 KJ mol-1
3
催化 剂
+ 2H2 压力,溶剂
231.8 KJ mol-1
4
催化 剂
+ H2 压力,溶剂
112.3KJ mol-1
(Z)
5.
催化剂
+ H2 压力,溶剂
H?
(Z)
6. CH2=CH-CH=CH-CH=CH2 + 3 H2 CH3(CH2)4CH3 -337 KJ mol-1
反键轨道
E 成键轨道
共振论
Ⅰ
Ⅱ
贡献大
键长,键角完全 相等的等价结构
Ⅲ
Ⅳ
Ⅴ
贡献小
键长、键角不等 的不等价结构
大学有机化学芳香烃PPT课件

复合技术
利用纳米技术可以制备出具有特殊功 能的芳香烃纳米材料,如纳米传感器、 纳米催化剂等。
将芳香烃与其他材料复合,可以制备 出具有优异性能的功能复合材料,如 导电高分子材料、耐高温材料等。
表面修饰技术
通过对芳香烃表面进行化学或物理修 饰,可以改变其表面性质,从而赋予 其新的功能,如超疏水、超亲水、抗 菌等。
生物活性评价方法简介
细胞毒性试验
通过测定药物对细胞的毒性作用, 评价药物的生物活性。常用的细 胞毒性试验方法包括MTT法、
LDH法等。
抗菌活性试验
对于具有抗菌作用的药物,可以 通过测定药物对细菌的抑制作用 来评价其生物活性。常用的抗菌 活性试验方法包括琼脂扩散法、
微量肉汤稀释法等。
抗肿瘤活性试验
通过测定药物对肿瘤细胞的增殖 抑制作用,评价药物的抗肿瘤活 性。常用的抗肿瘤活性试验方法 包括MTT法、克隆形成法ቤተ መጻሕፍቲ ባይዱ。
03
钯催化下烯烃与卤代芳烃的偶联反应,可高效构建C-C键,是芳
香烃合成的重要手段。
路线设计原则及实例分析
01
路线设计原则
02
原料易得、价格适中;
03
反应条件温和、操作简便;
04
产物易分离纯化、收率高;
05
符合绿色化学要求,减少废弃物排放。
06
实例分析:以苯乙烯为原料,通过Heck反应合成对甲基苯 乙烯。该路线原料易得,反应条件温和,产物收率高且易于 分离纯化。
高能源利用效率。
04
芳香烃在医药领域应用
药物合成中作用举例
苯环作为核心结构
许多药物都含有苯环,如阿司匹 林、对乙酰氨基酚等,这些药物
的合成离不开芳香烃。
芳香烃侧链修饰
课件《芳香烃》PPT全文课件_人教版1

苯的同系物的化学性质
1.氧化反应
①可燃性 如下图,A是制取溴苯的实验装置,B、C是改进后的装置,请仔细分析,对比三个装置,回答以下问题:
b、浓硫酸作用是催化剂、吸水剂
自从1845年人们从煤焦油内发现苯及其他芳香烃后,很长时间里煤是一切芳香烃的主要来源。
②可使酸性高锰酸钾褪色 书写苯的同系物的同分异构体时,苯环不变,变换取代基的位置及取代基碳链的长短即可。
②若该烃不能使溴水褪色,但能使酸性高锰酸钾溶液褪色,请写出它可能的结构简式并命名。 Ω值越大,则有机物的不饱和度越大。 如下图,A是制取溴苯的实验装置,B、C是改进后的装置,请仔细分析,对比三个装置,回答以下问题:
种特殊的键,所有碳碳键键长、键能全相等,键 物理性质:碳原子数较少的苯的同系物,在通常状况下都是无色、有特殊气味的液体,密度小于水,不溶于水,易溶于有机溶剂,其
预测苯的化学性质
苯的特殊结 构(介于单 双键之间)
苯具有特 殊性质
烷烃 取代
烯烃 加成
苯的化学性质
1)氧化反应——可燃性 如下图,A是制取溴苯的实验装置,B、C是改进后的装置,请仔细分析,对比三个装置,回答以下问题:
⑤不纯的硝基苯显黄色,因为溶有NO2,而纯净硝基苯是无色,有苦杏仁味,比水重油状液体。
下列各组物质用酸性高锰酸钾溶液和溴水都能区别的是( )
15) )3氧易.化挥将反发应(F密—封—e保可屑存燃)性加入烧瓶后,烧瓶内有什么现象?这说明什么?
2 B. 吸收反应中随HBr逸出的溴蒸气和苯蒸气
剧烈反应,轻微翻腾,有气体逸出。反应放热。 ②若该烃不能使溴水褪色,但能使酸性高锰酸钾溶液褪色,请写出它可能的结构简式并命名。
①浓硝酸和浓硫酸的混合酸要冷却到50~60℃以下,再 慢慢滴入苯,边加边振荡。(因为反应放热,温度过高, 苯易挥发,且硝酸也会分解,同时苯和浓硫酸在70~ 80℃时会发生反应。)
课件《芳香烃》精美PPT课件_人教版1

【思考与交流】填空 P37
反应的化学方程式
反应条件
苯与溴 发生取 代反应
苯与浓 硝酸发 生取代 反应
C6H6+Br2
C6H5Br +HBr
液溴. 铁粉做催化剂
50℃~60℃水浴 加热、浓硫酸做 催化剂吸水剂
苯与氢 气发生 加成反 应
C6H6+3H2
C6H12
镍做催化剂,加 热
设计制备溴苯实验方案
a、b煤、的石干油毒馏的催,化重密整 度大于水,难溶于水,易溶于有机溶剂。硝
基苯蒸气有毒性。 1、如何混合硫酸和硝酸的混合液?
反应过程中硝酸会部分分解。
(3)苯分子中碳碳键键长完全相等,是介于碳碳单键和碳碳双键之间的特殊的化学键。
1、如何混合硫酸和硝酸的混合液?
1.苯与硝酸的反应在50 ℃ --60℃ 时产物是硝基苯 用蒸馏水和氢氧化钠溶液洗涤,得纯硝基苯。
1.
切不可将浓硝酸注入浓硫酸中,因混和时要放出大量的热量,以免浓硫酸溅出,发生事故。
+ Br2 萘是一种主要的化工原料。
苯的磺化反应(取代)
FeBr3
2)苯的取代反应(卤代、硝化、磺化)
从上组反应中我们看到甲基受苯环影响使得甲基易被氧化;
Br+ HBr
5、如何得到纯净的硝基苯?
| 【| 注意】苯不能与溴水反应,但可以因为
4.哪些现象说明发生了取代反应而不是加成反应?
苯与溴反应生成溴苯的同时有溴化氢生成。
设计制备溴苯实验方案——改进
CCl4
硝酸银
②设硝化计苯(的苯分 硝子化中反的H应原实子验被硝 方基案取代的反应)
+ HO- NO 【注意】苯不能使酸性高锰酸钾溶液褪色。 2
第七章芳香烃-53页PPT文档资料

光 50℃
H Cl
CH l
H Cl
Cl 六 六 六 H 对 人 畜 有 害 , 世 界 禁 用 ,
HClHCl 我 国 从 83年 禁 用 。
三、氧化反应
O
2
V2O5 + 9O2
2 O +4CO2 +4H2O
450~500℃
O
顺 丁 烯 二 酸 酐
点 燃
2 +15O 2
12C O 2 + 6H 2O
55~60℃
+ Br2
Fe 或 FeBr3 55~60℃
+ 2Cl2 Fe 或 FeCl3
Cl
+
HCl
Br
+
HBr
Cl
+
Cl
+ 2H
烷基苯的卤代
CH3
CH3
FeC3l
Cl
+ Cl
CH3 + HCl
+ Cl2
光orΔ
CH2Cl
Cl2 光orΔ
CHC2l
Cl2 光or Δ
CC3l
氯化苄 (苯氯甲烷)
苯二氯 甲烷
H2S4 O , S3 O
S3 O H
变 慢 , 水 解 速 度 加 快 , 故 常 用 发 烟 硫 酸 进 行 磺 化 ,
30~50℃
以 减 少 可 逆 反 应 的 发 生 。
烷基苯比苯易磺化
CH3
+ H2SO4
CH3
SO3H +
CH3
邻甲基苯磺酸 43%
SO3H
对甲基苯磺酸
苯磺酸继续磺化比苯困难
2.一元取代苯的命名
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
•
5.所有进入现场使用的成品、半成品 、设备 、材料 、器具 ,均主 动向监 理工程 师提交 产品合 格证或 质保书 ,应按 规定使 用前需 进行物 理化学 试验检 测的材 料,主 动递交 检测结 果报告 ,使所 使用的 材料、 设备不 给工程 造成浪 费。
•
谢谢观看
•
1.我公司将积极配合监理工程师及现 场监理 工程师 代表履 行他们 的职责 和权力 。
四氯化碳溶液褪色 • 和H2完全加成的热效应△H=-
208.4kJ·mol-1,与碳碳双键与H2完全加成 的热效应的△H= -119.6kJ·mol-1)的三倍 比相差较大 • 苯中所有碳碳键的键长、键能相同
说明苯分子中不是单双建交替的结构的
苯分子中的碳碳键是介于碳碳单键和碳 碳双键之间的特殊的碳碳键。
•
5.所有进入现场使用的成品、半成品 、设备 、材料 、器具 ,均主 动向监 理工程 师提交 产品合 格证或 质保书 ,应按 规定使 用前需 进行物 理化学 试验检 测的材 料,主 动递交 检测结 果报告 ,使所 使用的 材料、 设备不 给工程 造成浪 费。
•
谢谢观看
有毒: 对人的神经系统、造血系统 有伤害,可导致白血病。
芳香烃对人体健康有伤害
二、苯分子的结构
1、分子式 C6H6
从苯的分子组成看,高度不饱和。
• 苯的结构——凯库勒式 H
H
CC
HC
CH
C H
C H
二、苯分子结构的探究
1、用取代产物验证
苯的邻位二取代物只有一种 2、用实验事实说明
苯不能像烯烃、炔烃那样使酸性KMnO4溶液 褪色,不能通过化学反应使溴水褪色。 往苯中加入酸性KMnO4溶上液层:无色,下层紫红色 往苯中加入溴水:上层橙红色,下层无色
•
3.在施工全过程中,严格按照经招标 人及监 理工程 师批准 的“施 工组织 设计” 进行工 程的质 量管理 。在分 包单位 “自检 ”和总 承包专 检的基 础上, 接受监 理工程 师的验 收和检 查,并 按照监 理工程 师的要 求,予 以整改 。
•
、4.贯彻总包单位已建立的质量控制 、检查 、管理 制度, 并据此 对各分 包施工 单位予 以检控 ,确保 产品达 到优良 。总承 包对整 个工程 产品质 量负有 最终责 任,任 何分包 单位工 作的失 职、失 误造成 的严重 后果, 招标人 只认总 承包方 ,因而 总承包 方必须 杜绝现 场施工 分包单 位不服 从总承 包方和 监理工 程师监 理的不 正常现 象。
新课标苏教版选修五 有机化学基础 第二单元 芳香烃
苯的结构与性质
芳香烃
芳香族化合物的含义
历史含义:具有香味的物质 现实意义:名称沿用 现代含义:含苯环的的有机化合物 芳香烃:芳香族化合物的一种
是芳香族碳氢化合物的简称 又称“芳烃”
一、苯的物理性质
无色液体,有特殊气味,熔点5.5℃, 沸点80.1℃ ,易挥发,比水轻,不溶 于水,是重要的有机溶剂。
3、从能量的角度探究 相同碳原子数的环己烯、环己二烯和苯在加氢时放出 的热量不成正比。
能量越低,越稳定 苯环是一种稳定的特殊结构 4、从键长、键角的角度分析 碳碳单键键长:1.54×10-10m 碳碳双键键长:1.34×10-10m 苯分子中C-C键长都相等,为1.40×10-10m
苯的结构
• 邻二取代物只有一种 • 不能因化学变化使酸性高锰酸钾溶液或溴的
所以凯库勒式仅有习惯性的纪念意义
三、苯的化学性质
1.卤代反应
FeBr
—Br +HBr
3
溴苯:无色油状液+体B,r2密度大于水
2.硝化反应
苯与浓硝酸、浓硫酸的 混合物在60℃时生成 一取代硝基苯,
+ HNO3
浓硫酸 60℃
—NO2 + H2O
硝基苯:苦杏仁味,有毒,无色油状液体,密度大于水
3.加成反应 ——工业制取环己烷的主要方法
•
3.在施工全过程中,严格按照经招标 人及监 理工程 师批准 的“施 工组织 设计” 进行工 程的质 量管理 。在分 包单位 “自检 ”和总 承包专 检的基 础上, 接受监 理工程 师的验 收和检 查,并 按照监 理工程 师的要 求,予 以整改 。
•
、4.贯彻总包单位已建立的质量控制 、检查 、管理 制度, 并据此 对各分 包施工 单位予 以检控 ,确保 产品达 到优良 。总承 包对整 个工程 产品质 量负有 最终责 任,任 何分包 单位工 作的失 职、失 误造成 的严重 后果, 招标人 只认总 承包方 ,因而 总承包 方必须 杜绝现 场施工 分包单 位不服 从总承 包方和 监理工 程师监 理的不 正常现 象。
+
3H2
Ni 18MPa
4.氧化反应(燃烧18)0~250℃
2C6H6+15O212CO2+6—H—2O冒浓的黑烟
苯环结构比较稳定,易发生取代反应,而 破坏结构的加成反应比较困难
难加成、易取代
•
1.我公司将积极配合监理工程师及现 场监理 工程师 代表履 行他们 的职责 和权力 。
•
2.我公司在开工前,将根据合同中明 确规定 的永久 性工程 图纸, 施工进 度计划 ,施工 组织设 计等文 件及时 提交给 监理工 程师批 准。以 使监理 工程师 对该项 设计的 适用性 和完备 性进行 审查并 满意所 必需的 图纸、 规范、 计算书 及其他 资料; 也使招 标人能 操作、 维修、 拆除、 组装及 调整所 设计的 永久性 工程。
•
2.我公司在开工前,将根据合同中明 确规定 的永久 性工程 图纸, 施工进 度计划 ,施工 组织设 计等文 件及时 提交给 监理工 程师批 准。以 使监理 工程师 对该项 设计的 适用性 和完备 性进行 审查并 满意所 必需的 图纸、 规范、 计算书 及其他 资料; 也使招 标人能 操作、 维修、 拆除、 组装及 调整所 设计的 永久性 工程。
