(整理)G109-94-3-MT7-NO3硝态氮和亚硝态氮.
废水总氮的去除介绍
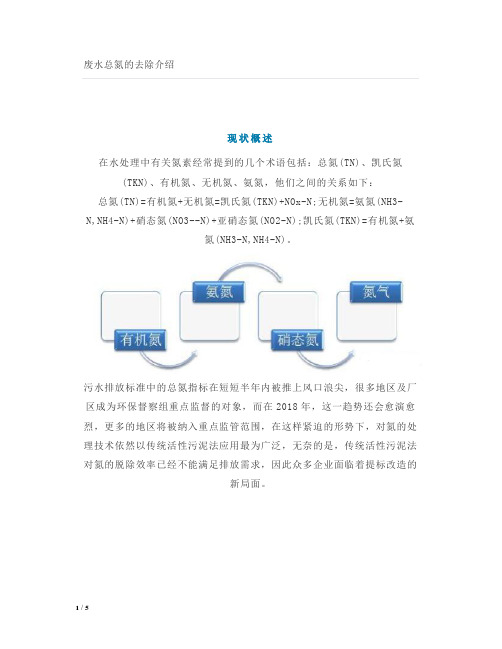
现状概述在水处理中有关氮素经常提到的几个术语包括:总氮(TN)、凯氏氮(TKN)、有机氮、无机氮、氨氮,他们之间的关系如下:总氮(TN)=有机氮+无机氮=凯氏氮(TKN)+NOx-N;无机氮=氨氮(NH3-N,NH4-N)+硝态氮(NO3--N)+亚硝态氮(NO2-N);凯氏氮(TKN)=有机氮+氨氮(NH3-N,NH4-N)。
污水排放标准中的总氮指标在短短半年内被推上风口浪尖,很多地区及厂区成为环保督察组重点监督的对象,而在2018年,这一趋势还会愈演愈烈,更多的地区将被纳入重点监管范围,在这样紧迫的形势下,对氮的处理技术依然以传统活性污泥法应用最为广泛,无奈的是,传统活性污泥法对氮的脱除效率已经不能满足排放需求,因此众多企业面临着提标改造的新局面。
基本原理在废水脱氮技术中广泛使用生物法进行处理,生物脱氮是依靠水体中微生物的生理代谢作用将不同形态的氮转化为氮气的过程,流程为:废水中难降解的有机氮通过水解氨化作用,分解为氨氮(NH3--N,NH4-N),氨氮在亚硝化作用及硝化作用下,转化为硝态氮(NOX-N),继而在反硝化作用下转化为氮气。
技术分析目前处理总氮的方法中生化法备受青睐,原因包括起源较早、技术成熟、成本较低等,在我国几十年的污水处理中,生化法一直占据着主体地位,但工艺上的不足也随着排放标准的提高逐渐显现而出,尤其对氮磷的去除效果仅依靠供给微生物的自然生理需求以得到一定程度的减少,在污水中氮磷浓度较高时,依靠传统污泥法往往达不到预想的结果。
当然,在活性污泥法的实践应用中也出现了很多变形工艺,包括膜生物反应器、生物滤池技术及生物转盘等,但一方面成本较高,另一方面,技术的不成熟使大多数企业不愿轻易尝试,因此很少有优质的案例作为模范,也很少有企业愿意共同尝试寻求技术的实践改进,使这些技术很难取得突破性进展。
实际应用在实际生产中,根据不同水质需求应对生化脱氮的不同环节进行强化,例如农药生产厂区产生的废水通常含有大量有机氮,因此需规模较大的水解工艺,将难降解的有机氮转化为容易被转化的小分子有机氮,从而转化为氨氮。
水中硝态氮的测定国标

水中硝态氮的测定国标摘要:I.硝态氮的概述A.硝态氮的定义B.硝态氮在水中的来源II.硝态氮的测定方法A.国标测定方法1.酚二磺酸法2.原理3.试剂配制4.测定步骤B.其他测定方法1.水杨酸—次氯酸盐分光光度法2.偶氮分光光度法III.硝态氮测定的应用A.环境保护1.水质监测2.污水处理B.农业生产1.土壤改良2.肥料施用正文:硝态氮是一种在水环境中广泛存在的氮形态,对水体的生态环境和人类健康具有重要影响。
因此,准确测定水中硝态氮的含量至关重要。
本文将介绍水中硝态氮的测定国标方法以及其在环境保护和农业生产中的应用。
一、硝态氮的概述硝态氮是指水中以硝酸根离子(NO3-)形式存在的氮。
它主要来源于含氮有机物的分解、硝酸盐化肥的施用以及污水排放等。
硝态氮对水生生物和人类健康有潜在危害,因此,在水环境中进行硝态氮的测定具有重要意义。
二、硝态氮的测定方法目前,我国已经建立了测定水中硝态氮的国家标准方法,即酚二磺酸法。
1.酚二磺酸法酚二磺酸法是一种分光光度法,其原理是在无水条件下,硝酸根离子与酚二磺酸试剂作用,生成硝基酚二磺酸。
生成物在酸性介质中无色,碱化后则为稳定的黄色盐溶液,可在400-425nm 处比色测定。
试剂配制:(1) 酚二磺酸显色剂:将3g 结晶纯酚与20.1ml 浓硫酸(比重1.84)混合,在沸水浴上加热6 小时,加热时瓶口用带长玻管的塞子塞住,以使酸不致于蒸发损失。
(2) 氨基苯磺酰胺溶液:10 克每升。
(3) 1-萘替乙二胺二盐酸盐溶液:1 克每升。
测定步骤:1) 水样做恰当的预处理。
2) 取10mL 预处理后的水样,加入0.5mL 氨基苯磺酰胺溶液,摇匀后放置5 分钟。
3) 加入0.5mL 1-萘替乙二胺二盐酸盐溶液,摇匀后放置30 分钟。
4) 用分光光度计在540nm 波长下测定溶液的吸光度。
2.其他测定方法除了酚二磺酸法外,还有其他一些测定水中硝态氮的方法,如水杨酸—次氯酸盐分光光度法和偶氮分光光度法。
脲酶抑制剂与硝化抑制剂对稻田土壤硝化、反硝化功能菌的影响

脲酶抑制剂与硝化抑制剂对稻田土壤硝化、反硝化功能菌的影响ZHANG Wen-xue;WANG Shao-xian;XIA Wen-jian;SUN Gang;LIU Zeng-bing;LI Zu-zhang;LIU Guang-rong【摘要】[目的]在农业生产中,脲酶抑制剂(urease inhibitor,UI)与硝化抑制剂(nitrification inhibitor,NI)常作为氮肥增效剂来提高肥料利用率.本文研究了在我国南方红壤稻田施用脲酶抑制剂与硝化抑制剂后,土壤中氨氧化细菌(ammonia oxidizing bacteria,AOB)、氨氧化古菌(ammonia-oxidizing archaea,AOA)以及反硝化细菌的丰度以及群落结构的变化特征,旨在揭示抑制剂的作用机理及其对土壤环境的影响.[方法]试验在我国南方红壤稻田进行,共设5个处理:1)不施氮肥(CK);2)尿素(U);3)尿素+脲酶抑制剂(U+UI);4)尿素+硝化抑制剂(U+NI);5)尿素+脲酶抑制剂+硝化抑制剂(U+UI+NI),3次重复.脲酶抑制剂与硝化抑制剂分别为NBPT[N-(n-butyl)thiophosphrictriamide,N-丁基硫代磷酰三胺]和DMPP(3,4-dimethylpyrazole phosphate,3,4-二甲基吡唑磷酸盐).通过荧光定量PCR(Real-time PCR)研究水稻分蘖期与孕穗期抑制剂对三类微生物标记基因拷贝数的影响,并分析土壤铵态氮、硝态氮与三种菌群丰度的相关性;利用变性梯度凝胶电泳(Denaturing Gradient Gel Electrophoresis,DGGE)分析抑制剂对土壤AOB、AOA以及反硝化细菌群落结构的影响,并对优势菌群进行系统发育分析.[结果]1)荧光定量PCR结果表明,施用氮肥对两个时期土壤中AOB的amoA基因与反硝化细菌nirK基因的拷贝数均有显著提高,而对AOA的amoA基因始终没有明显影响;AOB与nirK反硝化细菌的丰度与两个时期的铵态氮含量、分蘖期的硝态氮含量呈极显著正相关,与孕穗期的硝态氮含量相关性不显著;DMPP仅在分蘖期显著减少了AOB的amoA基因拷贝数,表明DMPP主要通过限制AOB的生长来抑制稻田土壤硝化过程;NBPT对三类微生物的丰度无明显影响;2)DGGE图谱表明,在分蘖期与孕穗期,施用氮肥均明显增加了图谱中AOB的条带数,而对AOA却没有明显影响;氮肥明显增加了孕穗期反硝化细菌的条带数;与氮肥的影响相比,抑制剂NBPT与DMPP对AOA、AOB以及反硝化菌的群落结构影响甚微;系统发育分析结果表明,与土壤中AOB的优势菌群序列较为接近的有亚硝化单胞菌和亚硝化螺菌.[结论]在南方红壤稻田中,施入氮肥可显著提高AOB与反硝化细菌的丰度,明显影响两种菌群的群落结构,而AOA较为稳定;NBPT对三类微生物的群落结构丰度无明显影响;硝化抑制剂DMPP可抑制AOB的生长但仅表现在分蘖期,这可能是其缓解硝化反应的主要途径;这也说明二者对土壤生态环境均安全可靠.【期刊名称】《植物营养与肥料学报》【年(卷),期】2019(025)006【总页数】13页(P897-909)【关键词】抑制剂;稻田;氨氧化细菌;氨氧化古菌;反硝化细菌【作者】ZHANG Wen-xue;WANG Shao-xian;XIA Wen-jian;SUN Gang;LIU Zeng-bing;LI Zu-zhang;LIU Guang-rong【作者单位】;;;;;;【正文语种】中文尿素是一种高浓度的酰胺态氮肥,因其较高的含氮量被作为农业生产上最常用的氮肥,但是尿素施入农田后会导致氮素损失是一直被关注的。
蔬菜的硝态氮累积及菜地土壤的硝态氮残留_王朝辉

蔬菜的硝态氮累积及菜地土壤的硝态氮残留王朝辉,宗志强,李生秀,陈宝明(西北农林科技大学资源环境学院,陕西杨陵712100,E -mail:zhao -huiw @)摘要:在不同季节对11类、48种蔬菜的测定表明,硝态氮含量高于325mg #kg -1,达到4级污染水平的有20种,占调查总数的4117%,包括全部叶菜类、部分瓜类、根菜类和葱蒜类蔬菜.其中硝态氮含量高于700mg #kg -1,超过4级污染水平的有5种,均为叶菜类蔬菜.叶菜硝态氮累积虽为严重,但其中部分蔬菜叶片的硝态氮含量却低于3级污染水平.对不同类型菜地和农田土壤的测定发现,菜地0~200cm 各土层的硝态氮残留量均高于农田土壤,常年露天菜地200cm 土层的硝态氮残留总量为135818kg #hm -2,2年大棚菜田为141118kg #hm -2,5年大棚则达152019kg #hm -2,而一般农田仅为24514kg #hm -2.菜地土壤的硝态氮残留严重威胁菜区地下水环境.关键词:蔬菜;土壤;硝态氮累积;硝态氮残留中图分类号:S15813 文献标识码:A 文章编号:0250-3301(2002)03-05-0079基金项目:国家重点基础研究专项经费资助项目(G1999011707);国家自然科学基金项目(49890330,39970429,30070429)作者简介:王朝辉(1968~),男,河北元氏人,博士,副教授,从事旱地土壤和作物系统氮素动态及其生态环境效应方面的研究.收稿日期:2001-04-13;修订日期:2001-07-27Nitrate Accumulation in Vegetables and Its Residual in Vegetable FieldsWang Zhaohui,Zong Zhiqiang,Li Shengx iu,Chen Baom ing (Colleg e of Resources and Env ironmental Sc-i ences ,Nort hw estern Science and T echnology U niversity of A griculture and Forestry ,Yang ling,Shaanx i 712100,China,E -mail:zhaohuiw @public.x )Abstract:Deter minations o f 11kinds,48varieties o f vegetables w ere car ried out at different seaso ns.T he results show edt hat nitr ate -N concentrations in 20veg etables reached Pollution L evel 4(N O -3-N>325mg #kg-1),w hich accounted for 4117%of the total number of the sampled veg etables and included all of the leafy ,and most of the melon,root,onionand garlic v eg etables.Among them,5leafy vegetables even ex ceeded L evel 4(N O -3-N >700mg #kg-1).A lthough leafy vegetables w er e usually apt to heavily accumulate nitrate,most of them w er e w ith nitrate -N concentrations lowert han Level 3(NO -3-N <325mg #kg -1)in leav e blades.Fur ther investig ation show ed that vegetable soils accumulated mor e nitrates in each lay er fro m 0cm to 200cm t han did cer eal crop soil.T he total amount of residual nitrate -N was135818kg #hm -2in the 200cm soil profile of usual v egetable fields,and 141118kg #hm -2and 152019kg #hm -2in the 2-yaers and the 5-years long plastic greenhouse fields r espectiv ely,how ever that in t he cereal crop fields was only 24514kg#hm -2.N itrate residual in vegetable soils for med ser ious threats to underground water in vegetable grow ing ar eas.Keywords:v eg etable;soil;nitrate accumulation;nitrate residual人类摄入的硝态氮有72%~94%来自蔬菜[1],蔬菜硝态氮累积对人类健康的危害已引起世界各国的重视[2,3]:荷兰规定莴笋的硝态氮含量不能超过1017mg #kg -1;德国规定菠菜不能超过791mg #kg -1[4].1997年欧共体对叶类蔬菜规定了更为严格的标准[5].1982年沈明珠等对我国34种蔬菜进行了检测,发现10种蔬菜硝态氮含量超过325mg #kg -1,达4级污染水平[6].近年来,为了提高蔬菜产量,满足市场不断增长的需求,菜农大量施用化学肥料,特别是氮肥,一些地方施氮量高达3300kg #hm -2[7],超过作物需求量的数倍.伴随着过量施用氮肥,环境污染也日益严重:未被作物吸收而残留在土壤中的氮素是水体和大气氮污染的重要来源.据估计,每年随径流或降水流入河、湖中的氮素约有60%来自施入农田的化肥[8].京、津、唐地区69个观测点的地下水,半数以上硝态氮含量超标,高者达6717m g #kg-1[9];黄土高原中南部的渭北旱塬第23卷第3期2002年5月环 境 科 学ENVIRONM ENTAL SCIENCEV ol.23,N o.3M ay,2002和关中灌区,近30%的地下水硝态氮超标[10].目前,我国蔬菜播种面积达1100万hm2,占全国农作物总面积的1/10[11].蔬菜生产中氮肥用量大,灌水数量和频率又高,菜地土壤的硝态氮残留一直受到人们关注.本文根据对多种蔬菜和不同类型菜地土壤的测定,讨论当前蔬菜生产中氮素污染的严重性.1材料及方法111蔬菜样品的采集和测定选取西北农林科技大学蔬菜市场、杨陵区康乐路蔬菜批发市场、西安市胡家庙蔬菜批发市场、炭市街农副产品批发市场等4个较大的蔬菜市场,分别于2000-04~2000-06(春季)、2000-11~2000-12(冬季),采集人们普遍食用的叶菜类、根菜类、瓜类、茄果类、豆类、花菜类、葱蒜类、芽菜类、薯芋类、水生类和食用菌类等11类,48种蔬菜.每次采样时,各种蔬菜在1个市场选取2~3个样品,分别装入塑料袋、标记密封,放入致冷箱.带回实验室,用自来水冲去根系表面粘附的泥土,并迅速用无氮吸水纸吸干,地上部分不冲洗.根据分析目的把蔬菜按器官、部位分开,迅速称重.然后将样品分别切碎混匀,装入塑料袋,标记密封,放于冰箱,在0e~ 4e保存.硝态氮在采样后当日或次日浸取.采用研磨浸提法[12],制成待测液.待测液中的硝态氮用连续流动分析仪测定.112菜地土壤样品的采集和测定分别自南庄村、杨陵、西北农林科技大学蔬菜试验站,选取5年大棚、2年大棚和常年露地3种菜田,并以距菜地200m的一般农田为对照,研究不同种植年限和栽培方式菜田土壤的硝态氮残留.3种不同类型的菜田在建棚或露天种植蔬菜前亦为小麦-玉米轮作的一般农田.土壤采样时间为2000-03-20~2000-04-10.此时,5年大棚菜地内生长着黄瓜、番茄和芹菜等;2年大棚内生长着菠菜、小白菜和芹菜;露地菜田经过冬季休闲、即将整地移栽甘蓝、辣椒和茄子;对照农田正值冬小麦生长季节.采样时,各种类型的菜田和农田分别选取4~5个不同的田块,根据其面积大小,每块地采3~5个样点.每个样点按20cm深度为一层取样,直至200cm.同一田块各样点同一土层的土壤分别混匀作为分析样品,每一分析样品约1000g左右鲜土.取好的土壤样品分别装入塑料袋、标记密封,放入致冷箱,带回实验室后,迅速过2mm 筛,取1/2放入冰箱,在0e~4e保存,用于测定土壤的硝态氮.土壤的硝态氮用1mol/L的KCl浸取[13],连续流动分析仪测定.2结果与分析211蔬菜可食部分的硝态氮累积硝态氮是蔬菜吸收的主要氮素形态,在氮素用量合适时,吸入的硝态氮会很快被还原转化.但在过量施用氮肥情况下,蔬菜吸收的硝态氮不能及时还原,便累积在体内.对48种蔬菜在不同季节采样测定的结果(表1)表明,累积硝态氮的数量因蔬菜种类和品种不同而有极大差异.从各类蔬菜不同品种硝态氮含量的平均值来看,叶菜类的硝态氮含量较高,平均为57614mg#kg-1;其次是根菜类、瓜类、葱蒜类和薯芋类蔬菜,平均值介于16513~27610mg# kg-1;茄果类、豆类、芽菜类、花菜类、水生类和食用菌类蔬菜的硝态氮含量较低,介于1915~ 10817mg#kg-1之间.同一类蔬菜中不同品种的硝态氮含量也存在显著差异.检测的15种叶菜中,芹菜的含量最高,达108917mg#kg-1,甘蓝含量最低,仅32613mg#kg-1;5种瓜菜中,西葫芦的含量为54311mg#kg-1,而黄瓜为5210mg#kg-1;5种葱蒜类蔬菜中,蒜苔的硝态氮含量为58815mg# kg-1,洋葱却仅为519mg#kg-1.同一种蔬菜的硝态氮含量因采样季节不同也有明显差异.春季的菠菜为112210mg#kg-1,而冬季的仅为29216mg#kg-1,相差数倍之多.芹菜、芫荽、茼蒿、西葫芦、蒜苔等多种蔬菜也有类似情况.其原因除蔬菜品种、肥水管理、光温等环境气候因素外[14],还与蔬菜从采收到销售之间的贮存期长短有关,贮存期延长,硝态氮因有充分的还原时间而含量降低,但这又有使蔬菜累积亚硝态氮的危险[15].根据蔬菜的食用卫生标准[6],调查的48种表148种蔬菜可食部分(鲜重)的硝态氮含量/mg#kg-1 Table1Nitrate-N contents in the edible parts of48vegetables 蔬菜采样时间类别名称春季冬季平均叶菜类芹菜14481073114108917小白菜927167851285614芫荽1254153431079818小茴香658177991072818菠菜1122102921670713空心菜5841458414大青菜5261952619生菜544174921051813油白菜458115241149111黄心菜4741847418茼蒿179147191144912莴笋433124201542619莴笋苗3361533615大白菜3301633016甘蓝344183071932613根菜类白萝卜597145001854911心里红2361423614白山药1861818618胡萝卜144101191513118瓜类西葫芦898191871354311佛手瓜1831418314苦瓜1001610016冬瓜91159115黄瓜241479175210葱蒜类蒜苔113113451858815蒜苗694112611347717韭菜571121061633819大蒜241824172417大葱42196152417韭黄1019819919洋葱516613519薯芋类生姜441181641330310土豆241430192716茄果类茄子246181221918418蕃茄1615139167810甜椒3911109197415尖辣椒301626142815豆类四季豆29012981819415芸豆1011610116肉豆73137313豇豆54145414豆角王351042103815花菜类菜花15213861411914绿菜花8912106189810芽菜类豆芽菜241575124918豆芽5810153615水生类莲藕281210181915蔬菜中,达到4级污染水平(硝态氮含量> 325mg#kg-1),既不宜生食、盐渍,也不宜熟食的蔬菜有20种,占被调查蔬菜总数的4117%,包括全部的叶菜类、部分根菜类和葱蒜类;其中有5种叶菜还超过4级污染水平(硝态氮含量>700mg#kg-1).硝态氮含量低于98mg#kg-1的优质蔬菜仅18种,占被调查蔬菜总数的3715%.可见,蔬菜的硝态氮累积比20世纪80年代初更加严重[6];叶菜类、根菜类和葱蒜类蔬菜的硝态氮累积更为突出.这些情况提示,硝态氮在蔬菜中的累积已对人类健康构成严重威胁.212叶菜类蔬菜不同部位的硝态氮累积和其它蔬菜相比,叶菜类蔬菜的硝态氮累积更为严重,但并非其可食部分各器官部位的硝态氮含量都一样高.10种叶菜不同器官硝态氮的测定(表2)表明,叶片的硝态氮含量均显表2叶菜不同部分的硝态氮含量(NO-3-N,鲜重)/mg#kg-1 Table2Nitrate-N contents in the di fferentparts of leafy vegetables蔬菜叶柄和茎秆1)叶片范围平均范围平均小白菜93511~1005179701441013~4651643810茼蒿86513~961159121544810~7381360212芹菜42412~1092117841927614~10371757619黄心菜60212~88315742198512~1751913015油白菜65013~755137021811818~1851815213大青菜35713~99717677155810~2011512917生菜59318~743126681537818~3941638617菠菜33011~65013501189413~1261711114大白菜25715~63812414121216~166119016甘蓝12219~847124071510313~20311130141)茼蒿和芹菜的测定值包括茎秆部分,其它蔬菜仅为叶柄.著低于叶柄和茎杆.如硝态氮累积量较高的小白菜叶柄含量为97014mg#kg-1,而叶片的含量仅为43810mg#kg-1,比叶柄低5419%;黄心菜叶柄的硝态氮含量为74219mg#kg-1,而叶片的含量只有13015mg#kg-1,比前者低8214%.虽然10种叶菜叶柄或茎秆的硝态氮含量均达到4级污染水平,但黄心菜、油白菜、大青菜、菠菜、大白菜和甘蓝的叶片硝态氮含量均不到3级污染水平(硝态氮含量<325mg #kg -1),既可盐渍,也可熟食.看来,即使在叶菜硝态氮污染较为严重的情况下,叶片仍是比较安全的食用部分.213 菜地土壤的硝态氮残留200cm 土层硝态氮总残留量计算:先根据所测定的各土层硝态氮含量和土壤容重计算每一土层(20cm)的硝态氮残留量(R i ):R i =c @(D @H @A )@10-6R i :每一土层的硝态氮(NO -3-N )残留量,单位:kg #hm -2;c :该土层土壤硝态氮含量,单位:mg #kg -1;D :该土层土壤容重,单位:kg #m -3;H :每一土层的厚度:012m;A :每公顷土地的面积:100m @100m;再由0~2m 深土壤中各土层的硝态氮残留量之和,求出200cm 土层硝态氮总残留量.不同类型菜地和农田0~200cm 土层硝态氮的测定(图1)表明,随土层深度增加,土壤硝态氮残留量降低,但下降速度因土层深度而异,在0~60cm 的土层中,硝态氮残留量迅速降低,在60~200cm 的土层中降低速度较慢,呈逐渐下降趋势,且不同类型菜地各土层的硝态氮残留量均高于农田.一般农田不同土层的硝态氮残留量介于11312~112kg #hm -2,而5年大棚菜田的硝态氮残留量介于50914~6116kg #hm -2,2年大棚菜地介于33219~5314kg #hm -2,常年露天菜地介于46716~5610kg #hm -2.从200cm 土层的硝态氮残留总量(各土层残留量之和)来看,常年露天菜地为135818kg #hm -2,2年大棚菜田为141118kg #hm -2,5年大棚为152019kg #hm -2,一般农田的残留总量仅为24514kg #hm -2.可见,菜田土壤的硝态氮残留量显著地高于一般农田,大棚菜地更为突出.如调查的两处大棚,种菜史虽然仅有2年和5年,硝态氮残留总量已分别比农田高出418和512倍;露天菜地也比农田土壤高出415倍.一般作物,如小麦、玉米的根系在土壤中的分布可达200cm 以上,而叶菜类、根菜类、葱蒜类、茄果类、瓜类和豆类等蔬菜的根系分布较浅,主要集中在表层0~40cm 的土层中[16],在菜地土壤中淋洗到40cm 以下的硝态氮就难以再被作物吸收;而且硝态氮又不易被土壤胶体吸附[17].因此会不断在雨水和灌溉水的淋洗作用下向土壤深层迁移,污染菜区地下水环境.调查的常年露地、2年和5年大棚菜田中,180~200cm 土层的硝态氮残留量分别为5610kg #hm -2,8913kg #hm -2和6713kg #hm -2以上,远高于一般农田土壤(213kg #hm -2).可见,菜区土壤的硝态氮淋洗现象非常严重.图1 不同类型菜地和农田土壤的硝态氮残留Fig.1 Nitrate -N residual in different vegetablesoils and cereal crop soil3 结论不同季节测定了48种蔬菜硝态氮的含量.结果表明,不同种类蔬菜可食部分的硝态氮累积存在明显差异.叶菜类蔬菜的硝态氮含量较高,平均为57614mg #kg -1;其次是根菜类、瓜类、葱蒜类和薯芋类蔬菜,平均值介于16513mg #kg -1~27610mg #kg -1;而茄果类、豆类、芽菜类、花菜类、水生类和食用菌类蔬菜的含量较低,介于1915m g #kg -1~10817mg #kg -1.蔬菜的硝态氮含量因品种、采样季节不同也有明显差异.叶菜类蔬菜的硝态氮累积还因器官部位而异,10种叶菜中,叶片的硝态氮含量均显著低于叶柄和茎秆.调查的48种蔬菜中,20种蔬菜的硝态氮含量达到4级污染水平,占被调查蔬菜总数的4117%,包括全部的叶菜类、部分瓜菜类、根菜类和葱蒜类蔬菜.其中硝态氮含量高于700mg #kg -1,超过4级污染水平的有5种,均为叶菜类蔬菜.而硝态氮含量低的优质蔬菜仅18种,占所调查蔬菜的3715%.叶菜的硝态氮累积虽为严重,但其中黄心菜、油白菜、大青菜、菠菜、大白菜和甘蓝的叶片硝态氮含量均低于3级污染水平,既可盐渍,也可熟食.蔬菜生产中过量施用氮肥,频繁和过量灌水,不仅使硝态氮在蔬菜体内大量累积,还在菜地土壤中大量残留,使菜田土壤的硝态氮残留量明显高于一般农田.常年露天菜地200cm土层的硝态氮残留总量可达135818kg#hm-2,2年大棚菜田为141118kg#hm-2,5年大棚为152019kg#hm-2,而一般农田仅为24514kg# hm-2.蔬菜作物的根系分布较浅,残留在菜地土壤深层的硝态氮难以被重新吸收利用;加之硝态氮又不易被土壤胶体吸附,在雨水和灌溉水的淋洗作用下会不断向土壤深层迁移,污染菜区的地下水环境.参考文献:1Walker R.Nitrate,nitrite and N-nitroso compounds:A re-view of the occurrence in food and diet and the tox i cologi cal implications.Food Add.Cont.,1990,7:717~768.2Dich J,Jrvinen R,Knekt P et al.Dietary intakes of nitrate, nitri te and NDM A in the Finish M obile Cli nic Health Exam-i nation Survey.Food Add.Contam.,1996,13:541~552. 3Choi B C K.N-nitroso compounds and human cancer:a molecular epidemiological approach.Am.J.Epidem., 1985,121:737~743.4Lillie A,Niels E N.A new cultivation method for the pro-ducti on of vegetables w ith low content of nitrate.S cientia Horticulturae,1992,49:167~171.5Santamari a P,Elia A,Parente A et al.Fertilizati on strate-gies for low ering nitrate accumulati on in leafy vegetables:Chicory and rocket salad cases.Journal of Plant Nutrition., 1998,21(9):1791~1803.6沈明珠,翟宝杰,东惠茹等.蔬菜硝酸盐累积的研究Ñ.不同蔬菜硝酸盐、亚硝酸盐含量评价.园艺学报,1982,9(4):41~48.7贾继文,李文庆等.山东省蔬菜大棚土壤养分状况与施肥状况的调查研究.见谢建昌,陈际型主编.菜园土壤肥力与蔬菜合理施肥.南京:河海大学出版社,1997.73~75. 8马立珊,钱敏仁.太湖流域水环境硝态氮和亚硝态氮污染的研究.环境科学,1987,8(2):60~65.9张维理,田哲旭,张宁等.我国北方农田氮肥造成地下水硝酸盐污染的调查.植物营养与肥料学报,1995,1(2): 80~87.10吕殿青,同延安,孙本华等.氮肥施用对环境污染影响的研究.植物营养与肥料学报,1998:4(2):8~15.11李国庆.我国人均占有蔬菜超过二百五十公斤.科技日报.1998年12月17日(第1版).12王朝辉,李生秀.蔬菜不同器官的硝态氮含量与水分、全氮、全磷含量的关系.植物营养与肥料学报,1996,2(2): 144~152.13李生秀,贺海香,李和生等.关于供氮指标的研究Ò.评价EUF析滤出的矿质氮在反映土壤供氮能力方面的效果.土壤学报,1993,30(4):447~452.14Blom-Zands tra M.Ni trate accumulation in vegetables and its relationship to quality.Ann.Appl.Biol.,1989,115:553 ~561.15M inotti P L.Potential nitrate levels in edible plant parts.Donald R,Ni elson J G,M acDonald(eds).Nitrogen in the Environment:Vol.2Soi-l Plant-Nitrogen Relationship.Aca-demic Press,New York,Son Francisco,London.1978.235~252.16庄舜尧,孙秀廷.肥料氮在蔬菜地中的去向及平衡.土壤,1997,29(1):80~83.17文启孝.土壤氮素的含量和形态.见朱兆良,文启孝主编.中国土壤氮素.南京:江苏科技出版社,1992.3~26.。
【国家自然科学基金】_no-3-n_基金支持热词逐年推荐_【万方软件创新助手】_20140801
53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85
大气沉降n 大亚湾 复合垂直流人工湿地 地裂缝 地膜覆盖 土壤蒸发 土壤矿质氮 土壤团聚体 土壤养分 土壤 土地利用类型 周质硝酸盐还原酶 叶片相对含水率 可溶性有机氮 可溶性总氮 反硝化除磷 反硝化聚磷菌 反硝化 双氰胺 单级好氧 华北平原 功能区 净化作用 元素硫 保水剂 二色补血草 上覆水 uasb反应器 uasb-anammox sbr ph n沉降 a2/o工艺
推荐指数 3 3 2 2 2 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1
2009年 序号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52
氮素运移转化 氮素利用率 氮矿化 模拟试验 植物吸氮量 植物修复 森林群落 森林土壤 根际土壤 根际ph值 根表土壤 根系活力 杉木人工林 有机负荷 有效n 更新格局 景观水体 无机氮 投加方式 微生物作用 循环速率 径流流失 异质性 异养菌 富营养化 大气氮沉降 外源n 外源c 土壤营养元素 土壤氮素 土壤有机层 土壤可矿化氮 土地利用变化 土体土壤 固相反硝化 团聚体 喷灌 含盐量 后向轨迹 可降解餐盒 反硝化除磷 反硝化潜势 原状土 华北落叶松 动态变化 凋落物 净硝化 净氮矿化速率 净氮矿化 冬小麦-夏玉米轮作 冬小麦 农业流域 免耕 修复
双波长分光光度法测定土壤硝态氮

211 主要仪器与试剂 UV - 2401 紫 外 - 可 见 分 光 光 度 计 ; 振 荡 器
收稿日期 : 2005 - 01 - 07 作者简介 : 涂常青 (1970 - ) , 女 , 广东平远人 , 高级实验师 , 在读硕士 , 主要从事环境分析化学的研究 。
— 50 —
千粒重 (g) 2610 2518 2517
实际产量 (kg/ hm2) 704715 671015 635510
差异显著性
0105
0101
a
A
b
AB
c
B
注 : LSD0105 = 282132 kg/ hm2 , LSD0101 = 401190 kg/ hm2 。
3 小结
促进水稻分蘖 , 从而提高有效穗和实粒数 , 最终产 生显 著 的 增 产 效 果 , 可 比 浅 施 、面 施 分 别 增 产
© 1994-2010 China Academic Journal Electronic Publishing House. All rights reserved.
土壤肥料 2006 (1)
21213 样品测定方法
准确称取 10 g 充分拌匀的鲜土壤 , 分别置于
y = 015283 x - 010009 …………………… (1)
3 结果与讨论
311 精密度和准确度实验 31111 沙田柚果园土壤硝态氮的测定
随机抽取 4 份沙田柚土壤 , 按 21213 所述方法 进r = 019999 (n = 7)
Abstract : A method of determining nitrate nitrogen concentration of vegetables applying nitrate electrode was introduced in this paper. The results showed that this method was convenient , swift , and precise according to the evaluation of re2 covery trial , contrast experiment , and precision test . The method could be applied to the swift determination of nitrate in vegetables. Key words : vegetable ; nitrate ; determination method ; nitrate electrode
AO-MBR工艺在生活污水处理中的应用

AO-MBR工艺在生活污水处理中的应用随着水资源的紧缺和人们环保意识的增强,污水再生利用是解决水资源短缺和水环境污染问题的重要策略之一。
厌氧/好氧(A/O)工艺是在普通的活性污泥法基础上研究开发的,该工艺具有适应能力强,耐冲击负荷高,在去除有机物的同时可以取得良好的脱氮效果。
膜生物反应器是由膜分离技术与污水处理工程中的生物反应器相结合组成的反应系统,它综合了膜分离技术与生物处理技术的优点,用超、微滤膜组件取代传统的活性污泥法的二沉池和常规过滤单元,使水力停留时间和泥龄完全分离。
其高效的固液分离能力使出水水质良好,悬浮物和浊度接近于零,并可截留大肠杆菌等生物性污染物,处理后出水可直接回用,特别适合于中水回用处理。
将生物膜法与常用的A/O污水处理脱氮工艺结合起来即形成A/O生物膜反应器,该复合工艺将生物膜工艺与活性污泥工艺有机地融合起来,综合了活性污泥法和生物膜法两者的优点,长泥龄的生物膜为生长缓慢的硝化菌提供了非常有利的生存环境,可以有效地提高硝化效果,出水水质优异,操作运行简单,污泥产率低,占地面积小等特点,使其应用范围和规模不断扩大。
1A/O-MBR组合工艺由膜分离技术和生物反应器相结合形成的生物化学反应系统――膜生物反应器,在水处理中的应用及其研究备受人们的关注。
刘国洋和李勇根据传统脱氮除磷工艺――好氧硝化缺氧反硝化原理,设计并制作了一种分置式A/O膜生物反应器,并且对其曝气方式进行合理改进,利用射流曝气强大的复氧能力和混合能力,使好氧区的泥水能更加均匀地混合以及能提供充足的氧气。
并就其对生活污水中污染物的去除效果及其机制进行了试验研究,结果表明,该改进后的膜生物反应器在连续运行60天内,系统不排泥,水力停留时间为16h时,对COD、总氮、氨氮有良好的去除效果,平均去除率分别达到94%,70.7%,98.4%,出水COD一总氮、氨氨浓度分别在50mg/L,15mg /L,1mg/L以下。
也有研究者将A/O工艺与MBR 工艺有机组合,并在A/O工艺中引入纤毛填料处理小区低碳氮比、高氨氮生活污水。
【值得收藏】氨氮,总氮,硝态氮、亚硝态氮,凯氏氮看完就可以分清楚了!

【值得收藏】氨氮,总氮,硝态氮、亚硝态氮,凯氏氮看完就可以分清楚了!前言水体中的氮,磷元素通常是导致水体富营养化的核心因素水体中氮元素的形式及转化进入水体中的氮主要有无机氮和有机氮之分。
无机氮包括氨态氮(简称氨氮)和硝态氮。
氨氮包括游离氨态氮NH3-N和铵盐态氮NH4+-N;硝态氮包括硝酸盐氮NO3--N和亚硝酸盐氮NO2--N。
有机氮主要有尿素、氨基酸、蛋白质、核酸、尿酸、脂肪胺、有机碱、氨基糖等含氮有机物。
可溶性有机氮主要以尿素和蛋白质形式存在,它可以通过氨化等作用转换为氨氮。
成分分析目前,国标针对水质中氮的分析主要分总氮、氨氮、硝酸盐氮、亚硝酸盐氮、凯氏氮5个方面。
总氮总氮是指可溶性及悬浮颗粒中的含氮量(通常测定硝酸盐氮、亚硝酸盐氮、无机铵盐、溶解态氨几大部分有机含氮化合物中氮的总和)。
可溶性总氮是指水中可溶性及含可过滤性固体(小于0.45µm 颗粒物)的含氮量。
总氮是衡量水质的重要指标之一。
总氮的测定方法,一是采用分别测定有机氮和无机氮化合物(氨氮、亚硝酸盐氮、硝酸盐氮)后加和的办法。
二是以过硫酸钾氧化,使有机氮和无机氮转变为硝酸盐后,通过离子选择电极法对溶液中的硝酸根离子进行测量,也可以用紫外法或还原为亚硝酸盐后,用偶氮比色法,以及离子色谱法进行测定。
氨氮氨氮是指游离氨(或称非离子氨,NH3)或离子氨(NH4+)形态存在的氨。
pH较高,游离氨的比例较高;反之,铵盐的比例高。
氨氮是水体中的营养素,可导致水富营养化现象产生,是水体中的主要耗氧污染物,对鱼类及某些水生生物有毒害。
氨氮对水生物起危害作用的主要是游离氨,其毒性比铵盐大几十倍,并随碱性的增强而增大。
氨氮毒性与池水的pH值及水温有密切关系,一般情况,pH值及水温愈高,毒性愈强。
常用来测定氨的两个近似灵敏度的比色方法是经典的纳氏试剂法和苯酚-次氯酸盐法;滴定法和电极法也常用来测定氨;当氨氮含量高时,也可采用蒸馏-滴定法。
(国标有纳氏试剂法、水杨酸分光光度法、蒸馏-滴定法)硝酸盐氮水中硝酸盐是在有氧条件下,各种形态含氮化合物中最稳定的氮化合物,通常用以表示含氮有机物无机化作用最终阶段的分解产物。
消态氮测试

硝态氮测试测试方法检测标准肥料中硝态氮检测09建立了环境水体中NO-2、NO-3及总氮含量的液相色谱测定方法。
采用HypersilODS(5μm,250mm×4.6mm i1d1)色谱柱;流动相:17.5mmol/L KH2PO4-2mmol/L H3PO4缓冲液(pH3.5)-乙腈(体积比92.5∶7.5);流速:0.8mL/min;柱温:30℃;紫外检测器:波长204nm。
结果表明:水体中NO-2和NO-3的线性范围(以N计):1~80ng,r= 0.9999;方法检出限:NO-2014ng、NO-30109ng;回收率为NO-299.2%~102.4%、NO-3 98.7%~99.3%,RSD为0.79%和0.25%。
NO-2、NO-3及总氮已列入环境水体的必检项目,建立环境水体中NO-2、NO-3及总氮的新型、快速、准确检测方法显得极其重要。
目前,同时测定亚硝酸盐和硝酸盐的方法主要采用化学发光法[1]、硝酸银电极法[2]、流动注射光度法[3-4]、二元线性解析-紫外分光光度法[5]及离子色谱法[6]等。
这些方法各有优缺点,其中离子色谱法已经被我国列入生活饮用水中NO-2和NO-3检验规范方法之一。
离子色谱法的采用,改善了NO-2和NO-3检测方法的灵敏度,但不普及。
迄今为止,使用高效液相色谱法测定NO-2和NO-3的文献报道很少。
文献[7]和姜华、何荣桓等[8]利用高效液相反相离子对色谱法成功分离并测定了水体中的NO-2和NO-3含量。
本文采用磷酸盐缓冲体系为流动相,建立了操作简便、准确可靠、灵敏度高且适用于环境水中NO-2、NO-3和总氮检测的高效液相色谱法。
GB/T3597-2002肥料中硝态氮含量的测定氮试剂重量法本标准规定了肥料中硝态氮含量的测定方法氮试剂重量法。
本标准适用于各种肥料。
本标准代替GB/T3597-1983。
水和土壤提取液中硝酸盐和亚硝酸盐的测定

去离子水to 1000 mL
将10 mL硫酸铜储备液, 10 mL硫酸锌储备液和2 g硫酸肼加入约600 mL去离子水中,稀释至1000 mL混合均匀。
用于土壤提取液的试剂(0.01 M CaCl2-溶液)
(流程图3)
氢氧化钠(NaOH)
只用于土壤分析
氢氧化钠40 g
去离子水to 1000 mL
氯化钙, CaCl2.2H2Oirritant
硫酸铜, CuSO4.5H2Oharmful
硫酸联胺, N2H4.H2SO4toxic
N-(1-萘基)乙二胺二盐酸, C12H14N2.2HCl.CH3OHirritant
磷酸, H3PO4corrosive
硝酸钾, KNO3oxidising
氢氧化钠, NaOHcorrosive
Brij-35, 30%溶液1 mL
将40g氢氧化钠溶入约600 mL去离子水中,稀释至1000 mL并加入1 mL Brij-35 (30%溶液)。
磷酸
仅用于土壤分析
磷酸3 mL
二磷酸四钠x10H2O(焦磷酸钠)4 g
去离子水to 1000 mL
Brij-35 (30%溶液)1 mL
小心地将3 mL磷酸加入约600 mL去离子水混合均匀。溶入4 g十水二磷酸四钠并混合均匀。稀释至1000 mL并加入1mLBrij-35 (30%溶液).
亚硝酸盐储备液, 1000mg/L N
亚硝酸钠4.930g
去离子水to 1000 mL
根据需要配制工作标准液。如果分析土壤或其它不是用纯水做提取液的样品,工作标准要用样品提取液稀释。
操作注意事项
1.特征参数(用AAII检测器)
Nitrate/NitriteNitrite
最新《环境工程学》知识要点整理(蒋展鹏、杨宏伟主编-第三版)-普通专升本考试资料

《环境工程学》知识要点整理蒋展鹏主编第3版普通专升本考试绪论与第一章水质标准和水体净化1、水质是指水和其所含的杂质共同表现出来的物理学、化学和生物学的综合性质。
水质指标则表示水中杂质的种类、成分和数量,是判断水质是否符合要求的具体衡量标准。
主要分为化学性指标、物理性指标、生物性指标。
2、COD:化学需氧量的简称,指在一定严格的条件下,水中各种有机物质与外加的强氧化剂(如K2Cr2O7、KMmO4)作用时消耗的氧化剂量,结果用氧的mg/L数来表示。
BOD:生物化学需氧量的简称,指在有氧的条件下,水中可分解的有机物由于好氧微生物的作用被氧化分解,这个过程所需要的氧量叫做生物化学需氧量,结果用氧的mg/L数来表示。
3、常用水质标准:《生活饮用水卫生标准》GB 5749—2006、《饮用水净水标准》CJ94-1999 、《地表水环境质量标准》GB 3838-2002 、《废水综合排放标准》GB8978-1996、《城镇污水处理厂污染物排放标准》GB18918-20024、水体自净:污染物质随污水排入水体后,经过物理的、化学的与生物学的作用,污染物质被分散,分离或分解,最后受污染的水体部分的或完全的恢复原状的现象。
净化机理:1)物理过程:稀释、扩散、挥发、沉淀、上浮等。
2)化学和物理化学过程:中和、絮凝、吸附、络合、氧化、还原等。
3)生物学和生物化学过程:进入水体中的污染物质,被水生生物吸附、吸收、吞食消化等过程,特别是有机物质由于水中微生物的代谢活动而被氧化分解并转化为无机物的过程。
第二章(1-2)水的物理化学处理方法1、格栅:格栅由一组(或多组)相平行的金属栅条与框架组成,倾斜安装在进水的渠道,或进水泵站集水井的进口处,以拦截污水中粗大的悬浮物及杂质。
分类:按格栅形状分:平面格栅、曲面格栅;按栅条间隙分:粗格栅 e=50-100mm、中格栅 e=10-40mm、细格栅 e=3-10mm;按清除方式分:人工清除格栅、机械清除格栅、水力清除格栅。
[整理版]no3-n测定方法
![[整理版]no3-n测定方法](https://img.taocdn.com/s3/m/2b4a19210a4c2e3f5727a5e9856a561252d3213c.png)
麝香草酚法测定水中硝酸盐氮1.基本原理在浓硫酸存在下,麝香草酚与硝酸盐生成硝基酚化合物,在碱性溶液中发生分子重排,产生黄色化合物,该颜色在420nm处有最大吸收。
氨基磺酸铵消除亚硝态氮的干扰,硫酸银消除氯离子的干扰。
2. 试剂配制试剂用水为纯水。
⑴硝酸盐氮标准贮备溶液称取7.218g在105~110℃烘过1h的硝酸钾(KNO3),溶于纯水中,并稀释至1000ml。
加2ml氯仿作保护剂,此液1.00ml含1.00mg硝酸盐氮。
⑵硝酸盐氮标准使用液吸取10.00ml硝酸盐氮标准贮备液于1000ml容量瓶中,加入纯水定容,此标准溶液1.00ml含硝酸盐氮10.0μg。
⑶ 1+4乙酸溶液⑷氨基磺酸铵溶液称取2g氨基磺酸铵,用1+4乙酸溶液溶解并稀释为100ml。
⑸ 0.5%麝香草酚乙醇溶液称取0.5g麝香草酚,溶于无水乙醇中并稀释至100ml。
⑹硫酸银硫酸溶液称取1.0g硫酸银溶于100ml浓硫酸中,摇匀。
⑺浓氨水。
3. 测定步骤⑴绘制校准曲线a.在一组7支50ml比色管中,分别加入0、0.05、0.1、0.3、0.5、0.7和1.0ml硝酸盐氮标准溶液,加纯水稀释至1.0ml。
加0.1ml氨基磺酸铵溶液,放置5min。
b.从管中央加入0.2ml麝香草酚溶液(勿使沿管壁流下),加2.0ml硫酸银硫酸溶液,混匀,放置5min。
c.加8ml纯水,混合后,加浓氨水至出现的黄色不再加深且氯化银沉淀溶解为止(约9ml左右)。
d.在波长420nm处,用光程10mm比色皿(G),以无氨水为参比,测量吸光度。
由测得的吸光度,减去参比水样的吸光度后,得到校正吸光度,绘制以硝酸盐氮含量(μg)对校正吸光度的校准曲线。
⑵测定水样分别取水样(原水1ml,出水0.1ml)加入干燥的比色管中,然后按校准曲线绘制的相同步骤操作,测量吸光度。
⑶计算由水样测得的吸光度减去空白试验的吸光度后,从校准曲线上查得硝酸盐氮含量。
(μg)。
m硝酸盐氮(N,mg/l)=Vm—由校准曲线查得的硝酸盐氮含量(μg);V—水样体积(ml)。
水中硝态氮的测定国标

水中硝态氮的测定国标水是人类生活中不可或缺的资源之一,然而,水质污染已经成为全球范围内的严重问题。
水中硝态氮作为最主要的水体污染指标之一,对人类健康和环境产生极大的影响。
为了保护水资源和人类健康,各国制定了相应的水质标准,并规定了水中硝态氮的测定方法。
本文将介绍中国国家标准中对水中硝态氮测定的要求和方法。
一、硝态氮的概述硝态氮是指水中存在的亚硝酸盐(NO2-)和硝酸盐(NO3-)。
它们主要来源于化肥、农药和生活废水等,过量的硝态氮会导致水体富营养化,引发水华和藻类大量繁殖,对水生态系统造成破坏。
此外,硝酸盐在人体内可转化为亚硝胺物质,与蛋白质反应形成致癌物质,对人体健康构成潜在威胁。
二、中国国家标准的要求中国国家标准GB 11893-89《水中硝酸盐测定纳量浊度试剂法》规定了水中硝态氮的测定方法,以下是该标准中的要求:1. 试剂的要求测定硝态氮所需的试剂主要有铁铝试剂、纳量浊度试剂和硫酸,其中,铁铝试剂和纳量浊度试剂的制备需符合标准规定。
2. 仪器设备的要求测定硝态氮所需的仪器设备主要有红外分光光度计和样品预处理设备(如过滤器、分液漏斗等),这些设备应符合标准要求。
3. 测定方法的要求测定硝态氮的方法采用纳量浊度试剂法,包括样品预处理、试剂添加和比色测定等步骤。
具体步骤及操作要求详见标准。
三、硝态氮的测定方法按照GB 11893-89标准,下面介绍水中硝态氮的测定方法:1. 样品的采集和处理从需要测定的水源中,采集一定数量的样品,尽量避免样品接触空气,以减少硝态氮的损失。
如果样品中有悬浮物或杂质,需要进行预处理,如过滤或沉淀。
2. 试剂的制备和添加按照标准要求,制备铁铝试剂和纳量浊度试剂。
将预处理后的样品与试剂按比例混合,并在特定的条件下反应。
3. 比色测定将反应后的样品转移到红外分光光度计中,设定特定的波长进行测定。
根据测定结果,计算出水中硝态氮的含量。
四、相关注意事项在进行硝态氮的测定过程中,需要注意以下事项:1. 严格按照标准要求操作,保证测定结果的准确性和可比性。
水中硝态氮的测定国标

水中硝态氮的测定国标水中硝态氮的测定是一项重要的分析化学方法,被广泛应用于环境监测、水质评价等领域。
硝态氮是水体中的一种主要污染物,其浓度的高低直接影响着水质的好坏。
硝态氮的测定国家标准主要包括两部分:GB6920.1-2014《卫生标准》,以及GB11893-89《水质污染物分析方法》。
首先,GB6920.1-2014《卫生标准》是针对饮用水的硝态氮浓度进行限制的标准。
该标准规定了饮用水中硝态氮的限值要求,对保护人体健康起到了重要作用。
根据该标准,饮用水中硝态氮的限制浓度为10mg/L。
其次,GB11893-89《水质污染物分析方法》则是对硝态氮的分析方法进行了规定。
该标准详细描述了硝态氮的测定原理和分析方法,并指导实验员进行水样的采集、处理和分析过程。
根据该标准,硝态氮的测定方法主要包括硫酸还原法、萘醌比色法、分光光度法、高效液相色谱法等。
其中,硫酸还原法是一种常用的硝态氮测定方法,适用于测定水样中的硝态氮含量。
其测定原理是将硝酸盐还原为亚硝酸盐,再通过碱性柠檬酸钠溶液将亚硝酸盐转化为氮气。
最后,通过对氮气的体积进行测定,便可计算出水样中硝态氮的含量。
萘醌比色法是另一种常用的硝态氮测定方法,该方法的原理是将硝酸盐还原为亚硝酸盐,再与萘醌反应生成呈粉红色的偶氮化合物。
最后,通过比色测定偶氮化合物的吸光度,就可以计算出水样中硝态氮的含量。
分光光度法则是利用硝酸盐与草酸反应生成淡黄色染料,进而通过该染料吸收特定波长的光线来测定水样中硝态氮的含量。
高效液相色谱法则是一种较为精确和灵敏的硝态氮分析方法,其测定原理是利用液相色谱技术分离和检测水样中的硝态氮。
该方法被广泛应用于环境监测和水质评价领域。
总之,水中硝态氮的测定国家标准包括GB6920.1-2014《卫生标准》和GB11893-89《水质污染物分析方法》。
这些标准规定了硝态氮的限值要求,并提供了多种分析方法供实验员选择。
这些标准的制定和实施,对于保障水质安全和环境保护具有重要意义。
水质中硝态氮和亚硝态氮测定

水质中的硝态氮测定(紫外分光光度法)原理:利用硝酸盐在220nm波长具有紫外吸收和在275nm波长不具吸收的性质进行测定,于275nm波长测出有机物的吸收值在测定结果中校正.试剂:1. 无硝酸盐纯水:采用重蒸馏或者蒸馏---去离子法制备,用于配制试剂及稀释样品.2. 盐酸溶液(1+11).3. 硝酸盐氮标准储备溶液[p(NO3---N)=100ug/mL]:称取经105`C烤箱干燥2h的硝酸钾(KNO3) 0.7218g,溶于纯水中并定容至1000mL,每升中加入2mL三氯甲烷,至少可稳定6个月.4. 硝酸盐氮标准使用溶液[p(NO3---N)=10ug/mL].仪器:1. 紫外分光光度计以及石英比色皿.2. 具有比色管:50mL分析步骤:1. 水预样处理:吸收50mL水样于50mL比色管中加1mL盐酸溶液酸化.2. 标准系列制备:分别吸收硝酸盐氮标准使用溶液0mL/L~7mg/L硝酸盐氮标准系列,用纯水稀释到50mL,各加1mL盐酸溶液.3. 用纯水调节仪器吸光度为0,分别在220nm和275nm波长测量吸光度.计算:在标准样品的220nm波长吸光度中减去2倍于275nm波长的吸光度,绘制标准曲线和在曲线上直接读出样品中的硝酸盐氮的质量浓度.注:若275nm波长吸光度的2倍大于220nm波长吸光度的10%时,本标准将不能适用.水质中亚硝态氮的测定(重氮偶合分光光度法)原理:在pH1.7以下,水中亚硝酸盐与对氨基苯磺酰胺氮化,再与盐酸N-(1-萘)-乙二胺产生偶合反应,生成紫红色的偶氮染料,比色定量.试剂:1. 氢氧化铝悬浮液2. 对氨基苯磺酰胺溶液3. 盐酸N-(1-萘)-乙二胺溶液4. 亚硝酸盐氮标准储备液[p(NO2—N)=50ug/mL]:称取0.2463g在玻璃干燥器内放置24h的亚硝酸钠(NaNO2),溶于纯水中,并定容至1000mL.每升中加2mL三氯甲烷保存.5. 亚硝酸盐氮标准使用溶液[p(NO2—N)=0.10ug/mL]仪器:1.具塞比色管:50mL.2.分光光度计.分析步骤:1. 若水样浑浊或色度较深,可先取100mL,加入2mL氢氧化铝悬浮液,搅拌后静置数分钟,过滤.2. 先将水样或处理后的水样用酸或碱调近中性.取50.0mL置于比色管中.3. 另取50mL比色管8支,分别加入亚硝酸盐氮标准液0,0.50,1.00,2.50,5.00,7.50,10.00和12.50mL,用纯水稀释至50mL.4. 向水样以及标准色列管分别加入1mL对氨基苯磺酰胺溶液,摇匀后放置2min~8min.加入1.0mL盐酸N-(1-萘)-乙二胺溶液,立刻混匀.5. 于540nm波长,用1cm比色皿,以纯水作参比,在10min至2h内,测定吸光度.如亚硝酸盐氮浓度低于4ug/L时,改用3cm比色皿.6. 绘制曲线,查出亚硝态氮含量.计算:水样中亚硝态氮质量浓度计算见式:P(NO2-N)= m / VP(NO2-N):mg/L,亚硝酸氮质量浓度M:从标准曲线上查的样品管中亚硝酸盐氮的质量,单位为微克(ug) V:水样体积,mL。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
使用水相标准和AA3比色计的特性数据:
硝酸盐/亚硝酸盐亚硝酸盐
测试范围0-1 mg /L 0-5mg/L 0-1mg/L 0-5mg/L
进样速率50样/h 50样/h 50样/h 50样/h
进样:清洗比5 : 1 5 : 1 5 : 1 5 : 1
6.干扰
普通干扰
粒径> 1 mm的颗粒物必须用滤膜过滤。
如果可以排除样品中硝酸盐和亚硝酸盐浓度损失,样品可以用活性炭过滤。
如果样品浓度> 30 g/L需稀释。
7.AA3比色计参数
对于不同长度的流通池有些参数会有变化
Nitrate/NitriteNitrite
测量范围:0-2 mg/L0-5 mg/L0-1 mg/L0-5 mg/L
Method No. G-109-94 Rev.3
水和土壤提取液中硝酸盐和亚硝酸盐的测定
测量范围: 0-0.9/0-10/0-30mg / L
原理描述:
硝酸盐在碱性环境下在铜的催化作用下,被硫酸肼还原成亚硝酸盐,并和对氨基苯磺酰胺及NEDD反应生成粉红色化合物在550nm波长下检测。加入磷酸是为了降低PH值,防止产生氢氧化钙和氢氧化镁。加入锌是为了抑制氧化物和铜的反应。
硫酸肼(参见注意事项3)
只用于土壤
硫酸铜储备液14 mL
硫酸锌储备液10 mL
硫酸肼6 g
去离子水to 1000 mL
将14mL硫酸铜储备液, 10 mL硫酸锌储备液和6 g硫酸肼加入约600 mL去离子水中,稀释至1000 mL混合均匀。
0.01 MCaCl2(土壤提取液:见注意事项5)
氯化钙1.47 g
灵敏度在0.80 0.48 0.50 0.58
试剂吸收0.06 0.01 0.0 1 0.01
变异系数(50%重复30次)0.2% 0.6% 0.7% 0.2%
校正系数(线性,5点)0.999 1.000 0.999 0.999
集中标准偏差(50次随机五级)0.012 mg/L 0.015mg/L 0.003 mg/L 0.01 mg/L
Addition of the cartridge MT7 (= MT8 with dialyzer).
Nitrite results added.
Revision B, April 1995
Corrected flowchart and consumables list.
Revision C, October 1996
易耗品:
以下估计以每天8小时,每年250天使用计算。
名称图上标记配件号估计一年消耗
ORN/GRN, 0.10 mL/min116-0549-041 pkg./12
ORN/WHT, 0.23 mL/min116-0549-064 pkg./12
BLK/BLK, 0.32 mL/min116-0549-073 pkg./12
Brij-35, 30%溶液1 mL
将40 g氢氧化钠溶入约600 mL去离子水中,稀释至1000 mL并加入1 mL Brij-35 (30%溶液)。
磷酸
仅用于土壤分析
磷酸3 mL
二磷酸四钠x10H2O4 g
去离子水to 1000 mL
Brij-35 (30%溶液)1 mL
小心地将3 mL磷酸加入约600 mL去离子水混合均匀。溶入4 g十水二磷酸四钠并混合均匀。稀释至1000 mL并加入1mLBrij-35 (30%溶液).
(3)建设项目对环境可能造成影响的分析、预测和评估。Glass tubingac170-0444-012 pcs.
Glass tubing Cam172-9038-011 pc.
Glass tubingv170-G014-011 pc.
《建设项目安全设施“三同时”监督管理暂行办法》(国家安全生产监督管理总局令第36号)第四条规定建设项目安全设施必须与主体工程“同时设计、同时施工、同时投入生产和使用”。安全设施投资应当纳入建设项目概算。并规定在进行建设项目可行性研究时,应当分别对其安全生产条件进行论证并进行安全预评价。Dialyzer Assy, 24" lower157-B370-011 pc.
亚硝酸盐储备液, 1000mg/L N
亚硝酸钠4.930g
去离子水to 1000 mL
根据需要配制工作标准液。如果分析土壤或其它不是用纯水做提取液的样品,工作标准要用样品提取液稀释。
操作注意事项
1.特征参数(用AAII检测器)
Nitrate/NitriteNitrite
2 mg/L5 mg/L1 mg/L5 mg/L
Added recipe for0.01 MCaCl2solution (soil extracts)
Revision D, March 1998
Added Na4P2O7to phosphoric acid reagent to avoid Ca(OH)2-precipitation; added flowchart for soil extracts.
亚硝酸钠, NaNO2toxic
磺胺, C6H8N2O2S--
十水二磷酸钠, Na4P2O7.10H2O--
硫酸锌, ZnSO4.7H2O--
稀释水和系统清洗液
Brij-35, 30%溶液2 mL
去离子水1000 mL
将2ml Brij-35 30%溶液加入1000mL去离子水中。
进样器清洗液
用没有活化剂的纯水。如果分析土壤提取液或其它不是用纯水提取的样品,进样器清洗液必须和样品提取液一致。
备件建议持有量
AAII Flowcell, 1.5 x15 mm199-B018-011 pc.
AA3 Flowcell, 1.0 x10 mm169+B040-101 pc.
AAIIFilter Assy,ilter Assy, 550 nm165+B044-551 pc.
Injection fitting,3 pt.a116-0489-011 pc.
Injection fitting,2 pt.b116-0492-011 pc.
Glass coil, 5 turns right5TR170-0103-012 pcs.
Glass coil, 5 turns left5TL170-0426-012 pcs.
RED/RED, 0.80 mL/min116-0549-102 pkg./12
YEL/BLU, 1.40 mL/min116-0549-191 pkg./12
BLU/BLU, 1.60 mL/min116-0549-131 pkg./12
Dialyzer Membrane 24"170-0472-021 pkg./12
硫酸肼2 g
去离子水to 1000 mL
将10 mL硫酸铜储备液, 10 mL硫酸锌储备液和2 g硫酸肼加入约600 mL去离子水中,稀释至1000 mL混合均匀。
用于土壤提取液的试剂(0.01 M CaCl2-溶液)
(流程图3)
氢氧化钠(NaOH)
只用于土壤分析
氢氧化钠40 g
去离子水to 1000 mL
氯化钙, CaCl2.2H2Oirritant
硫酸铜, CuSO4.5H2Oharmful
硫酸联胺, N2H4.H2SO4toxic
N-(1-萘基)乙二胺二盐酸, C12H14N2.2HCl.CH3OHirritant
磷酸, H3PO4corrosive
硝酸钾, KNO3oxidising
氢氧化钠, NaOHcorrosive
硫酸铜储备液
硫酸铜1 g
去离子水to 1000 mL
将1g硫酸铜溶入约600mL去离子水中,稀释至1000mL并混合均匀。
硫酸锌储备液
硫酸锌10 g
去离子水to 1000 mL
将10 g硫酸锌溶入约600 mL去离子水中,稀释至1000 mL并混合均匀。
显色剂
磺胺10 g
N-1-萘基乙二胺二盐酸(NEDD)0.5 g
(1)报送审批综合性规划草案和专项规划中的指导性规划草案时,将环境影响篇章或者说明一并报送。AA3 Coil, 7.7 mL169+B440-011 pc.
2)规划实施可能对环境和人群健康产生的长远影响。AA3 Controller, 115V/230V169+B430-01/021 pc.
(1)规划实施后实际产生的环境影响与环境影响评价文件预测可能产生的环境影响之间的比较分析和评估;Thermometer 32-42°C157-0283-011 pc.
Revision 1, February 1999
Added AA3 data; changed flow diagram
Revision 2, January 2000
Changed interference filter to 550 nm.
Revision 3, January 2000
Extended high range, added operating note 8, added orn/grn pump tube to list of consumables.
磷酸3 mL
去离子水to 1000 mL
Brij-35, 30%溶液1 mL
将10 g氢氧化钠溶入约600 mL去离子水中,小心地加入3 mL磷酸并混合均匀。稀释至1000 mL并加入1 mL Brij-35 (30%溶液)。
硫酸联胺(参见注意事项3)
只用于水和废水分析
硫酸铜储备液10 mL
硫酸锌储备液10 mL
Dialyzer Assy, 24" upper157-B371-011 pc.
