罗氏电化学发光免疫分析报告仪定标物保存方法
罗氏电化学发光免疫分析仪测试项目定标物保存方法
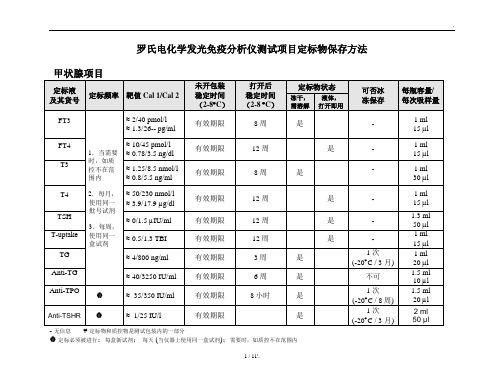
罗氏电化学发光免疫分析仪测试项目定标物保存方法无信息定标物和质控物是测试包装内的一部分定标必须被进行:每盒新试剂;每天 (当仪器上使用同一盒试剂);需要时,如质控不在范围内心肌标志物性激素项目肿瘤标志物贫血诊断指标、骨标志物传染病项目其它唐氏筛查先兆子痫罗氏电化学发光免疫分析仪定标物保存方法(简版)定标物不需要分装冰冻保存的项目:使用时从2-8︒C取出,摇均后吸200μl(此数据为国内实验室试验所得,不代表罗氏官方)到日立杯,马上将剩余定标品放回2-8︒CFT3、FT4、T3、T4、TSH、T-uptake、Anti-TG、HCG+β、HCG STAT、ProgesteroneCEA、CA 125、CA 153、CA 724、Cyfra21-1、NSE、Free PSA、HE4Myoglobin、Myoglobin - STAT 、Digoxin、Digitoxin、Ferritin、IgE、β-CrossLapsAnti-HAV、Anti-HAV IgM、HBsAg、HBsAg II quant、 Anti-HBs、HBeAg、Anti-HBe、Anti-HBc、 Anti-HBc IgM、 HIV combi、HIV Ag 、HIV combi PTToxo IgG、 Toxo IgM、Rubella IgG、Rubella IgM、CMV IgG、CMV IgM定标物需要分装冰冻保存的项目:定标物加水复溶,用子弹头进行分装(分装量为200μl(此数据为国内实验室试验所得,不代表罗氏官方)),然后放在-20︒C保存,使用时取出并平衡到室温TG、Anti-TPO、 Anti-TSHR、CK-MB、CK-MB STAT、ProBNP、Troponin T HS、Troponin T HS STAT free βHCG、PAPP-A、 Insulin、C-peptide、IL-6 、PCT、Anti-CCP.Cortisol、ACTH、Estradiol II、FSH、LH、Prolactin、Testosterone、DHEA-S、SHBG、PIGF、 sFlt-1、hGHAFP、CA 199、TPSA、S100Vitamin B12、Folate III 、N-MID、Total P1NP、PTH、PTH STAT、PTH(1-84)Vitamin D3、Vitamin D totalHSV-1 IgG、 HSV-2 IgG11 / 11'.。
罗氏 cobas e 801 电化学发光免疫分析仪使用说明书 - 检测抗 HBs 抗体的试剂盒

Elecsys Anti-HBs IIREFSYSTEM********************** 300cobas e 801EnglishSystem information Short name ACN (application code number) AHBS 2 10138 Immunoassay for the in vitro quantitative determination of human antibodies to the hepatitis B surface antigen (HBsAg) in human serum and plasma.Anti-HBs assays are used within the scope of hepatitis B vaccination to check the necessity and success of vaccination. In addition, anti-HBs assays are used to monitor the course of disease following acute hepatitis B infection. This test is not intended for diagnosis.The e lectro c hemi l uminescence i mmuno a ssay “ECLIA” is intended for use on the cobas e 801 immunoassay analyzer.Note: Please note that the catalogue number appearing on the package insert retains only the first 8 digits of the licensed 11-digit Catalogue Number: 07026854190 for the Elecsys Anti-HBs II assay. The last 3 digits -190 have been replaced by -119 for logistic purposes. SummaryAnti-HBs is a specific (generally IgG) antibody that is directed against the hepatitis B surface antigen (HBsAg).1,2 Anti ‑HBs can be detected several weeks after the disappearance of hepatitis B surface antigen.3,4 Anti ‑HBs can be formed following a hepatitis B infection or after hepatitis Bvaccination.3,4 Antibodies are formed against the HBsAg determinant a, which is common to all subtypes, and against subtype-specific determinants.1,5,6Anti ‑HBs assays are used within the scope of hepatitis B vaccination to check the necessity and success of vaccination.2,4,7 In addition, anti ‑HBs assays are used to monitor the course of disease following acute hepatitis B infection.3The Elecsys Anti ‑HBs II assay uses a mixture of purified antigens fromhuman serum (HBsAg subtype ad), and recombinant HBsAg subtype ay from CHO (Chinese Hamster Ovary) cells. Test principleSandwich principle. Total duration of assay: 18 minutes.▪ 1st incubation: Anti ‑HBs in the sample (24 μL), biotinylated HBsAg(ad/ay), and HBsAg (ad/ay) labeled with a ruthenium complex a) react to form a sandwich complex.▪ 2nd incubation: After addition of streptavidin-coated microparticles, thecomplex becomes bound to the solid phase via interaction of biotin and streptavidin.▪ The reaction mixture is aspirated into the measuring cell where themicroparticles are magnetically captured onto the surface of the electrode. Unbound substances are then removed with ProCell II M. Application of a voltage to the electrode then induces chemiluminescent emission which is measured by a photomultiplier.▪ Results are determined via a calibration curve which is instrument-specifically generated by 2‑point calibration and a master curve provided via the cobas link.a) Tris(2,2'-bipyridyl)ruthenium(II)-complex (Ru(bpy)32+)Reagents – working solutionsThe cobas e pack (M, R1, R2) is labeled as AHBS 2. M Streptavidin-coated microparticles, 1 bottle, 13.2 mL:Streptavidin-coated microparticles 0.72 mg/mL; preservative. R1 HBsAg~biotin, 1 bottle, 16.7 mL:Biotinylated HBsAg (ad/ay) human/recombinant, > 0.5 mg/L; MES b) buffer 85 mmol/L, pH 6.5; preservative. R2 HBsAg~Ru(bpy)32+, 1 bottle, 15.8 mL:HBsAg (ad/ay) human/recombinant, labeled with ruthenium complex > 0.3 mg/L; MES buffer 85 mmol/L, pH 6.5; preservative.b) MES = 2-morpholino-ethane sulfonic acidAHBS 2 Cal1 Calibrator 1, 1 bottle of 1.3 mL:Anti ‑HBs (human) in human serum; preservative.AHBS 2 Cal2 Calibrator 2, 1 bottle of 1.3 mL:Anti ‑HBs (human) in human serum; preservative.Precautions and warnings For in vitro diagnostic use.Exercise the normal precautions required for handling all laboratory reagents. Disposal of all waste material should be in accordance with local guidelines. Safety data sheet available for professional user on request.This kit contains components classified as follows in accordance with the Regulation (EC) No. 1272/2008:n ‑Octyl ‑N,N ‑dimethyl ‑3‑ammonio ‑1‑propanesulfonateEUH 208 May produce an allergic reaction.Product safety labeling primarily follows EU GHS guidance. All human material should be considered potentially infectious.The calibrators (AHBS 2 Cal1 and AHBS 2 Cal2) have been preparedexclusively from the blood of donors tested individually and shown to be free from HBsAg and antibodies to HCV and HIV. The testing methods applied were FDA ‑approved or cleared in compliance with the European Directive 98/79/EC, Annex II, List A.The HBsAg starting material used was inactivated prior to labeling with biotin or ruthenium by heating to 60 °C for 15 hours. In addition, any virus particles remaining were removed by ultracentrifugation.However, as no inactivation or testing method can rule out the potential risk of infection with absolute certainty, the material should be handled with the same level of care as a patient specimen. In the event of exposure, the directives of the responsible health authorities should be followed.8,9 Avoid foam formation in all reagents and sample types (specimens, calibrators and controls). Reagent handlingThe reagents (M, R1, R2) in the kit are ready-for-use and are supplied in cobas e packs. CalibratorsThe calibrators are supplied ready ‑for ‑use in bottles compatible with the system.Unless the entire volume is necessary for calibration on the analyzer, transfer aliquots of the ready ‑for ‑use calibrators into empty snap ‑cap bottles (CalSet Vials). Attach the supplied labels to these additional bottles. Store the aliquots at 2‑8 °C for later use.Perform only one calibration procedure per aliquot.All information required for correct operation is available via the cobas link. Storage and stability Store at 2‑8 °C. Do not freeze.Store the cobas e pack upright in order to ensure complete availability of the microparticles during automatic mixing prior to use. Stability of the cobas e pack: unopened at 2‑8 °Cup to the stated expiration date on the cobas e 801 analyzer 16 weeksStability of the calibrators: unopened at 2‑8 °C up to the stated expiration date after opening at 2‑8 °C 16 weeks on the cobas e 801 analyzer at 20‑25 °Cuse only onceadhering to the snap ‑cap.Specimen collection and preparationOnly the specimens listed below were tested and found acceptable.Serum collected using standard sampling tubes or tubes containing separating gel.K2‑EDTA and K3‑EDTA plasma.Criterion: Slope 1.00 ± 0.15 + intercept 0 ± 2 IU/L + bias at 10 IU/L: ≤ 30 %. Stable for 3 days at 20‑25 °C, 6 days at 2‑8 °C, 3 months at ‑20 °C(± 5 °C). The samples may be frozen 5 times.For plasma treated with lithium heparin, lithium heparin with gel or sodium heparin, the values found were on average up to 20 % lower than those obtained in serum. For plasma treated with sodium citrate, the values found were on average up to 30 % lower than those obtained with serum.The sample types listed were tested with a selection of sample collection tubes or systems that were commercially available at the time of testing, i.e. not all available tubes of all manufacturers were tested. Sample collection systems from various manufacturers may contain differing materials which could affect the test results in some cases. When processing samples in primary tubes (sample collection systems), follow the instructions of the tube manufacturer.Centrifuge samples containing precipitates and thawed samples before performing the assay.Do not use heat‑inactivated samples.Do not use samples and controls stabilized with azide.Ensure the samples and calibrators are at 20‑25 °C prior to measurement. Due to possible evaporation effects, samples and calibrators on the analyzers should be analyzed/measured within 2 hours.The performance of the Elecsys Anti‑HBs II assay has not been established with cadaveric samples or body fluids other than serum and plasma. Materials providedSee “Reagents –working solutions” section for reagents.▪ 2 x 6 bottle labelsMaterials required (but not provided)▪REF 11876317122, PreciControl Anti‑HBs, 16 x 1.3 mL▪REF 11776576322, CalSet Vials, 2 x 56 empty snap-cap bottles▪REF***********,DiluentUniversal,45.2mLsamplediluent▪▪cobas e 801 analyzerAccessories for the cobas e 801 analyzer:▪REF***********,ProCellIIM,2x2Lsystemsolution▪REF 04880293190, CleanCell M, 2 x 2 L measuring cell cleaning solution ▪REF***********,ReservoirCups,8cupstosupplyProCellIIMand CleanCell M▪REF***********,PreCleanIIM,2x2Lwashsolution▪REF***********,AssayTip/AssayCuptray,6magazinesx6magazine stacks x 105 assay tips and 105 assay cups, 3 wasteliners▪REF***********,LiquidFlowCleaningCup,2adaptorcupstosupply ISE Cleaning Solution/Elecsys SysClean for Liquid Flow CleaningDetection Unit▪REF***********,PreWashLiquidFlowCleaningCup,1adaptorcupto supply ISE Cleaning Solution/Elecsys SysClean for Liquid Flow Cleaning PreWash Unit▪REF 11298500316, ISE Cleaning Solution/Elecsys SysClean,5 x 100 mL system cleaning solutionAssayFor optimum performance of the assay follow the directions given in this document for the analyzer concerned. Refer to the appropriate operator’s manual for analyzer‑specific assay instructions.Resuspension of the microparticles takes place automatically prior to use. Place the cooled (stored at 2‑8 °C) cobas e pack on the reagent manager. Avoid foam formation. The system automatically regulates the temperature of the reagents and the opening/closing of the cobas e pack. Calibrators:Place the calibrators in the sample zone.Read in all the information necessary for calibrating the assay.CalibrationTraceability: This method has been standardized against the 1st WHO Reference Standard 1977.The predefined master curve is adapted to the analyzer using AHBS 2 Cal1 and AHBS 2 Cal2.Calibration frequency: Calibration must be performed once per reagent lot using AHBS 2 Cal1, AHBS 2 Cal2 and fresh reagent (i.e. not more than24 hours since the reagent kit was registered on the analyzer).Renewed calibration is recommended as follows:▪after 12 weeks when using the same reagent lot▪after 28 days when using the same cobas e pack on the analyzer▪as required: e.g. quality control findings with PreciControl Anti‑HBs outside the defined limitsQuality controlFor quality control, use PreciControl Anti‑HBs.Controls for the various concentration ranges should be run individually at least once every 24 hours when the test is in use, once per cobas e pack, and following each calibration.The control intervals and limits should be adapted to each laboratory’s individual requirements. Values obtained should fall within the defined limits. Each laboratory should establish corrective measures to be taken if values fall outside the defined limits.If necessary, repeat the measurement of the samples concerned.Follow the applicable government regulations and local guidelines for quality control.CalculationThe analyzer automatically calculates the analyte concentration of each sample in IU/L.Interpretation of the resultsNumeric result Result message Interpretation< 10 IU/L Non-reactive Negative for anti-HBs≥ 10 IU/L Reactive Positive for anti-HBsvary depending on the testing procedure used. Results obtained from a single sample using tests from different manufacturers can therefore differ by up to a factor of 4 (or even a factor of 10 in rare cases). If there is a change in the assay procedure used during the monitoring of vaccination protection, then the anti‑HBs values obtained upon changing over to the new method must be confirmed by parallel measurements by both methods. Vaccination strategies in certain risk groups are based on the measured anti‑HBs concentration. Respective recommendations are given by national or regional guidelines. Limitations - interferenceThe effect of the following endogenous substances and pharmaceutical compounds on assay performance was tested. Interferences were tested up to the listed concentrations and no impact on results was observed. Endogenous substancesCompound Concentration testedBilirubin ≤ 513 μmol/L or ≤ 30 mg/dL Hemoglobin ≤ 0.621 mmol/L or ≤ 1000 mg/dL Intralipid ≤ 1500 mg/dLBiotin ≤ 41 nmol/L or ≤ 10 ng/mL Rheumatoid factors ≤ 1200 IU/mLAlbumin ≤ 7.0 g/dLIgG ≤ 7.0 g/dLIgA ≤ 1.6 g/dLIgM ≤ 1.0 g/dL2 / 42017-09, V 1.0 Can EnglishCriterion: Recovery for samples from Limit of Detection to 10 IU/L:≤ ± 2 IU/L, and samples > 10 IU/L: ≤ ± 20 % of initial value.Samples should not be taken from patients receiving therapy with high biotin doses (i.e. > 5 mg/day) until at least 8 hours following the last biotin administration.Pharmaceutical substancesIn vitro tests were performed on 16 commonly used pharmaceuticals. No interference with the assay was found.In addition, the following special drugs used in hepatitis B therapy were tested. No interference with the assay was found.Special drugsDrug Concentration testedmg/LPeginterferon alfa‑2a ≤ 0.18Peginterferon alfa‑2b ≤ 1.6Lamivudine ≤ 300Adefovir ≤ 10Entecavir ≤ 10Tenofovir ≤ 600Telbivudine ≤ 245Due to high-dose hook effect c), results from anti‑HBs concentrations of> 200000 IU/L may be found below the upper limit of the measuring range of 1000 IU/L. In rare cases, a high-dose hook effect from anti HBs concentrations of < 20000 IU/L cannot be excluded. Therefore in case of any unexpected low result the sample should be diluted 1:100 (refer to chapter “Dilution”) and tested again.In rare cases, interference due to extremely high titers of antibodies to streptavidin and ruthenium can occur. The test contains additives which minimize these effects.c) High-dose hook effect: A sample with a true concentration clearly above the measuring range, but found within the measuring range.Limits and rangesMeasuring range2‑1000 IU/L (defined by the Limit of Detection and the maximum of the master curve). Values below the Limit of Detection are reported as< 2 IU/L.Values above the measuring range are reported as > 1000 IU/L (or up to 100000 IU/L for 100‑fold diluted samples).DilutionSamples with anti‑HBs concentrations above the measuring range can be diluted with Diluent Universal. The recommended dilution is 1:100 (either automatically by the analyzer or manually). The concentration of the diluted sample must be > 10 IU/L.After manual dilution, multiply the result by the dilution factor.After dilution by the analyzer, the software automatically takes the dilution into account when calculating the sample concentration.Manual dilution can also be made with negative human serum.Note: Antibodies to HBsAg are heterogeneous. In some isolated cases, this may lead to non-linear dilution behavior.Specific performance dataRepresentative performance data on the analyzer is given below. Results obtained in individual laboratories may differ.PrecisionPrecision was determined using Elecsys reagents, samples and controls in a protocol (EP05‑A3) of the CLSI (Clinical and Laboratory Standards Institute): 2 runs per day in duplicate each for 21 days (n = 84). The following results were obtained:cobas e 801 analyzerRepeatability d)Intermediateprecision e)Sample MeanIU/LSDIU/LCV%SDIU/LCV% Human serum 1 4.33 0.224 5.2 0.272 6.3 Human serum 2 12.0 0.237 2.0 0.277 2.3 Human serum 3 475 6.81 1.4 7.55 1.6 PC f) Anti-HBs 1 < 2.00 - - - -PC Anti-HBs 2 83.8 1.08 1.3 1.28 1.5d) Repeatability = within-run precisione) Intermediate precision = between-run precisionf) PC = PreciControlAnalytical specificityNo cross-reactions with HAV, HCV, HEV, CMV, EBV, HIV, Rubella, Toxoplasma gondii, Treponema pallidum, rheumatoid arthritis, autoimmune response or alcoholic liver disease were observed.Measurements were performed on each of the pathogens listed above using ≥ 8 serum or plasma samples which were positive for antibodies to the above-mentioned pathogens.Relative sensitivityPerformance of the Elecsys Anti‑HBs II assay has been assessed by testing a total of 669 samples at two different study sites. 296 samples from vaccinated persons and 373 samples from patients recovered from a hepatitis B infection have been measured with the Elecsys Anti‑HBs II assay and another commercially available fully automated anti‑HBs assay. Discrepant samples were tested with additional anti‑HBs assays to achieve a consensus.Characterization ofsamplesN ElecsysAnti‑HBs IIreactiveAnti‑HBscomparisontest reactiveSensitivity%Anti-HBs positive:vaccinees 296 296 296 100Anti-HBs positive:recovered from ahepatitis B infection373 373 373 100 Total 669 669 669 100 Relative specificityPerformance of the Elecsys Anti‑HBs II assay has been assessed by testing 2673 samples from blood donors negative for anti‑HBs at two different study sites and 1623 anti‑HBs negative samples from laboratory routine at three different study sites. Discrepant samples were tested with additional anti‑HBs assays to achieve a consensus.Characterization of samples N ElecsysAnti‑HBs IIfalsepositiveSpecificity%Anti-HBs negative: blood donors 2673 6 99.78 Anti-HBs negative: routinesamples1623 9 99.45 References1Seeger C, Zoulim F, Mason WS. Hepadnaviruses. In: Field’s Virology, Knipe DM, Howley RM (eds), 2007 5th edition, Lippincott Williams andWilkins, Philadelphia, USA. Chapter 76, pp2977-3029.2WHO. Hepatitis B vaccines. Wkly Epidemiol Rec 2009;84:405-420.3Liaw YF, Chu CM. Hepatitis B virus infection. Lancet2009;373:582-592.4Caspari G, Gerlich WH. The serologic markers of hepatitis B virus infection – proper selection and standardized interpretation. Clin Lab2007;53:335-343.5Kramvis A, Kew M, François G. Hepatitis B virus genotypes. Vaccine 2005;23:2409-2423.6Michel ML, Tiollais P. Hepatitis B vaccines: protective efficacy and therapeutic potential. Pathol Biol 2010;58:288-295.7Elgouhari HM, Abu-Rajab Tamimi TI, Carey WD. Hepatitis B virus infection: understanding its epidemiology, course, and diagnosis. Cleve Clin J Med 2008;75:881-889.8Occupational Safety and Health Standards: Bloodborne pathogens. (29 CFR Part 1910.1030). Fed. Register.9Directive 2000/54/EC of the European Parliament and Council of18 September 2000 on the protection of workers from risks related toexposure to biological agents at workFor further information, please refer to the appropriate operator’s manual for the analyzer concerned, the respective application sheets, the product information and the Method Sheets of all necessary components (if available in your country).A point (period/stop) is always used in this Method Sheet as the decimal separator to mark the border between the integral and the fractional parts of a decimal numeral. Separators for thousands are not used.SymbolsRoche Diagnostics uses the following symbols and signs in addition to those listed in the ISO 15223‑1 standard:CONTENT Contents of kitSYSTEM Analyzers/Instruments on which reagents can be used REAGENT ReagentCALIBRATOR CalibratorVolume after reconstitution or mixingGTIN Global Trade Item NumberCOBAS, COBAS E, ELECSYS and PRECICONTROL are trademarks of Roche. INTRALIPID is a trademark of Fresenius Kabi AB.All other product names and trademarks are the property of their respective owners. Additions, deletions or changes are indicated by a change bar in the margin.© 2016, Roche DiagnosticsRoche Diagnostics GmbH, Sandhofer Strasse 116, D-68305 Mannheim。
罗氏E411全自动电化学发光免疫分析仪常见问题及处理

罗氏E411全自动电化学发光免疫分析仪常见问题及处理发表时间:2015-10-23T14:00:43.717Z 来源:《医药前沿》2015年第24期供稿作者:陆绍科[导读] 贵州省独山县人民医院贵州独山处理方法:打开试剂盒盖子,检查试剂如加得太满,用移液器将试剂吸出后重新执行试剂扫描或手工注册即可。
陆绍科(贵州省独山县人民医院贵州独山 558200)【摘要】罗氏E411全自动电化学发光免疫分析仪它具有操作简便,自动化程度高,精密度高,重复性好样品用量少,节省试剂,检测速度快等优点。
是国际公认的“金标准”,而在使用过程中往往会出现一些小故障,需要自行尽快排除,以至于不影响日常工作。
【中图分类号】R197.3 【文献标识码】A 【文章编号】2095-1752(2015)24-0303-02 仪器在运行过程中,当出现报警信息时,在屏幕上方状态栏的颜色会发生改变,报警颜色呈红色或黄色,当报警颜色为红色时,仪器将发生停止工作,同时报警代码简要的描述以及报警类型及中文提示都会显示出来。
笔者就使用该仪器现场解决处理的一些经验报告如下。
1. 吸样针检测到某项目试剂盒中有气泡1.1 报警此信息多数都是由于用户为了节约试剂,将多个试剂拼装后,拼装的试剂加得太满所致。
处理方法:打开试剂盒盖子,检查试剂如加得太满,用移液器将试剂吸出后重新执行试剂扫描或手工注册即可。
在不能确认是哪瓶试剂所致的报警时,可执行试剂扫描,当试剂针探测到某个试剂有问题时就会马上报警,此致即可确认是某个试剂的问题即可将其取出。
1.2 报此信息的另一个问题是:试剂在运输过程中受到振动可能的产生气泡。
处理方法:此时应将试剂静置30分钟后再用。
日常工作在取出试剂使用时应当避免人为晃动或颠倒试剂。
2.由于电导率升高导致某项目试剂的液面误检/运动过程中,样本/试剂针液面感应错误2.1 报警此信息多数是样本/试剂针表面有静电或有污物附着,处理方法:在关机状态下,手工移动样本/试剂针到方便擦拭的位置,用纱布沾上70%酒精,轻轻擦拭针的表面和针尖;再用蒸馏水清洁1次即可。
罗氏电化学发光免疫分析仪定标物保存方法

罗氏电化学发光免疫分析仪定标物保存方法罗氏电化学发光免疫分析仪是一种常见的实验仪器,用于检测和定量分析生物样本中的特定生物分子,如蛋白质、抗体、激素等。
定标是使用已知浓度的标准物质来建立分析仪器的检测曲线和定量范围。
定标物的保存方法对于保证分析仪器的准确性和稳定性非常重要。
本文将从两个方面介绍罗氏电化学发光免疫分析仪定标物的保存方法,包括标准物质的选择和保存条件。
选择标准物质:在进行定标前,首先需要选择与待测分析物相同或相似的标准物质进行定标。
标准物质应具有以下特点:1.纯度高:标准物质的纯度应尽可能接近100%,以减少不纯物质对分析结果的影响。
2.稳定性好:标准物质应具有良好的化学稳定性和物理稳定性,以确保在保存期间不发生分解、降解或溶解。
3.可溶性好:标准物质应易于溶解于使用的溶剂中,以便在定标过程中进行稀释。
4.经济适用:标准物质的价格应相对较低,以降低实验成本。
保存条件:标准物质的保存条件直接影响着其稳定性和可靠性,因此需要注意以下几个方面:1.存储温度:一般来说,标准物质的保存温度应根据其化学性质和稳定性来确定。
一些易降解的标准物质需在低温下保存,如-20℃或更低。
而一些稳定性较好的标准物质可以在常温下保存,但应避免暴露在光照、高温或高湿环境中。
2.容器选择:标准物质应存放在密封、不透光的容器中,以防止光和空气的影响。
常见的存储容器有玻璃瓶、塑料管或聚丙烯封口袋等。
3.避免冷冻解冻:对于需要在冷冻状态下保存的标准物质,应避免频繁的冷冻解冻过程,以免影响其稳定性。
可以根据实验需要,将标准物质分装成适量的小份,每次只取一小部分使用,并立即将剩余的封存起来。
4.防潮防湿:标准物质应避免接触水分和湿气,以免发生水解、分解或结晶现象。
可以在存放容器中加入干燥剂,如无水硫酸钠、碳酸钠或干燥的硅胶等,以吸湿保持干燥环境。
5.定期检测:定期对保存的标准物质进行检测,以确保其浓度和稳定性。
可以使用同一批次的标准物质进行再次定标,以验证保存的标准物质是否保持稳定。
罗氏电化学发光免疫分析仪定标物保存方法
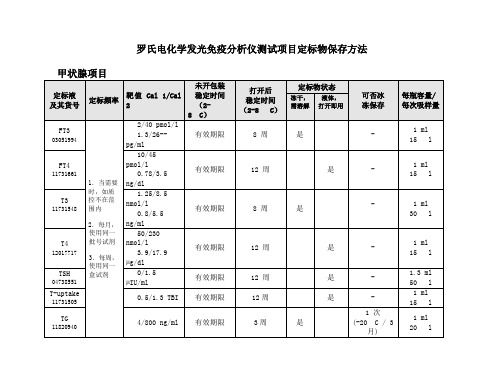
罗氏电化学发光免疫分析仪测试项目定标物保存方法Cal 1/Cal未开包装稳定时间(2-8C)打开后稳定时间(2-8 C)2/40 pmol/l 1.3/26-- pg/ml1 ml 15 l10/45pmol/l0.78/3.5 ng/dl1 ml 15 l1.25/8.5nmol/l0.8/5.5 ng/ml1 ml 30 l50/230nmol/l3.9/17.9 µg/dl1 ml 15 l0/1.5 µIU/ml 1.3 ml 50 l0.5/1.3 TBI1 ml 15 l4/800 ng/ml1 次(-20 C / 3月)1 ml20 lAnti-TG 0636860340/3250IU/ml有效期限 6 周是不可1.5 ml10 µlAnti-TPO 0647293135/350IU/ml有效期限8小时是1 次(-20 C / 8周)1.5 ml20 µlAnti-TSHR 1/25 IU/l有效期限是1 次(-20 C / 3月)2 ml50 µl无信息定标物和质控物是测试包装内的一部分定标必须被进行:每盒新试剂;每天 (当仪器上使用同一盒试剂);需要时,如质控不在范围内心肌标志物定标液及其货号定标频率靶值Cal 1/Cal2未开包装稳定时间(2-8C)打开后稳定时间(2-8C)定标物状态可否冰冻保存每瓶容量/每次吸样量冻干,需溶解液体,打开即用CK-MB11821601(18 min)1.当需要时,如质控不在范围内2.每月,使用同一批号试剂3.每周,使用同一盒试剂 1.5/25ng/ml有效期限 2 周是1次(-20 C / 3月)1 ml15 lCK-MB STAT11731572 (9 min) 1.5/25ng/ml有效期限 2 周是1次(-20 C / 3月)1 ml15 lMyoglobin 12178222 (18 min) 35/1200ng/ml有效期限12周是-1 ml15 µlMyoglobin STAT 11820893(9min) 35/1200ng/ml有效期限12周是-1 ml15 µlTroponin Ths 05092736 (9 min)0.1/10ng/ml有效期限2周是1次(-20 C / 3月)1 ml15 l0.1/10 ng/ml1次(-20 C / 3月)1 ml15 l140/2700pg/ml 16.6/320 pmol/l1次(-20 C / 3月)0.61/3.61ng/ml,0.78/4.62nmol/l5.00/60ng/ml,6.55/79nmol/l性激素项目Cal 1/Cal 未开包装稳定时间(2-8C)打开后稳定时间(2-8C)HCG+03302652 1.5/2000mIU/ml10/5000mIU/ml12.5/1000 nmol/l0.45/36 µg/dl1次(-20 C / 3月)15/120 pg/ml1 次(-20 C / 1月)1 ml50 l0.14/20µmol/l5/750 µg/dl1次(-20 C / 3月)73/11000 pmol/l20/3000 pg/ml1次(-20 C / 3月)1/55 mIU/ml1次(-20 C / 3月)1/45 mIU/ml1次(-20 C / 3月)0.6/169 nmol/l0.2/53 ng/ml2/2000 µIU/ml 0.09/94 ng/ml1次(-20 C / 3月)0/40 nmol/l1次(-20 C / 2月)< 1.2/ 40 nmol/l< 0.4/ 11.5 ng/ml1次(-20 C / 3月)0/10 ng/ml0/10000 pg/ml1次(-20 C / 28天)未开包装稳定时间(2-8C)打开后稳定时间(2-8C)5/50 IU/ml, 6/60 ng/ml1次(-20 C / 6周)1 ml10 l5/50 ng/ml1 ml 10 l35/500 U/ml 15/100 U/ml20/250 U/ml1次(-20 C / 2月)1/70 U/ml 0/50 ng/ml。
Cobas c 501分析仪用户操作手册解读

第一章系统概述罗氏Cobas 6000是全自动免疫测定与光度测定分析系统,可定性或定量测定检测项目,Cobas 6000包括两部分:cobas c 501生化分析模块:进行分光光度测定和离子选择电极测定cobas e 601免疫分析模块:进行电化学发光测定下面从控制单元、核心单元、cobas c 501生化分析模块等三部分介绍该系统(cobas e 601免疫分析模块不作介绍)。
1、控制单元A 显示器(连接cobas ) D 触摸式显示器(主机)B 键盘/鼠标(连接cobas) E 键盘/鼠标(主机)C 计算机(连接cobas) F 计算机(主机)G 人体学PC支架2、核心单元1)核心单元轨道A 核心单元 E 模块轨道B 急诊标本位 F 常规标本上机位C 条形码阅读器G 标本退出位D 标本架转盘急诊标本位A 标本架托盘B 标本架C 标本杯、微量杯2)标本架及标本容器标本架不同类型、颜色和相应编号如下:标本容器有三种类型:标本试管、标本杯、定标及质控小瓶标本试管直径为13mm或16mm,长度为75mm或100mm;标本杯可插入16 mm标本试管中用。
A 标本架上的标本杯 D 16mm×100mm试管B 16mm×75mm试管 E 16mm×100mm试管上的标本杯C 16mm×75mm试管上标本杯3、cobas c 501生化分析模块A、B 标本吸样区 E、F 试剂吸样区C 反应盘区 G 试剂盒装载区D ISE模块A、B 标本吸样区A 、B 标本针 D 标本针抽干区C 屏蔽管(防静电) E 标品针冲洗站C 反应盘区A SMS (位置2)、 Multiclean (位置1)B 水位感受器C 超声混合单元D 光度计单元 F 反应盘 G 杯冲洗装置 HHitergent从左往右依次为:Internal standard solution Internal standard solution Diluent solution Diluent solutionReference electrode solution更换以上系统试剂后,进入reagent—status,选择reagent volumn reset 后按ok,仪器即自动更新系统试剂可用量。
罗氏电化学发光仪Cobas e411使用体会

罗氏电化学发光仪Cobas e411使用体会芮桥安【摘要】@@ 电化学发光仪Cobas e411是罗氏公司2008年推出的Elecsys 2010的升级版,是全自动、随机的异相免疫分析系统.该系统采用最先进的电化学发光免疫分析技术,具有快速、准确、特异、灵敏度高的特点[1].本科室于2010年3月将Elecsys 2010更换成了罗氏电化学发光仪Cobas e411.该仪器对实验室条件、对定标、对耗材的要求更高,对试剂的封闭把关更加严格,因而具有更好的测试稳定性.作者就如何使用好Cobas e411谈几点体会.【期刊名称】《检验医学与临床》【年(卷),期】2012(009)006【总页数】1页(P768)【关键词】质量控制;检验;电化学发光仪【作者】芮桥安【作者单位】云南省丽江市人民医院检验科,674100【正文语种】中文电化学发光仪Cobas e411是罗氏公司2008年推出的Elecsys 2010的升级版,是全自动、随机的异相免疫分析系统。
该系统采用最先进的电化学发光免疫分析技术,具有快速、准确、特异、灵敏度高的特点[1]。
本科室于2010年3月将Elecsys 2010更换成了罗氏电化学发光仪Cobas e411。
该仪器对实验室条件、对定标、对耗材的要求更高,对试剂的封闭把关更加严格,因而具有更好的测试稳定性。
作者就如何使用好Cobas e411谈几点体会。
1 实验室条件该仪器最适宜操作温度18~32℃,湿度20%~80%,需要安装空调。
尽管丽江是四季如春的城市,但冬季、春季气温仍然偏低,不安装空调对测试结果有一定影响。
2 定标新批号试剂需定标。
最好直接向试剂供应商购买复溶分装好的定标液。
自己购买成套装的定标液来复溶分装,很容易使用不完而过期,造成浪费。
收到定标液后切忌反复冻融,须尽快定标。
如果当天来不及定标,可暂时放2~8℃冰箱保存。
定标时必须用该定标液的定标卡,不同批号定标液的定标卡不可混用。
罗氏E2010电化学发光分析仪常见报警及其处理

4101软盘读写故障
及时更换新的格式化过的软盘,并要做好备份工作
14
4401结果传输故障
检查硬件连接,检查软件启动情况,然后手工打开端口
15
500204样本不能被处理,系统没有定义
检查相关配套的稀释液、预处理液等
16
定标没有通过
检查定标液操作、保存有无异常,报告定标光子量给工程师
17
单独项目结果突然大批量的异常
检查结果的单位是否相互匹配
18
经定标过的试剂扫描后要重新定标
检查是否已经打开了“Daily Calib request”标选项
尽量不修改时间(有时用户为了适应过期试剂),否则会出现正常日期的项目丢失等现象。
LLD报警
1、清洁S/R针,2、检查水桶滤网有无异物,水质情况怎么样,3、检染病,样本不准用,特别是定标。专做管路清洁用的
4
S/R针、搅拌浆下降遇到故障
检查下降位置下面的试剂包的盖子是否会自己倒下。
或者试剂是否有结冰的现象。
5
扫描器不能扫描条码
用干布清洁扫描窗口
6
抓手故障
换备份软盘启动机器
7
19-01固体废弃物机械故障
拿出废物盒,伸手掏出溢出的头和杯
8
罗氏E2010电化学发光分析仪
常见故障报警及其处理
1
350107
370105吸样报警
1、检查S/R针电压,有无异常。2,检查蒸馏水情况。
3、反复擦洗SR针,以及用配比洗液冲洗SR针,
2
S/R冲洗站漏水
用户经过反复冲洗S/R冲洗站管路,依然水流不畅通,然后检查SIP针站下水情况,也不畅通。原因:SIP针站的不畅会导致S/R站下水也不畅通的。
CK-MB试剂盒说明书(罗氏)

11821598 322 100测试主要用途用免疫学方法定量测定人血清或血浆中肌酸激酶同工酶MB含量。
电化学发光免疫测定试剂,适用于罗氏Elecsys和cobas e免疫测定分析仪。
临床应用1、2、3肌酸激酶(CK)是一种二聚体酶,它有四种不同的形式:线粒体同工酶和胞浆同工酶CK-MM (肌型)、CK-BB(脑型)和CK-MB。
血清中CK-MB的测定值是诊断心肌缺血(例如急性心肌梗塞、心肌炎等)的重要指标。
CK-MB 在心脏症状出现3-8小时后即可检出并且可持续较长时间,这取决于病情经过。
CK-MB还可出现在其它临床条件下,例如横纹肌溶解症和中风。
实验室诊断方面,测定总体CK、肌钙蛋白T和/或肌红蛋百有助于鉴别这些临床疾病。
CK-MB测定的灵敏度与取样时间有关。
因此跟踪测定非常有意义。
Elecsys Ck-MB测定法采用了两种不同的直接对抗人CK-MB的单克隆抗体。
检测原理双抗体夹心法,总检测时间:18分钟●第一次孵育:15μl标本、生物素化的抗CK-MB单克隆抗体和钌(Ru)a标记的CK-MB特异性单克隆抗体一起反应生成抗原抗体夹心复合物。
●第二次孵育:添加包被链霉亲和素的磁珠微粒后,该复合物通过生物素和链霉素之间的反应结合到微粒上。
●将反应液吸入测量池中,通过电磁作用将磁珠吸附在电极表面。
未与磁珠结合的物质通过ProCell被去除。
给电极加以一定的电压,使复合体化学发光,并通过光电倍增器测量发光强度。
●仪器自动通过2点校正的定标曲线计算得到检测结果。
a)Tris(2,2’-bipyridyl) ruthenium(II)-complex (Ru(bpy){23}三联吡啶钌试剂-工作溶液M 包被链霉亲和素的磁珠微粒(透明瓶盖),1瓶,6.5ml;包被链霉亲和素的磁珠微粒,0.72mg/ml;防腐剂。
R1 生物素化的抗CK-MB抗体(灰盖),1瓶,10mL:生物素化抗CK-MB单克隆抗体(小鼠)1.2mg/L;磷酸盐缓冲液100mmol/L,pH值7.0;防腐剂。
化学发光免疫分析试剂操作规范

化学发光免疫分析试剂操作规范化学发光免疫分析试剂操作规范化学闪光免疫分析试剂操作规范一、试剂盒的保存1.保存条件:1.1试剂盒应放置于2~8℃冰箱中存放。
1.2试剂盒在取用过程中禁止颠倒,以避免试剂被污染。
1.3有特殊要求的试剂应严酷按照操作说明书要求的保存条件保存。
2.保存时间:2.1未开封试剂盒于2~8℃保存时,可在有用期以内正常使用。
2.2已开封试剂盒每次使用后需及时放回2~8℃冰箱内保存,应尽可能在开封后1个月内使用。
(按说明指示的开封的半制品有用期计算,尽量在半制品最短的有用期内用完)一、标本的处置惩罚以及保存1.标本收罗1.1.要注意避免出现严重溶血。
血红卵白中含有血红素基团,其有类似过氧化物的活性,因此,在以HRP为标记酶的酶促化学闪光测定中,如血清标本中血红卵白液体浓度较高,则其就很容易在温育过程中吸附于固相,从而使后面加入的HRP底物反应值偏高。
1.2.样本的收罗及血清分离中要注意尽量避免细菌污染,一则细菌的生长,其所分泌的一些酶可能会匹敌原抗体等卵白产生分解作用;二则一些细菌的内源性酶如大肠杆菌的β-半乳糖苷酶自己会对用相应酶作标记的测定要领产生非特异性干扰。
1.3.常规项目对标本收罗的要求:晨起空腹、安静状态下、或者休息半小时后收罗。
1.4.如无特殊说明,源德公司试剂盒合用的标本类型均为血清;故采血时应选用非抗凝采血管。
采血后应尽早离心,将血清分离后单独保存。
1.5.建议接纳真空采血管及蝶形针具,以免直接接触血液。
收罗器皿最好为一次性无菌密闭器皿。
采血后将真空采血管颠倒、轻轻混匀3~4次,不宜过猛,以避免溶血。
1.6.标本收罗时间及患者准备根据检测项目不同对标本的收罗要求也不相同,具体内部实质意义参见试剂盒说明书。
1.6.1激素:可的松峰值在早晨4~6点之间;生长激素、促黄体激素(LH)以及促卵泡激素(FSH)均以阵发性方式释放,须在密切相连的时间间隔内采取数份血样本,以资中心值为测定值。
Cobas e411电化学发光免疫分析仪用户操作手册

cobas e411(Disk)操作手册罗氏诊断产品(上海)有限公司广州分公司第一章一.二.三.四.五.第二章一.二.1.2.3.三.1.2.3.四.第三章一.二.三.四.五.第四章第一章系统概述一.e411主要部件A:操作开关 B:样本(30个位置)/试剂区(18个位置,具自动开关盖装置) C:测试区 D:消耗品区 E:显示及控制单元位于仪器右侧面位于仪器左侧面A:主电源开关 B:电源线 A:USB接口 C:HOST接口二. 控制单元三. 样品/试剂区A :取样区B :样品盘保护盖 A :磁珠搅拌针 B :冲洗站C :样本/试剂针BA :触摸屏B :虚拟键盘(触摸屏幕 上需输入内容区域 时,自动在屏幕下方 跳出)C :数字键盘 A :定标/质控条形码阅读口B :带开关盖装置的试剂仓 (18个位置) CA B四. 测试区A :孵育池(共32个孵育位)B :吸样位A :系统试剂保护门B :Sipple 针C :CleanCell (黑盖)D :ProCell (白盖)五. 消耗品区BDCA :吸头位1-2B :反应杯位3-5C :吸头丢弃位D :反应杯丢弃位废吸头/反应杯盒 A:蒸馏水桶 B:废液桶BABA:抓手B:抓手移动时的横纵轴C:吸头/反应杯区1(120个吸头,60个反应杯)D:吸头/反应杯区2(120个吸头,60个反应杯)E:吸头/反应杯区3(120个吸头,60个反应杯)第二章基本操作一.开机a.检查蒸馏水桶,将SysWash浓缩液配置为1:100的系统用水b.清空废液桶c.打开ProCell和CleanCell盖子,关好系统试剂保护门。
注意:运行过程中不能打开系统试剂保护门,否则仪器将停止运行。
d.打开仪器右面主电源开关,再打开仪器前面操作开关,等界面出现后,录入用户名和密码,仪器自动初始化后进入待机状态注意:仪器分不同级别及权限使用,可根据实际情况设定;添加用户名后,第一次输入的密码即为以后的密码。
罗氏电化学发光仪器e17-sop

罗氏电化学发光仪器E170 SOP仪器简介:E170 是罗氏诊断公司出品的全自动电化学发光免疫分析仪,是全自动,随机进样的免疫分析系统,可以对许多种检测项目进行体外的定量或者定性的分析。
该分析仪应用的是电化学发光技术(ECL)。
每个E模块系统每小时的标本处理量为170个试验(最多可以将4个E模块连接)。
只有在试验室条件下,经过培训的操整理方可操作E模块系统。
系统特色•可以24小时待机使用•标本条码扫描功能•试剂条码扫描功能•单个E模块的每小时处理能力为170个试验•自动保养功能•自动复查功能•自动发出定标信息•自动标本稀释功能•系统辅助的操作流程•一个E模块具有25个温控的试剂通道•1个模块可以安放672个反应杯•1个模块可以安放672个加样头•双向数据传输接口运行条件:水质要求◆无菌(< 10 cfu/ml),去离子水◆ 1.5 MΩ电阻值(最大1.0 Ms/cm)◆15-25 磅/英寸2 (0.5~3.5 kg/cm2 或49~343 kpa)◆耗水量:每E170模块消耗18升/小时环境条件◆无灰尘的、良好通风的环境◆无直接日照◆地面水平(角度:<1/200 º)◆地面足够坚硬能够承受仪器的重量(详细情况请见本章中的系统特点)◆温度:18~32摄氏度◆当系统启动时,温度的改变应该小于2度/小时◆屋内湿度:45%~85%◆电源电压没有明显的波动◆在附近没有会产生电磁波的仪器◆有接地的三相电源E170由三个类型的硬件单元组成:控制单元、核心单元以及检测单元。
控制单元介绍包括:•触摸屏幕的电脑•键盘•打印机•仪器管理电脑终端核心单元介绍核心单元将所有的标本从入口端经过E170仪器到出口端或者复查缓冲区。
下面所列位核心单元的组成部分。
•加样端•标本架转运通道•复查缓冲带•出口端•中心控制区•电源开关(在进样端的左侧面上)检测单元介绍分立式、随机进样的每小时170试验的免疫检测系统。
罗氏电化学发光ECL2010中文操作手册

3.光标移到POS栏。输入所需样本位置号,按ENTER。将样本放入指定位置。
4.如果以多样本盘形式运行,按第一个样本盘的POS,输入样本盘号(0-9),按ENTER。
5.按屏幕上试验项目键进行试验项目的选择。当某一项目被选择,此项目键变蓝色。
释放/拒绝定标:
A.按CALIBRATIONDATA屏幕上的试验键
B.按RALEASE或REJECT
C.按OK
红色:表明定标失败。
8.保养
8.1日常保养
注意不要清洗搅拌器
清洗样本/试剂针(S/R):
在关机状态下手工移动S/R针到方便擦拭的位置用纱布沾70%酒精擦拭针表面
注意:针的尖端部分不能擦拭
擦拭外表面 小心尖端部分
6.如需要,按SAMPLECUPNORMAL键转变成REDUCED而使样本死腔量减少。REDUCED
只是针对样品杯或试管顶部而言。
注:只有当样本稀释液在机,自动稀释功能才有效.按DILUTION FACTOR选择相应稀释倍数
7.按REGISTER键储存当前样本信息。
光标回到SAMPLEID栏。
顺序号被自动累加。
材料准备:
清洗液:SysClean
清洗液容器: SysClean adapter
将9ml左右清洗液倒入清洗液容器
放在系统试剂位3如左图位置:
进入Util-maintenance-liquid flow cleaning-start
完成清洗后将清洗液容器用蒸馏水冲洗干净,仪器废液桶也用次氯酸钠泡洗干净
♥C.按BC♥CARD♥SCAN。SCANNING出现在状态线上。在分析仪未回到STAND-BY
罗氏E601电化学发光免疫分析仪用户操作手册(中文)

第六章 仪器报警信息......................................................................... .. 51
- 2 - 201307 V1.0
第一章 系统概述
1、 控制单元
A 显示器(连接cobas link) B 键盘/鼠标(连接cobas link) C 计算机(连接cobas link) G 人体学PC支架
第四章 维护保养 1、每日保养 ......................................................................... ................ 46 2、每周保养 ......................................................................... .................46 3、每两周保养 ......................................................................... ............. 48 4、每季保养 ......................................................................... ................ 49 5、按需保养 ......................................................................... ................ 49
罗氏中文说明书:他克莫司检测试剂盒(电化学发光法)说明书

【产品名称】通用名称:他克莫司检测试剂盒(电化学发光法)英文名称:Tacrolimus【包装规格】100测试/盒【预期用途】主要用途主要用于定量测定人全血中他克莫司的含量。
本检测有助于接受他克莫司治疗的心、肝、肾移植病人的治疗。
电化学发光免疫测定试剂“ECLIA”,适用于罗氏Elecsys 和cobas e免疫测定分析仪。
临床应用他克莫司(又称KF506)是一种大环内酯类抗生素,1984年在日本被发现,是链霉菌属的代谢产物1.2,3。
研究表明他克莫司的免疫抑制活性是环孢霉素的10-100倍。
4他克莫司产生免疫抑制效应的主要原理在于它可以抑制T细胞的激活和增殖。
细胞内的他克莫司可结合一种抑免蛋白FK506-结合蛋白(FKBP-12),这种免疫复合物可抑制磷酸酶的活性。
5抑制磷酸酶可限制激活的T细胞(NFAT)的核因子的去磷酸化和核转位,由此调节包括IL-2、IL-4、TNF-α和γ-干扰素在内的多种细胞因子的转录,进一步限制淋巴细胞的激活和增殖。
6,7,8,9,10他克莫司具有很高的亲脂性,吸收不完全并且不稳定。
吸收后,他克莫司高效结合蛋白和红细胞,血浆中99%的药物都与白蛋白或α-1-糖蛋白结合。
11他克莫司的生物利用度和代谢主要受细胞色素P450药物代谢同工酶CYP3A4和CYP3A5以及流出泵P-糖蛋白的影响,在表达和功能方面在同一个体以及不同个体之间都变现出明显的差异。
12,13,14他克莫司在同一病人和不同病人间都表现出很大的变异性,无论剂量高低都可能出现严重不良反应。
他克莫司浓度不足可能导致对抑制器官的排异反应。
浓度过高又可导致严重不良反应。
他克莫司的主要不良反应包括肾毒性、神经毒性、胃肠道损害、糖尿病、高血压病和恶性肿瘤。
15,16为了让每个病人的体内药物浓度都维持在狭窄的治疗窗范围内,治疗药物监测的应用和浓度控制下给药作为标准临床实践的一部分已在临床上应用多年,它也是病人治疗的主要手段。
罗氏cobas-e601化学发光免疫分析仪标准操作程序

罗氏cobas e601化学发光免疫分析仪操作程序1目的正确使用与维护罗氏c obas e601全自动化学发光免疫分析仪。
2仪器简介、工作原理2.1 仪器名称:全自动化学发光免疫分析仪2.2 仪器型号:罗氏cobas e6012.3 生产厂商:罗氏诊断公司德国2.4仪器简介:cobas e601是采用目前国内、外最先进的电化学发光免疫分析技术(ECLIA),该技术在发光反应中加入了电化学反应,应用理想的标记物,标记物三联吡啶钌分子结构简单,可标记任何抗原、抗体、核酸等,稳定性好,可确保检测结果的重复性好,无放射性、可避免对人体和环境的危害。
ECLIA是继放射免疫、酶免疫、荧光免疫、化学发光免疫之后的新一代标记免疫测定技术。
该仪器秉承罗氏公司模块化设计,为实验室提供优秀服务。
3仪器运行环境3.1 环境条件为了确保系统操作的正常运转,应该保证以下的条件。
3.1.1 无尘良好通风的环境,无直接日照。
3.1.2 温度:18-32℃,温度的改变应该小于2℃/小时,屋内湿度:30%-80%。
3.1.3 输入电压220V(+/- 10%)50HZ,有良好接地的电源,单独接地线,对地阻抗小于10Ω,零地电压小于2V,仪器功率11KV A,建议UPS功率大于15KV A。
3.1.4 在附近没有会产生电磁波的仪器,环境噪音<85dB(A)。
3.2 供水要求3.2.1无菌去离子水(要求<10 cfu/ml,电导率≤1μS/cm), 水量: c701为50 L/h, c502为40 L/h,水压为0.5-3.5kg/cm2。
3.2.2 纯水水箱出水管口径1/2inch(约12mm内径),地面排水口距仪器排水出口在50--100mm,管长应小于5m。
3.3 操作人员3.3.1要求操作人员熟知相关指导方针与标准以及操作员手册中包含的信息与程序。
操作人员需要接受过罗氏诊断公司的培训,要求操作人员已仔细遵循操作员手册中详细说明的系统操作与维护程序,并取得罗氏公司培训合格的证书。
罗氏 2010全自动电化学发光 检测仪标准操作程序(SOP)

××××第页共页1. 目的规范罗氏2010全自动电化学发光检测仪的操作程序,正确使用该仪器,保证检测工作的顺利进行及其结果的准确性和可靠性。
2. 适用范围此操作规程适用于罗氏2010全自动电化学发光检测仪的操作及维护3. 职责3.1 操作人员:必须按照本规程操作仪器进行相关项目的测定,并对仪器进行日常维护,作使用登记。
3.2 管理责任人:负责监督仪器的使用是否符合规程,设置仪器的参数,对仪器进行定期维护、保养。
3.3 科室负责人:负责该仪器的综合管理及解释。
4. 该SOP变动程序本标准操作程序的改动,可由任一使用本SOP的工作人员提出并报经下述人员批准签字:专业主管、科主任。
5. 操作程序5.1 检测前准备5.1.1 检查UPS电源、电脑主机与仪器的接口,检查打印纸是否足够。
5.1.2 检查系统试剂、系统水、tip头、cup杯等试剂、耗材是否充足,液体及固体废弃物是否清空,样品针和试剂针是否清洁无弯曲。
5.2 标本检测程序5.2.1开机:打开中文报告电脑开关及打印机开关,打开中文软件及接收程序,打开UPS电源及仪器保护罩,打开系统试剂盖(procell和cleancell)、仪器显示器电源及主机电源,等待仪器启动及自检。
5.2.2 仪器启动后,显示屏上显示:“”,用手指轻触显示屏登陆操作界面。
5.2.3 打开试剂仓盖(抓住把手向左旋至OPEN标志,然后移开),放入要测试项目试剂至1-15号试剂位,通用稀释液放在16-18号位置,放好试剂后,盖上试剂仓盖,并旋至LOCK 位置。
5.2.4 扫描试剂:INVENTORY→Reagent Scan 查看试剂的位置、试剂量,试剂是否需要定标(提示RC标志)及消耗品使用情况。
××××第页共页5.2.5 当仪器扫描完成后,屏幕上方显示Stand-by时,在样品盘1-30号位置依次放入待测样本,在最后一个样本后面插上贴有中止码信息的试管。
某电化学发光仪冷冻试剂再利用的可行性研究

某电化学发光仪冷冻试剂再利用的可行性研究姚丽;王珊;李佳琪;王莎莎【摘要】目的探讨罗氏e601全自动电化学发光免疫分析仪冷冻后试剂再利用的可行性.方法冷冻复溶试剂更换M 试剂后分别检测三碘甲状腺原氨酸(T3)、甲状腺素(T4)、促甲状腺激素(TSH)、β-人绒毛膜促性腺激素(β-HCG)、黄体酮(PRG)的水平,进行精密度、准确度分析,并与原装试剂分别检测这5个项目的低、中、高3个水平的同一组血清标本,做均值比较及相关性分析.结果冷冻试剂更换M 试剂后检测T3 、T4 、TSH 、β-HCG 、PRG两个水平质控品批内、批间变异系数(CV )均符合相关标准;质控血清准确性在允许范围内;2种试剂检测血清标本结果呈良好的线性关系,差异无统计学意义( P>0 .05) .结论罗氏e601全自动电化学发光免疫分析仪的冷冻试剂更换M 试剂后可以进行T3 、T4 、TSH 、β-HCG 、PRG检测,能够保证检测质量,避免试剂浪费.【期刊名称】《检验医学与临床》【年(卷),期】2018(015)022【总页数】3页(P3455-3457)【关键词】冷冻试剂;M试剂;电化学发光【作者】姚丽;王珊;李佳琪;王莎莎【作者单位】山东省济宁市汶上县人民医院检验科 272500;山东省济宁市汶上县人民医院检验科 272500;山东省济宁市汶上县人民医院检验科 272500;山东省济宁市汶上县人民医院检验科 272500【正文语种】中文【中图分类】R-331电化学发光免疫分析(ECLIA)是电化学发光和免疫测定相结合的新一代标记免疫测定技术,现已广泛应用于各种激素、肿瘤标志物等测定。
罗氏e601全自动电化学发光免疫分析仪是目前检验科在该领域使用最广泛的仪器之一,具有高灵敏度、检测范围宽、重复性好、检验结果稳定可靠等优点。
电化学发光试剂为原装进口,价格相对较高,测定人份固定,扫描条码自动获取试剂信息。
每个检验项目试剂检测完毕后仍有30%~35%剩余量,造成了试剂的浪费,可以对试剂进行回收再利用[1-8]。
罗氏 E 601 电化学发光免疫分析仪用户操作手册(中文)

罗氏E 601 电化学发光免疫分析仪用户操作手册罗氏诊断产品(上海)有限公司目录第一章系统概述1、控制单元......................................................................... .. (3)2、核心单元......................................................................... (4)3、cobas e601免疫分析模块..................................................... .. . .. (5)第二章软件系统简介1、系统状态概览......................................................................... .. (12)2、日常工作菜单......................................................................... .. (13)第三章常规操作1、开机......................................................................... ................ .. (15)2、仪器准备......................................................................... . (16)3、增加新项目......................................................................... . (18)4、增加校准品........................................... ........ ...... .... ... ..... ..... (23)5、增加质控品 ........................................... ........ ...... .... ... ..... ..... (25)6、校准和质控检测 (30)7、样本检测 ........................................... ........ ...... .... ... ..... ..... ... .... .. 388、关机 ........................................... ........ ...... .... ... ..... ..... ... .... .. .... .. 44第四章维护保养1、每日保养......................................................................... . (46)2、每周保养......................................................................... .. (46)3、每两周保养......................................................................... . (48)4、每季保养......................................................................... . (49)5、按需保养......................................................................... . (49)第六章仪器报警信息......................................................................... .. 51第一章系统概述1、控制单元A 显示器(连接cobas link) D 触摸式显示器(主机)B 键盘/鼠标(连接cobas link) E 键盘/鼠标(主机)C 计算机(连接cobas link) F 计算机(主机)G 人体学PC支架2、核心单元1)核心单元轨道A 核心单元 E 模块轨道B 急诊标本位 F 常规标本上机位C 条形码阅读器G 标本退出位D 标本架转盘急诊标本位A 标本架托盘B 标本架C 标本杯、微量杯2)标本架及标本容器标本架不同类型、颜色和相应编号如下:标本容器有三种类型:标本试管、标本杯、校准及质控小瓶标本试管直径为13mm或16mm,长度为75mm或100mm;标本杯可插入16 mm标本试管中用。
罗氏cobase 411电化学发光仪使用体会及常见报警故障处理

罗氏cobase 411电化学发光仪使用体会及常见报警故障处理汪兴周;袁招红;刘士文【摘要】电化学发光是继放射免疫、酶免疫、荧光免疫、化学发光免疫之后的新一代免疫标记测定技术,其原理是采用双抗夹心原理,将形成的抗原抗体复合物通过生物素与链霉素亲和素间的反应结合到微粒上,在测量池中,微粒通过磁铁吸附到电极上经清洗电极加电压产生化学发光,光电倍增管将其测定到的发光强度自动对应标准曲线,查出结果,整个检测结果仅18分钟.罗氏Cobase 411全自动电化学发光免疫分析仪罗氏公司开发制造的产品,我院于2010年5月引进该仪器,经过近一年的使用,我们认为该仪器具有线性范围宽、准确性灵敏度高、检测速度快等特点.笔者将在使用过程中的体会及常见报警故障分析处理介绍如下.【期刊名称】《赣南医学院学报》【年(卷),期】2012(032)001【总页数】1页(P117)【作者】汪兴周;袁招红;刘士文【作者单位】江西省赣州市第三人民医院检验科,江西赣州341000;江西省赣州市第三人民医院检验科,江西赣州341000;江西省赣州市第三人民医院检验科,江西赣州341000【正文语种】中文【中图分类】R446.6电化学发光是继放射免疫、酶免疫、荧光免疫、化学发光免疫之后的新一代免疫标记测定技术,其原理是采用双抗夹心原理,将形成的抗原抗体复合物通过生物素与链霉素亲和素间的反应结合到微粒上,在测量池中,微粒通过磁铁吸附到电极上经清洗电极加电压产生化学发光,光电倍增管将其测定到的发光强度自动对应标准曲线,查出结果,整个检测结果仅18分钟。
罗氏Cobase 411全自动电化学发光免疫分析仪罗氏公司开发制造的产品,我院于2010年5月引进该仪器,经过近一年的使用,我们认为该仪器具有线性范围宽、准确性灵敏度高、检测速度快等特点。
笔者将在使用过程中的体会及常见报警故障分析处理介绍如下。
1.1 罗氏发光仪试剂昂贵,每盒试剂达到厂家设定的测定数后,试剂盒还能够剩下一些试剂,此时把白色条码撕去,将试剂盒黑色条码手工注册后,该试剂盒还能检测一定数量的样本,可以节约成本。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
罗氏电化学发光免疫分析仪测试项目定标物保存方法
无信息定标物和质控物是测试包装的一部分
定标必须被进行:每盒新试剂;每天 (当仪器上使用同一盒试剂);需要时,如质控不在围
心肌标志物
性激素项目
肿瘤标志物
贫血诊断指标、骨标志物
传染病项目
其它
唐氏筛查
罗氏电化学发光免疫分析仪定标物保存方法(简版)
定标物不需要分装冰冻保存的项目:
使用时从2-8︒C取出,摇均后吸200μl(此数据为国实验室试验所得,不代表罗氏官方)到日立杯,马上将剩余定标品放回2-8︒C
FT3、FT4、T3、T4、TSH、T-uptake、Anti-TG、
HCG+β、HCG STAT、Progesterone
CEA、CA 125、CA 153、CA 724、Cyfra21-1、NSE、Free PSA、HE4
Myoglobin、Myoglobin - STAT 、Digoxin、Digitoxin、Ferritin、IgE、β-CrossLaps
Anti-HAV、Anti-HAV IgM、HBsAg、HBsAg II quant、 Anti-HBs、HBeAg、Anti-HBe、Anti-HBc、 Anti-HBc IgM、 HIV combi、
HIV Ag 、HIV combi PT
Toxo IgG、 Toxo IgM、Rubella IgG、Rubella IgM、CMV IgG、
CMV IgM
定标物需要分装冰冻保存的项目:
定标物加水复溶,用子弹头进行分装(分装量为200μl(此数据为国实验室试验所得,不代表罗氏官方)),然后放在-20︒C保存,使用时取出并平衡到室温
TG、Anti-TPO、 Anti-TSHR、CK-MB、CK-MB STAT、ProBNP、Troponin T HS、Troponin T HS STAT free βHCG、PAPP-A、 Insulin、C-peptide、IL-6 、PCT、Anti-CCP
Cortisol、ACTH、Estradiol II、FSH、LH、Prolactin、Testosterone、DHEA-S、SHBG、PIGF、 sFlt-1、hGH
文档
AFP、CA 、TPSA、S100
Vitamin B12、Folate III 、N-MID、Total P1NP、PTH、PTH STAT、PTH(1-84) Vitamin D3、Vitamin D total
HSV-1 IgG、 HSV-2 IgG。
