融合蛋白标签
l融合标签技术概述

l融合标签技术概述
融合标签技术概述
融合标签技术的发展最初是为了简化蛋⽩质的纯化,即通
过重组蛋⽩质所含融合标签同固相介质中配体的特异相互作
⽤,实现重组蛋⽩质的亲和纯化陋哪“⽬。
⽬前,随着多种融合标
签系统的研究和发展,融合标签技术也得到了更为⼴泛的应⽤,
包括重组蛋⽩质的纯化、⽬的蛋⽩质的检测和定向固定、体内⽣
物事件的可视化、提⾼重组蛋⽩质的产量、增强重组蛋⽩质的可
溶性及稳定性。
融合标签的相对分⼦质量、来源、⽣理⽣化特性
各有不同陋191。
亲和融合标签既可以是⼩分⼦多肽⽚段如多聚组
氨酸标签,也可以是整个功能蛋⽩质如麦芽糖结合蛋⽩(MBP)。
这些融合标签的作⽤机制包括了酶与底物、细菌受体与⾎清蛋
⽩、多聚组氨酸与⾦属离⼦、抗原与抗体等f1¨q。
⼀些⾼表达的蛋
⽩质和分⼦伴侣如SUM0和NusA作为融合标签连接到⽬的蛋
⽩质上时,可以提⾼重组融合蛋⽩的表达量和可溶性,避免和减
少包涵体的产⽣,提⾼⽬标蛋⽩质的产量嗍。
如果融合标签的作
⽤类型为抗原和抗体,此类融合标签也被称为表位标签(epitope
tags)。
由于抗体对抗原的识别和结合有很⾼的特异性,⽽表位标
签通常为⼩分⼦多肽⽚段,对重组融合蛋⽩的结构和功能影响
较⼩,可以结合免疫检测技术⽤于追踪和定位⽬的蛋⽩,进⾏蛋
⽩质及蛋⽩质复合体的结构功能相关性研究哪52.11。
荧光蛋⽩如
绿⾊荧光蛋⽩(GYP)受激发时可以发出荧光,能够利⽤仪器定性
和定量检测。
有利于对含有融合荧光蛋⽩标签的重组蛋⽩的表
达、追踪、定位及相关结构功能研究刚础l。
FLAG标签融合蛋白纯化试剂盒使用说明书
FLAG标签(DYKDDDDK)融合蛋白纯化试剂盒Cat#:KAP0064(本品仅用于科学研究,不可用于诊断及治疗)1.背景信息Flag-Tag(DYKDDDDK),常用于真核蛋白质重组表达标记。
FLAG标签(DYKDDDDK)融合蛋白纯化试剂盒,主要成分是Anti-Flag亲和纯化凝胶(Anti-DYKDDDDK (Flag) Affinity Gel),由高品质的Flag兔多克隆抗体与Sepharose 4B琼脂糖颗粒共价偶联制成,具有高载量(至少为1.2mg protein/ml凝胶),高特异性,性质稳定,可反复使用的特点,可用于Flag 标签融合蛋白的亲和纯化。
2.性能指标应用范围:可用于Met修饰的N端Flag融合蛋白(Met-Flag–Protein),N端Flag融合蛋白(Flag–Protein)和C端Flag融合蛋白(Protein-Flag)的亲和纯化。
载量:1ml Sepharose 4B琼脂糖颗粒,共价偶联800μg Anti-Flag 兔多克隆抗体,可纯化至少1.2mg Flag融合蛋白。
强度:重力柱纯化,可反复使用5次以上。
保存方法:在加入了50%甘油和0.2‰叠氮钠的PBS保存液后,预装纯化柱可于-20℃可保存1年。
3.试剂盒组成50 mM Tris HCl, pH 7.4, 150 mMNaCl, 1 mM EDTA, and 1%Triton X-100(说明见5.3)4.使用方法4.1细胞裂解液制备4.1.1悬浮细胞和半贴壁细胞从细胞培养瓶上吹下来后放入离心管中,1000rpm离心5分钟。
贴壁细胞用细胞刮子轻轻从瓶壁上刮下来,放入离心管中1000rpm离心5分钟。
4.1.2预冷的PBS工作液重悬细胞,1000rpm离心3min,弃上清。
重复一次。
4.1.3根据细胞的量加入相应体积的细胞裂解液,反复吹打后冰上放置10-20min,让细胞充分裂解。
4.1.4用超声破碎仪将细胞裂解液超声,直至细胞裂解液透明,不再粘稠。
蛋白结合标签

蛋白结合标签
蛋白结合标签是一种广泛应用于生物医学研究领域的技术,它可以帮助科学家们更好地理解蛋白质在生物体内的功能和相互作用。
蛋白结合标签可以分为两种类型:共轭标签和荧光标签。
共轭标签是指将一种蛋白质与一种可共轭的分子结合,从而使该蛋白质带上共轭标记。
共轭标签可以与另一种蛋白质上的特定区域发生特异性结合,从而可以对这两种蛋白质进行研究。
共轭标签技术在生物学研究中具有重要意义,例如在研究细胞信号传导过程中,可以利用共轭标签来检测蛋白质与受体的结合情况。
荧光标签是指将一种蛋白质与一种可发射荧光的分子结合,从而使该蛋白质带上荧光标记。
荧光标签可以发出特定波长的光,从而可以对蛋白质在生物体内的位置和运动进行实时监测。
荧光标签技术在生物学研究中也有着重要的意义,例如在研究细胞内物质的运输过程中,可以利用荧光标签来追踪蛋白质的运输路径。
蛋白结合标签技术为生物医学研究提供了更加深入的研究手段,也为医学诊断和治疗提供了更多的可能性。
随着科技的不断发展,蛋白结合标签技术也在不断更新,未来它将在生物医学领域发挥更加重要的作用。
GFP标签融合蛋白亲和凝胶使用说明书

Anti-GFP亲和凝胶Cat#:IP0057(本品仅用于科学研究,不可用于诊断及治疗)1.背景信息GFP,绿色荧光蛋白(Green fluorescent protein),来源于维多利亚多管发光水母,由约238个氨基酸组成,从蓝光到紫外线都能使其激发出绿色萤光。
GFP常用于真核蛋白质重组表达标记。
Anti -GFP亲和凝胶,由高品质的GFP鼠单克隆抗体与Sepharose 4B琼脂糖颗粒共价偶联制成,具有高载量(至少为1.2mg protein/ml凝胶),高特异性,性质稳定,可反复使用的特点,可用于GFP标签融合蛋白的免疫(共)沉淀检测。
2.性能指标应用范围:可用于N端GFP融合蛋白(GFP–Protein)和C端GFP融合蛋白(Protein-GFP)的免疫(共)沉淀。
载量:1ml Sepharose 4B琼脂糖颗粒,共价偶联800μg Anti-GFP 鼠单克隆抗体,可沉淀至少1.2mg GFP融合蛋白。
成分:共价偶联Anti-GFP 鼠单克隆抗体的Sepharose 4B琼脂糖颗粒, 1ml溶于2ml PBS+50%甘油中。
保存方法:在加入了50%甘油和0.2‰叠氮钠的PBS保存液中,-20℃可保存1年。
3.使用方法3.1细胞裂解液制备3.1.1悬浮细胞和半贴壁细胞从细胞培养瓶上吹下来后放入离心管中,1000rpm离心5分钟。
贴壁细胞用细胞刮子轻轻从瓶壁上刮下来,放入离心管中1000rpm离心5分钟。
3.1.2预冷的PBS(pH7.2)重悬细胞,1000rpm离心3min,弃上清。
重复一次。
3.1.3根据细胞的量加入相应体积的细胞裂解液(推荐配方见5.3),反复吹打后冰上放置10-20min,让细胞充分裂解。
3.1.4用超声破碎仪将细胞裂解液超声,直至细胞裂解液透明,不再粘稠。
冰上放置30min之后,12000rpm,4℃离心10min。
取上清,冷冻保存。
3.2装柱及孵育3.2.1根据使用目的选用重力柱或离心管,移入适量亲和凝胶。
几种常用的蛋白标签
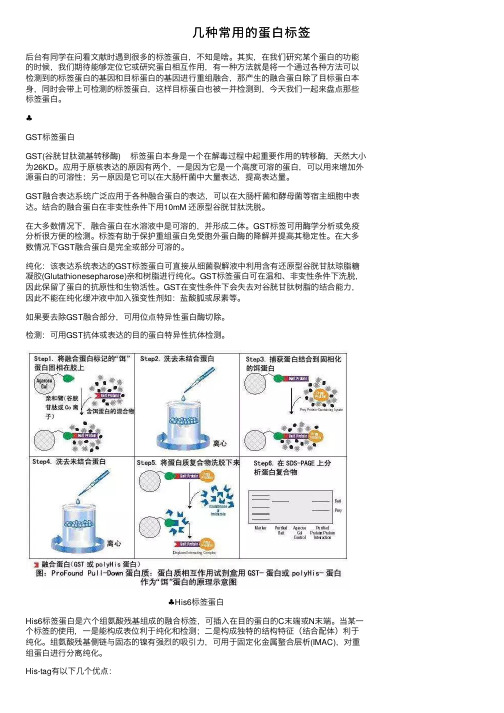
⼏种常⽤的蛋⽩标签后台有同学在问看⽂献时遇到很多的标签蛋⽩,不知是啥。
其实,在我们研究某个蛋⽩的功能的时候,我们期待能够定位它或研究蛋⽩相互作⽤,有⼀种⽅法就是将⼀个通过各种⽅法可以检测到的标签蛋⽩的基因和⽬标蛋⽩的基因进⾏重组融合,那产⽣的融合蛋⽩除了⽬标蛋⽩本⾝,同时会带上可检测的标签蛋⽩,这样⽬标蛋⽩也被⼀并检测到,今天我们⼀起来盘点那些标签蛋⽩。
♣GST标签蛋⽩GST(⾕胱⽢肽巯基转移酶) 标签蛋⽩本⾝是⼀个在解毒过程中起重要作⽤的转移酶,天然⼤⼩为26KD。
应⽤于原核表达的原因有两个,⼀是因为它是⼀个⾼度可溶的蛋⽩,可以⽤来增加外源蛋⽩的可溶性;另⼀原因是它可以在⼤肠杆菌中⼤量表达,提⾼表达量。
GST融合表达系统⼴泛应⽤于各种融合蛋⽩的表达,可以在⼤肠杆菌和酵母菌等宿主细胞中表达。
结合的融合蛋⽩在⾮变性条件下⽤10mM 还原型⾕胱⽢肽洗脱。
在⼤多数情况下,融合蛋⽩在⽔溶液中是可溶的,并形成⼆体。
GST标签可⽤酶学分析或免疫分析很⽅便的检测。
标签有助于保护重组蛋⽩免受胞外蛋⽩酶的降解并提⾼其稳定性。
在⼤多数情况下GST融合蛋⽩是完全或部分可溶的。
纯化:该表达系统表达的GST标签蛋⽩可直接从细菌裂解液中利⽤含有还原型⾕胱⽢肽琼脂糖凝胶(Glutathionesepharose)亲和树脂进⾏纯化。
GST标签蛋⽩可在温和、⾮变性条件下洗脱,因此保留了蛋⽩的抗原性和⽣物活性。
GST在变性条件下会失去对⾕胱⽢肽树脂的结合能⼒,因此不能在纯化缓冲液中加⼊强变性剂如:盐酸胍或尿素等。
如果要去除GST融合部分,可⽤位点特异性蛋⽩酶切除。
检测:可⽤GST抗体或表达的⽬的蛋⽩特异性抗体检测。
♣His6标签蛋⽩His6标签蛋⽩是六个组氨酸残基组成的融合标签,可插⼊在⽬的蛋⽩的C末端或N末端。
当某⼀个标签的使⽤,⼀是能构成表位利于纯化和检测;⼆是构成独特的结构特征(结合配体)利于纯化。
组氨酸残基侧链与固态的镍有强烈的吸引⼒,可⽤于固定化⾦属螯合层析(IMAC),对重组蛋⽩进⾏分离纯化。
优质原创总结 NusA标签 MBP标签 融合标签蛋白纯化原理及优缺点

融合MBP蛋白的纯化(双标签:MBP-His6)
更多蛋白表达/蛋白纯化相关原理/实验流程及FAQ请访问: /topics/dan-bai-biao-da.html 我们会不断的更新补充最全面、专业的蛋白表达相关知识, 欢迎收藏!
谢谢大家
融合NusA 和 MBP蛋白纯化
融合NusA和MBP蛋白纯化
定义
A
B
原理
方法
C
D
问题
NusA
NusA(antitermination protein
残基数:495
分子量: 54.87KDa
不具有独立的纯化标签功能,所以要与其它标签如His标签联用
关于NusA
NusA的 氨基酸序列
NusA的运用的优点和缺点
NusA标签的去除
NusA标签的去除 (TEV)
双标签融合蛋白NusA与His 6的纯化(试剂)
双标签融合蛋白NusA与His 6的纯化(流程)
双标签融合蛋白NusA与His 的纯化(分析)
6
MBP
麦芽糖结合蛋白(maltose binding protein. MBP)
关于MBP
关于MBP
MBP标签运用的优缺点
融合MBP蛋白的纯化(流程)
融合MBP蛋白的纯化(试剂)
融合MBP蛋白的纯化(MBP-RACK1蛋白多步纯化-亲和)
融合MBP蛋白的纯化(MBP-RACK1蛋白多步纯化-离子)
融合MBP蛋白的纯化(MBP-RACK1蛋白多步纯化-分子筛)
融合MBP蛋白的纯化(双标签:MBP-His6)
收藏:几种常用的蛋白标签

收藏:⼏种常⽤的蛋⽩标签后台有同学在问看⽂献时遇到很多的标签蛋⽩,不知是啥。
其实,在我们研究某个蛋⽩的功能的时候,我们期待能够定位它或研究蛋⽩相互作⽤,有⼀种⽅法就是将⼀个通过各种⽅法可以检测到的标签蛋⽩的基因和⽬标蛋⽩的基因进⾏重组融合,那产⽣的融合蛋⽩除了⽬标蛋⽩本⾝,同时会带上可检测的标签蛋⽩,这样⽬标蛋⽩也被⼀并检测到,今天我们⼀起来盘点那些标签蛋⽩。
♣GST标签蛋⽩GST(⾕胱⽢肽巯基转移酶) 标签蛋⽩本⾝是⼀个在解毒过程中起重要作⽤的转移酶,天然⼤⼩为26KD。
应⽤于原核表达的原因有两个,⼀是因为它是⼀个⾼度可溶的蛋⽩,可以⽤来增加外源蛋⽩的可溶性;另⼀原因是它可以在⼤肠杆菌中⼤量表达,提⾼表达量。
GST融合表达系统⼴泛应⽤于各种融合蛋⽩的表达,可以在⼤肠杆菌和酵母菌等宿主细胞中表达。
结合的融合蛋⽩在⾮变性条件下⽤10mM 还原型⾕胱⽢肽洗脱。
在⼤多数情况下,融合蛋⽩在⽔溶液中是可溶的,并形成⼆体。
GST标签可⽤酶学分析或免疫分析很⽅便的检测。
标签有助于保护重组蛋⽩免受胞外蛋⽩酶的降解并提⾼其稳定性。
在⼤多数情况下GST融合蛋⽩是完全或部分可溶的。
纯化:该表达系统表达的GST标签蛋⽩可直接从细菌裂解液中利⽤含有还原型⾕胱⽢肽琼脂糖凝胶(Glutathionesepharose)亲和树脂进⾏纯化。
GST标签蛋⽩可在温和、⾮变性条件下洗脱,因此保留了蛋⽩的抗原性和⽣物活性。
GST在变性条件下会失去对⾕胱⽢肽树脂的结合能⼒,因此不能在纯化缓冲液中加⼊强变性剂如:盐酸胍或尿素等。
如果要去除GST融合部分,可⽤位点特异性蛋⽩酶切除。
检测:可⽤GST抗体或表达的⽬的蛋⽩特异性抗体检测。
♣His6标签蛋⽩His6标签蛋⽩是六个组氨酸残基组成的融合标签,可插⼊在⽬的蛋⽩的C末端或N末端。
当某⼀个标签的使⽤,⼀是能构成表位利于纯化和检测;⼆是构成独特的结构特征(结合配体)利于纯化。
组氨酸残基侧链与固态的镍有强烈的吸引⼒,可⽤于固定化⾦属螯合层析(IMAC),对重组蛋⽩进⾏分离纯化。
His标签融合蛋白

默克生命科学服务热线:400 820 8872 bioteam@
高纯度包涵体的制备 以下操作可用于任何 BugBuster®系列产品抽提的包涵体纯化。 1. 如可溶蛋白抽提步骤1-4进行操作。 2. 将步骤“4”所得到的沉淀重悬于BugBuster(货号70584),BugBuster的量与当初重悬细胞糊的体积相同。
重复两次。再次重悬,于4℃,16,000g离心15分钟并去除上清。 7. 重悬最终的沉淀(即纯化的包涵体)于选定的缓冲液,最好是能与后续纯化方法兼容的缓冲液。包涵体可以
重悬于Novagen的蛋白重折叠试剂盒(货号70123)中的1×溶解缓冲液(参考操作手册TB234)或其它变性 剂。不溶的His•Tag®融合蛋白可以用含有变性剂的1×结合缓冲液重悬用于His•Bind®纯化(IDA或NTA)。
产品使用说明书
His·Tag 融合蛋白纯化操作手册
*建议同时参考本说明书英文原文(说明书编号TB273)。
采用 pET 系统进行原核蛋白表达,蛋白的表达量达到 20mg/100ml 培养物并不是困难的事。 在大肠杆菌中表达的目的蛋白,其可溶性(可溶蛋白或包涵体)、细胞定位(细胞质、细胞周 质、培养基上清),都会对后续的纯化策略造成影响。我们建议研究者在蛋白表达后,首先进 行目的蛋白的细胞定位(请参考 pET 系统操作手册);在进行大量纯化之前,小量纯化蛋 白,摸索确定适合于具体蛋白的纯化条件,也是值得推荐的好方法。外源蛋白在大肠杆菌中表 达,可能以可溶形式存在,也可能以包涵体形式存在。尤其在高水平表达的条件下,更容易形 成包涵体。包涵体的形成与外源蛋白本身性质、载体、宿主菌、以及表达水平都有关系,可以 通过选择不同表达载体和 E.coli 宿主菌组合,摸索生长条件和适宜诱导条件,达到优化蛋白表 达的目的。His·Tag®融合蛋白,可以在天然条件或变性条件下用 NTA His·Bind 树脂或 IDA His·Bind 树脂进行纯化。
融合蛋白的标签

重组蛋白表达技术现已经广泛应用于生物学各个具体领域, 特别是体内功能研究和蛋白质的大规模生产都需要应用重组蛋白表达载体。
蛋白表达载体按照表达宿主的不同分为3类,分别为表达宿主为大肠杆菌,哺乳动物细胞的,以及慢病毒载体,宿主可以为哺乳动物细胞和原代细胞。
当某一个标签的使用,一是能构成表位利于纯化和检测;二是构成独特的结构特征(结合配体)利于纯化。
除了必要的复制和筛选的元件,协助表达和翻译的元件外,本文将6个标签的功能初步介绍如下:(一) His 6His6是指六个组氨酸残基组成的融合标签,可插入在目的蛋白的C末端或N末端。
组氨酸残基侧链与固态的镍有强烈的吸引力,可用于固定化金属螯合层析(IMAC),对重组蛋白进行分离纯化。
使用His-tag有下面优点:1.标签的分子量小,只有~0.84KD,而GST和蛋白A分别为~26KD和~30KD,一般不影响目标蛋白的功能;2.His标签融合蛋白可以在非离子型表面活性剂存在的条件下或变性条件下纯化,前者在纯化疏水性强的蛋白得到应用,后者在纯化包涵体蛋白时特别有用,用高浓度的变性剂溶解后通过金属螯和亲和层析去除杂蛋白,使复性不受其它蛋白的干扰,或进行金属螯和亲和层析复性;3.His标签融合蛋白也被用于蛋白质-蛋白质、蛋白质-DNA相互作用研究;4.His标签免疫原性相对较低,可将纯化的蛋白直接注射动物进行免疫制备抗体;5.可应用于多种表达系统,纯化的条件温和;6.可以和其它的亲和标签一起构建双亲和标签。
(二) FlagFlag标签蛋白为编码8个氨基酸的亲水性多肽(DYKDDDDK),同时载体中构建的Kozak序列使得带有FLAG的融合蛋白在真核表达系统中表达效率更高。
Flag 作为标签蛋白,其融合表达目的蛋白后具有以下优点:1. Flag 作为融合表达标签,其通常不会与目的蛋白相互作用并且通常不会影响目的蛋白的功能、性质,这样就有利用研究人员对融合蛋白进行下游研究。
重组蛋白融合标签及对应的酶切酶

重组蛋白融合标签及对应的酶切酶一、概述重组蛋白是一种人工合成的蛋白质,通常用于生物技术和药物研发领域。
在研究和应用中,为了更好地研究和分析重组蛋白,通常需要在其N端或C端连接不同的标签,以便于对其进行纯化、检测和定位等操作。
而对于大多数重组蛋白而言,酶切酶是一个重要的工具,它可以通过切割特定的肽键来去除标签或实现蛋白质的精确裁剪。
重组蛋白融合标签及对应的酶切酶是重要的研究话题。
二、重组蛋白融合标签1. His标签His标签是一种常用的重组蛋白融合标签,它通常由6个组氨酸构成,其序列为His-His-His-His-His-His。
这种标签能够与金属离子亲和层析柱上的镍离子结合,便于对融合蛋白进行纯化。
常用的His标签融合蛋白包括His-tag、GST-His-tag等。
对应的酶切酶包括Thrombin、Enterokinase等,可以在需要的时候精确切割掉His标签。
2. FLAG标签FLAG标签是另一种常用的重组蛋白融合标签,它是一个八肽序列,其序列为DYKDDDDK。
FLAG标签常用于蛋白质检测和免疫印迹等分析中。
常用的FLAG标签融合蛋白包括pET21a-FLAG、CMV-FLAG等。
对应的酶切酶为Enterokinase等,可实现对FLAG标签的精确切割。
3. GFP标签GFP标签是一种表达在绿色荧光蛋白上的重组蛋白融合标签,其序列与GFP蛋白的序列相同,能够使融合蛋白在荧光显微镜下直接观察到。
常用的GFP标签融合蛋白包括pGFP、pGFP-V-RS等。
对应的酶切酶为Bgl II等。
4. HA标签HA标签是一种可溶酶敏感的蛋白质标签,其序列为YPYDVPDYA。
HA标签常用于蛋白质的免疫检测、纯化等。
对应的酶切酶为Enterokinase等。
5. Myc标签Myc标签是另一种常用的重组蛋白融合标签,其序列为EQKLISEEDL。
Myc标签常用于免疫印迹、免疫沉淀等研究中。
对应的酶切酶为Enterokinase等。
融合标签技术在蛋白质研究中的应用

融合标签技术在蛋白质研究中的应用摘要近年来,越来越多的科学家开始运用一种被称为融合标签的技术来研究蛋白质。
融合标签技术的快速发展给蛋白的快速纯化带来了福音。
本文主要介绍一些常用融合标签的原理、优缺点以及它们在蛋白质研究中的应用,并讨论了融合标签对蛋白研究产生的深远影响。
关键词蛋白质融合标签蛋白纯化前言蛋白质相互作用存在于每个细胞的新陈代谢过程中。
围绕着中心法则,我们可以发现,DNA复制、转录、逆转录、翻译等少不了蛋白质的参与,而且在细胞的信号转导,细胞死亡和凋亡等生命活动中,蛋白质的相互作用也都发挥了核心作用。
对蛋白质的研究,催生了结构生物学的蓬勃发展,而且,蛋白质相互作用的研究也成为了蛋白质研究不可或缺的一部分[1]。
利用蛋白质表达技术,快速、简便地进行有关活性代谢产物的高效表达而研究蛋白质生物学功能和理化性质成为一种很好的研究方法。
其中融合蛋白表达技术由于容易实现高效表达、纯化,兼有步骤简便、产物多以活性形式存在等优点,在蛋白质研究中得到了广泛的应用[2]。
蛋白融合即在蛋白序列上加上蛋白标签。
蛋白标签是指利用DNA重组技术与目的蛋白一起融合表达的一种多肽或蛋白质,以便于目的蛋白的表达、检测以及纯化[3]。
该技术的原理是通过基因操作技术,将目的基因片段与某些特定的蛋白标签串联,插入适当的载体中进行表达。
这些特定的基因因为带有标签,能够与特殊的介质进行亲和层析,使特定的蛋白能够纯化出来。
得到的融合蛋白还可以通过使用化学物质或者酶类的特定反应切除标签,从而得到纯化的目的蛋白,用于结晶或者特定功能研究。
常用的融合蛋白主要包括多聚组氨酸标记、硫氧还原蛋白、谷胱甘肽S-硫转移酶(GST)、融合了八个氨基酸的亲水性多肽、麦芽糖结合蛋白等。
根据其分子量大小,可将之分为两类:小的多肽标签,包括FLAG、His6(六聚组氨酸)、c-myc(人c-myc蛋白表位)、HA(流感病毒血凝素表面抗原决定簇)等;大的蛋白标签,包括SPA(葡萄球菌蛋白A)、GST(谷胱甘肽巯基转移酶)和GFP (绿色荧光蛋白)等。
融合蛋白标签

在蛋白质功能及结构研究过程中,研究的首要任务就是利用多种方法获得纯化的具有完整结构及生物学功能并能够正确折叠的高度纯化蛋白质。
除了蛋白质的研究,具有特定生物活性的高价值蛋白质的生产也需要对蛋白质产品进行纯化。
因此,科研人员和工业生产往往大量采用多种多样的表达系统来获得高表达的蛋白质,对其纯化后进行研究或加工,这些表达系统包括原核表达系统、酵母菌表达系统、昆虫动物细胞表达系统、真核细胞表达系统等。
如何将系统中表达的目标蛋白质与其他蛋白分离,一直是表达纯化中的一个重点。
为了克服从复杂样品中纯化单一蛋白质这种困难,科学家利用生物物质,特别是酶和抗体等蛋白质,具有识别某种特定物质并与该物质分子特异性结合的能力,利用生物分子间的这种特异性结合能力而形成的亲和纯化技术。
亲和标签纯化技术已广泛应用于蛋白质,特别是重组蛋白的分离纯化中。
在重组蛋白的亲和纯化中,利用基因工程技术,将经过改造优化的亲和标签与目标蛋白融合表达,通过一步简单快速的亲和层析,直接获得纯度较高的重组融合蛋白,已成为重组蛋白纯化的一个通用方法,具有结合特异性高、纯化步骤简便、纯化条件温和、适用性广泛等优点,为蛋白质的有效纯化提供了一条解决的途径,广泛应用于蛋白质结构与功能的研究及重组蛋白纯化工艺的开发中。
自从20世纪70年代中期融合标签技术出现以来,亲和标签已成为一种重组蛋白纯化十分有效的工具,具有结合特异性高、纯化条件温和、纯化步骤简便、适用性广泛等显着优势。
通常,亲和标签定义为对特定的生物或化学配基具有高度亲和力的一段氨基酸序列。
到目前为止,已经出现了种类众多、功能各异、用途多样的亲和标签,极大地促进了对重组蛋白的有效纯化。
根据自身分子量大小的不同,亲和标签可以分为两大类:一类是结合固定化配基的短肽标签,如His-tag、FLAG-tag、Strep-tagⅡ等;另一类是识别小分子配基的蛋白标签,如GST、MBP等。
短肽标签:His-tag:His标签是目前高通量蛋白纯化最普遍使用的亲和标签,广泛用于多种重组蛋白在各种表达系统的表达与纯化中。
蛋白融合pdi标签的用途

蛋白融合pdi标签的用途蛋白融合PDI标签的用途蛋白质折叠是生物学中一个重要的过程,它指的是蛋白质从线性氨基酸序列折叠成特定的三维结构的过程。
这个过程对于蛋白质功能的发挥非常重要,因为只有在正确的三维结构下,蛋白质才能发挥其生物学功能。
然而,蛋白质折叠的过程并不总是顺利进行,有时会出现错误的折叠或聚集,导致蛋白质失去功能或形成有害的聚集物。
为了解决这个问题,科学家们开发了一种蛋白质标签——蛋白质融合PDI标签,用于监测和促进蛋白质折叠的正确进行。
蛋白质融合PDI标签是一种蛋白质融合标签,其中PDI代表蛋白质二硫醇异构酶(protein disulfide isomerase)。
PDI是一种在内质网(endoplasmic reticulum,ER)中广泛存在的蛋白质,它在蛋白质折叠的过程中起着重要的作用。
蛋白质融合PDI标签利用了PDI的功能,将其与目标蛋白质融合,以监测和促进目标蛋白质的正确折叠。
蛋白质融合PDI标签的主要用途之一是在蛋白质表达和纯化过程中监测蛋白质折叠的质量。
蛋白质的折叠质量对于蛋白质的功能和稳定性至关重要,因此在表达和纯化过程中对折叠质量进行监测是必要的。
通过将PDI标签与目标蛋白质融合,可以利用PDI的二硫醇异构酶活性来检测目标蛋白质的折叠状态。
如果目标蛋白质折叠正确,PDI标签将保持在目标蛋白质上;而如果目标蛋白质折叠出现错误,PDI标签将与目标蛋白质分离。
通过监测PDI标签的状态,可以及时发现蛋白质折叠的问题,并采取相应的措施进行修复或改进。
除了在蛋白质表达和纯化中的应用,蛋白质融合PDI标签还可以用于研究蛋白质折叠的机制和调控。
蛋白质折叠是一个复杂的过程,涉及到许多分子和细胞机制的相互作用。
通过将PDI标签与不同的蛋白质融合,可以研究PDI在折叠过程中的作用和调控机制。
此外,还可以利用PDI标签来筛选和鉴定与蛋白质折叠有关的分子和药物,以及探索蛋白质折叠与疾病之间的关联。
常见tag蛋白标签

蛋白标签(protein tag)是指利用DNA体外重组技术,与目的蛋白一起融合表达的一种多肽或者蛋白,以便于目的蛋白的表达、检测、示踪和纯化等。
常用的蛋白标签有6xHIS、Flag、GST、Myc、eGFP/eCFP/eYFP/mCherryeGFP、HA、SUMO等。
TrxHISHis6是指六个组氨酸残基组成的融合标签,可插入在目的蛋白的C末端或N末端。
当某一个标签的使用,一是能构成表位利于纯化和检测;二是构成独特的结构特征(结合配体)利于纯化。
组氨酸残基侧链与固态的镍有强烈的吸引力,可用于固定化金属螯合层析(IMAC),对重组蛋白进行分离纯化。
使用His-tag有下面优点:•标签的分子量小,只有~0.84KD,而GST和蛋白A分别为~26KD和~30KD,一般不影响目标蛋白的功能;•His标签融合蛋白可以在非离子型表面活性剂存在的条件下或变性条件下纯化,前者在纯化疏水性强的蛋白得到应用,后者在纯化包涵体蛋白时特别有用,用高浓度的变性剂溶解后通过金属螯和亲和层析去除杂蛋白,使复性不受其它蛋白的干扰,或进行金属螯和亲和层析复性;•His标签融合蛋白也被用于蛋白质-蛋白质、蛋白质-DNA相互作用研究;•His标签免疫原性相对较低,可将纯化的蛋白直接注射动物进行免疫并制备抗体。
•可应用于多种表达系统,纯化的条件温和;•可以和其它的亲和标签一起构建双亲和标签。
•eCFPeCFP标签蛋白为增强型青色荧光蛋白eCFP,激发波长为433nm或453nm,发射波长为475nm或501nm,其是由野生型青色荧光蛋白CFP通过氨基酸突变和密码子优化而来的。
相对于CFP,eCFP荧光强度更强、荧光性质更稳定。
同时载体中构建的Kozak序列使得含有eCFP的融合蛋白在真核表达系统中表达效率更高。
eCFP作为标签蛋白,其融合表达目的蛋白后具有以下优点:•不用破碎组织细胞和不加任何底物,直接通过荧光显微镜就能在活细胞中发出绿色荧光,实时显示目的基因的表达情况,而且荧光性质稳定,被誉为活细胞探针。
FLAG标签融合蛋白纯化试剂盒使用说明书

FLAG标签融合蛋白纯化试剂盒使用说明书FLAG标签(DYKDDDDK)融合蛋白纯化试剂盒Cat#:KAP0064(本品仅用于科学研究,不可用于诊断及治疗)1.背景信息Flag-Tag(DYKDDDDK),常用于真核蛋白质重组表达标记。
FLAG标签(DYKDDDDK)融合蛋白纯化试剂盒,主要成分是Anti-Flag亲和纯化凝胶(Anti-DYKDDDDK (Flag) Affinity Gel),由高品质的Flag兔多克隆抗体与Sepharose 4B琼脂糖颗粒共价偶联制成,具有高载量(至少为1.2mg protein/ml凝胶),高特异性,性质稳定,可反复使用的特点,可用于Flag 标签融合蛋白的亲和纯化。
2.性能指标应用范围:可用于Met修饰的N端Flag融合蛋白(Met-Flag–Protein),N端Flag融合蛋白(Flag–Protein)和C端Flag融合蛋白(Protein-Flag)的亲和纯化。
载量:1ml Sepharose 4B琼脂糖颗粒,共价偶联800μg Anti-Flag 兔多克隆抗体,可纯化至少1.2mg Flag融合蛋白。
强度:重力柱纯化,可反复使用5次以上。
保存方法:在加入了50%甘油和0.2‰叠氮钠的PBS保存液后,预装纯化柱可于-20℃可保存1年。
3.试剂盒组成50 mM Tris HCl, pH 7.4, 150 mMNaCl, 1 mM EDTA, and 1%Triton X-100(说明见5.3)4.使用方法4.1细胞裂解液制备4.1.1悬浮细胞和半贴壁细胞从细胞培养瓶上吹下来后放入离心管中,1000rpm离心5分钟。
贴壁细胞用细胞刮子轻轻从瓶壁上刮下来,放入离心管中1000rpm离心5分钟。
4.1.2预冷的PBS工作液重悬细胞,1000rpm离心3min,弃上清。
重复一次。
4.1.3根据细胞的量加入相应体积的细胞裂解液,反复吹打后冰上放置10-20min,让细胞充分裂解。
融合蛋白名词解释

融合蛋白名词解释
融合蛋白(fusion protein)是由两个或多个不同的蛋白质序列
融合在一起形成的新的蛋白质分子。
融合蛋白可以由自然界中发现的已存在的蛋白质芯片和外部与之连接的序列组成。
融合蛋白通常由两个重要组分组成:信号序列(signal sequence)和标签序列(tag sequence)。
信号序列通常位于蛋
白质的N端(氨基末端)并起到引导蛋白质进入细胞内的作用,使其能够成功表达。
标签序列位于蛋白质的C端(羧基
末端),用于检测和纯化融合蛋白。
融合蛋白有多种应用。
一方面,融合蛋白可以用于重组蛋白的表达和纯化。
通过将目标蛋白与特定的标签蛋白序列融合,可以方便地利用标签的亲和性手段(如亲和色谱和免疫沉淀)从复杂的混合物中高效地纯化目标蛋白。
此外,融合蛋白还可以提高目标蛋白在大肠杆菌等常用表达宿主中的可溶性和稳定性,从而增加目标蛋白的表达量。
另一方面,融合蛋白还可用于生物学研究和药物开发。
通过将目标蛋白与其他功能蛋白(如酶、抗体、光敏色素等)融合,可以赋予目标蛋白新的性质和功能。
例如,将荧光蛋白与目标蛋白融合,可以实现对目标蛋白在细胞内或组织中的定位和追踪。
此外,融合蛋白还可用于开发新型的药物靶点和治疗方法,通过改变融合蛋白的结构和功能,可以实现对特定疾病相关的蛋白靶点的选择和干预。
总之,融合蛋白是一种重要的工具蛋白,广泛应用于蛋白表达、
纯化、生物学研究和药物开发等领域。
融合蛋白的设计和构建应考虑到目标蛋白的结构和功能,以及融合蛋白与目标蛋白之间的相互作用,从而实现对蛋白的定位、纯化和功能调控。
融合蛋白标签

在蛋白质功能及结构研究过程中,研究的首要任务就是利用多种方法获得纯化的具有完整结构及生物学功能并能够正确折叠的高度纯化蛋白质。
除了蛋白质的研究,具有特定生物活性的高价值蛋白质的生产也需要对蛋白质产品进行纯化。
因此,科研人员和工业生产往往大量采用多种多样的表达系统来获得高表达的蛋白质,对其纯化后进行研究或加工,这些表达系统包括原核表达系统、酵母菌表达系统、昆虫动物细胞表达系统、真核细胞表达系统等。
如何将系统中表达的目标蛋白质与其他蛋白分离,一直是表达纯化中的一个重点。
为了克服从复杂样品中纯化单一蛋白质这种困难,科学家利用生物物质,特别是酶和抗体等蛋白质,具有识别某种特定物质并与该物质分子特异性结合的能力,利用生物分子间的这种特异性结合能力而形成的亲和纯化技术。
亲和标签纯化技术已广泛应用于蛋白质,特别是重组蛋白的分离纯化中。
在重组蛋白的亲和纯化中,利用基因工程技术,将经过改造优化的亲和标签与目标蛋白融合表达,通过一步简单快速的亲和层析,直接获得纯度较高的重组融合蛋白,已成为重组蛋白纯化的一个通用方法,具有结合特异性高、纯化步骤简便、纯化条件温和、适用性广泛等优点,为蛋白质的有效纯化提供了一条解决的途径,广泛应用于蛋白质结构与功能的研究及重组蛋白纯化工艺的开发中。
自从20世纪70年代中期融合标签技术出现以来,亲和标签已成为一种重组蛋白纯化十分有效的工具,具有结合特异性高、纯化条件温和、纯化步骤简便、适用性广泛等显著优势。
通常,亲和标签定义为对特定的生物或化学配基具有高度亲和力的一段氨基酸序列。
到目前为止,已经出现了种类众多、功能各异、用途多样的亲和标签,极大地促进了对重组蛋白的有效纯化。
根据自身分子量大小的不同,亲和标签可以分为两大类:一类是结合固定化配基的短肽标签,如His-tag、FLAG-tag、Strep-tagⅡ等;另一类是识别小分子配基的蛋白标签,如GST、MBP等。
短肽标签:His-tag:His标签是目前高通量蛋白纯化最普遍使用的亲和标签,广泛用于多种重组蛋白在各种表达系统的表达与纯化中。
标签蛋白融合技术概述从分子生物学基础和生化基础到商...

标签蛋白融合技术概述:从分子生物学基础和生化基础到商用系统K. Terpe摘要: 随着蛋白质组学的迅猛发展,重组蛋白质的使用在近年来大大增加。
重组杂合体含有一个多肽融合担体也就是亲和标签可用于辅助目标蛋白的纯化,这已经被广泛使用。
许多不同的蛋白质,结构域或者肽类能与目标蛋白融合。
利用融合蛋白的有助于重组蛋白纯化和检测这个优点被广泛赞同。
然而,很难选择正确的纯化系统用于特定的目标蛋白。
本综述概述了使用最频繁的和有趣的系统:精氨酸标签(Arg-tag),钙调蛋白结合肽(calmodulin-binding peptide),纤维素结合结构域(cellulose-binding domain),DsbA,c-myc-tag,谷胱甘肽S -巯基转移梅(glutathione S-transferase), FLAGtag,HAT-tag, His-tag, 麦芽糖结合蛋白(maltose-binding protein), NusA, Stag,SBP-tag, Strep-tag,和硫氧还蛋白等。
引言生产高度纯化和性状确切的重组蛋白质已成为在医药工业工作的蛋白质化学家的主要任务,近年来,一些抗原表位的肽类和蛋白质已被用于大量生产重组蛋白质。
这些亲和标签系统具有以下特征:(a)一步的吸附纯化,(b)对三级结构和生物活性影响小,(c)可方便且专一的去除以产生天然蛋白质,(d)在纯化过程中重组蛋白的分析简便准确,(e)适用于大量的不同蛋白质。
然而,每一个亲和标签都在其特定的缓冲液条件下纯化得到(表1)。
因此有几种不同的策略用于大规模生产重组蛋白质。
其中一种办法是使用很小的肽标签,这些标签不会与融合的蛋白质发生干扰。
使用最为广泛的有多聚精氨酸,FLAG-,多聚组氨酸-, c-myc-, S-, and Strep II-tag. 对于某些应用,小标签无需去除。
这些标签不像大标签具有免疫原性,经常可以直接作为抗原用于产生抗体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
在蛋白质功能及结构研究过程中,研究的首要任务就是利用多种方法获得纯化的具有完整结构及生物学功能并能够正确折叠的高度纯化蛋白质。
除了蛋白质的研究,具有特定生物活性的高价值蛋白质的生产也需要对蛋白质产品进行纯化。
因此,科研人员和工业生产往往大量采用多种多样的表达系统来获得高表达的蛋白质,对其纯化后进行研究或加工,这些表达系统包括原核表达系统、酵母菌表达系统、昆虫动物细胞表达系统、真核细胞表达系统等。
如何将系统中表达的目标蛋白质与其他蛋白分离,一直是表达纯化中的一个重点。
为了克服从复杂样品中纯化单一蛋白质这种困难,科学家利用生物物质,特别是酶和抗体等蛋白质,具有识别某种特定物质并与该物质分子特异性结合的能力,利用生物分子间的这种特异性结合能力而形成的亲和纯化技术。
亲和标签纯化技术已广泛应用于蛋白质,特别是重组蛋白的分离纯化中。
在重组蛋白的亲和纯化中,利用基因工程技术,将经过改造优化的亲和标签与目标蛋白融合表达,通过一步简单快速的亲和层析,直接获得纯度较高的重组融合蛋白,已成为重组蛋白纯化的一个通用方法,具有结合特异性高、纯化步骤简便、纯化条件温和、适用性广泛等优点,为蛋白质的有效纯化提供了一条解决的途径,广泛应用于蛋白质结构与功能的研究及重组蛋白纯化工艺的开发中。
自从20世纪70年代中期融合标签技术出现以来,亲和标签已成为一种重组蛋白纯化十分有效的工具,具有结合特异性高、纯化条件温和、纯化步骤简便、适用性广泛等显著优势。
通常,亲和标签定义为对特定的生物或化学配基具有高度亲和力的一段氨基酸序列。
到目前为止,已经出现了种类众多、功能各异、用途多样的亲和标签,极大地促进了对重组蛋白的有效纯化。
根据自身分子量大小的不同,亲和标签可以分为两大类:一类是结合固定化配基的短肽标签,如His-tag、FLAG-tag、Strep-tagⅡ等;另一类是识别小分子配基的蛋白标签,如GST、MBP等。
短肽标签:His-tag:His标签是目前高通量蛋白纯化最普遍使用的亲和标签,广泛用于多种重组蛋白在各种表达系统的表达与纯化中。
His标签一般为5~15个组氨酸,被认为是重组蛋白纯化的首选标签,具有以下优点:(1)位于目标蛋白N端的His 标签与细菌的转录翻译机制相互兼容,利于蛋白的表达;(2)His标签几乎不影响目标蛋白的理化性质;(3)His标签很小,不会改变目标蛋白的可溶性;(4)His标签在目标蛋白结晶后对蛋白结构几乎没有影响;(5)采用固定化金属离子亲和层析纯化His标签融合蛋白时,其操作非常简便。
基于上述优点,几乎所有的大型结构基因组研究中心都把纯化His标签融合蛋白的固定化金属离子亲和层析(immobilized metal-ion affinity chromatography,IMAC)作为主要的蛋白纯化方法。
然而,并不是所有的蛋白质都可以与His标签融合后,采用固定化金属离子亲和层析分离纯化。
宿主蛋白中含有半胱氨酸及天然发生的组氨酸丰富区域,在固定化金属离子亲和层析时可能会导致其他蛋白的非特异性结合;目标蛋白含有金属离子,一般也不采用His标签与固定化金属离子亲和层析。
FLAG-tag:除了His标签外,另一个广泛使用的小分子短肽标签是FLAG标签。
FLAG标签是由8个氨基酸(DYKDDDDK)组成的一个短肽,分子量很小,因而不会遮盖融合蛋白中其他的蛋白表位与结构域,也不会改变融合蛋白的功能、分泌或运输。
该标签具有天然的亲水特性,很容易定位于融合蛋白的表面,便于利用抗体检测;同时含有一个肠激酶切割位点(DDDK),可以利用肠激酶切除标签。
FLAG标签有3个特异性的单克隆抗体,分别为M1单抗、M2单抗、M5单抗。
FLAG短肽合成成本较高,不适用于大规模纯化,且需要额外步骤除去结合在层析介质上的短肽。
Strep-tag Ⅱ:与His-tag、FLAG-tag相似,Strep-tag Ⅱ也是一个小分子的短肽标签,广泛用于多种目标蛋白在原核表达系统、哺乳动物细胞表达系统等的表达与纯化中。
在自然界中,链霉亲和素(streptavidin)与生物素(biotin)之间存在着非常强烈的非共价相互作用,其生物学上的解离常数极低;即使生物素与其他蛋白质共价结合之后,两者仍可以相互作用。
基于这两者之间的强烈相互作用,运用一系列蛋白质工程手段,通过对短肽文库的筛选,第一个链霉亲和素结合肽应运而生,即Strep-tag,极大地方便了重组蛋白的一步快速亲和纯化。
然而,Strep-tag 与链霉亲和素结合时需要一个自由的羧基末端,因而该标签只能位于目标蛋白的C端,限制了它的应用范围。
在Strep-tag的基础上,通过对合成短肽的筛选,获得了一个与其相似、由8个氨基酸(WSHPQFEK)组成的链霉亲和素结合肽,即Strep-tagⅡ,可以位于融合蛋白的任意位置,从而弥补了Strep-tag的不足。
同时,通过对链霉亲和素特定氨基酸的定向突变,获得了与Strep-tagⅡ具有更高亲和力的亲和介质Strep-tactin,在Strep-tagⅡ融合蛋白的亲和纯化中表现出良好的纯化效果,且蛋白质产量较高,所需成本适中。
Strep-tagⅡ系统的纯化条件比较宽泛,在普通缓冲液下就可与strep-Tactin层析介质结合,使用2.5mmol/L的脱硫生物素就可将Strep-tagⅡ融合蛋白洗脱下来,螯合剂、去污剂、还原剂及高达1mol/L的盐均可加入到缓冲液中。
此外,Strep-tag Ⅱ在纯化过程中不依赖金属离子,十分适合含金属离子蛋白质的纯化。
蛋白标签:GST:GST标签由211个氨基酸组成,大小约为26kDa,是目前广泛用于重组蛋白融合表达与亲和纯化的一种蛋白标签。
大量的表达实验发现,外源蛋白在大肠杆菌表达系统中过量表达时,常会以包涵体的形式形成不溶性的聚合体,大大降低了可溶性重组蛋白的产量,增加了后续蛋白分离纯化的难度。
然而,在融合GST标签进行原核表达的过程中发现,原本用于亲和纯化的GST标签能在一定程度上增大融合蛋白的可溶性,使融合蛋白以可溶形式存在于细胞质中,不仅促进了目标蛋白的正确折叠,提高了蛋白产量,而且有助于后续的蛋白纯化。
除了增大融合蛋白的可溶性之外,GST标签还具有高效的翻译起始、纯化条件温和、亲和树脂成本相对低廉等显著优点,成为重组蛋白融合表达经常使用的亲和标签。
MBP:MBP标签由大肠杆菌K12的malE基因编码的396个氨基酸组成,大小约为40kDa,是除了GST标签之外又一个很好的增大融合蛋白可溶性的蛋白标签。
MBP标签能够增大在原核表达系统中过量表达的融合蛋白的可溶性,提高其表达量,已在多个表达实验中得到确认。
研究发现,当改变MBP“开放”与“关闭”构象之间的平衡时,MBP增大融合蛋白可溶性的能力将受到明显影响,表明MBP增大融合蛋白可溶性的特性是由其“开放”构象所介导;同时,对MBP 配基结合间隙中保守的疏水性氨基酸残基进行定向突变,MBP表现出相似的表型,表明这个配基结合间隙在MBP增大融合蛋白可溶性的机制中具有一定的作用。
然而,从蛋白纯化的角度来看,MBP标签并不是一个最有效的亲和标签;在某些情况下,MBP标签并不能特异性地与亲和树脂有效结合,亲和层析后融合蛋白的纯度也并不合适。
自从上世纪70年代中期亲和标签融合技术出现以来,多种多样的短肽或蛋白亲和标签极大地方便了外源表达重组蛋白的分离与蛋白质复合体的纯化,已成为蛋白质研究领域不可或缺的工具。
一般而言,一个完美的亲和标签应该具备以下特性:(1)能够用于纯化任何表达宿主或表达系统所表达的重组蛋白;(2)可以位于目标蛋白的任意位置而不影响其结构;(3)增大目标蛋白的可溶性,促进其正确折叠,提高蛋白表达量;(4)便于重组蛋白的检测。
目前,商品化的亲和标签已具备其中诸多特性,但性能更加优越、纯化效果更加显著的亲和标签仍需不断寻找与开发。
重组蛋白表达技术现已经广泛应用于生物学各个具体领域。
特别是体内功能研究和蛋白质的大规模生产都需要应用重组蛋白表达载体。
美国GeneCopoeia的蛋白表达载体按照表达宿主的不同新推出3类,分别为表达宿主为大肠杆菌,哺乳动物细胞的,以及慢病毒载体,宿主可以为哺乳动物细胞和原代细胞。
除了必要的复制和筛选的元件,协助表达和翻译的元件外,本文将各类载体分别按照功能标签的不同确定种类并将个标签的功能初步介绍如下:His6:His6是指六个组氨酸残基组成的融合标签,可插入在目的蛋白的C末端或N 末端。
当某一个标签的使用,一是能构成表位利于纯化和检测;二是构成独特的结构特征(结合配体)利于纯化。
组氨酸残基侧链与固态的镍有强烈的吸引力,可用于固定化金属螯合层析(IMAC),对重组蛋白进行分离纯化。
使用His-tag有下面优点:1.标签的分子量小,只有~0.84KD,而GST和蛋白A分别为~26KD和~30KD,一般不影响目标蛋白的功能;2.His标签融合蛋白可以在非离子型表面活性剂存在的条件下或变性条件下纯化,前者在纯化疏水性强的蛋白得到应用,后者在纯化包涵体蛋白时特别有用,用高浓度的变性剂溶解后通过金属螯和亲和层析去除杂蛋白,使复性不受其它蛋白的干扰,或进行金属螯和亲和层析复性;3.His标签融合蛋白也被用于蛋白质-蛋白质、蛋白质-DNA相互作用研究;4.His标签免疫原性相对较低,可将纯化的蛋白直接注射动物进行免疫制备抗体;5.可应用于多种表达系统,纯化的条件温和;6.可以和其它的亲和标签一起构建双亲和标签。
Flag:Flag标签蛋白为编码8个氨基酸的亲水性多肽(DYKDDDDK),同时载体中构建的Kozak序列使得带有FLAG的融合蛋白在真核表达系统中表达效率更高。
FLAG作为标签蛋白,其融合表达目的蛋白后具有以下优点:1.FLAG作为融合表达标签,其通常不会与目的蛋白相互作用并且通常不会影响目的蛋白的功能、性质,这样就有利用研究人员对融合蛋白进行下游研究。
2.融合FLAG的目的蛋白,可以直接通过FLAG进行亲和层析,此层析为非变性纯化,可以纯化有活性的融合蛋白,并且纯化效率高。
3.FLAG作为标签蛋白,其可以被抗FLAG的抗体识别,这样就方便通过Western Blot、ELISA等方法对含有FLAG的融合蛋白进行检测、鉴定。
4.融合在N端的FLAG,其可以被肠激酶切除(DDDK),从而得到特异的目的蛋白。
因此现FLAG标签已广泛的应用于蛋白表达、纯化、鉴定、功能研究及其蛋白相互作用等相关领域。
MBP:MBP(麦芽糖结合蛋白)标签蛋白大小为40kDa,由大肠杆菌K12的malE 基因编码。
MBP可增加在细菌中过量表达的融合蛋白的溶解性,尤其是真核蛋白。
MBP标签可通过免疫分析很方便地检测。
