盐和化肥PPT课件
合集下载
盐和化肥复习PPT课件
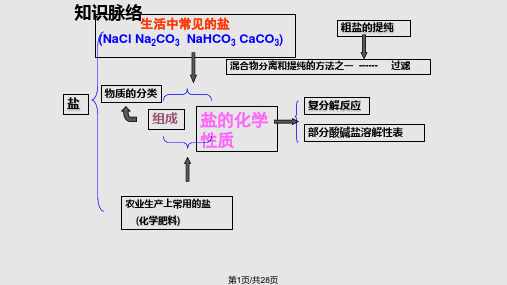
Ba(NO3)2溶 液和稀HNO3
HCl、NaCl、 AgNO3溶液 KCl、CaCl2 和稀HNO3
产生白色沉淀 白色沉淀不消失
产生白色沉淀 白色沉淀不消失
Na2CO3、 稀盐酸和澄 有无色气泡产 CaCO3、 清石灰水 生 澄清石灰水
K2CO3
变浑浊
有刺激性气味的气体
NH4HCO3 碱溶液(如NaOH) 产生气体,能使湿润的
碳酸钙
NaCl
食盐的主 要成分
作调味品,腌渍食品。医疗上 用来配制生理盐水,农业上来 选种。消除积雪。
Na2CO3
纯碱、苏打
用于生产玻璃、造纸、纺织、 洗涤剂。
NaHCO3 小苏打
发酵粉的主要成分,治疗胃 酸过多的药剂
CaCO3
大理石 石灰石主要 可用作建筑材料、补钙剂 成分
第2页/共28页
粗盐提纯
第21页/共28页
一看
<1>. N、P 、 K肥的区别 二闻
<2>. 几种氮肥的区别
第22页/共28页
三溶
CO(NH2)2 NH4Cl (NH4)2SO4 NH4NO3
Cl-、SO42- 、 CO32-、 NH4+的检验方法
离子 常见的物质 检验试剂
实验现象
SO42Cl-
CO32NH4+
H2SO4、 Na2SO4、 K2SO4
第26页/共28页
知识结构透视
常见的盐
NaCl
碳酸盐
粗盐的提纯 Na2CO3 NaHCO3 CaCO3
CO32-的检验
含金属离子(包括NH4+)和酸根离子的化合物
盐
复分解反应
概念 发生条件
生活中常见的盐及化学肥料PPT课件

一单元盐化肥
生活中常见的盐及化学肥料
1、了解食盐、纯碱、小苏打、碳酸钙 等盐在日常生活中的用途 2、知道一些化肥的名称和作用
氯化钠:俗称 食盐 碳酸钠:俗称 纯碱、苏打 面碱、口碱 碳酸氢钠:俗称 小苏打 碳酸钙:主要以大理石和 石灰石的形式存 在于自然界中
化肥的种类:
氮肥:氨 水、 碳酸氢铵、硫酸铵 NH3· H2O NH4HCO3 (NH4)2SO4 氯化铵、 硝酸铵、 尿 素 NH4Cl NH4NO3 CO(NH2)2
7、亚硝酸钠(化学式NaNO2)是一种外观极像食盐 且具有食盐一样咸味的有毒物质,因此这种工业 用盐常被冒充食盐掺假或被误作食盐食用,导致 多起中毒事故发生。请你阅读下表并结合已有化 学知识,用三种方法鉴别亚硝酸钠和氯化钠。
8、可用于除去氢氧化钠溶液中 混有少量碳酸钠的试剂是 A.氢氧化钙溶液 B.盐酸 C.氯化钡溶液 D.氯化钠溶液 答案:( A )
×××化学工业公司
5、⑴某学生家乡出现水稻倒伏现象,他通过 调查研究,发现主要原因是缺少 钾 肥,建议 4 农民适量施用草木灰或 KCl或K2SO (填化学式) ⑵大棚种植蔬菜在冬季需补充二氧化碳。某同学 在自家大棚内设计了补充二氧化碳的方法:将工 业废硫酸用水稀释后,盛放在塑料桶内,悬挂在 高处。每天向桶内加适量的碳酸氢铵,它和硫酸 反应生成硫酸铵、二氧化碳和水。 ①写出该反应的化学方程式:
钾肥:硫酸钾、 氯化钾 K2SO4 KCl 磷肥:磷矿粉、 钙镁磷肥、过磷酸钙
CO32-的鉴别: 试剂:稀盐酸和澄清石灰水 现象:产生气泡 澄清石灰水变浑浊
1、农作物栽培中使用的化肥种 类很多。下列属于复合肥料的 A.KNO3 C.NH4Cl B.CO(NH2)2 D.NH4HCO3 答案:( A )
生活中常见的盐及化学肥料
1、了解食盐、纯碱、小苏打、碳酸钙 等盐在日常生活中的用途 2、知道一些化肥的名称和作用
氯化钠:俗称 食盐 碳酸钠:俗称 纯碱、苏打 面碱、口碱 碳酸氢钠:俗称 小苏打 碳酸钙:主要以大理石和 石灰石的形式存 在于自然界中
化肥的种类:
氮肥:氨 水、 碳酸氢铵、硫酸铵 NH3· H2O NH4HCO3 (NH4)2SO4 氯化铵、 硝酸铵、 尿 素 NH4Cl NH4NO3 CO(NH2)2
7、亚硝酸钠(化学式NaNO2)是一种外观极像食盐 且具有食盐一样咸味的有毒物质,因此这种工业 用盐常被冒充食盐掺假或被误作食盐食用,导致 多起中毒事故发生。请你阅读下表并结合已有化 学知识,用三种方法鉴别亚硝酸钠和氯化钠。
8、可用于除去氢氧化钠溶液中 混有少量碳酸钠的试剂是 A.氢氧化钙溶液 B.盐酸 C.氯化钡溶液 D.氯化钠溶液 答案:( A )
×××化学工业公司
5、⑴某学生家乡出现水稻倒伏现象,他通过 调查研究,发现主要原因是缺少 钾 肥,建议 4 农民适量施用草木灰或 KCl或K2SO (填化学式) ⑵大棚种植蔬菜在冬季需补充二氧化碳。某同学 在自家大棚内设计了补充二氧化碳的方法:将工 业废硫酸用水稀释后,盛放在塑料桶内,悬挂在 高处。每天向桶内加适量的碳酸氢铵,它和硫酸 反应生成硫酸铵、二氧化碳和水。 ①写出该反应的化学方程式:
钾肥:硫酸钾、 氯化钾 K2SO4 KCl 磷肥:磷矿粉、 钙镁磷肥、过磷酸钙
CO32-的鉴别: 试剂:稀盐酸和澄清石灰水 现象:产生气泡 澄清石灰水变浑浊
1、农作物栽培中使用的化肥种 类很多。下列属于复合肥料的 A.KNO3 C.NH4Cl B.CO(NH2)2 D.NH4HCO3 答案:( A )
盐和化肥.ppt

的产 。
5、常见的盐
氯化钠(NaCl) • 白色晶体,易溶于水,有咸味,水溶液
呈中性
• 化工原料,用于生产氯气,烧碱,作调 味品,参与正常的生理活动,生理盐水 为0.9%的氯化钠溶液。
• 海水晒盐制粗盐,粗盐经过溶解,过滤, 蒸发可得精盐。
5、常见的盐
• 碳酸钠(Na2CO3) • 白色晶体,易溶于水,水溶液有涩味和滑
水溶液中析出的蓝色晶体为(CuSO4•5H2O) 俗称胆矾或蓝矾 • 精练铜,镀铜,配制杀菌剂波尔多液
盐
6、通过化学加工生产的肥料称为化学肥料(简称化
肥)。使用化肥可以促进农作物增产,解决粮食问题。
常用的化肥可以分成
肥(铵态和硝态),
肥,
肥,复合肥料,和微量肥料。
举例:
7、碳酸盐的检验: 铵盐的检验:
二、常见盐的物理性质
3。结晶水合物: 许多物质从水溶液里析出晶体时,晶体
里常含有一定数目的水分子,这样的水 分子叫做结晶水。含有结晶水的物质叫 做结晶水合物。 结晶水合物里的水分子属于结晶水合物 化学固定组成的一部分。结晶水合物属 于纯净物。
二、常见盐的物理性质
3。结晶水合物: 常见结晶水合物 五水合硫酸铜 胆矾(或蓝矾) CuSO4·5H2O 二水合硫酸钙 石膏 CaSO4·2H2O 七水合硫酸亚铁 绿矾 FeSO4·7H2O 十二水合硫酸铝钾 明矾 KAl(SO4)2·12H2O 十水合碳酸钠 石碱 Na2CO3·10H2O
一般来说盐都可以看作 中和反应 的产物。
如:
。ห้องสมุดไป่ตู้
3、盐的分类:根据盐的组成可将盐分成:
二、常见盐的物理性质
1。大多数盐常温下都是无色晶体,但有 些盐有颜色。
最新中考复习--- 盐和化学肥料(共19张PPT)教育课件

【例题1】
下列每组物质中,化学式和俗称不相匹配的是 ( C )
A. NaOH 烧碱 C. K2CO3 草木灰
B. Na2CO3 纯碱 D. CaO 生石灰
【例题2】
下列化肥中,从外观即可与其他化肥相区别的是 ( C )
A.硫酸钾
B.硝酸铵
C.磷矿粉
D.氯化钾
【例题3】对盐的组成叙述正确的是( B )
凡事都是多棱镜 ,不同的角度会
凡事都 是多棱镜,不同的角度会看到不同的结果。若能把一些事看淡了,就会有个好心境 ,若把很多事看开了,就会 有个好心情。让聚散离合犹如月缺月圆那样寻常,让得失利弊犹如花开花谢那样自 然,不计较,也不刻意执着 ;让生命中各种的喜怒哀乐,就像风儿一样,来了,不管是清风拂面,还是寒风凛冽,都报以自然的微笑,坦然的接受命运的馈赠,把是非曲折,都当作是人生的定数,不因攀比而困惑,不为贪婪而费神,无论欢乐还是忧伤,都用平常心去接受;无论得到还是失去,都用坦然的心去面对,人生原本就是在得与失中轮回的,让一切所有的经历,都化作脸上的云淡风轻。
溶于水
能力
钾肥
白色固体, 能溶于水
促进植物生长,增 强抗病虫害和抗倒 伏能力
硫酸钾、氯化钾
复合肥
含有两种及 两种以上营 养元素
能同时供给作物几 种养分
硝酸钾、磷酸二氢铵等
说明:化肥的作用可简记为“氮钾磷,叶茎根”。
(2)铵态氮肥的性质
应用:常利用此性质检验铵态氮肥。 应用:常利用此性质检验铵态氮肥。(NH4+的检验)
根据上述实验,下列说法错误的是( C ) A. X物质为尿素 B. Y物质为碳酸氢铵 C.常温下如要鉴别Y、Z两种样品,能采取闻气味的方法 D.如果实验Ⅱ中Y、Z两种样品没有另取,则会使检验结果不准确
盐与化肥课件

AgCl↓+NaNO3 Na2CO3+CaCl2
CaCO3↓+2NaCl
考点聚焦
反应发生的条件
①反应物盐须可溶; ②反应物金属须比生成物金属的活泼性强; ③K、Ca、Na 与盐溶液中的盐不发生置换
①反应物盐 BaSO4、AgCl 等除外; ②生成物须符合复分解反应发生的条件
①两反应物须都溶于水; ②生成物须符合复分解反应发生的条件
返回目录
基础整合
考点聚焦
3.化肥的简易鉴别 氮肥
看外观
钾肥 白色晶体
加水
全部溶于水
加熟石 灰 研磨
放出具有刺激性气味的氨 气
无具有刺激性气味的氨气 放出
磷肥 灰白色粉状 大多不溶于
水 或部分溶于
水
铵态氮肥不能与碱性物质混合使用,因 N 与 OH-能发生反应,放出 NH3, 降低肥效。
返回目录
基础整合
基础整合
考点聚焦
第十一单元 盐 化肥
返回目录
基础整合
考点聚焦
一、盐
1.常见的盐
常见 的盐
氯化钠
碳酸钠
碳酸氢钠
俗称
食盐
纯碱、苏打
小苏打
化学 式
NaCl
Na2CO3
NaHCO3
生活调味品、配制 玻璃、造纸、纺织 发酵粉、治疗
用途 生理盐水、农业选 和洗涤剂的生产
种等
等
胃酸过多等
组成
上的 共同
一般都含有金属离子和酸根离子
,b
。
(4)乙同学提出可用如图指导进行物质的制备:请写出 2 个有关硫酸亚铁生成的化学反 应方程式:
; 。
返回目录
基础整合
考点聚焦
CaCO3↓+2NaCl
考点聚焦
反应发生的条件
①反应物盐须可溶; ②反应物金属须比生成物金属的活泼性强; ③K、Ca、Na 与盐溶液中的盐不发生置换
①反应物盐 BaSO4、AgCl 等除外; ②生成物须符合复分解反应发生的条件
①两反应物须都溶于水; ②生成物须符合复分解反应发生的条件
返回目录
基础整合
考点聚焦
3.化肥的简易鉴别 氮肥
看外观
钾肥 白色晶体
加水
全部溶于水
加熟石 灰 研磨
放出具有刺激性气味的氨 气
无具有刺激性气味的氨气 放出
磷肥 灰白色粉状 大多不溶于
水 或部分溶于
水
铵态氮肥不能与碱性物质混合使用,因 N 与 OH-能发生反应,放出 NH3, 降低肥效。
返回目录
基础整合
基础整合
考点聚焦
第十一单元 盐 化肥
返回目录
基础整合
考点聚焦
一、盐
1.常见的盐
常见 的盐
氯化钠
碳酸钠
碳酸氢钠
俗称
食盐
纯碱、苏打
小苏打
化学 式
NaCl
Na2CO3
NaHCO3
生活调味品、配制 玻璃、造纸、纺织 发酵粉、治疗
用途 生理盐水、农业选 和洗涤剂的生产
种等
等
胃酸过多等
组成
上的 共同
一般都含有金属离子和酸根离子
,b
。
(4)乙同学提出可用如图指导进行物质的制备:请写出 2 个有关硫酸亚铁生成的化学反 应方程式:
; 。
返回目录
基础整合
考点聚焦
《盐和化肥(ppt)》课件 2022年人教版省一等奖PPT

·人教版
第14课时 │ 归类示例
(4)乙同学提出可用此图指导进行物质的制备,请写出2个 有关硫酸亚铁生成的化学反应方程式。
答:__Fe_+__H__2S_O__4=_=_=_F_e_S_O__4+__H__2↑_______________________; __F_e_O_+__H_2_S_O_4_=_=_=_F_e_S_O_4_+__H_2_O_________________________。
磷矿粉、钙镁磷肥、过 磷酸钙
硫酸钾(K2SO4)、氯化 钾(KCl)
硝酸钾(KNO3)、磷酸二 氢铵(NH4H2PO4)
作用
促进作物茎、叶的生长 茂盛、叶色浓绿(叶)
促进根系发达,增强抗 寒、抗旱能力 (根) 促进作物生长健壮,茎
秆粗硬 (茎) 同时供给几种养分,有
效成分高
·人教版
第14课时 │ 考点聚焦
·人教版
第14课时 │ 归类示例
► 类型三 复分解反应发生的条件 命题角度:给出反应物和生成物,判断是否能发生
复分解反应。 例3 根据复分解反应发生的条件,并利用下表所提供的 信息,判断下列物质间能否发生复分解反应。如能发生反应, 写出反应的化学方程式;如不能发生反应,请注明“不能”。
·人教版
第14课时 │ 归类示例
·人教版
第14课时 │ 归类示例
► 类型二 粗盐的提纯 命题角度:用粗盐来制备NaCl的实验操作。 例2 [2010·镇江]某兴趣小组进行粗盐提纯并配制
NaCl溶液,请回答下列问题:
·人教版
第14课时 │ 归类示例
(1)操作①、②、③依次为图14-3中的(填字母)_C_、__B_、__A_ 。
图14-3
第14课时 │ 盐和化肥
第14课时 │ 归类示例
(4)乙同学提出可用此图指导进行物质的制备,请写出2个 有关硫酸亚铁生成的化学反应方程式。
答:__Fe_+__H__2S_O__4=_=_=_F_e_S_O__4+__H__2↑_______________________; __F_e_O_+__H_2_S_O_4_=_=_=_F_e_S_O_4_+__H_2_O_________________________。
磷矿粉、钙镁磷肥、过 磷酸钙
硫酸钾(K2SO4)、氯化 钾(KCl)
硝酸钾(KNO3)、磷酸二 氢铵(NH4H2PO4)
作用
促进作物茎、叶的生长 茂盛、叶色浓绿(叶)
促进根系发达,增强抗 寒、抗旱能力 (根) 促进作物生长健壮,茎
秆粗硬 (茎) 同时供给几种养分,有
效成分高
·人教版
第14课时 │ 考点聚焦
·人教版
第14课时 │ 归类示例
► 类型三 复分解反应发生的条件 命题角度:给出反应物和生成物,判断是否能发生
复分解反应。 例3 根据复分解反应发生的条件,并利用下表所提供的 信息,判断下列物质间能否发生复分解反应。如能发生反应, 写出反应的化学方程式;如不能发生反应,请注明“不能”。
·人教版
第14课时 │ 归类示例
·人教版
第14课时 │ 归类示例
► 类型二 粗盐的提纯 命题角度:用粗盐来制备NaCl的实验操作。 例2 [2010·镇江]某兴趣小组进行粗盐提纯并配制
NaCl溶液,请回答下列问题:
·人教版
第14课时 │ 归类示例
(1)操作①、②、③依次为图14-3中的(填字母)_C_、__B_、__A_ 。
图14-3
第14课时 │ 盐和化肥
初中化学《盐和化肥》PPT课件

三. 粗盐的提纯
1、主要步骤: 溶解 、 过滤 、 蒸发 。
2、主要仪器: 铁架台(带铁圈)、 烧杯、玻璃棒 、蒸发皿、 酒精灯 、 漏斗 、 量筒 。
3、玻璃棒的作用:溶解时起 搅拌(加速溶解) 作用;过滤时起
引流 作用;蒸发时起 搅拌(防止液滴飞溅) 作用。
4、过滤时的操作要领: 一贴 、 二低 、 三靠 。
CD中白A..HF和色Ne2K2Ha发物H点NONCN酵 质OO盐H燃Ol332过是3+酸++N程KBKHFa2.O产C2eCCNOHCO生al3—l3H3—的溶—=CN—=酸O不液=a32,能2SNKCO又aN.O4能O溶CH3a引+液溶(OC起O液H发2N)F↑2泡ae+(CDH作O.l2溶OHN用a)液,(3C沉l这B淀种)
肥的种类 熟,穗粒增多,籽粒饱满。 碳重酸过钾磷酸K钙2CO3
钾肥: 含钾元素的肥料 能促使作物生长健壮、茎杆
硫酸钾 K2SO4
粗硬,增强抗病虫害和抗倒 氯化钾 KCl
伏能力等功能,并能促进糖
分和淀粉的生成。 复合肥:同两时 种含以两上种营或养
元素的肥料
磷酸二氢铵 NH4H2PO4
磷酸氢二铵 (NH4)2HPO4
四. 化学肥料
尿素 CO(NH2)2
氮肥: 含氮元素的肥料
氨水 NH3•H2O
氮肥能促进植物茎、叶铵盐 NH4NO3等 生长茂盛、叶色浓绿。 磷矿粉 Ca3(PO4)2
磷肥:含磷元素的肥料 促进作物生长,增强抗寒、抗
过磷酸钙 Ca(H2PO4)2
1、常见化 旱能力,还能促进作物提早成 和CaSO4混合物
磷酸二氢钾 KH2PO4
硝酸钾
KNO3
四. 化学肥料
常见的盐和化肥PPT课件讲义

碳酸氢铵 碳碳铵铵
17.7%
硝酸铵 硫酸铵 氯化铵 硝 硝铵 铵 肥 肥田 田粉 粉
35% 21.2% 26.2%
讨论:
• 为什么铵态氮肥不能与熟石灰、草木灰等 碱性物质混合使用?
• 怎样在实验室用简单方法检验铵盐?
铵根的检验:
1、把少量待测物和熟石灰粉末放在一起研磨, 若产生刺激性臭味的气体,则有铵根存在。 2、把少量待测溶液和氢氧化钠溶液混合加热, 若产生能使湿润的红色石蕊试纸变蓝的气体, 则有铵根存在。
或用玻璃棒沾浓氨水置于试管口(有大量的白烟) 干燥:碱石灰
不能用无水CaCl2、P2O5、浓硫酸干燥。
课外拓展:
2、有机氮肥——尿素:CO(NH2 )2 白色晶体
含氮量高,肥效持久,对土壤没有不良影响, 是一种优质氮肥。
3、氮肥、磷肥、钾肥的区别
氮肥
钾肥
看外观
白色晶体
加水
全部溶于水
加熟石灰 放出有刺激性气 无刺激
2)装置 固+固加热型(同O2)
3)收集:向下排空气法 4) 检验:湿润的红色石蕊试纸 (变蓝)或用玻璃棒沾浓氨水置于试管口(有量的白烟) 5) 干燥:碱石灰
不能用无水CaCl2、P2O5、浓硫酸干燥。
注意:消石灰不能用KOH、NaOH代替
• 问题想1:一如想何鉴: 别下列4种物质
NH4NO3、Na2SO4、 (NH4)2SO4、NaNO3
农家肥料
常含多种营养元素, 营养元素含量较小。
一般易溶于水, 易于被作物吸收,
肥效较快。
便于工业生产,成本较高。
有些品种化肥如长期 大量施用能使土壤板结。
一般较难溶于水,经腐熟 后逐步转化为可溶于水、 能被作物吸收的物质,肥
常见的盐和化肥ppt课件

1、俗称:食盐 (生活中的盐与化学中的盐) 2、存在:海水、盐湖、井盐、盐矿;
3、制取:晾晒海水,煮井盐水、盐湖水,开 采盐矿;
4、用途:调味、腌渍食品、生理盐水、化工 原料(制取碳酸钠、氢氧化钠、和盐酸等)
选种、化雪盐。
NaCl + NH3 + CO2 +H2O = NaHCO3↓+ NH4Cl
通电
玻璃棒 的作用
搅拌、引流、搅拌
加速溶解
防止受热不均匀使 液体溅出
烧 伤 病 人 的 治疗通 常是取 烧伤病 人的健 康皮肤 进行自 体移植 ,但对 于大面 积烧伤 病人来 讲,健 康皮肤 很有限 ,请同 学们想 一想如 何来治 疗该病 人
过滤后滤液仍浑浊的原因:
⑴过滤时滤纸破损。 ⑵倾倒液体时,液面超过滤纸边缘。 ⑶仪器不干净
的气体
不燃烧, 跳动或有
爆炸声
无明显变 化
磷肥
灰白色粉末 大多不溶或部
分溶于水 无明显变化
无明显变化
使湿润的红色石蕊试纸变蓝
烧 伤 病 人 的 治疗通 常是取 烧伤病 人的健 康皮肤 进行自 体移植 ,但对 于大面 积烧伤来治 疗该病 人
三、其它常见的盐
1、硫酸铜(CuSO4) 白色固体,溶于水得到蓝色溶液,无水硫酸铜 在实验中常用来检验水的存在。
CuSO4·5H2O 俗名:胆矾、蓝矾 CuSO4 +2NaOH = Cu(OH)2↓ + Na2SO4
CuSO4 + BaCl2 = CuCl2 + BaSO4↓
用途:有毒,农业上与熟石灰配制波尔多液杀 虫剂,游泳池常用其做消毒剂,精炼铜 的原料。
按金属元素分类:钠盐、钾盐、亚铁盐
按酸根分类:碳酸盐、盐酸盐、硫酸盐
3、制取:晾晒海水,煮井盐水、盐湖水,开 采盐矿;
4、用途:调味、腌渍食品、生理盐水、化工 原料(制取碳酸钠、氢氧化钠、和盐酸等)
选种、化雪盐。
NaCl + NH3 + CO2 +H2O = NaHCO3↓+ NH4Cl
通电
玻璃棒 的作用
搅拌、引流、搅拌
加速溶解
防止受热不均匀使 液体溅出
烧 伤 病 人 的 治疗通 常是取 烧伤病 人的健 康皮肤 进行自 体移植 ,但对 于大面 积烧伤 病人来 讲,健 康皮肤 很有限 ,请同 学们想 一想如 何来治 疗该病 人
过滤后滤液仍浑浊的原因:
⑴过滤时滤纸破损。 ⑵倾倒液体时,液面超过滤纸边缘。 ⑶仪器不干净
的气体
不燃烧, 跳动或有
爆炸声
无明显变 化
磷肥
灰白色粉末 大多不溶或部
分溶于水 无明显变化
无明显变化
使湿润的红色石蕊试纸变蓝
烧 伤 病 人 的 治疗通 常是取 烧伤病 人的健 康皮肤 进行自 体移植 ,但对 于大面 积烧伤来治 疗该病 人
三、其它常见的盐
1、硫酸铜(CuSO4) 白色固体,溶于水得到蓝色溶液,无水硫酸铜 在实验中常用来检验水的存在。
CuSO4·5H2O 俗名:胆矾、蓝矾 CuSO4 +2NaOH = Cu(OH)2↓ + Na2SO4
CuSO4 + BaCl2 = CuCl2 + BaSO4↓
用途:有毒,农业上与熟石灰配制波尔多液杀 虫剂,游泳池常用其做消毒剂,精炼铜 的原料。
按金属元素分类:钠盐、钾盐、亚铁盐
按酸根分类:碳酸盐、盐酸盐、硫酸盐
盐和化肥 ppt课件

6.2 盐和肥料
一、盐是中和反应的产物
▪ 写出氢氧化钠和盐酸、氢氧化钠与硫酸反应的化学 方程式
▪ NaOH + HCl → NaCl + H2O ▪ 2NaOH + H2SO4 → Na2SO4 + 2H2O ▪ 盐可以看作酸中的氢被金属元素取代后的产物 ▪ HCl、 H2SO4 被Na取代→ NaCl 、 Na2SO4 ▪ HCl、 H2SO4 被Mg取代→ MgCl 2、 MgSO4 ▪ 同一种金属可以取代不同酸中的氢
▪ 1、盐的组成:金属(包括铵根)+ 酸根
一、盐是中和反应的产物 2、盐的分类
(1)按盐的组成进行分类
钠盐Na 钾盐K 铵盐NH4 铜盐Cu
盐酸盐Cl
碳酸盐 CO3 硝酸盐 NO3 硫酸盐 SO4
NaCl Na2CO3 NaNO3 Na2SO4
KCl
NH4Cl
CuCl2
K2CO3 (NH4)2CO3 CuCO3 KNO3 NH4NO3 Cu(NO3)2
CuSO4 + BaCl2 → BaSO4 ↓ + CuCl2
CuSO4 + Fe
△
CuSO4·5H2O
Cu + FeSO4 CuSO4 + 5H2O
(2)硫酸盐——硫酸铜 ②用途:
▪ 干燥剂 ▪ 检验水的存在:白色粉末变成蓝色晶体 ▪ 杀菌剂 :把CuSO4与Ca(OH)2混合制成的
农药,其杀菌效率比单用CuSO4高,而对 作物的药害较小。因该农药首先在法国的 波尔多使用,故取名“波尔多液” ▪ 镀铜、制铜及铜的化合物
CuSO4 + 5H2O
CuSO4·5H2O
※ 白色的硫酸铜粉末可以用来检验水
一、盐是中和反应的产物
▪ 写出氢氧化钠和盐酸、氢氧化钠与硫酸反应的化学 方程式
▪ NaOH + HCl → NaCl + H2O ▪ 2NaOH + H2SO4 → Na2SO4 + 2H2O ▪ 盐可以看作酸中的氢被金属元素取代后的产物 ▪ HCl、 H2SO4 被Na取代→ NaCl 、 Na2SO4 ▪ HCl、 H2SO4 被Mg取代→ MgCl 2、 MgSO4 ▪ 同一种金属可以取代不同酸中的氢
▪ 1、盐的组成:金属(包括铵根)+ 酸根
一、盐是中和反应的产物 2、盐的分类
(1)按盐的组成进行分类
钠盐Na 钾盐K 铵盐NH4 铜盐Cu
盐酸盐Cl
碳酸盐 CO3 硝酸盐 NO3 硫酸盐 SO4
NaCl Na2CO3 NaNO3 Na2SO4
KCl
NH4Cl
CuCl2
K2CO3 (NH4)2CO3 CuCO3 KNO3 NH4NO3 Cu(NO3)2
CuSO4 + BaCl2 → BaSO4 ↓ + CuCl2
CuSO4 + Fe
△
CuSO4·5H2O
Cu + FeSO4 CuSO4 + 5H2O
(2)硫酸盐——硫酸铜 ②用途:
▪ 干燥剂 ▪ 检验水的存在:白色粉末变成蓝色晶体 ▪ 杀菌剂 :把CuSO4与Ca(OH)2混合制成的
农药,其杀菌效率比单用CuSO4高,而对 作物的药害较小。因该农药首先在法国的 波尔多使用,故取名“波尔多液” ▪ 镀铜、制铜及铜的化合物
CuSO4 + 5H2O
CuSO4·5H2O
※ 白色的硫酸铜粉末可以用来检验水
盐和化肥-课件

㈥ 酸性氧化物 + 碱=盐 + 水
反应条件:碱溶于水 练习: ⑴ CO2+NaOH─
⑵ CO2 + Ca(OH)2─ ⑶ SO2 + KOH─ ⑷ SO3 + Ba(OH)2─ ⑸ CO2 + Cu(OH)2 ─
正确答案:
⑴ CO2 + 2NaOH=Na2CO3 + H2O ⑵ CO2 + Ca(OH)2=CaCO3 + H2O ⑶ SO2 +2 KOH=K2SO3 + H2O ⑷ SO3 + Ba(OH)2=BaSO4 + H2O ⑸ CO2 + Cu(OH)2─××××
㈡ 碱 + 盐 = 新盐 +新碱
反应条件: 反应物都溶于水, 生成物中有沉淀出现。
练习:⑴Cu(OH)2 + Na2SO4─ ⑵NaOH + BaCl2─ ⑶CuCl2 + NaOH─ ⑷Ca(OH)2 + K2CO3─ ⑸NaOH + FeCl3─
正确答案:
⑴ Cu(OH)2+ Na2SO4─××× ⑵ NaOH + BaCl2─××× ⑶ 2NaOH + CuCl2=Cu(OH)2 + 2NaCl ⑷ Ca(OH)2 + Na2CO3=CaCO3 + 2NaOH ⑸ 3NaOH + FeCl3=Fe(OH)3 + 3NaCl
•
16、业余生活要有意义,不要越轨。2021/3/42021/3/4Marc h 4, 2021
•
17、一个人即使已登上顶峰,也仍要 自强不 息。2021/3/42021/3/42021/3/42021/3/4
谢谢观赏
You made my day!
盐-盐与化肥-PPT课件

阅读:P26候氏制碱法
农作物生长需要较多的是N、P、K 元素,土壤中常缺乏N、P、K,肥料 来源可分为有机肥和化肥。
“庄稼一枝花, 全靠肥当家”
四、盐与化肥
思考1:什么是化肥?
化学肥料是用矿物质、空气、水等作原 料,经过化学加工精制而成的肥料(简 称化肥)。
思考2:化肥有哪些类型 氮肥: 化肥主要含有氮元素的称氮肥如:NH4NO3 磷肥:化肥主要含有磷元素的称磷肥如:Ca3PO4 钾肥: 化肥主要含有钾元素的称钾肥如:KCl 复合肥化: 肥中含有两种或两种以上主要营养
①碳铵
A. 磷肥
a. 促进作物穗多粒满
②尿素 ③硫酸钾 ④磷酸二氢铵 ⑤重钙
B. 氮肥 C. 复合肥 D. 钾肥
b. 促进作物抗病能力 c. 促进作物茎叶生长
⑥钙镁磷肥
二. 三类常见的化肥
【例2】下列氮肥中,氮元素是质量分数最 大的是 (D )
A 氯化铵 B 硫酸铵 C 硝酸铵 D 尿素
【做一做】某硫酸铵化肥混有另一种氮肥,测 得该硫酸铵化肥中氮元素的质量分数为35%, 则其中混有的另一种氮肥可能是 ( D )
A 12
B 13 C 2 3 D 3 4
2. 下列属于复合肥料的是 (A D)
A. KH2PO4 B. K2CO3 C.NH4NO3 D. KNO3
3. 草木灰是农家肥料,其主要成分是碳酸钾, 它属于 ( C )
A 氮肥
B 磷肥
C 钾肥
D 复合肥料
【例1】将下列左项、中项、右项相关的项目用线 连接起来。
比一比,谁想的多!
制取盐的可能途经:
1、金属+酸——盐+氢气
2、酸+金属氧化物——盐+水 3、酸+碱——盐+水 4、酸+盐——新酸+新盐 5、碱+盐——新碱+新盐 6、碱+酸性氧化物——盐+水 7、金属+盐——新金属+新盐 8、盐+盐——新盐+新盐
农作物生长需要较多的是N、P、K 元素,土壤中常缺乏N、P、K,肥料 来源可分为有机肥和化肥。
“庄稼一枝花, 全靠肥当家”
四、盐与化肥
思考1:什么是化肥?
化学肥料是用矿物质、空气、水等作原 料,经过化学加工精制而成的肥料(简 称化肥)。
思考2:化肥有哪些类型 氮肥: 化肥主要含有氮元素的称氮肥如:NH4NO3 磷肥:化肥主要含有磷元素的称磷肥如:Ca3PO4 钾肥: 化肥主要含有钾元素的称钾肥如:KCl 复合肥化: 肥中含有两种或两种以上主要营养
①碳铵
A. 磷肥
a. 促进作物穗多粒满
②尿素 ③硫酸钾 ④磷酸二氢铵 ⑤重钙
B. 氮肥 C. 复合肥 D. 钾肥
b. 促进作物抗病能力 c. 促进作物茎叶生长
⑥钙镁磷肥
二. 三类常见的化肥
【例2】下列氮肥中,氮元素是质量分数最 大的是 (D )
A 氯化铵 B 硫酸铵 C 硝酸铵 D 尿素
【做一做】某硫酸铵化肥混有另一种氮肥,测 得该硫酸铵化肥中氮元素的质量分数为35%, 则其中混有的另一种氮肥可能是 ( D )
A 12
B 13 C 2 3 D 3 4
2. 下列属于复合肥料的是 (A D)
A. KH2PO4 B. K2CO3 C.NH4NO3 D. KNO3
3. 草木灰是农家肥料,其主要成分是碳酸钾, 它属于 ( C )
A 氮肥
B 磷肥
C 钾肥
D 复合肥料
【例1】将下列左项、中项、右项相关的项目用线 连接起来。
比一比,谁想的多!
制取盐的可能途经:
1、金属+酸——盐+氢气
2、酸+金属氧化物——盐+水 3、酸+碱——盐+水 4、酸+盐——新酸+新盐 5、碱+盐——新碱+新盐 6、碱+酸性氧化物——盐+水 7、金属+盐——新金属+新盐 8、盐+盐——新盐+新盐
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
常见的钾肥: 硫酸钾(K2SO4)、氯化钾(KCl)
叶尖及叶缘发黄, 甚至叶肉坏死。
4.复合肥料
复合化肥:含两种或两种以上营养元素的化肥。 如:磷酸二氢铵(NH4H2PO4)、磷酸铵氢 (NH4)2HPO4、硝酸钾(KNO3)
化肥和农药使用的利与弊:
利:化肥和农药对提高农作物的产量具有 重要作用。 弊:化肥和农药的不合理使用会带来很多 的环境问题。如土壤污染、水污染、大气 污染。
【课堂练习】
【例1】下列物质可以直接做肥料施用的是 ( B)
A. 磷酸钙 B. 氨水 C. 氢氧化钾 D. 硝酸
【课堂练习】
【例2】 下列化肥属于复合肥料的是:( C D )
A. NH4Cl C. KH2PO4
B. NH4NO3 D. KNO3
【课堂练习】
【例3】下列化肥不能与熟石灰混合施用的是 ( B)
1.氮肥
氮肥的作用: 氮是植物体内核酸、蛋白质和叶绿素的组成元素。 氮肥能促使植物的茎、叶生长茂盛,叶色浓绿。
农
作
物 缺 氮 的 表 现 :
叶 片 绿 色 减 淡
常见的氮肥:
• 尿素:CO(NH2)2 • 氨水:(NH3·H2O) • 铵盐:NH4HCO3、NH4Cl、(NH4)2SO4 • 硝酸盐:NH4NO3、NaNO3
A. 氯化钾 B. 碳酸氢铵 C. 氨水 D. 硝酸钾
【课堂练习】
【例4】某同学家中种植的植物比正常的植株矮
小瘦弱,叶片发黄,严重时叶脉呈淡棕色,你认为
应该施加下列哪一种化肥:( B )
A. 氯化钾 B. 硝酸钾 C. 过磷酸钙 D. 尿素
一句“好孩子”能让学生看到自己的进步与价值,而一句“坏孩子”学生会丧失进去的信心和斗志,甚至毁灭一生。——王玉章 卓越的人一大优点是:在不利与艰难的遭遇里百折不饶。——贝多芬 你可以用爱得到全世界,你也可以用恨失去全世界。 学习这件事,不是缺乏时间,而是缺乏努力。 最后的措手不及是因为当初游刃有余的自己 上辈子我欠你的,这辈子我来还,这辈子你欠我的,下辈子来还我。 天空黑暗到一定程度,星辰就会熠熠生辉。 吃别人吃不了的苦,忍别人受不了的气,付出比别人更多的,才会享受的比别人更多。 世界上没有比友谊更美好更令人愉快的东西了;没有友谊,世界仿佛失去了太阳。 心如镜,虽外景不断变化,镜面却不会转动,这就是一颗平常心,能景转而心不转。 你不要常常觉得自己很委曲,你应该要想,他对我这样已经很好了,这就是修行的功夫。 你微笑地看着我,不说一句话。而我知道,为了这个,我已经等了很久了。 活在当下,别在怀念过去或者憧憬未来中浪费掉你现在的生活。 不要太肯定自己的看法,这样子比较少后悔。 恋爱不是慈善事业,不能随便施舍的。感情是没有公式,没有原则,没有道理可循的。可是人们至死都还在执著与追求。
身体健康,学习进步! 为中华之崛起而读书。——周恩来
觉得自己做得到和做不到,其实只在一念之间。 我从来没有招惹你,你为什么要来招惹我?既然招惹了,为什么半途而废?
婚姻的最大杀手不是外遇或出轨,而是一地鸡毛的生活琐事。所以,平时的沟通很重要,而吵架也是另类的沟通,正所谓吵吵闹闹一辈子,不 吵不闹难白首! 记住:你是你生命的船长,走自己的路,何必在乎其它。
知识积累
①空气中虽然含有大量的氮气,但植物通常只能吸 收化合物中氮元素,不能直接吸收空气中的氮气。 ②根部有根瘤菌的豆科植物能把氮气转化为含氮 的化合物而吸收。 ③将氮气转化为氮的化合物的方法叫做氮的固定。
2.磷肥
磷是植物体内核酸、蛋白质和酶等多种重要化合物 的组成元素,参与各种重要的代谢活动,与植物的 细胞分裂、生成及有机物的转化等有密切的关系。 磷可促进作物生长,使之穗粒饱满,还可增强抗寒、 抗旱能力。
作物缺磷的表现:生长迟缓、产量降低。
常见的磷肥:
①磷矿粉:Ca3(PO4)2 ②钙镁磷肥:钙和镁的磷酸盐 ③过磷酸钙:Ca(H2PO4)2+CaSO4混合物Fra bibliotek3.钾肥
钾在植物代谢活跃的器官和组织中分布量较高。 钾具有保证各种代谢过程顺利进行、促进植物生 长、增强抗病虫害和抗倒伏能力等功能。
作物缺钾的 症状:
第十一元 盐 化肥
一、化肥简介
植物生长需要养分,土壤所能提供的养分是有限的, 因此要靠施肥来补充。最初使用的肥料是人畜粪便、 植物体等沤制的天然有机肥料。随着人们对化学元 素与植物生长关系的了解,出现了以化学和物理方 法制成的含农作物生长所需营养元素的化学肥料。 现在,施用化肥已经成为了农作物增产的最有力措 施,施用化肥的增产作用占各增产因素总和的 30%—60%。农作物所需的营养元素有许多种,其 中,氮、磷、钾的需要量较大,因此,氮肥、磷肥、 钾肥是最主要的化学肥料。
二、化肥的简易鉴别
氮肥
钾肥
磷肥
看外观 加水
灼烧
加熟石 灰
白色晶体 能溶于水
可燃烧, 熔化起泡
或冒烟 放出有刺 激性气味
的气体
白色晶体 能溶于水
不燃烧, 跳动或有
爆炸声 无明显变
化
灰白色粉末 大多不溶或部
分溶于水 无明显变化
无明显变化
铵盐与熟石灰反应:
2NH4NO3+Ca(OH)2=Ca(NO3)2+2H2O+2NH3↑ (NH4)2SO4+Ca(OH)2=CaSO4+2H2O+2NH3↑
