第六章 离子聚合与配位聚合反应
高分子化学 第6章 配位聚合
(4)配位聚合引发剂与单体
①引发剂和单体类型
Ziegler-Natta引发剂
-烯烃 有规立构聚合
二烯烃 有规立构聚合
环烯烃 -烯丙基镍型引发剂:专供丁二烯的顺、反1,4聚合 极性单体 烷基锂引发剂(均相) 有规立构聚合 二烯烃 茂金属引发剂(所有乙烯基单体)
②引发剂的相态和单体的极性
非均相引发剂,立构规整化能力强
δ +CH
Mt CH2 δ -
R
过渡金属阳离 子Mt +对烯烃 双键 碳原子的 亲电进攻
插入反应包括两个同时进行的化学过程。
单体的插入反应有两种可能的途径:
一级插入
δδ+
CH CH2 R
Mt
+
CH CH2 R
δδ+
CH CH2 CH CH2 R R
Mt
不带取代基的一端带负电荷,与过渡金属相连 接,称为一级插入。
全同1,2 、间同1,2、顺式1,4-聚丁二烯和反式 1,4-聚丁二烯。
n CH CH CH 2 CH 2 4 3 2 1
1,2加成 3,4加成
[ CH2 CH ]n CH CH2 (R)
丁二烯的1,2或3,4加成有全同和间同二种立构规整聚合物。
[ CH2 CH2 ]n C C H H
顺式1,4-聚丁二烯-1,3
最初的Ziegler-Natta引发剂由两组分构成。 主引发剂 是周期表中Ⅳ~Ⅷ过渡金属化合物。
1955年意大利的Natta改进了Ziegler引发剂。用TiCl3和烷 基金属化合物组成的配位引发剂使丙烯聚合,结果得到高相 对分子质量、高结晶度、耐热150℃的聚丙烯,并于1957年 实现了工业化。 Natta还用这些引发剂使乙烯聚合,所得到的PE无支链、 结晶度也很高, 这种PE、PP具有高的立构规整度。 Ziegler-Natta引发剂的出现使高分子科学和高分子工 业的发展有了重大突破,从而在高分子科学中开创了一 个新的研究领域----配位聚合。 Ziegler和Natta两位学者也于1963年同时获得诺贝尔 化学奖。
离子聚合和配位聚合课件

通过离子聚合和配位聚合的方法, 合成出具有特殊功能性的聚合物, 如导电聚合物、荧光聚合物等。
绿色合成路径的研究
无毒引发剂
研究无毒、环保的引发剂, 替代传统的有毒引发剂, 降低对环境的污染。
高效催化剂
研究高效、环保的催化剂, 替代传统的有毒催化剂, 降低对环境的污染。
循环利用
研究聚合物的循环利用技 术,实现聚合物的环保处 理和再利用,降低对环境 的污染。
配位聚合可以通过选择不同的 催化剂和聚合条件,实现对聚 合物分子链结构和性能的精细 调控。
配位聚合可以应用于合成高性 能纤维、功能性膜材料、液晶 材料等领域,具有广泛的应用 前景。
03
离子聚合与配位聚合的 比
聚合方式的比 较
离子聚合
通过正负离子之间的相互作用形 成聚合物链,聚合过程中无金属 催化剂参与。
配位聚合的实际应用
高性能聚合物制备
配位聚合可以合成高性能聚合物,如聚酰胺、聚酯等,用于制造 纤维、塑料和复合材料等。
高分子功能材料
通过配位聚合可以制备具有特殊功能的高分子材料,如导电聚合物、 光敏聚合物等,用于传感器、光电转换器件等领域。
高分子药物
配位聚合可以合成具有特定结构和药理性能的高分子药物,用于治 疗癌症、心血管等疾病。
配位聚合
通过过渡金属催化剂与配体形成 活性中心,再与单体进行配位反 应形成聚合物链。
聚合产物的比较
离子聚合
聚合物分子量分布较窄,但可能存在 支链和交联结构。
配位聚合
聚合物分子量分布较宽,但聚合物结 构规整,结晶度高。
应用领域的比较
离子聚合
主要用于合成橡胶、热塑性弹性体等材料。
配位聚合
广泛应用于合成纤维、塑料、涂料等领域。
第六章配位聚合

第六章 配位聚合6.1引言乙烯 丙烯和其他a-烯烃为石油裂解懂得主要产物30年代 仅作为燃料后 引发剂高温高压 PE (高压) 1953 Zieglev (德) 70~5034常压、AlEt Ti -θ HDPE 1954 Natta (意) Ti 3θ35)(GH Al - PP接着 Goodrich-Fire 公司 Ti 3524)(H C Al -θ 高顺式1、4-聚异戊二烯(天然橡胶) 同时 Fire-stene 轮胎和橡胶公司 锂或烷基锂(Z-N 引发剂)以后 以金属有机化合物-过渡金属化合物的洛合体系作引发剂单体配位而后聚合,聚合产物呈定向聚合—洛合聚合,配位聚合,定向聚合 (区别)常用术语的区别① 配位聚合和洛合为同义词—采用具有配位(或洛合)能力的引发剂,链增长(有时包括引发)都是单体先在活性种的空位上配位(洛合)并活化,然后插入烷基—金属键(R —M )中。
(配位比洛合表达的意义更明确)② 定向聚合和有规立构聚合是词义词—按IUPAC 规定,均指以形成有规立构聚合物为主的聚合过程。
③ Ziegler —Natto 聚合—指采用Ziegler —Natto 引发剂的任何单体的聚合或共聚合。
所得聚合物可以是立构规整的,也可以是无规聚合物。
6.2 结合物的立构规整性配位聚合,除R P 、n X 外,首先要考虑立构规整性问题。
异构现象—在有机化学中将分子式相同而结构不同因而性质不同的化合物叫异构体,这种现象称~分两类① 结构异构—由于分子中原子或基团相互连接次序不同引起的:如:头—尾和头—头或尾—尾相连的聚合物结构异构体② 立体异构 —由于分子中原子或基团相互连接次序不同引起的,称构型聚合物中同样存在复杂的立体异构现象⎭⎬⎫⎩⎨⎧几何异构光学异构 即:聚合物分子组成和结构相同,只是构型不同。
一、 立体异构⒈光学异构。
(存在手性中心)⎩⎨⎧*(左)右S R C )( —取代基(原子)在手性中心的排布顺序不而产生的立体异构α—烯烃聚合 NCH 2 =CH-R → —CH 2-CH-CH 2-CH-全同立构(等规)各个手性中心*C 构型相同,如~RRRR ~或~SSSS ~(St-pp)无规(at-pp ):手性中心的构型呈无规排列。
第六章 配位聚合

将侧基中含有手性C*的烯烃聚合 将侧基中含有手性C*的烯烃聚合 C*
CH2 CH *CHCH3 CH2 CH3
Et (S) CH3 CH CH2 * 2
Zn TiCl4
R / S = 50 / 50
CH2
* * CH CH2 CH *CHCH3 CH2 CH3 *CHCH3 CH2 CH3
(S = 100)
Mt CH2 δ-
过渡金属阳离子 Mtδ+ 对 烯 烃 双 键 β 碳原子的亲电进攻
插入反应包括两个同时进行的化学过程: 插入反应包括两个同时进行的化学过程:
几种聚合概念含义区别 几种聚合概念含义区别 概念
配位聚合、 配位聚合、络合聚合 在含意上是一样的, 在含意上是一样的,可互用 一般认为,配位比络合表达的意义更明确 一般认为, 配位聚合的结果: 配位聚合的结果: 可以形成有规立构聚合物 也可以是无规聚合物 定向聚合、有规立构聚合 定向聚合、 这两者是同意语, 这两者是同意语,是以产物的结构定义的 都是指以形成有规立构聚合物为主的聚合过程 乙丙橡胶的制备采用Z 催化剂,属配位聚合, 乙丙橡胶的制备采用Z-N催化剂,属配位聚合, 但结 构是无规的, 构是无规的,不是定向聚合
G. Natta
1963年 1963年,获Nobel化学奖 Nobel化学奖
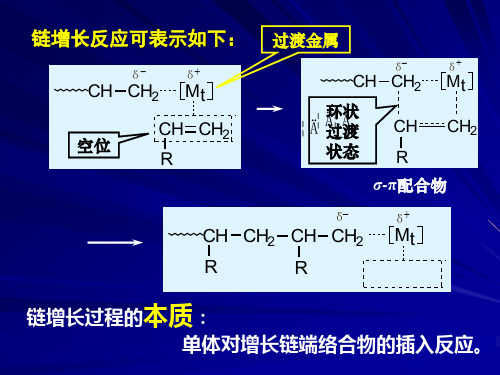
链增长反应可表示如下
过渡金属
δδ+
δ
δ+
CH CH2
空位
Mt
CH CH2 ¦¦ ¦¦ ¦ ¦
环状过 渡状态
δ
Mt CH2
CH CH2 R
CH R
δ+
CH CH2 CH CH2 R R
Mt
链增长过程的本质是单体对增长链端络合物的插入反应 链增长过程的本质是单体对增长链端络合物的插入反应 本质
3.2离子聚合和配位(聚丙烯)

b)立体规整度随引发剂不同而改变 不同引发剂生成的抗衡阴离子与增长链碳阳离 子的相互作用强度不同。 c)立体规整度以及立体规整性(全同立构亦或间同立构) 随溶剂极性不同而改变
非极性溶剂有利于立体规整度的提高。
非极性溶剂有利于全同立构的生成,而极性溶剂有利于 间同立构的生成。
阳离子聚合的工业应用 通过阳离子聚合可以合成可控制的分子量 剂分布的聚合物,同时可以获得一些特殊 结构的聚合物。 如端基为某官能团的聚合物 具有功能性悬挂基团的聚合物 嵌段聚合物 结构大单体
H2C CH X
降低电子云密度,易 与富电性活性种结合
H2C CH X
H R CH2 C X
分散负电性,稳定活性中心
X: -NO2, -CN, -COOR, -Ph, -CH=CH2
但对于一些同时具有给电子p-π共轭效应的吸电子取代基单 体,由于p-π给电子共轭效应减弱了吸电子诱导效应对双键 电子云密度的降低程度,因而不易受阴离子的进攻,不易 阴离子聚合。如:
(ii)碱金属与不饱和或芳香化合物的复合物:
如金属钠+萘引发苯乙烯聚合
- Na + Na+ 苯乙烯 ? + H2C CH Na+
H2C CH Na+ 2
Na+ - HC CH2 CH2 CH - Na+
引发聚合
电子间接转移引发
实施聚合反应时,先将金属钠与萘在惰性溶剂中反应后 再加入聚合体系引发聚合反应,属均相引发体系。
H2C CH Cl 氯乙烯 H2C CH O C CH3 O 乙酸乙烯酯
(2)羰基化合物:如HCHO
(3)杂环化合物:一般是一些含氧、氮等杂 原子的环状化合物
如:
第六章名词解释

(一)立构规整度:立构规整聚合物占聚合物总量的分率称作立构规整度。
(二)配位聚合:单体分子首先在活性种的空位上配位,形成络合物,随后单体分子相继插入
金属-烷基键中进行增长的反应。
(三)定向聚合:形成有规立构聚合物的聚合过程,又称立构规化聚合。
阳离子、阴离子聚合
也可能合成。
(四)定向聚合物:分子链具有高度立体规整性的聚合物,其性能与无规聚合物有着较大区别。
(五)配位定向聚合:一般指能生成定向聚合物的配位聚合反应。
(六)共轭双烯烃的聚合:获得高含量的顺式结构。
这是合成橡胶工业的重大进展,在此以前
是用阴离子催化剂合成的丁钠橡胶。
pcp离子型聚合和配位聚合jppt文档

特点
增长过程中来自引发剂的反离子始终处于中心阳 离子旁,形成离子对,其紧密程度与溶剂、反离 子性质、温度等有关,并影响聚合速率与分子量 。
增长过程中有的伴有分子内重排反应,异构成更 稳定的结构,通常叔碳正离子比仲碳正离子稳定 性高,伯碳正离子稳定性最低。 。
4.1.3.3 链终止
阳离子聚合的增长活性中心带有相同电荷,无法双分 子终止,因此只能通过单基终止和链转移终止。
与反离子结合发生终止反应
与 终止剂发生终止反应
通常加入水、醇、胺等质子剂来终止阳离子聚合 反应。
阳离子聚合的特征 快引发、快增长、易转移、难终止
4.1.3.4 链转移
聚合温度高时,就会明显发生链转移反应。可以向单体 链转移,也可向反离子链转移。
向单体链转移
向反离子链转移
4.1.4 阳离子聚合动力学
4.2 阴离子聚合
阴离子聚合单体 阴离子聚合引发剂 阴离子聚合的特征 活性聚合 阴离子聚合动力学 影响阴离子聚合的因素
4.2.1 阴离子聚合单体
阴离子聚合反应的通式
A B + M B M A
反应介质的影响
溶剂性质(极性或溶剂化能力)不同,离子间的结 合状态会不同,因此改变了离子对和自由离子的相 对浓度。溶剂的极性和溶剂化能力大的,自由离子 和离子对中松散对的比例都增加,结果,会使聚合 速率和聚合度都增大。
溶剂对苯乙烯正离子聚合的影响(HClO4 引发)
溶
剂
介电常数
Kp(25℃)l/mol.s
CM
kktrpM,CS
ktrS kp
X 1nkpkM t CMCS[[M S]]
在阳离子聚合中,聚合物的生成反应主要是链转 移反应,而不是链终止反应,这和自由基聚合正 好相反。
第六章 配位聚合

H C CH2 CH2 CH Mt CH2 反 式1,4-加成 加 Mt CH2
CH2
HC CH CH2
CH2
�
[Mt]+ -CH2 CH2 R
(iv)分子内转移 )
[Mt]+ -CH2 CH ( CH2 CH )nC2H5 R R [Mt]+ - -H + CH3 H2C CH R C ( CH2 CH)nC2H5 R R
[Mt]+ -CH2 CH2 R
第六章
(4)链终止 )
配 位 聚 合 反 应
羧酸, (i)醇,羧酸,胺,水等含活泼氢的化合物能与活性中心 ) 反应,使之失活: 反应,使之失活: ROH
第六章
(ii)单金属活性中心机理 )
R Cl Cl Ti Cl Cl
R CH CH3 CH2 转位 Cl Cl Ti Cl Cl
配 位 聚 合 反 应
配位 + H2C CH CH3 R Cl CH CH3 Cl Ti CH Cl Cl
Cl Cl Ti CH2CHR Cl Cl CH3 配位 CH3 CH CH2CHR CH3
第六章
6. 2 聚合反应基元反应 (1)链引发: )链引发:
配 位 聚 合 反 应
[Mt]+ - -C2H5 + H2C CH R
[Mt]+ -CH2 CH C2 H5 R
(2)链增长: )链增长:
[Mt]+ -CH2 CH C2H5 R + n H2C CH R [Mt]+ -CH2 CH ( CH2 CH )nC2H5 R R
六章节离子聚合

第六章 离子聚合
3. 其他引发剂 其它阳离子引发剂有碘、高氯酸盐、六氯化铅盐
等。如碘分子歧化成离子对,再引发聚合:
I2 I2
I+(I3)-
形成的碘阳离子可引发活性较大的单体,如对甲 氧基苯乙烯、烷基乙烯基醚等。
19
第六章 离子聚合
阳离子聚合也能通过高能辐射引发,形成自由
基阳离子,自由基进一步偶合,形成双阳离子活性
但当烷基换成芳基后,由于氧上未共有电子对也 能与芳环形成共轭,分散了双键上的电子云密度, 从而使其进行阳离子聚合的活性大大降低。
8
第六章 离子聚合
(3)共轭单体 苯乙烯,丁二烯等含有共轭体系的单体,由于
其π电子云的流动性强,易诱导极化,因此能进行 阳离子、阴离子或自由基聚合。但聚合活性较低, 远不及异丁烯和烷基乙烯基醚,故往往只作为共聚 单体应用。
6
第六章 离子聚合
更高级的α- 烯烃,由于空间位阻效应较大,一 般不能通过阳离子聚合得到高分子量聚合物。
异丁烯:唯一一个具有实际工业价值的 能进行阳离子聚合的α- 烯烃单体
7
第六章 离子聚合
(2)烷基乙烯基醚 烷氧基的诱导效应使双键电子云密度降低,但
是氧原子上的未共有电子对与双键形成 p -π共轭效 应,双键电子云增加。与诱导效应相比,共轭效应 对电子云偏移的影响程度更大。事实上,烷氧基乙 烯基醚只能进行阳离子聚合。
共引发剂过量可能生成氧鎓离子,其活性低于络 合的质子酸,使聚合速率降低。
BF3 H2O
H+(BF3OH)- H2O (H3O)+(BF3OH)-
17
第六章 离子聚合
在工业上,一般采用反应速率较为适中的AlCl3 —H2O引发体系。
离子聚合及 配位聚合

5.进行离子聚合时,一般多采用改变聚合反应温度或改变 溶剂极性的方法来控制聚合反应速度。
阴离子聚合一般为无终止聚合,所以通过引发剂的用量可 调节聚合物的相对分子质量。有时也可以加入链转移剂来调 节相对分子质量。
阳离子聚合极易发生链转移反应。链转移反应是影响聚合 物分子量的主要因素,而聚合反应温度对链转移反应的影响 很大。所以一般通过控制聚合反应温度来控制聚合物的相对 分子质量。有时也通过加入链转移剂来控制聚合物的相对分 子质量。
4 Ziegler-Natta 聚合:
采用Zigler-Natta引发剂的任何单体的聚合或共聚合。
Ziegler-Natta引发剂:
Zigler-Natta引发剂是一大类引发体系的统称,通常有两 个组份构成:主引发剂是Ⅳ~Ⅷ族过渡金属化合物。共引发剂 是Ⅰ~Ⅲ族的金属有机化合物。
5. 活性聚合:
当单体转化率达到100%时,聚合仍不终止,形成具有反 应活性聚合物(活性聚合物)的聚合叫活性聚合。
通常的测试方法有 1.沸腾正庚烷萃取法
沸腾正庚烷萃取剩余物重
聚丙烯的全同指数= (IIP)
未萃取时的聚合物总重
2. 红外光谱法(IR) 3.核磁共振法(NMR)
四、计算题
1. 以四氢呋喃为溶剂,用正丁基锂(n-C4H9Li)作为引 发剂,制备相对分子量为300 000的聚苯乙烯1000千克。
试求引发剂用量为多少千克?(已知n-C4H9Li的相对分
9. 写出合成下列聚合物的反应方程式,并注明主要反应条件。 (1)丁基橡胶
(2)SBS
(3)接近单分散的PS(GPC标样)
10. 什么是聚丙烯的全同指数?通常有哪几种测试方法? 简要说明。
高分子科学基础课件-离子聚合与配位聚合

CN
CN
4.1 陰 離 子 聚 合 反 應
再如甲基丙烯酸甲酯(MMA)陰離子聚合,其增長鏈陰
離子烯醇化後發生“尾咬”親核取代形成環己酮環末端,
而離去基團CH3O-對MMA無引發活性,使聚合反應終止:
CH3 CH2 C CH2
O C H3C
OCH 3 O
CH3 C CO2CH3 CH2
OCH 3
H2 C
如H2O對一般單體而言,不具備引發聚合活性,但對於一些 帶強吸電子取代基的1,1-二取代乙烯基,由於單體活性很高,
因此即使象H2O這樣非常弱的堿也能引發聚合,如:
CN n H2C C
H2O
CN ( CH2 C )n
CN
CN
4.1 陰 離 子 聚 合 反 應
(3)無雙基終止:由於鏈增長活性中心是負電性,相互之 間不可能發生雙基終止,只能與體系中其他的親電試劑反應 終止,如:
於陰離子的進攻,另一方面,形成的碳陰離子活性中心由於
取代基的共軛效應而穩定,因而易陰離子聚合:
H2C CH X
降低電子雲密度,易 與富電性活性種結合
H R CH 2 C
X
分散負電性,穩定活性中心
H2C CH X: -NO2, -CN, -COOR, -Ph, -CH=CH2 X
4.1 陰 離 子 聚 合 反 應
4.2 陽 離 子 聚 合 反 應
環內雙鍵也可進行陽離子聚合,如:
O
苯并呋喃
茚
-蒎烯
二聚戊二烯
CH2=CH(NRR’)和CH2=CHOR由於N和O原子上的未成對 電子能與雙鍵形成p-π共軛,使雙鍵電子雲密度增大,因 而特別活潑。
4.2 陽 離 子 聚 合 反 應
第六章离子聚合

第六章离子聚合、名称解释1. 阳离子聚合:增长活性中心为带正电荷的阳离子的连锁聚合。
2. 活性聚合:当单体转化率达到100% 时,聚合仍不终止,形成具有反应活性聚合物(活性聚合物)的聚合叫活性聚合。
3. 化学计量聚合:阴离子的活性聚合由于其聚合度可由单体和引发剂的浓度定量计算确定,因此也称为化学计量聚合。
4. 开环聚合:环状单体在引发剂作用下开环,形成线形聚合物的聚合反应。
5. Ziegler-Natta 引发剂:Zigler-Natta 引发剂是一大类引发体系的统称,通常有两个组份构成:主引发剂是W〜忸族过渡金属化合物。
共引发剂是I〜川族的金属有机化合物。
6. 配位聚合:单体与引发剂经过配位方式进行的聚合反应。
具体的说,采用具有配位(或络合)能力的引发剂、链增长(有时包括引发)都是单体先在活性种的空位上配位(络合)并活化,然手插入烷基—金属键中。
配位聚合又有络合引发聚合或插入聚合之称。
7. 定向聚合:任何聚合过程(包括自由基、阳离子、阴离子、配位聚合)或任何聚合方法(如本体、悬浮、乳液和溶液等),只要它是经形成有规立构聚合物为主,都是定向聚合。
定向聚合等同于立构规整聚合。
二、选择题1. 下列单体中哪一种最容易进行阳离子聚合反应-------------------------------------- (B )A .CH 2=CH 2 B.CH2=CHOCH 3 C.CH 2=CHCl D .CH2 =CHNO 22. 下列哪种物质不能作为阳离子聚合的引发剂---------------------------------------- (B )A .正碳离子盐B .有机碱金属C .质子酸D . Lewis酸3. 四氢呋喃可以进行下列哪种聚合-------------------------------------------- (C )A.自由基聚合 B .阴离子聚合C.阳离子聚合 D .配位聚合4. 在无终止的阴离子聚合中,阴离子无终止的原因是(C )A 阴离子本身比较稳定B 阴离子无双基终止而是单基终止C 从活性链上脱出负氢离子困难D 活化能低,在低温下聚合5. 合成聚合物的几种方法中,能获得最窄相对分子质量分布的是( A )A阴离子聚合B阳离子聚合C自由基聚合D自由基共聚合6. 能引发苯乙烯阴离子活性聚合,并且聚合度等于两倍的动力学链长的是(D)A. BuLiB. AIBNC. AlCl 3+H2OD. 萘+钠7. 制备分子量分别较窄的聚苯乙烯,应该选择(B)A 阳离子聚合B 阴离子聚合反应C 配位聚合反应D 自由基聚合反应8. 按阴离子聚合反应活性最大的单体是(A)A a氰基丙烯酸乙酯B乙烯C甲基丙烯酸甲酯D乙酸乙烯酯9. 高密度聚乙烯与低密度聚乙烯的合成方法不同,若要合成高密度聚乙烯所采用的引发剂是(B )A. BuLiB. TiCl4-AlR3C. BF3+H2OD. BPO10. Ziegler-Natta 引发剂引发丙烯聚合时,为了控制聚丙烯的分子量,最有效的办法是(D)A 增加引发剂的用量B 适当降低反应温度C 适当增加反应压力D 加入适量氢气11. 合成顺丁橡胶所用的引发剂为(D)A BPOB BuLiC Na + 萘D TiI+AlEt 312. 鉴定聚丙烯等规度所用的试剂是(D)A 正庚烷B 正己烷C 正辛烷D 沸腾的正庚烷13. 能采用阳离子、阴离子与自由基聚合的单体是(B)A、MMAB、StC、异丁烯D、丙烯腈14. 在高分子合成中,容易制得有实用价值的嵌段共聚物的是(B)A 配位阴离子聚合;B 阴离子活性聚合;C 自由基共聚合15 阳离子聚合最主要的链终止方式是(B)A 向反离子转移;B 向单体转移;C 自发终止16 能引发丙烯酸负离子聚合的引发剂是(A)A 丁基锂B 三氯化铝C 过氧化氢17 取代苯乙烯进行阳离子聚合反应时,活性最大的单体是(A)A 对甲氧基苯乙烯B 对甲基苯乙烯C 对氯苯乙烯D 间氯苯乙烯18 在具有强溶剂化中进行阴离子聚合反应时,聚合速率随反离子的体积增大而(B)A 增加B 下降C 不变D 无规律变化19 用强碱引发己内酰胺进行阴离子聚合反应时存在诱导期,消除的方法是(C)A 加入过量的引发剂B 适当提高温度C 加入少量乙酸酐D 适当加压20为了得到立构规整的1.4-聚丁二烯,1,3 -丁二烯可采用(D)聚合。
第六章 离子聚合

若采用极性溶剂,得高 结构(约 若采用极性溶剂,得高1, 2结构 约80%)聚丁二烯 结构 聚丁二烯 或75% 3, 4结构的聚异戊二烯 % 结构的聚异戊二烯 改变溶剂极性,有可能制得 ~ % 改变溶剂极性,有可能制得35~55% 1, 2结构乙 结构乙 烯基聚丁二烯
Page19
返回
高分子化学
§6 离子型聚合反应
有机金属化合物-- --阴离子引发 6.2.2.2 有机金属化合物--阴离子引发
金属氨基化合物( 液氨体系) 金属氨基化合物(NaNH2或KNH2-液氨体系)
2K + 2NH3
KNH2 K
2KNH2 + H2
+ NH2
NH2 + CH2=CH C6H5
H2N-CH2-CH 单阴离子 C6H5
自由阴离子引发体系, 自由阴离子引发体系,引发容易
Page14
返回
高分子化学
§6 离子型聚合反应
常用的溶剂为非质子溶剂: 二氧六环、 常用的溶剂为非质子溶剂:苯、二氧六环、 四氢呋喃、 二甲基甲酰胺。 四氢呋喃、N,N ’– 二甲基甲酰胺。
溶剂在离子型聚合中的影响作用
i.改变单体浓度 改变单体浓度 ii.溶剂的链转移作用 溶剂的链转移作用 iii.影响活性中心的结构和形态 影响活性中心的结构和形态 溶剂极性越大,表观增长速率常数 溶剂极性越大,表观增长速率常数kp越大
(C4H9Li)n
烷烃
C4H9Li
单体
C4H9 Li
C4H9 Li ..
+M
C4H9M Li C4H9 + [Li OC4H8]
采用THF作溶剂,引发活性显著提高 作溶剂, 采用 作溶剂
C4H9Li + OC4H8
第六章配位聚合

配位聚合
Ziegler-Natta催化剂在发现后仅2-3年便实现了工 业化,并由此把高分子工业带入了一个崭新的时代。
目前产品有: 高密度聚乙烯(high density Polyethylene ,HDPE) 全同(或等规)聚丙烯; 高顺式1,4 – 聚异戊二烯(95~97%) 高顺式1,4 – 聚丁二烯 乙丙橡胶(EPR)
• 1954年Natta等把Ziegler催化剂中的主 要 组 分 TiCl4 还 原 成 TiCl3 后 与 烷 基 铝 复 合 成功地进行了丙烯配位聚合。
• Goodrich Gulf公司采用Al(C2H5)3-TiCl4催 化体系使异戊二烯聚合,制备了高顺式1, 4的聚异戊二烯(合成“天然橡胶”)
2. 历程: ( 链增长)
配位聚合的增长反应分为2步: 1.单体在活性点(例如空位)上配位而活化 2.活化后的单体在金属-烷基键(Mt-R)中间 插入增长
上述两步反应反复进行,形成大分子长链 。
3. 配位阴离子聚合特点
1、单体π电子进入亲电性金属空轨道,配位形 成π络合物;
2.活性中心是阴离子性质的,故可称为配位阴离 子聚合
MtIV-VIIIX + MtI-IIIR
第一组分 (主引发剂)
第二组分 (助引发剂)
常用的主催化剂:TiCl4, TiCl3,VCl3, VOCl3,ZrCl3等,其中以TiCl3最常用;
助催化剂最有效的是一些金属离子半径小、 带正电性的金属有机化合物,因为它们的配 位能力强,易生成稳定的配位化合物。如Be, Mg,Al等金属的烷基化合物,其中以AlEt3和 AlEt2Cl最常用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
其引发反应可分两种情况: (i)不能“自离子化”的单独Lewis酸
与体系中微量的水发生水解生成H+引发聚合反应,如:
6.1 阳 离 子 聚 合 反 应
(ii)能“自离子化”的Lewis酸或不同Lewis酸的复合物 通过自离子化或不同Lewis酸相互离子化产生阳离子引发
6.2 阴 离 子 聚 合 反 应
6.2.3 链增长反 应
单体加成方式为首尾加成。 与阳离子聚合反应相似,增长链碳阴离子与抗衡阳离子间存 在离解平衡,其离解程度与抗衡阳离子以及溶剂性质等密切相 关。 ➢ 溶剂极性越强,离解程度越高,链增长活性越大;
6.2 阴 离 子 聚 合 反 应
➢ 抗衡阳离子(一般为碱金属离子)的影响较为复杂,在高极 性溶剂和低极溶剂性中的影响方向正好相反。
6.1 阳 离 子 聚 合 反 应
在这类引发体系中,通常把碳阳离子源称为引发剂(initiator), 而把Lewis酸称为活化剂(activator)。
6.1 阳 离 子 聚 合 反 应
6.1.3 链增长反应
(1)链增长活性中心与抗衡阴离子的离解平衡:
离解程度增加 反应活性增加
6.1 阳 离 子 聚 合 反 应
在高极性溶剂中,金属离子越小,越易溶剂化,与增长 活性中心的相互作用越小,离解程度越高,链增长反应越快; 在低极性溶剂中,溶剂化作用十分微弱,增长链碳阴离 子与抗衡阳离子之间的库仑力对活性中心离子对的离解程度 起决定性作用。金属离子越小,它与碳阴离子的库仑力越强, 离解程度越低,链增长反应越慢。
离解程度的影响因素:
➢ 链碳阳离子与抗衡阴离子间的相互作用:链碳阳离子与抗衡 阴离子的相互作用越弱,两者越易离解,链增长活性越高。
➢ 溶剂极性或溶剂化能力:极性大或溶剂化能力强的溶剂有利 于链增长活性中心与抗衡阴离子的离解,有利于聚合反应速率 的增大,如果溶剂极性太弱以致不能使两者离解而形成不具有 链增长活性的共价化合物,则聚合反应不能顺利进行。
链转移引发剂(inifer),如果聚合反应中不存在向单体等其它 的链转移反应,就可获得末端含-Cl的聚合产物。
6.1 阳 离 子 聚 合 反 应
6.1.4 链终止反应 阳离子聚合中除链转移反应会导致增长链失活外,还可
发生以下的终止反应: (1)链增长碳阳离子与抗衡阴离子结合:
如Cl3CCOOH/TiCl4引发的异丁烯聚合
种形式: (1)向单体链转移:增长链碳阳离子以H+形式脱去β-氢给 单体,这是阳离子聚合中最主要普遍存在的也是难以抑制的 内在副反应(built-in side-reaction):
链转移与链增长是一对竞争反应,降低温度、提高反应介质 的极性,有利于链增长反应,从而可提高产物分子量 。
6.1 阳 离 子 聚 合 反 应
离子稳定化的首-尾加成结构,即阳离子活性中心与双键加成时总是进攻不带取 代基的C,生成的碳阳离子可被取代基共振稳定化:
(3)阳离子聚合反应过程中的异构化反应: 碳阳离子可进行重排形成更稳定的碳阳离子,在阳离子聚合中也存在这种重排
反应,如:
6.1 阳 离 子 聚 合 反 应
6.1.4 链转移反应 链转移反应是阳离子聚合中常见的副反应,可有以下几
➢ 共轭烯烃,如:
➢ (π+n)给电子取代乙烯,如:
该类单体由于N和O原子上的未成对电子能与双键形成p-π 共轭,使双键电子云密度增大,因而特别活泼。
6.1 阳 离 子 聚 合 反 应
(2)异核不饱和单体R2C=Z,Z为杂原子或杂原子基团; 如醛RHC=O,酮RR’C=O(丙酮除外,因其最高聚合
温度为-273 oC),硫酮RR’C=S等。 (3)杂环化合物:阳离子开环聚合
1954年Natta等把Ziegler催化剂中的主要组分TiCl4还 原成TiCl3后与烷基铝复合成功地进行了丙烯聚合。
聚合反应。如:
6.1 阳 离 子 聚 合 反 应
两种Lewis酸复合时,酸性较强的起受体作用,从酸性 较弱的一方夺取负离子而产生离子化,如:
(3)碳阳离子引发剂:碳阳离子源/Lewis酸复合引发体系 碳阳离子源是指一些在Lewis酸的活化下能产生碳阳离
子的化合物:三级(或苄基)卤代烃、醚、醇、酯等,在 Lewis酸的活化下产生碳阳离子引发聚合反应,如:
(iii)有机金属化合物: 有机金属化合物是最常用的阴离子聚合引发剂。多为碱
金属的有机金属化合物(如丁基锂),Ca和Ba的有机金属 化合物也具引发活性,但不常用。
6.2 阴 离 子 聚 合 反 应
有机金属化合物的活性与其金属的电负性有关,金属的电 负性越小,活性越高。 (iv)格氏试剂:
烷基镁由于其C-Mg键极性弱,不能直接引发阴离子聚合, 但制成格氏试剂后使C-Mg键的极性增大,可以引发活性较大 的单体聚合。
6.2 阴 离 子 聚 合 反 应
此外,有些中性分子如R3P(膦)、R3N、吡啶、ROH、 H2O等都有未共用电子对,为Lewis碱,可以通过亲核加成机 理引发阴离子聚合,但它们的引发活性较低,只能用于活泼 单体的聚合,如活性很高的α-氰基丙烯酸乙酯(502胶水)遇 水可以被引发聚合:
单体与引发剂之间具有选择性:能引发A单体聚合的引发剂, 不一定能引发B单体聚合。强碱性高活性引发剂能引发各种活性 的单体,而弱碱性低活性引发剂只能引发高活性的单体。
此外,凡是容易与碳阳离子反应使之失去活性的溶剂都不 宜选做阳离子聚合溶剂。
因此,适合于用做阳离子聚合的溶剂并不多,常用的有 芳香烃(如甲苯、苯、硝基苯)、卤代烃(如CH2Cl2)等。
6.1 阳 离 子 聚 合 反 应
(2)链增长过程中单体单元链接方式: 与自由基聚合相似,通常乙烯基单体阳离子聚合一般得到能使链增长碳阳
6.2 阴 离 子 聚 合 反 应
(i)金属氨基化合物: 金属氨基化合物一般认为是通过自由阴离子方式引发
聚合反应:
6.பைடு நூலகம் 阴 离 子 聚 合 反 应
(ii)烷氧阴离子: 先由金属与醇(酚)反应制得烷氧阴离子,然后再加入聚
合体系引发聚合反应。如: 2 Na + 2 CH3OH → 2 CH3ONa + H2
6.1 阳 离 子 聚 合 反 应
(3)链增长碳阳离子与与亲核性杂质的链终止
在聚合体系中,若存在亲核性杂质,如水、醇、酸、酐、 酯、醚等,它们虽然可以作为质子或碳阳离子源在Lewis酸 活化下引发阳离子聚合。但它们的含量过高时,则可导致转 移性链终止反应,以水为例:
6.1 阳 离 子 聚 合 反 应
6.1 阳 离 子 聚 合 反 应
一般质子酸(如H2SO4,HCl等)由于生成的抗衡阴离子 SO42-、Cl-等的亲核性较强,易与碳阳离子生成稳定的共价键, 使增长链失去活性,因而通常难以获得高分子量产物;
超强酸由于酸性极强,离解常数大,活性高,引发速率快, 且生成的抗衡阴离子亲核性弱,难以与增长链活性中心成共价 键而使反应终止。
(2)向反离子链转移 增长链碳阳离子上的β-质子也可向反离子转移,这种转移
方式又称自发终止:
(3)向高分子的链转移反应: 如在苯乙烯以及衍生物的阳离子聚合中,可通过分子内亲
电芳香取代机理发生链转移:
6.1 阳 离 子 聚 合 反 应
(4)向引发剂的链转移,如:
该反应中 做
既是引发剂又是链转移剂,通常叫
6.2 阴 离 子 聚 合 反 应
6.2.4 链转移与链终止反 应
链转移:阴离子聚合从增长链上脱去氢阴离子H-发生链转 移的活化能相当高,一般难以进行;
HH CC HX
Mt+ + CH2=CHX
活化能高
H
H
C C + H3C C
HX
X
链终止:在阴离子聚合反应中,由于其链增长活性中心为阴 离子,不能进行双基终止;抗衡阳离子为金属离子,链增长 碳阴离子难以与其形成共价键而终止。
因此,对于理想的阴离子聚合体系如果不外加链终止剂 或链转移剂,一般不存在链转移反应与链终止反应。
6.3 配 位 聚 合 反 应
6.3.1 Ziegler-Natta催化 剂
1953年,Ziegler等从一次以Et3Al为催化剂从乙烯合 成高级烯烃的失败实验出发,意外地发现以乙酰丙酮的 锆盐和Et3Al催化时得到的是高分子量的乙烯聚合物,并 在此基础上开发了的乙烯聚合催化剂TiCl4 - AlEt3。
6.1.5 阳离子聚合的工业应用
由于适于阳离子聚合单体种类少,加之其聚合条件苛刻, 如需在低温、惰性气体保护、高纯有机溶剂中进行,因而限 制了它在工业上的应用。聚异丁烯和丁基橡胶是工业上用阳 离子聚合的典型产品。
异丁烯阳离子聚合通常用H2O / BF3 、 H2O/AlCl3、H2O / TiCl4等作为引发剂。在0~ -40℃下聚合时得到的是低分子量 (Mn<5万)油状或半固体状低聚物,可用作润滑剂、增粘剂、 增塑剂等。在-100℃以下聚合时,则可得到高分子量聚异丁 烯(Mn = 5×104~106),它是橡胶状固体,可用作粘合剂、 管道衬里及塑料改性剂等。
易发生在抗衡阴离子亲核性较强或溶剂极性不利于抗衡 阴离子与链增长碳阳离子离解的聚合体系中。
6.1 阳 离 子 聚 合 反 应
(2)链增长碳阳离子与抗衡阴离子团中某阴离子结合生成 稳定的共价键
如H2O/BCl3引发的异丁烯聚合
抗衡阴离子团中B-OH键比B-Cl键强,更易脱去Cl-与增长链碳 阳离子结合生成较稳定的C-Cl键,而新形成的Lewis酸BCl2OH不 足以活化C-Cl键产生碳阳离子,从而导致反应终止。
高分子科学基础
第六章 离子聚合与配位聚合反应
6.1 阳 离 子 聚 合 反 应
6.1.1 单体
具有阳离子聚合活性的单体主要包括以下几类: (1)带给电子取代基的烯烃: 取代基的给电子能力越强, 双键上电子云密度越高,单体聚合活性越高。 ➢ 偏二烷基取代乙烯,如:
