2005版中国药典收载的氨基酸原料药
药物分析

第一章绪论(一)A型题1、药物分析是药学领域的一个重要组成部分,其研究的目的是A、提高药物分析的研究水平B、提高药物的经济效益C、保证药物的绝对纯净D、保证用药的安全性和有效性E、提高药效的疗效2、我国现行的国家药品质量标准是A、《中国药典》B、《局颁药品标准》C、《临床研究用药品质量标准》D、A和B项E、A、B、C三项均是3、关于药典的叙述,不正确的是A、药典是判断药品质量的准则,具有法律作用B、国家颁布的药典所收载的药品,一般称为法定药C、凡是药典收载的药品,如其质量不符合药典的要求均不应使用D、生产企业必须按规定的工艺生产法定药E、药典收载的药物的品种和数量是永久不变的4、关于中国药典的叙述,最确切的是A、是收载所有药品的法典B、是一部药物词典C、是我国制定的药品质量标准的法典D、是由国家统编的重要技术参考书E、是从事药品生产、使用、科研及药学教育的唯一依据5、关于药典的性质,下列叙述中正确的是A、是由国家统一编制的重要技术参考书B、是从事药物生产、使用、科研及药学教育的唯一依据C、是国家记载药品质量标准的国家法典,具有法律作用D、药典未收载的药物品种,一律不准生产、销售和使用E、药典已收载的药物品种,地方可根据地区的情况作适当处理6、对10%葡萄糖注射液进行分析检验,其结果仅含量测定不符合《中国药典》2005年版中所规定的要求,则该品为A、合格药品B、优等品C、二等品D、三等品E、不合格药品7、《中国药典》2005年版规定,“称取0.1g”系指A、称取重量可为0.05~0.15gB、称取重量可为0.06~0.14gC、称取重量可为0.07~0.13gD、称取重量可为0.08~0.12gE、称取重量可为0.09~0.11g8、药品的鉴别是证明A、未知药物的真伪B、已知药物的真伪C、已知药物的疗效D、药物的纯度E、药物的稳定性9、用移液管量取的25ml溶液,应记成A、25mlB、25.0mlC、25.00mlD、25.000mlE、25ml±1ml10、精密度是指A、测量值与真值接近的程度B、同一个均匀样品,经多次测定所得结果之间的接近程度C、表示该法测量的正确性D、在各种正常实验条件下,对同一样品分析所得结果的准确程度E、表示该法能准备测定供试品的最低量11、取样要求,当样品数为X时一般应按A、X≤300时,按X的1/30取样B、X≤300时,按X的1/10取样C、X≤3时,只取1件D、X≤3时,每件取样E、X﹥300件时,随便取样12、药品检验的工作程序A、性状、检查、含量测定、检验报告B、性状、检查、含量测定、原始记录C、检品审查、取样、检验(性状观测、鉴别、检查、含量测定)、记录和报告D、取样、鉴别、检查、含量测定E、性状、鉴别、含量测定、报告(二) B型题[13—16]A、JPB、BPC、USPD、Ch.PE、Ph.Eur13、《中国药典》英文缩写为 D14、《英国药典》英文缩写为B15、《日本药局方》英文缩写为 A16、《美国药典》英文缩写为C(三)X型题17、药物分析是研究化学结构已经明确的合成药物或天然药物及其制剂的质量,主要包括A、药物结构分析B、药物成品的化学检验C、药物生产过程的质量控制D、药物贮藏过程的质量考察E、药物营销过程的质量分析18、评价药物的质量主要包括A、药物的纯度B、药物的贮藏C、药物的剂型D、药物的毒副作用E、药物的疗效19、《中国药典》2005年版第二部收载的药品有A、抗生素B、化学药品C、生物制品D、生化药品E、中药成方制剂20、用碘量法测定维生素C原料药时,要求碘量法应验证的主要项目有A、专属性B、定量限C、精密度D、准确度E、线性21、进行药品检验时,要从大量药品中取出少量样品应考虑取样的A、多样性B、真实性C、代表性D、科学性E、选择性第二章物理常数测定法(一)A型题1、下列不属于物理常数的是A、相对密度B、黏度C、比旋度D、折光率E、旋光度2、相对密度测定法中的比重瓶法适合于测定A、不挥发或挥发性很小的液体药物B、固体药物C、易挥发的液体药物D、气体药物E、受热晶型易改变药物3、用韦氏比重秤测定相对密度时,当500mg的砝码放在第5格上时读数为A、0.5B、0.05C、0.005D、0.0005E、0.000054、测定易挥发、易燃液体的馏程时,加热方法应选用A、煤气灯加热B、电炉加热C、酒精灯加热D、恒温水浴加热E、直接火焰加热5、测定熔点在80℃以下固体药物熔点时,可选用下列哪种物质做传温液A、水B、硅酮C、液状石蜡D、乙醇E、丙酮6、折光率测定时,通常情况下,当温度升高时折光率A、不变B、开始时升高,然后降低C、升高D、降低E、开始降低然后升高7、药物在水溶液中的折光率校正公式为A、n T D=n t D+0.0001(T-t)B、n T D=n t D+0.0001(t-T)C、n T D=n t DD、n T D=n t D+0.0001E、n T D= 0.0001(t-T)8、《中国药典》2005年版规定的液体的相对密度是指A、20℃时,某物质的密度与水的密度之比B、18℃时,某物质的密度与水的密度之比C、22℃时,某物质的密度与水的密度之比D、30℃时,某物质的密度与水的密度之比E、15℃时,某物质的密度与水的密度之比9、熔点是指固体物质在一定条件下加热A、开始初熔时的温度B、固体刚好熔化一半时的温度C、分解时的温度D、开始初熔至全熔时的温度E、被测物晶型转化时的温度10、《中国药典》2005年版表示物质的旋光性常用的物理常数是A、比旋度B、旋光度C、液层厚度D、波长E、溶液浓度11、《中国药典》2005年版対药物进行折光率测定时,采用的光线是A、日光B、钠光D线C、紫外光线D、红外光线E、可见光线12、在药物分析中,测定药物的折光率主要是为了A、测定药物的化学结构B、测定药物的浑浊程度C、检查水分影响D、测定药物黏度的大小E、用以鉴别药物和检查药物的纯度13、比旋度是指A、偏振光透过长1cm且每1ml中含旋光物质1g的溶液,在一定波长与温度下测定的旋光度B、偏振光透过长1dm且每10ml中含旋光物质1g的溶液,在一定波长与温度下测定的旋光度C、偏振光透过长1dm且每1ml中含旋光物质1g的溶液,在一定波长与温度下测定的旋光度D、偏振光透过长1dm且每100ml中含旋光物质1g的溶液,在一定波长与温度下测定的旋光度E、偏振光透过长1cm且每100ml中含旋光物质1g的溶液,在一定波长与温度下测定的旋光度14、黏度的大小随温度变化而变化,当温度越高A、开始时升高,然后降低B、黏度越高C、黏度越小D 、开始降低然后升高E 、不变15、20℃时水的折光率是A 、1.3316B 、1.3325C 、1.3305D 、1.3313E 、1.333016、熔点测定有三种方法,主要因为A 、供试品的溶解度不同B 、供试品的固体状态不同C 、供试品量的多少不同D 、供试品的熔点不同E 、供试品的分子量不同17、物理常数不可用于A 、鉴别官能团B 、测定含量C 、检查纯度D 、鉴别真伪E 、测定平均分子量(二) B 型题[18—22]A 、测定挥发性小或不挥发的液体的相对密度B 、液体物质的鉴别C 、受热不分解的固体药物鉴别D 、旋光物质的鉴别或含量测定E 、高分子的液体物质的鉴别18、黏度测定可用于 E19、旋光度法可用于 D20、比重瓶法可用于 A21、熔点测定法可用于 C22、馏程测定法可用于 B[23—26]A 、pa ·sB 、2m m /sC 、[ ]D 、[α]t DE 、n t D23、折光率 E24、动力黏度单位 A25、运动黏度单位 B26、比旋度 D (三) X 型题27、影响旋光度测定的因素包括A 、浓度B 、温度C 、压强D 、波长E 、液层厚度28、平氏粘度计可用于测定A 、运动粘度B 、动力黏度C 、特性黏度D 、比旋度E 、扭力矩29、影响折光率测定的因素有A 、浓度B 、温度C 、压强D 、波长E 、溶剂第三章 药物的杂质检查(一) A 型题1、药物杂质检查的目的是A、控制药物的纯度B、控制药物疗效C、控制药物的有效成分D、控制药物的毒性E、检查生产工艺的合理性2、检查药物中氯化物时,为排除某些弱酸盐的干扰,应加入一定量的A、稀氨液B、硫酸C、稀硫酸D、稀硝酸E、稀盐酸3、对照法检查药物中的氯化物,氯化物的最大允许量存在于A、供试品中B、供试品溶液中C、标准氯化钠溶液中D、对照溶液中E、白色浑浊中4、检查硫酸盐时,对照溶液的制备是用A、NaCl溶液B、标准NaCl溶液C、氯化钡溶液D、K2SO4溶液E、标准的K2SO4溶液5、检查硫酸盐杂质时,一般取用标准硫酸钾溶液(100μg/ml)1~5ml,其原因是A、沉淀反应完全B、避免弱酸盐干扰C、所产生的浑浊梯度明显D、所产生的梯度最浓E、药物中硫酸盐杂质的量均在此范围内6、检查铁盐时,要求酸性条件的原因是A、防止Fe+3还原B、防止Fe+3的水解C、提高反应灵敏度D、使生成颜色稳定E、防止Fe+3与Clˉ形成配位化合物7、检铁盐的方法中,加入氧化剂过硫酸铵的作用是A、防止Fe+3的水解B、防止Fe+2变成Fe+3C、将存在的Fe+2氧化成Fe+3D、增加[Fe(SCN)6]-3稳定性 E、加快生成[Fe(SCN)6]-3的速度8、以硫代乙酰胺为显色剂检查重金属,供试品溶液调整的最佳pH值是A、1.5B、3.5C、6.5D、8.5E、11.59、炽灼残渣如需留作重金属检查时,炽灼温度应采用A、800℃以上B、700~800℃C、600~700℃D、500~600℃E、500℃以下10、在古蔡法检砷装置中,装入醋酸铅棉花的目的是A、吸收多余的氢气B、吸收氯化氢气体C、吸收硫化氢气体D、吸收砷化氢气体E、吸收二氧化碳气体11、用古蔡法检砷时,和溴化汞试纸作用生成砷斑的化合物是A、HgBr2 B、SnCl2C、KID、AsH3E、AsH(HgBr)212、古蔡法检砷中,加入碘化钾和氯化亚锡的主要目的是A、将As+5还原为As+3B、将As+3还原为As+5C、排除硫酸物的干扰D、延缓氢气的产生E、以上个性都不对13、检查氯化钠的酸碱度,采用的方法是A、酸碱滴定法B、指示剂法C、pH值测定法D、广泛pH值试纸法E、以上都不对14、检查硫酸阿托品中的莨菪碱,采用的方法是A、测定旋光度B、测定吸光度C、测定折光率D、测定熔点E、测定酸碱度15、TLC供试品溶液自身稀释对照法检查杂质,所用的对照溶液是A、杂质对照品溶液B、浊度标准液C、标准比色液D、供试品溶液E、供试品溶液的稀释液16、TCL供试品溶液自身稀释对照法检差杂质,若要杂质限量符合规定,则供试品溶液杂质斑点的颜色应不深于A、对照品杂质斑点颜色B、对照溶液主斑点颜色C、供试品溶液主斑点颜色D、供试品溶液杂质斑点颜色E、对照药材杂质斑点颜色17、检查肾上腺素中的肾上腺酮,采用的方法是A、薄层色谱法B、纸色谱法C、分光光度法D、旋光法E、折光法18、下列关于硫化物检查的叙述不正确的是A、硫化物与盐酸作用产生硫化氢气体B、检查装置与砷盐检查中的古蔡法相同C、导气管中不装入醋酸铅棉花D、硫化氢与醋酸铅试纸产生“硫斑”E、检查时需要加入无砷锌粒(二) B型题[19—23]A、硝酸银试液作沉淀剂B、氯化钡溶液作沉淀剂C、硫代乙酰胺试液作显色剂D、硫氰酸铵溶液作显色剂E、溴化汞试纸作显色剂19、重金属检查 C20、氯化物检查 A21、硫酸盐检查 B22、铁盐检查 D23、砷盐检查 E[24—28]A、有色杂质B、不溶性杂质C、遇硫酸呈色的有机杂质D、金属的氧化物或盐类E、水份24、易碳化物检查法是检查 C25、澄清度检查法是检查 B26、炽灼残渣检查法是检查D27、溶液颜色检查法是检查A28、干燥失重检查法是检查E(三)X型题29、药物中的杂质一般来源于A、生产过程B、使用过程C、贮存过程D、体内过程E、附加剂30、检查药物中的氯化物杂质,需要用下列哪些试剂A、稀盐酸B、稀硫酸C、稀硝酸D、硝酸银试液E、标准氯化钠溶液31、检查药物中重金属杂质,常用的显色剂有A、硫化铵B、硫化钠C、硫酸钠D、硫代硫酸钠E、硫代乙酰胺32、《中国药典》2005年版收载的古蔡法检查砷的基本原理是S气体A、与锌、酸作用生成H2B、与锌、酸作用生成AsH3气体C、产生的气体遇醋酸铅棉花产生砷斑D、比较供试品砷斑与标准品砷斑的面积大小E、比较供试品砷斑与标准品砷斑的颜色强度33、费休试液由下列哪些试剂组成A、碘B、溴C、二氧化硫D、吡啶E、甲醛34、澄清度检查时,配制浊度标准液所用的试剂是A、硫代乙酰胺B、硫酸肼C、硫酸铜D、乌洛托品E、水合氯醛35、盐酸吗啡中检查罂粟酸,取本品一定量加水溶解后,加稀盐酸及三氯化铁试液,不得显红色,该杂质检查的方法为A、物理法B、化学法C、灵敏度法D、对照法E、利用药物与杂质化学性质上的差异第四章醇、酚、醚、醛、酮类药物的分析(一)A型题1、某药物水溶液,加入氢氧化钠试液和碘试液,即发生碘仿的臭气,并生成黄色沉淀,该药物是A、乙醇B、甘油C、甘露醇D、山梨醇E、二巯基丙醇2、甘露醇的鉴别方法之一为在一定条件下,加入酰化剂反应,通过测定衍生物熔点进行鉴别试验,此酰化剂为A、乙醇B、丙醇C、醋酐D、甘油E、乙醇3、《中国药典》2005年版规定二巯基丙醇的含量测定方法为A、酸碱滴定法B、非水溶液滴定法C、沉淀滴定法D、碘量法E、高碘酸钠法或高碘酸钾法4、某药物水溶液,加三氯化铁试液,既显蓝紫色,该药物是A、苯酚B、甲酚C、乙醇D、甘油E、甘露醇5、某药物饱和水溶液,加三氯化铁试液,即显易消失的蓝紫色,该药物是A、苯酚B、甲酚C、乙醇D、甘油E、甘露醇6、某药物水溶液,加溴试液,即生成瞬即溶解的白色沉淀,但溴试液过量时,即生成持久的沉淀,该药物是A、苯酚B、乙醇C、甘油D、山梨醇E、甲酚7、某药物饱和水溶液,加溴试液,即析出淡黄色的絮状沉淀,该药物是A、苯酚B、乙醇C、甘油D、山梨醇E、甲酚8、某药物水溶液,加盐酸,即发生白色乳浊,加热煮沸数分钟,析出油状液,放冷,凝固成白色蜡状固体,该药物是A、乙醇B、甲酚C、盐酸苯海拉明D、乌洛托品E、扑米酮9、盐酸苯海拉明加盐酸分解,其结构中的醚键断裂,生成水溶性较小的化合物用于鉴别,该化合物是A、甲醇B、二苯甲醇C、乙醇D、甘油E、二甲氨基乙醇10、麻醉乙醚检查过氧化物时,采用的试液是A、硝酸银试液B、氢氧化钠试液C、碘化钾-淀粉试液D、三氯化铁试液E、碱性酒石酸酮试液11、《中国药典》2005年版规定盐酸苯海拉明的含量测定方法是A、酸碱滴定法B、非水溶液滴定法C、沉淀滴定法D、碘量法E、高碘酸钠法或高碘酸钾法12、某药物水溶液,加氢氧化钠试液,溶液显浑浊,加温后成澄明的两液层,并发生三氯甲烷的臭气,该药物是A、甘油B、甲酚C、盐酸苯海拉明D、水合氯醛E、乌洛托品13、某药物加稀硫酸溶解后,加热,产生甲醛的特臭,能使润湿的氨制硝酸银试纸显黑色,再加过量的氢氧化钠试液,产生氨臭,能使润湿的红色石蕊试纸变成蓝色,该药物是A、山梨醇B、苯酚C、麻醉乙醚D、水合氯醛E、乌洛托品14、《中国药典》2005年版规定,水合氯醛的含量测定方法是A、剩余酸碱滴定法B、非水溶液滴定法C、沉淀滴定法D、碘量法E、高碘酸钠法或高碘酸钾法15、某药物加变色酸试液,置水浴上加热一定时间,即显紫色,该药物是A、麻醉乙醚B、盐酸苯海拉明C、扑米酮D、月桂氮卓酮E、吡喹酮(二) B型题[16—20]A、草酸盐B、还原糖C、醇合三氯乙醛D、过氧化物E、有关物质16、水合氯醛需检查的杂质是C17、甘露醇需检查的杂质是 A18、麻醉乙醚需检查的杂质是 D19、盐酸苯海拉明需检查的杂质是 E20、山梨醇需检查的杂质是B(三)X型题21、下列药物中采用高碘酸钠法或高碘酸钾法测定其含量的是A、乙醇B、甘油C、甘露醇D、山梨醇E、二巯基丙醇22、下列药物需检查不挥发杂质的有A、苯酚B、麻醉乙醚C、乙醇D、水合氯醛E、甲酚23、麻醉乙醚检查的杂质有A、酸度B、醛类C、过氧化物D、异臭E、不挥发物24、麻醉乙醚检查醛类杂质时,其条件有A、亚硫酸氢钠溶液B、淀粉指示液C、碘滴定液D、碳酸氢钠E、碘化钾25、与水合氯醛含量测定内容相关的条件有A、氢氧化钠滴定液B、酚酞指示液C、硫酸滴定液D、铬酸钾指示液E、硝酸银滴定液第五章芳酸及其酯类药物的分析(一)A型题1、苯甲酸的钠盐水溶液与三氯化铁试液作用产生A、紫堇色B、紫红色C、赭色沉淀D、米黄色沉淀E、猩红色沉淀2、具有升华性的药物是A、苯甲酸B、苯甲酸钠C、丙磺舒D、泛影酸E、布美他尼3、鉴别泛影酸分子结构中有机碘的方法是A、直接加硝酸银试液B、置坩埚中,小火加热,即分解产生紫色的碘蒸汽C、纸色谱D、加热破坏后,加硝酸银试液E、加盐酸破坏后,加硝酸银试液4、泛影酸中检查项目不包括A、游离碘B、卤化物C、碘化物D、氨基化合物E、有机碘化合物5、《中国药典》2005年版规定采用双相酸碱滴定法测定含量的药物是A、苯甲酸B、阿司匹林C、水杨酸D、苯甲酸钠E、布洛芬6、苯甲酸和水杨酸理化性质很相似,若需验证苯甲酸中是否混有水杨酸,可予以检查的试剂是A、溴试液B、三氯化铁试液C、硝酸银试液D、氢氧化钠试液E、A项和B项7、用双相酸碱滴定法测定苯甲酸钠含量时,选用的指示剂是A、结晶紫B、酚酞C、甲基橙D、甲基红E、甲酚红8、《中国药典》2005年版规定泛影酸的含量测定方法采用A、重氮化法B、碘量法C、双相酸碱滴定法D、非水滴定法E、银量法9、阿司匹林中检查水杨酸,是利用杂质与药物的A、溶解性差异B、化学性质的差异C、熔点差异D、对光的吸收性差异E、旋光性差异10、阿司匹林与碳酸钠试液共热,放冷后用稀硫酸酸化,析出的白色沉淀是A、乙酰水杨酸B、醋酸C、水杨酸钠D、水杨酸E、苯甲酸11、阿司匹林片及肠溶片含量测定时,为避免枸橼酸、水杨酸、醋酸等干扰应选用A、直接酸碱滴定法B、水解酸碱滴定法C、双相酸碱滴定法D、置换酸碱滴定法E、两步酸碱滴定法12、对氨基水杨酸中的特殊杂质是A、间氨基苯酚B、氨基酚C、苯酚D、氨基化合物E、水杨酸13、氯贝丁酯可发生异羟肟酸铁反应,是其因结构中含有A、酯键B、羧基C、有机氯D、醚E、苯环(二) B型题[14—18]A、三氯化铁反应B、异羟肟酸铁反应C、重氮化-偶合反应D、有机碘反应E、水解反应14、阿司匹林极易发生E15、鉴别泛影酸用 D16、鉴别水杨酸用A17、鉴别布洛芬用B18、鉴别对氨基水杨酸钠中的芳香第一胺用C[19—23]A、双相酸碱滴定法B、亚硝酸钠法C、银量法D、两步酸碱滴定法E、高效液相色谱法19、阿司匹林栓的含量测定采用E20、阿司匹林片的含量测定采用D21、泛影酸的含量测定采用C22、对氨基水杨酸钠的含量测定采用B23、苯甲酸钠的含量的测定采用A[24—28]A、阿司匹林B、对氨基水杨酸钠C、氯贝丁酯D、布美他尼E、泛影酸24、水杨酸是【A】中特殊的杂质25、氨基化合物是【 E】中特殊的杂质26、芳香第一胺是【D】中特殊的杂质27、间氨基酚是【B】中的特殊杂质28、对氯酚是【C】中的特殊杂质(三)X型题29、采用两步滴定法测定阿司匹林片含量的目的是A、消除所加稳定剂(枸橼酸或酒石酸)的干扰B、消除空气中二氧化碳的干扰C、消除水解产物(水杨酸、醋酸)的干扰D、消除空气中氧气的干扰E、便于操作30、能与三氯化铁试液产生颜色反应的药物有A、水杨酸B、丙磺舒C、苯甲酸D、阿司匹林E、对氨基水杨酸钠31、需检查游离水扬酸的药物有A、阿司匹林B、布洛芬C、苯丁酸氮芥D、苯甲酸E、羟苯乙酯32、采用异羟肟酸铁反应鉴别的药物有A、水杨酸B、苯甲酸钠C、氯贝丁酯D、布洛芬E、阿司匹林33、《中国药典》2005年版规定采用酸碱滴定法测定含量的药物有A、泛影酸B、苯甲酸C、阿司匹林D、水杨酸E、苯甲酸钠第六章胺类药物的分析(一)A型题1、下列药物中,可以发生重氮化-偶合反应的是A、盐酸克仑特罗B、肾上腺素C、苯佐卡因D、盐酸丁卡因E、盐酸利多卡因2、下列药物中,经水解后可以发生重氮化-偶合反应的是A、苯佐卡因B、肾上腺素C、对乙酰氨基酚D、盐酸普鲁卡因E、盐酸丁卡因3、在下列药物水溶液中,加入三氯化铁试液,即显蓝紫色,该药物应是A、苯佐卡因B、醋氨苯砜C、对乙酰氨基酚D、盐酸普鲁卡因E、盐酸利多卡因4、《中国药典》2005年版规定,盐酸普鲁卡因注射液应检查的特殊杂质是A、对氨基酚B、对氨基苯甲酸C、对氨基苯乙酸D、氨基苯E、硝基苯5、《中国药典》2005年版规定,肾上腺素应检查酮体,其检查的方法是A、比色法B、旋光法C、薄层色谱法D、紫外-可见分光光度法E、折光法6、《中国药典》2005年版规定,重酒石酸去甲肾上腺素注射液含量测定的方法是A、旋光法B、紫外-可见分光光度法C、高效液相色谱法D、溴量法E、非水溶液滴定法7、1ml高氯酸滴定液(0.1mol/L)相当于【】mg的马来酸氯苯那敏(C16H19CIN2•C4H4O4,M﹦390.87)A、39.09B、19.54C、40.89D、20.44E、42.698、亚硝酸钠滴定法中,常加入溴化钾的作用是A、防止亚硝酸逸失B、增加亚硝酸钠的稳定性C、抑制生成的重氮盐分解D、避免温度的影响E、加快重氮化反映的速度9、用非水溶液滴定法测定盐酸丁卡因含量时,加入醋酸汞试液的目的是A、指示剂B、催化剂C、稳定剂D、消除盐酸的干扰E、增强丁卡因的碱性(二) B型题[10—13]A、紫外-可见分光光度法B、比色法C、薄层色谱法D、旋光法E、比浊法10、肾上腺素中特殊杂质酮体的检查方法是A11、对乙酰氨基酚特殊杂质有关物质的检查方法是C12、对乙酰氨基酚特殊杂质对氨基酚的检查方法是 B13、盐酸普鲁卡因注射液中特殊杂质对氨基苯甲酸的检查方法是 C[14—18]A、亚硝酸钠滴定法B、紫外-可见分光光度法C、溴量法D、非水溶液滴定法E、旋光法14、盐酸去氧肾上腺素药物的含量测定是 C15、盐酸普鲁卡因的含量测定是A16、盐酸利多卡因的含量测定是 D17、盐酸布比卡因的含量测定是D18、对乙酰氨基酚的含量测定是B(三)X型题19、《中国药典》2005年版规定,对乙酰氨基酚检查的特殊杂质有A、乙醇溶液的澄清度与颜色B、有关物质C、对氨基酚D、对氨基苯甲酸E、苯胺20、鉴别盐酸普鲁卡因的反应有A、重氮化-偶合反应B、三氯化铁反应C、重金属离子反应D、水解反应E、氯化物反应21、鉴别肾上腺素的反应有A、重氮化-偶合反应B、三氯化铁反应C、甲醛-硫酸反应D、水解反应E、氧化反应22、测定马来酸氯苯那敏含量的方法有A、非水溶液滴定法B、银量法C、酸性染料比色法D、亚硝酸钠滴定法E、紫外分光光度法23、亚硝酸钠滴定法指示终点的方法有A、内指示剂法B、外指示剂法C、自身指示剂法D、永停滴定法E、电位滴定法24、下列药物中,可用三氯化铁反应鉴别的有A、对乙酰氨基酚B、盐酸普鲁卡因C、盐酸利多卡因D、肾上腺素E、盐酸异丙肾上腺素第七章巴比妥类药物的分析(一)A型题1、巴比妥药物属于A、镇静催眠药B、解热镇痛药C、麻醉药D、生物碱类药E、抗生素类药2、关于巴比妥类药物的结构叙述不正确的是A、具有同样的基本结构B、C2位的氧可被硫取代C、N1位和N3位可同时被取代D、C5位可被苯取代E、《中国药典》2005年版规定收载的主要是5,5-取代巴比妥类药物3、下列不属于巴比妥类药物性质的是A、具有紫外吸收B、具有弱酸性C、具有氧化性D、能溶解于稀碱溶液中E、可与酮吡啶试液形成配位化合物4、苯巴比妥钠与酮吡啶试液反应生成物是A、红色B、紫色C、绿色D、蓝色E、黄绿色5、硫喷托钠与酮吡啶试液反应生成物为A、红色B、紫色C、绿色D、蓝色E、黄绿色6、巴比妥类药物的基本结构为A、氨基醚B、对氨基苯甲酸C、丙二酰脲D、对氨基苯磺酰胺E、吡喹酮7、用硝酸银鉴别巴比妥类药物时的现象为A、开始无沉淀,最后出现沉淀B、开始有沉淀,沉淀最后消失C、开始出现沉淀,但很快消失,最后沉淀不在消失D、开始有少量沉淀,沉淀越来越多E、开始沉淀很多,沉淀越来越少8、苯巴比妥发生亚硝基化反应是因分子中具有A、胺基B、乙基C、甲基D、酰脲E、苯环9、在哪种溶液中,巴比妥类药物会产生明显的紫外吸收A、酸性溶液B、中性溶液C、碱性溶液D、乙醇溶液E、三氯甲烷溶液10、钠盐的焰色反应产生的焰色是A、黄绿色B、紫堇色C、绿色D、砖红色E、鲜黄色11、巴比妥类药物的酸度检查主要是检查A、制备过程中生成的丙二酰脲B、制备过程中反应不完全的丙二酰脲C、贮存过程中生成的丙二酰脲D、同类酸性杂质E、巴比妥酸12、《中国药典》2005年版中采用银量法测定苯巴比妥含量所用的指示剂是A、内指示剂法B、自身指示剂法C、电位指示法D、外指示剂法E、混合指示剂法13、下列药物中,可用碘试液进行鉴别的是A、巴比妥B、苯巴比妥C、异戊巴比妥D、司可巴比妥E、硫喷妥钠14、在碱性溶液中加铅离子生成白色沉淀,加热后,沉淀变黑,此药物是A、巴比妥B、苯巴比妥C、异戊巴比妥D、司可巴比妥E、硫喷妥钠15、下列药物中,能与氢氧化钠共沸放出氨气的是A、对乙酰氨基酚B、阿司匹林C、水杨酸D、苯巴比妥E、水合氯醛(二) B型题[16—20]A、酸碱滴定法B、银量法C、溴量法D、紫外分光光度法E、旋光法16、《中国药典》2005年版规定,测定葡萄糖注射液含量采用 E17、《中国药典》2005年版规定,测定苯巴比妥钠含量采用B18、《中国药典》2005年版规定,测定注射用硫喷妥钠含量采用D19、《中国药典》2005年版规定,测定司可巴比妥钠含量采用C20、《中国药典》2005年版规定,测定阿司匹林采用A(三)X型题21、巴比妥类药物具有A、弱酸性B、水解性C、与硝酸银生成白色沉淀D、与酮吡啶试液生成有色物质E、具有紫外吸收22、巴比妥类药物的含量测定方法有A、银量法B、紫外分光光度法C、酸碱滴定法D、高锰酸钾发E、溴量法23、巴比妥类药物的特殊杂质检查项目有A、酸度B、中性或碱性物质C、乙醇溶液的澄清度D、对氨基苯甲酸E、水杨酸第八章磺胺类药物的分析(一)A型题1、下列磺胺类药物的鉴别反应中,属于芳香第一胺基性质的是A、成铜盐的反应B、重氮化-偶合反应C、红外分光光度法D、N4取代基的反应E、灼烧实验2、下列试验为判断磺胺类药物具有酸碱两性的方法是A、pH计B、酚酞指示液和甲基橙指示液C、广泛用pH试纸D、稀酸和稀碱液E、石蕊试纸。
中国药典2005

中国药典2005药品杂质分析杂质定义任何影响药品纯度的物质。
在药品质量标准中的杂质系指在按照经国家有关药品监督管理部门依法审查批准的规定工艺和规定的原辅料生产的药品中,由其生产工艺和原辅料带入的杂质,或经稳定性试验确证的在贮存过程中产生的降解产物。
药品质量标准中的杂质不包括:•变更生产工艺或变更原辅料而产生的新的杂质:重新申报•掺入或污染的外来物质:假劣药品,非法定方法予以检测新发现的杂质生产《中国药典》2005版的收载的产品,若含有药典规定以外的杂质:增加杂质控制项目,并经国家药典委员会审核后,报国家食品药品监督管理局批准新药研究(或新发现)的杂质和新降解产物:分离纯化制备或合成制备,用以进行结构鉴定,安全性及质量研究杂质检查项目的确定•新原料药和新制剂中的杂质研究–国家有关新药申报要求–ICH文本:Q3A(新原料药中的杂质)Q3B(新制剂中的杂质)Q3C(残留溶剂)•定性或确证结构:•表观含量≥0.1%的杂质或降解产物•表观含量<0.1%,具强烈生物作用或毒性的杂质,以及降解产物杂质检查分析方法1.分离度:主成分与杂质和降解产物均能分开2.灵敏度:LOD (限度检查), LOQ (定量检查)3.方法验证杂质检查分析方法应专属、灵敏。
并尽量采用现代分离分析手段。
色谱法杂质限度检查受色谱参数设置的影响较大。
液相色谱法进行有关物质检查仪器要求:1.检测灵敏度:波长,灯能量,流通池,检测器采样速率(响应时间)进样量等色谱条件2.数据处理:积分参数•已知杂质:采用对照品,或相对保留时间定位•专属性:采用DAD确定UV光谱或不同波长的响应情况•定量:已知杂质:测定对主成分的相对响应因子(0.9~1.1)未知杂质:主成分自身对照品液相色谱进行有关物质检查注意事项•杂质确定•DAD, MSD确定杂质峰的数目•空白试验:空白溶剂,空白梯度•灵敏度:•紫外灯的能量,采样速率•检测器流通池大小•仪器连接管线应尽量减小柱外体积,避免色谱峰的扩散•系统残留•手动进样阀的清洗•自动进样器应采用洗针进样模式。
药物分析

药物中的亚硫酸氢钠对下列哪种含量测定方法有干扰?•A、非水溶液滴定法•B、紫外分光光度法•C、汞量法•D、碘量法正确答案: D 我的答案:D 得分:3.3分2中国药典正确的表达为?•A、中华人民共和国药典••B、中国药典(2015年版)••C、Ch.P••D、中国药典•正确答案: B 我的答案:B 得分:3.3分答案解析:3以下哪种药物中检查对氨基酚?•A、盐酸普鲁卡因•B、对乙酰氨基酚•C、阿司匹林•D、对氨基水杨酸钠正确答案: B 我的答案:D 得分:0.0分4有氧化产物存在时,吩噻嗪类药物的鉴别或含量测定方法可选择?•A、钯离子比色法•B、非水溶液滴定法•C、紫外分光光度法•D、酸碱滴定法正确答案: A 我的答案:C 得分:0.0分5四氮唑比色法可用于哪个药物的含量测定?•A、黄体酮注射液•B、炔诺酮片•C、氢化可的松乳膏•D、甲基睾丸素片正确答案: C 我的答案:C 得分:3.3分6一般不用于巴比妥类药物鉴别的金属盐是•A、铜盐••B、银盐••C、汞盐••D、锌盐••E、钴盐•正确答案: D 我的答案:D 得分:3.3分7《中国药典》中的“精密称定”是指称取重量应准确至所取重量的•A、10%••B、15%••C、百分之一••D、千分之一••E、万分之一•正确答案: D 我的答案:D 得分:3.3分8乙醇未指明浓度时,均系指•A、无水乙醇••B、30%(ml/ml)乙醇••C、50%(ml/ml)乙醇••D、75%(ml/ml)乙醇••E、95%(ml/ml)乙醇•正确答案: E 我的答案:E 得分:3.3分9采用TLC法鉴别药物时,常常比较供试品与对照品的•A、比移值••B、斑点形状••C、••D、理论板数••E、分离度•正确答案: A 我的答案:A 得分:3.3分10中国药典中,检查维生素E的生育酚杂质所采用的检查方法是•A、薄层色谱法••B、纸色谱法••C、碘量法••D、••E、紫外分光光度法•正确答案: D 我的答案:D 得分:3.3分11各国药典对甾体激素类药物的含量测定主要采用HPLC法,主要原因是•A、它们没有紫外吸收,不能采用紫外分光光度法••B、不能用滴定法进行分析••C、由于“其它甾体”的存在,色谱法可消除它们的干扰••D、色谱法比较简单,精密度好••E、色谱法准确度优于滴定分析法•正确答案: C 我的答案:C 得分:3.3分12中国药典(2005年版)三部中收载的药物主要是•A、化学合成药•B、抗生素•C、放射性药物•D、生物制品•E、生化药物正确答案: D 我的答案:D 得分:3.3分二.多选题(共11题,36.3分)1药品质量标准分析方法的验证指标包括?•A、耐用性•B、检测限与定量限•C、精密度与准确度•D、专属性•E、线性与范围正确答案: ABCDE 我的答案:ABCDE 得分:3.3分2药用芳酸一般为弱酸,其酸性:•A、较碳酸弱•B、较盐酸弱•C、较酚类强•D、较醇类强•E、较碳酸强正确答案: BCDE 我的答案:BCDE 得分:3.3分3亚硝酸钠滴定法中,可用于指示终点的方法有?•A、内指示剂法•B、永停法•C、外指示剂法•D、电位法•E、自身指示剂法正确答案: ABCD 我的答案:BD 得分:1.6分4用于吡啶类药物鉴别的开环反应有?•A、茚三酮反应•B、戊烯二醛反应•C、二硝基氯苯反应•D、坂口反应•E、硫色素反应正确答案: BC 我的答案:BC 得分:3.3分5原料药的含量测定方法一般考虑采用•A、紫外分光光度法••B、准确度高的方法••C、专属性强的方法••D、容量分析法••E、高效液相色谱法•正确答案: BD 我的答案:BCD 得分:0.0分6下列试剂中,可用于氢化可的松反应呈色鉴别的有•A、2,4-二硝基苯肼/H+••B、浓硫酸••C、硫酸苯肼/H+••D、异烟肼/H+••E、红四氮唑/H+•正确答案: ABCDE 我的答案:ABCDE 得分:3.3分7影响酸性染料比色法的因素有•A、水相的pH•B、染料及其浓度的选择••C、有机溶剂的选择••D、容器的选择••E、水分的影响•正确答案: ABCE 我的答案:ABCE 得分:3.3分8下列方法中,可用于苯巴比妥类药物含量测定的有•A、碘量法••B、银量法•C、紫外分光光度法••D、酸碱滴定法••E、溴量法•正确答案: BCDE 我的答案:BCDE 得分:3.3分9药物分析的任务是•A、常规药品检验••B、制订药品标准••C、参与临床药学研究•D、药物研制过程中的分析监控••E、药理动物模型研究•正确答案: ABCD 我的答案:ABCD 得分:3.3分10鉴别药物的方法有•A、化学方法••B、分光光度法••C、色谱法••D、生物学方法•E、干法•正确答案: ABCD 我的答案:ABCD 得分:3.3分11色谱法用于定量的参数是•A、保留时间••B、峰高••C、峰面积••D、峰宽••E、死时间正确答案: BC 我的答案:BC 得分:3.3分三.判断题(共7题,24.1分)1水杨酸可在碱性条件下与三氯化铁试液反应生成紫堇色配位化合物。
中国药科大学--药物分析--期末试卷A卷(4套)

中国药科大学药物分析期末试卷(A卷)2006-2007学年第一学期一、选择题(请将应选字母填在每题的括号内。
共40分)(一)、最佳选择题(每题的备选答案中只有一个最佳答案。
每题1分)1. 微孔滤膜法是用来检查( )。
A.氯化物B.砷盐C.重金属D.硫化物E.氟化物2. 药典所指的"精密称定"系指称取重量应准确至所取重量的( )。
A.百分之一B.千分之一C.万分之一D.十万分之一E.百万分之一3. 药用规格是指药物( )。
A.符合分析纯的规定B.绝对不存在杂质C.对病人无害D.不超过该药物杂质限量的规定E.含量符合药典的规定4. 醋酸可的松的鉴别方法为( )。
A.二银盐沉淀法B.四氮唑比色法C.甲醛硫酸反应法D.重氮化反应法E.三氯化铁比色法5. 中国药典收载的原料药品种项下不包括( )。
A.品名B.性状C.含量规定D.含量均匀度E.检查6.下列叙述中不正确的说法是( )。
A.鉴别反应完成需要一定时间B.鉴别反应不必考虑"量"的问题C.鉴别反应需要有一定专属性D.鉴别反应需在一定条件下进行E.温度对鉴别反应有影响7. 维生素E含量测定方法为( )。
A. UVB. GCC. IRD. 异烟肼法E. 非水溶液滴定法8. 青霉素碘量法测定中,空白试验应加入( )。
A. 盐酸B. 高氯酸C. 氢氧化钠D. 样品E. 不加样品9. 头孢菌素类药物中聚合物检查用的柱填料为( )。
A. ODSB. 硅胶C. GDXD. 葡聚糖凝胶E. 蓝色葡聚糖10. 鉴别氯氮卓的方法可采用酸水解后呈色的反应为( )。
A. 重氮化-偶合反应B. 三氯化铁反应C. 茚三酮反应D. 亚硝基铁氰化钠反应E. 四氮唑盐反应11.麦芽酚反应可用于鉴别的药物为( )。
A. 雌激素B. 链霉素C. 维生素B1D. 皮质激素E. 维生素C12.维生素C注射液碘量法中应加入( )。
A. 甲酸作掩蔽剂B. 甲醇作掩蔽剂C. 丙酮作掩蔽剂D. 丙醇作掩蔽剂E. 氢氧化钠试液13. 回收率试验用于药品质量标准分析方法验证的内容为( )。
关于《中国药典》2010年版盐酸组氨酸及谷氨酸中其他氨基酸项下系统适用性要求的商榷

关于《中国药典》2010年版盐酸组氨酸及谷氨酸中其他氨基酸项下系统适用性要求的商榷程速远;张慧;梁成罡【期刊名称】《中国药品标准》【年(卷),期】2013(014)003【摘要】盐酸组氨酸和谷氨酸是《中国药典》2010年版二部收载的氨基酸类药物,且二者均收载于《英国药典》和《欧洲药典》。
盐酸组氨酸收载于《美国药典》,《日本药局方》未收载这两个品种。
《中国药典))2005年版二部收载的这两个品种的其他氨基酸检查项下均无系统适用性要求,2010年版增加了系统适用性要求。
但是,系统适用性试验结果都存在一些问题,前者的系统适用性结果是脯氨酸的斑点不够清晰,加大上样量后斑点清晰度提高;后者系统适用性结果是门冬氨酸的斑点不显色,无法判定系统适用性是否符合要求,增加门冬氨酸浓度后斑点显色明显,为此笔者认为对系统适用性溶液的配制及点样量提出商榷。
【总页数】2页(P168-169)【作者】程速远;张慧;梁成罡【作者单位】中国食品药品检定研究院,北京100050;中国食品药品检定研究院,北京100050;中国食品药品检定研究院,北京100050【正文语种】中文【中图分类】R921.2【相关文献】1.2010年版《中国药典》中动物药质量标准商榷 [J], 高晓晨;孙佳明;刘冬;杜婷婷;张辉2.《中国药典》2000年版二部中有关颗粒剂项下值得商榷的问题 [J], 邵建强3.关于在《中国药典》2010年版一部儿茶[检查]项下增加水中不溶物检查的建议及含量测定的探讨 [J], 曾德成4.关于《中国药典》2005年版二部阿昔洛韦含量测定项下系统适用性试验溶液配制的商榷 [J], 杨兴明;黄慧芬5.中国药典(2000年版,一部)人参健脾丸项下当归的检验标准商榷 [J], 刘志荣;姜文茹;杨志伟;郭颖;冯榜超因版权原因,仅展示原文概要,查看原文内容请购买。
生化药物质量标准中的生物检定及其进展

生长激素
重法和胫骨法
重组人胰岛素 小鼠或家兔血糖法 HPLC
降钙素
大鼠血钙法
HPLC
低分子肝素 血浆凝固法或家兔 分光光度法 全血凝固法
ChP2005 BP2007 ChP2005 BP2007 ChP2005 BP2007 BP2007
在本实验室已用理化测定代替生物测定 两种方法间具有良好相关性(P﹤0.01)的品种
活性测定分类
活性测定---定量:质量标准中生物效价 测定(HCG、HMG、肝素)
---半定量 ---定性
活性测定------半定量
半定量------当理化测定占主导地位,生物效价 测定降为辅助作用,只用于活性检查,设定限 值,采用半定量方法,不需精确的生物统计, 尽可能减少实验动物用量
如治疗二型糖尿病新药重组人胰高血糖素类多 肽-1(7-36)质量标准中采用半定量方法(限 值为小鼠血糖降低应大于20%)进行活性检查
生化药名
生物测定方法
理化测定方法 收载标准
伟素
大鼠血脂清除率法 分光光度法
(Sulodexide)
重组绒促性素 幼小鼠子宫增重法 HPLC (rHCG)
重组卵泡刺激 幼大鼠卵巢增重法 HPLC 素(rFSH)
重组黄体生成 幼大鼠精囊增重法 HPLC 素(rLH)
企业标准 企业标准 企业标准 企业标准
BP2007版胰岛素采用HPLC法
ChP2005版二部,动物胰腺提取的胰岛素定量生物测定
中国药典2010年版二部生化药品专业科研项目
1、药品中氨基酸分析方法的研究(归纳分类)。(中检所负责) 2、蛋白质含量测定方法的规范化研究,增订附录。(上海所负
责) 3、人工肠液和胃液中所用酶试剂的标准化研究。(中检所和北
甘氨酸全面介绍

甘氨酸全面介绍甘氨酸科技名词定义中文名称:甘氨酸英文名称:glycine;Gly定义:学名:2-氨基乙酸。
非手性分子,最简单的天然氨基酸。
L-甘氨酸是蛋白质合成中的编码氨基酸,哺乳动物非必需氨基酸,在体内可以由葡萄糖转变而来,因具有甜味而得名。
符号:G。
应用学科:生物化学与分子生物学(一级学科);氨基酸、多肽与蛋白质(二级学科)以上内容由全国科学技术名词审定委员会审定公布甘氨酸(Glycine)又名氨基乙酸,为非人体必需氨基酸。
名称缩写:Gly 甘氨酸是氨基酸系列中结构最为简单,人体非必需的一种氨基酸,在分子中同时具有酸性和碱性官能团,在水溶液中为强电解质,在强极性溶剂中溶解度较大,基本不溶于非极性溶剂,而且具有较高的沸点和熔点,通过水溶液酸碱性的调节可以使甘氨酸呈现不同的分子形态。
目录成分及性质1.基本信息2.性能描述3.物理参数4.用途说明5.危险说明6.物化性质7.甘氨酸的生理作用8.甘氨酸的合成9.极性药物分析用途1.食品级甘氨酸2.医药级甘氨酸3.饲料级甘氨酸4.工业级甘氨酸2010版中国药典内容展开成分及性质1.基本信息2.性能描述3.物理参数4.用途说明5.危险说明6.物化性质7.甘氨酸的生理作用8.甘氨酸的合成9.极性药物分析用途1.食品级甘氨酸2.医药级甘氨酸3.饲料级甘氨酸4.工业级甘氨酸2010版中国药典内容展开成分及性质基本信息甘氨酸产品编号:FZS118中文名称:甘氨酸中文别名:甘氨酸;氨基乙酸,氨基醋酸英文名称:Aminoacetic acid英文别名:Gly ;Amino acetic acid;Aminoethanoic acid;Glycine 线性分子式:NH2CH2COOH分子结构式[1]等级:ARCAS号:56-40-6分子式:C2H5NO2分子量:75.07相对密度1.595[2]熔点182℃[2]性能描述外观描述:白色结晶或结晶性粉末。
味甜。
溶于水,微溶于吡啶,不溶于乙醚。
中国药典2005年版收载毒性常用中药简介_孙桂凤

苷 、松醇(pino1)等化合物
9
半夏
辛, 温
脾 、胃 、肺
含 β-谷 甾 醇 及 其葡 萄 糖 苷 , 胆 碱 ;尚 含 高龙 胆 酸(homogen tisic acid)、草 酸 钾等 无 机 盐和 天 门 冬氨 酸 、谷 氨 酸 、精氨酸 、β-与 γ-氨基 丁酸 、半 乳糖 、粘液质 、少量挥 发 油 、原儿茶醛(prot ocatechuic aldehyde)、三萜类化合物 、原 儿茶酸等 ;还分离出一种结晶性蛋白质为半夏蛋白
北乌头 :含总碱 0.7 % ~ 1.3 %。 南乌 头(贵州):含总 碱 0.82 %~ 1.56 %
斑蝥素
外用适 量 , 研 末 涂 患 处, 或 捣烂以纱布包擦患处
一般炮制后 用 , 生品 内服 宜 慎。 炮制后多入丸散 , 每次 0.03 ~ 0.06g ;外用适量
性味 辛 、温 苦, 寒
苦 、辛 , 温
〔9〕张治锬 .抗生素药品检验〔M 〕.北京 :人民卫生出版社 , 1987 , 80. 〔10〕赵肃清 , 蔡燕飞 , 文永新 , 等 .银杏外种皮提取液对农作物病原菌
抑制效应研究〔J〕.农业环境保护 , 2001 , 20(5):368-369. 〔11〕陈雄 , 乔昕 , 林向东 , 等 .大 蒜油抗菌 作用的 初步研 究〔J〕.中国
毒的概念是广义的 , 药物各有偏性 , 这种偏性就是毒 。 明 代医家张景 岳〔2〕 对于 作为 药物 偏性 之毒 的含 义也 作了 明确 的阐述 :“ 药 以治 病 , 因 毒 为能 , 所谓 毒 药 , 是 以 气 味 有偏 也 … … 。” 魏晋以后 , 毒药的含义逐渐衍变成专指那些药性 强烈 、 服后容易出现毒副作用甚至致死的药物 。 这种认识与现代对 毒药的认识比较接近 , 毒 , 不再指药物的偏性 。 现代中草药书
药物分析习题集含答案

一、单选题(A1型题-最佳选择题)(本大题共42小题,共42分)1. 英文缩写字母GLP代表A.《药品非临床研究质量管理规定》B.《药品生产质量管理规范》C.《药品经营质量管理规范》D.《药品临床试验管理规范》2. 我国现行药品质量标准有A、国家药典和地方标准B、国家药典、部颁标准和国家药监局标准C、国家药典、国家药监局标准(部标准)和地方标准D、国家药监局标准和地方标准E、国家药典和国家药品标准(国家药监局标准)3. 药典规定取用量为“约”若干时,系指取用量不得超过规定量的A、±0.1%B、±1%C、±5%D、±10%E、±2%4. 中国药典(2000年版)中规定,称取“2.00g”系指A.称取重量可为1.5-2.5gB.称取重量可为1.95-2.05gC.称取重量可为1.995-2.005gD.称取重量可为1.9995-2.0005g5. 药典中若规定取样量为“称取2g”,系指称取重量范围为:A.1.0~3.0gB.1.5~2.5gC.1.6~2.4gD.1.00~2.00g6. 我国药典修订一次是A.10年B.7年C.5年D.3年E.1年7. 滴定液的浓度系指:A.mol/LB.mmol/LC.g /100mlD.%(ml/ml)8. 原料药含量百分数如未规定上限,系指不超过A、100.1%B、101.0%C、100.0%D、100%E、110.0%9. 中国药典主要内容分为A、正文、含量测定、索引B、凡例、制剂、原料C、鉴别、检查、含量测定D、前言、正文、附录E、凡例、正文、附录10. 2009年以前,中华人民共和国共出版了几版药典A.6版B.7版C.8版D.9版11. 中国药典规定溶液的百分比,指A、100mL中含有溶质若干毫升B、100g中含有溶质若干克C、100mL中含有溶质若干克D、100g中含有溶质若干毫克E、100g中含有溶质若干毫升12. 药物中氯化物杂质检查的一般意义在于A.它是有疗效的物质B.它是对药物疗效有不利影响的物质C.它是对人体健康有害的物质D.可以考核生产工艺中容易引入的杂质13. 药物纯度合格是指A、含量符合药典的规定B、符合分析纯的规定C、绝对不存在杂质D、对病人无害E、不超过该药杂质限量的规定14. 检查芳环或芳杂环有机药物的重金属时,需先破坏有机物,炽灼温度为:A、500~700℃B、600~800℃C、400~500℃D、500~600℃15. 炽灼残渣检查后,将残渣留作重金属检查时,炽灼温度是:A.400~500℃B.500~600℃C.600~700℃D.700~800℃16. 利用药物和杂质在物理性质上的差异是指:A、臭味及挥发性、颜色、溶解性、旋光性质、对光选择吸收性质B、臭味及挥发性、颜色、溶解性、酸碱性、色谱行为C、臭味及挥发性、颜色、旋光性质,对光选择吸收性质及氧化还原性D、臭味及挥发性、颜色、溶解性、酸碱性及氧化还原性17. 称取柠檬酸钠2.0g,加水溶解,加稀醋酸10ml与水适当使成25ml,依规定方法检查重金属,与1.0ml标准铅溶液(10μg/ml)用同法制成的对照液比较,不得更深。
关于颁布布和执行中国药典2005年版有关事宜的通知

关于颁布布和执行《中国药典》2005年版有关事宜的通知各省、自治区、直辖市食品药品监督管理局(药品监督管理局):根据《药品管理法》及《药品管理法实施条例》的有关规定,现颁布《中华人民共和国药典》(以下简称《中国药典》2005年版,于2005年7月1日起执行。
《中国药典》是国家h保证药品质量、保护人民用药安全有效而制定的法典;是执行《药品管理法》、监督检验药品质量的技术法规;是我国药品生产、经营、使用和监督管理所必须遵循的法定依据。
《中国药典》收载品种的标准为国家对该药品品种的最基本要求。
《中国药典》2005年版在标准要求、形式内容等方面,与2000年版相比均有重大改进和提高,更加符合当前我国药品生产、经营和管理的实际情况。
作好宣传、执行新版《中国药典》,对于保证药品质量、促进我国医药工业的发展都具有十。
分重要的作用。
各级药品监督管理部门要给予高度重视。
现就执行《中国药典》2005年版的有关事宜通知如下:一、自执氘之日起,与《中国药典》2005年版同品种的原国家药品标准和试行标准停止执行。
2005年7月1目前生产的药品,仍按原标准进。
行检验。
对于检测项目多于药典规定的或检测指标高于药典要求的应当按原批准的标准执行。
二、《中国药典》2000年版及其增补本和《中国生物制品规程》2000年版及其增补本收载,但《中国药典》2005年版未收载的品种,暂仍按原标准执行。
《中国药典》2005年版品种项下未列出的规格应当按批准证明文件执行。
三、自执行之日起所生产的《中国药典》品种,其新印制的药品包装、标签及说明书必须注明《中国药典》2005年版规定的药品通用名称。
对于名称已作修订的药品,其原通用名称过渡使用至2006年12月31日。
执行之日前印制的药品包装、标签及说明书,可以继续流通使用完毕。
四、为指导临床用药,保证中成药在临床中使用安全有效,《中国药典》2005年版对中成药标准项下【功能与主治】进行了规范,各药品生产企业要关注各自的品种,按我局《药品注册管理办法》有关要求,做好说明书修改工作。
2005药典一部薄层、含量测定检索表
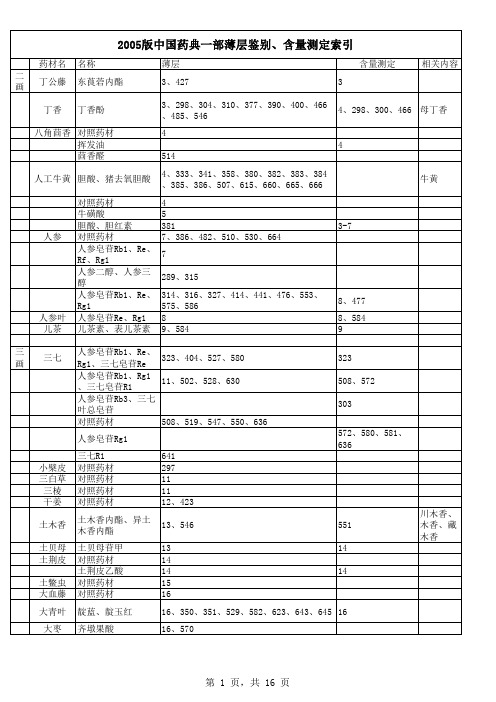
59、294、312、321、322、335、352、354 、355、356、357、358、368、420、423、 435、436、455、479、493、510、519、 564、565、570、585、589、590、601、 608、618、654 59、557、570 60 60 305、349、370、374、388、399、428、 518、520、618、621、625 306、311、399、 480 423、468、479、 520、570 305 60 61 62、452 64 296、297 64、416 65、416 川贝母、湖北贝母 65 、伊贝母、土贝母 66、418、486 418 67 67 67 第 4 页,共 15 页
牛蒡子
对照药材 牛蒡苷
第 3 页,共 15 页
牛膝 毛诃子 升麻 片姜黄 化橘红 丹参
齐墩果酸 对照药材 没食子酸 阿魏酸 异阿魏酸 对照药材 柚皮苷 对照药材 丹参酮ⅡA 原儿茶酸 原儿茶醛 丹酚酸B 丹参素
49、325、361、491、505、570 471 50 50 50 51 51 52、375、452、500、550、584 52、375、394、398、426、481、527、575 、655 361 290、640 52 372、404、501、528、624、653 53 53 54 54 54 55
54
55 55 56 57 56 57 58 58
五画
玉竹 功劳木
58 58
甘草
对照药材
甘草酸铵 甘草苷 甘草次酸
甘草酸 甘青青蓝 对照药材 甘遂 对照药材 石韦 绿原酸 石菖蒲 对照药材 石膏 含水硫酸钙 节裂角茴香 对照药材 龙胆 龙胆苦苷 平贝母 北豆根 仙茅 白及 平贝碱甲 对照药材 蝙蝠葛碱 仙茅苷 对照药材
中国药典版二部概况

各论的增修订情况(1):名称与性状
含量限度 (原料药) ➢ 一般换算成以干燥品或无水物或炽灼品计算的含量。
✓ (1)“按干燥品计算”—检查“干燥失重” ✓ (2)“按无水物计算”—检查“水分” ✓ (3)“按无水物与无溶剂物计算”—如含挥发性有机溶剂
且有机溶剂量明显影响含量结果时(如:秋水仙碱、盐酸帕 罗西汀)
➢ 两个色阶相邻,可用“或”来描述 ➢ 类白色或微黄色结晶性粉末
➢ 色阶之间相隔两个以上,应采用“至”来描述 ➢ 类白色至淡黄色结晶性粉末
➢ 引湿性:更多品种中增加了对引湿性的描述(中国药典2005年版二部附 录XIX J“药物引湿性指导原则)。实验时是关键信息 (对照品的处理)。
标准中有较大变化的部分制剂品种(4)
• 呋噻米注射液,吡哌酸胶囊、片,吲哚美 辛肠溶片、乳膏,利福平注射液,谷氨酸 钾注射液,泛酸钙片,阿司匹林肠溶片, 阿普唑仑片,环扁桃酯胶囊,苯巴比妥钠 片,注射用苯妥英钠,非诺贝特片、胶囊, 罗通定片,洛莫司汀胶囊,辛伐他汀片、 胶囊,非诺贝特胶囊,
标准中有较大变化的部分制剂品种(5)
• 复方十一烯酸锌软膏,复方酮康唑乳膏, 复方磺胺嘧啶片,盐酸肾上腺素注射液, 依诺沙星片、胶囊,法莫替丁注射液,苯 苯海明片,苯硷缓释片,枸橼酸他莫苷芬 片,枸橼酸芬太尼注射液,枸橼酸喷托维 林片,氟康唑氯化钠注射液,氢化可的松 注射液,氢氯噻嗪片,氢溴酸东莨菪硷注 射液,重酒石酸间羟胺注射液,复方卡托 普利片,复方克霉唑乳膏,复方盐酸阿米 洛利片,复方磺胺甲噁唑注射液,
标准中有较大变化的部分制剂品种(8)
• 盐酸罗通定片,盐酸哌唑嗪片,盐酸哌替 啶片、注射液,盐酸氟奋乃近片、注射液, 盐酸美沙酮片、注射液,盐酸倍他司汀片, 盐酸胺碘酮片、注射液、胶囊,盐酸麻黄 碱注射液、滴鼻液,盐酸维拉帕米缓释片, 盐酸氯西那林片,盐酸氯米帕明片,盐酸 氯胺酮注射液,盐酸普鲁卡因注射液,
我国生化药的现状和发展趋势

ATP-2Na注射液
利巴韦林胶囊
注射用ATP-2Na
利巴韦林颗粒
肌苷
利巴韦林滴眼液
肌苷口服溶液
利巴韦林滴鼻液
肌苷片 肌苷注射液 肌苷胶囊 更昔洛韦 更昔洛韦氯化钠注射液 注射用更昔洛韦 利巴韦林
利巴韦林口服液 利巴韦林片 利巴韦林含片
注射用利巴韦林
利巴韦林氯化钠注射液 利巴韦林葡萄糖注射液 泛昔洛韦 泛昔洛韦片 泛昔洛韦胶囊 阿昔洛韦 阿昔洛韦片 阿昔洛韦乳膏 阿昔洛韦咀嚼片
甘露聚糖 甘露聚糖口服溶液 甘露聚糖片 甘露聚糖注射液 甘露聚糖胶囊 银杏蜜环口服溶液 盐酸氨基葡萄糖 云芝胞内糖肽 云芝胞内糖肽口服溶液 云芝胞内糖肽片 香菇菌多糖 香菇菌多糖片 云芝胞内糖肽胶囊
2021/8/2
26
脂(国家标准)
大豆磷脂粉 卵磷脂 卵磷脂片 角鲨烯 角鲨烯胶丸 多烯酸乙酯 多烯酸乙酯胶丸 蛹油α-亚麻酸乙酯 蛹油α-亚麻酸乙酯胶丸
4.多肽, 7%
3.酶与辅酶, 17%
1.aa及其衍生物 3.酶与辅酶 5.多糖 7.其它 2021/8/2
2.蛋白 4.多肽 6.核苷酸及其衍生物
19
氨基酸及其衍生物(国家标准)
乙酰半胱氨酸(供滴眼剂用) 乙酰半胱氨酸滴眼液 乙酰谷酰胺 乙酰谷酰胺注射液 门冬氨酸钾镁片 小儿盐酸赖氨酸颗粒 谷丙甘氨酸胶囊 复方谷氨酰胺肠溶胶囊 复方亮氨酸颗粒(3AA) 复方盐酸赖氨酸片 复方氨基酸注射液(6AA) 复方氨基酸注射液(17AA-1)
2021/8/2
23
多肽(国家标准第十六册)
脑蛋白水解物注射液 肌氨肽苷注射液 小牛血去蛋白提取物注射液 骨肽注射液 转移因子溶液 转移因子口服溶液 转移因子注射液 转移因子胶囊 注射用转移因子 氨碘肽注射液 胸腺肽溶液
氨基酸与生化药物

膜的副作用
碳酸钙, 甘氨酸 胃-肠酸过高
丙 氨 酸, 盐 酸赖 氨 营养制剂
酸, 盐 酸谷氨酸, 酪
氨酸
碳酸 氢钠, 枸橼酸, 抗高酸
阿 司 匹 林, 苯丙 氨
酸
硫 酸 新 霉 素, 杆 菌 外 用 粉和 软 膏 剂,
肽锌, 甘氨酸, 半胱 皮肤细菌感染
氨酸, 苏氨酸
美 Am ino-Cer v
氨基酸和生物资源 Amino Acids & Biot ic R esou rces 1999, 21(4) : 1~3
·1·
氨基酸与生化药物X
张天民 王凤山
( 山东医科大学药学院 济南 250012)
摘要 回顾中国氨基酸类药物的发 展历程, 并对2000年后的发展提出意见。 关键词 氨基酸 生化药物 发展 历程 展望
由表7可见, 国外的氨基酸制剂涉及面广, 充分利用了氨基酸的营养, 无毒性和对酸、碱的 缓冲作用等。在这方面, 我国的发展潜力很大, 在 21 世纪 将 有 更 多的 、有 特 色 的氨 基 酸 制剂 问 世。
参考文献
1 张天民 , 姚世文, 唐永业. 中 国生化药物杂志, 1995, 16( 5) : 240
生化药物是从生物体分离、纯化所得, 用于 预防、治疗和诊断疾病的生化基本物质, 以及用 化学合成或现代生物技术制得的这类药物[ 1] 。 其生化本质主要是氨基酸、肽、蛋白质、酶及辅 酶、多糖、脂质、核酸及其降解产物等。氨基酸是 一类重要的生化药物。新中国建立后, 50年来氨 基酸类药物有了长足的发展, 现对其发展历程 进行回顾, 并对2000年后的发展加以展望。
Amino Acids and Biochemical Drugs
Zhan T ianmin Wang Fengshan ( College of P harmacy, Sha ndong Medical Univesity, J inan 250012)
中国药典2005二部凡例及附录

二 部凡例目次(增修订的附录)附录Ⅰ制剂通则Ⅰ A 片剂Ⅰ B 注射剂Ⅰ C 酊剂Ⅰ D 栓剂Ⅰ E 胶囊剂Ⅰ F 软膏剂乳膏剂糊剂Ⅰ G 眼用制剂Ⅰ H 丸剂Ⅰ J 植入剂(增订)Ⅰ K 糖浆剂Ⅰ L 气雾剂粉雾剂喷雾剂Ⅰ M 膜剂Ⅰ N 颗粒剂Ⅰ O 口服溶液剂口服混悬剂口服乳剂Ⅰ P 散剂Ⅰ Q 耳用制剂Ⅰ R 鼻用制剂Ⅰ S 洗剂冲洗剂灌肠剂Ⅰ T 搽剂涂剂涂膜剂Ⅰ U 凝胶剂Ⅰ V 贴剂附录Ⅳ分光光度法Ⅳ A 紫外-可见分光光度法Ⅳ C 红外分光光度法Ⅳ D 原子吸收分光光度法Ⅳ E 荧光分析法Ⅳ F 火焰光度法附录Ⅴ色谱法Ⅴ B 薄层色谱法Ⅴ D 高效液相色谱法Ⅴ E 气相色谱法Ⅴ G 毛细管电泳法Ⅴ H 分子排阻色谱法附录ⅥⅥ E 旋光度测定法Ⅵ G 黏度测定法Ⅵ H pH值测定法附录ⅦⅦ H 脂肪与脂肪油测定法附录ⅧⅧ L 干燥失重测定法Ⅷ N 炽灼残渣检查法Ⅷ P 残留溶剂测定法(原有机溶剂残留量测定法)Ⅷ Q 热分析法Ⅷ R 制药用水中总有机碳测定法(增订)附录ⅨⅨ A 溶液颜色检查法Ⅸ C 注射剂中不溶性微粒检查法Ⅸ D 结晶性检查法Ⅸ E 粒度和粒度分布测定法Ⅸ F X射线粉末衍射法Ⅸ G 渗透压摩尔浓度测定法Ⅸ H 可见异物检查法(原澄明度检查法)Ⅸ J 质谱法(增订)附录ⅩⅩ A 崩解时限检查法Ⅹ C 溶出度测定法Ⅹ D 释放度测定法Ⅹ E 含量均匀度检查法Ⅹ G 片剂脆碎度检查法Ⅹ H 吸入气雾剂、吸入粉雾剂、吸入喷雾剂的雾滴(粒)分布测定法Ⅹ J 锥入度测定法(增订)Ⅹ K 贴剂黏附力测定法(增订)附录ⅪⅪ A 抗生素微生物检定法Ⅺ C 异常毒性检查法Ⅺ D 热原检查法Ⅺ E 细菌内毒素检查法Ⅺ G 降压物质检查法Ⅺ H 无菌检查法Ⅺ J 微生物限度检查法Ⅺ K 过敏反应检查法(增订)附录ⅫⅫ O 降钙素生物检定法(增订)Ⅻ P 生长激素生物测定法(增订)附录ⅩⅥ制药用水附录ⅩⅦ灭菌法附录ⅩⅨⅩⅨ A 药品质量标准分析方法验证指导原则ⅩⅨ B 药物制剂人体生物利用度和生物等效性试验指导原则ⅩⅨ C 原料药与药物制剂稳定性试验指导原则ⅩⅨ D 缓释、控释和迟释制剂指导原则ⅩⅨ E 微囊、微球与脂质体制剂指导原则ⅩⅨ F 药品杂质分析指导原则(增订)ⅩⅨ G 正电子类放射性药品质量控制指导原则(增订)ⅩⅨ H 含锝[99m Tc]放射性药品质量控制指导原则(增订)ⅩⅨ J 药物引湿性指导原则(增订)返回顶端凡 例《中华人民共和国药典》简称《中国药典》,是国家监督管理药品质量的法定技术标准。
2005年版中国药典抗生素

2005年版《中国药典》抗生素品种高效液相色谱法的增修订情况简介余立(北京药检所)一、 概述2005年版《中国药典》中收载的抗生素品种共有284个,其中使用了HPLC法的品种有205个,约占70%。
用于检测的项目有:鉴别、有关物质检查、组分测定、含量均匀度和含量测定。
与2000年版《中国药典》相比,2005年版《中国药典》抗生素品种对HPLC法的使用在应用范围上有所扩大。
2005年版《中国药典》抗生素品种中有41个2000年版《中国药典》原有品种在鉴别项中增加了HPLC法,替代了原来专属性不强的项目,有效减少了不同药品具有相同鉴别反应现象的几率。
比如:红霉素硫酸显色→HPLC青霉素钠、钾酶灭活→HPLC依诺沙星丙二酸+醋酐显色→HPLC绝大多数新增品种在鉴别项中选用了HPLC法,如新增的沙星和头孢类品种。
有39个2000年版《中国药典》原有品种将含量测定方法由微生物效价检定法、UV法、电位滴定法等专属性不强的方法改用了HPLC 法,使降解产物、辅料不再干扰对主成分的测定,高科技造假物也不能鱼目混珠了。
同时对于某些品种也简化了实验操作,缩短了检验时限,降低了对实验者操作技能的要求。
比如:克拉霉素、罗红霉素由微生物效价→HPLC甲砜霉素/肠溶片/胶囊由电位滴定法→HPLC氯霉素/滴耳液由UV→HPLC大多数的新增品种在含量测定中选用了HPLC法,如:几乎所有的新增喹诺酮类和头孢类品种。
2005年版《中国药典》抗生素品种中有61个原有品种用HPLC 法增订了有关物质,其中有22个品种是从原来量加和较为困难的TLC法转用HPLC法的,还有30个增订品种的有关物质检查项选用了HPLC法另外,2005年版《中国药典》抗生素品种中有15个品种的组分测定采用了HPLC法。
二、色谱系统适用性试验的变化趋势HPLC法虽然是药物分析中定性、定量的一个很好的方法,但是色谱系统的有效性是其能否圆满完成使命的保证。
色谱系统的有效性通常是通过系统适用性试验来检验的。
(完整word版)药剂学填空题

1、随着药剂学的内容的发展,已形成工业药剂学、物理药剂学、药用高分子材料学、生物药剂学及临床药剂学、医学情报等分支学科。
2、《中国药典》2005年版的一部收载的为中药材和中成药,二部为化学药品、抗生素及其制剂,三部为生物制品。
3、药物制剂的发展可以分为以下几代:普通制剂、缓释制剂、控释制剂和体内反馈信息给药系统。
4、GMP是药品生产和管理的基本原则,其检查对象是人、生产环境和制剂生产的全过程。
5、医生处方具有法律、技术和经济的意义。
6、与固体制剂相比,液体制剂中的药物是以微粒或分子分散在介质中,故给药后吸收快。
7、液体制剂常用的半极性溶剂主要有乙醇、乙二醇和聚乙二醇。
8、液体制剂常用附加剂主要有增溶剂、助溶剂、潜溶剂、防腐剂、矫味剂和着色剂等。
9、酊剂的制备方法有溶解法、浸渍法和渗漉法。
10、制备高分子溶液要经过的2个过程是有限溶胀和无限溶胀。
11、乳剂是由油相、水相和乳化剂三者组成。
12、常用的湿热灭菌方法有热压蒸汽灭菌法、流通蒸汽灭菌法和低温间歇灭菌法。
13、影响湿热灭菌法的因素有微生物的种类、微生物的数量、蒸汽性质、药品性质及灭菌时间。
14、洁净度级别有100级、10000级、100000级和300000级。
15、洁净室要求温度为18~26℃,相对湿度为45~65%。
16、无菌检查方法有直接接种、波膜过滤法。
热原的检查方法有家兔实验法、鲎试剂法。
17、热原的基本性质有耐热性、过滤性、水溶性、不挥发性等。
18、出去热源的方法有高温法、酸碱法、吸附法、离子交换法等。
19、注射剂的附加剂主要有增溶剂、抗氧剂、pH调节剂、抑菌剂等。
20、制造安贞的玻璃主要有中性玻璃、含钴玻璃和含钡玻璃,其中含钴玻璃具有更高的化学稳定性,耐酸耐碱性能好。
21、注射液的配制方法有浓配法和稀配法,注射液灌装后封口的方法有拉封和顶封两种。
22、常用的助滤剂有硅藻土、活性炭、滑石粉、纸浆等。
23、常用的过滤器具有垂熔玻璃滤器、砂滤棒、板框式压滤机、微孔滤膜过滤器等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2005版中国药典收载的氨基酸原料药
L-胱氨酸的生产方法有:提取、发酵、合成;主要用途有:促进毛发生长,防治肝炎,增加巨细胞。
L-谷氨酸的的生产方法有:合成、发酵;主要用途有:改善高血氨症状,治疗肝昏迷。
L-门冬氨酸的生产方法有:酶工程;主要用途有:离子载体、促进尿素生成,降血氨。
L-甘氨酸的生产方法有:合成;主要用途有:治疗肌肉疾病,胃酸过多症,促进脂肪代谢。
L-色氨酸的生产方法有:提取合成;主要用途有:改善脑神经功能,促进红细胞再生,乳汁合成。
L-络氨酸的生产方法有:提取、发酵;主要用途有:治疗震颤性麻痹症,改善肌肉运动。
L-苏氨酸的生产方法有:发酵、合成、酶工程;主要用途有:促进生长发育,抗脂肪肝,治疗贫血。
L-亮氨酸的生产方法有:提取、发酵、合成;主要用途有:改善营养状态,维持脂肪正常代谢。
L-异亮氨酸的生产方法有:发酵、酶工程;主要用途有:促进蛋白质、激素合成、促进生长发育。
乙酰半胱氨酸的主要生产方法有:合成;主要用途有:溶解粘液,祛痰。
牛磺酸的生产方法有:合成;主要用途有:抗心肌缺铁损伤,抗癫痫。
L-丙氨酸的生产方法有:提取、酶工程;主要用途有:组成复合氨基酸注射液积口服液等的原料。
L-谷氨酸的生产方法有:发酵;主要用途有:促进氨代谢i,促进红细胞生成,抗癫痫。
甲硫氨酸的生产方法有:合成;主要用途有:参与体内生物合成与代谢,调节中枢神经系统。
L-精氨酸的生产方法有:提取;主要用途有:促进尿素循环,治疗按昏迷。
L-门冬酰胺的生产方法有:酶工程;主要用途有:辅助治疗乳腺小叶增生。
L-结氨酸的生产方法有:提取;主要用途有:作为营养补剂,促进蛋白质合成。
L-组氨酸的生产方法有:提取、发酵;主要用途有:镇静副交感神经,治疗消化性溃疡。
L-丝氨酸的生产方法有:提取、合成;主要用途有:作为营养补剂,解除疲劳,恢复体力
L-脯氨酸的生产方法有:发酵、合成;主要用途有:参与能量代谢及解毒作用。
