抗缪勒管激素测定试剂盒(化学发光免疫分析法)产品技术要求mairui
抗缪勒氏管激素检测SOP文件(iFlash3000)

抗缪勒氏管激素检测SOP文件1.检验目的:本试剂盒用于体外定量测定人血清和(或)血浆中的抗缪勒氏管激素。
2.检验原理:3.性能参数:3.1线性范围:0.10 ng/mL-16.00 ng/mL;3.2最低检测限:不大于0.010 ng/mL;3.3准确度:回收率在85.0%~115.0%范围内;3.4重复性:重复性检测的变异系数(CV)不大于10.0%;3.5批间差:3个批号试剂批间变异系数(CV)不大于15.0%;3.6特异性:用FSH浓度不低于200 IU/L的样本进行检测,检测结果不高于0.01ng/mL;用LH浓度不低于200 IU/L的样本进行检测,检测结果不高于0.01 ng/mL。
4.样品要求:4.1检测标本:血清和血浆(肝素锂、肝素钠、EDTA和柠檬酸钠抗凝)是推荐使用的样本类型。
尚未验证其他抗凝剂能否适用。
4.2采集及处理:在进行离心操作前需让血清样本完全凝结(凝结时间不小于1小时)。
所有的待测样本在测试前均应进行离心操作。
顶部含脂质的离心样本,需转移澄清、无脂质的部分到新的样本管中。
在测试前,确保已去除了残余的纤维蛋白和细胞类物质。
应小心处理患者样本,避免交叉污染。
在测试前,确保患者样本、校准品、质控品均已平衡至环境温度(20-25°C)。
为避免蒸发可能带来的影响,样本和校准品应在上机后2小时内完成测试。
4.3样品储存:在室温(20-25°C)下,样本保存时间不得超过4小时。
在2-8°C条件下,样本保存时间不得超过3天。
冷冻样本在融化后必须进行充分混匀。
样本冷冻次数不得超过1次5.设备和试剂:5.1仪器:iFlash 3000化学发光免疫分析仪。
5.2试剂:抗缪勒氏管激素测定试剂盒(化学发光法);包装量:2×50人份/盒;5.3储存要求:(1)储存:存放在2-8°C,保持竖直向上。
(2)有效期:试剂瓶及校准品未开封存放于2-8°C:可稳定365天;试剂瓶使用后存放于2-8°C或在机存储:可稳定28天;校准品复溶后在-20°C保存:可稳定28天(仅可冻融一次)。
抗缪勒氏管激素测定试剂盒(化学发光免疫分析法)产品技术要求新产业

2. 性能指标
2.1 外观和性状
试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰,准确、牢固;试剂盒内组分(磁性微球除外)应为澄清的液体,无沉淀、无悬浮物、无絮状物。
2.2 批内精密度
批内变异系数(CV)应≤8%。
2.3 批间精密度
批间变异系数(CV)应≤15%。
2.4 准确度
回收率应在(90.0%~110.0%)范围内。
2.5 空白限
空白限应≤0.020 ng/mL。
2.6 线性
在(0.100~25.0)ng/mL浓度区间内,线性相关性系数(r)绝对值应≥0.9900。
2.7 校准品均一性
校准品均一性(CV)应≤8%。
2.8 质控品测量准确度
质控品1测定结果应在[2.80~5.20] ng/mL范围内,质控品2测定结果应在[11.2~20.8]ng/mL范围内。
2.9 质控品均一性
质控品均一性(CV)应≤8%。
2.10 溯源性
本试剂盒校准品可以溯源至企业内部校准品。
第1页共1页。
抗缪勒氏管激素(AMH)测定试剂盒(光激化学发光法)产品技术要求kemei

抗缪勒氏管激素(AMH)测定试剂盒(光激化学发光法)适用范围:本试剂盒用于体外定量测定人血清中抗缪勒氏管激素(AMH)的含量。
1.1 产品型号说明:1. 校准品浓度批特异,详见定值单。
2. 质控品质控范围批特异,详见定值单。
2.1 外观试剂盒组分齐全,内外包装均完整,标签清晰,液体试剂无渗漏。
2.2空白限不高于0.02ng/mL。
2.3准确性回收率应在85.00%~115.00%范围内。
2.4线性在[0.02,24.00]ng/mL区间内,试剂盒剂量-反应曲线线性相关系数(r)应不小于0.9900。
2.5重复性质控品测定结果的变异系数(CV)应不大于8.00%。
2.6批间差在三个不同批次产品之间,质控品测定结果的变异系数(CV)应不大于15.00%。
2.7质控品测定值同一套质控品的测定结果应在本试剂盒规定的范围之内。
2.8特异性2.8.1与促黄体生成素(LH)浓度为500IU/L的LH在本试剂盒上测定的测定结果应不高于0.02ng/mL。
2.8.2 与促卵泡生成激素(FSH)浓度为500IU/L的FSH在本试剂盒上的测定结果应不高于0.02ng/mL。
2.8.3与抑制素A(Inhibin-A)浓度为100ng/mL的抑制素A在本试剂盒上的测定结果应不高于0.02ng/mL。
2.8.4与激活素A(Activin-A)浓度为100ng/mL的激活素A在本试剂盒上的测定结果应不高于0.02ng/mL。
2.9 稳定性取2℃~8℃保存至失效期3个月内的试剂盒,检测2.1、2.2、2.3、2.4、2.5、2.7、2.8项,结果应符合相应规定。
2.10 溯源性按照GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》提供所用AMH校准品的来源、赋值过程以及测量不确定度等内容,本试剂盒配套校准品溯源至本公司抗缪勒试管激素工作校准品。
抗缪勒管激素(AMH)测定试剂盒(磁微粒化学发光法)产品技术要求ldm

抗缪勒管激素(AMH)测定试剂盒(磁微粒化学发光法)适用范围:该产品用于体外定量测定人血清样本中的抗缪勒管激素(AMH)含量。
1.1 规格100测试/盒50测试/盒。
1.2 主要组成成分试剂盒由试剂1、试剂2、磁分离试剂、校准品和质控品组成。
校准品和质控品浓度具有批特异性,具体浓度见瓶标签。
2.1外观2.1.1试剂盒各组分应齐全、完整、液体无渗漏;2.1.2磁分离试剂摇匀后为均匀悬浊液,无明显凝集;2.1.3液体组分应澄清,无沉淀或絮状物;2.1.4包装标签应清晰,易识别。
2.2线性在[0.02, 30.00]ng/mL的测量范围内,试剂盒的相关系数(r)应≥0.9900。
2.3空白限应不大于0.015ng/mL。
2.4准确度回收率应在85.0%~115.0%范围内。
2.5重复性批内变异系数(CV)应不大于10.0%。
2.6批间差批间变异系数(CV)应不大于15.0%。
2.7质控品的赋值有效性质控品的测量值应在质控范围内。
2.8分析特异性试剂盒与表1中有关潜在交叉反应物应无显著的交叉反应。
表1特异性2.9 校准品和质控品的批内瓶间差2.9.1 校准品的批内瓶间差校准品A的S(瓶间)≤1.0,校准品B~校准品F的批内瓶间差CV≤10.0%。
2.9.2 质控品的批内瓶间差质控品的批内瓶间差CV≤10.0%。
2.10 溯源性根据GB/T 21415及有关规定提供校准品的来源、赋值过程以及不确定度等内容,抗缪勒管激素(AMH)校准品溯源至企业校准品,企业校准品与已上市产品比对赋值。
2.11 稳定性2.11.1 效期稳定性试剂盒在2℃~8℃条件下储存,有效期为12个月,取超过有效期一个月内的试剂盒检测线性、空白限、准确度、重复性、质控品的赋值有效性应符合2.2、2.3、2.4、2.5、2.7的要求。
2.11.2 复溶稳定性2.11.2.1校准品和质控品开瓶复溶后,室温保存,可稳定4小时,在第5个小时再次检测,其中校准品A的绝对偏差应在±1ng/mL范围内,校准品B~校准品F和质控品相对偏差应在±10%范围内。
抗缪勒氏管激素测定试剂盒(化学发光法产品技术要求丽珠

2性能指标
2.1外观
试剂盒应各组分应齐全、完整,液体无渗漏;包装标签应清晰、准确、牢固。
2.2检出限
空白限(limitofblank,LoB)不大于0.01ng/mL,检出限(limitofdetection,LoD)为0.02ng/mL。
产品名称
抗缪勒氏管激素测定试剂盒(化学发光法)
型号、规格
3×14人份/盒
结构及组成
1、抗缪勒氏管激素免疫反应测试筒抗缪勒氏管激素结合磁微粒:抗抗缪勒氏管激素鼠单克隆抗体(包被抗体)包被磁微粒;抗缪勒氏管激素酶标抗体:含碱性磷酸酶标记的抗缪勒氏管激素鼠单克隆抗体(检测抗体)。2、测试筒支架
产品适用范围/预期用途
2.3准确度
将已知浓度的抗缪勒氏管激素样本加入到低值样本中,其回收率应在[85%,115%]。
2.4线性
线性范围不窄于0.05 ng/mL~23ng/mL,线性相关系数|r|应不低于0.990。
2.5重复性
测试重复性参考品,所得结果的变异系数(CV)应不大于8%。
2.6批间差
测试重复性参考品,所得结果的的变异系数(CV)应不大于10%。
抗缪勒氏管激素(AMH)测定试剂盒(光激化学发光法)产品技术要求
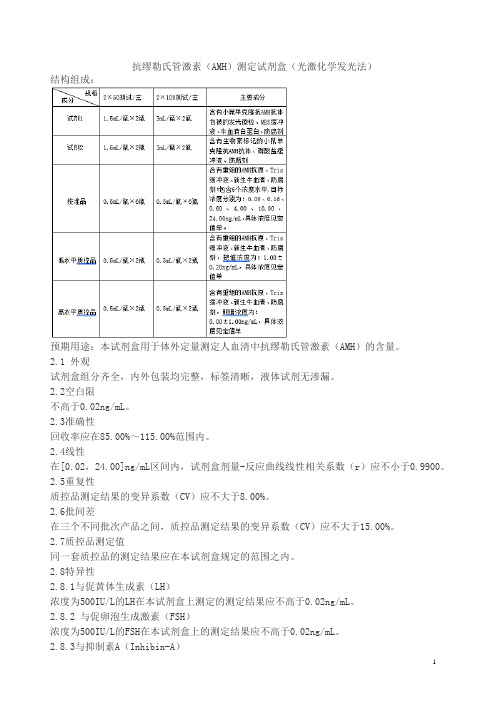
抗缪勒氏管激素(AMH)测定试剂盒(光激化学发光法)结构组成:预期用途:本试剂盒用于体外定量测定人血清中抗缪勒氏管激素(AMH)的含量。
2.1 外观试剂盒组分齐全,内外包装均完整,标签清晰,液体试剂无渗漏。
2.2空白限不高于0.02ng/mL。
2.3准确性回收率应在85.00%~115.00%范围内。
2.4线性在[0.02,24.00]ng/mL区间内,试剂盒剂量-反应曲线线性相关系数(r)应不小于0.9900。
2.5重复性质控品测定结果的变异系数(CV)应不大于8.00%。
2.6批间差在三个不同批次产品之间,质控品测定结果的变异系数(CV)应不大于15.00%。
2.7质控品测定值同一套质控品的测定结果应在本试剂盒规定的范围之内。
2.8特异性2.8.1与促黄体生成素(LH)浓度为500IU/L的LH在本试剂盒上测定的测定结果应不高于0.02ng/mL。
2.8.2 与促卵泡生成激素(FSH)浓度为500IU/L的FSH在本试剂盒上的测定结果应不高于0.02ng/mL。
2.8.3与抑制素A(Inhibin-A)浓度为100ng/mL的抑制素A在本试剂盒上的测定结果应不高于0.02ng/mL。
2.8.4与激活素A(Activin-A)浓度为100ng/mL的激活素A在本试剂盒上的测定结果应不高于0.02ng/mL。
2.9 稳定性取2℃~8℃保存至失效期3个月内的试剂盒,检测2.1、2.2、2.3、2.4、2.5、2.7、2.8项,结果应符合相应规定。
2.10 溯源性按照GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》提供所用AMH校准品的来源、赋值过程以及测量不确定度等内容,本试剂盒配套校准品溯源至本公司抗缪勒试管激素工作校准品。
抗缪勒氏管激素质控品产品技术要求博粹

抗缪勒氏管激素质控品产品技术要求博粹抗缪勒氏管激素(Anti-Müllerian Hormone, AMH)是一种重要的生物标志物,用于评估卵巢储备功能和女性生殖健康状况。
其测试结果对于评估女性的生殖健康状态、确定生育年龄、进行不孕不育疾病的诊断和治疗具有重要意义。
1.纯度要求:抗AMH质控品的纯度要求高,必须纯净且不含其他有可能对测试结果造成干扰的杂质。
其纯度可以通过高效液相色谱(HPLC)和酶联免疫吸附测定(ELISA)等技术进行验证。
2.稳定性要求:抗AMH质控品应具有良好的稳定性,以确保其在长期储存和使用过程中的一致性和可靠性。
稳定性可以通过长期储存试验、温度敏感性试验等进行验证。
3.活性要求:抗AMH质控品应具有高度的活性,能够与AMH快速、特异地结合,并能够准确地模拟AMH在生物体内的生理功能。
其活性可以通过生物活性试验、逆向酶联免疫吸附测定等进行验证。
4.重复性要求:抗AMH质控品的制备应具备良好的重复性,确保每一批制备的质控品在不同的实验条件下具有一致的检测结果。
重复性测试可以通过同批次和不同批次的重复性试验进行验证。
5.安全性要求:抗AMH质控品应符合生物安全要求,不得存在有害成分,并且对操作人员和环境无危害。
安全性可通过毒理学试验进行验证。
总之,抗缪勒氏管激素质控品的产品技术要求包括纯度、稳定性、活性、重复性和安全性等方面。
制造商在生产过程中应严格按照相关质量标准进行操作,确保质控品的质量稳定和一致,并通过严格的质量控制措施
确保质控品的合格率和可靠性,以满足AMH检测试剂盒的准确性和可靠性要求。
人生长激素测定试剂盒(化学发光免疫分析法)产品技术要求mairui

1 性能指标2.1外观和性状试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰,准确、牢固;Ra 组分应为棕色含固体微粒的液体,无板结、无絮状物。
Rb 组分应为清澈透明的液体,无沉淀、无悬浮物、无絮状物;校准品应为清澈透明液体,无沉淀、无悬浮物、无絮状物。
分装瓶应为透明塑料管,盖有塑料外盖。
2.2装量应不少于试剂的标示装量值。
2.3准确度2.3.1将hGH 国家标准品配成两个浓度水平的样品,用待检试剂盒进行检测,其检测结果与标定靶值的相对偏差在±10%范围内。
2.3.2对具有溯源性的两个浓度水平的正确度控制品进行检测,检测结果与标定浓度的相对偏差在±10%范围内。
2.4最低检测限应不大于0.02 ng/mL。
2.5线性试剂盒在0.03 ng/mL~50 ng/mL 区间内,其相关系数(r)应不低于0.9900。
2.6重复性变异系数CV 应≤ 5%。
2.7批间差变异系数CV 应≤ 10%。
2.8校准品均一性2.8.1校准品瓶内均一性C0的标准差(SD)应不大于0.024ng/mL,C1和C2的变异系数(CV)应不大于8.0%。
2.8.2校准品瓶间均一性C0 的标准差(SD)应不大于0.02 ng/mL,C1 和C2 的变异系数(CV)应不大于5.0%。
2.9生物安全性使用国家权威管理机构认可的、且不低于我国法定用于血源筛查体外诊断试剂灵敏度的检测试剂,对校准品中乙型肝炎病毒表面抗原、人类免疫缺陷病毒抗体(HIV-I 型和HIV-II1型)、丙型肝炎病毒抗体、梅毒螺旋体抗体的检测应为阴性。
2.10稳定性2~8℃避光保存,试剂盒有效期为365 天。
到有效期后90 天内的试剂盒应符合2.1、2.3、2.4、2.5、2.6、2.8 的要求。
2。
抗缪勒管激素(AMH)测定试剂盒(磁微粒化学发光法)产品技术要求北京华科泰生物
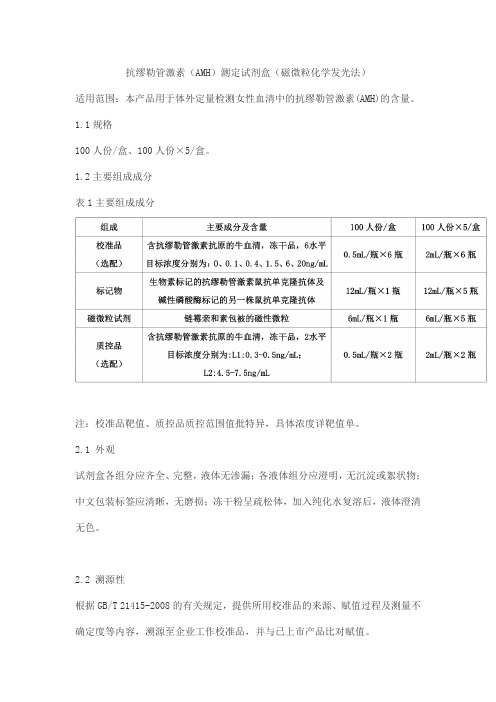
抗缪勒管激素(AMH)测定试剂盒(磁微粒化学发光法)适用范围:本产品用于体外定量检测女性血清中的抗缪勒管激素(AMH)的含量。
1.1规格100人份/盒、100人份×5/盒。
1.2主要组成成分表1主要组成成分注:校准品靶值、质控品质控范围值批特异,具体浓度详靶值单。
2.1 外观试剂盒各组分应齐全、完整,液体无渗漏;各液体组分应澄明,无沉淀或絮状物;中文包装标签应清晰,无磨损;冻干粉呈疏松体,加入纯化水复溶后,液体澄清无色。
2.2 溯源性根据GB/T 21415-2008的有关规定,提供所用校准品的来源、赋值过程及测量不确定度等内容,溯源至企业工作校准品,并与已上市产品比对赋值。
2.3 准确度回收率应在90%~110%之间。
2.4 线性在线性范围内[0.1,20]ng/mL,相关系数(r)应不低于0.99。
2.5 重复性分别检测高值和低值两个样本,重复性(CV%)应不高于10.0%。
2.6 批间差在三个不同批次产品之间,样本测定结果的变异系数(CV%)应不高于15.0%。
2.7 空白限空白限应不高于0.05ng/mL。
2.8 特异性表2与FSH、LH的交叉反应2.9 质控品赋值有效性测定高值、低值浓度质控品,其结果均应在质控范围内。
2.10 稳定性2.10.1 效期稳定性2℃~8℃储存,有效期12个月,效期后分别检测2.3、2.4、2.5、2.7、2.8、2.9项,其结果应符合各项要求。
2.10.2 复溶稳定性2.10.2.1 校准品开瓶后(复溶后),-20℃以下储存,有效期1个月,效期后分别检测2.3、2.4、2.5、2.7、2.8、2.9项,其结果应符合各项要求。
2.10.2.2 质控品开瓶后(复溶后),-20℃以下储存,有效期1个月,效期后分别检测2.5、2.9项,其结果应符合各项要求。
抗缪勒氏管激素测定试剂盒、制备方法及检测方法[发明专利]
![抗缪勒氏管激素测定试剂盒、制备方法及检测方法[发明专利]](https://img.taocdn.com/s3/m/eb3e88102e60ddccda38376baf1ffc4ffe47e2f2.png)
(19)中华人民共和国国家知识产权局(12)发明专利申请(10)申请公布号 (43)申请公布日 (21)申请号 202010797714.5(22)申请日 2020.08.10(71)申请人 深圳市宇诺生物技术有限公司地址 518110 广东省深圳市龙华区观澜街道新澜社区观光路1303号鸿信工业园3号厂房501;1号厂房501(72)发明人 肖宇强 张平 马金玉 周玲 赖鹏飞 (51)Int.Cl.G01N 33/74(2006.01)G01N 33/58(2006.01)G01N 33/577(2006.01)G01N 33/558(2006.01)G01N 33/543(2006.01)(54)发明名称抗缪勒氏管激素测定试剂盒、制备方法及检测方法(57)摘要本发明公开了一种抗缪勒氏管激素测定试剂盒,其特征在于,包括反应物质,所述反应物质包括检测线荧光偶合物及质控线荧光偶合物,所述检测线荧光偶合物含有荧光微球标记的抗缪勒氏管激素单克隆抗体,所述质控线荧光偶合物含有荧光微球标记的鸡IgY抗体、兔IgG抗体或鼠IgG抗体中的一种,反应物质由检测线荧光偶合物及质控线荧光偶合物在冻干保护液的保护下经过冷冻干燥制成。
该试剂盒检验准确度高、特异性强、重现性好、操作快捷。
权利要求书2页 说明书16页 附图2页CN 111999509 A 2020.11.27C N 111999509A1.一种抗缪勒氏管激素测定试剂盒,其特征在于,包括反应物质,所述反应物质包括检测线荧光偶合物及质控线荧光偶合物,所述检测线荧光偶合物含有荧光微球标记的抗缪勒氏管激素单克隆抗体,所述质控线荧光偶合物含有荧光微球标记的鸡IgY抗体、兔IgG抗体或鼠IgG抗体中的一种。
2.根据权利要求1所述的抗缪勒氏管激素测定试剂盒,其特征在于,所述反应物质由检测线荧光偶合物及质控线荧光偶合物在冻干保护液的保护下经过冷冻干燥制成。
3.根据权利要求1所述的抗缪勒氏管激素测定试剂盒,其特征在于,所述荧光微球为时间分辨荧光微球,所述时间分辨荧光微球包埋稀土离子,同时所述时间分辨荧光微球表面修饰有氨基、羧基或羟基中至少一种功能基团;所述稀土离子选自镧系元素中Sm钐、Eu铕、Gd钆、Tb铽、Dy镝中的至少一种。
抗缪勒氏管激素(AMH)试剂盒已上市对照产品信息

储存,有效期12个 月。应避免阳光直接 照射。 2.铝箔袋开 封后,请在1小时内
保存,保存期限有效 期为18个月;组份2保 存于2~8℃保存,保 存期限有效期为18个
2℃~30℃保存,切勿 冷冻。有效期为18个 月
使用。
月
件下,产品稳定性符合
其质量要求。
抗缪勒氏管激素 (AMH)检测试剂盒 (免疫荧光法)
由试剂R1、R2、M、S1 、S2、C1、C2、试剂卡 和校准品卡组成。其 中:R1:生物素化的抗 AMH抗体,1瓶, 6.5mL;R2:吖啶酯标 记的抗AMH抗体,1瓶, 6.5mL;M:链霉亲和素 磁珠,1瓶,2.5 mL; S1:校准品1;S2:校 准品2;C1:质控品1; C2:质控品2
适用于体外定量测定人全血
型号:型号W,型号 L;规格: 50人份/ 盒,2×50人份/盒
100人份/盒
主要组成 成分
试剂由测试卡、样本稀释液 和ID芯片组成。其中: 试剂盒主要由磁珠 (1)测试卡由试纸条、塑 包被物(R1)、酶标 料盒组成。试纸条上的主要 记物(R2)、校准品 成分有:样本处理垫、硝酸 和质控品(选配) 纤维素膜、吸水纸、PVC板 组成。其中R1为含 及其它试纸条支持物。硝酸 有AMH抗体1包被磁 纤维素膜上包被有AMH单克 珠,R2为AMH抗体2 隆抗体和鸡IgY,样本处理 标记碱性磷酸酶标 垫含有AMH单克隆抗体和羊 记物。校准品含AMH 抗鸡IgY(GAC)。(2)样 重组抗原,质控品 本稀释液主要成分为Tris- 含AMH重组抗原 HCl缓冲液
抗缪勒氏管激素 (AMH)检测试剂盒 (荧光免疫层析法)
抗缪勒氏管激素 检测试剂盒(免 疫荧光法)
抗缪勒氏管激素 (AMH)检测试剂盒 (荧光免疫层析法)
抗缪勒管激素测定试剂盒(化学发光免疫分析法)说明书

Statistical Approach; Approved Guideline. [9] CLSI EP09C-ED3:2018 Measurement Procedure Comparison and Bias Estimation Using
I
YY/T XXXXX—XXXX
前言
本标准按照GB/T 1.1—2009给出的规则起草。 本标准的某些内容可能涉及专利,本文件的发布机构不承担识别这些专利的责任。 本标准由国家药品监督管理局提出。 全国医用临床检验实验室和体外诊断系统标准化技术委员会(SAC/TC136)归口。 本标准起草单位: 本标准主要起草人:
V cs
100%
................................... (1)
式中:
R—回收率;
V—样品A液的体积;
V0—样本B液的体积; C—样本B液加入A液后的检测浓度;
C0—测量B液的浓度; Cs—样本A液的浓度。
4.4 重复性 用同一批号试剂盒,对至少2个不同浓度的质控品或临床样本(高值质控或临床样本浓度不低于
Patient Samples; Third Edition. _________________________________
5
4 试验方法 4.1 外观
在自然光下以正常视力或矫正视力目视检查,检测结果应符合3.1的要求。
4.2 检出限 生产企业应提供试剂盒的空白限、检出限及参考区间等相关信息。根据制造商提供的信息,对5
北京协和洛克抗缪勒氏管激素测定试剂盒(酶联免疫吸附法)产品技术要求

抗缪勒氏管激素测定试剂盒(酶联免疫吸附法)结构组成:预期用途:用于体外定量测定女性血清中抗缪勒氏管激素(AMH)的浓度。
2.1.外观1)试剂盒各组分齐全、完整,内外包装均应完整,标识清晰。
2)液体试剂无渗漏,冻干组分呈疏松体,复溶后液体均匀(无肉眼可见颗粒、无沉淀)2.2.质控品赋值有效性分别取高、低两个浓度质控品,检测其浓度值,每个测试值均应在所示的质控范围内。
2.3.准确度回收率为85%~115%。
2.4.空白限不高于0.04ng/ml2.5.线性试剂盒的线性范围为[0.05,18]ng/mL,相关系数r不小于0.9900。
2.6.重复性用高、低2个浓度水平的样本各重复检测10次,其变异系数(CV)不大于13%。
2.7. 瓶内均一性用同一批次的1套校准品和质控品作为样本重复检测10次,除校准品A外各点测值变异系数(CV)不大于13%,校准品A吸光度值变异系数(CV)不大于13%。
2.8. 批内瓶间差用同一批次的10套校准品和质控品作为样本检测,除校准品A外各点测值变异系数(CV)不大于13%,校准品A吸光度值变异系数(CV)不大于13%。
2.9.批间差用3个批号试剂盒检测同一份样本,变异系数(CV)不大于15%。
2.10.特异性浓度为促卵泡激素(FSH)200ng/mL、促黄体生成素(LH)200ng/mL的作为样本进行特异性反应,交叉反应率应小于5%。
2.11.稳定性2.11.1 效期稳定性试剂盒在2℃~8℃保存,有效期12个月,取效期后产品进行检测,检测结果应符合2.1~2.6、2.10项要求。
2.11.2 校准品复溶稳定性校准品开瓶复溶后,在2℃~8℃保存,可以稳定3天后检测准确度和线性区间,应符合2.3、2.5项要求。
2.11.3 质控品复溶稳定性质控品开瓶复溶后,在2℃~8℃保存,可以稳定3天后检测质控品重复性和赋值有效性。
质控品重复性的变异系数(CV)不大于13%,赋值有效性应符合2.2项要求。
抗缪勒氏管激素测定试剂盒(化学发光免疫分析法)产品技术要求万孚

1性能指标
1.1外观
外观应符合如下要求:
a)磁珠包被物R1摇匀后应为棕褐色悬浊液;静止久后,棕褐色磁珠沉降于底部,上清液应为无色液体;酶标记物R2应为无色液体,无沉淀或絮状物;校准品和质控品应为外观均匀,成形完整,呈乳白色的冻干品,复溶后较清亮,无浑浊及沉淀;
b)试剂盒各组分应齐全、完整,液体无渗漏;
c)中文包装标签清晰,无磨损。
1.2准确度
将具有溯源性的两个浓度准确度参考品进行检测,检测结果与标定浓度的相对偏差在±10%范围内。
1.3空白限
不大于0.007ng/mL。
1.4线性
试剂盒在0.01ng/mL~23ng/mL 区间内,其相关系数(r)的绝对值不低于0.9900。
1.5重复性
变异系数CV≤8%。
1.6批间差
变异系数CV≤10%。
1.7校准品
1.7.1校准品准确度
测定校准品,C1,C2 测定结果的相对偏差在±10%范围内。
1.7.2校准品瓶内均一性
校准品C1,C2 瓶内均一性≤8%。
1.7.3校准品瓶间均一性
校准品C1,C2 瓶间均一性≤5%。
1.8质控品
1.8.1瓶内均一性
变异系数CV≤8.0%。
1.8.2瓶间均一性
变异系数CV≤5.0%。
1.8.3靶值及靶值范围
每批质控品均应提供本批产品的靶值单,并应提供赋值方法程序文件。
质控品的测试值应在靶值范围内。
抗缪勒管激素检测试剂盒(荧光免疫层析法)产品技术要求 广州天宝颂原生物

医疗器械产品技术要求编号:
抗缪勒管激素检测试剂盒(荧光免疫层析法)
1. 性能指标
试剂盒性能指标
1.1 物理性状
1.1.1外观
测试卡外壳应整洁完整,印刷内容清晰;测试卡内部试纸条应整洁完整、无毛刺、无破损、无污染;材料附着牢固。
稀释液应澄清无沉淀。
1.1.2 宽度
测试卡内部试纸条宽度应在 4.1mm±0.2mm 范围内。
1.1.3 移行速度
液体移行速度应不低于10mm/min。
1.2精密度
1.2.1 批内精密度
用AMH浓度为2.00ng/mL、7.00ng/mL、15.00ng/mL的企业参考品进行检测,其变异系数CV不大于10%。
1.2.2 批间精密度
任取3批测试卡,用AMH浓度为2.00ng/mL、7.00ng/mL、15.00ng/mL的企业参考品进行检测,其批间变异系数CV不大于15%。
1.3 准确度
用AMH浓度为2.00ng/mL、7.00ng/mL、15.00ng/mL的企业参考品进行检测,其相对偏差(B%)不大于±10%。
1.4 空白限
AMH空白限应不高于0.10ng/mL。
1.5分析测量范围
AMH分析测量范围为0.10ng/mL-20.00ng/mL,相关系数r2≥0.9900。
1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1 性能指标
2.1外观和性状
试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰,准确、牢固;Ra 组分应为棕色含固体微粒的液体,无板结、无絮状物。
Rb 组分应为清澈透明的液体,无沉淀、无悬浮物、无絮状物;
校准品复融前外观应呈现粉末块状固体,不起泡,不塌陷,复融后应为清澈透明液体,无沉淀、无悬浮物、无絮状物。
分装瓶应为棕色玻璃瓶,盖有塑料外盖。
2.2装量
应不少于试剂的标示装量值。
2.3准确度
对具有溯源性的两个浓度水平的正确度控制品进行检测,检测结果与标定浓度的相对偏差在±10%范围内。
2.4最低检测限
应不大于0.007 ng/mL。
2.5线性
试剂盒在0.01 ng/mL ~23 ng/mL 区间内,其相关系数(r)应不低于0.9900。
2.6重复性
变异系数CV 应≤ 5%。
2.7批间差
变异系数CV 应≤ 10%。
2.8校准品均一性
2.8.1校准品瓶内均一性
C0 的标准差(SD)应不大于0.016 ng/mL,C1 和C2 的变异系数(CV)应不大于8.0%。
2.8.2校准品瓶间均一性
C0 的标准差(SD)应不大于0.01 ng/mL,C1 和C2 的变异系数(CV)应不大于5.0%。
2.9生物安全性
使用国家权威管理机构认可的、且不低于我国法定用于血源筛查体外诊断试剂灵敏度的检测试剂,对校准品中乙型肝炎病毒表面抗原、人类免疫缺陷病毒抗体(HIV-I 型和HIV-II 型)、丙型肝炎病毒抗体、梅毒螺旋体抗体的检测应为阴性。
2.10稳定性
2~8℃避光保存,试剂盒有效期为365 天。
到有效期后90 天内的试剂盒应符合2.1、2.3、2.4、2.5、2.6、2.8 的要求。
